Influência das Condições de Formação de Nanomateriais Pd / SnO2 nas Propriedades dos Sensores de Hidrogênio
Resumo
Sensores de óxido de metal foram criados usando dióxido de estanho nanométrico obtido por um método sol-gel. Camadas sensíveis a gás dos sensores foram impregnadas com PdCl 2 soluções de diferentes concentrações para aumentar a sensibilidade dos sensores propostos. A influência de diferentes condições de temperatura da formação do sensor nas propriedades do sensor foi estudada. Verificou-se que diminuir a duração do tratamento do sensor de alta temperatura evita o aumento das partículas dos materiais sensíveis ao gás. Foi mostrado que os sensores baseados em materiais com tamanhos de partícula menores mostraram respostas de sensor mais altas a 40 ppm H 2 . Os resultados obtidos foram explicados em termos da influência substancial do comprimento dos limites comuns entre as partículas de dióxido de estanho e paládio nas propriedades sensíveis ao gás dos sensores. Os sensores obtidos possuíam resposta e tempo de recuperação rápidos e demonstraram características estáveis durante sua operação de longo prazo.
Histórico
Hoje em dia, o hidrogênio é amplamente utilizado para síntese química na indústria e como fonte de energia ecologicamente correta [1,2,3]. O hidrogênio é um gás explosivo e, portanto, o controle de H 2 conteúdo em áreas de seu uso, transporte e armazenamento é necessário. Dispositivos de análise de gás baseados em sensores de óxido metálico podem ser promissores para realizar tal controle [4,5,6].
É bem conhecido que os materiais nanométricos têm algumas propriedades físico-químicas únicas, ou seja, optoeletrônica [7], magnética [8] e catalítica [9]. SnO 2 é um material de perspectiva para criar os sensores de óxido de metal devido à sua inércia química, estabilidade térmica e capacidade de quimisorver oxigênio. É por isso que os nanomateriais baseados em dióxido de estanho são muito interessantes para estudar como camadas sensíveis ao gás dos sensores para medir H 2 no ar. O aumento das respostas do sensor ao hidrogênio pode ser obtido pela adição na camada sensível ao gás dos sensores de aditivos catalíticos ativos, incluindo Pd, que é um dos catalisadores mais ativos em uma reação de oxidação do hidrogênio [6, 10].
A composição do material do sensor, o método de sua preparação e as condições de formação do material podem influenciar no tamanho da partícula [11,12,13] e, portanto, nas propriedades sensíveis ao gás do material.
A morfologia do material da camada sensorial, incluindo seu tamanho de partículas e sua distribuição, tem grande importância para criar sensores de óxido metálico altamente eficientes [14,15,16]. Sabe-se que diminuir o tamanho de partícula do material da camada sensitiva do sensor deve aumentar a resposta do sensor [17]. Ao mesmo tempo, sabe-se que a criação dos sensores requer sua sinterização em alta temperatura. No entanto, a sinterização em alta temperatura leva ao aumento das partículas de nanomateriais. É por isso que as condições de um processo de sinterização a alta temperatura do sensor devem impedir o alargamento das partículas e proporcionar simultaneamente resistência mecânica dos sensores e suas condutividades através da formação de contatos entre as nanopartículas do material do gás sensível camada [18].
A temperatura ideal da sinterização do sensor que deve satisfazer as condições listadas acima pode ser alcançada pelos valores de temperatura exigidos e pelo tempo de duração de estágios definidos da sinterização de alta temperatura dos sensores. As condições de formação do nanomaterial sensor também devem proporcionar a completa finalização da cristalização e estabilização de suas nanopartículas.
O objetivo deste trabalho é estudar a influência das condições de formação de Pd / SnO 2 nanomateriais com diferentes conteúdos de paládio nas propriedades de sensores semicondutores para hidrogênio.
Métodos
Síntese de dióxido de estanho nanométrico
Síntese de SnO nanométrico 2 materiais foi realizada por um método sol-gel. A amostra de SnCl 4 · 5H 2 O ( m =1,5 g) foi dissolvido em 15 ml de etilenoglicol. A solução obtida foi evaporada a 110-120 ° C. Após evaporação do etilenoglicol, formou-se um gel castanho escuro. O gel resultante foi seco a 150 ° C para formar um xerogel. O xerogel foi triturado e colocado em uma placa de cerâmica. Para obter SnO nanométrico 2 , a decomposição térmica do xerogel foi realizada no ar usando um forno de alta temperatura Gero (Alemanha). SnO nanométrico 2 , carboximetilcelulose e PdCl 2 foram usados para obter os materiais sensíveis ao gás.
Preparação de sensores semicondutores de adsorção
Sensores semicondutores de adsorção foram preparados pela deposição de uma pasta do material sensível ao gás na placa de cerâmica do sensor que possuía contatos elétricos de medição e um aquecedor [19]. A pasta foi preparada misturando o SnO sintetizado 2 nanomaterial e solução aquosa (3% em peso) de carboximetilcelulose. Um volume definitivo da pasta (3 μL) foi colocado na placa de cerâmica do sensor usando a seringa de Hamilton 85 RN SYR (5 μL) para fornecer a mesma espessura da camada do sensor. De acordo com os dados do SEM, a espessura da camada do sensor era de cerca de 70 μm (Arquivo adicional 1:Figura S1, Seção de Informações de Apoio). Os sensores foram secos a 90 ° C durante 1 h ao ar. A introdução de paládio nas camadas sensíveis ao gás dos sensores foi realizada impregnando-os com solução de cloreto de paládio de certas concentrações (CPdCl 2 =0,05 × 10 −2 –0,15 M). Após a impregnação, os sensores foram secos e sinterizados em um forno de alta temperatura usando dois modos de temperatura diferentes que incluíam o aquecimento gradual dos sensores (Fig. 1a, b). Os sensores e materiais sensíveis ao gás obtidos pelos modos de aquecimento de temperatura 1 ou 2 foram denominados S 1 ou S 2 respectivamente.
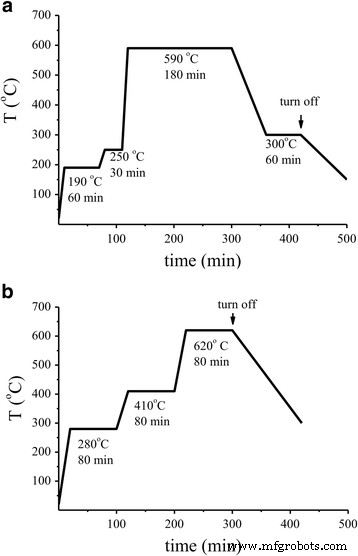
Esquemas de aquecimento de temperatura dos sensores baseados em SnO 2 . a Modo 1. b Modo 2
Métodos de medição
Para medir um valor do sinal do sensor, os sensores foram colocados em câmaras e conectados a um suporte elétrico especial [20]. A medição foi realizada utilizando o fluxo de gás analisado com uma taxa de 400 ml / min. A temperatura necessária do sensor foi garantida por um valor definido de tensão no aquecedor do sensor. A medição da temperatura do sensor foi realizada em um pirômetro Optris Laser Sight (Optris, Alemanha). Os sensores foram estabilizados por envelhecimento a 400 ° C durante 1 semana em ar com tratamento periódico dos sensores pela mistura hidrogênio-ar com 1000 ppm H 2 antes de medir as propriedades sensíveis ao gás.
Razão de um valor da resistência elétrica do sensor no ar ( R 0 ) a um valor de sua resistência elétrica na presença de 40 ppm H 2 ( R H2 ) foi escolhido como uma medida da resposta do sensor. O tempo de resposta do sensor ( t 0,9 ) foi estimado como o tempo necessário para o sensor atingir 90% de um valor de sinal de equilíbrio quando o ar está sendo substituído por um gás analisado. O tempo de recuperação ( τ 0.1 ) foi estimado como um tempo necessário para o sensor retornar a 10% acima do sinal inicial no ar quando o gás analisado está sendo substituído pelo ar.
As características dos sensores foram estudadas usando misturas de hidrogênio-ar com várias concentrações de H 2 . Misturas de ar com H 2 , CO, CH 4 , e H 2 e CO ou H 2 e CH 4 foram usados para estimar a seletividade dos sensores obtidos. Todas as misturas de gases analisadas foram preparadas e testadas no Centro de Certificação e Metrologia da Ucrânia.
Estabilidades das respostas a 40 ppm de H 2 para os sensores S 2 (S-67 e S-69) durante 6 meses de sua operação foram estudados.
A determinação da superfície do material sensor específico foi realizada pelo método Brunauer-Emmett-Teller (BET).
O conteúdo de paládio nos materiais do sensor foi determinado por um método de absorção atômica usando um espectrofotômetro AAS1N Carl Zeiss (Jena, Alemanha) com um atomizador flamejante. A atomização do paládio foi realizada em chama de acetileno-ar (2350 ° C).
O estudo da composição das fases foi realizado utilizando um difratômetro Bruker D &Advance (radiação Cu Kα ) A identificação da fase da amostra foi realizada comparando os resultados obtidos e os dados cristalográficos publicados.
O estudo da morfologia dos materiais sensores pelo método TEM foi realizado em microscópio eletrônico de transmissão SELMI PEM-125 K com tensão de aceleração de 100 kV. A análise do tamanho de partícula com base em imagens TEM foi realizada usando o programa Kappa Image Base. Para obter informações sobre a distribuição do tamanho de partícula para os nanomateriais obtidos, cerca de 300 partículas na imagem TEM foram levadas em consideração.
As amostras dos nanomateriais obtidos foram estudadas pelo método FESEM usando um microscópio eletrônico de varredura por emissão de campo JEOL JSM-6700F (JEOL Ltd., Japão) e pelo método HRTEM usando um microscópio eletrônico de transmissão JEM-2100F (JEOL Ltd., Japão).
A espessura da camada do sensor foi estimada usando um microscópio eletrônico de varredura JEOL JSM-6060LA (JEOL Ltd., Japão) com uma tensão de trabalho de 30 kV.
Resultados e discussão
Os nanomateriais sintetizados baseados em SnO 2 [21] com um tamanho médio de partícula de 8 nm foram usados para criar os sensores e estudar a influência de diferentes condições de aquecimento de temperatura da preparação do sensor nas propriedades sensíveis ao gás.
Foi descoberto anteriormente [19, 22, 23] que a formação da camada sensível ao gás dos sensores que foram preparados usando o modo de aquecimento de temperatura 1 com temperatura final em uma faixa de 590-620 ° C durante 180 min foi conduzida a formar as partículas com tamanhos de 5 a 30 nm (um tamanho médio de 17 nm). Imagem TEM do nanomaterial do sensor S 1 obtido usando o modo de aquecimento de temperatura 1 com uma temperatura final de 590 ° C é apresentado na Fig. 2a. A resposta ( R 0 / R H2 ) do sensor com base no material foi igual a 6,7. O aumento da resposta do sensor pode ser fornecido pelo uso de materiais com tamanhos de partícula menores. Essas partículas podem ser obtidas usando o modo de aquecimento por temperatura com menor duração na temperatura final de sinterização do sensor. Verificou-se que a diminuição da duração do aquecimento do sensor de 180 para 80 min na temperatura final do modo de aquecimento 1 (590 ° C) levou à formação de valores muito pequenos das respostas do sensor para 40 ppm H 2 ( R 0 / R H2 ~ 2) e altos valores dos sensores de resistências elétricas no ar (> 500 MOhm) para a maioria dos sensores criados. Essas condições de sinterização do sensor provavelmente não levaram à formação de quantidade suficiente de contatos entre as partículas do material para permitir a passagem de corrente elétrica pelo sensor.
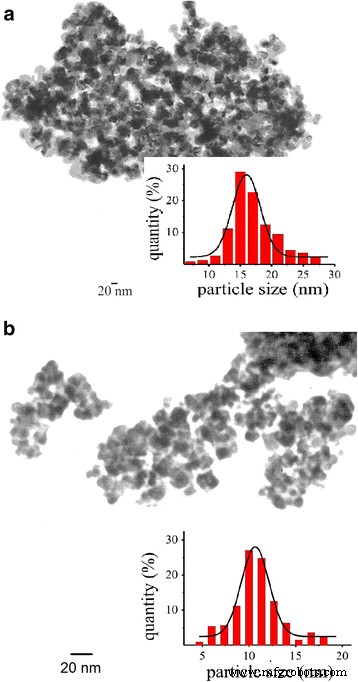
Imagens TEM dos nanomateriais sensíveis a gás a S 1 e b S 2
Para fornecer a formação da condutividade do sensor e sua resistência mecânica, a duração do aquecimento do sensor foi reduzida para até 80 min com aumento simultâneo da temperatura final de sinterização do sensor para 620 ° C. Além disso, a duração do aquecimento do sensor neste modo de temperatura foi aumentada para 80 min nas regiões de baixa temperatura da sinterização, ou seja, a 280 e 410 ° C, que corresponderam às temperaturas de CMC e decomposição do cloreto de paládio [24,25 , 26]. Essas mudanças nas regiões de baixa temperatura da formação do sensor são causadas pela necessidade de formação de um número maior de contatos no material do sensor. O aumento do tamanho das partículas do material nas regiões de baixa temperatura certamente não deve ser tão intenso como deveria ser a 620 ° C. O esquema do modo 2 de aquecimento de temperatura mais suave da sinterização do sensor é apresentado na Fig. 1b.
Análise de micrografias TEM dos materiais sensores obtidos S 2 (Fig. 2b) mostrou que esses materiais incluem partículas que eram menores do que as partículas do material sensor S 1 (Fig. 2a):um tamanho médio de partícula de dióxido de estanho para ambos os modos de aquecimento de temperatura estudados 1 e 2 foi de 17 e 11 nm, respectivamente. Tal diminuição do tamanho de partícula do material sensor S 2 contribuiu para um aumento do valor da superfície específica do dióxido de estanho para 47 m 2 / g em vez de 39 m 2 / g que foi encontrado para o material do sensor S 1 .
Foi demonstrado que o conteúdo de paládio no Pd / SnO 2 nanomateriais obtidos por impregnação do SnO nanométrico 2 por soluções de PdCl 2 aumenta quando a concentração de cloreto de paládio também aumenta. Em particular, quando a concentração de PdCl 2 a solução foi alterada de 0,05 mol / L para 15 × 10 −2 mol / L, o conteúdo de aditivos de paládio nos nanomateriais foi alterado de 0,001 para 0,193% em peso.
De acordo com dados de XRD, dióxido de estanho não modificado e Pd / SnO 2 nanomateriais com diferentes teores de paládio obtidos em ambos os modos de temperatura têm estrutura de cassiterita com parâmetros de rede idênticos a =0,4738 nm, b = c =0,3187 nm [21].
A imagem FESEM do material do sensor obtido (Fig. 3a) demonstra os grãos de SnO 2 partículas de nanomaterial e Pd (mostrado pelas setas na Fig. 3a). Limites claros entre as partículas do nanomaterial do sensor podem ser vistos nas imagens HRTEM (Fig. 3b, c).

a FESEM e b , c Imagens HRTEM do sensor Pd / SnO 2 nanomaterial
Foi mostrado (Fig. 4a, b) que a dependência dos valores de resistência elétrica no ar dos sensores contendo Pd no conteúdo de paládio em diferentes temperaturas do sensor tem um caráter complicado com mínimo em baixos teores de paládio e amplo máximo em Pd muito mais alto conteúdo para ambos os modos de aquecimento de temperatura diferentes dos sensores.
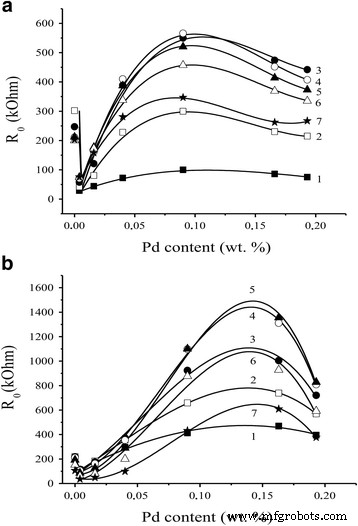
Dependência de R 0 valores dos sensores a S 1 e b S 2 baseado em Pd / SnO 2 sobre o conteúdo de paládio em diferentes temperaturas dos sensores: 1 410 ° C, 2 382 ° C, 3 355 ° C, 4 327 ° C, 5 295 ° C, 6 261 ° C e 7 225 ° C
Para explicar os resultados obtidos, deve-se notar que os valores da resistência R 0 e a resposta do sensor com adição de metais (ou óxidos) no material da camada sensível ao gás foi fornecida pela formação de limites comuns entre as partículas dos aditivos ativos e o dióxido de estanho [19, 27, 28]. Quando o sensor é aquecido no ar, esses limites participam da quimissorção de oxigênio com localização dos elétrons da banda de condutividade do semicondutor. Tal quimissorção influencia nos valores da resistência elétrica do sensor. Na presença de um gás analisado, uma reação catalítica heterogênea de oxidação do gás por oxigênio adsorvido quimicamente está ocorrendo na superfície do semicondutor. Os elétrons localizados no oxigênio adsorvido quimicamente retornam à banda de condutividade do semicondutor, e ocorre a diminuição da resistência elétrica do sensor. Nesse caso, a quantidade de oxigênio estacionário na superfície do sensor que ocorre como resultado de um estado de equilíbrio dinâmico da reação de oxidação determinará o valor de resistência do sensor. Uma mudança no valor da resistência do sensor quando o ar é substituído pelo gás analisado determina o valor da resposta do sensor. Em condições idênticas (mesmo gás de concentração definida e mesma temperatura do sensor), o valor da resistência elétrica do sensor no ar e sua variação na presença do gás analisado (resposta do sensor) dependerá do comprimento do limite entre as partículas de paládio e dióxido de estanho. O conteúdo de paládio no material do sensor afetará o valor do comprimento do limite e, portanto, determinará as propriedades do sensor.
Como pode ser visto na Fig. 4a, b, a introdução de paládio (até 0,05% Pd) afeta o valor do sensor R 0 da mesma maneira, independentemente do modo de aquecimento da temperatura da sinterização do sensor. A redução inicial observada no valor da resistência elétrica do sensor pode ser decorrente da existência de paládio metálico que se forma na superfície do sensor de acordo com os dados XPS obtidos [19]. Um aumento adicional do conteúdo de paládio leva a um ligeiro aumento nos valores das resistências dos sensores S 1 e S 2 devido à baixa quimissorção de oxigênio no limite de um comprimento muito pequeno entre SnO 2 e partículas de paládio. Deve-se notar que valores semelhantes das resistências dos sensores S 1 e S 2 na faixa de tais teores de paládio baixos não indicam nenhuma influência significativa do paládio nas propriedades dos sensores que são determinadas pelas próprias propriedades do dióxido de estanho nestas condições. Verificou-se que o valor da resistência elétrica de SnO 2 praticamente não dependeu da temperatura de sinterização do sensor na faixa de temperatura de 590–620 ° C como foi encontrado em [19,22 ,, 21–23].
Mudança do modo de aquecimento da temperatura de criação dos sensores S 1 e S 2 afeta o valor de sua resistência significativamente quando o conteúdo de paládio é aumentado (> 0,05% Pd) (Fig. 4a, b). Na verdade, a resistência para os sensores S 2 têm valores muito maiores do que os dos sensores S 1 em condições de mesmo conteúdo de paládio na faixa de concentração de 0,05–0,2% Pd. Isso está de acordo com a suposição sobre um papel estabilizador do paládio [29] que evita o aumento das partículas de nanomateriais, e o modo de aquecimento por temperatura suave 2 da sinterização do sensor contribui para esse processo. O comprimento dos limites entre as partículas de paládio e dióxido de estanho sob essas condições de temperatura suave será maior para o material S 2 e, portanto, devido a uma grande quantidade de oxigênio quimicamente absorvido nas fronteiras, os valores de resistência para os sensores S 2 deve ser maior do que aqueles para os sensores S 1 . Isso é confirmado em um experimento (Fig. 4a, b). A formação das partículas menores para os nanomateriais contendo Pd obtidos nas condições de temperatura suave do modo de aquecimento 2 também foi confirmada pelo método TEM (Fig. 2b).
Finalmente, em teores de paládio muito altos, o processo de agregação de partículas de Pd pode começar e irá diminuir o comprimento dos limites comuns, resultando na diminuição dos valores de resistência elétrica dos sensores (Fig. 4b).
Em geral, uma mudança nas respostas do sensor ao hidrogênio está correlacionada com uma mudança em sua resistência elétrica (Figs. 4a, b e 5a, b):um aumento nos valores da resistência elétrica dos sensores leva a um aumento na valores de suas respostas do sensor para H 2 . As respostas dos sensores S 2 a 40 ppm de hidrogênio são maiores do que as respostas dos sensores S 1 (Fig. 5). Como pode ser visto (Fig. 5), diminuindo a resposta do sensor para H 2 é observado para os maiores teores de aditivos de Pd em comparação com o sensor S 2 . Provavelmente pode ser devido à agregação dos aglomerados de paládio que cobrem a superfície do semicondutor em grande extensão, e a superfície do dióxido de estanho torna-se indisponível para o hidrogênio. É por isso que a diminuição da resposta do sensor é observada no experimento.
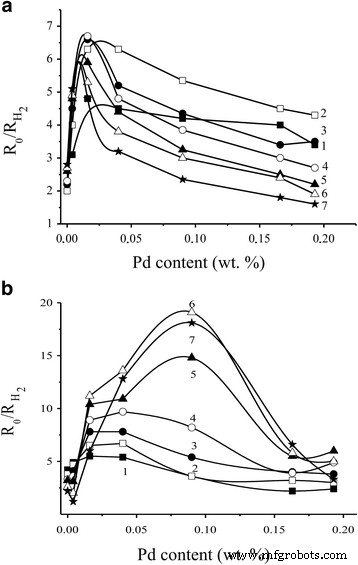
Dependência da resposta do sensor a 40 ppm H 2 para os sensores a S 1 e b S 2 baseado em Pd / SnO 2 sobre o conteúdo de paládio em diferentes temperaturas dos sensores: 1 410 ° C, 2 382 ° C, 3 355 ° C, 4 327 ° C, 5 295 ° C, 6 261 ° C e 7 225 ° C
Verificou-se que as posições dos valores máximos das resistências elétricas do sensor (Fig. 4a, b) e das respostas do sensor (Fig. 5a, b) para o sensor S 2 em comparação com o sensor S 1 são deslocados para uma região de maior conteúdo de paládio. Pode ser o resultado da existência de um conteúdo de paládio relativamente maior na superfície do sensor em um estado não agregado para o material SnO 2 com tamanho menor de suas partículas. Tal estado do material promoverá o aumento do valor da resistência elétrica do sensor no ar e a resposta do sensor ao hidrogênio.
Para o sensor mais sensível S 2 com base em 0,09% Pd / SnO 2 nanomaterial, outras propriedades do sensor foram estudadas. Verificou-se que este sensor é sensível ao hidrogênio em uma ampla faixa de suas concentrações nas diferentes temperaturas de operação do sensor (Fig. 6). Uma dependência da condutividade dos sensores em H 2 a concentração é praticamente linear em uma faixa testada de H 2 concentração (2–1000 ppm H 2 ) nas diferentes temperaturas do sensor (327 e 382 ° C) (Fig. 6). Não linearidade da condutividade do sensor na ampla faixa de H 2 a concentração a 261 ° C está provavelmente associada a várias ligações de energia do oxigênio adsorvido quimicamente na superfície do sensor. Foi descoberto que um limite de detecção de H 2 a medição para o sensor mais sensível é igual a 2 ppm no ar. Uma mudança na condutividade do sensor que atinge 44-52% para essa baixa concentração de hidrogênio depende da temperatura do sensor. Deve-se notar que a resposta a 2 ppm H 2 ( R 0 / R H2 =2,1 a 261 ° C) para o sensor criado é maior do que uma resposta ao mesmo H 2 concentração ( R 0 / R H2 =1,3 a 265 ° C) para o sensor baseado em nanosized SnO 2 estudado em [30].
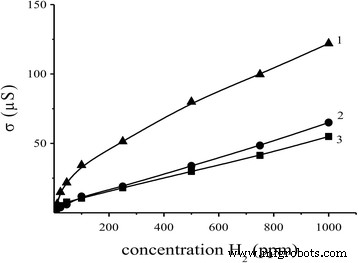
Dependência da condutividade do sensor S 2 com base em 0,09% Pd / SnO 2 nanomaterial na concentração de hidrogênio em diferentes temperaturas do sensor: 1 261 ° C, 2 327 ° C, 3 382 ° C
Foi mostrado que o sensor baseado em S 2 material (0,09% Pd / SnO 2 ) possuem uma resposta rápida ( t 0,9 =3 s) e recuperação ( τ 0.1 =12 s) tempo a 261 ° C (Fig. 7). Deve-se notar que os sensores criados também têm uma alta resposta do sensor ( R 0 / R H2 =19,5) para microconcentração (40 ppm H 2 ) de hidrogênio. É muito melhor em comparação com as características correspondentes do sensor baseado em Pd / SnO 2 nanomaterial estudado em [31] onde a resposta do sensor a 50 ppm H 2 é igual a R 0 / R H2 =15,9 e o tempo de resposta e recuperação são iguais a t 0,9 =120 se τ 0.1 =15 min.
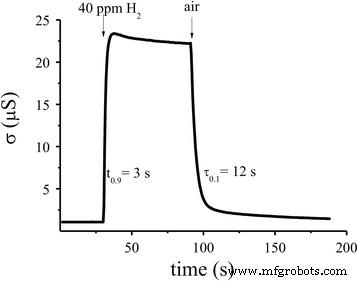
Mudança na condutividade versus tempo para o sensor dopado com Pd ideal (0,09% Pd / SnO 2 ) na temperatura do sensor 261 ° C
Os resultados no estudo de seletividade para H 2 para os sensores S 2 contendo 0,09% em peso de Pd ( T =261 ° C) na presença de CO e CH 4 são mostrados na Fig. 8. Comparação da resposta do sensor para H 2 , CH 4 , ou CO da mesma concentração (500 ppm) mostra que a resposta do sensor a H 2 é muito maior do que para CH 4 ou CO. É por isso que a presença de CH 4 ou CO de concentração de 500 ppm na mistura de gás analisada com 500 ppm de H 2 praticamente não influencia na medição de hidrogênio (Fig. 8). Essa influência também está ausente para a medição da microconcentração de H 2 (20 ppm) no caso de sua mistura com 500 ppm de CH 4 ou CO. Tal comportamento dos sensores pode ser explicado por diferentes valores da temperatura ótima do sensor necessária para fornecer o valor máximo da resposta do sensor para cada um dos gases testados. A temperatura ideal do sensor para medir H 2 é muito mais baixo (261 ° C) do que para CH 4 (382 ° C) e CO (327 ° C). Temperatura baixa do sensor para medir H 2 é explicado por uma maior atividade de H 2 em comparação com CH 4 e atividades de CO na reação de oxidação na superfície do sensor. Ausência prática de interferência do CH 4 e CO para a resposta do sensor a H 2 (Fig. 8) nas condições estudadas também pode ser explicado por uma reação de oxidação de hidrogênio predominante em execução na superfície devido à maior reatividade de H 2 em comparação com CO e CH 4 .
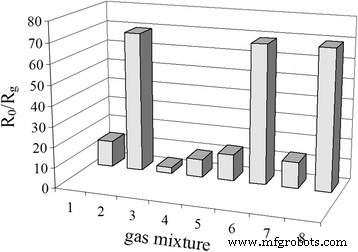
Resposta do sensor S 2 contendo 0,09% em peso de Pd ( T =261 ° C) após exposição à mistura de gás analisada de ar com 1 20 ppm H 2 , 2 500 ppm H 2 , 3 500 ppm CH 4 , 4 500 ppm CO, 5 20 ppm H 2 + 500 ppm CH 4 , 6 500 ppm H 2 + 500 ppm CH 4 , 7 20 ppm H 2 + 500 ppm CO e 8 500 ppm H 2 + 500 ppm CO
Estabilidade da resposta do sensor de operação de longo prazo para dois sensores S 2 com base em 0,09% Pd / SnO 2 nanomaterial durante 6 meses foi estudado. Verificou-se que os sensores S 2 não perderam suas respostas do sensor e não tiveram nenhum desvio direcionado da resposta do sensor após 6 meses de operação do sensor (Fig. 9). Este resultado mostra a possibilidade de aplicar os sensores criados na prática.
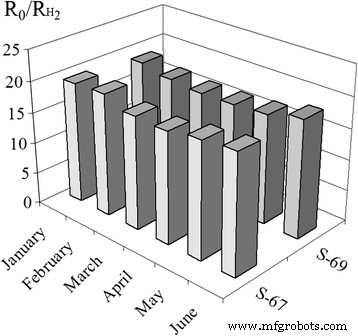
Resposta a 40 ppm H 2 dos sensores S 2 (S-67 e S-69) com base em 0,09% Pd / SnO 2 nanomaterial durante 6 meses de sua operação na temperatura do sensor 261 ° C
Conclusões
Mudança das condições de tratamento de alta temperatura dos sensores com base em Pd / SnO 2 levou a formar partículas menores de nanomaterial da camada sensível ao gás do sensor que permitiu atingir um valor significativo de resposta do sensor ( R 0 / R H2 =19,5) para microconcentração de hidrogênio (40 ppm) na temperatura do sensor 261 ° C. Os sensores criados podem medir hidrogênio em uma ampla faixa de sua concentração (2–1089 ppm H 2 ), tem um limite baixo de H 2 detecção e demonstrar uma resposta rápida e tempo de recuperação. Os sensores criados são estáveis durante sua operação de longo prazo.
Nanomateriais
- Funcionamento do sensor virtual e suas aplicações
- Sensor de ocupação funcionando e suas aplicações
- Sensor de porta funcionando e suas aplicações
- Fundamentos de sensores magnéticos digitais
- Compreendendo os sensores
- Sensor de posição sem contato indutivo
- Sensores eliminam faíscas em veículos de hidrogênio
- Sensores vestíveis detectam vazamentos de gás
- Os sensores eliminam o risco de faíscas em veículos a hidrogênio
- Sensor de fluxo e temperatura Lab-On-Chip



