Efeitos do pH microambiental do lipossoma na estabilidade química do fármaco carregado
Resumo
O lipossoma é um sistema transportador promissor para a entrega de moléculas bioativas. No entanto, a entrega bem-sucedida de moléculas sensíveis ao pH ainda é limitada pela instabilidade intrínseca das cargas úteis no ambiente fisiológico. Aqui, desenvolvemos um sistema especial de lipossomas que possui um microambiente ácido na câmara aquosa interna para melhorar a estabilidade química de cargas úteis sensíveis ao pH. Foram preparados lipossomas carregados com curcumina (Cur-LPs) com valores de pH interno variados (pH 2,5, 5,0 ou 7,4). Esses Cur-LPs têm tamanho de partícula semelhante de 300 nm, estabilidades físicas comparáveis e perfis de liberação in vitro análogos. Curiosamente, a estabilidade química da curcumina lipossomal em 50% de soro fetal bovino e sua eficácia anticâncer in vitro são ambas dependentes do pH microambiental (Cur-LP-2.5> Cur-LP-5.0> Cur-LP-7.4). Essa estabilidade do soro ainda tem espaço para ser aprimorada para melhorar a aplicabilidade do Cur-LP. Em conclusão, a criação de um microambiente ácido na câmara interna do lipossoma é viável e eficiente para melhorar a estabilidade química de cargas úteis sensíveis ao pH.
Histórico
O lipossoma, um veículo de membrana artificial, tem mostrado grande potencial na liberação de fármacos devido à sua capacidade de carga, biodegradabilidade e biocompatibilidade [1,2,3,4]. O lipossoma clássico é semelhante às células vivas em estrutura, normalmente consistindo em uma bicamada de fosfolipídeo e uma câmara interna aquosa [5,6,7]. Devido a esta estrutura, o lipossoma é capaz de solubilizar as moléculas insolúveis do fármaco e prevenir o fármaco carregado do ambiente fisiológico hostil [8,9,10]. Além disso, a superfície do lipossoma pode ser modificada para prolongar o tempo de circulação sanguínea e / ou atingir tecidos específicos [11,12,13,14,15]. Com essas vantagens acima mencionadas, vários sistemas de lipossomas foram clinicamente aprovados [8, 9, 16].
Embora a distribuição de muitos medicamentos tenha sido melhorada pela incorporação em lipossomas, a distribuição de alguns medicamentos sensíveis ao pH ainda é limitada pela instabilidade da própria molécula do medicamento no ambiente fisiológico (valores de pH neutros). Geralmente, o lipossoma é preparado em uma solução tampão neutra e, portanto, as moléculas do fármaco carregadas também estão em um ambiente neutro após a incorporação no lipossoma. Consequentemente, aquelas moléculas que são estáveis apenas em ambiente ácido seriam ainda instáveis, mesmo na forma de lipossoma. Portanto, o desenvolvimento de uma nova abordagem para aumentar a estabilidade de drogas sensíveis ao pH é de grande importância para a entrega bem-sucedida dessas cargas pelo lipossoma.
Como mencionado acima, o lipossoma tem um espaço aquoso em sua câmara interna, que pode ser usado para fornecer cargas úteis de drogas com um microambiente ácido (Fig. 1). Neste presente trabalho, usamos a curcumina como um fármaco modelo e visamos fornecer uma nova abordagem para aumentar a estabilidade química de moléculas de fármaco carregadas em lipossomas. É bem conhecido que a curcumina é uma molécula lipofílica e tem sido amplamente utilizada em alimentos, medicamentos e cosméticos devido às suas várias bioatividades [17,18,19,20,21]. No entanto, sua entrega é altamente limitada por sua insolubilidade e instabilidade em fluidos biológicos [22,23,24,25]. Até o momento, ainda não cumpriu sua promessa clínica, em parte devido à instabilidade mediada pelo pH [26]. Portanto, a curcumina é um fármaco modelo adequado para este trabalho.
Esquemas do lipossoma com acidez microambiental variada em sua câmara aquosa interna
Métodos
Materiais
Os fosfolípidos (lecitina de soja para uso em injeção) foram adquiridos à Shanghai Tai-Wei Pharmaceutical Co., Ltd., (Xangai, China). O colesterol foi obtido da Amresco (Solon, OH, EUA). Poloxamer 188 (F68) foi gentilmente doado pela BASF (China) Co., Ltd., (Xangai, China). A curcumina foi fornecida pela Sigma (St. Louis, MO, EUA). O soro fetal bovino (FBS) foi adquirido à HyClone (Logan, UT, EUA). Todos os outros reagentes químicos usados neste estudo eram de grau analítico ou melhor.
Preparação de lipossomas carregados com curcumina (Cur-LPs)
Os lipossomas com valores de pH microambientais variados foram preparados pelo método de evaporação de acordo com trabalhos anteriores com algumas modificações [27, 28]. Resumidamente, fosfolípidos (75 mg) e colesterol (5 mg) foram dissolvidos em 0,5 ml de etanol contendo 2 mg / ml de curcumina. A solução de etanol foi misturada com 5 ml de PBS 0,001 M contendo 1% ( w / v ) F68 que serviu como um surfactante para estreitar a distribuição de tamanho. Após agitação magnética por 1 min (misturador magnético de temperatura constante, DF-101S, Zhengzhou Greatwall Scientific Industrial e Trade Co., Ltd., Zhengzhou, China), a emulsão resultante foi evaporada sob vácuo e no escuro por 30 min a 35 ° C para remova o etanol. A acidez na câmara interna do Cur-LP foi ajustada por meio do uso de PBS com valores de pH variados de 2,5, 5,0 ou 7,4 durante a preparação. A suspensão resultante foi centrifugada a baixa velocidade (3000 rpm, 5 min) para precipitar a curcumina livre. O sobrenadante foi então centrifugado em alta velocidade (16 krpm, 10 min), e os peletes foram ressuspensos em PBS (pH 7,4) antes do uso posterior. Este procedimento forneceu a esses LPs um ambiente externo idêntico. Os lipossomas obtidos com diferentes valores de pH microambientais foram apresentados como Cur-LP-2.5, Cur-LP-5.0 e Cur-LP-7.4, respectivamente. Lipossomas em branco também foram fabricados como acima.
Caracterização do lipossoma
O tamanho hidrodinâmico, distribuição de tamanho e potencial zeta são os três parâmetros básicos para sistemas de lipossomas. O tamanho e o potencial zeta de LP foram determinados por espalhamento dinâmico de luz (DLS) e espalhamento eletroforético de luz (ELS), respectivamente, usando ZetasizerNano ZS90 (Malvern Instruments Ltd., Malvern, Reino Unido) a 25 ° C [29]. O ciclo de medição foi determinado automaticamente pelo sistema do instrumento. O tamanho das partículas foi apresentado pela distribuição de intensidade, e a distribuição do tamanho foi avaliada pelo índice de polidispersidade (PDI).
Determinação da eficiência de encapsulamento (EE)
EE, um parâmetro importante para o controle de qualidade, é de grande importância no desenvolvimento de sistemas de entrega baseados em lipossomas. A determinação de EE foi baseada no método de centrifugação em alta velocidade. Resumidamente, 100 μl de Cur-LPs foram centrifugados em baixa velocidade (3000 rpm, 5 min) para precipitar a curcumina livre não dissolvida e 50 μl de sobrenadante foram submetidos a centrifugação em alta velocidade (16 krpm, 10 min) para separar Cur- LPs da minúscula curcumina dissolvida. Os pellets foram ressuspensos em 500 μl de PBS (ou seja, diluição de 10 vezes), uma alíquota de 10 μl do qual foi misturada com 300 μl de etanol por vórtice e sonicação por 30 s. A intensidade fluorescente da curcumina na solução resultante foi determinada (comprimento de onda de excitação (Ex), 458 nm; comprimento de onda de emissão (Em), 548 nm) e apresentada como F e , isto é, a intensidade fluorescente da curcumina encapsulada. Outros 50 μl de Cur-LP fresco contendo curcumina encapsulada e livre também foram diluídos 10 vezes com PBS, e 10 μl da solução diluída foram misturados com 300 μl de etanol. A intensidade fluorescente da solução resultante foi medida e apresentada como F t , isto é, a intensidade fluorescente da curcumina total. O EE foi, portanto, calculado com a seguinte equação:EE = F e / F t .
Microscopia Eletrônica de Varredura (SEM)
A morfologia do LP foi observada por microscopia eletrônica de varredura (SEM, INSPECT F, FEI, Holanda) [30]. Resumidamente, a suspensão LP foi diluída 100 vezes com água destilada e uma gota da suspensão diluída foi colocada em uma folha de vidro limpa. Após a secagem ao ar, a amostra foi revestida com ouro imediatamente antes do SEM.
Estabilidade física dos lipossomas
A estabilidade física é um parâmetro muito significativo para armazenamento e transporte de um sistema coloidal. A estabilidade física do lipossoma foi apresentada pela estabilidade coloidal e investigada de acordo com um método anterior [31]. Resumidamente, 100 μl de LP foram adicionados aos tubos e mantidos a 37 ° C. Em diferentes intervalos de tempo, o tamanho do LP foi medido e comparado ao tamanho inicial para indicar a estabilidade termodinâmica. Além disso, outros 300 μl de LP também foram adicionados aos tubos e mantidos a 37 ° C. Nos mesmos intervalos de tempo, 100 μl do líquido da camada superior foram coletados. A transmitância dos corpos-de-prova coletados foi medida a 550 nm e comparada ao valor inicial para indicar a estabilidade cinética.
Lançamento In Vitro
O perfil de liberação do lipossoma desempenha um papel importante na previsão do destino in vivo e na eficácia do lipossoma. A liberação in vitro de curcumina de Cur-LP foi estudada usando o método de diálise dinâmica [32]. Resumidamente, 1 ml de cada Cur-LP foi adicionado a um saco de diálise (peso molecular de corte, 10 kD), que foi usado para reter o lipossoma, mas manter as moléculas de curcumina liberadas permeáveis. O saco de diálise carregado com a amostra foi embebido em 4 ml de meio de liberação (0,001 M PBS contendo 0,1% Tween 80, pH 7,4), e o estudo de liberação foi conduzido longe da luz (37 ° C, 100 rpm). Em cada intervalo de tempo fixo, o meio de liberação foi coletado e substituído por 4 ml de meio fresco de modo a simular as condições de dissipação. O meio recolhido foi diluído para 5 ml com PBS e posteriormente diluído 15 vezes com etanol. A curcumina na solução resultante foi quantificada por espectrofotometria de fluorescência (Ex 458 nm, Em 548 nm). Além disso, a curcumina em pó foi dissolvida no meio de liberação acima, e a liberação da solução de curcumina foi conduzida a pH 7,4 para investigar se o saco de diálise reteria moléculas de curcumina.
Estabilidade química da curcumina lipossomal
A estabilidade química é um parâmetro chave para prever o metabolismo, eficácia e toxicidade do medicamento. A estabilidade química de Cur-LPs foi examinada em 50% de FBS. Resumidamente, 100 μl de Cur-LPs foram diluídos 10 vezes com PBS (pH 7,4) e depois misturados com 1 ml de FBS. Os espécimes foram agitados em um agitador horizontal longe da luz (37 ° C, 100 rpm). Em intervalos de tempo fixos, uma alíquota de 10 μl da amostra foi coletada e misturada com 300 μl de etanol imediatamente seguido por centrifugação (16 krpm, 5 min). A curcumina remanescente no sobrenadante foi quantificada como acima.
Eficácia anticâncer in vitro
A eficácia anticâncer preliminar dos três Cur-LPs foi investigada usando células HepG2 de carcinoma hepatocelular de fígado humano. Resumidamente, as células HepG2 foram semeadas em placas de cultura de células de 96 poços a uma densidade de 10.000 células por poço e cultivadas sob condições padrão (37 ° C / 5% CO 2 ) por 24 h em meio de cultura PRIM-1640 suplementado com 10% de FBS. Posteriormente, o meio de cultura foi removido e as células foram lavadas com PBS. Os Cur-LPs foram diluídos em meio de cultura sem soro (4 μg / ml de curcumina) e adicionados às células, seguido de incubação contínua por 1 e 3 dias a 37 ° C. O valor de DO de células viáveis foi medido pelo ensaio cck-8. As células tratadas com meio de cultura em branco serviram como controle e a viabilidade celular (%) foi o valor de DO percentual das amostras em relação ao controle.
Estatísticas
Todos os dados são apresentados como média ± dp (desvios padrão). As diferenças entre dois grupos, analisadas por t do Aluno teste, foram considerados estatisticamente significativos quando o p o valor era inferior a 0,05.
Resultados e discussão
Caracterização do lipossoma
O pH microambiental do lipossoma refere-se à acidez na câmara aquosa interna do lipossoma (Fig. 1), que é diferente do pH do ambiente externo. Neste trabalho, o pH ambiental externo de todas as suspensões de lipossomas foi de 7,4, a menos que indicado de outra forma.
Tamanho de partícula, potencial zeta e eficiência de encapsulamento (EE) são parâmetros importantes para o controle de qualidade do lipossoma. O tamanho de três Cur-LPs era semelhante entre si (cerca de 300 nm, Fig. 2a). O PDI de cada formulação foi inferior a 0,2, indicando uma distribuição de tamanho estreita. Curiosamente, o potencial zeta negativo de Cur-LP-7.4 (−9 mV) é significativamente menor do que o dos outros dois Cur-LPs (~ −18 mV). Normalmente, o potencial zeta negativo diminuiria e até mesmo se converteria em valor positivo com a diminuição do pH da fase dispersa devido ao aumento de H + concentração. De fato, observamos esse fenômeno ao preparar Cur-LPs em soluções não tampão de HCl / NaOH com pH de 2,5, 5,0 e 7,4 (Fig. 2b). No caso do PBS, entretanto, a existência do PO 4 3− , HPO 4 2− , e / ou H 2 PO 4 - e sua interação com o LP pode levar a situações mais complicadas e resultados diferentes. É bem conhecido que o potencial zeta desempenha um papel fundamental na manutenção da estabilidade coloidal da suspensão em nanoescala. Em geral, um valor absoluto mais alto de potencial zeta leva a um sistema de suspensão coloidal mais estável.
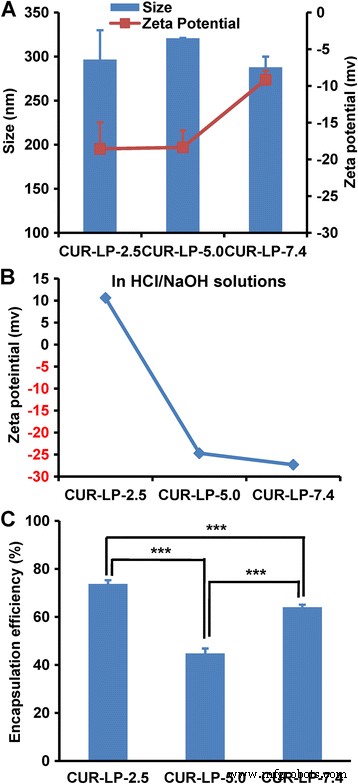
Caracterização físico-química de lipossomas. a Tamanho hidrodinâmico e potencial zeta de Cur-LPs fabricados em PBS com pH 2,5, 5,0 e 7,4, respectivamente. b Potencial zeta de Cur-LPs fabricados em soluções de HCl / NaOH com pH 2,5, 5,0 e 7,4, respectivamente. c Eficiência de encapsulação de Cur-LPs preparados em PBS. Dados apresentados como média ± dp ( n =3). Significância estatística entre os grupos:*** p <0,001
EE é uma preocupação durante o desenvolvimento de lipossomas. Normalmente, aumentar a EE é importante para reduzir custos e aumentar a eficácia. Neste trabalho, o EE de Cur-LP-2.5 é de 74% (Fig. 2c), que é o maior entre Cur-LP-5.0 (45%) e Cur-LP-7,4 (64%), indicando que Cur- LP-2.5 é a melhor formulação para entregar curcumina do ponto de EE. As razões para a variedade de EE em diferentes valores de pH não são muito claras, mas podem estar relacionadas à solubilidade da curcumina, que é solúvel em álcali ou em solventes extremamente ácidos [33].
A morfologia dos lipossomas examinados por MEV é mostrada na Fig. 3. As partículas de LP-2.5 (Fig. 3a) e LP-5.0 (Fig. 3b) são de forma esférica e têm uma distribuição de partícula uniforme. O LP-7.4 também mostra uma forma esférica, mas a adesão entre as partículas pode ser claramente observada (Fig. 3c), indicando que o processo de secagem durante a preparação do espécime em MEV levaria à agregação do LP-7.4. Isso pode ser devido ao valor absoluto relativamente baixo do potencial zeta de LP-7.4 (Fig. 2a). Além disso, o tamanho de partícula medido por MEV é menor que o tamanho hidrodinâmico medido por DLS, o que se deve à perda da concha de hidratação do lipossoma após o processo de secagem por MEV.
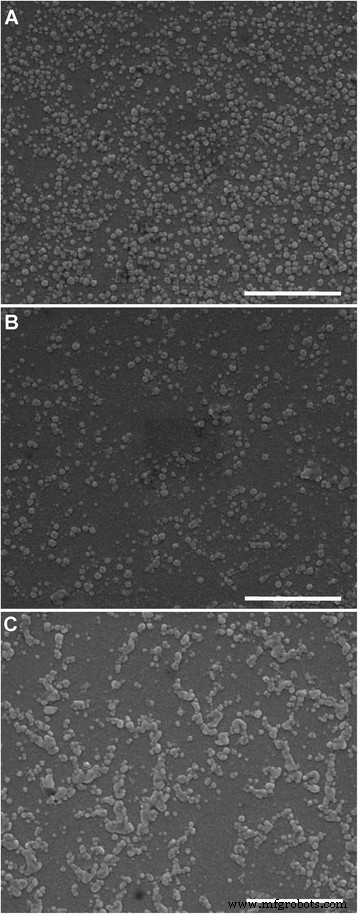
Imagens SEM de lipossomas com pH microambiental de a 2,5, b 5.0 e c 7,4 Barra de escala , 1 μm
Estabilidade física do lipossoma
O lipossoma é um sistema coloidal e sua estabilidade física pode ser apresentada pela estabilidade coloidal, que tem impactos substanciais no armazenamento do lipossoma e em outras aplicações [34, 35]. A agregação de partículas (instabilidade termodinâmica) e sedimentação (instabilidade cinética) são os dois aspectos essenciais da instabilidade coloidal. A agregação leva a um tamanho aparente maior e a sedimentação leva a mudanças na transmitância da suspensão. Mais importante, o aumento de tamanho pode afetar diretamente a eficácia dos nanossistemas, uma vez que o tamanho das partículas mostrou ter grandes impactos na captação celular, citotoxicidade, perfil farmacocinético e distribuição nos tecidos [36, 37].
Aqui, examinamos as propriedades de agregação e sedimentação de três sistemas de lipossomas para indicar sua estabilidade termodinâmica e cinética, respectivamente. Conforme mostrado na Fig. 4a, os três LPs não mostraram mudanças substanciais no tamanho hidrodinâmico em 72 h, indicando que todos esses LPs têm uma estabilidade termodinâmica muito alta. Enquanto isso, a mudança de transmitância de todos os três LPs foi inferior a 10% (Fig. 4b), indicando pouca sedimentação de partículas e, portanto, uma alta estabilidade cinética. Esses resultados sugerem que os três LPs apresentam excelente estabilidade coloidal em 72 h, sendo que o pH microambiental não tem influência na estabilidade física do lipossoma.
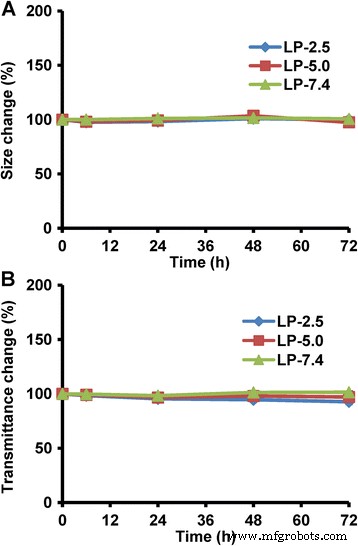
Estabilidade física de lipossomas com valores de pH microambientais variados (pH 2,5, 5,0 e 7,4). a Estabilidade termodinâmica indicando agregação de partículas. b Estabilidade cinética indicando sedimentação de partículas. Os dados são apresentados como média ± dp ( n =3)
Lançamento In Vitro
O perfil de liberação da droga do lipossoma é geralmente examinado para avaliar a qualidade da formulação, fornecer referência para o regime de dosagem e prever a eficácia in vivo. Em geral, quase todos os sistemas lipossomais têm uma propriedade de liberação sustentada de fármaco. Aqui, examinamos o comportamento de liberação in vitro de três Cur-LPs em PBS (pH 7,4). Enquanto isso, a liberação da solução de curcumina também foi examinada para confirmar se a membrana de diálise afetaria a difusão da curcumina. Conforme mostrado na Fig. 5a, a curcumina foi liberada muito rapidamente de sua solução (> 80% em 6 h), indicando que a bolsa de diálise não teve efeito sobre a difusão da curcumina. Em contraste com a liberação rápida da solução de curcumina, todos os Cur-LPs mostraram uma propriedade de liberação sustentada óbvia (Fig. 5b), e os perfis de liberação eram muito semelhantes entre si, indicando que o pH microambiental não teve efeito significativo sobre a curcumina velocidade de liberação. Em detalhes, a curcumina foi liberada um pouco mais rápido nas primeiras 8 horas, provavelmente devido à liberação inicial do burst (a porcentagem de liberação cumulativa foi em torno de 5%). Após 8 h, a curcumina foi liberada um pouco mais lentamente e a porcentagem de liberação cumulativa foi de ~ 30% em 72 h. Presume-se que a velocidade de liberação in vivo ou na presença de soro seria substancialmente mais rápida devido, em parte, ao metabolismo do lipídeo.
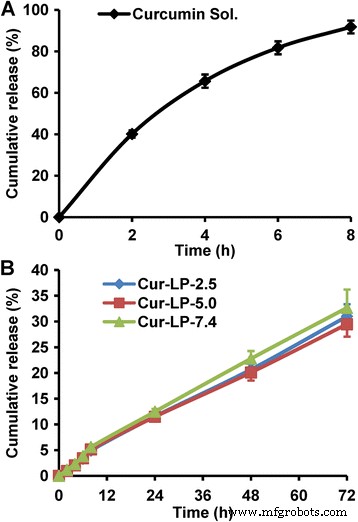
Perfis de liberação in vitro de diferentes formulações de curcumina em PBS (pH 7,4). a Solução de curcumina, na qual a curcumina foi dissolvida em PBS contendo Tween 80 a 0,1% (pH 7,4). b Cur-LPs com pH microambiental variado de 2,5, 5,0 e 7,4, respectivamente. Os dados são apresentados como média ± dp ( n =3)
Curiosamente, os perfis de lançamento de todos os três Cur-LPs são próximos de linhas retas. Portanto, foi realizado o ajuste linear aos três perfis de liberação. Conforme mostrado na Tabela 1, todos esses perfis apresentaram linearidade muito boa com grau de ajuste superior a 0,99 (equações de regressão também são exibidas), sugerindo que a liberação de Cur-LPs ajustou-se à cinética de ordem zero. Em outros estudos semelhantes, a liberação de curcumina do lipossoma foi considerada não linear [38, 39]. Do ponto de vista de pesquisa e desenvolvimento de drogas, a cinética de liberação de ordem zero é o perfil de liberação mais ideal porque fornece uma taxa de liberação de droga constante e, portanto, é capaz de manter o efeito terapêutico por um longo tempo, diminuir os tempos de administração e reduzir os efeitos colaterais . Portanto, os LPs preparados neste trabalho podem ser portadores promissores para a entrega controlada de medicamentos.
Efeito do pH microambiental na estabilidade química de Cur-LP
A estabilidade química da curcumina lipossomal em FBS é mostrada na Fig. 6. Após a incubação por 2 h, 89% de curcumina permaneceu para Cur-LP-2.5, significativamente maior do que 74% para Cur-LP-5.0 e 61% para Cur-LP -7,4 ( p <0,001). Em 4 h pós-incubação, 69% de curcumina permaneceu para Cur-LP-2.5, significativamente maior do que 53% para Cur-LP-5.0 e 40% para Cur-LP-7.4 ( p <0,01). Às 6 h pós-incubação, 55% de curcumina permaneceu para Cur-LP-2.5, ainda significativamente maior do que 43% para Cur-LP-5.0 e 34% para Cur-LP-7.4 ( p <0,05). É claro que a estabilidade química de Cur-LPs é dependente do pH microambiental:Cur-LP-2.5> Cur-LP-5.0> Cur-LP-7.4. Esta estabilidade química dependente do pH de Cur-LP é consistente com outro trabalho, que mostrou a estabilidade dependente do pH da curcumina livre [26]. A liberação in vitro foi realizada em meio isento de soro, podendo a liberação cumulativa ser de 30% em 72 h. No entanto, o estudo de estabilidade química foi realizado em solução contendo soro, em que as enzimas séricas poderiam degradar a curcumina liberada e também quebrar o lipossoma e, assim, degradar a curcumina não liberada. Esta é a razão pela qual 30% de curcumina foi liberada em 72 h no estudo de liberação in vitro, mas apenas 55% permaneceram em 6 h para Cur-LP-2.5 no estudo de estabilidade sérica.
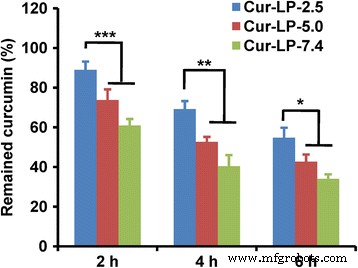
Estabilidade química da curcumina lipossomal (Cur-LPs) com valores de pH microambientais variados (pH 2,5, 5,0 e 7,4). A estabilidade foi examinada pela quantificação da curcumina remanescente após incubação de Cur-LPs com FBS a 50%. Os dados são apresentados como média ± dp ( n =3). Significância estatística entre os grupos:*** p <0,001, ** p <0,01, * p <0,05
Os lipossomas consistem em duas partes na estrutura:uma é a bicamada lipídica hidrofóbica e a outra é a câmara aquosa hidrofílica interna. É fácil entender que um fármaco hidrofílico sensível ao pH estaria localizado na câmara aquosa interna e sua estabilidade seria significativamente afetada pelo pH microambiental na câmara aquosa, onde o volume de tamponamento e a capacidade de tamponamento seriam muito maiores do que na bicamada lipídica. Em contraste, a curcumina é uma molécula hidrofóbica e estaria localizada na bicamada lipídica. Por esta razão, é bastante interessante encontrar a estabilidade química dependente do pH microambiental da curcumina lipossomal. Supõe-se que o espaço na bicamada lipídica não seria absolutamente anidro, embora seja hidrofóbico. Como sabemos, a membrana da célula viva não é absolutamente anidra em sua bicamada lipídica. Em vez disso, ele contém um certo pequeno volume de solução aquosa para o transporte de moléculas solúveis em água e íons. Da mesma forma, um certo pequeno volume de solução tampão com os mesmos componentes da câmara interna também existiria na bicamada lipídica hidrofóbica após a preparação bem-sucedida do lipossoma. Assim, o fármaco hidrofóbico localizado na bicamada lipídica pode ser diretamente afetado pelo pH microambiental do lipossoma. Além disso, o microambiente ácido pode reduzir as atividades de algumas enzimas que apresentam melhor atividade em condições fisiológicas normais. Isso também contribui para a maior estabilidade química da curcumina lipossomal no pH microambiental mais baixo. Foi relatado que os lipossomas compostos de fosfatidilcolina de ovo (EPC) perderam rapidamente seu gradiente de pH interno em tampão (pH 7,4), e a capacidade de manutenção do gradiente de pH foi substancialmente aumentada pela substituição de EPC (temperatura de transição de fase ( T m ) ≈ −5 ° C) com o alto T m (41 ° C) lipídio DPPC (dipalmitoil fosfatidilcolina) e por adição de colesterol [40]. Neste presente trabalho, o lipossoma é composto por lecitina de soja ( T m é cerca de 238,2 ° C [41]) e colesterol. Portanto, pode-se esperar que o gradiente de pH microambiental dos lipossomas preparados neste trabalho se mantenha por um longo período. Este é um forte suporte para os resultados e premissas mostrados acima.
Eficácia anticâncer in vitro
Demonstramos a estabilidade química dependente do pH microambiental da curcumina lipossomal acima. Aqui, conduzimos um estudo preliminar in vitro para investigar a eficácia anticâncer dessa curcumina lipossomal. Curiosamente, os LPs em branco poderiam aumentar o crescimento celular no dia 1 e manter essa função até certo ponto até o dia 3 em comparação com o grupo de controle (Fig. 7). Isso indica que os LPs em branco podem fornecer nutrição às células, o que é consistente com nosso relatório anterior [27]. A curcumina livre mostrou pouca eficácia anticâncer devido à sua solubilidade bastante limitada. Em contraste, Cur-LPs demonstrou eficácia anticâncer significativa de uma maneira dependente do pH microambiental. Após o tratamento por 1 dia, Cur-LP-2.5 e Cur-LP-5.0 mostraram uma capacidade significativamente mais forte de inibir o crescimento de células HepG2 do que Cur-LP-7.4 (a viabilidade celular foi de 80% para Cur-LP-2.5 e Cur-LP -5,0 e 90% para Cur-LP-7.4). No dia 3 pós-tratamento, a viabilidade celular diminuiu substancialmente, e Cur-LP-2.5 e Cur-LP-5.0 mostraram eficácia anticâncer comparável e significativamente maior do que Cur-LP-7.4. A viabilidade celular foi de 24% para Cur-LP-2.5 ( p <0,05 vs Cur-LP-7.4), 21% para Cur-LP-5.0 ( p <0,01 vs Cur-LP-7.4) e 39% para Cur-LP-7.4. Estes resultados indicam que a eficácia anticancerígena da curcumina lipossomal depende do pH e do tempo do microambiente. Em consideração ao maior EE e estabilidade química de Cur-LP-2.5 do que Cur-LP-5.0, o lipossoma com pH microambiental de 2,5 teria o maior potencial para aplicação prática.
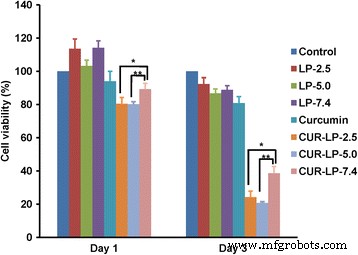
Eficácia anticancerígena da curcumina lipossomal com pH microambiental variado (2,5, 5,0 e 7,4). A viabilidade das células HepG2 nos dias 1 e 3 após o tratamento por LPs em branco, curcumina livre e Cur-LPs foi examinada pelo ensaio cck-8. As células tratadas com meio de cultura em branco contendo soro serviram como controle. Os dados são apresentados como média ± dp ( n =3). Significância estatística entre os grupos:** p <0,01, * p <0,05
Conclusões
O lipossoma, como um sistema de entrega de drogas amplamente utilizado, é capaz de melhorar a solubilidade de drogas insolúveis em água, protegendo as cargas úteis de drogas do ambiente fisiológico hostil e entregando as cargas úteis a um tecido-alvo. No entanto, a distribuição de medicamentos sensíveis ao pH ainda é limitada por sua instabilidade natural em condições fisiológicas (ambiente neutro). Neste presente trabalho, propomos uma nova abordagem para aumentar a estabilidade química de cargas úteis de fármacos sensíveis ao pH, regulando a acidez microambiental do lipossoma. Os resultados mostram que a estabilidade química e a eficácia in vitro do modelo de medicamento sensível ao pH, a curcumina, é significativamente aumentada pela acidificação do microambiente do lipossoma. Em conclusão, a regulação do pH microambiental do lipossoma é viável para aumentar a estabilidade química de cargas úteis de fármacos sensíveis ao pH, mesmo para os fármacos hidrofóbicos que estão localizados na bicamada lipídica.
Nanomateriais
- Moagem Química de Liga de Titânio
- Propriedades físicas e químicas do tungstênio
- Propriedades químicas do titânio
- O que é deposição de vapor químico?
- Efeitos de circuito
- Adesivo de nicotina
- Nanofibras e filamentos para entrega aprimorada de drogas
- Reaproveitamento de drogas
- Os 4 principais plásticos resistentes a produtos químicos
- Torno horizontal promove estabilidade



