O efeito do plasma sem equilíbrio de contato nas propriedades estruturais e magnéticas de Mn Х Fe3 - X О4 Spinels
Resumo
Ferritas de manganês nanométricas Mn х Fe 3 - х О 4 ( х =0-1,3) foram preparados usando plasma de contato sem equilíbrio (CNP) em dois pH diferentes (11,5 e 12,5). A influência das condições de síntese (por exemplo, razão catiônica e pH inicial) na composição da fase, tamanho do cristalito e propriedades magnéticas foram investigadas empregando difração de raios-X (XRD), análise térmica diferencial (DTA), infravermelho por transformada de Fourier (FTIR), varredura microscopia eletrônica (SEM), microscopia eletrônica de transmissão (TEM) e técnicas de medição magnética. A formação de partículas de ferrita facetadas monodispersas em х =0–0,8 foi mostrado. Os espectros de FTIR revelaram reflexão na região 1200–1700 cm −1 causada pela presença de água adsorvida na superfície do Fe 3 - x Mn x O 4 microgrânulos ou embutidos em sua estrutura cristalina. A maior sensibilidade dos espectros de reflexão às mudanças de composição ocorre dentro de 400–1200 cm −1 intervalo, típico para as vibrações de alongamento de Fe (Mn) –O (até 700 cm −1 ), Fe (Mn) –OH e Fe (Mn) –OH 2 ligações (mais de 700 cm −1 ) Os resultados de XRD mostraram que o nanocristalino Mn х Fe 3 - х О 4 (0 < x <1,0) tinha estrutura de cristal de espinélio cúbico com tamanho médio de cristalito 48-49 A. A diminuição do tamanho cristalino com o x aumento também foi observado.
Histórico
A capacidade dos espinelos nanodispersivos com metais polivalentes de formar uma série de soluções e compostos sólidos oferece possibilidades ilimitadas de controlar as propriedades tecnológicas dos compostos dos espinelos. Por muito tempo, grande atenção de muitos pesquisadores tem sido dada às investigações de ferritas de manganês (Fe 3 O 4 - Mn 3 O 4 sistema) devido à sua ampla aplicação na indústria. Eles são amplamente utilizados em fornos de microondas e dispositivos de armazenamento magnético, bem como catalisadores altamente ativos na produção de hidrogênio via desidrogenação de metano em etileno ou acetileno, adsorventes [1,2,3,4,5,6].
A síntese de espinélio de ferrita de manganês é tecnologicamente complexa. Atualmente, existem poucos métodos para a síntese de partículas de ferrita de manganês, como cerâmica [7], coprecipitação [8,9,10,11,12], método hidrotérmico [13], micela reversa [14, 15], sol- gel [16], método de combustão [17], mecanossíntese [18,19,20], tecnologias de alta energia [21, 22] e dopagem mecânica [23, 24]. Os métodos de hidrofase permitem regular a composição, cristalinidade e morfologia das partículas.
Tais métodos foram estudados por muitos pesquisadores e são aplicados com sucesso para a síntese de ferritas [9, 25, 26] com tamanho de partícula de 30–50 nm a 50–150 ° С, que é significativamente menor do que para a tecnologia de cerâmica. Os métodos de hidrofase, via de regra, incluem vários estágios:o primeiro - deposição, o segundo - síntese direta de ferrita, realizada devido à oxidação, envelhecimento, etc. Os métodos para início do segundo estágio principal de síntese de ferrita usando tratamento de ultrassom, microondas influência, ultravioleta e várias descargas [27,28,29] têm sido usadas recentemente. Durante o tratamento de soluções com descarga de CNP, ocorre um complexo complexo de reações químicas envolvendo partículas radicais e elétrons livres. Os principais produtos dessas interações são oxigênio, hidrogênio e peróxido de hidrogênio. A atividade oxidativa de soluções plasmoquimicamente "ativadas" pode ser usada para a síntese de compostos de óxidos complexos.
O espectro de emissão [30,31,32] mostrou que as principais contribuições para o espectro de emissão do plasma de vapor d'água são OH, hidrogênio atômico e o radical oxigênio. No caso do modo de bolha, quando as serpentinas enchem toda a bolha, uma emissão significativa do segundo sistema positivo de nitrogênio e do íon de nitrogênio (primeiro sistema negativo). A descarga opera em dois modos diferentes. Para pequenas condutividades do líquido, a descarga é uma descarga direta do streamer de líquido (modo líquido). Este modo é semelhante às chamadas descargas corona típicas na água. Para condutividades acima de 45 μS cm −1 uma grande bolha de vapor é formada. No modo bolha, os streamers estão localizados na interface líquido-bolha. A eficiência de formação do peróxido de hidrogênio depende da potência com um máximo para potências intermediárias. A eficiência de formação de peróxido de hidrogênio é significativamente menor no modo de bolha do que no modo líquido. No trabalho [33], foram estimados os parâmetros cinéticos dos elétrons para a descarga da barreira dielétrica com um eletrodo líquido à pressão atmosférica. Assim, podemos supor que o CNP possuirá atividade química no que diz respeito à sua aplicação na realização dos diferentes processos oxidativo-redutivos.
Nossos estudos preliminares de tratamento de soluções com plasma mostraram que a composição da solução oxidante sintetizada depende de uma ampla gama de fatores [29]. O uso do CNP garante alto grau de homogeneidade na distribuição dos componentes tanto na solução inicial quanto no produto formado durante a oxidação, o que estimula a interação efetiva entre eles com formação de ferritas com estrutura e composição homogênea.
O objetivo do trabalho é estudar a possibilidade de obtenção de nanopartículas Mn Х Fe 3 - Х О 4 espinélio de soluções aquosas usando plasma de contato fora de equilíbrio. Como as ferritas são soluções sólidas, é importante estabelecer o grau de sua homogeneidade estrutural e de concentração nas condições de síntese selecionadas. O método experimental consistiu na comparação do ferrospinel obtido a partir de sulfatos de manganês e ferro em diferentes proporções de cátions.
Tal pesquisa comparativa das amostras permite estabelecer a influência da composição química da solução inicial e das condições de síntese no estado de fase estrutural dos compostos preparados por tratamento com CNP.
Métodos
Para a síntese de ferrita de manganês, os autores usaram soluções aquosas de FeSO 4 · 7H 2 O, MnSO 4 · 5H 2 O, e uma solução aquosa de NaOH foi usada como um precipitante. Usamos soluções de 0,5 M de sais de ferro e manganês. Todos os produtos químicos e solventes empregados para a síntese eram de qualidade analítica e usados como recebidos sem purificação adicional. Água desionizada foi usada como solvente em todo o procedimento.
Estudos preliminares [25] mostraram que em pH <11 óxidos e oxihidróxidos não magnéticos foram formados, então dois conjuntos de amostras foram preparados. O primeiro conjunto inicial рН =11,5 e o segundo em 12,5. Os compostos coprecipitados foram preparados vertendo, sob agitação contínua, a mistura correspondente de soluções de sulfato com a razão catiónica necessária. O tratamento posterior foi realizado com CNP.
O tratamento foi realizado em um reator cilíndrico com diâmetro interno de 45 mm e altura de 85 mm. A mistura de reação foi resfriada pela circulação contínua de água fria na camisa externa. Um dos eletrodos de aço inoxidável (diâmetro 4 mm) foi localizado na parte inferior do reator, e o outro (diâmetro 2,4 mm) foi localizado 10 mm acima da superfície da solução. A tensão inicial foi fornecida ao transformador elevador. A corrente CA da bobina secundária foi entregue ao retificador de ponte e, em seguida, agora a tensão pulsante, foi entregue por meio de um resistor de lastro para os eletrodos do reator. A unidade de ignição foi adicionalmente conectada ao ânodo. Essa unidade formou pulsos com amplitude de até 15 kV e largura de 1,5 ms. Os pulsos foram sincronizados estritamente com a fase da tensão pulsante. No instante em que o pulso de ignição foi formado, houve uma quebra entre os eletrodos do reator no espaço de vácuo criado pela rarefação para 0,06–0,08 MPa. A resistência caiu drasticamente e uma corrente anódica começou a fluir, criando assim uma descarga. A tensão de queima da descarga permaneceu quase inalterada em 750–900 V. A corrente na lacuna de descarga foi determinada pela resistência do plasma e a tensão aplicada ao sistema formado pela descarga do plasma e o controlador de lastro. A tensão foi controlada pelo princípio do método de fase, isto é, a tensão anódica média aplicada ao reator dependia da fase da tensão pulsante no anodo e do instante em que um pulso de ignição foi entregue.
O plasma apareceu no instante da ignição e se extinguiu com o término das pulsações de voltagem anódica (Fig. 1). A frequência de repetição do processo foi de 100 Hz. A corrente de descarga foi controlada alterando o instante de ignição em relação à fase das pulsações de tensão do ânodo com um dispositivo de sincronização. A duração do tratamento com plasma variou de 10 a 40 min. Todos os precipitados foram lavados até a reação negativa no íon sulfato. Os precipitados lavados e filtrados foram secos a 150 ° С. Propriedades magnéticas relativas (de magnetização de saturação I S (emu 2 / g), força coercitiva Нс (Oe)) foram avaliados por magnetômetro [29].

O pilar de plasma sem equilíbrio de contato entre o eletrodo na fase gasosa e a superfície do líquido
A concentração de Mn 2+ nas amostras obtidas foi determinada complexometricamente. A concentração de ferro foi determinada pelos métodos do permanganato e bicromato. Para monitorar o processo de reação, o reator foi equipado com um sistema de eletrodos. O [Fe 2+ ] / [Mn 2+ ] proporção em Mn х Fe 3 - х О 4 composto foi calculado de acordo com a fórmula:
$$ \ frac {C _ {\ mathrm {Mn}}} {C _ {\ mathrm {Fe}}} =\ frac {x} {3-x} $$
e os valores eram iguais a х =0; 0,2, 0,4, 0,6, 0,8, 0,9, 1, 1,1, 1,2 e 1,3 foram escolhidos. Espectro de reflexão infravermelho com transformada de Fourier de ferritas de manganês Mn x Fe 3 - x O 4 ( x =0,0, 0,2, 0,4, 0,6, 0,8, 0,9, 1,0, 1,1, 1,2, 1,3) foram medidos dentro de 400-4000 cm −1 usando um espectrômetro de infravermelho com transformada de Fourier (FTIR) Nicolet iS10. Para estudar as transformações que ocorrem com o aquecimento dos pós obtidos, usamos a análise térmica diferencial (DTA) e a análise termogravimétrica diferencial (DTG). As curvas DTA, TG de perda de massa e DTG de taxa de perda de massa foram registradas no Derivatograph Q-1500D (F. Paulik, J. Paulik e L. Erdey). A temperatura variou na faixa de 20–1000 ° C a uma taxa de aquecimento de 10 ° / min. γ-Al 2 O 3 foi usado como uma referência. A massa de cada amostra era de 200 mg. A morfologia dos pós de ferrita e o tamanho das partículas foram estudados em microscopia eletrônica de varredura. A composição de fase (XRD) e a estrutura das amostras de ferrita foram estudadas usando difratômetro de raios-X DRON-2 em Cо-K monocromatizado α radiação. O tamanho do cristalito e o grau de micro deformação foram calculados usando o método de aproximação. O tamanho e a forma das partículas foram determinados usando microscópio eletrônico “Jem 1010” (JEOL) com tensão de trabalho de 200 kV. Microscopia eletrônica de varredura com microanálise de raios-X foi realizada usando REMMA-102 (SELMI, Ucrânia).
Resultados e discussão
As propriedades dos materiais magnéticos baseados em ferritas de manganês dependem de seu estado estrutural e de fase. A síntese de tais ferritas requer a preparação de um produto monofásico com estrutura espinélica sem óxido de ferro residual ou outras fases, que são produtos intermediários da formação de ferrita a partir dos óxidos. Em par com a composição da fase, as propriedades magnéticas são significativamente influenciadas pela oxidação dos cátions de ferro e manganês e pelo caráter de sua localização no local da rede cristalina do espinélio. Sabe-se que cátions divalentes (Zn 2+ , Mn 2+ ) estão localizados principalmente em posições tetraédricas e trivalentes (Fe 3+ ) —Em posições octaédricas da rede de cristal do espinélio. De acordo com a teoria de relaxação de Néel, tal arranjo fornece valor máximo de magnetização do material. Durante a preparação de ferritas, oxidação de Mn 2+ para Mn 3+ é possível, o que pode ser acompanhado pela redução de Fe 3+ para Fe 2+ e rearranjo de cátions em sub-redes, com transferência parcial de Fe 2+ em tetraédrico e Mn 3+ —Em nós octaédricos da rede cristalina, que impacta negativamente as propriedades magnéticas das ferritas. Oxidação de Mn 2+ ocorre na taxa mais alta em 900–1000 ° С, e em condições ideais para sinterização de ferritas de manganês para tecnologia de cerâmica - 1000–1200 ° С. Os dados disponíveis em várias fontes da literatura sobre a discussão da estrutura magnética e propriedades das ferritas de manganês são contraditórios, o que provavelmente está relacionado à variação no arranjo dos íons de ferro e manganês e sua polivalência. Os dados da dependência do parâmetro de rede no valor de х no caso de várias tecnologias, é possível assumir o caráter de arranjo catiônico na rede.
Os resultados da avaliação das amostras preparadas podem ser formulados da seguinte forma:todas as amostras incluem água quimicamente ligada em várias quantidades. Em ambos os conjuntos, o maior teor de água é encontrado em amostras com х =0,4, 1,1… 1,3. O primeiro conjunto apresentou propriedades magnéticas fracas (Figs. 2 e 3), por isso não foi considerado em detalhes.
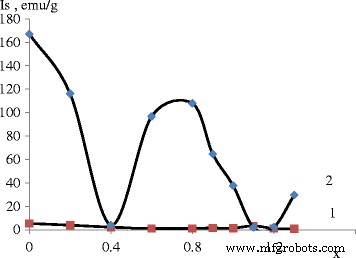
Dependência da magnetização de saturação na razão molar catiônica em diferentes рН:1 — рН =11,5 e 2 — рН =12,5
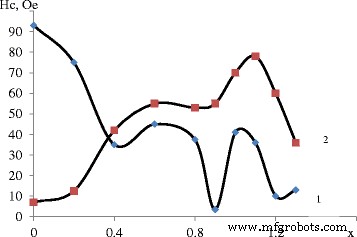
Dependência da força coerciva na razão molar catiônica em diferentes рН:1 — рН =11.5 e 2 — рН =12.5
Como pode ser visto na Fig. 1, existem algumas diferenças na magnetização de saturação de ambos os conjuntos. O valor mais alto para o conjunto 1 corresponde à proporção 1,1 Mn 1,0 Fe 0,9 Mn 0.1 О 4 . O valor mais alto é alcançado em рН =12,5 e proporção de х =0,8 (Mn 0,8 Fe 0,2 Fe 2 О 4 ) Essa proporção é diferente da ferrita de manganês estequiométrica.
Ao avaliar a magnetização de saturação, pode-se dizer que a amostra nos. 1, 2, 3 e 8 têm valores mais baixos devido à sua estrutura amorfa e presença de fases não magnéticas.
A Figura 4 mostra os padrões de XRD de amostras do segundo conjunto. Os padrões de XRD podem ser divididos em duas categorias - primeiras amostras 6–10 que têm estrutura de cristal monofásica correspondente à ferrita de fase espinela (JCPDS 10-0467). Linhas relativamente nítidas e intensas de ferritas de fase espinélica podem ser observadas nos padrões de XRD das amostras. As linhas relacionadas às fases de óxido de Fe 2 O 3 e MnO x estão ausentes nos padrões de XRD (Fig. 4).
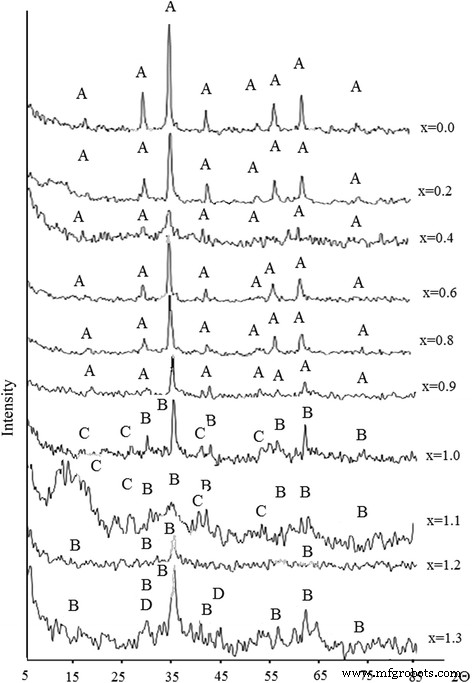
Padrões de XRD de ferrita obtidos em diferentes proporções de componentes (Tabela 1):A — Fe 3 O 4 , B — MnFe 2 O 4 , C — Mn 3 O 4 e D — β-MnO 2
O segundo conjunto tem menos cristalino com poucas fases presentes. Nos padrões de DRX das amostras, preparadas com maior teor de manganês, as linhas são ligeiramente alargadas, o que pode indicar alterações em sua estrutura em comparação com a amostra estequiométrica. A presença de outras fases no caso de maior teor de manganês foi constatada pelo método XRD. Os picos amplos podem ser observados em padrões de XRD, que podem ser indexados como (311) de fase espinélio de ferrita (JCPDS 74-2403). Na região dos ângulos correspondentes às linhas de maior intensidade para Fe 3 O 4 e Mn 3 O 4 , é observado um halo de baixa intensidade, o que pode indicar a presença desses óxidos nas amostras. Existe uma correlação clara entre as características magnéticas e o grau de cristalinidade e homogeneidade do produto.
Levando em consideração que Mn 2+ cátions são os maiores de todos, pode-se supor que, como o valor de x aumenta, é possível aumentar o parâmetro de rede. A análise dos padrões de XRD (Fig. 5) mostra que o parâmetro da rede cristalina а =8,4196 À (para ferrita de manganês tetragonal estequiométrica MnFe 2 O 4 а =8,51 À). O valor visivelmente menor do parâmetro de rede pode ser explicado com a formação de ferrita de manganês em рН =12,5 seguindo o mecanismo de formação de magnetita. Após a oxidação de Mn 2+ :
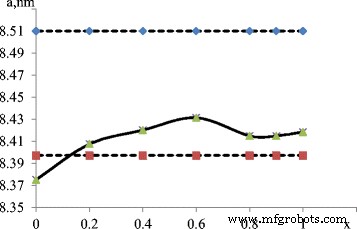
Dependência do parâmetro de rede cristalina na razão catiônica х
3Mn 2+ → 2Mn 3+ + □
vagas são formadas, o que facilita a redução dos parâmetros de rede. A magnetita é formada no segundo conjunto, e a substituição gradual de cátions de ferro por cátions de manganês leva à redução das propriedades magnéticas para a proporção de 0,4 (o primeiro pico) após 1-1,1, correspondendo à ferrita de manganês estequiométrica. Análise das Figs. 2 e 3 permite estabelecer que a formação dos compostos do segundo conjunto ocorre de acordo com o mecanismo de formação da maghemita.
Conforme indicado na Tabela 1, ferrita Mn Х Fe 3 - X О 4 foi obtido no nanorange. O tamanho médio de cristalito de nanopartículas Mn Х Fe 3 - X О 4 variaram de 5 a 8 nm e atingiram um máximo em x =0. O Mn calculado Х Fe 3 - X О 4 o tamanho cristalino excedeu o tamanho do cristalito de ferrita na imagem TEM em quatro vezes devido à agregação de nanopartículas.
Além disso, a Tabela 1 mostra a variação da temperatura de Curie, parâmetro de rede com razão x em FeMn 2 - x O 4 . A temperatura de Curie diminui à medida que o conteúdo de manganês de cátions aumenta. Como se pode saber, a temperatura de Curie é determinada principalmente pela interação de super troca mais forte em ferritas. Os fatores que diminuem essa interação levam a uma diminuição da temperatura de Curie. Com o aumento do teor de manganês, o parâmetro de rede aumenta (Tabela 1). Isso leva a um aumento nas distâncias iônicas e também a uma diminuição na temperatura de Curie.
O presente pressuposto requer um estudo adicional. A análise dos padrões de derivatografia indica a formação de ferrita de manganês nas amostras nos. 4 e 5 e isomorfismo de propriedades para as amostras 5–10 (Fig. 6). Os compostos de várias composições são formados nas amostras 1–5. As menores perdas de massa também são observadas para composições estequiométricas. As primeiras regiões dos padrões de derivatografia demonstram vários efeitos endo e exotérmicos correspondentes à oxidação do manganês e dos cátions de ferro. A região de alta temperatura corresponde ao rearranjo da rede cristalina (endo-efeitos sem alterar a massa).
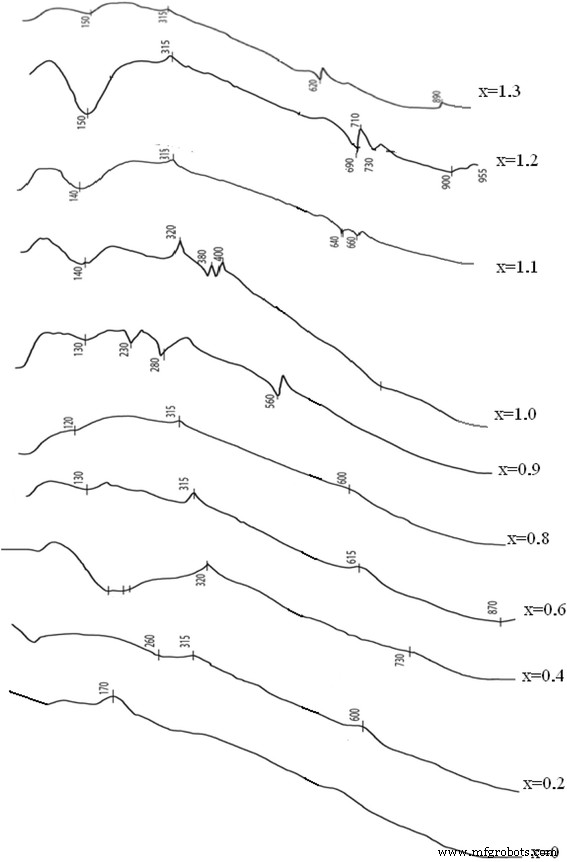
Padrões de derivatografia de amostras sintetizadas em рН =12,5
As curvas DTG demonstram que, para todas as composições, a perda de massa principal corresponde à perda de água livre a 100 ° С e ligada a 160 ° С. Para a composição 4, correspondente à ferrita estequiométrica, são observados picos exotérmicos, que correspondem à oxidação do cátion manganês a vários estados de oxidação. No trabalho [34], os autores apresentaram o seguinte conjunto de reações ocorrendo em várias temperaturas.
- 1.
3 Fe 2+ → 2Fe 3+ + □ temperatura 280 ° C
- 2.
4 Mn 3+ → 3Mn 4+ + □ temperatura 330 ° C
- 3.
3 Mn 2+ → 2Mn 3+ + □ temperatura 360 ° C
- 4.
3Mn 4+ + □ → 4Mn 3+ temperatura 420 ° C
- 5.
2Mn 2+ → Mn 3+ temperatura 600 ° C
Após o aquecimento a 450–500 ° С, uma estrutura de γ-Fe 2 O 3 tipo é formado.
Pode-se supor que os picos a 600 ° C correspondem à oxidação e redução dos cátions de ferro e manganês. A oxidação posterior é acompanhada pela transição da rede cúbica para a romboédrica, na qual todos os cátions são trivalentes. A formação de α-Fe 2 O 3 e α-Mn 2 O 3 ocorre na faixa de 600 a 1000 ° С. A análise de DRX dos produtos obtidos após aquecimento a 1000 ° С indica a presença de fase magnética de ferrita de manganês romboédrica para as amostras com razão estequiométrica de ferro e manganês formadas a partir de óxidos de ferro e manganês.
Além disso, na posição das amostras 1–10 a 1000 ° С (Tabela 1), a formação de óxido de ferro e manganês complexo ocorre por meio de mecanismo semelhante. Os compostos formados têm picos semelhantes, independentemente da composição inicial. Isso está relacionado à estrutura romboédrica, na qual todos os cátions são trivalentes. Uma vez que a hematita e a hausmanita têm estrutura semelhante, todos os padrões de XRD têm características semelhantes.
De acordo com os resultados do TEM, todas as amostras sintetizadas pelo método CNP são compostas por partículas com forma facetada regular, com tamanho variando de 50 a 100 nm (Fig. 7). O produto é monodisperso com tamanho médio de partícula de 70–80 nm. As partículas facetadas observadas são policristalinas. Os dados adquiridos usando SEM confirmam que as partículas grandes de ferrita são compostas de partículas primárias muito pequenas e seu tamanho não está de acordo com os valores calculados usando o tamanho do cristalito (Tabela 1).

Imagem TEM ( a ) e imagem SEM ( b ) da amostra no. 4 conjunto 2
É conhecido de fontes da literatura que nos padrões de IR de γ-Fe 2 O 3 e Fe 3 O 4 , existem dois grupos principais de linhas características que permitem julgar diferenças estruturais intrincadas. Estas são linhas relacionadas às vibrações das ligações М – О e М – О – Н. Introdução de diferentes íons metálicos em óxido de ferro, causando distorção de simetria do ambiente de coordenação de Fe 3+ ou mudanças na constante de ligação Fe-O, podem levar à divisão ou deslocamento das linhas características das vibrações da ligação Fe-O. No caso de distribuição homogênea de íons de natureza diferente na rede cristalina da estrutura do espinélio, geralmente podemos observar apenas o deslocamento dos máximos da linha de absorção das oscilações características.
A Figura 8 mostra os espectros de IV das amostras estudadas. A distribuição espectral acima de 1200 cm −1 é bastante independente da composição da amostra (Fig. 8).
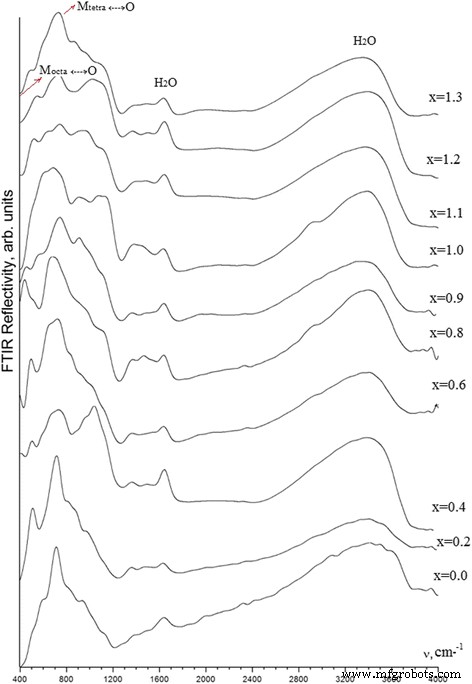
Espectros de reflexão de IV de amostras com рН =12,5 sintetizados em diferentes proporções de cátions
A reflexão nesta região é causada pela presença de água que é adsorvida na superfície do Fe 3 - x Mn x O 4 microgrânulos ou embutidos em sua estrutura cristalina. As bandas dentro de 1200–1700 cm −1 estão relacionadas às vibrações de flexão H – O – H e aquelas dentro de 2400–3700 cm −1 variação são devido às vibrações de alongamento das ligações O – H.
A maior sensibilidade dos espectros de reflexão às mudanças de composição ocorre dentro de 400–1200 cm −1 intervalo, típico para as vibrações de alongamento de Fe (Mn) –O (até 700 cm −1 ), Fe (Mn) –OH e Fe (Mn) –OH 2 ligações (mais de 700 cm −1 ) A posição espectral da banda mais intensiva é variada com o x mudando. Seu maior deslocamento, de 715 cm −1 no Fe 3 O 4 espectro ( x =0,0) até 688 cm −1 , ocorre para a amostra com x =0,8. O alargamento desta banda com o x aumento também é observado (Fig. 8). Além disso, uma nova banda em 445 cm −1 é detectado com segurança nos espectros de amostras com x =0,8 e 0,9. Além desses recursos, devemos mencionar uma redistribuição espectral significativa no x Espectro =0,4, como resultado do aumento de 1039 cm −1 banda de reflexão em relação à banda em 715 cm −1 no x =0,0 espectro.
De acordo com os dados cristalográficos, os íons de metal (Mn, Fe) podem ocupar posições com vizinhança tetraédrica e octaédrica do oxigênio [35]. As posições mais prováveis para íons de manganês na concentração de x <1.3 são as posições tetraédricas correspondentes ao Mn 2+ estado de carga. O aparecimento de íons de manganês coordenados por octaédricos com o mesmo estado de carga é detectado para os valores de x dentro de um intervalo de 0,8-1,2. O preenchimento das posições octaédricas com Mn 3+ íons começa em x =1.0, e a parte deles em x =1,3 não é mais do que 23% da quantidade total de íons de manganês [35].
Esta é a razão para explicar as mudanças observadas no x Espectro =0,8 começando o preenchimento das posições octaédricas com Mn 2+ íons.
O levantamento de 1039 cm −1 banda no x O espectro =0,4 pode estar relacionado às variações estruturais na vizinhança dos íons de metal (Mn, Fe), que resulta na mudança do momento dipolo.
Uma análise mais detalhada é, infelizmente, complicada pela sobreposição essencial de bandas ampliadas que é típica para soluções sólidas contendo complexos tetraédricos e octaédricos com átomos centrais cujas massas estão próximas umas das outras.
Conclusões
No presente trabalho, encontramos uma nova rota para a síntese de ferrita de manganês ultrafina do tipo Mn Х Fe 3 - X О 4 em um amplo Mn 2+ intervalo de substituição de x por coprecipitação com tratamento CNP. A coprecipitação seguida de tratamento com CNP é um método eficaz para a preparação de pó de ferrita de manganês. As propriedades magnéticas de Mn Х Fe 3 - X О 4 as amostras aumentaram com o aumento dos valores de pH. O processo de ferritização foi eficaz apenas em pH =12,5. A formação de compostos em pH =11,5 ocorre pelo mecanismo de formação de maghemita. Propriedades magnéticas elevadas exibiram ferrita nanodispersa obtida a pH =12,5, x =0,6–0,8. O tamanho médio dos cristalitos variou de 50 a 80 A. As ferritas nanodispersas tinham forma facetada e partículas uniformes. O padrão de XRD indica os nanocristais de fase espinélica única com estrutura espinélica cúbica em 0 < x <0,8.
A espectroscopia FTIR confirmou os resultados das medições magnéticas. A diminuição no valor da saturação magnética começando com x =1.0 é devido ao preenchimento das posições octaédricas com Mn 2+ íons.
Abreviações
- CNP:
-
Plasma sem equilíbrio de contato
- DTA:
-
Análise térmica diferencial
- DTG:
-
Análise termogravimétrica diferencial
- FTIR:
-
Transformada de Fourier Infra-vermelho
- I S :
-
Magnetização de saturação
- SEM:
-
Microscopia eletrônica de varredura
- T C :
-
Temperatura
- TG:
-
Perda de massa
- XRD:
-
Difração de raios X
- Нс:
-
Força coercitiva (Oe)
Nanomateriais
- Preparação e propriedades magnéticas de nanopartículas de espinélio FeMn2O4 dopadas com cobalto
- Síntese fácil e propriedades ópticas de pequenos nanocristais de selênio e nanorods
- Nanocompósitos de poli (N-isopropilacrilamida) magnético:efeito do método de preparação nas propriedades antibacterianas
- Síntese de pontos quânticos de sulfeto de antimônio solúvel em água e suas propriedades fotoelétricas
- Síntese fácil de óxido de estanho mesoporoso semelhante a buraco de minhoca via auto-montagem induzida por evaporação e propriedades aprimoradas de detecção de gás
- Efeito do método de síntese de La1 - xSr x MnO3 nanopartículas de manganita em suas propriedades
- Sondando as propriedades estruturais, eletrônicas e magnéticas dos aglomerados Ag n V (n =1–12)
- Influência do parâmetro de ajuste de pH para modificação de sol-gel na estrutura, microestrutura e propriedades magnéticas da ferrita de estrôncio nanocristalina
- Síntese Verde de Nanopartículas de Metal e Óxido de Metal e Seu Efeito na Alga Unicelular Chlamydomonas reinhardtii
- Síntese e propriedades de pontos quânticos de CdTe com liga de Mn com emissão de azul solúvel em água



