Eletricidade estática
Foi descoberto há séculos que certos tipos de materiais se atraíam misteriosamente depois de serem esfregados. Por exemplo, depois de esfregar um pedaço de seda contra um pedaço de vidro, a seda e o vidro tenderiam a aderir. Na verdade, havia uma força atrativa que poderia ser demonstrada mesmo quando os dois materiais estavam separados:
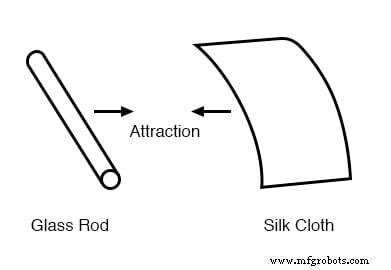
Vidro e seda não são os únicos materiais conhecidos por se comportar assim. Qualquer pessoa que já esbarrou em um balão de látex e descobriu que ele tentava grudá-lo, experimentou o mesmo fenômeno. A cera de parafina e o tecido de lã são outro par de materiais que os primeiros experimentadores reconheceram como manifestando forças atraentes após serem friccionados:
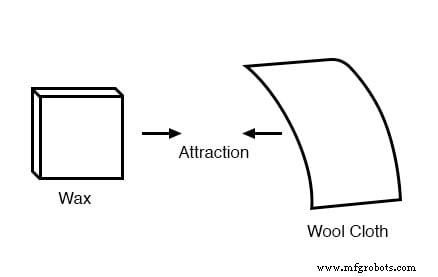
Este fenômeno tornou-se ainda mais interessante quando se descobriu que materiais idênticos, após serem friccionados com seus respectivos panos, sempre se repeliam:
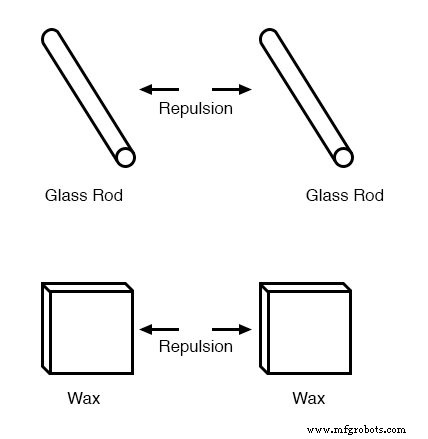
Também foi notado que quando um pedaço de vidro esfregado com seda era exposto a um pedaço de cera esfregado com lã, os dois materiais se atraíam:
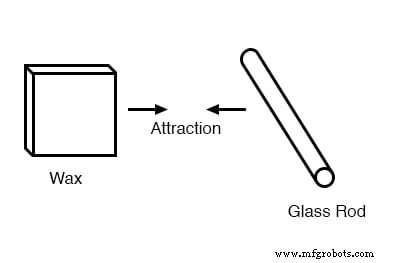
Além disso, verificou-se que qualquer material que demonstrasse propriedades de atração ou repulsão após ser esfregado poderia ser classificado em uma de duas categorias distintas:atraído pelo vidro e repelido pela cera, ou repelido pelo vidro e atraído pela cera. Era um ou outro:não foram encontrados materiais que fossem atraídos ou repelidos pelo vidro e pela cera, ou que reagissem a um sem reagir ao outro.
Mais atenção foi dirigida aos pedaços de pano usados para esfregar. Foi descoberto que depois de esfregar duas peças de vidro com duas peças de tecido de seda, não apenas as peças de vidro se repeliam, mas também os tecidos. O mesmo fenômeno ocorreu com os pedaços de lã usados para esfregar a cera:
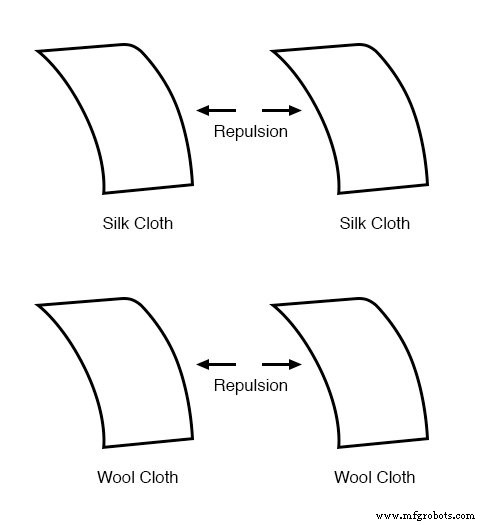
Agora, isso era realmente estranho de se testemunhar. Afinal, nenhum desses objetos foi visivelmente alterado pela fricção, mas eles definitivamente se comportaram de maneira diferente do que antes de serem friccionados. Qualquer mudança que tenha ocorrido para fazer esses materiais se atraírem ou se repelirem era invisível.
Alguns experimentadores especularam que “fluidos” invisíveis estavam sendo transferidos de um objeto para outro durante o processo de fricção e que esses “fluidos” eram capazes de efetuar uma força física à distância. Charles Dufay foi um dos primeiros experimentadores que demonstrou que havia definitivamente dois tipos diferentes de mudanças provocadas pela fricção de certos pares de objetos. O fato de haver mais de um tipo de mudança manifestada nesses materiais era evidente pelo fato de haverem dois tipos de forças produzidas: atração e repulsão . A hipotética transferência de fluido tornou-se conhecida como carga .
Um pesquisador pioneiro, Benjamin Franklin, chegou à conclusão de que havia apenas um fluido trocado entre os objetos esfregados e que as duas “cargas” diferentes não eram nada mais do que um excesso ou uma deficiência daquele fluido. Depois de experimentar com cera e lã, Franklin sugeriu que a lã grossa removesse um pouco desse fluido invisível da cera lisa, causando um excesso de fluido na lã e uma deficiência de fluido na cera. A disparidade resultante no conteúdo de fluido entre a lã e a cera causaria uma força atrativa, à medida que o fluido tentava recuperar seu equilíbrio anterior entre os dois materiais.
Postular a existência de um único "fluido" que foi ganho ou perdido através da fricção foi o melhor responsável pelo comportamento observado:que todos esses materiais caíram nitidamente em uma das duas categorias quando friccionados e, o mais importante, que os dois materiais ativos friccionaram um contra o outro. outros sempre caíram em categorias opostas como evidenciado por sua atração invariável um pelo outro. Em outras palavras, nunca houve um momento em que dois materiais esfregassem um no outro ambos tornou-se positivo ou negativo.
Seguindo a especulação de Franklin sobre a lã esfregando algo da cera, o tipo de carga associada à cera esfregada tornou-se conhecido como "negativo" (porque era suposto ter uma deficiência de fluido), enquanto o tipo de carga associado à fricção a lã passou a ser conhecida como “positiva” (porque deveria ter excesso de fluido). Mal sabia ele que sua conjectura inocente causaria muita confusão para os estudantes de eletricidade no futuro!
Medições precisas de carga elétrica foram realizadas pelo físico francês Charles Coulomb na década de 1780 usando um dispositivo denominado equilíbrio torcional medir a força gerada entre dois objetos eletricamente carregados. Os resultados do trabalho de Coulomb levaram ao desenvolvimento de uma unidade de carga elétrica chamada em sua homenagem, o coulomb . Se dois objetos "pontuais" (objetos hipotéticos sem nenhuma área de superfície apreciável) fossem igualmente carregados a uma medida de 1 coulomb e colocados a 1 metro (aproximadamente 1 jarda) de distância, eles gerariam uma força de cerca de 9 bilhões de newtons (aproximadamente 2 bilhões libras), atraindo ou repelindo, dependendo dos tipos de cargas envolvidas. A definição operacional de um coulomb como a unidade de carga elétrica (em termos de força gerada entre cargas pontuais) foi considerada igual a um excesso ou deficiência de cerca de 6.250.000.000.000.000.000 de elétrons. Ou, dito em termos inversos, um elétron tem uma carga de cerca de 0,00000000000000000016 coulombs. Sendo que um elétron é o menor portador conhecido de carga elétrica, este último valor de carga para o elétron é definido como a carga elementar .
Foi descoberto muito mais tarde que este "fluido" era na verdade composto de pedaços extremamente pequenos de matéria chamados elétrons , assim chamado em homenagem à palavra grega antiga para âmbar:outro material que exibe propriedades carregadas quando esfregado com pano.
A composição do átomo
A experimentação revelou que todos os objetos são compostos de “blocos de construção” extremamente pequenos, conhecidos como átomos e que esses átomos são, por sua vez, compostos de componentes menores, conhecidos como partículas . As três partículas fundamentais que compreendem a maioria dos átomos são chamadas de prótons , nêutrons e elétrons . Embora a maioria dos átomos tenha uma combinação de prótons, nêutrons e elétrons, nem todos os átomos têm nêutrons; um exemplo é o isótopo protium (1H1) do hidrogênio (Hydrogen-1) que é a forma mais leve e comum de hidrogênio que tem apenas um próton e um elétron. Os átomos são muito pequenos para serem vistos, mas se pudéssemos olhar para um, poderia ter a seguinte aparência:
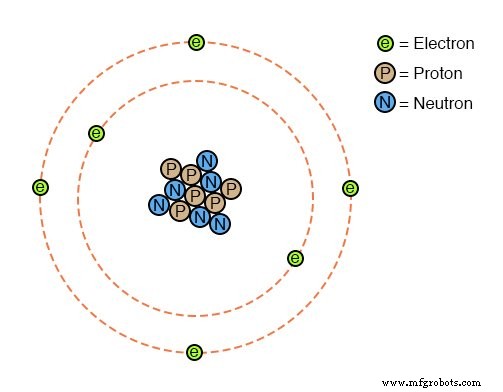
Mesmo que cada átomo em um pedaço de material tenda a se manter unido como uma unidade, na verdade há muito espaço vazio entre os elétrons e o aglomerado de prótons e nêutrons que residem no meio.
Este modelo bruto é o do elemento carbono, com seis prótons, seis nêutrons e seis elétrons. Em qualquer átomo, os prótons e nêutrons estão intimamente ligados, o que é uma qualidade importante. O aglomerado fortemente ligado de prótons e nêutrons no centro do átomo é chamado de núcleo , e o número de prótons no núcleo de um átomo determina sua identidade elementar:mude o número de prótons no núcleo de um átomo, e você muda o tipo de átomo que ele é. Na verdade, se você pudesse remover três prótons do núcleo de um átomo de chumbo, você teria realizado o sonho dos velhos alquimistas de produzir um átomo de ouro! A forte ligação dos prótons no núcleo é responsável pela identidade estável dos elementos químicos e pelo fracasso dos alquimistas em realizar seus sonhos.
Os nêutrons têm muito menos influência sobre o caráter químico e a identidade de um átomo do que os prótons, embora sejam tão difíceis de adicionar ou remover do núcleo, por serem tão fortemente ligados. Se nêutrons forem adicionados ou ganhos, o átomo ainda manterá a mesma identidade química, mas sua massa mudará ligeiramente e pode adquirir um nuclear estranho propriedades como radioatividade.
No entanto, os elétrons têm significativamente mais liberdade para se mover em um átomo do que os prótons ou nêutrons. Na verdade, eles podem ser arrancados de suas respectivas posições (mesmo deixando o átomo inteiramente!) Por muito menos energia do que o necessário para desalojar partículas no núcleo. Se isso acontecer, o átomo ainda retém sua identidade química, mas ocorre um desequilíbrio importante. Elétrons e prótons são únicos pelo fato de serem atraídos uns pelos outros à distância. É essa atração pela distância que causa a atração entre os objetos friccionados, onde os elétrons são movidos para longe de seus átomos originais para residir em torno dos átomos de outro objeto.
Os elétrons tendem a repelir outros elétrons à distância, assim como os prótons com outros prótons. A única razão pela qual os prótons se ligam no núcleo de um átomo é por causa de uma força muito mais forte chamada de força nuclear forte que tem efeito apenas em distâncias muito curtas. Por causa desse comportamento de atração / repulsão entre partículas individuais, diz-se que elétrons e prótons têm cargas elétricas opostas. Ou seja, cada elétron tem uma carga negativa e cada próton uma carga positiva. Em números iguais dentro de um átomo, eles neutralizam a presença um do outro, de modo que a carga líquida dentro do átomo é zero. É por isso que a imagem de um átomo de carbono tem seis elétrons:para equilibrar a carga elétrica dos seis prótons no núcleo. Se os elétrons saem ou elétrons extras chegam, a carga elétrica líquida do átomo será desequilibrada, deixando o átomo "carregado" como um todo, fazendo com que ele interaja com partículas carregadas e outros átomos carregados próximos. Os nêutrons não são atraídos ou repelidos por elétrons, prótons ou mesmo outros nêutrons e, conseqüentemente, são categorizados como sem carga alguma.
O processo de chegada ou saída de elétrons é exatamente o que acontece quando certas combinações de materiais são friccionadas:elétrons dos átomos de um material são forçados pela fricção a deixar seus respectivos átomos e se transferir para os átomos do outro material. Em outras palavras, os elétrons constituem o “fluido” hipotetizado por Benjamin Franklin.
O que é eletricidade estática?
O resultado de um desequilíbrio deste "fluido" (elétrons) entre os objetos é chamado de eletricidade estática . É chamado de “estático” porque os elétrons deslocados tendem a permanecer estacionários após serem movidos de um material isolante para outro. No caso da cera e da lã, foi determinado por meio de novas experiências que os elétrons da lã realmente se transferiram para os átomos da cera, o que é exatamente o oposto da conjectura de Franklin! Em homenagem à designação de Franklin de que a carga da cera é "negativa" e a carga da lã é "positiva", diz-se que os elétrons têm uma influência de carga "negativa". Assim, um objeto cujos átomos receberam um excedente de elétrons é considerado negativamente carregado, enquanto um objeto cujos átomos não têm elétrons é considerado positivamente cobrado, por mais confusas que essas designações possam parecer. No momento em que a verdadeira natureza do "fluido" elétrico foi descoberta, a nomenclatura de carga elétrica de Franklin estava muito bem estabelecida para ser facilmente alterada e assim permanece até hoje.
Michael Faraday provou (1832) que a eletricidade estática era igual à produzida por uma bateria ou gerador. A eletricidade estática é, na maior parte, um incômodo. O pó preto e o pó sem fumaça têm grafite adicionado para evitar a ignição devido à eletricidade estática. Causa danos aos circuitos de semicondutores sensíveis. Embora seja possível produzir motores alimentados por alta tensão e características de baixa corrente de eletricidade estática, isso não é econômico. As poucas aplicações práticas da eletricidade estática incluem a impressão xerográfica, o filtro de ar eletrostático e o gerador Van de Graaff de alta tensão.
REVER:
- Todos os materiais são feitos de pequenos “blocos de construção” conhecidos como átomos .
- Todos os átomos de ocorrência natural contêm partículas chamadas elétrons , prótons e nêutrons , com exceção do isótopo protium ( 1 H 1 ) de hidrogênio.
- Os elétrons têm carga elétrica negativa (-).
- Os prótons têm carga elétrica positiva (+).
- Nêutrons não têm carga elétrica.
- Os elétrons podem ser desalojados dos átomos muito mais facilmente do que os prótons ou nêutrons.
- O número de prótons no núcleo de um átomo determina sua identidade como um elemento único.
PLANILHAS RELACIONADAS:
- Planilha de eletricidade estática
- Planilha de estrutura atômica
Tecnologia industrial



