Matrizes nanopilar de GaAs com cobertura au fabricada por corrosão química assistida por metal
Resumo
Matrizes de nanopilar de GaAs foram fabricadas com sucesso por corrosão química assistida por metal usando matrizes de nanodot de Au. As matrizes de nanopontos foram formadas em substratos por deposição a vácuo através de uma máscara de alumina porosa com uma matriz ordenada de aberturas. Usando um decapante com uma alta concentração de ácido e baixa concentração de oxidante em uma temperatura relativamente baixa, a área ao redor da interface Au / GaAs pode ser atacada seletivamente. Sob as condições ideais, arranjos de nanopilares de GaAs com cobertura de Au foram formados com uma periodicidade ordenada de 100 nm e alturas de pilar de 50 nm.
Histórico
Os semicondutores compostos III-V têm atraído a atenção como materiais de próxima geração e potenciais alternativas aos semicondutores baseados em silício por causa de suas excelentes propriedades, incluindo mobilidade de portadora superior e gap direto de banda. Nanoestruturas com periodicidade ordenada e / ou alta razão de aspecto são consideradas um elemento importante em várias aplicações, incluindo dispositivos ópticos e optoeletrônicos devido ao seu baixo custo e alta eficiência de conversão em comparação com dispositivos convencionais baseados em filme fino [1,2,3,4] . Em geral, para fabricar semicondutores de baixa dimensão (por exemplo, nanofios), processos secos, como epitaxia de feixe molecular, epitaxia de vapor-líquido-sólido e epitaxia de fase de vapor metal-orgânica são usados [1, 5,6,7]. Embora esses métodos tenham muitas vantagens, incluindo alta precisão de padronização, suas desvantagens incluem alto custo e limitações de tamanho da área de padronização em aplicações práticas. Portanto, métodos alternativos que permitem a fabricação simples e econômica de nanoestruturas são necessários.
A corrosão química assistida por metal, proposta por Li e Bohn em 2000 [8], é um método de fabricação comumente utilizado devido à sua relativa simplicidade e baixo custo. Estudos recentes demonstraram que a corrosão química assistida por metal pode ser aplicada para fabricar nanoestruturas complexas, como nanoporos retos e profundos, nanoporos helicoidais, canais inclinados, cicloides e espirais [4, 9,10,11,12]. No entanto, desde o relatório de Li et al., A maioria dos estudos relatou a fabricação de nanoestruturas de silício; poucas investigações se concentraram na nanofabricação de semicondutores compostos III-V [13, 14], e a formação de estruturas ordenadas em escala nanométrica em substratos de GaAs é particularmente mal compreendida. Para expandir a gama de aplicações de corrosão química assistida por metal, é desejável desenvolver um método de nanofabricação para semicondutores compostos III-V que não dependa das dimensões dos padrões resultantes.
Em um estudo anterior, nós fabricamos matrizes de microbump de InP [15] e padrões de linha e matrizes de pilar de GaAs [16] usando corrosão química assistida por metal. No entanto, as dimensões dos padrões resultantes (por exemplo, periodicidade e larguras dos padrões de linha) variaram de vários micrômetros a várias dezenas de micrômetros. Até onde sabemos, nenhum estudo relatou a formação de nanoestruturas de GaAs ordenadas com escala submicron ou menor periodicidade usando corrosão química assistida por metal pelas seguintes razões:(1) é difícil controlar a forma e o tamanho dos metais nobres usado como um catalisador na escala nanométrica e (2) o fenômeno de corrosão do GaAs é menos compreendido em comparação com o caso do silício. Assim, tentamos esclarecer o mecanismo de corrosão do GaAs em escala nanométrica. Neste estudo, demonstramos que arranjos de nanopilares ordenados com uma periodicidade de 100 nm podem ser fabricados em substratos de GaAs usando corrosão química assistida por metal com um catalisador de Au padronizado. Os efeitos da composição do condicionador e do tempo de condicionamento na morfologia do substrato de GaAs gravado também são investigados.
Métodos
O princípio da fabricação de matrizes de nanopilar de GaAs por meio de corrosão química assistida por metal é mostrado esquematicamente na Fig. 1. Uma máscara de alumina porosa através de orifício com uma matriz ordenada de aberturas foi preparada por anodização de duas etapas seguida por anodização de duas camadas [ 17]. A primeira anodização foi realizada em alumínio polido eletroquimicamente (pureza 99,99%) a uma tensão constante de 40 V em 0,3 mol dm −3 ácido oxálico a 30 ° C durante 3 h. A tensão de anodização de 40 V está bem estabelecida como uma condição de auto-ordenação que produz um arranjo de poros altamente ordenado em alumina anódica [18].
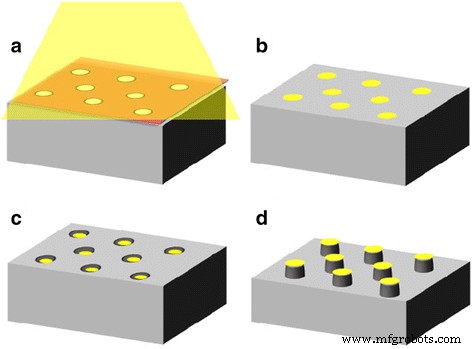
Modelo esquemático da fabricação de arranjos nanopilar de GaAs. a Deposição a vácuo de Au em um substrato de GaAs através de máscara de alumina porosa. b Remoção da máscara. c , d Gravura química de GaAs usando matrizes de nanodot de Au como catalisador
Após a primeira anodização, a primeira camada de alumina anodizada foi removida em uma solução mista de ácido fosfórico e ácido crômico a 80 ° C. Posteriormente, a segunda anodização foi conduzida por 1,5 min nas mesmas condições da primeira anodização. Com base no princípio da anodização de duas camadas, a amostra foi anodizada novamente a uma tensão constante de 40 V em 12 mol dm −3 ácido sulfúrico a 5 ° C por 8 min para preparar uma camada sacrificial de alumina. A máscara de alumina porosa através do orifício foi formada dissolvendo a camada de alumina sacrificial em 2% em peso de ácido fosfórico a 30 ° C por 20 min. A gravação química adicional foi conduzida em 5% em peso de ácido fosfórico a 30 ° C por 15 min para aumentar o diâmetro dos poros da máscara de alumina.
Depois de enxaguar a máscara de alumina em água destilada, a máscara de alumina obtida foi fixada em um substrato de GaAs tipo n [dopado com Si, 2,35-2,67 × 10 −3 Ω cm, (100) orientação do cristal]. Posteriormente, uma camada de Au de 30 nm de espessura foi evaporada através da máscara de alumina usando um sistema de deposição a vácuo pela fórmula de aquecimento por resistência (ULVAC KIKO Inc., VPC-410) com uma pressão abaixo de 1 × 10 −3 Pa (Fig. 1a). A espessura da camada de Au foi medida usando uma microbalança de cristal de quartzo, e a taxa de deposição de Au foi de 0,02 nm s −1 . Após a deposição do metal, a máscara de alumina foi removida em 5% em peso de ácido fosfórico a 25 ° C por 30 min (Fig. 1b).
O substrato de GaAs revestido com Au foi quimicamente gravado em HF contendo KMnO 4 (Fig. 1c). KMnO 4 atua como um agente oxidante em uma solução ácida [19,20,21,22]. As morfologias da máscara de alumina, camada de Au depositada e substrato de GaAs gravado foram avaliadas por microscopia eletrônica de varredura por emissão de campo (FE-SEM; JEOL JSM-6701F). A composição química do substrato de GaAs gravado foi avaliada por espectroscopia eletrônica de trado (AES; JEOL JAMP-9500F). Os espectros de elétrons Auger são facilmente adquiridos de pontos selecionados ou áreas da superfície. Aqui, a imagem de mapeamento elementar AES foi adquirida com uma tensão de aceleração e uma corrente de emissão de 30 kV e 15 nA, respectivamente.
Resultados e discussão
Na corrosão química assistida por metal, é essencial controlar com precisão as dimensões do catalisador de metal para obter o desenho desejado na superfície do substrato. Como a morfologia da estrutura resultante depende do padrão geométrico inicial e das dimensões do catalisador de metal, um catalisador de metal padronizado é necessário para fabricar nanoestruturas ordenadas em superfícies semicondutoras. Neste estudo, uma máscara de alumina com uma matriz ordenada de aberturas foi usada para controlar o tamanho e a disposição do catalisador de metal. Para um processo de deposição de metal a seco, a espessura da máscara é crítica porque a deposição de metal através de uma máscara espessa com aberturas estreitas é fisicamente difícil. No caso da alumina porosa, a espessura da máscara pode ser ajustada com alta reprodutibilidade alterando o tempo de anodização. Aqui, uma máscara de alumina porosa de orifício de passagem de aproximadamente 300 nm de espessura foi preparada em um substrato de GaAs. A máscara de alumina foi fixada com a superfície voltada para cima. Os diâmetros superior e inferior das aberturas na máscara de alumina eram de aproximadamente 80 e 70 nm, respectivamente. O diâmetro ligeiramente maior da abertura superior em comparação com a abertura inferior foi atribuído à corrosão química durante a preparação da máscara de alumina.
A Figura 2 mostra um arranjo típico de nanopontos de Au bem ordenado em um substrato de GaAs. A matriz de nanopontos corresponde à configuração da matriz de poros auto-ordenada na máscara de alumina anódica, como mostrado na Fig. 2a. Embora a capacidade de controle da deposição de Au deva ser melhorada, a deposição de metal através da máscara de alumina demonstrada neste documento é adequada para a produção em grande escala de padrões de pontos de metal nobre ordenados em substratos semicondutores em termos de simplicidade e eficiência do processo de fabricação. Observe que cada nanoponto de Au tinha quase o mesmo diâmetro de aproximadamente 70 nm; este diâmetro foi determinado pelo tamanho do poro da parte inferior da máscara de alumina, enquanto as alturas dos nanopontos de Au foram determinadas principalmente pelo tempo de deposição. Neste estudo, a altura de cada nanoponto de Au foi ajustada para ser ~ 30 nm, conforme mostrado na Fig. 2b.

a Superfície e b imagens de SEM em corte transversal de uma matriz de nanopontos de Au formada em um substrato de GaAs através de uma máscara de alumina anódica porosa
Após a formação de matrizes Au dot em substratos GaAs, os espécimes foram imersos em uma solução de HF e KMnO 4 para gravação química assistida por metal. Na gravação química assistida por metal convencional, a gravação prossegue localmente na interface entre o catalisador e o substrato subjacente, resultando na formação de poros ou trincheiras na direção perpendicular ao substrato, e o catalisador de metal afunda no semicondutor, como mostrado em Fig. 1c. O uso de um decapante composto por uma alta concentração de ácido e uma baixa concentração de oxidante é considerado para promover o consumo suave dos orifícios positivos gerados (h + ) na interface metal / semicondutor. Neste estudo, espera-se que a oxidação de GaAs na interface Au / GaAs prossiga diretamente pelo h + gerado .
A Figura 3 mostra uma imagem SEM típica da superfície GaAs gravada usando o catalisador Au padronizado. A corrosão química foi conduzida em solução contendo 0,001 mol dm −3 KMnO 4 e 20 mol dm −3 HF a uma temperatura relativamente elevada de 45 ° C. Neste estudo, a concentração de KMnO 4 estava baixo (0,001 mol dm −3 ) para suprimir a corrosão lateral. De acordo com relatórios anteriores de DeJarld et al. e Cheung et al., a taxa de corrosão lateral aumentou com o aumento do agente oxidante (KMnO 4 ) concentração [19, 21].

Imagem SEM da superfície superior do substrato de GaAs após ataque químico assistido por Au em solução contendo 0,001 mol dm −3 KMnO 4 e 20 mol dm −3 HF por 600 s a 45 ° C
Catalisadores de Au, que foram detectados como pontos brilhantes circulares, foram observados dentro dos poros em muitas áreas do substrato GaAs, como mostrado na Fig. 3. O diâmetro dos poros observados na Fig. 3 coincidiu com os tamanhos dos nanopontos de Au depositados mostrados na Fig. 2. Estes resultados indicam que o ataque químico assistido por metal convencional, que é mostrado esquematicamente na Fig. 1c, ocorreu apenas na interface Au / GaAs e procedeu anisotropicamente perpendicular ao substrato, ou seja, na direção <100>.
Na corrosão química assistida por metal, a composição e a temperatura de corrosão afetam a dinâmica da difusão do transportador, oxidação e remoção do produto [19]. Para abrir novas aplicações de substrato de GaAs gravado, tentamos fabricar matrizes de nanopilar de GaAs alterando as condições de gravação química assistida por metal. A Figura 4 mostra imagens SEM em corte transversal típicas de superfícies de GaAs gravadas obtidas usando o catalisador Au padronizado. Aumentando a concentração de KMnO 4 , a morfologia da estrutura resultante pode ser alterada. Em todos os casos, nanopilares de GaAs dispostos hexagonalmente em toda a área do espécime foram obtidos. As pontas dos pilares foram ligeiramente afiladas como resultado do ataque lateral. As periodicidades das matrizes nanopilar de GaAs foram de aproximadamente 100 nm, correspondendo às das matrizes de pontos Au usadas como catalisador e aos poros da alumina porosa usada como máscara inicial. Até onde sabemos, as dimensões (por exemplo, periodicidade) das estruturas obtidas em GaAs por meio de corrosão química assistida por metal neste estudo são menores do que as relatadas para outras estruturas de GaAs [19,20,21,22].

Imagens SEM de matrizes de nanopilar de GaAs fabricadas por corrosão química assistida por Au em soluções contendo 0,01 mol dm −3 KMnO 4 e 5, 10 ou 20 mol dm −3 HF por 5 s em a 20 e b 45 ° C
Quando o ataque foi conduzido a uma temperatura relativamente baixa de 20 ° C, o catalisador Au foi observado na ponta de cada pilar, conforme indicado pelas setas. A Figura 4a mostra que a taxa de corrosão aumentou com o aumento da concentração de HF na mesma concentração de oxidante. Na alta concentração de HF de 20 mol dm −3 , a altura do pilar de GaAs residual foi a mais alta.
Ao contrário da expectativa de que a oxidação de GaAs na interface Au / GaAs prossegue pelo h + gerado , nenhuma dissolução química na área de contato entre o catalisador Au e o substrato GaAs subjacente foi observada no caso da Fig. 4. O padrão de corrosão é considerado dependente da temperatura do decapante. Em baixa temperatura (por exemplo, 20 ° C), a taxa de h + o consumo na interface Au / GaAs é considerado menor do que a taxa de h + injeção; portanto, h + difundido na área ao redor de GaAs revestido de Au. Eventualmente, um nanopilar de GaAs foi formado sob a área de contato entre o catalisador de Au e o substrato de GaAs subjacente porque o ataque seletivo local ocorreu na superfície de GaAs exposta. Em outras palavras, os nanopontos de Au também atuaram como uma máscara protetora para evitar a dissolução do substrato de GaAs. Este fenômeno de corrosão, conforme mostrado esquematicamente na Fig. 1d, é chamado de corrosão química assistida por metal inverso [19, 22]. Em 2010, também demonstramos a formação de matrizes de microbombas InP usando corrosão química assistida por metal inversa sob irradiação UV [15]. Em contraste com a corrosão química assistida por metal convencional, a corrosão química assistida por metal inversa prossegue nas superfícies do semicondutor composto III-V exposto em torno das áreas revestidas com metal pela difusão de h + de catalisador de metal e subsequente corrosão química local-seletiva. Esse comportamento único de corrosão não foi observado em materiais de silício.
Quando a corrosão química assistida por metal é conduzida a uma temperatura elevada de 45 ° C, o h + gerado espera-se que seja consumido assim que atingir o limite entre Au, GaAs e condicionador, resultando na promoção de corrosão vertical. Mesmo neste caso, no entanto, ocorreu a corrosão química assistida por metal inversa. Conforme mostrado na Fig. 4b, a taxa de gravação aumentou com o aumento da concentração de HF da mesma forma que o comportamento de gravação da Fig. 4a. No entanto, a uma alta temperatura de corrosão de 45 ° C e uma alta concentração de HF de 20 mol dm −3 , os catalisadores Au foram separados das pontas dos pilares de GaAs porque o excesso h + gerado pela temperatura relativamente alta, mesmo no curto tempo de ataque de 5 s, promoveu o ataque lateral do GaAs na presença do catalisador Au. A capacidade de controle da forma dos pilares será melhorada pela otimização adicional das condições de corrosão (por exemplo, composição de corrosão, concentração e temperatura). Tentativas de esclarecer os efeitos da concentração do agente oxidante na geração de h + e a morfologia de GaAs gravados estão atualmente em andamento.
Para examinar o efeito do tempo de corrosão na geometria da estrutura GaAs gravada, a corrosão química foi prolongada em 20 mol dm −3 HF e 0,01 mol dm −3 KMnO 4 a uma temperatura relativamente baixa de 20 ° C. Conforme mostrado na imagem em corte transversal na Fig. 5a, a profundidade dos nanopilares de GaAs atingiu ~ 50 nm. Uma das características notáveis das matrizes de nanopilar de GaAs obtidas neste estudo é que a ponta de cada pilar foi coberta com Au, como mostrado no detalhe da Fig. 5a. A Figura 6 mostra a análise elementar AES do mesmo espécime. Os mapas AES para Ga e Au do GaAs gravado indicam a presença de Au na ponta de cada pilar, mesmo após o condicionamento químico assistido por metal por 10 s.

Imagens de SEM em corte transversal de uma matriz de nanopilar de GaAs fabricada por corrosão química assistida por Au a 20 ° C para a 10 e b 60 s em uma solução contendo 20 mol dm −3 HF e 0,01 mol dm −3 KMnO 4 . Inserido mostra uma imagem de superfície de uma matriz de nanopilar de GaAs capada com Au

a Imagem do substrato GaAs após ataque químico assistido por Au e mapas AES correspondentes para b Ga e c Au. As condições de corrosão foram as mesmas da Fig. 5a
Como a altura do pilar foi determinada principalmente pelo tempo de corrosão, a corrosão foi ainda mais prolongada de 10 s para 1 min para formar matrizes de pilares mais altos em GaAs. No entanto, o tempo de corrosão prolongado de 1 min resultou na diminuição da altura do pilar, como mostrado na Fig. 5b. A diminuição na altura do pilar foi atribuída ao ataque lateral na presença do catalisador Au e ao subsequente desprendimento dos pontos Au usados como catalisador.
Embora a corrosão química assistida por metal, que controla precisamente a difusão de h + do catalisador metálico, ainda não totalmente realizado, a nanofabricação de semicondutores compostos III-V usando corrosão química assistida por metal oferece uma alternativa promissora para o projeto de estruturas tridimensionais ordenadas sem o uso de processos a seco. Além disso, os arranjos nanopilares de GaAs capeados com Au têm potenciais aplicações tecnológicas e científicas em dispositivos optoeletrônicos, como células solares que empregam nanoestruturas plasmônicas para aumentar o aprisionamento de luz [23, 24].
Conclusões
Em resumo, demonstramos a fabricação de arranjos nanopilares de GaAs ordenados em substratos de GaAs (100) por meio de corrosão química assistida por Au. Matrizes de nanopontos de Au com padrões de rede hexagonal e periodicidades ordenadas de 100 nm foram formadas por deposição a vácuo através de uma máscara de alumina porosa. Os nanopontos de Au tinham diâmetros de aproximadamente 70 nm, correspondendo ao diâmetro da parte inferior da máscara de alumina, e serviam como catalisador e máscara protetora. A uma temperatura relativamente baixa, arranjos de nanopilares de GaAs capeados com Au podem ser formados por corrosão seletiva do local na superfície circundante de GaAs exposta. Essas descobertas fornecem a primeira evidência para o controle mais preciso de nanoestruturas em substratos de GaAs usando uma abordagem viável baseada em corrosão química assistida por metal. A técnica de litografia não convencional para a nanofabricação de semicondutores compostos III-V apresentada nesta comunicação supera as desvantagens dos métodos convencionais e tem aplicações tecnológicas e científicas potenciais em vários campos de pesquisa.
Abreviações
- AES:
-
Espectroscopia de elétrons Auger
- FE-SEM:
-
Microscopia eletrônica de varredura por emissão de campo
Nanomateriais
- Propriedades químicas do titânio
- Matrizes C#
- Matrizes C++
- Matrizes C
- C Matrizes Multidimensionais
- Matrizes Java
- Desvendando a evolução morfológica e cinética de corrosão de nanofios de silício poroso durante a corrosão química assistida por metal
- Efeitos do pH microambiental do lipossoma na estabilidade química do fármaco carregado
- Biocompatibilidade aprimorada em TaO anódico x arranjos de nanotubos
- MATLAB - Matrizes



