Nanomateriais de carbono para o tratamento de água contaminada por metais pesados e remediação ambiental
Resumo
A nanotecnologia é um campo avançado da ciência com a capacidade de resolver uma variedade de desafios ambientais, controlando o tamanho e a forma dos materiais em nanoescala. Os nanomateriais de carbono são únicos devido à sua natureza não tóxica, grande área de superfície, biodegradação mais fácil e remediação ambiental particularmente útil. A contaminação por metais pesados na água é um grande problema e representa um grande risco para a saúde humana. Os nanomateriais de carbono estão recebendo cada vez mais atenção devido às suas propriedades físico-químicas superiores, que podem ser exploradas para o tratamento avançado de água contaminada por metais pesados. Nanomateriais de carbono, nomeadamente nanotubos de carbono, fulerenos, grafeno, óxido de grafeno e carvão ativado, têm grande potencial para a remoção de metais pesados da água devido à sua grande área de superfície, tamanho em nanoescala e disponibilidade de diferentes funcionalidades e são mais fáceis de serem quimicamente modificados e reciclado. Neste artigo, revisamos os avanços recentes nas aplicações desses nanomateriais de carbono no tratamento de água contaminada por metais pesados e também destacamos sua aplicação na remediação ambiental. Aspectos toxicológicos de nanomateriais à base de carbono também foram discutidos.
Introdução
A poluição é denominada como a presença de entidades / entidades químicas indesejáveis que impedem o processo natural ou causam efeitos adversos aos organismos vivos e ao meio ambiente [1,2,3]. A industrialização e o imenso aumento da população, levando à crescente urbanização, causam o aumento da poluição em taxas alarmantes [2, 4]. Melhorar a qualidade da água, do solo e do ar é um imenso desafio da era moderna. A identificação e o tratamento de poluentes ambientais e sua prevenção é um passo fundamental na proteção do meio ambiente. A ciência dos materiais desempenha um papel vital na realização do objetivo ambiental limpo, e a tecnologia da ciência dos materiais progrediu exponencialmente na última década, especialmente os nanomateriais [1, 5]. A água pura e limpa está ficando escassa devido à industrialização, e o mundo está enfrentando uma escassez de água limpa, especialmente no mundo em desenvolvimento [6]. Os contaminantes da água podem ser orgânicos, bactérias, vírus, corantes e íons de metais pesados, como chumbo, cádmio, zinco, níquel, arsênio, cromo e mercúrio com natureza não biodegradável que representa um grande risco para a saúde humana. Os íons de metais pesados podem causar muitos efeitos adversos, como câncer, danos renais, hepatite, abortos espontâneos, anemia, encefalopatia e síndrome nefrítica [7,8,9,10]. Os íons de chumbo são liberados no meio ambiente geralmente pelas indústrias de mineração de metais de baterias de chumbo ácido, papel, vidro e indústrias de polimento. O cádmio é geralmente encontrado na água descarregada de projetos de galvanoplastia de baterias, células fotovoltaicas, processos de metalurgia e fábricas de tecidos [11]. Os íons de níquel podem causar doenças de pele quando contatados com lixo de joias, zíperes, relógios, moedas, etc. Os íons de cromo metálico (VI) causam doenças como danos ao fígado, nefrite e problemas estomacais, e os íons Cr (VI) também são a principal causa de úlcera da mucosa nasal [12]. A Figura 1 mostra a adsorção de íons de metais pesados no nanomaterial de carbono (grafeno), e a Figura 2 destaca as diferentes fontes de contaminação por metais pesados no meio ambiente. Devido a esses efeitos adversos graves, a remoção de íons de metais pesados da água é de importância primordial para salvar vidas humanas de tais problemas de saúde problemáticos. Íons metálicos tóxicos podem ser removidos por vários métodos, como troca iônica, osmose reversa, filtração por precipitação, biossorção, coagulação e extração [13, 14]. A adsorção é considerada o melhor método por ser econômica, altamente eficiente e fácil de operar para remover níveis de traços de íons de metais pesados [15]. Diferentes materiais têm sido aplicados para o tratamento de água, tais como adsorventes de plantas e materiais de natureza orgânica, especialmente ácido húmico, que tem sido amplamente aplicado para desinfecção de água e para a remoção de íons de metais pesados [8, 16,17,18,19]. Wang et al. revisaram de forma abrangente o ácido húmico e seu nanocompósito no tratamento de água [20].
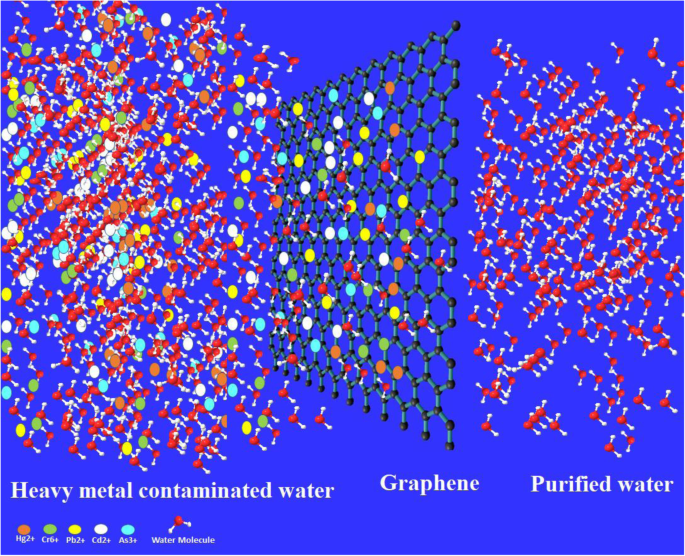
Resumo gráfico mostrando que o processo de purificação de água contaminada com metais pesados usando grafeno e outros materiais à base de carbono também pode fazer o mesmo
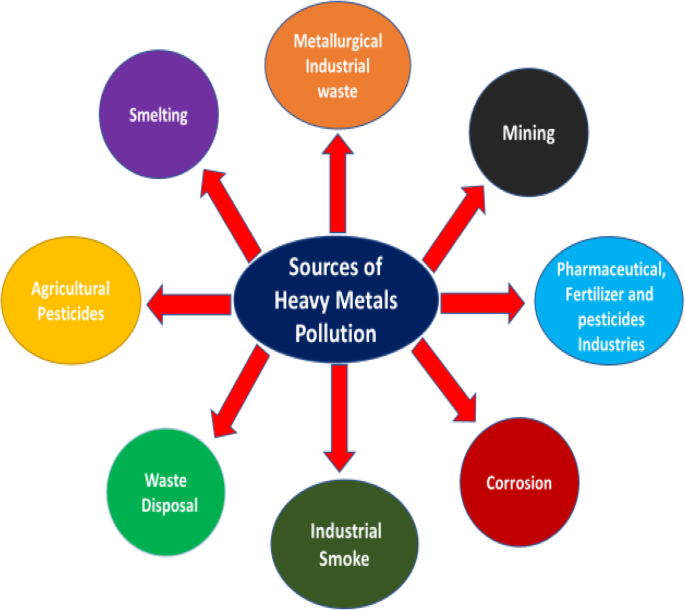
Fontes de contaminação por metais pesados no meio ambiente
A plataforma de nanotecnologia encontra aplicação em quase todos os campos, como ciências ambientais, ciências da saúde, eletrônica, separação industrial, tratamento portátil de água, plantas de grande / pequena escala, catalisador, armazenamento de energia e geração de energia [21,22,23]. Os nanomateriais fornecem uma plataforma especial para a purificação de água contaminada devido à alta área de superfície dos nanosorventes e sua capacidade de modificação química e regeneração mais fácil. Nanomateriais estão sendo explorados cada vez mais para a remoção de diferentes tipos de poluentes, nomeadamente orgânicos, íons metálicos, contaminantes biológicos e arsênio da água [24,25,26,27]. Nanomateriais de carbono, ou seja, grafeno, óxido de grafeno, nanotubos de carbono, fulerenos e carvões ativados têm sido amplamente utilizados em armazenamento de energia, sensores, eletrônicos, purificação de água, distribuição de drogas, diagnóstico de doenças, etc. devido à sua excepcional qualidade química, mecânica, térmica e características elétricas. Neste artigo, tentamos revisar os últimos avanços na aplicação de nanomateriais de carbono, ou seja, fulerenos, nanotubos de carbono (CNTs), grafeno, óxido de grafeno e carvão ativado na purificação de água contaminada com íons de metais pesados.
Saúde humana e toxicidade por metais pesados
Os metais pesados são geralmente definidos com base em seus pesos atômicos; no entanto, o termo metais pesados também se refere a elementos tóxicos para criaturas vivas [28]. Certos metais pesados são letais para a saúde humana e outras criaturas vivas em suas diferentes formas e doses (Tabela 1). Freqüentemente, os metais pesados são considerados tóxicos; no entanto, metais mais leves também podem ser letais, por exemplo, berílio e lítio. Nem todos os metais pesados são tóxicos para a saúde, pois alguns são fundamentais, por exemplo, ferro e Cr (III). Os metais tóxicos mais comumente conhecidos são Pb, Cd, Cr, Mn, Hg, As e metais radioativos. Os metais radioativos apresentam toxicidade radiológica e química. A toxicidade dos metais pesados revelou-se uma grande ameaça e existem muitos riscos para a saúde associados a eles. O impacto letal desses metais é o fato de não terem função biológica; no entanto, eles podem imitar como um elemento do corpo e interferir nos processos metabólicos e biológicos. Alguns metais como o alumínio podem ser facilmente eliminados pelo sistema de excreção, enquanto certos metais se acumulam na cadeia alimentar e no corpo. A toxicidade induzida por metal depende da dose, rota de exposição e tempo de contato (por exemplo, aguda ou crônica). Detalhes da toxicidade associada a diferentes metais pesados são fornecidos abaixo.
Toxicidade de Mercúrio (Hg)
Mercúrio (Hg) é um elemento do bloco d com um número atômico 80 e está na forma líquida sob condições padrão. O mercúrio é encontrado em depósitos de sulfeto de mercúrio chamados cinabre. A poluição do mercúrio é causada por indústrias farmacêuticas, preservação de papel e celulose, indústria de produção de soda cáustica, indústria agrícola, etc. [47]. O mercúrio é o metal pesado mais tóxico do meio ambiente, e o envenenamento por mercúrio é chamado de doença rosa, também conhecida como acrodinia. O mercúrio pode se combinar com compostos orgânicos e inorgânicos. Os níveis elevados de exposição ao mercúrio em qualquer forma podem danificar os rins, o cérebro, o desenvolvimento do feto, etc. [48]. A agência de proteção ambiental declarou o metilmercúrio e o cloreto de mercúrio como cancerígenos. A exposição ao mercúrio também pode causar danos aos pulmões, erupções cutâneas, problemas de memória e queda de cabelo. A Organização Mundial da Saúde (OMS) estabeleceu o padrão para água potável com níveis mais baixos de mercúrio para 0,01 mg / l [29].
Toxicidade do chumbo (Pb)
O chumbo (Pb) é um elemento com número atômico 82 e é considerado um metal pesado de aspecto prateado azulado que se torna cinza opaco pela ação do ar [30]. Existem várias fontes de poluição por chumbo, principalmente resíduos de indústrias de baterias, fertilizantes e pesticidas, galvanização e operações de acabamento, exaustão, aditivos na gasolina, pigmentos em automóveis e fundição de minérios. Este metal tóxico pesado está se tornando uma preocupação ambiental e de saúde em todo o mundo devido ao seu uso generalizado [31]. O chumbo (Pb) é um elemento cancerígeno declarado pela Agência de Proteção Ambiental (EPA). A intoxicação por chumbo é um termo usado para designar sua toxicidade e pode ser aguda ou crônica. O envenenamento por chumbo pode causar retardo mental, defeitos congênitos como autismo, alergias, dislexia, paralisia, dano cerebral e dano renal e também pode resultar em morte [32].
Toxicidade do arsênico (As)
O arsênio é um elemento metalóide com um número atômico de 33 e ocorre na forma mineral comumente em combinação com enxofre, alguns outros metais, sais de ferro, cálcio, sódio e cobre, e também na forma elementar pura [33]. A água está contaminada por pesticidas à base de arsênio, depósitos de minerais naturais e descarte inadequado de reagentes ou produtos químicos à base de arsênio. O arsênico na forma de arseniato e arsenito é letal para o meio ambiente e para as criaturas vivas. O arsênio perturba o protoplasma das células ao interagir com o grupo sulfidrila das células, causando mau funcionamento da respiração e afetando a mitose e as enzimas celulares [34].
Toxicidade do cádmio (Cd)
O cádmio tem um número atômico de 48 e é um metal macio branco-azulado com propriedades químicas semelhantes às do mercúrio e do zinco do grupo 12 [30]. Eles estão sendo produzidos a partir da fundição de seus minérios, galvanoplastia, baterias, plastificantes, ligas, pigmentos, indústria nuclear e fumaça de cigarro. Geralmente, o cádmio está presente em níveis baixos no meio ambiente; no entanto, os resíduos industriais aumentaram muito esses níveis. A toxicidade induzida por cádmio pode causar danos aos rins, sistema respiratório e esqueleto e é cancerígena para humanos [30, 33]. O cádmio é classificado como o sétimo metal mais tóxico pela Agência de Registro de Substâncias Tóxicas e Doenças (ATSDR) [34].
Toxicidade do cromo (Cr)
O cromo (Cr) é um elemento de número atômico 24, com aparência cinza metálico [35]. O cromo ocorre em diferentes estados, por exemplo, estados divalente, tetravalente, pentavalente e hexavalente; entretanto, as formas trivalente e hexavalente são as mais estáveis. O cromo (III) é um suplemento nutricional essencial para humanos e animais [35]. No entanto, a forma de cromo (VI) é altamente tóxica e carcinogênica por natureza [36, 37]. O cromo é produzido em matrizes ambientais (ar, água e solo) de diferentes fontes, por exemplo, águas residuais e ar liberado principalmente de indústrias metalúrgicas e químicas. O cromo hexavalente Cr (VI) é um poluente industrial estabelecido como carcinógeno humano [38, 39]. A concentração de Cr (VI) nas águas subterrâneas e superficiais é superior e a Organização Mundial da Saúde (OMS) estabeleceu o limite de 50 μg por litro [40].
Toxicidade do Zinco (Zn)
Zinco (Zn) é um elemento de número atômico 30 e colocado no grupo 2 da tabela periódica. Embora o zinco seja um traço de metal essencial para humanos, a absorção excessiva de zinco pode suprimir a absorção de ferro. Os íons zinco são altamente tóxicos para as plantas, peixes vertebrados, invertebrados, etc. [41,42,43].
Classificação de nanomateriais de carbono com base em suas dimensões
Os nanomateriais com todas as três dimensões inferiores a 100 nm são designados como nanomateriais de dimensão zero (0-D); exemplos são fulereno e pontos quânticos [44]. Os nanomateriais com apenas uma dimensão maior que 100 nm e duas dimensões menores que 100 nm são denominados como nanomateriais unidimensionais (1-D), por exemplo, nanotubos de carbono e titânio [45, 46]. Os nanomateriais cujas duas dimensões são maiores que 100 nm são denominados nanomateriais bidimensionais, um exemplo famoso é o grafeno. Os materiais tridimensionais cujas dimensões são maiores que 100 nm são denominados materiais tridimensionais (3-D); exemplos são grafite e alguns compostos de nanomateriais [46]. A Figura 3 mostra alguns materiais de carbono de estrutura famosa representativos com diferentes dimensões, por exemplo, fulereno 0-D, nanotubo de carbono de parede única 1-D, grafeno 2-D e grafite 3-D.
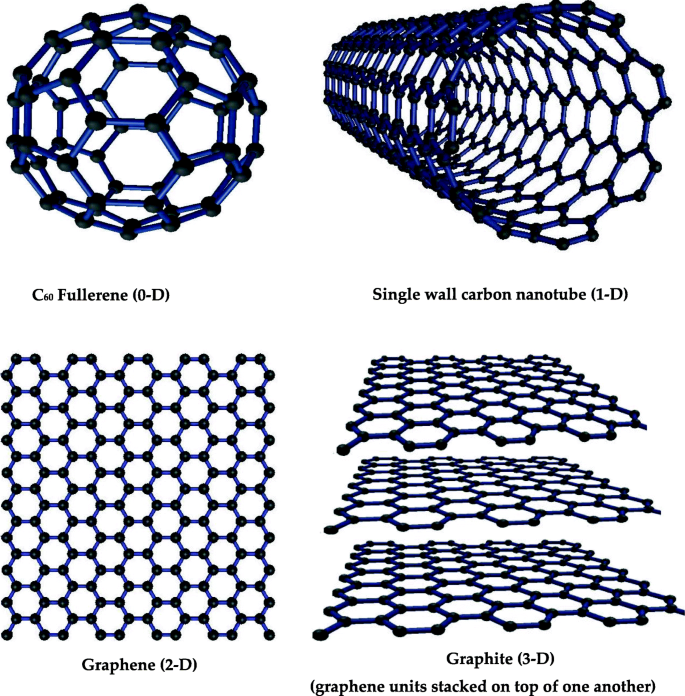
Os exemplos de nanomateriais de carbono de diferentes dimensões
Aplicação de Fulerenos em Remediação Ambiental e Purificação de Água
Fulerenos foram descobertos em 1985 a partir de poeira interestelar, e eles têm uma estrutura de anel pentagonal e hexagonal em gaiola fechada, representada com a fórmula de C 20 + m onde m é um número inteiro [49]. Eles têm um caráter hidrofóbico, alta afinidade eletrônica e alta proporção entre superfície e volume e defeitos de superfície. Essas propriedades físico-químicas únicas os tornam um material ideal para várias aplicações, como semicondutores, eletrônica, ciências biomédicas, células solares, sensores, cosméticos, fotossíntese artificial e revestimentos de superfície [50,51,52]. Brunet et al. mostraram que fulerenos funcionalizados hidrofílicos (C 60 ) também foram aplicados para matar os microrganismos patogênicos na água, utilizando um processo fotocatalítico. Os fulerenos também são materiais verdes limpos ideais para armazenamento de hidrogênio, pois as moléculas de fulereno podem ser facilmente convertidas em ligações C – C em C – H por causa das energias de ligação mais baixas do carbono e do hidrogênio [27]. Foi relatado que os fulerenos têm armazenamento máximo de 6,1% de hidrogênio por causa de sua química e estrutura molecular da gaiola, e a estrutura do fulereno pode ser facilmente revertida por causa das energias de ligação C – C mais altas [3, 53, 54]. Camadas condutoras de carbono são aplicadas na superfície do eletrodo de supercapacitores, e sua capacitância depende da área de superfície, distribuição de tamanho de poro e condutividade elétrica [55, 56]. Os nanomateriais à base de carbono fornecem maior condutividade elétrica do que os materiais ortodoxos disponíveis devido à maior área de superfície [57]. Foi relatado que materiais compósitos à base de fulereno mostram maior capacitância específica de 135,36 Fg - 1 do que o material de grafeno puro que não foi hibridizado com fulereno. Além disso, o composto à base de fulereno exibiu melhor taxa de tempo de retenção de 92,35%, mesmo após um círculo de carga / descarga de 1000 [58]. Os fulerenos também têm sido utilizados em baterias de íon de lítio como ânodo e proporcionam melhor eficiência com substituição de ânodos metálicos não degradáveis, provando ser benéficos em termos de eficiência e um material ecologicamente correto. As propriedades físico-químicas dos fulerenos também os tornam candidatos adequados para a extração de diferentes espécies do meio aquoso [59, 60]. Pickering et al. projetou compostos de fulereno solúveis em água e os aplicou com sucesso como sensibilizador para produzir espécies reativas de oxigênio (ROS) na água após irradiação de radiações visíveis e ultravioleta. Os ROS podem fotodegradar os contaminantes orgânicos da água e, além disso, os fulerenos solúveis em água (fuleróis) também atuam como antioxidantes. Mais importante ainda, os fulleróis podem ser facilmente removidos da água após desempenhar a função de fotodegradação [53].
Acredita-se que as espécies adsorvidas de fulerenos pela penetração de adsorbatos nos espaços / defeitos entre os nanoclusters de carbono, e além dos defeitos, menor tendência de agregação e grande área superficial os tornam nanomateriais úteis para serem aplicados na adsorção de íons de metais pesados de água [61, 62]. Alekseeva et al. conduziram estudos comparativos de filmes de fulereno e nanocompósito-poliestireno para a remoção de Cu 2+ íons; eles descobriram que os fulerenos mostraram melhor eficiência [60]. Eles também descobriram que os fulerenos seguem o modelo de Langmuir de adsorção para Cu 2+ íons [60]. Eles estabeleceram que o Cu 2+ a eficiência de remoção de fulerenos é maior no primeiro caso, e a isoterma de equilíbrio do Cu 2+ a adsorção no fulereno se ajusta ao modelo de Langmuir. Embora os fulerenos tenham grande potencial para aplicação de adsorção de água, seu custo é muito alto, o que restringe sua utilização. No entanto, a quantidade residual de fulerenos pode ser usada para fabricar outros materiais como carvão ativado, lignina e zeólitas para aumentar sua eficiência de adsorção [63]. A fabricação do fulereno aumenta o caráter hidrofóbico que torna os materiais melhores para serem aplicados na adsorção e também ajuda na reciclagem mais fácil [64]. Foi relatado que o material antibacteriano é formado por enxerto de fulereno C 60 com polivinilpirrolidona (PVP) que tem potencial para ser aplicado na desinfecção de água. A tecnologia de membrana está recebendo cada vez mais atenção na purificação de sais, matérias orgânicas, partículas e gases da água. O desempenho da membrana depende da composição do material, pois é responsável pela reatividade, seletividade e resistência mecânica. Os fulerenos têm grande potencial para serem aplicados na tecnologia de membrana devido à sua fácil funcionalização, alta afinidade eletrônica, grande força, capacidade de ajustar o tamanho, etc. Os fulerenos podem ser úteis no enxerto de nanoadsorventes para melhorar sua eficiência de adsorção.
Biocompatibilidade dos Fulerenos
Nanomateriais à base de fulereno têm sido explorados para aplicação biomédica e diferentes estudos revelaram sua biocompatibilidade com organismos vivos. Tem sido usado como um bioreceptor, bem como um biossensor e também explorado na engenharia biomédica, e foi relatado como biocompatível com sistemas vivos [65,66,67,68,69]. O fulereno é um material não tóxico que pode ser explorado para filtração, adsorventes e material de membrana para aplicações ambientais e de tratamento de água.
Nanotubos de carbono (CNTs)
Nanotubos de carbono foram descobertos por Lijima em 1999, e eles podem ser uma parede única (SWCNTs), por exemplo, grafeno enrolado em camadas ou nanotubos de carbono multicamadas (MWCNTs), por exemplo, grafeno enrolado em várias camadas [70]. Os CNTs têm sido o foco da pesquisa em nanotecnologia desde sua descoberta devido às suas propriedades físico-químicas únicas. Esses alótropos de nanoestrutura cilíndrica de carbono estão sendo aplicados em eletrônica, semicondutor, emissão de campo, armazenamento de energia, catálise, biomédicos, filtros de ar e água, etc. Seu diâmetro pode ser de 1 nm a vários nanômetros com uma grande área de superfície específica (150- 1500 m 2 / g), e possuem mesoporos que os tornam os candidatos ideais para a remoção de íons de metais pesados por adsorção [71, 72]. Além disso, os CNTs podem ser facilmente funcionalizados com várias moléculas orgânicas que podem torná-los específicos para a seleção de adsorbatos e sua capacidade de adsorção pode ser melhorada [73]. O mecanismo de sorção de metais pesados por CNTs depende da característica da superfície, potencial eletroquímico e processo de troca iônica [11, 73].
Aplicação Ambiental de CNTs / Tecnologia Verde Baseada em CNT
Há um imenso aumento na demanda global de energia, e muitos esforços são feitos para desenvolver um material simples, econômico e ecologicamente correto para tecnologias confiáveis para materiais de recursos energéticos. A energia solar é produzida por conversão solar elétrica e conversão solar térmica [74]. No entanto, a baixa eficiência de conversão térmica em coletores solares é o principal obstáculo.
Nanofluidos de carbono estão sendo amplamente aplicados na conversão térmica solar devido ao seu bom desempenho como absorvedores solares [75]. As células fotovoltaicas baseadas em nanotubos de carbono (PVCs) chamaram a atenção dos cientistas, pois podem ser semicondutores do tipo p com excelente mobilidade e sua combinação com doadores de elétrons é uma ideia nova e única [76, 77]. Os dispositivos fotovoltaicos orgânicos podem ser facilmente projetados pela fabricação de CNTs com polímeros [78]. As células solares baseadas em heterojunção CNT -Si (p-n) foram projetadas resultando em excelentes películas condutoras e transparentes. Além disso, os CNTs com arsenieto de gálio tipo n (n-GaAs) também foram relatados com melhor eficiência de 3,8% para laser verde e lâmpada de mesa [79]. Os CNTs também têm sido amplamente explorados como dispositivos de armazenamento de energia que trabalham com os princípios dos capacitores eletroquímicos de camada dupla (EDLCs) como ultracapacitores [80]. A incorporação de CNTs em eletrodos de ultracapacitores resultou em muitas melhorias na vida útil, com mais de 300.000 ciclos [81]. Além disso, os CNTs de supercapacitores também têm sido utilizados em diodos em vez de transistores convencionais, pois eles podem fazer junções p-n perfeitas devido às suas excelentes propriedades mecânicas e elétricas [58]. Os CNTs também têm sido amplamente utilizados em tecnologia de sensor avançada, pois podem melhorar a sensibilidade, seletividade, tempo de resposta, custo-benefício e vida útil do produto químico e biossensores [90]. Esses resultados sugerem que os melhores CNTs são materiais ideais com excelente mobilidade e melhor eficiência, sem impacto negativo no meio ambiente, o que é uma grande desvantagem com os materiais do tipo p baseados em metal mais comumente aplicados.
Aplicação de CNTs na fotocatálise
Fotocatálise é uma das tecnologias avançadas sendo aplicada para o tratamento de águas residuais que utiliza semicondutores [82]. Vários materiais semicondutores estão sendo aplicados, nomeadamente Fe 3 O 4 , ZnO e TiO 2 ; entretanto, a eficiência quântica desses materiais não é alta e, além disso, sua foto-resposta ultravioleta também é lenta [83]. Os CNTs são materiais avançados promissores para a catálise por causa de sua eficiência quântica melhorada, tamanho nanométrico, alta estabilidade química, estrutura de tubo oco e região de adsorção de luz estendida devido à sua grande área de superfície específica [84]. Gao et al. projetado SWCNTs-TiO com base em fotocatalisador de rede ultrafina 2 e aplicado com sucesso para a purificação de água do óleo [85]. Park et al. decorado com titânia em aerogel de SWCNTs e aplicado com sucesso para a remoção de azul de metileno da água [86]. Zhao et al. MWCNTs-TiO fabricado 2 e aplicado para a fotodegradação de azul de metileno [87]. Xu et al. fotocatalisadores projetados pela combinação de hidroxi-MWCNTs e PbO 2 ânodo nanocristalino e aplicado com sucesso para a remoção de piridina da água [88].
SWCNTs na purificação de água contaminada por metais pesados
SWCNTs são nanomateriais de carbono unidimensionais (1-D) compostos de um tubo oco com paredes tendo a espessura de um átomo. Este material 1-D exibe propriedades físico-químicas excepcionais devido à sua estrutura única. Os SWCNTs estão sendo amplamente aplicados em diferentes campos, como semicondutores, eletrônica, ciências biomédicas, química e biossensores [44, 89,90,91,92,93]. Os SWCNTs também são amplamente usados para o controle da poluição ambiental devido à sua estrutura porosa, alta área de superfície, fácil funcionalização da superfície e nanodimensionamento. Essas propriedades dos SWCNTs são muito promissoras para sua aplicação no tratamento de água. Alijani et al. projetou nanocompósitos baseados em SWCNT, fabricando-os com sulfeto de magnetita e cobalto, e os nanocompósitos resultantes foram aplicados para a remoção de mercúrio; os resultados mostraram alta adsorção de mais de 99,56% em um período mais curto de 7 min [94]. Em comparação a isso, os SWCNTs isoladamente adsorvem 45,39% de mercúrio [94]. Anitha et al. conduziu uma simulação de dinâmica molecular de SWCNTs nus e suas contrapartes funcionalizadas, por exemplo, SWCNTs-OH, SWCNTs-NH 2 e SWCNTs-COOH para as capacidades de adsorção de íons de metais pesados, por exemplo, Cd 2+ , Cu 2+ , Pb 2+ e Hg 2+ a partir de meio aquoso. Os resultados revelaram que os SWCNTs-COOH têm muitas capacidades de adsorção de cerca de 150–230% mais altas em comparação com os SWCNTs nus. Os SWCNTs-OH e SWCNTs-NH foram considerados fracos na adsorção, uma vez que mostraram uma adsorção 10-47% maior em comparação com os SWCNTs [95]. SWCNTs-COOH também foram relatados para a adsorção de Pb 2+ , Cu 2+ e Cd 2+ íons com capacidade de adsorção de 96,02, 77,00 e 55,89 mg / g, respectivamente. Em comparação com isso, os SWCNTs não funcionalizados foram encontrados para adsorver 33,55, 24,29 e 24,07 mg / g, para o Pb 2+, Cu 2+ e Cd 2+ íons respectivamente [96]. Zazouli et al. projetou nanocompósitos SWCNT por funcionalização deles com l-cisteína. Eles aplicaram os nanocompósitos projetados para a remoção de mercúrio da água. A eficiência de adsorção do SWCNTs-cisteína projetado foi de 95% [97]. Gupta et al. projetou membrana baseada em nanocompósito de polissulfona SWCNTs e aplicada para a remoção de metais pesados. A incorporação de SWCNTs resultou em uma redução no tamanho dos poros da membrana e superfície mais lisa. A membrana projetada demonstrou apresentar alta capacidade de rejeição de íons metálicos e removeu 96,8% de Cr + 6 , 87,6% como + 3 e 94,2% Pb + 2 íons. A membrana sem SWCNTs mostrou apenas 30,3%, 28,5% e 28,3% de rejeição para Cr + 6 , Como + 3 e Pb + 2 íons respectivamente. Esses resultados mostram a melhora na eficiência da membrana devido à incorporação de SWCNTs [98]. Dehghani et al. SWCNTs aplicados para a remoção de Cr + 6 íons da água e avaliou o efeito de diferentes parâmetros, por exemplo, tempo de contato, pH inicial e Cr + 6 inicial concentração de íons na capacidade de adsorção. Observou-se que a eficiência de adsorção era dependente do pH, a eficiência máxima foi encontrada em pH 2,5 e a adsorção segue o modelo de isoterma de Langmuir [99]. Esses estudos sugeriram que os nanotubos de carbono de parede única são adequados para o tratamento de água contaminada com metais pesados.
MWCNTs na purificação de água contaminada por metais pesados
Os nanotubos de carbono com múltiplas camadas laminadas de grafeno são chamados de nanotubos de carbono de múltiplas paredes (MWCNTs), como mostrado na Fig. 4. Os MWCNTs exibem propriedades únicas, como alta área de superfície, alta elétrica, condutividade térmica e alta resistência à tração [100]. Por causa dessas propriedades físico-químicas, eles são amplamente aplicados em eletrônica, células solares, sensores e ciências biomédicas [101,102,103]. Os MWCNTs também têm sido amplamente aplicados no tratamento de água e, especialmente, íons de metais pesados são adsorvidos por interação química com grupos funcionais de MWCNTs. Foi relatado que os MWCNTs oxidados têm alta capacidade de adsorção e eficiência para o Cr 6+ , Pb 2+ e Cd 2+ íons da água [104, 105]. A adsorção de íons metálicos também depende do valor do pH, e esta propriedade pode ser aplicada para a dessorção de íons alterando o pH, e os MWCNTs podem ser reutilizados. Alguns estudos revelaram que os MWCNTs oxidados por plasma têm as melhores propriedades de adsorção do que os oxidados quimicamente; isso pode ser atribuído a um maior número de grupos funcionais oxigenados presentes na superfície dos nanotubos de carbono. Além disso, foi relatado que MWCNTs oxidados por plasma podem ser facilmente reciclados e reutilizados [72, 106].
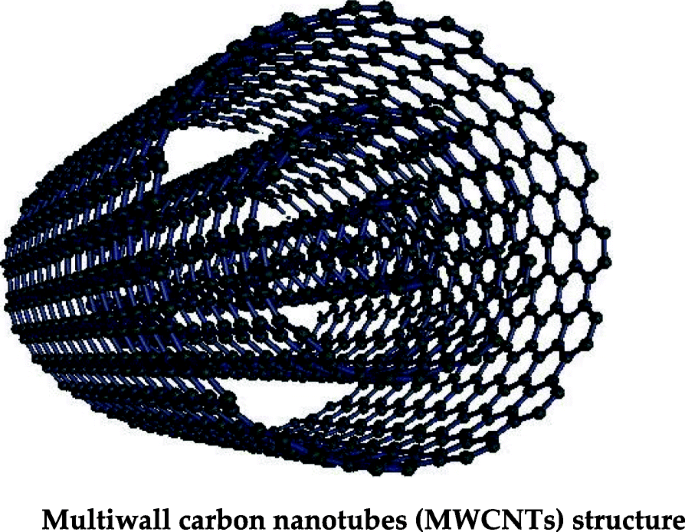
Estrutura de nanotubo de carbono de parede múltipla (MWCNT)
O material composto de MWCNTs também tem sido utilizado para a adsorção de íons de metais pesados da água. O MWCNTs-Fe 2 O 3 , MWCNTs-ZrO 2 , MWCNTs-Fe 3 O 4 , MWCNTs-Al 2 O 3 , e MWCNTs-MnO 2 -Fe 2 O 3 nanocompósitos foram aplicados com sucesso para a remoção de íons pesados de Cr 6+ , Como 3+ , Ni 2+ , Pb 2+ e Cu 2+ íons de água [107,108,109,110]. As condições experimentais de soluções, incluindo pH e concentrações de íons metálicos, podem afetar as características de adsorção de MWCNTs e o modelo de adsorção de Freundlich satisfeito com seus dados experimentais [81, 111]. A eficiência de adsorção de MWCNTs funcionalizados aumentou em comparação com outros materiais de óxidos orgânicos, e também é previsto que MWCNTs funcionalizados são 20 vezes mais eficazes na adsorção de íons metálicos do que MWCNTs não oxidados [112]. Acredita-se geralmente que as ligações de íons e a ocorrência da superfície polar do nanotubo de carbono são o principal mecanismo de sorção, [113, 114]. MWCNTs oxidados também mostraram capacidade e eficiência de sorção excepcionalmente altas para Pb 2+ , Cd 2+ e Cr 6+ da água. A eficácia de sorção de MWCNTs com tratamento ácido aumenta o potencial para remover íons de chumbo, cromo e cádmio com grupo funcional de oxigênio formando os complexos de íons ou precipitados de sais nas superfícies [115]. Adsorção de MWCNTs tratados com HNO concentrado 3 increases significantly mainly due to oxygen functional groups created on the surface of acidified nanotubes that can react with metal ions to form complex or salt precipitates on the surface. The MWCNT composites with certain compounds like iron (III) oxide, zinc oxide, and aluminum oxide are formed by a coprecipitation method, and resulting composites are successfully applied for the removal of chromium, nickel, lead, copper, and arsenic ions. The adsorption efficiency of these nanocomposites was found to be dependent on the pH value and temperature, and the sorption process can be accomplished by changing these parameters [116, 117]. Depending on the pH and temperature, the sorption capacity of these composites varied from 10 to 31 mg/g. The adsorption process for these nanocomposites was well described by the Langmuir model [118]. The nanocomposites of oxidized multiwalled MWCNTs with manganese oxide/iron (III) oxide are reported to remove Cr 6+ ions with maximum adsorption capacity of 186.9 mg/g with the maximum removal capacity of 85% at the optimum pH 2.1 studies. Their promising adsorption was due to the surface polarity of the adsorbents. It has also been reported that plasma-oxidized MWCNTs are better in adsorption compared to chemically oxidized ones as the prior ones have more oxygenated functional groups [119]. Plasma-oxidized technique has also been reported for the formation of nanotubes with titanium oxide and manganese dioxide and utilized for the removal of lead ions from water. The results showed that these hybrid systems can act as an effective adsorbent for the lead ions in the first case; the adsorption capacity was 137 mg/g, and in the second case, it was 78.74 mg/g [120]. In a heterogeneity adsorbent surface, sites combined twice are fitted in the isotherms models of the Langmuir-Freundlich equation that was used to differentiate between two types of adsorption sites with greater and lesser energy affinities for the Ni 2+ ions [121]. It is believed that nickel ion sorption mainly occurs at the sites of energy with modified nanocomposites of MWCNTs and the nano-modification leads to a 20% increase in the adsorption capacity at small (up to 0.1 mol/l) equilibrium adsorbate concentrations. Another modification reported for MWCNTs is their functionalization with hydroxyquinoline and their application for the removal of copper, lead, cadmium, and other toxic ions [122]. The carbon nanotubes alone as well as in their oxidized and in their composite forms have tremendous ability to adsorb the heavy metal ions, and a lot of research is in progress for their applications in purification of water. Elsehly et al. applied commercial MWCNTs for the removal of the manganese and iron which could reach 71.5% and 52% respectively with a concentration in aqueous solution of 50 ppm of these metal ions [123]. In another study, CNT-based nanocomposites have been applied for the removal iron and manganese from the water [124].
Biocompatibility of CNTs
Carbon nanotubes have great potential to be applied for multidisciplinary fields like drug delivery, diagnosis, biosensors, electronics, semiconductors, and environmental remediations [125]. Different studies revealed the biocompatibility of CNTs as it has been widely exploited for biomedical applications [126, 127]. Carbon-based materials like CNTs are safe to be applied for the environmental remediation and in particularly for water treatment.
Graphene Based Material for Environmental Remediation
Graphene-based material for the adsorption of gaseous contaminants
Carbon dioxide (CO2 ) has been the environmental concern because of its immense effect in global warming [128]. Nanomaterials have been found to be promising materials as compared to conventional materials both with respect to cost and efficiency [129]. Graphene-based materials have been utilized for the adsorption of gaseous contaminants [130]. Gosh et al. showed the successful application of graphene-based nanomaterials for the capture of CO2 e H 2 . A single layer of graphene has been reported to capture 37.93% of CO2 [130]. Graphene has been reported to selectively adsorb CO2 as compared to methane (CH4 ) and nitrogen (N2 ) gases. Selectivity of graphene oxide (GO) for CO2 can be attributed to higher dipole moment of carbon dioxide which can easily interact with polar oxygenated functional groups of CO2 [74, 131]. Other studies have also been reported for tuning the graphene chemistry for the improved selectivity of the desired gaseous contaminant [75, 131].
Graphene Oxide in Removal of Organic Dyes from Water
Graphene-based nano-adsorbents are excellent advanced materials for the removal of the organic contaminants from the water because of their nano-scaled size, high surface area, ability to interact via pi-pi stacking, hydrogen bonding, and electrostatic interactions [26]. In comparative adsorption studies of GO and graphite using methylene blue and malachite green as standard organic dyes, it was found that GO showed much better adsorption than graphite [26]. GO has also been utilized for the removal of cationic dyes namely methylene blue (MB), crystal violet (CV), and rhodamine B (RhB) from water. It was found that the higher the initial dye concentration, the higher will be the adsorption with adsorption capacities of 199.2, 195.4, and 154.8 mg g −1 for MB, CV, and RhB, respectively [76]. GO has also successfully applied for the removal of anionic dyes like Acid Orange 8 (AO8) and Direct Red 23 (DR23) from aqueous solutions [77].
Graphene-Based Photocatalytic Materials for Water Decontamination
Although adsorption can remove the contaminant from water, the adsorption technique is unable to destroy/degrade the contaminants and disposal step is required [77]. Photocatalysis is a useful approach for water remediation/wastewater treatment for the complete degradation and mineralization of organic/biological contaminants [78]. Graphene-based photocatalysts have been reported for their improved activity because of their high surface area, nanosize, and more electronic movements as compared to the traditionally used materials [78, 132]. Rommozzi et al. designed reduced graphene oxide (rGO) with a greener reduction method using glucose and ammonium hydroxide and successfully designed a photocatalyst which is visible by the fabrication with TiO2 . The designed rGO-TiO2 photocatalyst was successfully applied for the refractory dye named Alizarin Red S (ARS) [133]. In other studies, graphene oxide fabricated with TiO2 and ZnO exhibited much photodegradation of methylene blue as compared to TiO2 /ZnO alone [79, 80].
Graphene and Graphene Oxide-Based Adsorbents for the Purification of Heavy Metal-Contaminated Water
Graphene is one-atom-thick-layered hexagonal lattice of carbon atoms and is known as the thinnest material with the strength of 200 times than steel. Graphene was discovered in 2004 by Sir Andre Geim and Sir Konstantin Novoselov, who were awarded a Nobel prize for their discovery in 2010. Graphene (2-D) is being used widely in almost every field such as in touch screens, mobiles, LCDs, semiconductors, computer chips, batteries, energy generation, water filters, supercapacitors, solar cells, and biomedical and environmental sciences [134,135,136,137]. These 2-D graphene-based materials are getting more and more attention in water treatment due to their unique physicochemical characteristics namely electronic properties, high surface area, thermal mobility, high mechanical strength, and tunable surface chemistry [118, 134, 138, 139]. Tabish et al. designed porous graphene and applied it as an adsorbent for the removal of heavy metal ions as well as other pollutants from water. They applied this porous graphene material for As 3+ removal from water and found 80% efficiency. The material was found to retain its water treatment properties after regeneration and recycling [138]. Guo et al. designed a nanocomposite of partially reduced graphene oxide by its fabrication with Fe3 O 4 via in situ co-precipitation method and applied it for the removal of Pb 2+ ions from water. The designed nanocomposite was found to be excellent in removing the Pb 2+ ions from aqueous solution with an adsorption capacity of 373.14 mg/g [140]. Zhang et al. functionalized the reduced graphene oxide with 4-sulfophenylazo (rGOs) and applied it for the removal of a variety of heavy metal ions from aqueous solution. The designed material showed the maximum adsorption capacity of 689, 59, 66, 267, and 191 mg/g for the Pb 2+ , Cu 2+ , Ni 2+ , Cd 2+ , and Cr 3+ respectively [141]. Diana et al. designed a graphene-based self-propelled microbot system whose structure was made up of nanosized multilayered consisting of graphene oxide, nickel, and platinum. Each layer performed a different function, e.g., graphene oxide captures the heavy metal Pb 2+ ions, the middle layer of Ni enables the control of microbots with the help of external magnetic field, and the inner layer of platinum helps the engine in self-propelling [142]. The designed system was found to remove the 80% of the Pb 2+ water solution. Figure 5 shows the schematic illustration of the working principle of microbots. Yang et al. designed hydrogen beads using graphene oxide and sodium alginate (GO-SA) and successfully applied them for the removal of Mn 2+ ions from the aqueous solution with excellent adsorption capacity of 56.49 mg/g [9]. Zheng et al. designed nanocomposites by fabrication of zinc oxide with tea polyphenol with reduced graphene oxide (TPG-ZnO). Designed material was applied for the removal of heavy metal ions with an added advantage of antibacterial properties [143]. They applied this material for the removal of Pb 2+ ions from aqueous solution with adsorption efficiency of 98.9%, and the adsorbent was found to possess antibacterial properties against Streptococcus mutans with 99% eradication [143]. Mousavi et al. designed nanocomposites of graphene oxide with iron oxide magnetite nanoparticles Fe3 O 4 and applied them for the removal of Pb 2+ ions from water and the material showed 98% removal efficiency with a capacity of 126.6 mg/g [144]. Considering functionalized graphene as an adsorbent to remove Pb 2+ ions from an aqueous medium, the highest record of Pb 2+ ion removal over graphene is 406.6 mg/g at pH of 5.0 in 40 min [145]. Graphene-hydrogel lingo sulfonate functionalized nanocomposites having oxygenated functional groups making the surface highly polar reported to increase the rate of adsorption of Pb 2+ ions with maximum efficacy of 1308 mg/g with the equilibrium reached in 40 min. Awad et al. modified graphene oxide with chloroacetic acid (GO-COOH) and ethylenediamine (GO-amino). The designed systems were applied for the removal of mercury (Hg 2+ ) from water and found that the nanocomposites (GO-COOH) and (GO-amino) have an adsorption capacity of 122 mg/g and 230 mg/g. In addition to this, designed systems retained their adsorption efficiency after the recycling process [146]. Yan et al. designed magnet graphene oxide for the rapid removal and separation of Fe (II) and Mn (II) from micropolluted water [147]. Ali et al. designed graphene-based adsorbent successfully for the removal of noxious pollutants namely Cu (II), Pb (II), Fe (II), and Mn (II) [148].
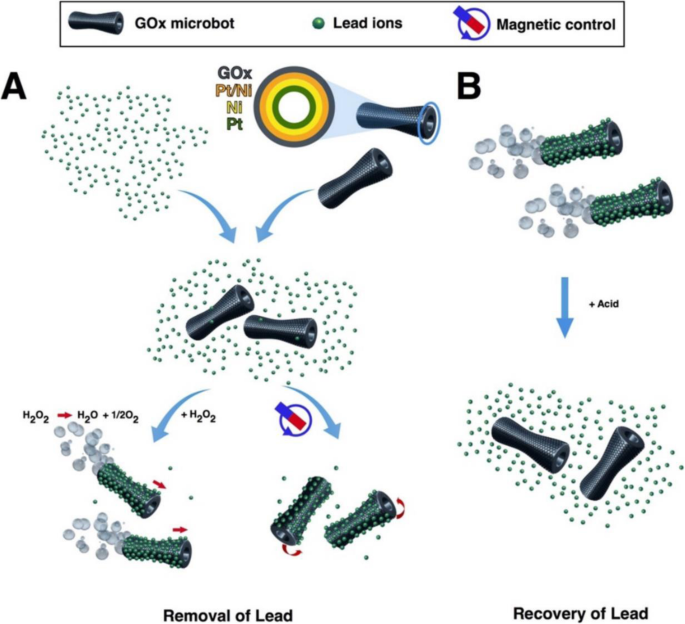
Scheme of GOx-microbot-based approach for lead decontamination and recovery. a Decontamination of polluted water using GOx-microbots fabricated by electrodeposition of nanolayers of graphene oxide (GOx), Pt/Ni layer, Ni magnetic layer, and Pt catalytic inner layer. The decontamination strategy for lead ions can be carried out by two different techniques:self-propulsion of the GOx-microbots in the presence of H2 O 2 or by using an external rotating magnetic field. b Recovery of lead ions from the GOx-microbots in the presence of acidic media [117]
Biocompatibility of Graphene-Based Nanomaterial
Graphene-based nanomaterials have been applied in different fields like electronics, chemical sensors, biosensors, drug delivery, theragnostic, and other related biomedical fields. These studies also report the cytocompatibility of graphene-based materials both by in vitro as well as in vivo animal studies [122, 133, 149,150,151,152]. These findings suggest that the graphene-based materials are safe for the environmental remediation application as they are just used for the removal and degradation of pollutants and are not consumed by humans directly.
Activated Carbon in Environmental Remediation
Activated carbon is a fabulous material because of its high surface area, highly porous structure, and ease of preparation with variety of starting materials. Because of its ideal physicochemical properties, it has wide application in environmental remediations in different industries like pharmaceutics, fertilizer plants, petroleum, cosmetics, automobiles, and textiles [153] It is also widely applied for the adsorption of gases, solvent recovery, and wastewater treatment especially for the removal of organic dyes/other pollutants; not only this, but it is also used as a catalyst in biodiesel production. It is also applied as a low-cost material for the treatment and removal of water containing COD, BOD, and TSS and stabilizing and maintaining the optimum pH for biological uses [154,155,156]. Maguana et al. prepared activated carbon from the pear seed cake and successfully applied it for the removal of methylene having an adsorption capacity of 260 mg/g [157]. Antonio et al. prepared activated carbon from the kenaf plant and applied it successfully for the treatment of the wastewater of hospitals containing paracetamol as the main pollutant [158]. The above literature suggests that the activated carbon is the pretty useful economical material which can easily be prepared and it has immense application in environmental remediations.
Activated Carbon as Adsorbents in the Purification of Heavy Metal-Contaminated Water
Activated carbon (AC) is also known as activated charcoal, and this of type carbon material is formed under some treatment protocols resulting in micro/nanopores and having the large surface area of more than 3000 m 2 [159]. The AC is produced on a large scale from coal, wood, and agricultural wastes [160]. In addition to its porous nature (as shown in Fig. 6), AC also has a high mechanical strength which enables its applications in catalyst support, capacitors, electrodes, and gas storage and most importantly used as the adsorbent for removal of metal ions, organic wastes, and gases from water [160,161,162]. The high mechanical strength of activated carbon enables its periodic cleaning, regeneration, and reutilization [160]. Abeer et al. reported the preparation of AC from apricot stone and its application in removal of Zn + 2 and Al + 3 ions with removal efficiency of 92% [163]. Ebrahim et al. designed AC from sewage sludge, applied it for the removal of Cu + 2 ions from water, and found that the designed material showed maximum adsorption capacity of above 50% [164].
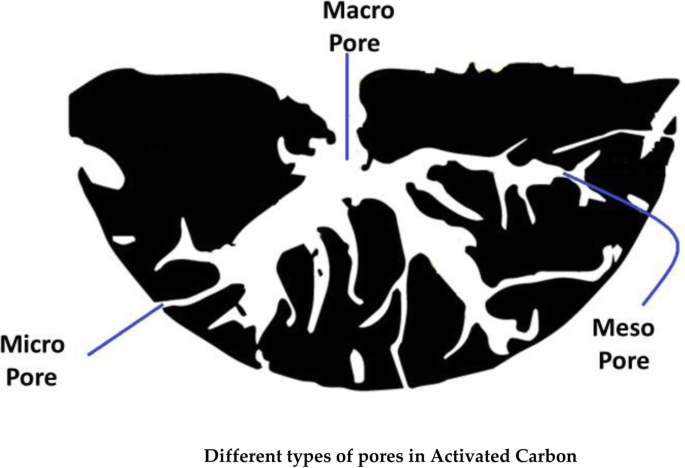
Different types of pores in activated carbon
Li et al. prepared the AC from sewage sludge produced from the wastewater treatment plant and functionalized it with sulfur [165]. They applied sulfonated AC for the removal of Pb 2+ , Cd 2+ , Cu 2+ e Ni 2+ ions from water. The adsorption capacity of metal ions were found to be 238.1 mg/g, 96.2 mg/g, 87.7 mg/g, and 52.4 mg/g for Pb 2+ , Cd 2+ , Cu 2+ e Ni 2+ respectively [165]. Cao et al. designed multipore activated carbon (MPAC) with a large surface area using the agricultural waste of long-root Eichhornia crassipes and applied it for removing heavy metal ions, e.g., Pb 2+ , Cd 2+ , Cu 2+ , Ni 2+ , and Zn 2+ . They found that at 30 °C adsorption capacity being 1.34 mmol/g, 1.07 mmol/g, 1.22 mmol/g, 0.97 mmol/g, and 0.93 mmol/g for Pb 2+ , Cd 2+ , Cu 2+ e Ni 2+ respectively [166]. Dong et al. investigated the application of spent activated carbon (AC) for heavy metal ion removal from water and found high adsorption capacity of 95% and 86% for Pb 2+ and Cd 2+ ions respectively [167]. M. Bali et al. [168] applied commercial AC for the removal of heavy metal ions and found that adsorption equilibrium of Cd 2+ ion took 15 min while for Pb 2+ , Zn 2+ , and Cu 2+ it took 45 min with percentage removal of 64% for all these ions and with Cd 2+ being the highest [10]. Kongsuwan et al. prepared the activated carbon from the agricultural waste of eucalyptus bark. They applied it for the removal of Cu 2+ and Pb 2+ from water with maximum removal capacity of 0.45 and 0.53 mmol per gram of AC respectively, with adsorption being the main mechanism of ion uptake [169]. AC poultry litter has also been reported and applied for the treatment of heavy metal-contaminated water and found that for 1 kg of poultry litter AC adsorbs 404 mmol, 945 mmol, 236 mmol, and 250–300 mmol of Cu 2+ , Pb 2+, Zn 2+ , and Cd 2+ ions respectively [170]. This adsorption is significantly higher than the commercially available AC derived from coconut and bituminous. The AC of wood saw dust of rubber plant has also been reported for the removal of heavy metal ions of Cr + 6 from water with adsorption capacity of 44 mg/g [171]. AC formed from Moso and Ma bamboo was found to be highly efficient in removing the heavy metal ions, i.e., Pb 2+, Cu 2+ , Cr 3+ , and Cd 2+ with the maximum adsorption capacity of more than 90% removal [172]. Naser et al. prepared AC from rice husk and applied them for the removal of Cu 2+ from aqueous solution, and maximum capacity was found to be 33.92%. Similar results have also been reported for the removal of Cu 2+ from the AC formed from Palm shell [173]. AC of love stones has been reported for the adsorption of Cd + 2 and Ni + 2 with adsorption capacity of 1.85 mg/g and 0.67 mg/g respectively in two different studies [174, 175]. AC prepared from olive stone using the microwave method has been applied for the removal of Fe 2+, Pb 2+, Cu 2+, Zn 2+, Ni 2+ , and Cd 2+. from wastewater. Another study reported on the olive stone AC prepared via microwave to remove a group of metal ions from synthetic wastewater:Fe 2+ , Pb 2+ , Cu 2+, Zn 2+ , Ni 2+ , and Cd 2+ with removal efficiency of more than 98% [176]. Tamarind wood AC has been reported for the highest adsorption capacity of above 97% for Pb 2+ from water [177]. Activated carbon has been applied as an adsorbent for the removal of Fe (II) and Mn (II) with great efficiency [178, 179]. The activated carbon is easy to synthesize, is cheaper, and is the most promising material for the adsorption of heavy metal ions and can be prepared at a large scale from a variety of carbon sources especially form agricultural waste. In addition to easier preparation, AC can easily be functionalized. Table 2 summarizes the effect of different parameters on the process of metal ion adsorption.
Biocompatibility of the Activated Carbon
Different studies have been conducted for the biocompatibility evaluation of the activated carbon materials prepared form different carbon sources. Activated carbon has been applied for the treatment of cystitis and was found to be effective and nontoxic compared to the antibiotics being applied [180]. Biocompatibility of activated carbon can be attributed to its inertness, and it has also been functionalized and fabricated with other materials to confer on the disinfection properties [181]. The activated carbon is also given orally to human beings as a sorbent for the removal of toxins from the human body and has also been utilized in biomedical applications [182, 183]. These studies strongly suggest the biocompatibility of the activated carbon.
Conclusion
In this review, environmental and special purification of heavy metal from heavy metal contaminants by the applications of carbon nanomaterials, namely fullerene carbon nanotubes, graphene, graphene oxide, and activated carbon discussed. These carbon nanomaterials have been utilized in the purification of heavy metal-contaminated water with great success. The reason behind the successful application is due to their fascinating properties like high surface area, ease of recycling, and easiness to desorb the adsorbed metal ions; only using mineral acid solution and regenerated material can be reused with retention of adsorption capability. In addition to these properties, the carbon nanomaterials can easily be fabricated with other nanomaterials and are easy to be functionalized resulting in multifunctional nano-adsorbent. Carbon-based materials are highly biocompatible with living organisms and environment. There is also an immense effect of different parameters such as pH, contact time, and type of adsorbents on the process of metal ion adsorption. Based on this literature review, it can be concluded that carbon nanomaterials have fascinating physicochemical properties and have great potential to be exploited in the environmental remediation and water purification.
Disponibilidade de dados e materiais
Todos os dados estão totalmente disponíveis sem restrição.
Abreviações
- AC:
-
Activated carbon
- GO:
-
Óxido de grafeno
- MWCNTs:
-
Multiwall carbon nanotubes
- r-GO:
-
Óxido de grafeno reduzido
- SWCNTs:
-
Single-wall carbon nanotubes
Nanomateriais
- A fórmula perfeita para alinhar operações e manutenção
- Os prós e contras dos anéis de fibra de carbono
- A diferença entre fibra de carbono e fibra de vidro
- Materiais:Vidro e PP reforçado com fibra de carbono para automotivo
- Os cinco principais problemas e desafios para 5G
- Avanços e desafios dos nanomateriais fluorescentes para aplicações biomédicas e de síntese
- Entendendo o conceito de IoT no tratamento e gerenciamento de águas residuais
- Lanterna lunar para procurar água na lua
- O equipamento certo para as configurações certas
- A importância do tratamento térmico eficaz para punções, matrizes, lâminas e aços para ferramentas



