Nanotubos de carbono de parede única direcionados para terapia fototérmica combinada com inibição de ponto de verificação imune para o tratamento de câncer de mama metastático
Resumo
Os maiores contribuintes para a mortalidade por câncer são as metástases e as consequências de seu tratamento. Aqui, apresentamos um novo tratamento de câncer de mama metastático que combina terapia fototérmica com nanotubos de carbono de parede única direcionados (SWCNTs) e imunoestimulação com um inibidor de checkpoint. Descobrimos que a ablação fototérmica de infravermelho próximo seletiva de tumores de mama EMT6 ortotópicos primários em camundongos BALB / cJ singênicos usando um bioconjugado SWCNT funcionalizado com anexina A5 (ANXA5) aumenta sinergicamente uma proteína 4 associada a linfócitos T anticitotóxicos (anti-CTLA- 4) resposta abscopal dependente, resultando em um aumento da sobrevivência (55%) em 100 dias após a inoculação do tumor. Em comparação, não houve sobrevida em 100 dias para a terapia fototérmica por si só ou para a imunoestimulação por si só. Antes da terapia fototérmica, o bioconjugado SWCNT-ANXA5 foi administrado sistemicamente a uma dose relativamente baixa de 1,2 mg / kg, onde então se acumulou na vasculatura tumoral via ligação dependente de ANXA5. Durante a terapia fototérmica, a temperatura média máxima no tumor atingiu 54 ° C (duração 175 s). O mecanismo de sobrevivência prolongada resultante da ablação fototérmica combinatória e estimulação imune foi avaliado por quantificação por citometria de fluxo de células efetoras imunes antitumorais esplênicas e quantificação de citocinas séricas.
Introdução
A metástase e as consequências de seu tratamento são a maior causa de morte no câncer [1]. Por exemplo, quando o câncer de mama sofre metástase, as taxas de sobrevida de 5 anos do paciente caem para menos de 25%. Embora nos últimos 60 anos mais de 200 novos medicamentos antineoplásicos tenham melhorado os desfechos dos pacientes, a sobrevida geral permanece baixa na doença metastática [2]. Aqui, uma nova combinação de terapia fototérmica facilitada por um bioconjugado de nanotubo de carbono de parede única (SWCNT) direcionado a tumor e a inibição do ponto de verificação de proteína 4 associada a linfócitos T anticitotóxicos (anti-CTLA-4) é estudada para o tratamento de câncer de mama metastático em um modelo ortotópico murino.
As propriedades exclusivas dos SWCNTs como nanomateriais geraram um interesse significativo em seu uso como uma ferramenta potencial na luta contra o câncer. Embora os SWCNTs exerçam uma variedade de efeitos biológicos, o uso de SWCNTs no tratamento do câncer tem se concentrado principalmente em sua interação com a luz infravermelha próxima (NIR) e o efeito fototérmico resultante, onde os SWCNTs aquecem rapidamente o tumor no processo denominado terapia fototérmica (PTT). Numerosos grupos investigaram o potencial dos SWCNTs para serem usados em estratégias de tratamento baseadas em PTT em vários modelos de câncer de mama [3,4,5,6,7,8,9,10]. Esses trabalhos se concentraram amplamente na capacidade do PTT de tratar tumores primários em profundidades não superiores a vários mm, onde a atenuação da luz NIR é quase completa.
Anteriormente, mostramos que os tumores ortotópicos primários da mama em camundongos singênicos poderiam ser quase completamente eliminados usando luz laser NIR suave em conjunto com um bioconjugado SWCNT com potencializador fototérmico [11]. Neste bioconjugado, os SWCNTs foram funcionalizados com a proteína anexina A5 (ANXA5), que se liga com alta afinidade ao fosfolipídio aniônico fosfatidilserina expresso externamente em células tumorais e em células endoteliais da vasculatura tumoral, mas não em células normais na vasculatura [ 12,13,14]. Este conjugado foi visualizado usando microscopia de força atômica (AFM) para mostrar que a altura do conjugado estava entre 2,5 e 5,0 nm, que é semelhante à de outros conjugados SWCNT-proteína [11]. Embora capaz de erradicar tumores primários neste modelo metastático anterior, a terapia fototérmica por si só estendeu modestamente a sobrevida. No entanto, encontramos evidências preliminares sugerindo que o tratamento concomitante com imunomoduladores, como a ciclofosfamida, foi capaz de aumentar a sobrevida.
Recentemente, o potencial de imunomoduladores, como a ciclofosfamida, para aumentar sinergicamente o PTT direcionado por SWCNT tem sido o assunto de muito interesse. Uma categoria de agentes imunomoduladores promissores são os inibidores de checkpoint. Os inibidores de checkpoint são anticorpos, como anti-CTLA-4, anti-PDL-1 e anti-PDL-1, que se ligam a proteínas celulares críticas responsáveis por modular a resposta do corpo ao câncer. Esses anticorpos bloqueiam os principais "pontos de verificação" biológicos onde o corpo pode regular negativamente a resposta do sistema imunológico ao câncer. Essas proteínas normalmente desempenham um papel importante no controle da resposta imunológica do corpo. Ao bloquear a ação dessas proteínas, os inibidores de checkpoint removem um mecanismo pelo qual o sistema imunológico normalmente suprime sua resposta antitumoral natural. Recentemente, vários grupos observaram que a combinação de inibição do ponto de verificação anti-CTLA-4 com PTT aprimorado de SWCNT tem o potencial de promover uma resposta imune robusta no câncer de mama [15, 16].
No estudo atual, avaliamos a combinação de nossa nova modalidade PTT em conjunto com o agente imunoestimulador proteína 4 associada a linfócitos T citotóxicos (anti-CTLA-4). Originalmente aprovado para o tratamento do melanoma metastático [17], o anti-CTLA-4 agora está sendo testado para o tratamento do câncer de mama em ensaios clínicos combinados com outros agentes imunoestimuladores [18]. Nós avaliamos o mecanismo de imunidade antineoplásica aumentada em PTT em combinação com a inibição do checkpoint anti-CTLA-4, bem como o destino de longo prazo de SWCNTs em órgãos-alvo.
Materiais e métodos
Materiais
O plasmídeo que codifica ANXA5, pET-30 Ek / LIC / ANX, foi previamente construído neste laboratório [11]. Albumina de soro bovino (BSA), Triton X-100, EDTA, β-mercaptoetanol, fluoreto de fenilmetilsulfonil (PMSF) e tampão Tris-acetato-EDTA foram da Sigma-Aldrich (St Louis, MO). O fosfato de sódio e o dodecilsulfato de sódio (SDS) eram da Mallinckrodt Chemicals (Phillipsburg, NJ). O etanol de qualidade para HPLC era da Acros Organics (Waltham, MA). As colunas His-trap eram da GE Healthcare (Chicago, IL). Tampão de coloração de citometria de fluxo, tampão de fixação / permeabilização, tampão de permeabilização, kit de quantificação de endotoxina cromogênica e cassetes de diálise Slide-A-Lyzer (3,5 kDa) foram da Thermo Fisher Scientific (Waltham, MA). As membranas de diálise de 2 e 100 kDa eram da Spectrum Laboratories (Rancho Dominguez, CA). O meio celular do Roswell Park Memorial Institute (RPMI-1640) e a solução salina balanceada de Hank eram da ATCC (Manassas, VA). O soro fetal bovino (FBS) era de Atlanta Biologicals (Lawrenceville, GA). Triptona, extrato de levedura e monossulfato de canamicina foram obtidos de Alfa Aesar (Ward Hill, MA). O hidróxido de sódio, o cloreto de potássio e o cloreto de sódio eram da VWR Inc (Radnor, PA). A protease HRV-C3 era da Sino Biologics (Portland, OR). Anticorpo monoclonal de camundongo anti-CTLA-4 (clone:9H10) e kits de ELISA de citocina de camundongo (TNF-α, IFN-γ, IL-6) foram obtidos de BioLegend (San Diego, CA). Os SWCNTs do CoMoCAT (diâmetro médio 0,8 ± nm, comprimento médio 1,5 ± 0,5 µm) foram obtidos no CHASM (Boston, MA). O método CoMoCAT é conhecido por produzir SWCNT de um pequeno número de ( n , m ) quiralidades com alta seletividade [19]. A amostra usada neste estudo é altamente enriquecida em [5, 6] SWCNTs, que exibe uma forte absorção de luz NIR em um comprimento de onda de 980 nm. Esta absorção corresponde ao S 11 transição para este tipo de nanotubo entre uma singularidade de van Hove ocupada para a correspondente não ocupada. Portanto, para maximizar a absorção de radiação pelo SWCNT depositado nos tumores, o comprimento de onda do laser usado neste estudo foi de 980 nm para corresponder exatamente ao do S 11 transição óptica [20]. A Figura S1 no arquivo adicional 1 mostra os espectros de fluorescência, mostrando claramente o S 11 Emissão de NIR após excitar a transição S22 com luz visível.
Cultura de células
As células de câncer de mama EMT6 da ATCC (Manassas, VA) foram cultivadas em meio MB 752/1 da Waymouth com L-glutamina 2 mM suplementado com FBS a 15%. Todas as células foram cultivadas a 37 ° C e 100% de umidade sob 5% de CO 2 . Todas as células foram passadas usando 0,25% (p / v) de tripsina em 0,53 mM de EDTA. A linhagem celular e o status de livre de micoplasma foram confirmados por meio de teste de STR (Charles River) e testado como livre de endotoxina pelo ensaio de limulus.
Produção ANXA5 e SWCNT-ANXA5
O conjugado SWCNT-ANXA5 foi preparado usando um procedimento que desenvolvemos anteriormente que fornece 2,5 mg ANXA5 / mg SWCNT [11]. Resumidamente, E. coli transfectadas com um plasmídeo que codifica ANXA5, pET-30 Ek / LIC / ANX, foram cultivadas e purificadas usando cromatografia de afinidade de metal imobilizado com Ni 2+ imobilizado para isolar o ANXA5, que envolveu a clivagem enzimática para remover um (His) 6 marcação. CoMoCAT SWCNTs liofilizados foram dispersos em 1% de dodecil sulfato de sódio (SDS) usando dois ciclos de sonicação de sonda a 20 W e centrifugação a 29.600 g por 30 min cada. Os SWCNTs suspensos foram caracterizados por fluorescência NIR (arquivo adicional 1:Figura S1) e, em seguida, conjugados a um ligante 1,2-distearoil-sn-glicero-3-fosfoetanolamina-polietilenoglicol-maleimida (DSPE-PEG-maleimida) por 30 min à temperatura ambiente para permitir a interação hidrofóbica entre os SWCNTs e o grupo funcional DSPE. Isto foi então seguido por uma diálise de 8 h em água destilada para remover o excesso de ligante e SDS. O conjugado dialisado foi então reagido com ANXA5, que contém um grupo de cisteína, por 2 he bloqueado com 1,5 mg ml −1 L-cisteína. O produto final, SWCNT-ANXA5, foi dialisado contra tampão de fosfato de sódio 20 mM por 8 h para remover o excesso de ANXA5 e L-cisteína. O peso e a pureza da proteína foram caracterizados por SDS-PAGE. O conteúdo SWCNT e ANXA5 do bioconjugado foi caracterizado por espectroscopia de fluorescência UV-Vis-NIR, espectroscopia de infravermelho com transformada de Fourier (FT-IR), análise Raman e ensaio de Bradford (arquivo adicional 1:Figura S2).
Estudos In Vivo
Todos os procedimentos obedeceram a um protocolo aprovado pelo Comitê de Uso e Cuidado Institucional de Animais (IACUC) da Universidade de Oklahoma. Foram usados ratos fêmeas BALB / cJ com 6 semanas de idade (Jackson Laboratory, Bar Harbor, ME). Os camundongos foram alimentados com uma dieta alimentar padrão. Durante a irradiação fototérmica de tumores com uma luz laser NIR, os camundongos foram anestesiados com 2% de isoflurano e 98% de oxigênio usando um cone nasal.
Os tumores foram induzidos por injeção ortotópica de 10 6 Células de câncer de mama de camundongo EMT6 em 100 µL de PBS na almofada de gordura mamária IV. Os tumores puderam crescer por 12 dias e quando atingiram um volume de 60 mm 3 (~ 5 mm de diâmetro), os camundongos receberam uma via intravenosa sistêmica. injeção de 1,2 mg / kg de SWCNT-ANXA5 (mg de SWCNT por kg de peso corporal) bioconjugado através da veia lateral da cauda. Após 3 h, uma região 5 mm em excesso do limite do tumor foi irradiada com luz NIR (980 nm) a um nível de energia e potência de 175 J / cm 2 e 1 W / cm 2 , respectivamente (tempo de 175 s; laser Diodevet-50 NIR, B&W Tek Inc., Newark, DE). A inibição do ponto de verificação foi realizada por via i.p. administração de 200 µg de anticorpo anti-CTLA-4 em 100 µl de PBS nos dias 8, 11 e 16 após a inoculação do tumor. O volume do tumor foi calculado com a fórmula elipsoide modificada \ (V =\ frac {1} {2} \ times {\ text {length}} \ times {\ text {largura}} ^ {2} \) usando medidas do calibre do maior dimensão e largura perpendicular. A temperatura do tumor foi monitorada por uma câmera térmica FLIR TG165 Spot portátil (Raymarine ITC, Fareham, Reino Unido) configurada para varredura automática para a temperatura máxima detectada. Os órgãos alvo foram colhidos para avaliação de toxicidade e fixados em formalina tamponada neutra a 10%, e lâminas coradas com formalina fixada e embebida em parafina (FFPE) foram preparadas e coradas com hematoxilina e eosina para análise de toxicidade.
Detecção Ex Vivo SWCNT
Os camundongos receberam uma injeção sistêmica de 1,2 mg / kg de SWCNT-ANXA5 (mg de SWCNT / kg de peso corporal) através da veia lateral da cauda. Em determinados momentos, ratos ( n =3) foram sacrificados, necropsiados e os órgãos-alvo removidos para análise. As amostras de tecido foram preparadas conforme descrito anteriormente [21]. A presença de SWCNTs em amostras de tecido ex vivo foi então determinada por espectroscopia de fluorescência NIR relativa usando um NS3 NanoSpectralyzer (Applied NanoFluorescence, Houston, TX).
Citometria de fluxo
Os camundongos foram sacrificados 14 dias após o tratamento e as células efetoras imunes antitumorais esplênicas foram quantificadas conforme descrito anteriormente [21].
Detecção de citocinas
Após o tratamento conforme descrito acima, camundongos ( n =4-5) foram sacrificados 7 dias após a terapia fototérmica para coleta de sangue. A concentração do fator de necrose tumoral alfa (TNF-α), interferon gama (IFN-γ) e interleucina 6 (IL-6) em amostras de soro diluídas foi quantificada por ELISA de acordo com o protocolo do fornecedor.
Análise estatística
Os dados foram analisados com o software Graphpad Prism. A significância estatística foi avaliada usando ANOVA de uma via e teste de comparações múltiplas de Tukey-Kramer. A significância estatística das curvas de sobrevivência foi determinada pelo teste de log-rank de Mantel-Haenszel. A significância estatística da concentração de citocinas no soro foi analisada por ANOVA de uma via e teste de comparações múltiplas de Dunnett. As comparações múltiplas foram corrigidas pelo limiar de Bonferroni. O erro é representado graficamente como erro padrão da média, a menos que o erro não exceda o tamanho do símbolo de ponto médio traçado, caso em que as barras foram excluídas para maior clareza.
Resultados
Cinética Térmica
Usando uma dose de 1,2 mg / kg de SWCNT-ANXA5, a temperatura máxima dos tumores foi registrada ao longo do tratamento com luz NIR, conforme indicado na Fig. 1. Os camundongos que receberam SWCNT-ANXA5 antes da irradiação tiveram temperaturas tumorais mais altas para o todo o tratamento com luz NIR em comparação com camundongos que receberam solução salina fisiológica. A temperatura média do tumor para camundongos que receberam SWCNT-ANXA5 foi significativamente diferente do que era para camundongos que receberam solução salina fisiológica (54 ° C vs. 37 ° C, p <0,05). Como resultado desta terapia fototérmica melhorada, apenas no grupo SWCNT-ANXA5 ocorreu a ablação do tumor visível. A ablação do tumor foi caracterizada por rápida descoloração, seguida de contratura da pele e aparecimento de rugas. Em 48 h, uma escara significativa se formou no local da ablação fototérmica. O crescimento completo da pele levou várias semanas.
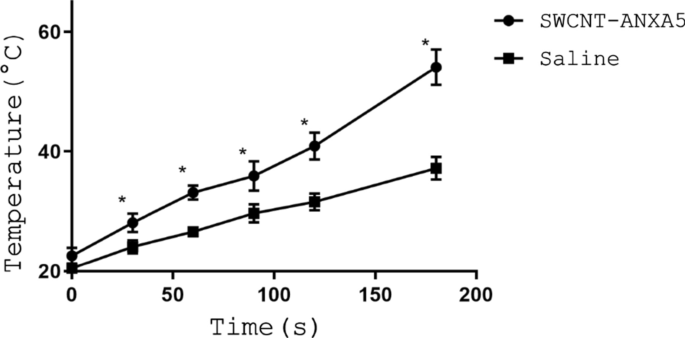
Cinética térmica resultante da radiação de tumores com luz NIR a 980 nm. Ratinhos BALB / cJ com tumores EMT6 foram injectados por i.v. na veia da cauda com 1,2 mg / kg de SWCNT-ANXA5. Depois de esperar 3 horas para permitir a eliminação de SWCNTs da circulação, os tumores foram irradiados com um laser NIR a uma densidade de energia e potência de 175 J / cm 2 e 1 W / cm 2 , respectivamente ( t =175 s). A temperatura máxima do tumor foi registrada em função do tempo. A temperatura dos tumores de camundongos que receberam SWCNT foi significativamente mais alta do que para camundongos que receberam solução salina fisiológica em t =175 s ( p <0,05). Os dados são apresentados como média ± SE ( n =3)
Terapia fototérmica e inibição de checkpoint
Os resultados da combinação da terapia fototérmica com a inibição do checkpoint usando o anticorpo monoclonal anti-CTLA-4 são mostrados na Fig. 2. Embora a terapia fototérmica por si só tenha erradicado prontamente a neoplasia primária do câncer de mama, a incapacidade da luz do laser NIR de penetrar além de alguns mm limitou o tratamento da metástase do câncer de mama. A fim de superar as deficiências do tratamento antineoplásico fototérmico NIR localizado, exploramos a combinação desta modalidade de tratamento terapêutico única com a inibição de checkpoint sistêmico (Fig. 2). Enquanto a terapia fototérmica foi excelente na destruição de tumores EMT6 primários (Fig. 2a), este tratamento falhou em erradicar a metástase e apenas aumentou modestamente a sobrevivência de camundongos com tumores ortotópicos EMT6 (Fig. 2b). Em contraste, a inibição do checkpoint com anti-CTLA-4 aumentou a sobrevida global, mas apenas retardou temporariamente o crescimento do tumor primário. Embora nenhuma das terapias por si só tenha produzido qualquer aumento na sobrevida global, a combinação de terapia fototérmica aprimorada de SWCNT-ANXA5 e inibição do ponto de verificação anti-CTLA-4 melhorou a sobrevida geral, levando a 55% de sobrevida em 100 dias após a inoculação do tumor.
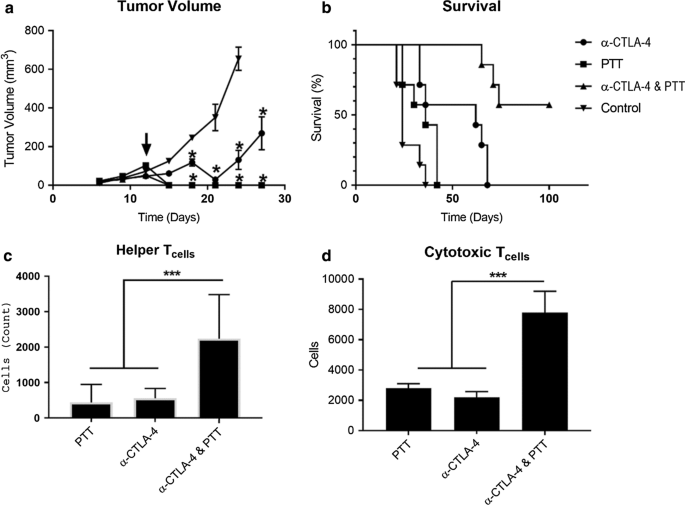
Resultados da terapia fototérmica combinatória (PTT) e da inibição do checkpoint (anti-CTLA-4) em tumores EMT6. Camundongos com tumores singênicos ortotópicos bem desenvolvidos ( d ≥ 5 mm) foram administrados i.v. dose sistêmica de 1,2 mg / kg de SWCNT-ANXA5. a Os volumes do tumor foram então monitorados após irradiação (seta) com luz laser NIR por 175 s a uma densidade de potência de 1 W / cm 2 no dia 12 após a inoculação. Além de PTT, grupos selecionados receberam anti-CTLA-4 (100 µg) nos dias 8, 11 e 16. Os camundongos no grupo de controle foram injetados i.v. com soro fisiológico. Volume do tumor mostrado como média ± SE ( n =7). A significância em comparação com o controle é indicada por * ( p <0,05). b A combinação de terapia fototérmica e inibição do ponto de controle imunológico aumentou significativamente a sobrevida em comparação com os controles ( p <0,05, n =7). c , d Somente quando os camundongos receberam terapia fototérmica em conjunto com a inibição do ponto de verificação anti-CTLA-4 aumentaram significativamente nos números relativos de CD4 + e CD8 + esplenócitos observados 2 semanas após o PTT. Esplenócitos mostrados como média ± SE ( n =3). A significância é indicada por *** ( p <0,005)
A análise citométrica de células efetoras esplênicas após o tratamento revelou um mecanismo putativo de sobrevivência melhorada em camundongos que receberam terapia fototérmica combinatória e inibição de checkpoint. Os camundongos foram inoculados com EMT6 e tratados conforme descrito anteriormente. Duas semanas após o tratamento, os camundongos foram sacrificados e as porcentagens e o número relativo de vários tipos de efetores imunes foram quantificados. As populações de células T auxiliares, células T citotóxicas, neutrófilos, células supressoras derivadas de mieloide (MDSC), monócitos, células T regulatórias FoxP3 e macrófagos foram avaliadas (arquivo adicional 1:Figura S3). A análise dessas populações revelou diferenças significativas entre as populações de tratamento e controles apenas em camundongos que receberam a combinação de terapia fototérmica e inibição do ponto de verificação anti-CTLA-4 juntos. Naqueles animais que receberam esta combinação, observamos um aumento no número relativo de células T auxiliares (CD4 + ) e células T citotóxicas (CD8 + ), (Fig. 2c, d). Aumentos no CD4 + e CD8 + as contagens de células correlacionadas com aumentos brutos nos tamanhos do baço observados após a necropsia.
Além da análise citométrica de células efetoras esplênicas, a concentração de citocinas no soro foi determinada 7 dias após o PTT para ajudar a elucidar os mecanismos de imunidade antitumoral. Os níveis das citocinas pró-inflamatórias IL-6, IFN-γ e TNF-α são apresentados na Fig. 3. Nem o tratamento com SWCNT nem com o anti-CTLA-4 isoladamente aumentaram significativamente os níveis de citocinas em comparação com o grupo de controle não tratado. No entanto, o tratamento com PTT sozinho foi capaz de aumentar o TNF-α significativamente. A adição adicional de anti-CTLA-4 ao tratamento com PTT aumentou significativamente os níveis de TNF-α, IL-6 e IFN-γ.
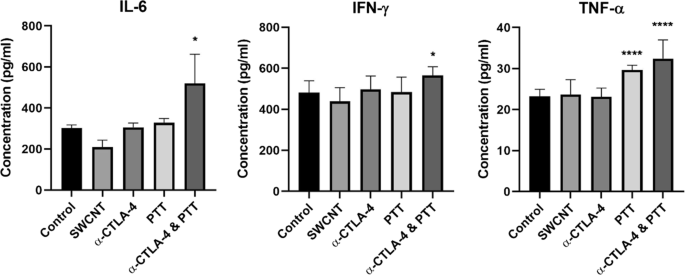
Concentração de citocinas no soro. A quantificação dos níveis de citocinas séricas no soro de camundongo 7 dias após o PTT mostrou um aumento significativo dos níveis de IL-6, IFN-γ e TNF-α em camundongos após PTT em conjunto com a inibição do ponto de verificação (anti-CTLA-4). Os resultados são mostrados para o controle não tratado, tratamento SWCNT apenas, tratamento anti-CTLA-4 apenas, tratamento PTT e tratamento PTT + anti-CTLA-4. Os dados são apresentados como média ± SE ( n =4-5). A significância estatística foi analisada para os grupos tratados em comparação com o grupo de controle não tratado por ANOVA de uma via com teste de comparações múltiplas de Dunnett. A significância estatística é indicada por * ( p <0,05) e **** ( p <0,0001)
Biodistribuição e toxicidade de SWCNT-ANXA5
A biodistribuição de SWCNT-ANXA5 após a administração para intensificação da terapia fototérmica em vários órgãos foi monitorada com quantificação fluorescente de SWCNT em lisados de tecido ex situ em comparação com os padrões (arquivo adicional 1:Figura S4). A biodistribuição nos órgãos alvo foi seguida durante um período de 4 meses após a administração i.v. injeção de 1,2 mg / kg de SWCNT-ANXA5 em camundongos saudáveis (Fig. 4a, b). Em contraste, o acúmulo de SWCNT-ANXA5 em camundongos com tumor EMT6 após a administração, de acordo com o protocolo de injeção descrito anteriormente, foi determinado 3 h após a administração. (O momento em que a terapia fototérmica foi realizada no estudo de tratamento.) Durante o período de 4 meses anterior à colheita do órgão, os camundongos foram monitorados para efeitos colaterais físicos e comportamento anormal. Nenhum efeito colateral foi observado em qualquer camundongo injetado com SWCNT-ANXA5 durante este período de tempo. Nenhuma toxicidade histopatológica foi observada durante o exame de seções FFPE coradas com hematoxilina e eosina de órgãos-alvo na conclusão do estudo (Arquivo adicional 1:Figura S5).
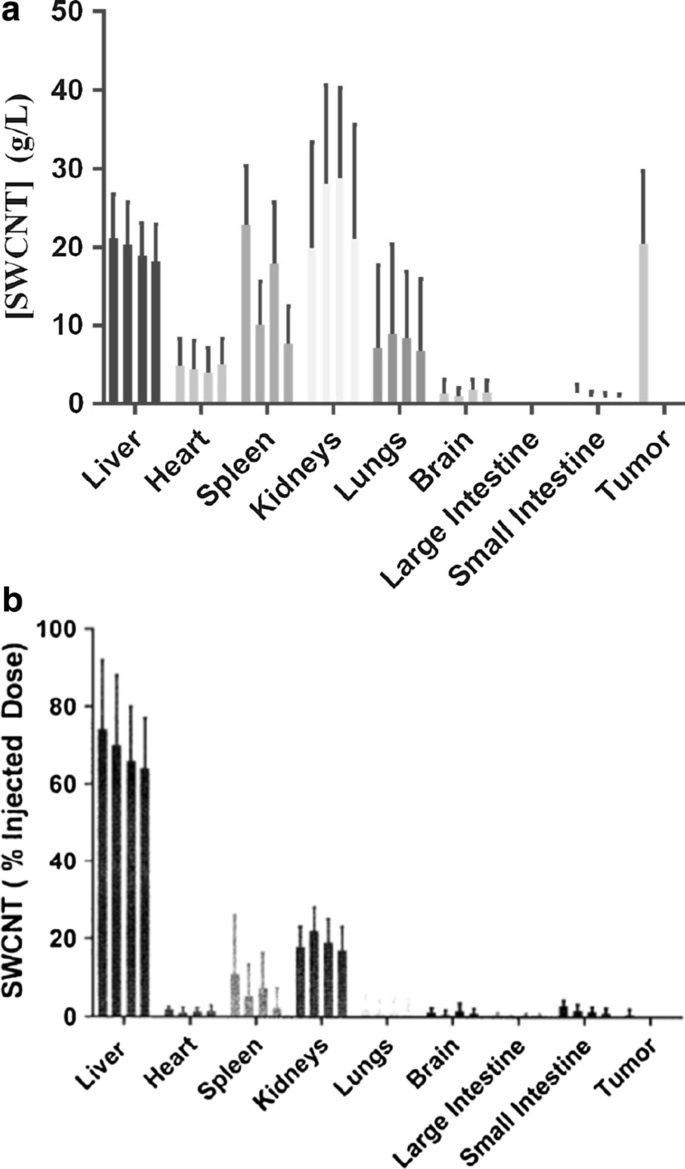
Biodistribuição de SWCNT-ANXA5 medida como% da dose injetada ( a ) e concentração de tecido em g / L ( b ) O conjugado SWCNT-ANXA5 era i.v. injetado em camundongos Balb / cJ a uma dose de 1,2 mg / kg. A concentração de SWCNT foi medida em vários órgãos de camundongos sem tumores após 1, 2, 3 e 4 meses (da esquerda para a direita). Para camundongos com tumores, a concentração de SWCNTs foi medida no momento, pois seria imediatamente antes do tratamento com terapia fototérmica. Os dados são mostrados como média ± SE ( n =3)
Discussão
Os dados apresentados aqui fornecem suporte para a eficácia da combinação de terapia fototérmica direcionada e inibição do ponto de verificação imunológico para o tratamento do câncer de mama metastático. Esse fenômeno é conhecido como “efeito abscopal”, que descreve a capacidade da radiação localizada de iniciar uma resposta antitumoral que suprime o crescimento do tumor distante do alvo primário. Já na década de 1950, os pesquisadores observaram que a irradiação de tumor localizado teve um efeito significativo em tumores distantes [22]. Estudos estabeleceram que a natureza sistêmica do efeito abscopal é devido à resposta imune do hospedeiro [23,24,25]. Embora a irradiação γ tenha sido o foco principal da maioria das pesquisas abscopais, um crescente corpo de trabalho demonstra que a terapia fototérmica pode induzir um efeito abscopal também. Numerosos estudos demonstraram que a ablação térmica em combinação com o inibidor do checkpoint anti-CTLA-4, produz uma resposta imune aumentada [16, 26,27,28,29]. Observamos uma resposta abscopal semelhante após ablação fototérmica direcionada e bloqueio anti-CTLA-4 no modelo EMT6 de câncer de mama.
O efeito abscopal é ilustrado pelos dados nas Fig. 2a, b. Os tumores ortotópicos EMT6 crescem rapidamente e já apresentam metástase no momento em que são tratados pela terapia fototérmica. Esta é a razão pela qual camundongos com tumores tratados apenas com terapia fototérmica tiveram apenas um ligeiro aumento na sobrevida em comparação com camundongos controle não tratados, mesmo que o tumor primário tenha sido completamente ablado. A administração de anti-CTLA-4 sozinho atrasou o crescimento do tumor em comparação com o controle e aumentou o tempo de sobrevivência para 68 dias, mas não levou à cura. Um resultado semelhante de crescimento retardado do tumor EMT6 foi observado por Jure-Kunkel et al. quando anti-CTLA-4 foi administrado [30]. Para a combinação de terapia fototérmica e anti-CTLA-4, 55% dos camundongos tratados sobreviveram 100 dias após a inoculação do tumor e provavelmente estão curados.
A compreensão do mecanismo de imunidade antitumoral foi avaliada usando citometria de fluxo para quantificar as populações de células efetoras do sistema imunológico no baço. Em comparação com a terapia fototérmica ou com o anti-CTLA-4 sozinho, a terapia de combinação resultou em um aumento de sete vezes no CD4 auxiliar + Células T e um aumento de três vezes no citolítico CD8 + Células T, ambos os resultados sendo altamente significativos do ponto de vista estatístico ( p <0,005). Estes resultados fornecem evidências adicionais de uma resposta abscopal potencial pela combinação de fototerapia e terapia de coestimulação de células T com inibição do ponto de controle imunológico.
Aumentos no CD4 + e CD8 + as contagens de células correlacionadas com aumentos nos tamanhos do baço observados durante a necropsia. O tamanho do baço aumentado indica uma resposta imunológica aumentada. O baço é composto por vários tipos de células, sendo os mais comuns do CD4 + , CD8 + e linhagens de células B [31, 32]. Embora não explorado neste corpo de trabalho, esperaríamos que as contagens de células B aumentassem junto com CD4 + e CD8 + Contagens de células T [33]. Helper CD4 + As células T auxiliam na imunidade humoral, facilitando outras células imunológicas por estimulação de citocinas e interações células-células diretas. CD8 citolítico + As células T matam diretamente as células tumorais. Aumentos no CD4 + e CD8 + as contagens de células são indicativas de uma resposta imune abscopal sistêmica.
A presença de uma resposta imune abscopal sistêmica após o tratamento de combinação é ainda suportada por aumentos nos níveis de citocinas pró-inflamatórias no soro de camundongo (Fig. 3). O TNF-α ativa macrófagos associados a tumores para apresentar efeitos antitumorais [34, 35]. O IFN-γ desempenha um papel importante na vigilância do tumor [36, 37]. A IL-6 promove a proliferação de macrófagos e linfócitos [38]. O aumento significativo destas moléculas efetoras no soro de camundongo 7 dias após o tratamento com PTT combinado com anti-CTLA-4 suporta ainda a existência de uma resposta imune antitumoral.
Na conclusão da irradiação dos camundongos que receberam SWCNT, a temperatura média máxima do tumor foi de 54 ° C; esta temperatura foi suficiente para ablação completa do tumor (Fig. 1). Isso está dentro da faixa de 45–60 ° C na qual ocorre a inativação da enzima e lesão mitocondrial [39]. A temperatura dos tumores no grupo de controle com solução salina permaneceu abaixo de 40 ° C, uma temperatura que fornece benefício terapêutico mínimo [39,40,41].
Observamos que a maior parte do acúmulo de SWCNT-ANXA5 com base na concentração ocorreu principalmente no fígado, coração, baço, rins, pulmões e tumor (Fig. 4a). Em camundongos com tumores EMT6, observamos que a concentração de SWCNT-ANXA5 era semelhante à do fígado e rins (Fig. 4a, b). Traços de SWCNT-ANXA5 foram detectados no cérebro, intestino grosso e intestino delgado. É importante notar que a biodistribuição de SWCNT com base na% da dose injetada (ID) não se correlaciona bem com a concentração absoluta de SWCNT dentro de um tecido alvo. Isso se deve principalmente às diferenças entre os pesos dos órgãos. Por exemplo, uma determinada% ID em um órgão corresponderá a uma concentração mais alta em órgãos menores e a concentrações menores em órgãos maiores. A comparação de amostras com base na concentração de SWCNT revela que a concentração mais alta está no rim, seguida de perto pelo fígado e baço (Fig. 4a).
Há alguma evidência de degradação de SWCNTs em vários órgãos durante o período do estudo de biodistribuição (Fig. 4a, b). A degradação de SWCNTs em órgãos é esperada com base em uma descoberta anterior de que nanotubos de carbono de paredes múltiplas são degradados em macrófagos [42]. Os SWCNTs usados em nosso estudo têm diâmetro médio de 0,8 nm e comprimento médio de 1500 µm. Não se prevê que esse tamanho seja citotóxico com base em um estudo de Zhu et al. [43], que classificou o potencial de dano da bicamada lipídica pela toxicidade dos nanotubos de carbono com base no comprimento e diâmetro. De acordo com esta classificação, os SWCNTs que usamos estão na categoria "biologicamente suaves", minimizando a citotoxicidade, o que é consistente com nossas observações nos estudos em camundongos onde não observamos quaisquer efeitos colaterais ou toxicidade histopatológica como resultado da administração do SWCNT Conjugado -ANXA5.
Conclusões
Aqui, demonstramos uma nova modalidade de tratamento combinatório onde obtemos uma taxa de sobrevivência relativamente alta em camundongos com câncer de mama metastático agressivo usando terapia fototérmica com o bioconjugado SWCNT-ANXA5 combinado com a inibição do ponto de verificação à base de anti-CTLA-4. O uso da proteína de direcionamento vascular tumoral ANXA5 minimizou a quantidade de SWCNT entregue sistemicamente necessária para erradicar tumores primários em uma dose única baixa. Curiosamente, notamos um aumento na sobrevida de camundongos com câncer metastático tratados com terapia combinatória, embora apenas o tumor primário tenha sido irradiado. Um estudo mecanístico que quantificou o número de células efetoras anti-tumorais esplênicas importantes revelou que apenas a combinação de ambas as modalidades de tratamento aumentou o número de CD4 + auxiliar e CD8 + células T citotóxicas. Nossa hipótese é que este aumento nas células T reflete uma resposta abscopal, onde as células efetoras antitumorais suprimiram a metástase tumoral. Embora os SWCNTs ainda estivessem presentes nos órgãos 4 meses após a administração, nenhum efeito colateral ou toxicidade tecidual aparente foram observados durante o curso dos experimentos.
Disponibilidade de dados e materiais
Todos os dados estão totalmente disponíveis sem restrição.
Abreviações
- SWCNT:
-
Nanotubo de carbono de parede simples
- ANXA5:
-
Anexina A5
- anti-CTLA-4:
-
Proteína 4 associada a linfócitos T anticitotóxicos
- EDTA:
-
Ácido etilenodiaminotetracético
- SDS-PAGE:
-
Sodium dodecyl sulfate–polyacrylamide gel electrophoresis
- DSPE:
-
1,2-Distearoyl-sn-glycero-3-phosphoethanolamine
- PTT:
-
Terapia fototérmica
Nanomateriais
- Nanotubos de carbono ultrapassam o limite da eletrônica flexível
- Nanopartículas para terapia do câncer:progresso e desafios atuais
- Nanorods de ouro revestidos com BSA para terapia fototérmica NIR-II
- As propriedades elétricas de compostos híbridos baseados em nanotubos de carbono multifoliados com nanoplacas de grafite
- Composto mecânico de LiNi0.8Co0.15Al0.05O2 / nanotubos de carbono com desempenho eletroquímico aprimorado para baterias de íon-lítio
- Nanopartículas lipídicas de PLGA rastreadas com 131I como transportadores de administração de drogas para o tratamento quimioterápico direcionado do melanoma
- Nanopartículas de albumina carregadas de resveratrol com circulação sanguínea prolongada e biocompatibilidade aprimorada para terapia de tumor pancreático direcionada altamente eficaz
- Ajuste do modo de movimento deslizante de nanotubos de carbono por meio de grupos hidroxila
- Síntese fácil em um vaso de pontos de carbono de polidopamina para terapia fototérmica
- Carbon Dots @ Platinum Porfirina Composto como Nanoagente Teranóstico para Terapia Eficiente Fotodinâmica do Câncer



