Geração de espécies reativas de oxigênio em soluções aquosas contendo nanopartículas de GdVO4:Eu3 + e seus complexos com azul de metileno
Resumo
Nesta carta, relatamos o estudo da geração de radicais livres e espécies reativas de oxigênio (ROS) em soluções de água contendo ortovanadato de gadolínio GdVO 4 :Eu 3+ nanopartículas (VNPs) e seus complexos com fotossensibilizador de azul de metileno (MB). A atividade catalítica foi estudada sob radiação UV-Vis e raios-X por três métodos (teste de dienos conjugados, radical OH · e detecção de oxigênio singlete). Foi demonstrado que os complexos VNPs-MB revelam alta eficiência de geração de ROS sob irradiação UV-Vis associada com alta eficiência de geração de radicais OH · por VNPs e geração de oxigênio singlete por MB devido à transferência de energia de excitação não radiativa de VNPs para moléculas de MB . Ao contrário do que ocorre com a irradiação de raios-X, o forte OH . radicais eliminando por VNPs foram observados.
Histórico
A radioterapia (RT) continua sendo um componente importante do tratamento do câncer com aproximadamente 50% de todos os pacientes com câncer recebendo RT durante o curso da doença [1,2,3]. O mecanismo exato de morte celular devido à radiação ainda é uma área de investigação ativa. As quebras de fita dupla do DNA nuclear são consideradas o efeito celular mais importante da radiação, levando à perda irreversível da integridade reprodutiva da célula e eventual morte celular [4]. Tais danos de radiação podem ser causados por (i) ionização direta e (ii) ionização indireta via radicais livres e espécies reativas de oxigênio (ROS), espécies quimicamente reativas contendo oxigênio, formadas a partir da radiólise de água celular e moléculas de oxigênio [2,3, 4]. Na terapia clínica, o dano é comumente ionizante indireto. No processo, a água perde um elétron e se torna altamente reativa. Então, por meio de uma reação em cadeia de três etapas, a água é sequencialmente convertida em uma série de radicais e produtos moleculares:elétrons hidratados (\ ({e} _ {aq} ^ {-} \ Big) \), átomo de hidrogênio ( H ∙ ), radical hidroxila OH ·, radical hidroperoxila (\ ({HO} _2 ^ {.} \ Big) \), peróxido de hidrogênio (H 2 O 2 ) e moléculas de hidrogênio (H 2 ) [5, 6]. Elétrons hidratados e átomos de hidrogênio são fortes agentes redutores. Em contraste, os radicais hidroxila são espécies oxidativas muito fortes e removem imediatamente os elétrons de qualquer molécula em seu caminho, transformando essa molécula em um radical livre e, assim, propagando uma reação em cadeia [5]. Quando o oxigênio molecular dissolvido é apresentado na água irradiada, sua redução produz o radical superóxido (\ ({O} _2 ^ {.-} \)) e é o precursor da maioria das outras ROS, incluindo o oxigênio singlete ( 1 O 2 ) [7].
Recentemente, foi demonstrado que nanopartículas (NPs) de elevado número atômico (Au, Ag, Hf, Gd, Ti) [8,9,10,11], NPs semicondutores (óxido metálico TiO 2 ZnO, CuO, CeO 2 , Al 2 O 3 ; pontos quânticos ZnS, ZnS, LaF 3 , etc.) [8, 12,13,14], e alguns NPs inorgânicos (nanotubos de carbono) [15, 16] aumentam a eficiência da RT. Os princípios teóricos da interação raios-X-NP são bem descritos [8, 12, 14]. Uma interação em cascata de fótons de alta energia com a rede do NP ocorre através do efeito fotoelétrico e principalmente do efeito de espalhamento Compton. Elétrons Compton, Photo- ou Auger podem induzir a emissão de elétrons secundários, que podem escapar para o ambiente e serão capturados por um aceptor (ou seja, água, biomolécula, oxigênio, óxidos de nitrogênio) localizado próximo à superfície dos NPs e induzir radicais biomoleculares e produção de ROS [8, 12, 14]. Os efeitos de radiossensibilização dos NPs estão associados aos radicais biomoleculares e à geração de ROS como um estágio final da interação dos raios-X com os NPs. Em NPs semicondutores, como NPs de óxido metálico, o efeito citotóxico associado à geração de ROS também pode ser induzido pela irradiação UV [17,18,19,20]. O mecanismo é que quando NPs são irradiados com a luz UV (energia maior que o gap), a separação de carga é induzida gerando um buraco (h + ) na banda de valência e um elétron (e - ) na banda de regência. Elétrons e lacunas apresentam alta capacidade de redução e oxidação, respectivamente [18]. Os elétrons podem reagir com o oxigênio molecular para produzir o radical superóxido (\ ({O} _2 ^ {\ cdotp -} \)) por meio de um processo redutor, enquanto os buracos podem abstrair elétrons da água e / ou íons hidroxila gerando radicais hidroxila (OH ·) Por meio de um processo oxidativo [18,19,20]. Para TiO 2 , CeO 2 , Al 2 O 3 e nanopartículas de ZnO, o 1 O 2 geração através da oxidação de \ ({O} _2 ^ {\ cdotp -} \) foi relatada [18, 21, 22].
Mais uma abordagem para aumentar a eficiência da terapia do câncer (terapia fotodinâmica, PDT) usando NPs cintilantes foi proposta por Chen e Zhang [23]. Esta abordagem combina NPs excitados por raios-X (cintilantes) e moléculas fotossensibilizadoras (PS). NPs cintilantes servem como um transdutor de energia, transferindo a energia coletada da irradiação de raios-X para o PS que gera oxigênio singlete para a destruição do tumor. Esta abordagem permite o tratamento profundo do câncer e melhora tanto a PDT quanto a RT. Até agora, uma variedade de NPs de cintilação e seus complexos com PS foram estudados como agentes fotodinâmicos induzíveis por raios X [12, 14, 23,24,25,26,27,28].
Recentemente, relatamos a criação de complexos na base de NPs de ortovanadato de gadolínio cintilante dopados com íons de európio GdVO 4 :Eu 3+ (VNPs) e fotossensibilizador de azul de metileno (MB) e estudo da transferência eletrônica de energia de excitação nos complexos [29]. Foi demonstrado que devido à conversão de energia de excitação efetiva nos complexos, eles podem ser prospectivos como um agente fotodinâmico indutível por raios-X. O objetivo deste trabalho foi estudar a eficiência da geração de ROS em soluções aquosas contendo VNPs e seus complexos com MB sob irradiação UV e raios-X.
Experimental
Químicos
Cloreto de gadolínio GdCl 3 · 6H 2 O (99,9%), cloreto de európio EuCl 3 · 6H 2 O (99,9%), EDTA dissódico · 2Na (99,8%) e metavanadato de sódio anidro NaVO 3 (96%) foram obtidos da Acros Organic (EUA) e todos usados sem purificação adicional. O hidróxido de sódio NaOH (99%) foi adquirido na Macrohim (Ucrânia). Ortovanadato de sódio Na 3 VO 4 solução foi obtida pela adição de uma solução 1 M de NaOH em solução aquosa NaVO 3 a pH =13. L-a-fosfatidilcolina (PC) de gema de ovo, corante catiônico 3,7-bis (dimetilamino) cloreto de fenazationio (azul de metileno (MB), M w =373,90 g / mol), 1,2-Benzopirona (Coumarin, M w =146,14 g / mol) foram adquiridos da Sigma-Aldrich (EUA) e usados como recebidos. Sal dissódico do ácido antraceno-9,10-dipropiônico (ADPA, M w =366,32 g / mol) foi obtido da coleção de corantes do Dr. Igor Borovoy (Instituto de Materiais de Cintilação, NAS da Ucrânia) com a pureza controlada por cromatografia de camada fina. Todos os outros produtos químicos eram de qualidade analítica.
Síntese de GdVO 4 :Eu 3+ soluções coloidais
Soluções coloidais aquosas de nanopartículas de ortovanadato de gadolínio dopadas com íons de európio Gd 0,9 Eu 0.1 VO 4 (GdVO 4 :Eu 3+ ) foram sintetizados de acordo com o método relatado anteriormente [30]. Primeiro, 0,4 mL de solução aquosa de cloreto de gadolínio (1 M) foram misturados com 0,05 mL de cloreto de európio (1 M) e então 49,55 mL de água bidestilada foram adicionados à mistura. Em seguida, a solução obtida foi misturada com 37,5 mL de solução de EDTA dissódico (0,01 M). Em seguida, 37,5 mL de Na 3 VO 4 (0,01 M) fluiu gota a gota (рН =10,5). A mistura foi intensamente agitada usando um agitador magnético e aquecida em banho-maria sob um condensador de refluxo durante 24 h a 100 ° C. A solução transparente incolor obtida espalha a luz sob a iluminação lateral (o cone de Tyndall). Em seguida, a solução foi resfriada e dialisada contra água por 24 horas para remoção do excesso de íons. Para tanto, a solução obtida foi ronronada em saco de diálise (Cellu Sep T2, membrana com peso molecular de corte de 12 KDa, tamanho de poro ~ 2,5 nm) e colocada em um copo de 2 L com água destilada. Após cada 6 h, a água foi renovada.
Instrumentação e caracterização
VNPs sintetizados foram caracterizados usando microscopia eletrônica de transmissão (microscópio eletrônico TEM-125 K, Selmi, Ucrânia) e método de espalhamento de luz dinâmico (analisador ZetaPALS, Brookhaven Instruments Corp., EUA). Os espectros de absorção foram medidos usando um espectrômetro Specord 200 (Analytik Jena, EUA). Os espectros de fluorescência e excitação de fluorescência foram obtidos com um espectrofluorímetro Lumina (Thermo Scientific, EUA).
Preparação de complexos VNPs – MB
As soluções para as investigações foram preparadas como segue. Primeiro, foram preparadas soluções estoque de MB em água (1 mmol / L). Para obter soluções aquosas de VNPs – MB, a quantidade necessária da solução estoque de corante e solução aquosa de VNPs foram adicionadas em um frasco e cuidadosamente agitadas usando um evaporador rotativo (Rotavapor R-3, Buchi) durante 1 h para uma evaporação completa do clorofórmio. Em seguida, 1 mL de uma solução aquosa de VNPs foi adicionado em um frasco e agitado suavemente durante 1 h para a formação do complexo VNPs-MB. A concentração de MB na solução obtida foi de 10 μmol / L. As concentrações de nanopartículas foram de 0,1, 1 ou 10 mg / mL.
Detecção de oxigênio ativo e espécies de radicais livres
A formação de ROS sob a irradiação UV / raios X de soluções aquosas contendo VNPs, MB ou complexos VNPs-MB foi detectada espectroscopicamente usando vários métodos.
Teste de formação de dienos conjugados
A oxidação de lipídios sob irradiação UV foi medida usando suspensão de lipossomas PC. Vesículas lipídicas unilamelares de PC foram preparadas pelo método de extrusão [31]. Resumidamente, a quantidade apropriada de PC (25 mg / ml) em clorofórmio foi colocada em um frasco e seca até a evaporação completa do clorofórmio usando um evaporador rotativo (Rotavapor R-3, Buchi). O filme fino de corantes lipídicos foi então hidratado com 10,8 ml de água bidestilada. A suspensão lipídica obtida foi finalmente extrudida através de um filtro de policarbonato de tamanho de poro de 100 nm usando uma mini-extrusora (Avanti Polar Lipids, Inc., EUA). A concentração de PC foi de 1,2 mmol / L. Para o teste de formação de dienos conjugados, 1 mL da suspensão de lipossomas PC foi misturado com 1 mL de solução aquosa de VNPs (solução aquosa MB ou solução aquosa VNPs – MB). A concentração final de MB foi 10 μmol / L e VNPs, 1 g / L. A concentração de PC nas soluções foi de 0,6 mmol / L. As soluções aquosas obtidas foram colocadas em cubetas de quartzo (10 × 10 mm) e irradiadas com lâmpada de mercúrio 250 W (passa banda l =310–400 nm, o fluxo de luz era 43 W / cm 2 ) por 30 min. Em seguida, a absorbância das suspensões foi registrada a 234 nm (máximo de dienos conjugados) usando um espectrofotômetro Specord 200 (Analytik Jena, Alemanha). A concentração de dienos conjugados formados em água sem quaisquer aditivos (complexos NPs, MB ou VNPs – MB) foi tomada como controle. Cada ponto experimental foi o valor médio de pelo menos três testes independentes. O processamento estatístico foi realizado no pacote de software Statistika v. 5.0 (StatSoft, EUA).
OH · detecção de radical
Para detectar a formação do radical hidroxila na solução sob irradiação UV, a cumarina foi usada como uma molécula sonda. A cumarina reage com os radicais OH · produzindo 7-hidroxicumarina altamente fluorescente [32, 33]. O procedimento experimental foi o seguinte. A solução aquosa de cumarina (0,1 mmol / L) foi misturada com soluções aquosas MB (10 μmol / L), VNPs (0,1, 1 ou 10 g / L) ou VNPs – MB. As soluções aquosas obtidas foram colocadas em cubetas de quartzo (10 × 10 mm) e irradiadas com laser He-Cd λ exc =325 nm por 1 h. No caso de irradiação de raios-X, a cubeta foi irradiada de cima (da parte aberta) por um raio-X usando o aparelho ISOVOLT 160 Titan E com um cátodo de tungstênio por 30 min. A tensão no tubo era de 30 kV (20 mA). A distância do tubo de raios X às amostras irradiadas foi de 25 cm. Os espectros de fluorescência (excitados em 325 nm) das soluções foram registrados com um espectrofluorímetro Lumina (Thermo Scientific, EUA). A intensidade relativa da fluorescência da 7-hidroxicumarina foi analisada.
Detecção de oxigênio singlete
1 O 2 a produção nas soluções contendo VNPs, MB ou complexos VNPs – MB foi analisada na avaliação dos espectros de fluorescência ADPA [34, 35]. As medidas foram realizadas em cubetas de quartzo (10 × 10 mm). A solução aquosa de ADPA (10 μmol / L) foi misturada com MB (10 μmol / L), NPs (1 g / L) ou soluções aquosas de VNPs – MB em uma cubeta. As soluções foram irradiadas a 457 nm usando Laser de Estado Sólido Azul de Alta Estabilidade MBL-457, 50 mW (Changchun New Industries Optoelectronics Tech. Co., Ltd.). A emissão de fluorescência do ADPA excitado em 378 nm foi coletada em diferentes escalas de tempo (0, 10, 20, 30, 40 e 60 min) usando um espectrofluorímetro Lumina (Thermo Scientific, EUA).
Resultados e discussões
Característica de VNPs sintetizados
Figura 1a e arquivo adicional 1:a Figura S1 mostra as imagens TEM de VNPs sintetizados com um histograma de distribuição lateral e um padrão de XRD, que oferece suporte ao GdVO 4 :Eu 3+ Estrutura cristalina dos NPs. GdVO sintetizado 4 :Eu 3+ NPs são de forma semelhante a um fuso com um tamanho de 8 × 25 nm ± 5 nm e estrutura de fase tetragonal do tipo zircão. A carga negativa da superfície dos NPs (potencial ζ é - 18,75 ± 0,15 mV, pH =7,8) é devido aos grupos carboxilato do estabilizador EDTA dissódico usado durante a síntese. O diâmetro hidrodinâmico excedente de GdVO 4 :Eu 3+ nanopartículas é 44,0 ± 0,3 nm. O espectro de absorção de GdVO 4 :Eu 3+ NPs representa a banda larga intensa na faixa espectral de 250–350 nm que corresponde a uma transferência de carga de ligantes de oxigênio para o átomo de vanádio no grupo \ ({VO} _4 ^ {3-} \) (Fig. 1b) [36 ] Doping GdVO 4 NPs com Eu 3+ íons conferem fluorescência forte para VNPs na faixa espectral vermelha, que é governada pela transição dentro da configuração de elétron f dos íons de európio [37] (não será discutido neste artigo).
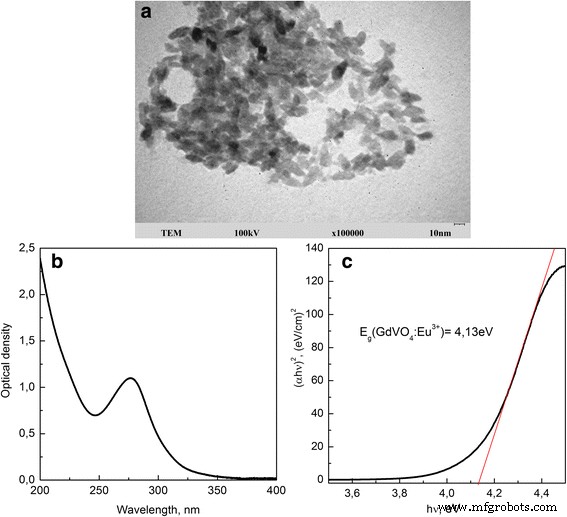
Imagem TEM ( a ), espectro de absorção ( b ), e dependência energética de ( αhv ) 2 ( c ) de GdVO 4 :Eu 3+ nanopartículas
Sabe-se que o tamanho das NPs afeta o gap de energia óptica em materiais semicondutores. A energia do band gap, E g , pode ser estimado a partir do comprimento de onda da borda de absorção da transição entre bandas de acordo com a relação de Tauc [38]:
$$ {\ left (a \ mathrm {hv} \ right)} ^ {\ left (1 / n \ right)} =A \ cdot \ left (\ mathrm {hv} - {E} _g \ right), $ $ (1)
onde a é o coeficiente de absorção, hv é a energia do fóton incidente, A é a constante independente de energia (o parâmetro de cauda da banda), e n é a constante (fator de potência do modo de transição), que depende da natureza do material (cristalino ou amorfo). O valor de n denota a natureza da transição, n =1/2 para transições diretas permitidas, n =3/2 para transições proibidas diretas, n =2 para transições indiretas permitidas e n =3 para transição proibida indireta [39]. GdVO 4 é um semicondutor de gap direto, para o qual n =1/2 [40] Assim, a Eq. (1) pode ser reescrito como:
$$ {\ left (\ alpha \ mathrm {hv} \ right)} ^ 2 =A \ cdot \ left (\ mathrm {hv} - {E} _g \ right) $$ (2)
Coeficiente de absorção ( a ) é calculado a partir da absorbância como a =2,303 D / l , onde D é absorvância e l é o comprimento do caminho óptico.
A Figura 1c representa a dependência energética de ( a hv) 2 para GdVO sintetizado 4 :Eu 3+ nanopartículas. O valor do intervalo de banda E g foi determinado por extrapolação da porção linear do ( a hv) 2 curva versus a energia do fóton hv a zero. O valor obtido E g =4,13 eV é maior do que o relatado para GdVO 4 :Eu 3+ pós com tamanho de cristalito variando de 14,4 a 43 nm (3,56-3,72 eV) [41, 42]. Supomos que pode ser devido à diferença nos métodos de síntese usados que, em nosso caso, dá NPs menores com banda de absorção estreita e desviada para o azul em comparação com aquela obtida pelos métodos hidrotérmicos ou de Pechini.
Geração de radicais livres induzida por foto (teste de dienos conjugados)
É comumente aceito que os tipos de árvore de ROS (\ (\ mathrm {OH} \ cdotp, {\ mathrm {O}} _ 2 ^ {\ cdotp -} \) e 1 O 2 ) a geração em sistemas NPs sob irradiação UV contribui para o principal estresse oxidativo em sistemas biológicos [43, 44]. Embora a atividade fotocatalítica de NPs de óxido de metal como TiO 2 , ZnO, CuO, CeO 2 , Al 2 O 3 , e Fe 2 O 3 está bem descrito [17,18,19,20], poucas pesquisas estudaram a atividade fotocatalítica de ReVO 4 NPs [45,46,47,48]. Foi demonstrado que ReVO 4 NPs são eficazes na destruição fotocatalítica de poluentes orgânicos. No entanto, nenhuma pesquisa estudou os tipos de ROS gerados pelo ReVO 4 NPs sob irradiação UV.
Para imitar o ambiente biológico, usamos a suspensão de lipossomas de PC e detectamos a geração de radicais livres sob irradiação UV nas suspensões contendo MB, VNPs ou complexos VNPs-MB na oxidação de lipídios (teste de formação de dienos conjugados) [49,50,51]. A oxidação de lipídios por oxigênio molecular via reações em cadeia de radicais pode ser iniciada por radiação ionizante quando ROS e radicais livres aparecem no sistema [43, 44]. Reações em cadeia radical envolvendo ácidos graxos poliinsaturados causam um rearranjo das ligações duplas levando a dienos conjugados. Os dienos conjugados resultantes exibem uma banda de absorção a 234 nm que pode ser detectada fotometricamente. A Figura 2 mostra as concentrações relativas de dienos conjugados formados em suspensões de lipídios contendo complexos MB, VNPs ou VNPs – MB. Pode-se observar que em todas as soluções, a concentração de dienos conjugados aumenta em comparação com a suspensão de lipossomas PC pura. No entanto, a eficiência desse processo é diferente. O azul de metileno é uma das moléculas fotossensibilizadoras convencionais com os principais máximos de absorção λ máximo =665 nm e uma banda de absorção menos intensa na faixa espectral de UV (Arquivo adicional 1:Figura S2). Sob irradiação UV de MB, os dois principais processos fotoquímicos podem ocorrer [34, 52]. MB excitado por luz ultravioleta passa por processo de cruzamento intersistema ( Q p =0,54 [53]) para o estado de trigêmeo de longa duração ( 3 MB * ) e reage com as moléculas de oxigênio ( 3 O 2 ) formando oxigênio singlete ( 1 O 2 ):
$$ {\ mathrm {MB}} ^ {+} + hv \ to {} ^ 3 {\ mathrm {MB}} ^ {+ ^ {\ ast}} $$ (3) $$ {} ^ 3 {\ mathrm {MB}} ^ {+ ^ {\ ast}} + {} ^ 3 {\ mathrm {O}} _ 2 \ para {\ mathrm {MB}} ^ {+} + {} ^ 1 {\ mathrm {O }} _ 2 $$ (4)
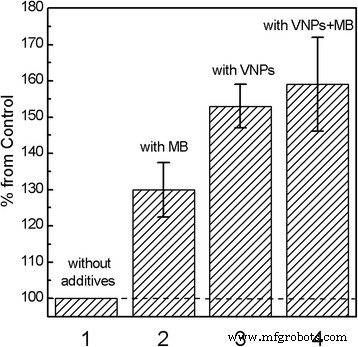
Eficiência relativa de formação de dienos conjugados em suspensões lipídicas:1 - sem aditivos; 2 - com MB; 3 - com VNPs; 4 - com complexos VNPs-MB
O segundo processo fotoquímico pode ocorrer em altas concentrações de MB. As moléculas MB do estado fundamental podem funcionar como agentes redutores doando um elétron ao tripleto MB e formando o radical semi-reduzido (MB ·) e o radical semi-reduzido, respectivamente (MB · 2+ ) [52]:
$$ {} ^ 3 {\ mathrm {MB}} ^ {+ ^ {\ ast}} + {\ mathrm {MB}} ^ {+} \ para \ mathrm {MB} \ cdotp + {\ mathrm {MB} } ^ {\ cdotp 2+} $$ (5)
A oxidação do MB · pelo oxigênio molecular, retornando o corante do estado fundamental e levando à produção do radical superóxido (\ ({O} _2 ^ {\ cdotp -} \)):
$$ \ mathrm {MB} \ cdotp + ^ 3 {\ mathrm {O}} _ 2 \ kern0.5em \ to {\ mathrm {MB}} ^ {+} + {O} _2 ^ {\ cdotp -} $$ (6)
Os radicais singlete de oxigênio e superóxido, bem como os radicais MB formados nas Reações (4) - (6), podem afetar o processo de oxidação lipídica. Em solução diluída onde nenhuma formação de dímero MB é observada ([MB] <20 μM), as Reações (3) e (4) irão dominar [52]. No entanto, em complexos VNPs – MB devido ao aumento da concentração de MB na superfície de VNPs [29], o segundo processo fotoquímico pode ocorrer. Assim, o aumento da formação de dieno conjugado na suspensão de lipídios contendo MB pode ser explicado pela ação do MB como 1 O 2 fotogerador sob irradiação UV. Deve-se notar que a eficiência desse processo é muito menor do que sob excitação MB no máximo de absorção de comprimento de onda longo.
Na suspensão contendo GdVO 4 :Eu 3+ nanopartículas, a oxidação de lipídios é mais eficaz. Este efeito pode ser atribuído ao comportamento fotocatalítico de VNPs sob irradiação UV. Elétrons de banda condutora (e - ) e orifícios de banda de valência (h + ) formado sob irradiação UV ( E > E g ) pode interagir com o oxigênio molecular e as moléculas de água adsorvidas na superfície das NPs seguindo as reações [18, 20, 47]:
$$ {} ^ 3 {\ mathrm {O}} _ 2+ {e} ^ {-} \ to \ kern0.5em {\ mathrm {O}} _ 2 ^ {.-} $$ (7) $$ {\ mathrm {H}} _ 2 \ mathrm {O} + {\ mathrm {h}} ^ {+} \ to \ mathrm {OH} \ cdot $$ (8)
Os íons hidroxila formados durante a fotólise da água e adsorvidos na superfície dos NPs também podem interagir com orifícios para produzir radicais hidroxila:
$$ {\ mathrm {OH}} ^ {-} + {\ mathrm {h}} ^ {+} \ to \ mathrm {OH} \ cdot $$ (9)
Além disso, a oxidação de \ ({O} _2 ^ {\ cdotp -} \) produz oxigênio singlete [18, 21, 22]:
$$ {\ mathrm {O}} _ 2 ^ {\ cdotp -} + {\ mathrm {h}} ^ {+} {\ to} ^ 1 {\ mathrm {O}} _ 2 $$ (10)
Sua reação com íons de hidrogênio leva à formação de peróxido de hidrogênio:
$$ 2 {\ mathrm {O}} _ 2 ^ {\ cdotp -} + 2 {\ mathrm {H}} ^ {+} \ to {\ mathrm {H}} _ 2 {\ mathrm {O}} _ 2 $$ (11)
como resultado de sua interação com elétrons, radicais hidroxila e íons hidroxila podem ser formados:
$$ {\ mathrm {H}} _ 2 {\ mathrm {O}} _ 2 + {\ mathrm {e}} ^ {-} \ to \ mathrm {OH} \ cdot + {\ mathrm {O} \ mathrm {H} } ^ {-} $$ (12)
Assim, o aumento na eficiência da concentração de dienos conjugados em uma suspensão contendo VNPs (Fig. 2, coluna 3) pode ser atribuído aos produtos gerados por meio das Reações (7) - (12) e facilitando a oxidação de lipídios.
Na suspensão lipídica contendo complexos VNPs – MB, as concentrações mais altas de dienos conjugados podem ser explicadas pelos produtos gerados por meio das Reações (3) - (6) e da Reação (7) - (12) (Fig. 2, coluna 4). Além disso, em complexos VNPs-MB nas Reações (3) e (4), a geração de oxigênio singlete poderia ocorrer tanto devido à excitação MB direta quanto via transferência de energia de excitação não radiativa de VNPs para MB que é bastante eficaz nesta composição [29].
Detecção de radical hidroxila
A próxima etapa foi examinar mais exatamente a eficiência de OH · e 1 O 2 geração nas soluções sob irradiação UV / raios-X. A cumarina foi usada como uma molécula sonda para validar o aparecimento de radicais hidroxila nas soluções em consideração. Sabe-se que os radicais OH · são um dos principais produtos da fotólise / radiólise da água sob radiação UV / raios X [5, 6]. Em solução aquosa, os radicais OH · interagem com as moléculas de cumarina para formar o produto 7-hidroxicumarina altamente fluorescente (ver esquema na Fig. 3) que pode ser detectado espectroscopicamente pelo aparecimento de uma nova banda ( λ máximo ~ 460 nm) deslocada em direção à região espectral de comprimento de onda longo em relação à banda de fluorescência de cumarina ( λ máximo ~ 400 nm), Fig. 3 [32, 33]. Quanto maior a concentração de radicais OH · na solução, mais eficaz é a oxidação da cumarina e, conseqüentemente, mais intensa é a banda de comprimento de onda longo. Assim, a análise da intensidade relativa da banda de comprimento de onda longo poderia fornecer informações sobre a concentração de radicais OH · na solução sob efeito de vários fatores.
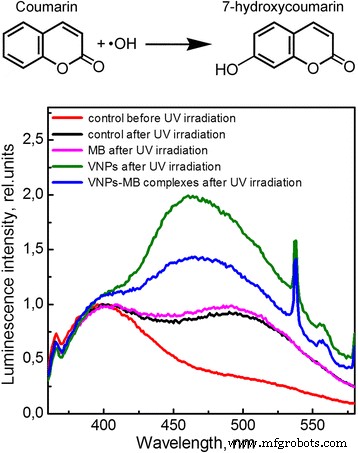
Reação da cumarina com o radical hidroxila para formar 7-hidroxicumarina fluorescente. Espectros de fluorescência normalizados de solução de água cumarina, λ exc =325 nm
Os espectros de emissão de fluorescência da solução de água de cumarina contendo complexos MB, VNPs ou VNPs – MB medidos após 1 h de iluminação UV são apresentados na Fig. 3. É mostrado que a irradiação de UV da solução de água de cumarina sem quaisquer aditivos (controle) provoca uma formação de uma nova banda de fluorescência de comprimento de onda longo que indica a geração de radicais OH · e a oxidação da cumarina (Fig. 3). Na presença de moléculas MB na solução, a intensidade relativa desta banda não muda, o que indica nenhum efeito adicional de MB na geração de radicais OH (Fig. 3). Na solução contendo VNPs, a intensidade da banda da 7-hidroxicumarina aumenta notavelmente (Fig. 3) devido à atividade fotocatalítica dos VNPs sob irradiação UV, Reações (8), (9) e (12). Notemos que os picos agudos em torno de 535-540 nm pertencem à fluorescência do íon európio em GdVO 4 :Eu 3+ nanopartículas (transições de intraconfiguração). Na solução contendo complexos VNPs-MB, a intensidade relativa da banda de 7-hidroxicumarina foi cerca de duas vezes menor em comparação com a da solução contendo VNPs que aponta para a produção de radicais OH · menos eficaz (Fig. 3). Isso pode ser explicado pelo fato de que a adsorção do corante MB na superfície dos VNPs pode impedir a adsorção de moléculas de água e íons hidroxila e, conseqüentemente, reduzir a atividade fotocatalítica dos VNPs na geração de radicais OH · via Reações (8) e (9). Além disso, em complexos VNPs-MB, uma parte da energia adsorvida é transferida de forma não radiativa para moléculas MB [29], o que também diminui a eficiência da produção de pares elétron-buraco e, conseqüentemente, a capacidade dos VNPs de geração de radicais OH · em tais complexos.
Resultados inesperados foram observados sob irradiação de raios-X das soluções contendo VNPs (Fig. 4). Ao contrário do caso da irradiação UV, observamos que a intensidade relativa da banda de 7-hidroxicumarina diminui em comparação com a solução aquosa de cumarina sem nanopartículas, o que indica a eliminação dos radicais OH · formados nas soluções como resultado da radiólise da água. O efeito observado é fortemente dependente das concentrações de VNP (Fig. 4). Deve-se notar que a discussão principal a respeito da capacidade das nanopartículas de servir como um eliminador de ROS está focada principalmente em CeO 2 nanocristais (nanoceria) [54,55,56,57]. As principais características que força os nanocérios a agirem como eliminadores de ROS são geralmente atribuídas ao alto conteúdo de vacâncias de oxigênio e Ce 3+ íons em nanoceria e sua comutação entre os estados de oxidação 3+ e 4+. No entanto, a dependência crítica da atividade biológica dos nanocerios em seu tamanho e mecanismo de autorregeneração ainda está em discussão [54,55,56,57]. Observamos também que os efeitos protetores do GdVO 4 :Eu 3+ e CeO 2 NPs contra danos induzidos por raios-X foram observados em nosso grupo em experimentos in vivo anteriores [57]. Até onde sabemos, a capacidade do GdVO 4 :Eu 3+ nanopartículas para varrer os radicais OH · gerados na solução de água sob irradiação de raios-X foram observadas pela primeira vez e requerem pesquisas mais aprofundadas.
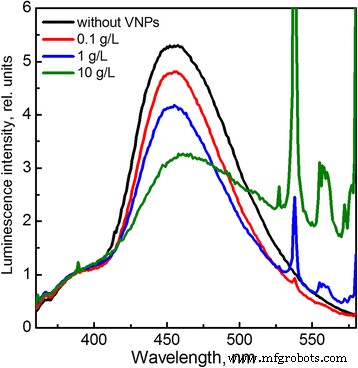
Espectros de fluorescência normalizados de solução de água de cumarina contendo diferentes concentrações de VNP registrados após 30 min de irradiação de raios-X
Geração de oxigênio singlet
Para avaliar a eficiência dos complexos VNPs – MB de 1 O 2 geração na água, usamos a oxidação ADPA baseada no método por oxigênio singlete com uma formação de endoperóxido não fluorescente ADPAO 2 (Fig. 5). Assim, na presença de oxigênio singlete, a fluorescência ADPA é extinta irreversivelmente. Devemos observar que, sob irradiação UV, as moléculas de ADPA passam por forte fotodegradação que complica a identificação dos impactos dos complexos MB, VNPs ou VNPs – MB associados ao 1 O 2 geração. Para superar essa desvantagem, aplicamos irradiação de laser a 457 nm, que corresponde a um dos picos de excitação de Eu 3+ íons dopados em GdVO 4 nanocristais (arquivo adicional 1:Figura S3). A Figura 5 mostra que as moléculas de ADPA não sofrem reações fotoquímicas na irradiação de luz de 457 nm. Na solução contendo MB, pode ser observada uma ligeira diminuição da intensidade do ADPA com o tempo (Fig. 5) que está associada à ligeira excitação do MB neste comprimento de onda e ação como fotossensibilizador de acordo com a Reação (3) e (4). O mesmo efeito é observado para a solução contendo VNPs (Fig. 5) e pode ser atribuído à formação de radicais \ ({O} _2 ^ {\ cdotp -} \) na superfície de VNPs (Reação (7)) seguido por sua oxidação de acordo com a Reação (10) com geração de oxigênio singlete. A extinção de fluorescência ADPA mais forte é observada em complexos VNPs-MB. A eficiência desse processo é duas vezes maior do que na solução com MB ou VNPs. A maior eficiência de geração de oxigênio singlete na solução contendo complexos VNPs – MB está associada à transferência de energia dos VNPs para o MB nos complexos, nos quais os VNPs atuam como transdutores de energia para o fotossensibilizador MB.
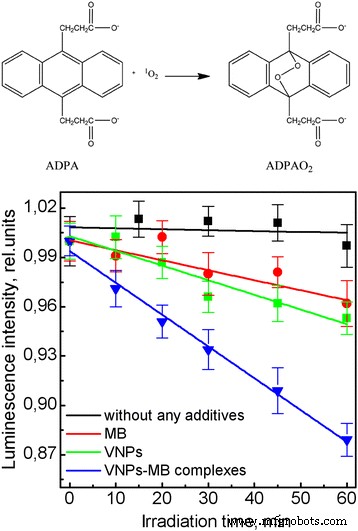
Reaction of ADPA with singlet oxygen to form endoperoxide ADPAO2 . ADPA photobleaching after irradiation with λ = 457 nm in water solutions
Unfortunately, due to ADPA sensor instability, we were not successful to measure the efficiency of the 1 O 2 generation in water solution under X-ray excitation.
Conclusões
The efficiency of ROS generation in water solutions containing GdVO4 :Eu 3+ nanoparticles and their complexes with MB have been analyzed under UV-Vis and X-ray irradiation by three methods (conjugated dienes test, OH· radical, and singlet oxygen detection). Complexes VNPs–MB reveal high efficiency of ROS generation under UV-Vis irradiation associated with both high efficiency of OH· radicals generation by VNPs and 1 O 2 generation by MB due to nonradiative excitation energy transfer from VNPs to MB molecules. For the first time, the strong OH· radicals scavenging by VNPs has been observed under X-ray irradiation. Our observation indicates that VNPs–MB complexes can be potentially used to activate photodynamic therapy.
Abreviações
- MB:
-
Azul de metileno
- PS:
-
Photosensitizer
- ROS:
-
Reactive oxygen species
- VNPs:
-
Gadolinium orthovanadate GdVO4 :Eu 3+ nanopartículas
Nanomateriais
- Problemas legais em computação em nuvem e suas soluções
- Manutenção reativa explicada:desafios e soluções comuns
- Nanopartículas multifuncionais de ouro para aplicações diagnósticas e terapêuticas aprimoradas:uma revisão
- Preparação de nanopartículas de mPEG-ICA carregadas com ICA e sua aplicação no tratamento de dano celular H9c2 induzido por LPS
- Ajustando a toxicidade de espécies reativas de oxigênio na terapia avançada de tumor
- Estados eletrônicos do nanocristal dopado com oxigênio e emissão visível em silício negro preparado por ns-Laser
- Síntese fácil de compósito CuSCN colorido e condutor revestido com nanopartículas de CuS
- A preparação da nanoestrutura de casca de gema de Au @ TiO2 e suas aplicações para degradação e detecção de azul de metileno
- Promoção do crescimento celular SH-SY5Y por nanopartículas de ouro modificadas com 6-mercaptopurina e um peptídeo penetrador de neurônio
- Síntese fácil e ecológica de nanofios de Co3O4 e sua aplicação promissora com grafeno em baterias de íon-lítio



