Síntese fácil e ecológica de nanofios de Co3O4 e sua aplicação promissora com grafeno em baterias de íon-lítio
Resumo
Neste trabalho, desenvolvemos uma estratégia ecologicamente correta para preparar Co 3 O 4 nanofios. O processo consistiu em duas etapas:síntese controlável de nanofios de cobalto metálico seguida de uma etapa de oxidação fácil pelo ar. A estrutura de nanofio 1D com uma alta proporção de aspecto foi facilmente alcançada por meio de uma automontagem assistida por campo magnético de complexos de íon cobalto durante a redução. Após as calcinações com ar, o Co 3 O 4 nanofios foram preparados em larga escala e prontos para serem usados como o material do ânodo para baterias de íon-lítio. O Co 3 O 4 nanofios, que possuíam um comprimento variando de 3 a 8 μm com a razão de aspecto superior a 15, exibiam uma capacidade de armazenamento de lítio reversível de até ~ 790 mAh / g ao usar uma pequena quantidade de flocos de grafeno sem defeitos como aditivos condutores. Os desempenhos eletroquímicos superiores foram atribuídos ao efeito sinérgico “flat-on” entre os nanofios 1D e o grafeno 2D. Portanto, o Co 3 O 4 nanofio / compósito de grafeno tem aplicação promissora para baterias de íon-lítio.
Histórico
Com as demandas de rápido crescimento por estratégia de energia limpa e sustentável, os dispositivos de armazenamento de energia elétrica têm uma necessidade urgente para muitas aplicações, como veículos elétricos e dispositivos eletrônicos portáteis. As baterias de íon de lítio (LIBs) podem fornecer uma densidade de energia relativamente alta e fornecer várias vantagens, como longa vida útil, baixo custo e boa reversibilidade. Óxidos de metais de transição têm sido considerados ânodos promissores para LIBs devido à sua abundância, baixo custo e alta capacidade teórica [1, 2], entre os quais o óxido de cobalto (Co 3 O 4 ) tem atraído muita atenção devido à sua alta capacidade teórica (890 mAh / g) [2,3,4]. No entanto, a condutividade intrinsecamente baixa, grande volume e mudança durante o ciclo, bem como o baixo coeficiente de utilização de Co 3 O 4 , levam a baixo desempenho eletroquímico, dificultando sua aplicação prática [5, 6].
Nos últimos anos, o desenvolvimento da nanociência e da nanotecnologia estão trazendo oportunidades revolucionárias para melhorar ainda mais o desempenho do LIB, especialmente as nanoestruturas 1D (por exemplo, nanofios, nanobelts, nanofibras). Eles têm atraído muita atenção devido às suas extraordinárias propriedades eletroquímicas, incluindo área de superfície elevada, caminho de transporte iônico / eletro curto e boa capacidade para acomodar a expansão de volume durante carga / descarga [5, 7,8,9,10].
Embora esses nanomateriais 1D, como Co 3 O 4 nanofios (Co 3 O 4 NWs), são atrativos como materiais de eletrodo, a síntese de tais nanoestruturas tem despertado amplo interesse, mas ainda permanece bastante desafiadora. Muitos métodos para preparação de nanofios, incluindo métodos hidrotérmicos e solvotérmicos [11,12,13], eletrodeposição baseada em modelo [14] e redução química úmida [15], estão bem desenvolvidos durante as últimas décadas. Essas abordagens, no entanto, muitas vezes envolvem condições de síntese severas, como alta pressão / temperatura, modelo caro ou ácido forte (como HF, amplamente utilizado para dissolver o modelo), dificultando assim a aplicação prática de tais nanomateriais. Por exemplo, Dong et al. preparado Co 3 O 4 NWs aquecendo uma folha de cobalto puro na atmosfera, mas o tempo de reação, a temperatura e a umidade precisavam ser controlados com cuidado. O processo de preparação era complicado e demorado [16]. Ji et al. usou o método de síntese baseado em modelo para obter Co 3 O 4 NWs nos poros estreitos do molde AAO, enquanto o ácido forte e o molde eram indispensáveis [14]. Dos resultados de Xu et al., Co 3 O 4 NWs foram sintetizados através de um método hidrotérmico modificado com alta pressão [11]. Como encontrado em muitas literaturas, as abordagens existentes sofreram de muitas desvantagens, como operação complicada, dificuldade de purificação, alto custo e poluição ambiental severa. É de grande importância desenvolver um novo método para sintetizar estruturas de nanofios, com escalabilidade, viabilidade e compatibilidade ambiental aprimoradas para superar as múltiplas dificuldades que têm impedido a aplicação em larga escala de tais nanoestruturas por muito tempo.
Aqui, relatamos um método novo, fácil e ecológico para preparar Co 3 O 4 NWs. Um método de duas etapas foi adotado no presente estudo:síntese assistida por campo magnético de nanofios de Co (CoNWs) e oxidação de CoNWs. Com eficiência e simplicidade superiores, o método atual ampliaria a aplicação eletroquímica de Co 3 O 4 materiais, em comparação com abordagens de síntese anteriores. Até onde sabemos, não há nenhum relatório relevante sobre esta nova estratégia de síntese. Neste relatório, o Co 3 O 4 Os NWs exibem uma estrutura relativamente firme com a razão comprimento-diâmetro de ~ 15, benéfica para a construção de vias de transmissão de elétron / íon. Com o auxílio de uma pequena quantidade de grafeno (3% em peso) atuando como suporte condutor, como Co 3 O 4 Os materiais NWs / grafeno têm capacidades reversíveis de ~ 790 mAh / ge boas capacidades de taxa quando comparados ao Co 3 comum O 4 nanopartículas (Co 3 O 4 NPs), tornando-o um bom candidato para aplicação em bateria de íon-lítio.
Experimental
Materiais
Hexa-hidrato de cloreto de cobalto (II) (CoCl 2 · 6H 2 O, 99% em peso), sal dissódico de ácido etilenodiamina tetraacético (EDTA-2Na, 99% em peso), hidróxido de sódio (NaOH, 98% em peso), cloreto de sódio (NaCl, 99,5% em peso), cloreto de potássio (KCl, 99,5% em peso ), polivinilpirrolidona K30 (PVP (–CH (NCH 2 CH 2 CH 2 CO) CH 2 -) n , M w =29.000-35.000), e monohidrato de hidrazina (N 2 H 4 · H 2 O, 80 vol%) foram adquiridos de Chengdu KeLong Reagent Co., Ltd. (China), e hexa-hidrato de ácido cloroplatínico (H 2 PtCl 6 · 6H 2 O, 38% em peso) foi adquirido do Shenyang Research Institute of Non-Ferrous Metals (China). Todos os produtos químicos eram de grau analítico sem purificação adicional. Todas as soluções aquosas foram preparadas com água desionizada (água D.I.). O Co 3 disponível comercialmente O 4 NPs obtidos de Shanghai Aladdin Bio-chem Technology Co., Ltd. foram usados como grupo de controle.
Síntese de CoNWs
Em uma síntese típica, 0,6 mmol CoCl 2 · 6H 2 O e 0,6 mmol de EDTA-2Na foram colocados em um copo de PTFE com capacidade de 100 mL, dissolvido em 60 mL D.I. agua. O valor de pH da solução foi ajustado para 14 por titulação de NaOH diluído e 0,15 g de PVP como surfactante foi dissolvido na solução sob agitação vigorosa. Depois de bem disperso, o béquer foi colocado entre dois imãs (no banho-maria), com campo aplicado de 35 mT medido por um medidor de tesla HT20, e o banho-maria foi regulado para 80 ° C. Quando a temperatura da solução de reação atingiu 80 ° C, 0,30 mL N 2 H 4 · H 2 O atuou como redutor foi adicionado à solução acima para redução de Co 2+ e 0,12 mL de 0,0253 mol / L H 2 PtCl 6 · 6H 2 O (funcionou como iniciador) foram misturados na solução. Os CoNWs formaram-se gradualmente em 10 min. Após a reação, o composto foi retirado da solução com um ímã e lavado ultrassonicamente várias vezes usando etanol e água destilada para remover as impurezas. Por fim, as amostras foram secas em estufa de congelação a vácuo por 12 h.
Síntese de Co 3 O 4 NWs
0,01 g da amostra preparada foi colocado em um barco de porcelana misturado com 0,3 g de KCl e 0,2 g de NaCl uniformemente. Em seguida, a mistura foi mantida em uma mufla e aquecida a 650 ° C por 4 h. Após o resfriamento natural da mufla, o produto foi retirado e lavado por D.I. água três vezes e seca na estufa de secagem a 80 ° C por 4 h. O processo de formação do Co 3 O 4 NWs foi mostrado na Fig. 1.
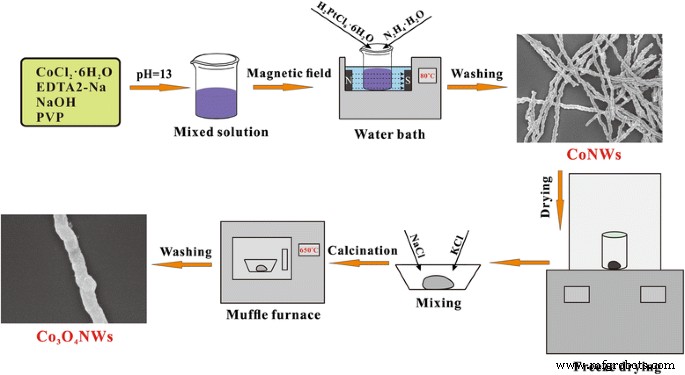
Ilustração esquemática para a preparação Co 3 O 4 NWs
Caracterização
Caracterização de materiais
A fase de composição dos produtos obtidos foi verificada e comparada por análise de difração de raios-X (XRD, Philips X’Pert Pro MPD) usando CuKα como fonte de radiação (λ =0,154249 nm) em voltagem de 40 kV. Os ângulos de difração (2 θ ) foram definidos entre 20 ° e 90 °, com um tamanho de etapa de 4 ° min −1 . A identificação da fase foi obtida comparando o padrão de difração da amostra com os cartões padrão no banco de dados ICDD-JCPDS.
A morfologia das microestruturas das amostras foi caracterizada por um microscópio eletrônico de varredura por emissão de campo (SEM, JSM-6701F, JEOL, Japão) a uma tensão de aceleração de 150 kV. Todas as amostras foram revestidas com ouro antes da observação SEM.
As imagens de microscopia eletrônica de transmissão (TEM) e de alta resolução (HRTEM) foram obtidas em um Tecnai-G20 TEM (FEI, EUA) para caracterização microestrutural com uma tensão de aceleração de 200 kV. A difração de elétrons de área selecionada (SAED) também foi registrada usando o mesmo equipamento.
Medições eletroquímicas
Os desempenhos eletroquímicos de Co 3 O 4 NWs e Co 3 O 4 NPs foram medidos com base em células de meia moeda CR2025. As nanofolhas de grafeno livres de defeitos (df-GNS) foram produzidas por meio de uma esfoliação de fase líquida modificada [17] e, em seguida, usadas como componente condutor no eletrodo. O grafeno livre de defeitos com espessura de até ~ 0,5 nm e tamanho lateral de ~ 1 μm foi preparado e disperso em N -metil-pirrolidona (NMP). O eletrodo de trabalho livre de aglutinante foi fabricado revestindo a pasta de mistura, que era composta de materiais ativos (Co 3 O 4 NWs / Co 3 O 4 NPs) e nanofolhas de grafeno (GNS) em uma proporção de peso de 100:3, em um coletor de corrente de folha de cobre. A carga de material ativo foi de 0,5 ~ 1 mg por célula.
A solução de eletrólito era 1 mol / L LiPF 6 dissolvido em uma mistura de carbonato de etileno (EC), carbonato de propileno (PC) e carbonato de dietila (DEC) com a razão de volume de EC / PC / DEC =1:1:1. A membrana Celgard 2325 foi usada como separador. As células tipo moeda foram montadas em uma caixa de luvas cheia de argônio, onde o conteúdo de oxigênio e umidade era inferior a 0,1 ppm.
Os ciclos de carga-descarga galvanostática foram testados usando um sistema de teste de bateria (LAND 2001A) dentro de uma janela de tensão de 0,01 ~ 3 V. Voltamogramas cíclicos (CV) de Co 3 O 4 O eletrodo NWs / df-GNS foi realizado em uma estação de trabalho eletroquímica comercial dentro de uma faixa de voltagem de 0,01 ~ 3,0 V a uma taxa de varredura de 0,5 mV / s. A espectroscopia de impedância eletroquímica (EIS) foi realizada em uma tensão de circuito aberto em uma faixa de frequência entre 0,1 Hz ~ 100 kHz com uma amplitude de tensão de 5,0 mV.
Resultados e discussão
As fases dos CoNWs, Co 3 O 4 NWs e Co 3 O 4 NPs foram investigados pela primeira vez por XRD. Os picos de difração de Bragg deles são mostrados na Fig. 2a-c), respectivamente. Pode-se ver que os picos de difração CoNWs foram bem indexados com as reflexões de Co cúbico centrado na face (fcc) (JCPDS No. 15-0806). Dois picos característicos típicos de fcc Co a valor 2-teta de 44 ° e 76 ° correspondentes aos índices de Miller (111) e (220) foram observados, respectivamente. O Co 3 O 4 NW e Co 3 O 4 Os picos de difração NP foram bem indexados com as reflexões de Co cúbico de face centrada (fcc) 3 O 4 (JCPDS No. 15-0806). Os picos de difração registrados de Co 3 O 4 NPs e Co 3 O 4 NWs em 2-teta =19 °, 31 °, 37 °, 39 °, 45 °, 56 °, 59 ° e 65 ° foram bem atribuídos a (111), (220), (311), (222), (400), (422), (511) e (440) planos de hcp Co 3 O 4 , respectivamente, com o parâmetro de célula de a =8,084 Å, b =8.084 Å, e c =8,084 Å. Enquanto isso, os picos de difração agudos e altos sugeriram que o Co 3 preparado O 4 NWs teve um alto grau cristalino. Em seguida, os tamanhos médios de grãos cristalinos foram estimados a partir dos padrões de XRD de acordo com a fórmula de Scherrer D = λk / ( β cos θ ) (onde D é o tamanho médio do cristalito, λ é o comprimento de onda de raios-X 0,1542 nm, k é o fator de forma da partícula, β denota a largura da linha angular de meia intensidade máxima, e θ representa o ângulo de Bragg) com os valores de 18,67 e 25,35 nm para CoNWs e Co 3 O 4 NWs, respectivamente. Ficou evidente que esses valores eram menores do que os tamanhos de uma única partícula de nanofios de Co conforme observado por SEM, o que implicava que cada partícula de nanofios consistia de vários grãos de cristal. Nenhum pico característico devido às impurezas foi detectado, indicando que a alta pureza do Co 3 O 4 NWs. Também foi surpreendente ter tantos CoNWs-to-Co 3 O 4 O rendimento da conversão NWs via simples oxidação do ar, o que poderia ser atribuído à reatividade superior de CoNWs ao oxigênio por causa de sua alta área de superfície específica.
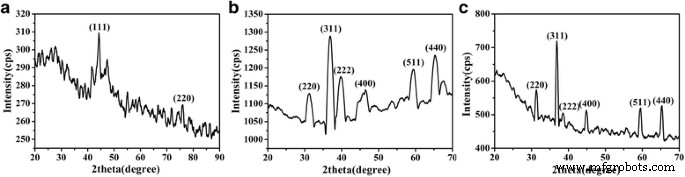
Padrão de XRD de CoNWs ( a ), Co 3 O 4 NWs ( b ), e Co 3 O 4 NPs ( c )
As morfologias das amostras obtidas foram caracterizadas por microscopia eletrônica de varredura (MEV). A imagem SEM mostrou o Co 3 O 4 As amostras de NPs possuíam diâmetros homogêneos de 80 nm e a maioria das amostras eram de morfologia esférica intacta (ver na Fig. 3a). CoNWs uniformes com ~ 150 nm de diâmetro e 20 μm de comprimento foram observados como mostrado na Fig. 3b. Uma clara morfologia de superfície semelhante a um colar composta de minúsculas partículas interconectadas pôde ser vista, verificando o mecanismo de reação que propusemos acima. Além disso, os CoNWs tinham uma integridade estrutural robusta que manteve a forma de um fio mesmo após a ultrassonicação por seis vezes (1 minuto de cada vez). Depois de enxaguar os CoNWs com água e etanol várias vezes, os CoNWs foram prontamente transformados em Co 3 O 4 NWs por simples oxidação do ar. As imagens de Co 3 O 4 NWs (Fig. 3c, d) exibiram os nanofios relativamente lisos e permaneceram cerca de 180 nm de diâmetro, o que indicou que os nanofios ainda mantinham a estrutura semelhante a um fio após as calcinações. Portanto, a oxidação do ar foi uma abordagem fácil e válida para obter Co 3 O 4 NWs.

Imagens SEM de Co 3 O 4 NPs ( a ), CoNWs ( b ), e o Co 3 O 4 NWs ( c , d ) com diferentes ampliações
A microestrutura de Co 3 O 4 NPs, CoNWs e Co 3 O 4 As amostras NWs foram ainda investigadas por microscopia eletrônica de transmissão (TEM), difração de área selecionada (SAED) e microscopia eletrônica de transmissão de alta resolução (HRTEM), como mostrado na Fig. 4a-f. Imagens típicas de TEM foram exibidas na Fig. 4a-c, e a morfologia e estrutura das amostras foram quase consistentes com o que foi observado nas imagens de SEM. Além disso, como as inserções na Fig. 4a-c mostram, os padrões de anéis concêntricos de Co 3 O 4 NPs e Co 3 O 4 NWs (Fig. 4a, c) observados podem ser atribuídos aos planos (200), (311), (440) e (511) de Co 3 O 4 , e os padrões de anéis concêntricos de CoNWs (Fig. 4b) observados podem ser atribuídos aos planos (111) e (220) de Co. O SEAD era exatamente idêntico à rede cúbica de Co e Co 3 O 4 , respectivamente, o que foi consistente com os resultados de XRD. A orientação da rede dos CoNWs nas imagens HRTEM da Fig. 4e, como o precursor de Co 3 O 4 NWs, tiveram uma distância interplanar de 0,12 e 0,21 nm, correspondendo aos planos (111) e (211) da estrutura de Co. O espaçamento da rede (Fig. 4d, f) ao longo das direções (220), (311), (440) e (511) foram estimados em 0,28, 0,25, 0,15 e 0,14 nm, que estavam próximos dos dados padrão de 0,29, 0,24, 0,15 e 0,14 nm.

As imagens TEM de Co 3 O 4 NPs ( a ), CoNWs ( b ), e Co 3 O 4 NWs ( c ) As inserções ( a , b , e c ) mostraram os padrões de difração de elétrons de área selecionada (SAED) das amostras correspondentes. Imagens TEM de alta resolução de Co 3 O 4 NPs, CoNWs e Co 3 O 4 NWs em ( d , e , e f )
Os CoNWs foram preparados por meio de uma rota de reação baseada em solução. Na Fig. 5, propomos o possível mecanismo de formação. No início, EDTA-2Na coordenado com Co 2+ íons para gerar complexos na solução. Então, as moléculas de PVP se auto-montaram em micelas esféricas na água [18, 19], e os núcleos de Co foram envolvidos e possivelmente absorvidos na superfície de micelas esféricas a fim de reduzir a energia livre de Gibbs da superfície. Posteriormente, com a introdução de N 2 H 4 · H 2 O na solução, uma porção de N 2 H 4 substituiu incessantemente o EDTA 2− ânions e coordenado com Co 2+ cátions para formar [Co (N 2 H 4 ) 3 ] 2+ complexos, e o resto deles serviu como agente redutor entrou no minirreator e converteu [Co (N 2 H 4 ) 3 ] 2+ a pequenas nanopartículas de Co. O Co, bem como seus compostos, foi preferido para formar microesferas de acordo com a literatura anterior [20, 21]. Devido à natureza magnética intrínseca do Co metálico, os momentos magnéticos dipolares dos átomos de Co estão alinhados em relação à direção do campo magnético externo. Como resultado, as nanopartículas de Co se alinharão ao longo das linhas de indução magnética para formar CoNWs.
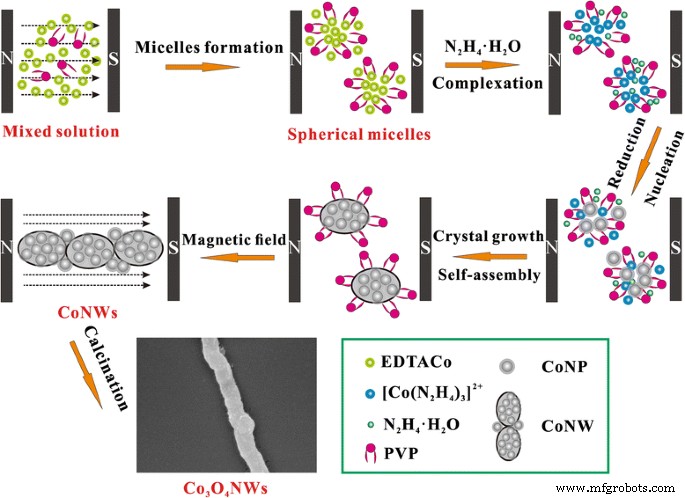
Desenhos esquemáticos do Co 3 O 4 Mecanismo de formação NW assistido por campo magnético externo
Tirando vantagem da característica geométrica 1D de Co 3 O 4 NWs, preparamos os eletrodos usando uma pequena quantidade de grafeno livre de defeitos 2D (df-grafeno) como o suporte condutor para construir uma estrutura híbrida 1D-2D (O método de preparação de df-grafeno foi descrito em um estudo anterior [17] ) A Figura 6a mostra a morfologia de Co 3 O 4 Eletrodo NWs / df-GNS. Para a fabricação de eletrodos, o Co 3 O 4 NWs na forma de pó foram adicionados à dispersão de df-GNS / NMP e, em seguida, a pasta de mistura foi sonicada por 10 min antes de fundir gota a gota em folha de cobre. Como pode ser visto na Fig. 6b, devido à natureza de baixa dimensão dos nanofios e nanofolhas, Co 3 O 4 NWs e df-GNS formaram uma morfologia "plana" no coletor atual com nanofios embutidos entre as nanofolhas. Esta estrutura pode fornecer várias vantagens:(1) pode evitar que esses nanomateriais se autoagreguem, especialmente a autoagregação e o empilhamento de Co 3 O 4 NWs, que é a principal desvantagem para a aplicação prática de tais nanoestruturas; (2) df-GNS pode não apenas oferecer vias rápidas de elétrons, mas também atuar como amortecedor flexível para acomodar a mudança de volume de Co 3 O 4 NWs durante a carga / descarga; (3) a nanoestrutura 1D-2D oferece vários poros e nanotunnels para impulsionar o transporte de íons porque a área de superfície externa, área de micropore e tamanho médio de poro de Co 3 O 4 NWs foram detectados em 28,554 m 2 / g, 43,697 m 2 / g, 14,682 nm, respectivamente.
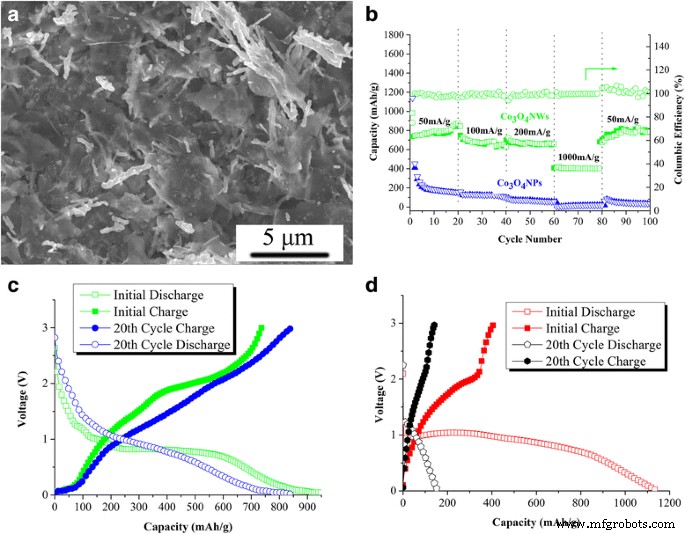
a Imagens SEM de Co 3 O 4 Eletrodo NWs / df-GNS. b Capacidades de taxa de Co 3 O 4 NWs e Co 3 O 4 NPs sob várias densidades de corrente variando de 50 a 1000 mA / g. c , d Curvas típicas de carga e descarga inicial / 20º ciclo de Co 3 O 4 NWs ( c ) e Co 3 O 4 NPs ( d )
O desempenho eletroquímico dos eletrodos preparados foi avaliado por ciclos de carga / descarga galvanostática em várias densidades de corrente variando de 50 a 1000 mA / g. Como pode ser visto, o Co 3 conforme preparado O 4 Eletrodos NWs / df-GNS entregam capacidades reversíveis de ~ 790 mAh / g após 20 ciclos em densidades de corrente de 50 mA / g, pequena queda de capacidade foi observada durante os primeiros 20 ciclos de carga / descarga (como visto na Fig. 6c). Enquanto isso, o Co 3 O 4 Eletrodos NPs / df-GNS pareciam ter capacidade inicial relativamente alta de ~ 1130 mAh / g na primeira descarga, ainda maior do que Co 3 O 4 NWs / df-GNS (~ 980 mAh / g) e a capacidade teórica de Co 3 O 4 (890 mAh / g). Consideramos que esta alta capacidade irreversível inicial é atribuível à formação da camada de interface de eletrólito sólido (SEI) resultante da decomposição do eletrólito. No entanto, a alta capacidade inicial de Co 3 O 4 NPs / df-GNS parecia ser altamente irreversível que decai para ~ 400 mAh / g no segundo ciclo. Após 20 ciclos em densidades de corrente de 50 mA / g, apenas ~ 150 mAh / g foi observado para Co 3 O 4 Eletrodo NPs / df-GNS (como mostrado na Fig. 6d). Quando a densidade da corrente aumentou para 100, 200 e 1000 mA / g, o Co 3 O 4 O eletrodo NWs / df-GNS entregou capacidades de ~ 680, ~ 650 e ~ 400 mAh / g, respectivamente, enquanto o Co 3 O 4 O eletrodo NPs / df-GNS exibe capacidade muito baixa (menos de 150 mAh / g em 100–200 mA / ge menos de 20 mAh / g em 1000 mA / g).
Quando a densidade de corrente volta a 50 mA / g, uma capacidade próxima a 800 mAh / g foi obtida em Co 3 O 4 NWs / df-GNS, enquanto o Co 3 O 4 O eletrodo NPs / df-GNS quase perdeu sua capacidade de armazenamento de íons de lítio. A razão para o severo enfraquecimento da capacidade de Co 3 O 4 NPs / df-GNS podem ser atribuídos aos seguintes fatores:(1) grande mudança de volume durante a inserção / extração de lítio, que induziu a perda de contato entre os materiais ativos e o enchimento condutor / coletor de corrente. Durante os processos de ciclagem, o Co 3 O 4 O eletrodo NPs gradualmente perdeu sua via de transmissão de elétrons e então acabou resultando no desvanecimento da capacidade; (2) configuração de nanopartículas auto-agregadas levou a um Li 2 Matriz O e / ou camada de polímero semelhante a gel envolvendo o agrupamento de nanopartículas, o que poderia impedir a difusão de íons e / ou elétrons para o núcleo do agrupamento. Pelo contrário, heteroestrutura 1D / 2D de nanofio / grafeno em Co 3 O 4 O eletrodo NWs / df-GNS não apenas construiu a configuração “plana” que poderia acomodar a grande mudança de volume, mas também ofereceu vários vazios e poros para aumentar a transmissão de íons / elétrons. Como resultado, os desempenhos de ciclo e taxa de Co3O4NWs / df-GNS foram significativamente melhorados em comparação com Co3O4NPs / df-GNS, mantendo alta capacidade após 100 ciclos.
Além dos testes de carga-descarga galvanostática, os voltamogramas cíclicos (CV) do Co 3 fabricado O 4 NWs / df-GNS foram apresentados na Fig. 7a. No primeiro ciclo, dois picos catódicos foram observados na faixa de voltagem ~ 1,1 e ~ 0,4 V, o que poderia ser correlacionado à redução eletroquímica multipasso de Co 3 O 4 por Li para dar Co metálico (litiação) [22]. O pico anódico principal em 2,2 V é atribuível à reação de oxidação do Co metálico para reformar Co 3 O 4 . Esta reação de conversão eletroquímica reversível pode ser resumida da seguinte forma:
$$ {\ mathrm {Co}} _ 3 {\ mathrm {O}} _ 4 + 8 \ mathrm {Li} {\ displaystyle \ begin {array} {c} \ mathrm {descarga} \\ {} \ leftrightharpoons \\ { } \ mathrm {charge} \ end {array}} 3 \ mathrm {Co} +4 {\ mathrm {Li}} _ 2 \ mathrm {O} $$
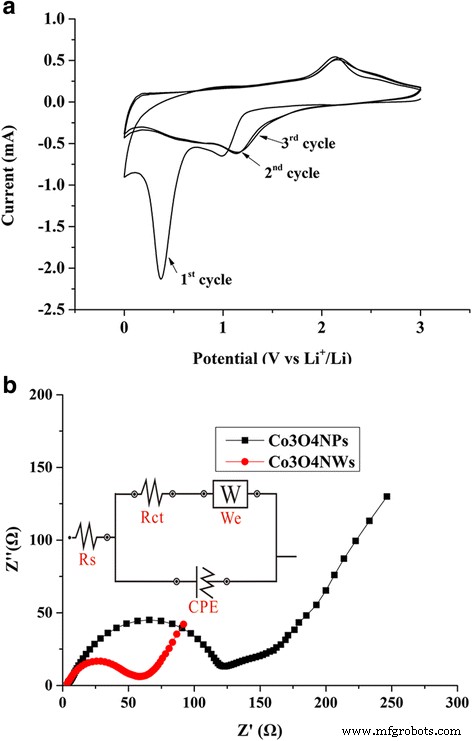
a Voltamogramas cíclicos de Co 3 O 4 Eletrodo NWs / df-GNS a uma taxa de varredura de 0,5 mV / s. b Espectro de impedância eletroquímica de Co 3 O 4 NPs / df-GNS e Co 3 O 4 Eletrodos NWs / df-GNS obtidos pela aplicação de uma onda senoidal com amplitude de 5,0 mV na faixa de frequência de 100 kHz ~ 0,1 Hz
Um enorme pico catódico forte em ~ 0,4 V no primeiro ciclo foi observado; no entanto, o pico catódico no segundo e terceiro ciclo nesta região de voltagem surgiu apenas como um "aumento". Concluímos isso com a formação de um filme de interface de eletrólito sólido (SEI) durante o primeiro processo de descarga, que se manteve estável nos ciclos subsequentes. Como resultado, as curvas CV do segundo e terceiro ciclos quase se sobrepõem, mostrando picos catódicos em 1,2 e 0,7 V e pico anódico amplo em 2,1 V. Este comportamento sugeriu as camadas SEI estabilizadas e alta reversibilidade eletroquímica de Co 3 O 4 Eletrodos NWs / df-GNS. O Co 3 O 4 NWs / df-GNS e o Co 3 O 4 Eletrodos NPs / df-GNS também foram caracterizados por espectroscopia de impedância eletroquímica (EIS). Os gráficos de Nyquist de dois eletrodos, mostrados na Fig. 7b, ambos exibem um semicírculo na região de alta frequência e uma linha inclinada na região de baixa frequência. Os dados de impedância podem ser ajustados no circuito elétrico equivalente mostrado na inserção da Fig. 7b, em que CPE é o elemento de fase constante relacionado à capacitância de camada dupla, We é a impedância de Warburg e Rs e Rct representam a resistência do sistema eletroquímico e a resistência de transferência de carga, respectivamente. A resistência de transferência de carga Rct de Co 3 O 4 NWs / df-GNS foi calculado em 52,6 Ω; no entanto, o de Co 3 O 4 NPs / df-GNS foi de 109 Ω. Sugerimos que esta capacidade superior de transferência de carga dos nanofios contribuiu para o desempenho da taxa do eletrodo.
Conclusões
Em resumo, propusemos uma estratégia nova, fácil e ecológica para sintetizar Co 3 O 4 NWs com eficiência e custo-benefício superiores. Excelentes propriedades de armazenamento de lítio foram observadas em tais nanomateriais. Os resultados de XRD e SAED indicaram que o Co 3 obtido O 4 As amostras NW apresentaram boa qualidade na composição química e de fase. O Co 3 O 4 NWs com diâmetro médio de aproximadamente 180 nm e comprimento variando de 3 a 8 μm foram observados por MEV e TEM. Esses nanofios exibem bom desempenho eletroquímico, alcançando capacidade de armazenamento de lítio superior a 700 mAh / g, como resultado do transporte rápido de elétrons e da natureza adaptável à mudança de volume da nanoestrutura híbrida 1D-2D exclusiva em conjunto com grafeno 2D.
Abreviações
- Co 3 O 4 :
-
Óxidos de cobalto
- Co 3 O 4 NPs:
-
Co 3 O 4 nanopartículas
- Co 3 O 4 NWs:
-
Co 3 O 4 nanofios
- CV:
-
Voltamogramas cíclicos
- DEC:
-
Carbonato de dietila
- df-GNS:
-
Nanofolhas de grafeno sem defeitos
- EC:
-
Carbonato de etileno
- EIS:
-
Espectroscopia de impedância eletroquímica
- GNS:
-
Nanofolhas de grafeno
- HRTEM:
-
TEM de alta resolução
- LIBs:
-
Baterias de íon-lítio
- NMP:
-
N -Metil-pirrolidona
- PC:
-
Carbonato de propileno
- SAED:
-
Difração de elétrons de área selecionada
- SEI:
-
Interface de eletrólito sólido
- SEM:
-
Microscópio eletrônico de varredura de emissão
- TEM:
-
Microscopia eletrônica de transmissão
- XRD:
-
Análise de difração de raios X
Nanomateriais
- Síntese fácil e propriedades ópticas de pequenos nanocristais de selênio e nanorods
- Síntese de pontos quânticos do tipo II / tipo I suprimida por reabsorção / CdS / ZnS Core / Shell Quantum Dots e sua aplicação para ensaio de imunossorvente
- Síntese e propriedades eletroquímicas de materiais catódicos de LiNi0,5Mn1,5O4 com dopagem composta Cr3 + e F− para baterias de íon-lítio
- Síntese fácil de compósito CuSCN colorido e condutor revestido com nanopartículas de CuS
- Síntese fácil de nanofios de prata com diferentes proporções de aspecto e usados como eletrodos transparentes flexíveis de alto desempenho
- Síntese de nanocristais de ZnO e aplicação em células solares de polímero invertido
- Preparação de micrromateriais híbridos MnO2 revestidos com PPy e seu desempenho cíclico aprimorado como ânodo para baterias de íon-lítio
- Síntese de aquecimento de estado sólido de composto de poli (3,4-etilenodioxitiofeno) / ouro / grafeno e sua aplicação para determinação amperométrica de nitrito e iodato
- Síntese de pontos quânticos de sulfeto de antimônio solúvel em água e suas propriedades fotoelétricas
- Síntese de um vaso de nanoplacas Cu2ZnSnSe4 e sua atividade fotocatalítica orientada por luz visível



