Estudo de Espectroscopia de Absorção de Raios-X Síncrotron da Estrutura Local em Pós BiFeO3 Dopados com Al
Resumo
O BiFeO dopado com Al 3 , ou seja, BFA x Amostras de pó O com x =0, 0,025, 0,05 e 0,1, foram preparados por meio da rota hidrotérmica. Os efeitos da substituição de Al nas propriedades estruturais, elétricas e ópticas do BFA x O amostras foram investigadas. Verificou-se que a substituição de íons Al no sítio B de BiFeO 3 não causou mudança estrutural e ainda retém a estrutura perovskita romboédrica com R3c simetria, que foi confirmada pela difração de raios X (XRD) e medidas Raman. Estrutura fina de absorção de raios-X (XAFS) acima do Fe K -edge e Bi L 3 -edge no BFA x O pó também foi medido e analisado. Os íons exibem estados de valência mistos (Fe 2+ / Fe 3+ ) enquanto os íons Bi mantêm o estado de valência + 3 em todas as amostras. Fe K -edge XAFS também indicou que havia uma competição entre a hibridização de Fe 3 d e Al 3 d com O 2 p orbitais e ocorrência dos mais 4 p orbitais com doping Al. O Bi L 3 -edge XAFS revelou essa transição de 2 p 3/2 a 6 d estado aumentou, assim como a energia de 6 d Estado. Além disso, o dopagem de íons de Al afetou tanto o vizinho mais próximo quanto as camadas de coordenação do átomo de Fe e as camadas do vizinho mais próximo do átomo Bi. Os resultados da espectroscopia ultravioleta-visível (UV-Vis) mostram o BFA x O preparado por método hidrotérmico pode ser um material fotocatalítico de luz visível apropriado.
Histórico
Multiferroicos são materiais que apresentam simultaneamente propriedades ferroicas, como ferroeletricidade, ferromagnetismo e ferroelasticidade [1]. Tais materiais apresentam comportamentos interessantes como a polarização elétrica, que pode ser controlada com a aplicação de um campo elétrico externo ou vice-versa. O interesse por esses materiais se deve às suas amplas aplicações em biossensores químicos, dispositivos nanoeletrônicos e de armazenamento de dados de alta densidade, etc [2, 3]. Estruturas de perovskita têm a fórmula geral ABO 3 , onde O é um íon (geralmente se refere ao oxigênio) e A e B são cátions, respectivamente. Geralmente, o cátion A-site é maior com um estado de valência inferior, que combina com O 2- para formar uma camada compactada (isto é, no canto da célula unitária). O cátion de sítio B é menor com estado de valência mais alto, que pode ser adotado em um ambiente de coordenação octaédrica de oxigênio (ou seja, no centro de um octaedro de ânions de oxigênio) [4]. Por definição, quase todos os multiferróicos são antiferromagnéticos (AFM) ou ferromagnéticos fracos (FM) com baixas temperaturas de transição. Eles são divididos em duas classes:monofásica e composta. No entanto, os materiais multifásicos monofásicos raramente são encontrados na natureza, o que mostra as propriedades ferroelétricas (FE) e FM simultaneamente [5]. Entre todos os materiais multiferróicos conhecidos hoje, a ferrita de bismuto (BiFeO 3 ; BFO) é um dos materiais monofásicos que têm um tipo de rede perovskita distorcida em formato romboédrico com grupo de espaço polar R3c . O BFO mostra FE com temperatura de Curie de T C ≈ Pedido de AFM de 1103 k e tipo G com temperatura Neel de T N ≈ 643 k acima da temperatura ambiente (RT) [6]. Este material exibe a configuração de rotação AFM tipo G ao longo do [111] c ou [001] h direções em sua estrutura pseudo-cúbica ou romboédrica e tem uma estrutura de spin espiral sobreposta com uma periodicidade de cerca de 62 Å ao longo do [110] h eixo em RT [7]. Possui uma grande polarização espontânea intrínseca de cerca de 90 μC / cm 2 atribuída à distorção de FeO octaédrica 6 , devido à presença de 6 s 2 par solitário de elétrons [8]. Além disso, há um acoplamento magnetoelétrico entre FE e parâmetros de ordem magnética. As propriedades de FE dependem dos elétrons do par solitário e as propriedades de FM dependem das camadas internas parcialmente preenchidas, isto é, a polarização vem do Bi-site (A-site), enquanto a magnetização vem do Fe-site (B-site).
Além do acima, infelizmente, as principais desvantagens do BFO são sua baixa resistividade ou grande corrente de fuga, devido aos defeitos de carga, como bismuto e vacâncias de oxigênio, fases de impureza, flutuações de valência de ferro e má qualidade interfacial [9]. Além disso, é difícil obter o BFO de alta qualidade por causa de algumas fases de impureza como Bi 2 Fe 4 O 9 (grupo espacial Pbam ) e Bi 25 FeO 39 (grupo espacial I23 ) É inevitável que as impurezas sejam geradas no processo de preparação. Para resolver esses problemas e limitações, vários grupos de pesquisa têm usado vários métodos para superar os defeitos de BFO, por exemplo, modificação de cepas, substituição de dopagem de íons de terras raras e divalentes. Agora, dentro deste campo de estudo, com elemento de terra rara ou dopagem de íon de metal de transição no local A ou local B, ou co-dopagem no local A e B, as propriedades multiferróicas do BFO podem ser aumentadas. Por exemplo, a dopagem com elemento de terra rara pode estabilizar a estrutura da perovskita, reter a não centrosimetria e controlar a vaporização de Bi 3+ íons [10]. Dopagem com íon de metal de transição pode reduzir a flutuação de valência de Fe 3+ íons. Elementos como Pr, Sm, Eu, Gd e La [11, 12] para substituição no local A e Mn, Cr e Ti [13,14,15] para substituição no local B já foram relatados. Além disso, as propriedades magnéticas, dielétricas e ferroelétricas podem ser aumentadas com co-dopagem. Para a co-dopagem de sítios A e B de BFO, La-Gd, Ba-Ni, Dy-Cr, Y-Mn e Tb-Ti foram relatados [16,17,18,19,20]. Até agora, várias rotas, incluindo sol-gel [21], mecanoquímico [22], autocombustão [23], deposição de laser pulsado [24] , e hidrotermal [25, 26] foram relatados para preparar BFO. O método hidrotérmico tem sido amplamente aplicado devido às suas propriedades de economia de energia, dispersão fina, baixo custo e tamanho de partícula pequeno [27]. A temperatura da reação deve ser alta o suficiente para formar o BFO e também usada para remover as fases secundárias durante a preparação da amostra. A maioria dos estudos anteriores de Al dopado em ambos os locais A e B do BFO foram investigados para propriedades estruturais, ópticas e de transporte por Azam et al [28]. Madhu et al. [29] relataram as aplicações fotocatalíticas do BFO dopado com Al no local B. Outro relatório de Jawad et al. [30] exploraram o comportamento dielétrico de cerâmicas BFO nanoestruturadas. O trabalho de Wang et al. [31] estudaram os cristais ocos de BFO dopado com Al em detalhes. No entanto, algumas propriedades físicas importantes ainda não foram compreendidas, como os efeitos da dopagem do local B na estrutura eletrônica local dos materiais. No estágio atual, a espectroscopia de estrutura fina de absorção de raios-X (XAFS) é uma das formas poderosas de estudar o ambiente local de um átomo e fornece informações estruturais dos materiais, bem como energia de absorção, estado de valência do elemento, transferência de carga, e tipo de ligação [32]. Até onde sabemos, não foram encontrados relatórios sobre o efeito do doping com Al no local B na estrutura eletrônica local da investigação de BFO pelo XAFS.
Neste trabalho, o BFO não dopado e as composições alvo BiFe 1- x Al x O 3 (BFA x O) com x =0, 0,025, 0,05 e 0,1 foram sintetizados por via hidrotérmica. O foco principal é a investigação do efeito do doping com Al no local B nas propriedades do BFO, que são comparadas com o BFO não dopado. As propriedades estruturais foram investigadas em detalhes.
Métodos
O método hidrotérmico foi usado para obter BFO não dopado e BFA x Ó amostras. Os reagentes químicos usados neste trabalho foram nitrato de bismuto (Bi (NO 3 ) 3 · 5H 2 O), nitrato de ferro (Fe (NO 3 ) 3 · 9H 2 O), nitrato de alumínio (Al (NO 3 ) 3 · 6H 2 O) e hidróxido de potássio (KOH). Todos os reagentes químicos foram usados como recebidos sem purificação adicional. Bi (NÃO 3 ) 3 · 5H 2 O e Fe (NÃO 3 ) 3 · 9H 2 O foram usados como materiais de origem, enquanto Al (NO 3 ) 3 · 6H 2 O e KOH foram usados como aditivos. Água desionizada foi usada para fazer todas as soluções aquosas. Uma execução típica para a preparação de pós de BFO é a seguinte:Os 20 mL de cada um de Bi (NO 3 ) 3 · 5H 2 O, Fe (NÃO 3 ) 3 · 9H 2 O e Al (NÃO 3 ) 3 · 6H 2 O foram colocados em uma autoclave de aço inoxidável de 80 mL e bem misturados. Depois disso, uma quantidade apropriada de solução de KOH foi lentamente gotejada para a solução de mistura anterior até que 65-80% do seu volume fosse preenchido, que foi transferido para o aparelho de agitação magnética forte para agitar por 2 ~ 3 h a 80 ° C para obtenha uma solução clara. De acordo com o procedimento do método, a solução marrom escura obtida foi transferida para autoclave de aço inoxidável revestida com Teflon. O tratamento hidrotérmico foi realizado a uma temperatura de 200 ° C por 10 h sob pressão autógena. A taxa de aquecimento foi de 2 ° C / min. Depois que a reação hidrotérmica foi concluída, os produtos resultantes foram resfriados até a temperatura ambiente naturalmente. Posteriormente, os pós resultantes foram coletados e lavados várias vezes com acetona, água desionizada e etanol até que o valor de pH das soluções atingisse 7. Finalmente, o BFA x Os pós O foram colocados em um forno de secagem com termostato por 6 h a 70 ° C e, em seguida, secos para posterior caracterização. Preparamos quatro conjuntos de amostras de BFA x O, variando a concentração de Al (NO 3 ) 3 · 6H 2 O de 0–0,1 M.
A estrutura cristalina do BFA x As amostras de O foram determinadas por difração de raios-X (XRD, Mac Science M18XHF22-SRA). A espectroscopia Raman (Renishaw InVia Reflex) com radiação de um laser Ar + foi empregada para determinar as propriedades estruturais dos pós em RT. Os dados XAFS foram coletados no modo de transmissão em várias concentrações na linha de luz 1W2B da Beijing Synchrotron Radiation Facility (BSRF), China. Fe K Espectro de borda com uma resolução de energia de Δ E / E :2 × 10 −4 e Bi L 3 Espectro de borda com uma resolução de energia de Δ E / E :1 × 10 −4 foram medidos para o BFA x O amostras em RT. Para obter os melhores dados XAFS, BFA x Os pós O foram moídos em um almofariz de ágata, depois misturados com BN e finalmente prensados em pellets. A correção de fundo, normalização e região pré-borda e pós-borda do espectro de absorção foram ajustados pelo ATHENA, um software para processamento de dados XAFS, dentro do programa IFEFFIT [33]. O E o o valor foi determinado pelo máximo na primeira derivada na região da borda. Extraímos o χ ( k ) perfil no k espaço de 0–12 Å −1 . O k 3 × χ ( k ) perfil foi Fourier transformado para o R espaço de 0–8 Å, usando a função de janela Hanning. The Fe 2 O 3 e Bi 2 O 3 foram medidos como os compostos de referência. As propriedades ópticas dos pós foram avaliadas usando espectrofotômetro ultravioleta-visível (UV-Vis, UV 3900H). Neste trabalho, a investigação é limitada à baixa concentração de dopagem de 0 ≤ x ≤ 0,1.
Resultados e discussão
Os padrões de XRD do BFO não dopado ( x =0) e BFA x O pós, que digitalizou de 2 θ valor de 15-60 °, são mostrados na Fig. 1. Os espectros completos dos padrões de XRD na Fig. 1a indicam que todas as amostras podem ser identificadas como os dados de difração padrão da estrutura perovskita distorcida romboédrica correspondente (Arquivo JCPDS Card No. 20 -0169, grupo espacial: R3c ) Também pode ser visto que todas as amostras exibem padrões de difração puros com uma pequena quantidade de fases secundárias. Traços de uma fase secundária podem ser vistos em 27,6 ° e 32,8 ° (marcados com “*” para Bi 2 Fe 4 O 9 e “#” para Bi 25 FeO 40 ) para x =0,5 e x =0,1 amostras que podem ser resultantes da natureza de volatilização de Bi na alta temperatura de sinterização [34]. Isso é freqüentemente observado nos pós de BFO sintetizados por diferentes rotas [35,36,37]. As fases secundárias aumentam continuamente no alto valor de dopagem. Portanto, a substituição do Fe por Al no local B não pode promover a fase pura do BFO; no entanto, as propriedades elétricas das amostras não seriam afetadas. Da Fig. 1a, pode-se ver que todos os picos de difração para as amostras dopadas primeiro mudam para 2 θ valores com Al doping. Para maior clareza, uma parte dos padrões de XRD no 2 θ região de 21 a 24 ° são amplificados na Fig. 1b. A partir desta visão ampliada dos picos de difração, pode ser observado que o pico de difração (101) tem uma mudança óbvia em direção a 2 θ valores em relação ao BFO não dopado, o que confirma que Al é dopado com sucesso no local B do BFO. Em analogia com o BFO não dopado, o pico de difração (101) para as amostras dopadas sofre uma mudança em 2 θ valores primeiro, em seguida, um pequeno deslocamento em 2 θ inferior valores quando x =0,1 (circundado por uma linha tracejada), conforme mostrado na Fig. 1c. Os padrões de XRD ampliados nas vizinhanças de 37–40 °, 50–52 ° e 55–57 ° são apresentados na Fig. 1d. Existem alguns picos gêmeos, viz., (003) e (021), (113) e (211), (104) e (122), no espectro de XRD. Com o aumento do conteúdo de Al, a intensidade desses picos primeiro aumenta e depois diminui quando x atinge 0,1. Como sabemos, a intensidade dos picos costuma estar relacionada à cristalinidade. A diminuição dos picos de difração indica que a cristalinidade do BFA x O diminui. Desde Al 3+ (0,51 Å) tem um raio iônico menor do que Fe 3+ (0,65 Å), é facilmente incorporado na rede BFO quando a quantidade de dopagem é pequena, mas o íon de dopagem excessivo torna a rede BFO instável. A redução da cristalinidade pode ser devido ao fato de o Al favorecer a criação de mais sítios de nucleação que, por sua vez, inibem o crescimento dos grãos de cristal. Cristalinidade diminuída também foi encontrada em outro BFO dopado com Al [28, 30]. Por outro lado, isso pode ocorrer se houver uma criação de vacâncias de oxigênio e transformação de algum Fe 3+ para Fe 2+ devido ao desequilíbrio de carga criado no sistema por Al 3+ substituição. Fenômeno semelhante foi observado em BFO dopado com Sr [38]. A mudança nos picos de difração pode ser atribuída à contração da célula unitária, por causa do pequeno raio iônico do Al em comparação com o Fe 3+ . Os resultados do XRD mostram que o trivalente Al 3+ a substituição no BFO não leva a uma transformação estrutural observável.
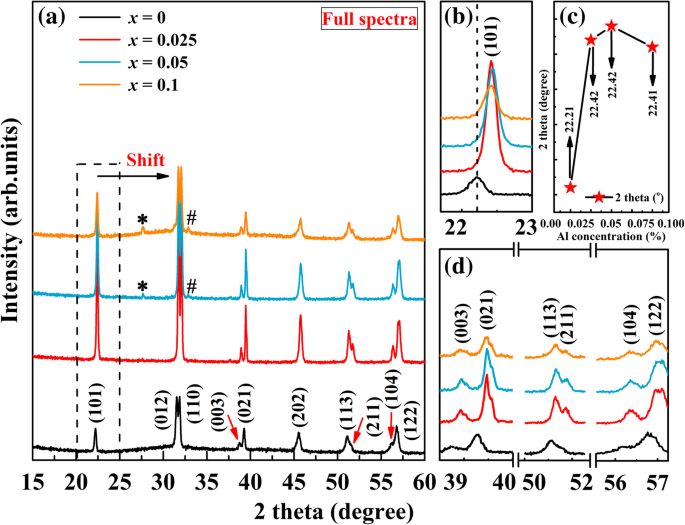
a Padrões de XRD de BFA x O (0 ≤ x ≤ 0,1). b Visão ampliada dos padrões de XRD na faixa de 21–24 °. c A (101) posição do pico em função da concentração de Al. d Padrões de XRD ampliados na vizinhança de 37-40 °, 50-52 ° e 55-57 °
A estrutura confirmada por XRD também pode ser caracterizada pela posição e intensidade dos modos ativos Raman. O espectro Raman é sensível ao deslocamento e distribuição atômica. Os espectros de espalhamento Raman do BFO não dopado e BFA x Os pós O são dados na Fig. 2. Com base na teoria dos grupos, os 13 modos ativos Raman de fônon óptico e 5 modos inativos (ou seja, 5 A 2 ) de BFO são previstos para as perovskitas de distorção romboédrica com grupo espacial R3c [39]. A análise teórica das vibrações da rede na perovskita R3c estrutura é a seguinte:
$$ {\ varGamma} _ {R3c} =4 {A} _1 \ left (z, \ kern0.5em {x} ^ 2, {y} ^ 2, \ kern0.5em {z} ^ 2 \ right) + 5 {A} _2 \ left (- \ right) + 9E \ left (x, \ kern0.5em y, \ kern0.5em {x} ^ 2- {y} ^ 2, \ kern0.5em xy, \ kern0. 5em xz, \ kern0.5em y \ right) $$ (1)
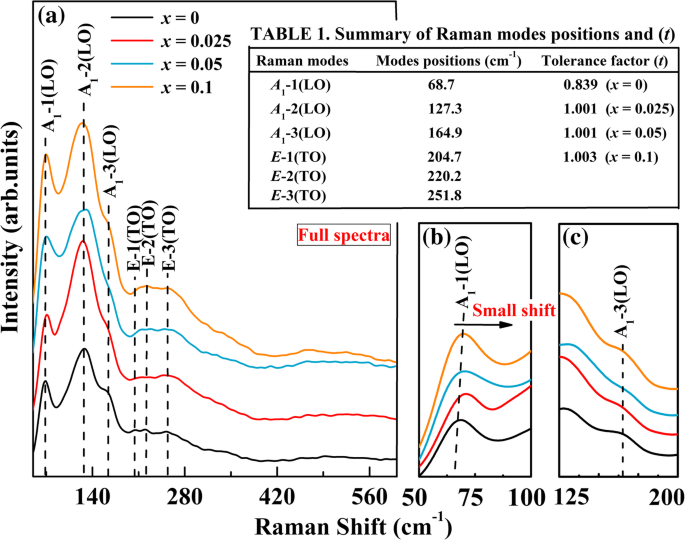
a Espectro Raman de BFA x O (0 ≤ x ≤ 0,1). b Espectro Raman ampliado nas faixas de 50–100 cm −1 e c 125–200 cm −1
onde A é o modo óptico longitudinal (LO) e E é o modo óptico transversal (TO). No espectro completo mostrado na Fig. 2a, o número de modos ativos Raman claramente vistos em RT é muito menor do que o previsto. Neste trabalho, observamos seis modos ativos Raman (3 A 1 (LO) + 3 E (PARA)) para BFA x Ó pós. Isso pode ser devido às degenerescências acidentais entre as bandas no espectro e à incapacidade de distinguir bandas fracas de ruído de fundo [40], ou vazamento dielétrico na amostra. Para o BFO não dopado, os picos forte e largo atingem 68,7 cm −1 , 127,3 cm −1 e 164,9 cm −1 foram atribuídos a A 1 -1 (LO), A 1 -2 (LO) e A 1 Modos -3 (LO), respectivamente. Picos em 204,7 cm −1 , 220,2 cm −1 e 251,8 cm −1 foram atribuídos a E -1 (PARA), E -2 (PARA), e E Modos -3 (TO), respectivamente (consulte a Tabela 1 na Fig. 2). A partir dos espectros, pode ser visto claramente que estes E Os modos (PARA) são invisíveis. Sabe-se que A 1 Os modos -1 (LO) são atribuídos às ligações Bi-O, enquanto os modos de inclinação A 1 Modos -3 (LO) são vistos como FeO 6 octaedro. E Os modos (TO) são atribuídos à vibração Fe-O [41]. O resultado Raman confirma que o BFO não dopado preparado pertence à estrutura perovskita distorcida romboédrica com grupo espacial R3c . Observa-se que todas as quatro amostras apresentam padrão Raman e modos de vibração semelhantes. Isso indicou o mesmo romboédrico R3c grupo espacial, mas suas intensidades e frequências eram um pouco diferentes. Na visão geral do padrão Raman do BFA x O amostras, a posição de pico do A 1 Os modos -1 (LO) são ligeiramente alterados para uma frequência mais alta e os picos de A 1 Modos -3 (LO) foram ampliados, indicando que o dopante Al está indo para o local B do BFO. As intensidades do E -1 (PARA), E -2 (PARA), e E Os modos -3 (TO) são ligeiramente aumentados para as amostras dopadas. Para maior clareza, o A 1 -1 (LO) e A 1 Modos -3 (LO) na região de 50–100 cm −1 e 125–200 cm −1 são mostrados na Fig. 2b e c. A partir desse espectro ampliado, é claro que A 1 Os modos -1 (LO) exibem uma pequena mudança para frequências mais altas com o aumento do conteúdo de Al. Em comparação com os do BFO não dopado, os picos para A 1 Modos -3 (LO) foram ampliados para as amostras dopadas. A pequena mudança do A 1 Modos -1 (LO), ligeiro alargamento de A 1 Modos -3 (LO), e mudança das intensidades de alguns E Os modos (TO) podem estar relacionados à mudança das ligações covalentes Bi-O e Fe-O e uma tensão compressiva na amostra dopada com Al [42, 36]. Por outro lado, é possível que todas as alterações acima sejam devido ao fato de que o B-site Fe 3+ íons foram parcialmente substituídos por Al 3+ íons. Aparentemente, esses resultados Raman são consistentes com as observações de XRD. O fator de tolerância Goldschmidt ( t ) é amplamente utilizado para avaliar a estabilidade geométrica e distorção de estruturas cristalinas [43], onde t é definido pela razão de três tipos de raios iônicos, como segue:
$$ t =\ frac {\ left ({r} _ {\ mathrm {A}} + {r} _ {\ mathrm {O}} \ right)} {\ sqrt {2} \ \ left ({r} _ {\ mathrm {B}} + {r} _ {\ mathrm {O}} \ right)} $$ (2)
onde r A é o raio de Bi 3+ , r B é o raio médio de Fe 3+ e Al, e r O é o raio de O 2- . No entanto, os raios de Al e Fe 3+ são 0,51 Å e 0,65 Å, enquanto o Bi 3+ e O 2- têm os raios de 1,03 Å (de acordo com a Ref. [44]) e 1,38 Å, respectivamente. O t valores para nossos compostos de perovskita estudados BFA x O são encontrados para ser 0,839, 1,001, 1,001 e 1,003 para x =0, 0,025, 0,05 e 0,1, respectivamente (ver Tabela 1 na Fig. 2). O ABO 3 ideal compostos adotam uma estrutura cúbica compactada quando o valor de t é 1, enquanto quando t <1 ou> 1, surge uma deformação geométrica [45, 46]. À medida que a concentração de Al aumenta, o raio iônico médio do local B diminui, o que leva a um aumento adicional no t valor de 0,839 a 1,003. Isso pode ser devido à pequena mudança em um estado simétrico baixo do BFO. É bem conhecido que o cátion B-site em perovskita é rodeado por seis ânions de oxigênio, e quando substituído por íons menores, a distância de coordenação diminuirá. Assim, para analisar claramente os efeitos da substituição de Al, é necessário estudar a estrutura eletrônica local do BFA x Ó amostras.
O XAFS é dividido em dois tipos, isto é, absorção de raios-X perto da estrutura da borda (XANES) e estrutura fina de absorção de raios-X estendida (EXAFS). Nesta medição, quando o raio X penetra na laje com a distância x , a intensidade do feixe de raios-X será reduzida para I = eu o e - μ x . O XAFS mede a absorção dos raios X em função da energia dos raios X E , isto é, o coeficiente de absorção de raios-X μ ( E ) =- d ln eu / dx é determinado a partir da queda na intensidade do feixe de raios-X I com distância x [47]. A proporção de I / eu o é plotado como uma função de E acima dos limites Fe K -edge (7112 eV) e Bi L 3 (13.419 eV), que pode fornecer informações importantes sobre a forma do µ ( E ) As transições eletrônicas devem seguir a regra de seleção de dipolo. Uma absorbância de raios-X μ ( ω ) podem ser obtidos pela regra de ouro de Fermi, da seguinte forma:
$$ \ upmu \ left (\ omega \ right) \ propto \ sum \ limits_f {\ left | \ left \ langle f \ left | D \ right | \ left.i \ right \ rangle \ right. \ right |} ^ 2 \ \ delta \ left \ langle {E} _i- {E} _f + \ omega \ right \ rangle $$ (3)
onde | i ⟩ É o estado inicial, | f ⟩ É o estado final, D é o operador dipolo, E i é a energia de | i ⟩, E f é a energia de | f ⟩ E ω é a frequência do fóton. Os recursos do XANES contêm informações úteis que estão associadas à estrutura eletrônica do absorvedor e ao ambiente local de uma estrutura atômica. Função XANES χ ( E ) é definido da seguinte forma:
$$ \ chi (E) =\ kern0.5em \ left [\ frac {\ mu (E) - {\ mu} _ {\ mathrm {o}} (E)} {\ varDelta {\ upmu} _ {\ mathrm {o}}} \ right] $$ (4)
onde μ o ( E ) é o plano de fundo semelhante ao atômico suave e Δμ o é um fator de normalização que surge do aumento líquido na borda de absorção atômica total de fundo. A Eq. Padrão (4) foi usado para a subtração e remoção do fundo durante o processamento dos dados XANES. Em primeiro lugar, uma função de pré-borda suave é subtraída para remover o fundo dos instrumentos. Em segundo lugar, μ ( E ) é normalizado e, em seguida, uma função de fundo suave pós-borda é subtraída de μ ( E ) para obter o μ o ( E ) A Figura 3a mostra os espectros completos do Fe K -edge XANES de um BFO não dopado e BFA x O pós juntamente com o composto de referência Fe 2 O 3 investigado neste trabalho, enquanto a Fig. 3b relata o espectro XANES na faixa de energia de 7100–7180 eV. Na Fig. 3b, pode-se ver que a forma de todos os espectros e posições de pico são semelhantes entre si. As bordas de absorção mudam ligeiramente para energias mais baixas com o aumento da concentração de Al, o que pode ser atribuído ao efeito de mudança química. A energia da borda de absorção muda para menor energia com a diminuição do estado de carga, sugerindo uma configuração de ligação complexa no local B. É bem conhecido que o deslocamento da borda pode ser usado para obter um estado de oxidação médio. As energias de borda de absorção para nossas amostras estudadas BFA x O são encontrados para ser 7124,95 eV, 7123,87 eV, 7123,84 eV e 7123,80 eV para x =0, 0,025, 0,05 e 0,1, respectivamente. Para o composto de referência Fe 2 O 3 , a energia da borda de absorção é 7126,14 eV (consulte a Tabela 2 na Fig. 3). A borda de absorção de amostras dopadas é menor do que a do Fe 2 O 3 (Fe 3+ ) composto de referência. Aumentando x valores levam à mudança gradual da borda de absorção em direção ao FeO (Fe 2+ ) [48]. A partir disso, podemos notar que BFA x O é um valente misto (Fe 3+ / Fe 2+ ) sistema. Em outro aspecto, três características principais, pico pré-borda A1 e picos pós-borda A2 e A3, são observados em todas as quatro amostras. O pico pré-borda A1, típico para BFO, corresponde à transição quadrupolo elétrica proibida do O 1 s nível para Fe 3 d uns, com uma pequena mistura de Al 3 d estados. À medida que a concentração de Al aumenta, a intensidade do pico pré-borda A1 exibe um pequeno aumento para as amostras dopadas (ver Fig. 3c). O pico pós-borda A2 é atribuído ao O 2 p transferência de banda para o Fe 3 d órbita, o chamado processo de transferência de carga de ligante para metal [49], enquanto o pico A3 é causado por 1 s a 4 p transição permitida por dipolo [50]. Com o aumento da concentração de Al, a intensidade desses dois picos pós-borda pode ser claramente vista aumentar para as amostras dopadas (ver Fig. 3d). Todas as mudanças acima na intensidade do pico pré-borda e pós-borda podem ser entendidas em termos de competição entre a hibridização de Fe 3 d e Al 3 d com O 2 p orbitais. Além disso, após o doping com Alion, há mais desocupados 4 p orbitais ocorrendo em BFA x O. Exceto estes, os espectros inteiros não mostram mudanças significativas e esses resultados provam que os íons Al são parcialmente dopados no local B do BFA x O.
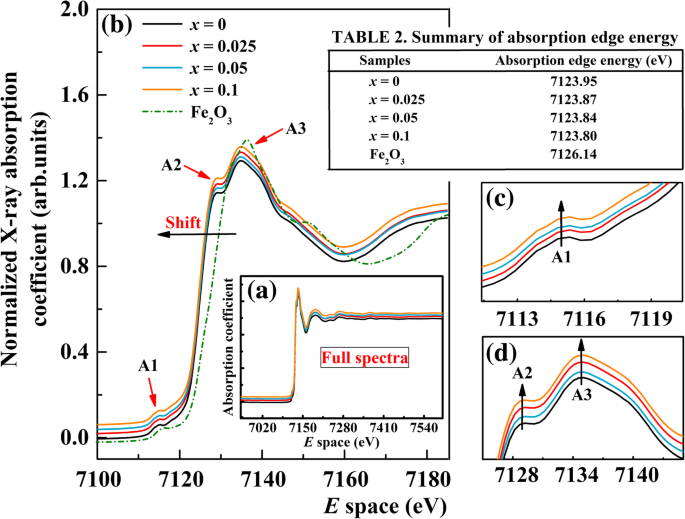
a Fe K -edge espectros XANES de BFA x O (0 ≤ x ≤ 0,1) e referência Fe 2 O 3 . b Espectro XANES na faixa de 7100–7180 eV. c Visão ampliada do pico A. d Pico B e pico C
As distribuições de ligações Fe-O, Fe-Fe / Al (isto é, Fe-O-Fe / Al) e Bi-O são obtidas ajustando o k 3 ponderado ( k 3 × χ ( k )) dados brutos, como segue:
$$ k =\ sqrt {\ frac {2m \ left (E- {E} _ {\ mathrm {o}} \ right)} {\ mathrm {\ hbar}}} $$ (5)
onde E o é a energia da borda de absorção e ħ é a constante de Planck. Ajustes adicionais (algumas aproximações e oscilações) são feitos usando a equação EXAFS padrão, como segue:
$$ \ chi (k) =\ sum \ limits_R {S} _ {\ mathrm {o}} ^ 2 {N} _ {\ mathrm {R}} \ frac {\ left | f (k) \ right |} {k {R} ^ 2} \ sin \ left (2 kR + 2 {\ delta} _ {\ mathrm {c}} + \ phi \ right) {e} ^ {\ frac {-2R} {\ lambda ( k)}} {e} ^ {- 2 {\ sigma} ^ 2 {k} ^ 2} $$ (6)
onde \ ({S} _ {\ mathrm {o}} ^ 2 \) (\ (0 <{S} _ {\ mathrm {o}} ^ 2 <1 \)) é o fator de redução, N R é o número de átomos retroespalhados à distância R , f ( k ) é a amplitude de retroespalhamento, δ c é a mudança de fase do centro, ϕ são os átomos retroespalhados, λ é a vida útil do furo central, σ 2 é o fator Debye-Waller de múltiplas distâncias, e k é o caminho livre médio do fotoelétron. A região EXAFS é normalmente referida à faixa de energia de 20-30 eV acima do salto de borda, que é sensível a tipos de pedido de curto alcance, distâncias de ligação e números de coordenação em materiais. Embora, a Eq. (6) poderia fornecer algumas informações sobre as aproximações e oscilações EXAFS, não é uma forma particularmente conveniente para visualizar o conteúdo de informação de um espectro EXAFS. Portanto, a transformação de Fourier pode ser usada para decompor um k sinal do espaço em suas diferentes frequências constituintes [32]. A transformação de Fourier é uma função complexa da distância interatômica R , cuja amplitude é representada pela função real de χ ( R ) Nessa função, a posição dos picos está relacionada às distâncias da ligação e aos íons vizinhos. A equação (6) pode ser transformada de k espaço para R espaço pela transformada de Fourier, como segue:
$$ \ chi (R) =\ frac {1} {\ sqrt {2 \ pi}} {\ int} _ {k _ {\ mathrm {min}}} ^ {k _ {\ mathrm {max}}} \ omega (k) {k} ^ n \ chi {e} ^ {- 2 ikR} dk $$ (7) $$ \ left \ {\ begin {array} {c} \ genfrac {} {} {0pt} {} {\ kern2.5em 0 \ kern7.5em k <{k} _ {\ mathrm {min}} \} {\ sin ^ 2 \ left [\ frac {\ pi \ left (k- {k} _ {\ mathrm {min}} \ right)} {2 \ left ({k} _2- {k} _ {\ mathrm {min}} \ right)} \ right] \ kern3.25em {k} _ {\ mathrm {min} }
onde k máximo e k min são os valores máximos e mínimos de k transformados espaço, respectivamente, χ (R) é a função da janela Hanning, ω ( k ) é a função da janela gaussiana, e k n é o fator de peso ( n =0, 1, 2, 3). O k 2 e k 3 valores para o BFA x O são 2 e 10, respectivamente, e o valor de n é 2. Transformada de Fourier de Fe K -edge EXAFS do BFA x Amostras O são realizadas, conforme mostrado na Fig. 4a. O pico assimétrico (rodeado pela primeira linha tracejada) centrado em ~ 1,503 Å é identificado como uma ligação Fe-O, devido ao espalhamento dos ânions de oxigênio. O segundo pico forte (rodeado pela segunda linha tracejada) em torno de ~ 3,527 Å corresponde às ligações Fe-Fe / Al, o que pode ser explicado pelo espalhamento de ânions de oxigênio do átomo de Fe / Al próximo ao vizinho mais próximo cartuchos. A distância para a primeira e segunda camadas de coordenação foi resumida na Tabela 3 na Fig. 4. A partir da posição do pico, em comparação com a amostra BFO não dopada, Fe-O e ligação Fe-Fe / Al tendem a se deslocar ligeiramente para menor R valores com o aumento de x . Isso indica que a dopagem por íons de Al não afeta apenas a estrutura local do vizinho mais próximo do átomo de Fe central, mas também afeta as camadas de coordenação mais próximas do átomo de Fe. Por outro lado, a mudança da ligação Fe-O para R menor valores podem resultar de que o raio dos íons de Al é menor do que o dos íons de Fe. Isso é consistente com os dados XRD. A mudança de Fe-Fe / Al para R menor os valores também indicam que o comprimento médio da ligação Fe-Fe / Al (onde os dois Fe 3+ íons estão nos centros do octaédrico de oxigênio vizinho) gradualmente se torna mais curto e o ângulo de ligação é modificado nas amostras dopadas com Al. No entanto, há um pequeno aumento da intensidade de pico da distribuição de Fe-O para as amostras dopadas, enquanto a intensidade de pico da distribuição de Fe-Fe / Al quase não é alterada. Isso revela que a estrutura vizinha ao ferro do Fe-O foi modificada pelo doping com Al. As ligações Fe-Fe / Al mais curtas em amostras dopadas com Al podem explicar porque os picos principais (101) no XRD mudam para 2 θ ângulos (ver Fig. 1b). Isso indica que a substituição de Al por Fe pode afetar o octaédrico de oxigênio, o que reduz ainda mais a distância de coordenação entre os dois átomos de Fe vizinhos. A Figura 4b mostra o Fe K -edge EXAFS do BFA x Amostras O processadas em k 3 × χ ( k ) oscilação com um k space of 0–10 Å −1 . As can be seen, all the k 3 × χ ( k ) spectra show similar patterns at the smaller k values but different at larger k values with some various noise (surrounded by the dash line). Al-doped samples show a broader k 2 × χ ( k ) spectrum than those of undoped BFO in the k space of 8.2–9.3 Å −1 , implying an enhanced short-range structural disorder in BFAx O samples. The noises are observed in a k space of 10–10.4 Å −1 . These changes indicated that the local structure of center atoms has changed due to B-site Al doping, similar to what was reported by Li et al. [51].
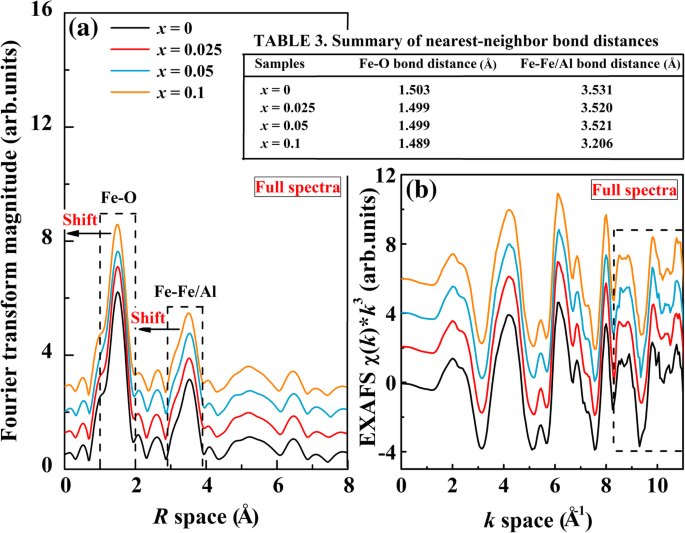
a Fourier transforms of Fe K -edge k 3 -weighted EXAFS data, for the BFAx O (0 ≤ x ≤ 0.1). b EXAFS χ ( k ) × k 3 spectra of BFAx O (0 ≤ x ≤ 0.1). The spectra were aligned along the Y -axis for better comparison
The peak positions, intensities, and shapes of the line in the Bi L 3 -edge XANES spectrum are well known to depend on the local electronic structure of the Bi atoms, which could provide information on the Bi valence. The full spectra of Bi L 3 -edge XANES of undoped BFO and BFAx O samples are also shown in Fig. 5a, while Fig. 5b shows the Bi L 3 -edge XANES spectrum in the energy region of 13,400–13,480 eV. The analysis of these spectra helps to investigate the local electronic structure of Bi ions in the doped system. From Fig. 5b, it can be seen that the shape of all spectra are the same to each other and there is almost no change of absorption edge in the whole series. The absorption edge energies for our study are found to be 13,429.1 eV, 13,429.4 eV, 13,429.3 eV, 13,429.3 eV, and 13,429.8 eV for x =0, 0.025, 0.05, and 0.1 and the reference compound Bi2 O 3 , respectively (see Table 4 in Fig. 5). The absorption edges slightly shift toward higher energies with increasing Al concentration. The absorption edge in the Bi L 3 -edge of the BFAx O samples matches well with that of the reference compound Bi2 O 3 , which indicates that the valence state of Bi ions in all the samples is in + 3 valence state. However, there are two post-edge peaks found in all samples and marked as B1 and B2, respectively. These two post-edge peaks are caused by the electric-forbidden transition from 2p 3/2 level to the 6d ones. Compared with undoped BFO, the intensity of peak B2 can be clearly seen to increase for the doped samples (see Fig. 5c), which means the transition from 2p 3/2 to 6d state increases, so does the energy of 6d Estado. Except these, there is no other significant change in the whole spectrum.
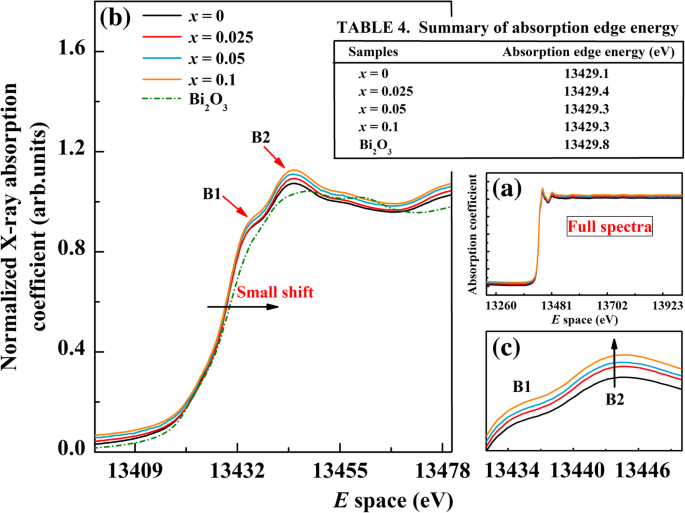
a Bi L 3 -edge XANES spectra of BFAx O (0 ≤ x ≤ 0.1) and reference Bi2 O 3 . b XANES spectrum in the range of 13,400–13,480 eV. c Enlarged view of the peak D and peak E
Fourier transform of Bi L 3 -edge EXAFS radial distribution functions is performed, as shown in Fig. 6a. A high-intensity peak located at around 1.618 Å corresponds to the nearest Bi-O coordination shell (surrounded by the dash line), which is a result from scattering from the nearest-neighbor atomic shell of Bi, i.e., oxygen anions. However, the position of Bi-O bond shifts toward larger R values for the doped samples (see Table 5 in Fig. 6). This indicates that the substitution of Al for Fe could affect the nearest-neighbor local structure of the central Bi atom. It also indicates the extension of Bi-O bond length. The peak intensity of the Bi-O distribution exhibited a small increase with increasing Al content, which suggests that the iron-neighboring structure of Bi-O has changed. Figure 6b shows the Bi L 3 -edge k 3 × χ ( k ) EXAFS spectra with a k space of 0–14 Å −1 . From Fig. 6b, it can be seen that all the spectra shape shows similar patterns except some error noises. The error noises are observed in the k space of 12–14 Å −1 (surrounded by the dash line). This result may imply that the k 3 × χ ( k ) EXAFS function of the center Bi atoms has changed with Al doping. This also suggests that the B-site Al substitution influences short-range structural disordering.
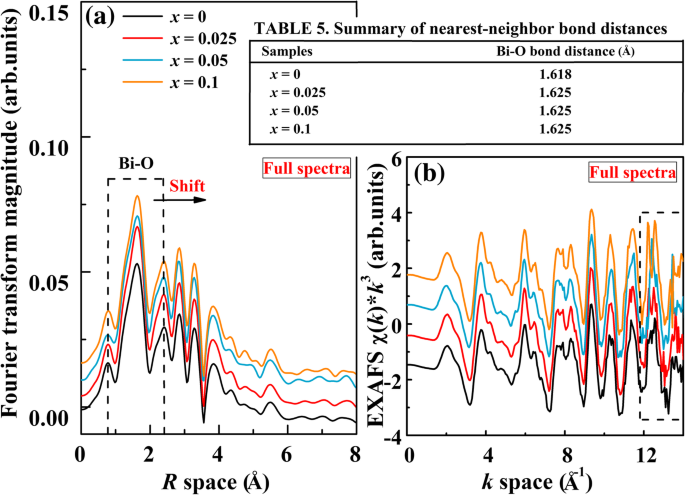
a Fourier transforms of Bi L 3 -edge k 3 -weighted EXAFS data, for the BFAx O (0 ≤ x ≤ 0.1). b EXAFS χ ( k ) × k 3 spectra of BFAx O (0 ≤ x ≤ 0.1). The spectra were aligned along the Y -eixo
The optical properties of the samples are studied by using RT UV-Vis, which is used to characterize the optical properties of the materials. The UV-Vis absorption spectra of undoped BFO and BFAx O samples in the wavelength of 300–800 nm are shown in Fig. 7a. As a result, the UV-Vis spectra of the undoped BFO and BFAx O samples show two absorption edges (marked by dashed arrows). One is a band around 650 nm, which is due to the metal-to-metal transition. The other is a band around 760 nm, which is caused by crystal field transition [52]. In addition, the strong absorption band is observed at about 490 nm (marked by dashed arrow), which is attributed to the electronic transition from O 2p to Fe 3d state in the BFO. These strong bands indicate that the BFO prepared by hydrothermal method could be a promising visible-light photocatalytic material. BFO is of direct transition with a value of n as 2. The absorption edge of the doped samples shifted from 659 to 619 nm, suggesting that the BFAx O powders absorb visible light in the wavelength range of 600–659 nm (see Fig. 7a). A similar blue-shift phenomenon was observed earlier in other element-doped BFO [53,54,55]. This blue shift in the absorption spectra of Al-doped samples in comparison with the undoped BFO shows that doping Al causes a change in the local structure for BFO. From Fig. 7a, one can see that the absorption spectra of the Al-doped samples exhibit a sharp increase around 490 nm and it suggests that all samples can absorb remarkable amounts of visible light. For the sample with x =0.025, the absorption spectrum shows a sudden increase. It means that it has a wider absorption range than the other samples in this range of visible light. The optical band gap of the samples has been calculated by Tauc’s formula, as follows:
$$ ahm=A{\left( hm-E\mathrm{g}\right)}^n $$ (9)
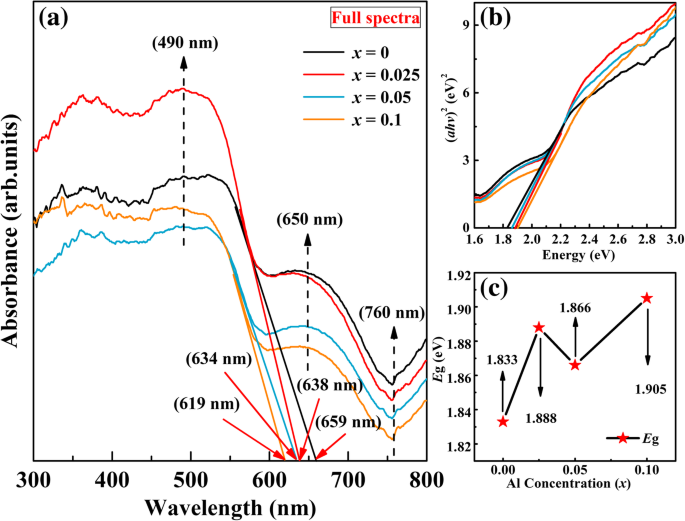
a UV-Vis absorption spectrum of BFAx O (0 ≤ x ≤ 0.1). b Plots of (ahν ) 2 vs. photon energy. c E g values as a function of Al concentration
onde a is the absorption coefficient, A is the parameter, h is the Planck’s constant, m is the frequency of the incident photon, E g is the optical band gap, and n (for direct n =2, for indirect n =0.5) is a constant associated with different types of electronic transitions, as shown in Fig. 7b. The calculated E g values are found to be 1.833 eV, 1.888 eV, 1.866 eV, and 1.905 eV for x =0, x =0.025, x =0.05, and x =0.1 samples, respectively. It is easy to see that the band gap increases with the substitution ratio, as shown in Fig. 7c. The increase in the band gap is attributed to the doping effect. O E g value for the undoped BFO is about 1.833 eV, which is lower than the previous reports [56, 57].
Conclusão
In summary, the BFAx O (x =0, 0.025, 0.05, and 0.1) multiferroic powder samples were successfully synthesized via hydrothermal route. Effects of Al substitution on the structural, electrical, and optical properties of the samples were studied. The structural study reveals that Al-doped BiFeO3 shows the existence of secondary phases and lattice contraction due to lower ionic radii of Al doped into B-site, which still retains its rhombohedral R3c perovskite structure. Raman scattering measurement infers six Raman active phonon modes, which further confirms the result of XRD. XAFS studies on the Fe K -edge and B L 3 -edge of the BFAx O samples and of the reference compounds Fe2 O 3 and Bi2 O 3 were performed, and the obtained results were compared in order to determine the valance states of Fe and Bi ions in the system. The Fe K -edge XAFS results revealed that BFAx O is a mixed-valent (Fe 3+ /Fe 2+ ) system. The results of Fe K -edge XAFS also illustrate a competition between the Fe 3d and Al 3d orbitals on hybridization with the O 2p and occurrence of the more 4p orbitals with Al doping. Besides, Al ion doping affects both the nearest-neighbor and next-nearest coordination shells of the Fe atom. The B L 3 -edge XAFS results indicate that valence states of Bi ions in all the samples are in + 3 and the transition from 2p 3/2 to 6d state and the energy of 6d state increases. Substitution Al for Fe could affect the nearest-neighbor local structure of central Bi atom. The BFAx O prepared by hydrothermal method could be an appropriate visible-light photocatalytic material due to a strong absorption band in the visible region.
Abreviações
- AFM:
-
Antiferromagnético
- BFAx O:
-
BiFe1-x Alx O 3
- BFO:
-
BiFeO 3
- EXAFS:
-
X-ray absorption fine structure
- FE:
-
Ferroelectric
- FM:
-
Ferromagnético
- RT:
-
Temperatura do quarto
- UV-Vis:
-
Ultraviolet-visible
- XAFS:
-
X-ray absorption fine structure
- XANES:
-
X-ray absorption near edge structure
- XRD:
-
Difração de raios X
Nanomateriais
- Absorção de luz aprimorada por plasma em células solares nanowire de GaAs de junção (p-i-n):um estudo de método de simulação FDTD
- Expansão Térmica Anômala de HoCo0.5Cr0.5O3 Sondada por Difração de Pó Síncrotron de Raios-X
- O estudo de um novo sistema micelar em forma de verme aprimorado por nanopartículas
- Investigação sobre polarização de superfície de heteroestrutura GaN / AlGaN / GaN capeada por Al2O3 por espectroscopia de fotoelétrons de raios-X com resolução de ângulo
- Estudo antitumoral de nanogéis de sulfato-metotrexato de condroitina
- Melhoria de modulação e absorção de frequência do microbolômetro THz com estrutura de microponte por antenas tipo espiral
- Estrutura Eletrônica e Características I-V das Nanoribbons InSe
- Propriedades ópticas de filmes ZnO com dopagem Al-Dopada na região infravermelha e suas aplicações de absorção
- Estudo dos primeiros princípios de defeitos pontuais na superrede de GaAs / AlAs:a estabilidade de fase e os efeitos na estrutura da banda e na mobilidade do portador
- Espectroscopia de Absorção Aprimorada por Cavidade (CEAS) para Detecção de Ozônio



