Desenvolvimento de uma estratégia geral de fabricação de nanocompósitos de metal nobre carbonáceo com propriedade fototérmica
Resumo
Este estudo demonstra um método hidrotérmico simples, embora possa ser generalizado para a síntese controlável de nanoestruturas carbonáceas metálicas nobres (por exemplo, Au @ C, Ag @ C) sob condições moderadas (180–200 ° C), que também fornece uma abordagem única para a fabricação de ocos estruturas carbonáceas por remoção de núcleos (por exemplo, prata) por meio de um processo de corrosão redox. A microestrutura e a composição das nanopartículas conforme obtidas foram caracterizadas usando várias técnicas microscópicas e espectroscópicas. O brometo de cetiltrimetilamônio (CTAB), atuando como surfactante no sistema de reação, desempenha um papel fundamental na formação dos nanocabos Ag @ C, Au @ C e seus correspondentes nanotubos carbonáceos ocos neste trabalho. O crescimento dinâmico e mecanismo de formação de nanoestruturas carbonáceas foram discutidos em detalhes. E, finalmente, a propriedade fototérmica induzida por laser de nanocompósitos de Au @ C foi examinada. Os resultados podem ser úteis para projetar e construir metal (s) carbonáceo (s) ou óxido (s) metálico (s) nanoestruturas com aplicações potenciais nas áreas de catálise eletroquímica, armazenamento de energia, adsorventes e biomedicina.
Resumo gráfico
Este estudo demonstra uma síntese hidrotérmica fácil de nanocompósitos carbonáceos de metais nobres (por exemplo, Au @ C) com procedimentos simples em condições suaves, que podem ser expandidos como um método geral para a preparação de diversas nanopartículas de núcleo-casca carbonáceos. As nanoestruturas carbonáceas Au @ C exibem propriedades UV-Vis interessantes, dependendo da espessura da casca.
Destaques
-
Desenvolva um método hidrotérmico simples para gerar nanoestruturas núcleo-casca de metal nobre @ C
-
Os núcleos Ag ou Au gerados são bem cristalizados, mas a bainha carbonácea é amorfa
-
A glicose desempenha um papel múltiplo como um redutor de íons metálicos, um modificador de forma e proteção de superfície
-
Reação hidrotérmica de baixa temperatura (60-100 ° C) para ataque ácido Ag @ C núcleo-casca para obter bainha carbonácea oca
-
Nanocompósitos Rodlike Au @ C apresentam efeito fototérmico, potencial para aplicações biomédicas
Introdução
Os materiais de carbono têm se tornado cada vez mais importantes na ciência e tecnologia de materiais. Uma série de partículas de carbono foram investigadas no passado, como nanotubos de carbono, esferas / pontos de carbono [1,2,3] e óxido de grafeno (GO) [4, 5]. Entre eles, as nanoestruturas carbonosas exibiram algumas propriedades únicas, como boa estabilidade (<200 ° C), paredes tubulares porosas, propriedades lubrificantes superiores, dispersão fácil em água e biocompatibilidade, bem como prontamente hibridizadas com metais (por exemplo, Au, Ag ) e / ou óxidos de metal para a geração de nanoestruturas funcionais híbridas [6,7,8,9,10,11,12,13].
Especificamente, os nanocompósitos de metal carbonáceo têm atraído mais interesses devido à sua excelente biocompatibilidade em aplicações médicas. Para atingir tais partículas carbonáceas ou suas estruturas híbridas metálicas, uma série de métodos foram desenvolvidos, por exemplo, método hidrotérmico, usando açúcar ou amido como material de partida [14], por exemplo, síntese hidrotérmica em uma etapa de nanocabos e nanotubos de prata carbonácea após a gravação de núcleo de prata s [15], uma abordagem de modelo para preparar nanocabos coaxiais Ag / Cu @ poli (álcool vinílico) (PVA), nanoestruturas de telúrio (Te) @PVA [16] e modelo baseado em membrana porosa e modelos rígidos positivos [17,18,19,20] para a síntese de nanoestruturas carbonosas. No entanto, a remoção do (s) molde (s) rígido (s) pode levar a problemas nos pós-tratamentos (corrosão química ou calcinação a alta temperatura), como quebra ou colapso da estrutura [14,15,16,17,18,19,20,21 , 22]. Além disso, pouco foi relatado para elucidar o mecanismo de formação / evolução de nanoestruturas de metal nobre carbonáceo obtido nas condições relatadas.
A terapia fototérmica foi desenvolvida porque causa menos danos aos tecidos saudáveis por meio da geração de calor localizado, especialmente nas etapas iniciais de metástase ou quando o tumor está no estágio primário. Nanopartículas de ouro (GNPs) são uma das seleções excelentes para essa abordagem. Avanços recentes no design multifuncional de GNPs permitem a geração de calor localizado na proximidade de tecidos cancerígenos e, adicionalmente, permitem a distribuição de vários medicamentos desejados de maneira controlada e direcionada. Os GNPs têm muitos benefícios que os tornam adequados para o tratamento fototérmico de tumor ou câncer, porque podem ser entregues na área local do tumor, minimizando a distribuição não específica, ativada por luz de laser infravermelho próximo (NIR), criando a capacidade de penetrar profundamente em tecidos biológicos e modulado para criar terapia fototérmica de câncer multifacetada [23,24,25].
Aqui, demonstramos um método de síntese simples, mas eficaz para gerar nanoestruturas carbonáceas de Au @ C ou Ag @ C em condições moderadas (180–200 ° C). Curiosamente, os núcleos de Ag, em vez de Au, podem ser gravados ou removidos da estrutura carbonácea por corrosão em baixa temperatura (60 ° C por dezenas de horas) sem a necessidade de quaisquer tratamentos de alta temperatura. A microestrutura dos nanocompósitos preparados será caracterizada e os possíveis mecanismos de formação serão compreendidos. A propriedade fototérmica das nanoestruturas de Au @ C, como um estudo de caso, será examinada, por referência a estudos recentes [23,24,25]. Este estudo pode oferecer uma estratégia fácil, mas eficaz para preparar nanocompósitos de metal carbonáceo com aplicações potenciais em ciência de materiais, catálise e bioquímica.
Método Experimental
Químicos
Os seguintes produtos químicos foram adquiridos da Sigma-Aldrich e usados como recebidos sem purificação adicional:nitrato de prata (> 99%), d -glucose (99%), brometo de cetiltrimetilamônio (CTAB,> 98%) e cloreto de ouro (III) tri-hidratado (HAuCl 4 · 3H 2 O,> 99,9%). Todas as vidrarias foram limpas com água régia fresca, enxaguadas extensivamente com água destilada e / ou etanol por algumas vezes e secas antes do uso.
Síntese de nanoestruturas carbonáceas de Ag @ C e Au @ C
Normalmente, algumas etapas foram envolvidas no procedimento de síntese. In s tep 1, 2,0 mL 0,01 M de AgNO 3 e 6,0 mL de solução de glicose 0,01 M foram adicionados a um copo de vidro de 50 mL contendo 10 mL de solução 0,12 M de CTAB, em seguida, misturados e agitados para garantir a homogênea eit y. In s tep 2, o volume total da solução de mistura foi fixado em 35 mL usando água destilada sob agitação durante 10 min para homogeneidade. A cor da solução da mistura gradualmente tornou-se amarelo claro, provavelmente devido à formação do precipitado de AgBr na presença de CTAB. E em etapa 3, a solução misturada foi transferida para uma autoclave de aço inoxidável com um forro de Teflon de 50 mL de capacidade e aquecida em um forno a 180 ° C por algumas horas.
Semelhante ao procedimentos para preparar nanopartículas de Au @ C, a substituição de AgNO 3 por HAuCl 4 · 3H 2 A solução foi realizada neste trabalho. Em termos de preparação de nanobastões de Au @ C carbonáceos, os nanobastões de Au foram sintetizados primeiro, com base em nosso trabalho anterior [26,27, - 28], em que o CTAB desempenha um papel fundamental no controle de o formação de nanobastões de Au. Os nanobastões de Au foram dispersos em solução de glicose para posterior reação hidrotérmica a 180 ° C por 6 - 24 h.
Ataque para estrutura carbonácea oca
Nanoestruturas carbonáceas ocas foram fabricadas por ataque ácido de núcleos de Ag a partir de nanocompósitos Ag @ C, mantendo a mesma solução de reação a 60 ° C por dezenas de horas, embora isso não seja viável para decapagem do núcleo de Au de Au @ C. Por meio de um processo de reação dinâmica, os núcleos Ag foram removidos , e, portanto, , as estruturas carbonáceas ocas formadas. As amostras resultantes foram enxaguadas com água destilada três tempos para posterior caracterização.
Caracterização
Os processos de formação, crescimento e corrosão das nanoestruturas carbonáceas de Au @ C e Ag @ C preparadas foram caracterizados usando várias técnicas, incluindo microscopia eletrônica de transmissão (TEM, JEOL-1400), microscopia eletrônica de varredura (SEM, FEI Nova NanoSEM 230 FESEM), TEM de alta resolução (HRTEM) usando um canhão de emissão de campo Phillips CM200 TEM operado a 200 kV, espectros de UV-Vis por espectrofotômetro Cary 5000 UV-Vis NIR com uma célula de quartzo de 1 cm, infravermelho de transformada de Fourier (FT-IR ) espectro pelo microscópio Perkin Elmer Spotlight 400 FT-IR (650–4000 cm −1 ), Espectroscopia Raman (espectrômetro Raman Renishaw RM1000, comprimento de onda de excitação 514 nm) e um sistema de difração de raios-X multifuncional Philips X’pert usando Cu-K α ( λ =0,15406 nm) radiação a 40 kV e 100 mA, na faixa de medição de 10–80 ° com uma etapa de varredura de 0,02 ° / s.
Medições fototérmicas
Um termopar foi usado para a medição da temperatura fototérmica com base em relatórios anteriores [23,24,25, 29,30,31]. A medição do termopar usou Delta OHM HD2128.2 tipo T. A fonte de luz é uma potência de laser com densidade de 0,17 W / cm 2 . Para ser mais preciso e confiável, as temperaturas foram medidas por uma câmera Cedip Titanium 560 M IR, com imagens de resolução de 640 × 512 pixels em taxas de quadro de até 100 Hz. Os pixels são quadrados com dimensão 24 × 24 μm. O chip do dispositivo de carga acoplada (CCD) na câmera é sensível a um comprimento de onda de 3,6-5,1 μm, portanto, apenas a emissão térmica do fluido pode ser vista nas imagens, já que o comprimento de onda do laser de 0,8 μm é invisível para o sensor da câmera . A faixa de temperatura é definida para uma faixa de 0–60 ° C. Para a medição fototérmica, escolhemos as estruturas carbonáceas de Au @ C (nanobastões de Au com razão de aspecto de ~ 3,7), como um estudo de caso, devido à forte estabilidade e não toxicidade do Au em biossistemas.
Resultados e discussão
Microestrutura de Nanoestruturas Carbonaceous Ag @ C
A morfologia e composição das nanopartículas obtidas foram caracterizadas usando técnicas de TEM e SEM. A Figura 1a mostra as imagens TEM dos nanocabos Ag @ C preparados, junto com uma inserção de imagem de ampliação, em que o diâmetro dos cabos foi estimado em 30–50 nm, enquanto o núcleo Ag de 10–20 nm de largura. Isso também é confirmado por SEM, como mostrado na Fig. 1b, onde os nanocabos Ag @ C não são retos, mas curvados. Aqui, foi descoberto que apenas nanocabos Ag @ C unidimensionais, mas esferas carbonáceas foram formadas, indicando que a autonucleação e o processo de crescimento por meio da carbonização da glicose foram significativamente suprimidos, e o processo de revestimento no núcleo de Ag é dominante sob nosso condições relatadas.

Nanoestruturas Ag @ C: a TEM e b Imagens SEM para nanocabos carbonosos. c , d TEM para nanotubos carbonosos
Posteriormente, os nanocabos Ag @ C puderam ser atacados mantendo a mesma solução de reação a 60 ° C por 24 h, sem a adição de agentes de corrosão, e então os tubos carbonosos ocos foram obtidos, como mostrado na Fig. 1c, d com ampliações diferentes. Claramente, o núcleo Ag pode ser removido ou gravado a partir dos nanocabos (Fig. 1a) pela reação hidrotérmica projetada. Em comparação, os nanotubos estão ligeiramente encolhidos, mas sem peças danificadas ou quebradas, sugerindo que as conchas carbonáceas são relativamente estáveis em estrutura nas condições relatadas.
Para melhor compreender os processos de formação e crescimento dos nanocompósitos de Ag @ C, diferentes tempos de reação foram considerados para monitorar a reação dinâmica (Fig. 2). Com o tempo aumentando de 1 h (a) a 3 h (b), 6 h (c), 12 h (d) e 24 h (e) sob a temperatura de reação de 180 ° C, formou-se o Ag @ C carbonáceo , em que o Ag gradualmente se formou de pontos (a) para hastes curtas (b – d) e, finalmente, para hastes / fios (e). Os nanobastões de prata nas nanoestruturas Ag @ C estão bem cristalizados, confirmados por imagens HRTEM nas Fig. 2f e g, juntamente com o padrão de difração eletrônico inserido na Fig. 2g. Os planos Ag {111} cristalinos com um espaço de rede de 0,238 nm foram claramente inspecionados por imagem HRTEM (Fig. 2g).

Processo de formação estrutural do núcleo-casca Ag @ C com o tempo: a 1 h, b 3 h, c 6 h, d 12 h, e e 24 h; f Padrão ED com planos indexados e g HRTEM de Ag bastonetes de nanocompósitos Ag @ C com espaço de rede de 0,238 nm atribuído a {111} planos
De acordo com os experimentos atuais, dois mecanismos possíveis podem ser usados para a explicação da formação do Ag @ C. Primeiro, o precipitado AgBr foi formado por Br - íons (de CTAB) reagindo com Ag + íons (de AgNO 3 ) devido a um K muito pequeno sp (5,0 × 10 −13 ) à temperatura ambiente em solução aquosa, enquanto o AgBr não é termicamente estável e, portanto, forma Ag metálico sob o tratamento térmico, atuando como um centro de nucleação para a formação e crescimento da casca carbonácea. O CTAB também desempenhou outro papel na modificação da superfície, promovendo a formação de orientação de nanobastões ou nanofios de prata, porque as moléculas de CTAB são preferencialmente adsorvidas nos planos de cristal de eixo longo das partículas de Ag em crescimento [32]. Em segundo lugar, a glicose atuou como um agente redutor para reduzir o Ag + livre íons para Ag 0 átomos em alta temperatura (> 140 ° C) [33], por causa de seus ricos grupos −OH e aldeído. Em seguida, os núcleos de Ag recém-formados atuaram como um centro de nucleação para a adsorção de moléculas de glicose e, subsequentemente, polimerizaram como uma bainha carbonácea no esqueleto da prata [34,35,36,37].
Como uma confirmação adicional, a técnica de XRD foi usada para rastrear a formação de nanocabos de Ag @ C e bainha carbonácea. Medições de XRD dependentes do tempo foram empregadas para monitorar a alteração da composição dos intermediários e produtos finais das nanopartículas de Ag @ C. O processo geral consiste em duas etapas, dependendo da temperatura de reação. No primeiro estágio, glicose, AgNO 3 e CTAB foram usados como materiais de partida para a preparação de nanocabos de Ag @ C em alta temperatura (180 ° C). Na segunda etapa, a temperatura de reação do mesmo sistema foi diminuída para 60 ° C para o tratamento hidrotérmico. Os intervalos de tempo são de 4 e 3 h para os processos de crescimento e corrosão, respectivamente, conforme mostrado na Fig. 3c.
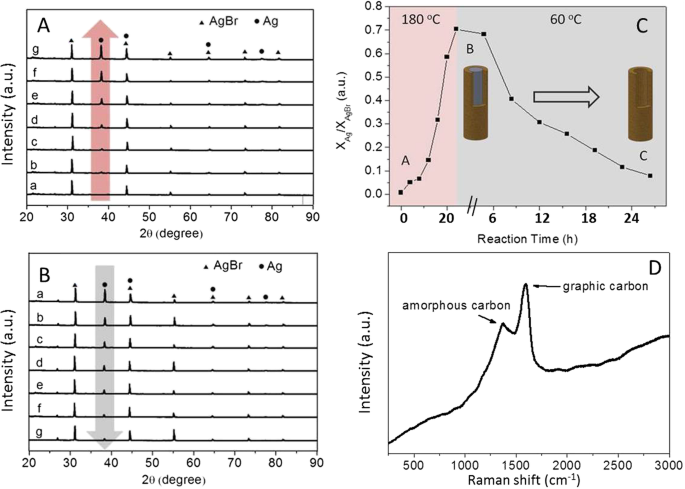
XRD ilustrando os processos de formação de nanobastões de Ag com casca carbonácea ( A ) e autodigestão gradual Ag ( B ), a formação e a curva de corrosão / evolução para o núcleo Ag ( C ), e espectro Raman para nanocabos Ag @ C carbonáceos ( D )
A Figura 3 mostra os padrões de XRD que a cor marrom inicialmente formada precipita e exibe dois picos de difração intensiva, indexados como AgBr cúbico (200) e (220) (cartão JCPDS nº 079-0149), respectivamente. No início, não foram observados picos de difração de Ag até que a reação prosseguisse por 8 h sob aquecimento, na qual o pico de Ag (111) metálico emergiu em ~ 38,1 ° (cartão JCPDS nº 087-0717). Um aumento gradual na intensidade do pico Ag (111) típico com o tempo indica que o Ag metálico se formou e atingiu sua intensidade máxima por volta de 24 h nas condições relatadas. Notou-se que alguns picos de difração, por exemplo, Ag (200) e AgBr (220), são sobrepostos no padrão de XRD de alguma forma. Curiosamente, quando a temperatura da reação foi ajustada para baixo para 60 ° C, o processo de corrosão dos núcleos de Ag ocorreu, confirmado pela intensidade gradualmente reduzida do pico de difração de Ag (111) típico localizado a ~ 38,1 °. Ao longo de dezenas de horas, a corrosão resultou no desaparecimento de núcleos de Ag, confirmado pelo pico de Ag (111) quase desaparecido. A análise do produto em função do tempo de reação foi conduzida, conforme mostrado na Fig. 3c. Isso indica que os núcleos de Ag podem quase ser removidos sob as condições térmicas, de acordo com as observações do TEM (Fig. 1c, d). Além disso, o espectro Raman (Fig. 3D) mostra a formação dos dois tipos de carbono:amorfo e gráfico neste sistema de reação.
Com base na análise de XRD acima, um equilíbrio termodinâmico pode existir entre a redução de Ag + íons pela glicose para formar núcleos de Ag e a oxidação de Ag por Br - íons, consistente com relatórios anteriores [38,39,40]. Por exemplo, Zhou et al. [39] demonstraram que os nanofios de Ag não foram formados até que a temperatura da reação estivesse acima de 140 ° C, confirmado pelo trabalho de Hussain [40]. Para a carbonização de carboidratos (por exemplo, glicose, sacarídeo), foi amplamente aceito que o produto carbonáceo pode ser sintetizado em temperaturas variando de 170 a 240 ° C [41, 42]. No entanto, a bainha carbonosa dos nanocabos é amorfa, diferente daqueles nanotubos de carbono ou grafeno obtidos sob tratamentos de recozimento de alta temperatura [1,2,3].
Especificamente em núcleos de ataque químico de Ag, as moléculas de oxigênio possuem um alto potencial de eletrodo de E 0 =+1,229 V vs. eletrodo de hidrogênio padrão (SHE), que é suficiente para oxidar Ag 0 para Ag + íons no sistema considerado. Isso pode ser apoiado por estudos anteriores, nos quais a corrosão oxidada na presença de íons haleto (Br - ) às nanopartículas de metal com formas regulares é anisotrópico em todas as direções [43, 44]. Xu et al. [43] relatou que o Cl - ou Br - íons preferidos para gravar (110) o plano de nanocristais de Ag. Esta seletividade pode ser atribuída à diferença nas energias livres de superfície dos planos de cristal de Ag (111, 110 e 100). Guo et al. [44] controlou o ponto de partida da corrosão seletiva do lado do nanorod, reduzindo a passivação da superfície do surfactante e, portanto, aumentando a reatividade nos planos laterais. A corrosão do núcleo Ag também foi confirmada por nossas observações experimentais para as nanopartículas Ag @ C sob condições de reação semelhantes, como mostrado na Fig. 4. Os pequenos pontos pretos (Fig. 4b) podem ser originados da decomposição de AgBr como pontos Ag sob um tratamento térmico. Um esquema diagramático pode ser usado para ilustrar o processo de síntese de Ag @ C e a formação de concha carbonácea oca (Fig. 4c).
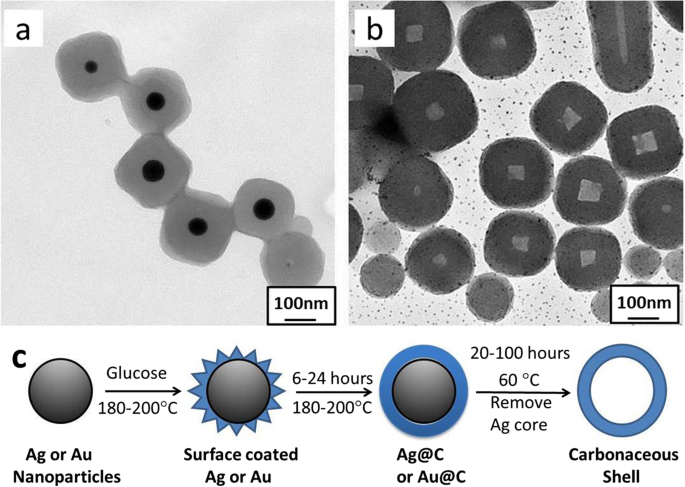
A corrosão de núcleo Ag de nanopartículas de camada de núcleo Ag @ C ( a ) para estrutura carbonácea oca ( b ) c Um esquema diagramático que ilustra a formação e autodigestão de nanoestruturas de Ag @ C
A propriedade UV-Vis correspondente dos nanocabos de núcleo-casca Ag @ C sintetizados e a estrutura carbonácea oca também foram medidos, como mostrado na Fig. 5. Isso também pode confirmar que o núcleo Ag foi gravado a partir de nanocabos. Os nanocabos Ag @ C mostram um pico de absorção intensivo localizado a ~ 382 nm (curva A na Fig. 5b), indicando a existência de prata metálica, que pode produzir forte ressonância de plasma de superfície [39]. Pelo contrário, os nanotubos carbonosos não mostram picos de absorção, como mostrado na curva C da Fig. 5b. Além disso, o espectro FT-IR (Fig. 5a) é principalmente para confirmar a formação de bainha carbonácea, rica em grupos funcionais como C =O, C – OH e OH [35].
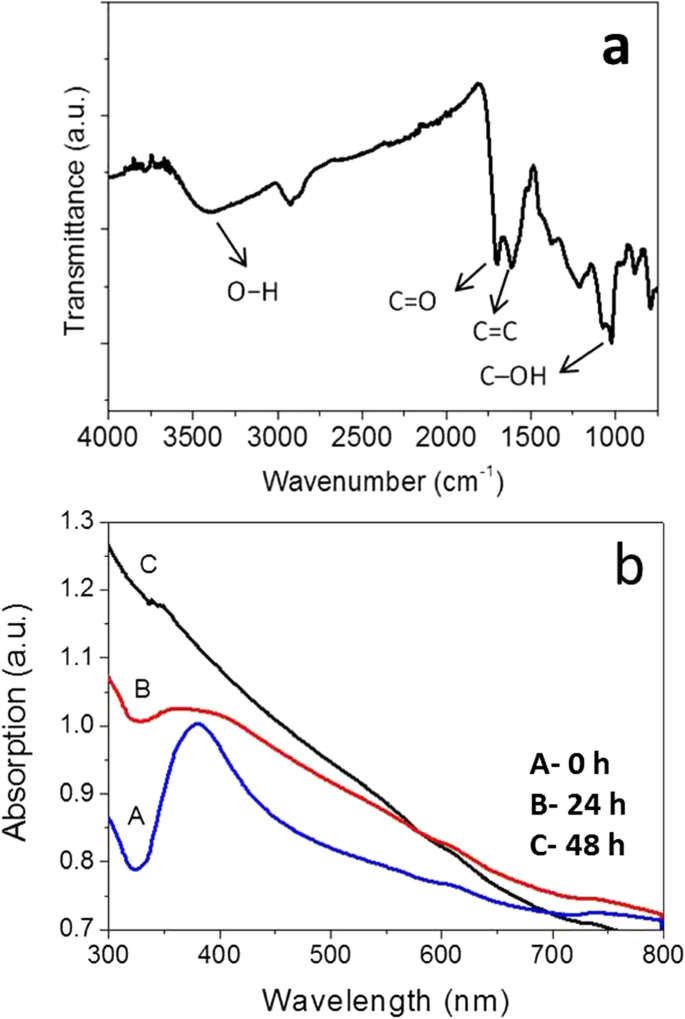
As propriedades ópticas de nanocompósitos Ag @ C e estruturas carbonáceas ocas medidas pelo espectro FT-IR ( a ) e espectros de UV-visível ( b )
A disponibilidade deste método de síntese foi validada para ser geral, não apenas para prata, mas também para outros metais nobres (por exemplo, ouro). Aqui, o AuCl 4 - íons foram selecionados e são mais fáceis de serem reduzidos pela glicose do que Ag + íons sob as mesmas condições, uma vez que o potencial eletroquímico padrão de AuCl 4 - / Au 0 par (0,99 V vs. SHE) é maior do que o de Ag + / Ag 0 par (0,799 V vs. SHE) [45, 46]. É importante ressaltar que o Au é mais estável do que o Ag e não é tóxico, o que é benéfico para o efeito fototérmico em aplicações biomédicas.
A Figura 6 mostra que as nanoestruturas carbonáceas Au @ C foram formadas com o tempo. Foi claramente observado que as nanopartículas de Au não esféricas (Fig. 6a) foram formadas dentro de 1 h nas condições relatadas, onde o AuCl 4 - os íons foram reduzidos pela glicose primeiro; enquanto isso, a bainha carbonosa foi formada em torno das nanopartículas de Au via polimerização de glicose a uma temperatura de 180 ° C por algumas horas, como mostrado na Fig. 6c-e. Com o aumento do tempo, a espessura da bainha carbonácea tornou-se mais espessa de alguns nanômetros (Fig. 6d) para dezenas de nanômetros (Fig. 6e), e a geometria da bainha está altamente relacionada à forma das próprias partículas de Au. O padrão de difração eletrônico de nanopartículas de núcleo-casca Ag @ C foi indexado como anéis de difração, correspondendo aos planos (100), (110), (111), (200) e (210) (Fig. 6f), respectivamente.

Estrutura de núcleo-casca Au @ C formada com o tempo: a 1 h, b 3 h, c 6 h, d 12 h, e e 24 h, respectivamente; f O padrão ED para partículas e os anéis de difração foram indexados como (100), (110), (111), (200) e (210); g uma única nanopartícula Au @ C, junto com sua imagem HRTEM ( h ) e o padrão ED indexado ( i ) mostrando em um único cristal
A rede cristalina de nanocristal de Au único (Fig. 6g) na estrutura núcleo-casca foi caracterizada pela técnica HRTEM. A Figura 6h mostra a imagem HRTEM em que o espaçamento da rede de ~ 0,238 nm pode ser atribuído ao plano Au (111) [47, 48]. Os pontos de difração eletrônica na Fig. 6i foram indexados como planos (100), (200) e (300), sugerindo o cristal único de Au formado nas condições relatadas.
Para confirmar ainda mais a estratégia de síntese proposta, nanobastões de Au também estavam disponíveis para revestimento carbonáceo como estruturas de núcleo-casca sob as condições hidrotérmicas relatadas. A Figura 7 mostra o processo de revestimento da bainha carbonosa em nanobastões de Au com razão de aspecto de ~ 3,7, como um estudo de caso. Com o aumento do tempo, a espessura da bainha carbonácea em nanobastões de Au tornou-se mais espessa de ~ 6 nm (Fig. 7b) a ~ 15 nm (Fig. 7c) e ~ 23 nm (Fig. 7d), e a bainha carbonácea torna-se esférica como após 24 h, não é afetado pelo comprimento dos nanobastões de Au (Fig. 7d). Um contraste significativo para bainha carbonácea (cor cinza) e nanobastões de ouro (cor preta) foi observado. A Figura 7e e f mostram as imagens HRTEM de nanorod de Au único antes e depois do revestimento carbonáceo. O espaçamento da rede de ~ 0,204 nm pode ser atribuído ao plano Au (200). A análise espectroscópica de dispersão de energia (EDS) para nanoestruturas de Au @ C e Ag @ C foi conduzida, conforme mostrado no Arquivo adicional 1:Figura S1. Verificou-se que a bainha carbonosa tem menor impacto na estrutura dos monocristais de ouro neste trabalho.

Estrutura do núcleo-casca Au @ C obtida com diferentes tempos de reação: a 0 h (nanobastões de ouro originais), b 4 h, c 12 h e d 24 h. e Imagem HRTEM para um único Au rod. f Imagem HRTEM para um único nanorod carbonáceo Au @ C
Propriedades ópticas
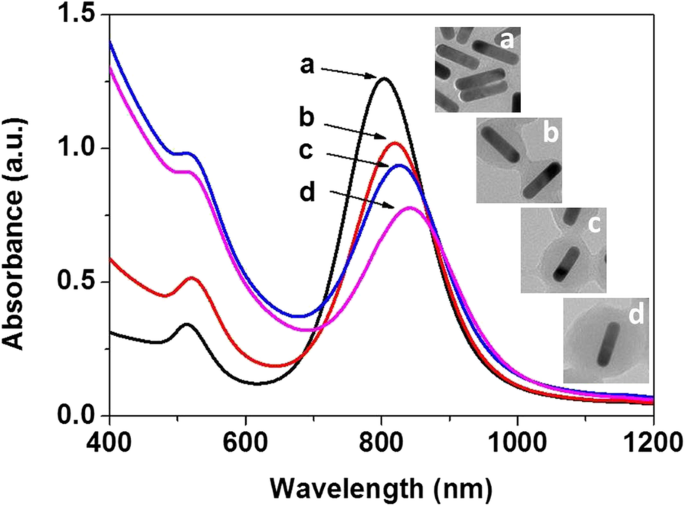
As propriedades ópticas correspondentes das nanoestruturas de Au @ C foram medidas por espectroscopia de UV-Vis, como mostrado na Fig. 8. Os espectros de absorção de UV-Vis para nanopartículas de Au @ C (Fig. 6a-e) desvio para o vermelho gradualmente de 560 nm ( a) para ~ 565 nm (b), ~ 580 nm (c), ~ 590 nm (d) e ~ 620 nm (e), respectivamente, para o pico de absorção intensa na Fig. 8A, com aumento da espessura da bainha (Fig. . 6c – d). Da mesma forma, para os nanobastões de Au @ C na Fig. 7a-d, a espessura da bainha carbonácea influencia a ressonância plasmônica de superfície intensa (modo longitudinal) dos nanobastões de Au e leva ao desvio do vermelho do original ~ 810 nm (a) para ~ 820 nm (b), ~ 826 nm (c) e ~ 848 nm (d), respectivamente, como mostrado na Fig. 8B, enquanto outra ressonância plasmônica de superfície (modo transversal) localizada em cerca de 518 nm é quase mantida na mesma posição. Ou seja, a bainha carbonácea realmente afeta a ressonância plasmônica de superfície dos nanocompósitos de Au @ C [36].
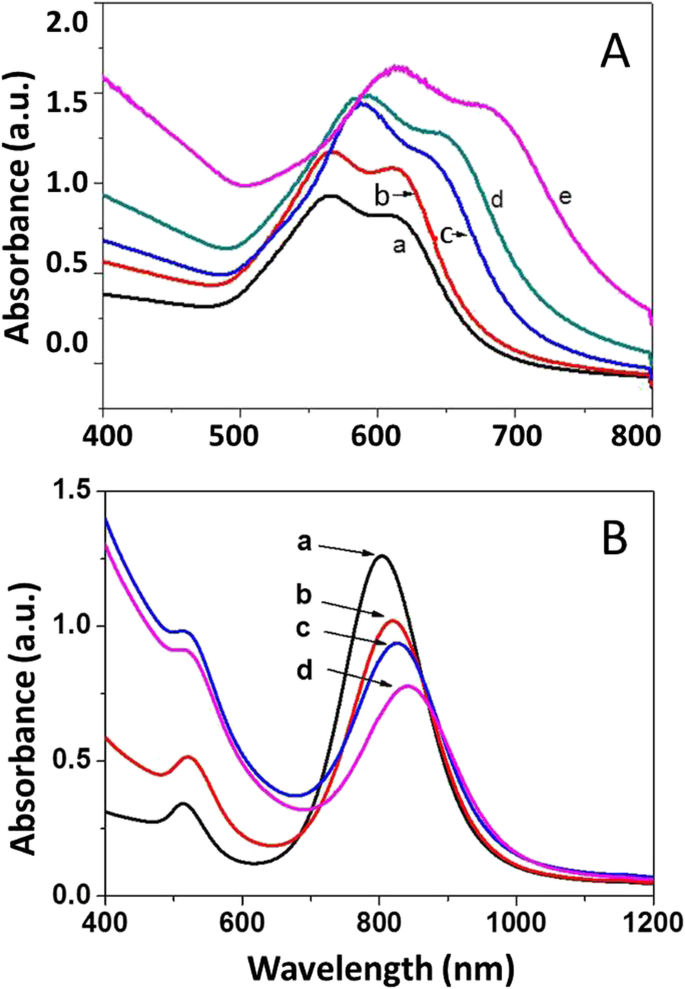
Espectros de UV-Vis para nanocompósitos de Au @ C: A Nanopartículas carbonáceas não esféricas de Au @ C obtidas em 1, 3, 6, 12 e 24 h, respectivamente. B Nanobastões carbonados Au @ C obtidos em 0, 4, 12 e 24 h, respectivamente
Como se sabe, Au é um metal nobre e suas nanopartículas podem apresentar intensa ressonância plasmônica de superfície (SPR), que pode ser influenciada por seu tamanho, morfologia e meio circundante. Ambas as nanopartículas não esféricas de Au @ C (Fig. 6a-e) e os nanobastões Au @ C (Fig. 7a-d) mostram SPR intenso com picos que se deslocam gradualmente para o vermelho nos espectros de UV-Vis (Fig. 8A, B ), provavelmente causado pelo aumento da espessura da casca carbonácea na superfície do Au. Isso pode ser apoiado por estudos anteriores [49,50,51,52]. Os autores relataram que a modificação da superfície de nanoestruturas fotônicas, como nanopartículas de ouro (Au), pode levar a novos fenômenos físicos, incluindo interações seletivas de luz-matéria e processos rápidos de transferência de energia [49,50,51]. Outros relataram que o componente de carbono também pode influenciar as interações luz-matéria para tais sistemas híbridos, por exemplo, reduzindo os efeitos de espalhamento. A presença de camadas multicamadas de grafeno (espessura sub-5 nm) influenciou as propriedades ópticas e a estabilidade (química e térmica) das nanopartículas de Au encapsuladas [52].
A propriedade térmica induzida por laser (fototérmica) das nanoestruturas carbonáceas de Au @ C foi examinada. Au @ C foi escolhido como um estudo de caso, porque Au é mais estável que Ag e não é tóxico em biossistemas. A Figura 9 mostra a propriedade fototérmica do Au @ C com diferentes espessuras de casca de cerca de 6 nm, 15 nm e 23 nm. A mudança de cor de azul (frio) para vermelho (quente), o que indica o aumento da temperatura dentro da suspensão de Au @ C. As mudanças de temperatura detalhadas foram registradas e mostradas na Fig. 9B. Dentro dos primeiros 600 s de irradiação, o aumento da temperatura é rápido para todas as quatro amostras. A temperatura assintoticamente se aproximou de um estado estacionário ao longo de 1200 s. Claramente, o revestimento de superfície pode reduzir a absorção de luz para nanocompósitos de Au @ C, exibindo temperatura mais baixa do que nanobastões de Au nus como ~ 10,6 ° C a ~ 9,3 ° C e ~ 8,1 ° C, respectivamente, correspondendo a ~ 6 nm, ~ 15 nm, e nanobastões de Au revestidos com camada carbonácea de ~ 23 nm. Uma tendência semelhante foi observada para Au @ SiO 2 nanocompósitos, onde um SiO mais espesso 2 shell levou a uma diminuição da temperatura, por exemplo, um SiO de 5 nm 2 shell resultou na redução de ~ 5 ° C em comparação com os nanobastões de Au nus [53].
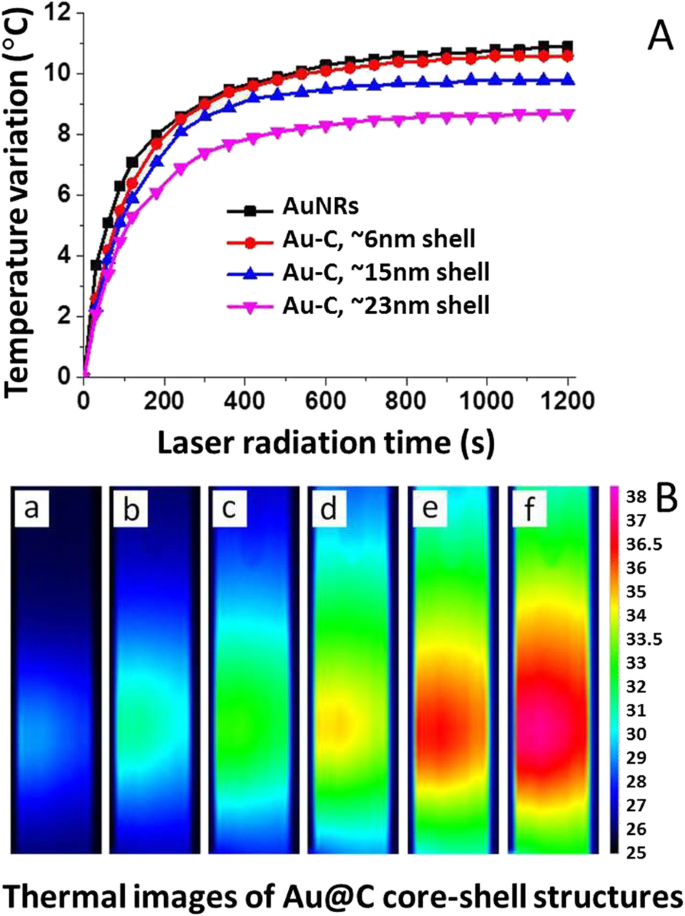
Teste de efeito fototérmico induzido por laser do nanocompósito carbonáceo Au @ C com densidade de potência do laser de 0,17 W / cm 2 . A A relação entre a temperatura e o tempo de irradiação para a solução aquosa de nanoestruturas de Au @ C com diferentes espessuras:nanobastões de Au nus sem revestimento carbonáceo, ~ 6 nm, ~ 15 nm e ~ 23 nm, em que a concentração de cada sistema foi ajustada para dar uma intensidade de extinção de 1,0 a 800 nm. B Imagens fototérmicas de nanoestruturas carbonáceas de Au @ C representam tempos diferentes em (a) 30, (b) 60, (c) 90, (d) 180, (e) 360 e (f) 840 segundos abaixo de 0,17 W / cm -2 irradiação
Embora a casca carbonácea tenha levado à diminuição da temperatura, ainda é atraente porque as nanopartículas de Au nuas não estão disponíveis para aplicações diretas em biossistemas devido à reação com biomoléculas (proteínas, aminas). Obviamente, os parâmetros concorrentes devem ser otimizados para uma aplicação específica em trabalhos futuros. Em geral, o invólucro de carbono deve ser bem controlado de modo a não torná-lo muito espesso para evitar uma redução significativa na absorção de luz, e também o invólucro não é muito fino para ser quebrado sob irradiação de luz. Obviamente, tanto os nanobastões de Au nus quanto os nanocompósitos de Au @ C podem levar a um aumento significativo de temperatura para uma faixa adequada (por exemplo, 37-47 ° C) por irradiação a laser, potencial para terapia fototérmica, embora associados a moléculas de drogas direcionadas. Regarding the relationship between optical and photothermal properties, both of them for Au@C nanostructures are dependent on SPR from noble metallic Au. The SPR, a unique phenomenon to plasmonic Au nanoparticles, leads to strong electromagnetic fields on the particle surface and consequently enhances all the radiative properties such as absorption and scattering. Additionally, the strongly absorbed light is converted to heat quickly via a series of nonradiative processes, if external light acts on the surface of Au nanoparticles. As noted, the photothermal property is mainly caused by NIR light but not visible light [54]. It is needed to be pointed out that more works are needed to be conducted in the near future, focusing on the optimization of pertinent parameters in concentration, pH, particle size, and surface modification for real biomedical applications of such Au@C carbonaceous nanocomposites.
Conclusões
This study developed a general strategy for the synthesis of noble metal carbonaceous nanocomposities (Au@C, Ag@C) with different morphologies by controlling hydrothermal conditions. A few interesting findings can be summarized as follows:
- i)
A high-temperature hydrothermal reaction (180–200 °C) could result in the formation of noble metal@C core-shell nanostructures, in which the glucose played a multiple role:reductant for metallic ions, shape modifier, and surface protection;
- ii)
A low-temperature (60–100 °C) hydrothermal reaction for the Ag@C core-shell system was beneficial for etching Ag to obtain hollow carbonaceous sheath, due to the etchant (Br − / O 2 ) This may open a simple path for fabricating hollow carbon nanostructures (e.g., tubes). However, the Au@C core-shell nanoparticles are quite stable under the same conditions;
- iii)
The generated Ag or Au cores are well crystallized, but the carbonaceous sheath is amorphous; e
- iv)
The rodlike Au@C nanocomposites were laser-induced to show photothermal effect, and the thickness of carbonaceous shell can tune the photothermal temperature, potential for biomedical applications.
Generally, this work may offer a simple but effective synthesis strategy, not only for noble metals but also for other metals, metal oxides, and inorganic materials to design and construct controllable carbonaceous nanostructures with potential applications in sensor, energy storage, catalysis, and biomedicine.
Disponibilidade de dados e materiais
The data and material provided in this study are available in Additional file 1.
Abreviações
- Ag@C:
-
Silver carbonaceous nanostructure
- Au@C:
-
Gold carbonaceous nanostructure
- CCD:
-
Dispositivo de carga acoplada
- CTAB:
-
Cetyltrimethylammonium bromide
- EDS:
-
Energy dispersion spectroscopy
- FT-IR:
-
Transformada de Fourier Infra-vermelho
- GO:
-
Óxido de grafeno
- HRTEM:
-
Microscopia eletrônica de transmissão de alta resolução
- PVA:
-
Álcool polivinílico)
- SEM:
-
Microscopia eletrônica de varredura
- SHE:
-
Eletrodo de hidrogênio padrão
- SPR:
-
Ressonância de plasmon de superfície
- TEM:
-
Microscopia eletrônica de transmissão
- UV-Vis:
-
Ultraviolet-visible spectrometer
- XRD:
-
Difração de raios X
Nanomateriais
- Estruturas de suporte para impressão 3D com metal - uma abordagem mais fácil
- Nanofibras de polímero por eletrofiação decoradas com nanopartículas de metal nobre para detecção química
- Fabricação e propriedade fotocatalítica de novos nanocompósitos SrTiO3 / Bi5O7I
- Uma nova microestrutura de cluster de nanocônios com propriedades anti-reflexo e superhidrofóbicas para dispositivos fotovoltaicos
- Fabricação controlada por morfologia de nanoestruturas de prata dendríticas em grande escala para aplicações de catálise e SERS
- A importância dos modelos CAD para projetos de fabricação de metais
- Uma visão geral para iniciantes:o que é fabricação de metal?
- 4 equívocos comuns sobre preços para fabricação de metal
- Por que a rebarbação é importante para projetos de fabricação de metal?
- Que tipo de fabricação de chapas metálicas é ideal para mim?



