Tecnologias de captura e armazenamento de carbono
Tecnologias de captura e armazenamento de carbono
A captura e armazenamento de carbono também chamado de sequestro (CCS) envolve a captura, transporte, injeção e contenção de CO2 (dióxido de carbono) em estruturas geológicas como reservatórios de petróleo e gás esgotados, aquíferos salinos onshore e offshore localizados nas profundezas da crosta terrestre, cavernas de sal ou leitos de carvão inexploráveis. É uma abordagem para aumentar a produção das operações de petróleo e gás existentes, bem como um meio para reduzir as emissões de gases de efeito estufa (GEE).
A CCS fornece uma alternativa adicional na utilização de energia baseada em combustível fóssil, ao mesmo tempo em que fornece um tempo de transição adicional para que os sistemas de energia avancem para combustíveis com carbono (C) reduzido ou zero C, como as energias renováveis. Há uma série de benefícios econômicos e sociais da CCS, como (i) redução das emissões de CO2 na atmosfera, potencialmente mitigando mudanças climáticas perigosas, (ii) inovação, acesso a tecnologias de ponta, criação de empregos e desenvolvimento econômico contínuo e mais sustentável, (iii) fluxo de receita secundária, pois as emissões de GEE que são capturadas e armazenadas podem ser convertidas em uma mercadoria comercializável que pode ser vendida no mercado internacional, (iv) redução da poluição do ar, pois poluentes potencialmente nocivos têm a ser removido para acomodar a captura de CO2 e oportunidade para recuperação aprimorada de petróleo e gás.
Existem vários desafios para a implantação do CCS. Alguns dos desafios para o CCS incluem (i) reduzir o custo de captura e ampliar os processos de captura, (ii) identificar o impacto ambiental da captura, (iii) determinar as implicações do acúmulo de pressão em uma formação de armazenamento, (iv) ) determinar para onde a água deslocada vai em uma injeção em grande escala e qual é o risco para a água subterrânea, (v) como prever com segurança o tamanho da pluma de CO2 e para onde ela migra, (vi) como ganhar confiança na seleção do local, (vii) desenvolver estratégias de monitoramento econômicas e limites de detecção, (viii) envolver as indústrias de finanças e seguros, (ix) maior certeza regulatória e política em todos os níveis de governo, (x) treinar uma força de trabalho para implantação em larga escala e (xi) melhorar a conscientização e aceitação do público.
As tecnologias CCS podem ser aplicadas aos processos com emissões em larga escala, incluindo geração de energia a carvão e gás, processamento de gás natural e produção de fertilizantes, bem como a fabricação de materiais industriais como ferro e aço, cimento e papel e celulose etc. A aplicação de tecnologias CCS a esses processos pode desempenhar um papel importante na redução das emissões de GEE. As tecnologias de separação e captura de carbono estão em operação em larga escala nas indústrias de gás natural e fertilizantes há décadas. As tecnologias envolvidas em um sistema CCS têm quatro componentes, a saber (i) captura, (ii) transporte, (iii) injeção e (iv) monitoramento.
A captura é a separação do CO2 de um fluxo de efluente e sua compressão para um estado líquido ou supercrítico. Na maioria dos casos, hoje, a concentração de CO2 resultante é superior a 99%, embora concentrações mais baixas possam ser aceitáveis. A captura é normalmente necessária para poder transportar e armazenar o CO2 economicamente.
O transporte consiste no transporte do CO2 de sua fonte até o reservatório de armazenamento. O CO2 é seco e geralmente comprimido antes de ser transportado para armazenamento. A compressão torna o transporte do gás mais eficiente. O CO2 é usado comercialmente em várias indústrias, principalmente na indústria de bebidas, e tem sido transportado em larga escala para uso na recuperação de óleo de reservatórios (recuperação aprimorada de óleo). Embora o transporte por caminhão, trem e navio seja possível, o transporte de grandes quantidades de CO2 é mais economicamente possível com um duto. É necessário construir uma grande infraestrutura de pipeline para implementar o CCS em larga escala, e isso apresenta desafios.
A injeção consiste na deposição de CO2 no reservatório de armazenamento. Os reservatórios de armazenamento subterrâneo dependem das formações geológicas. A segurança do armazenamento de CO2 é de primordial importância. Os riscos locais de armazenamento de CO2 incluem (i) vazamento de CO2 do local de armazenamento, (ii) alteração da química do solo e da água potável e (iii) deslocamento de fluidos potencialmente perigosos que podem estar no reservatório onde o CO2 é armazenado. Os reservatórios potenciais incluem o oceano profundo, sedimentos oceânicos ou mineralização (conversão de CO2 em minerais). Embora seja possível algum uso comercial de CO2, a quantidade que pode ser usada em comparação com a quantidade de CO2 que é emitida é muito pequena.
Uma vez que o CO2 é injetado, o local de armazenamento deve ser monitorado para mostrar que o CO2 permanece no reservatório. O CO2 não é tóxico nem inflamável, portanto, representa apenas um risco mínimo para o meio ambiente, a saúde e a segurança. O principal objetivo do monitoramento é garantir que a operação de sequestro seja eficaz, o que significa que quase todo o CO2 fica fora da atmosfera por séculos. O programa de monitoramento começa antes da injeção para estabelecer dados de linha de base. O monitoramento durante a fase operacional é para o registro do comportamento dinâmico do CO2 à medida que é injetado e dentro do reservatório. Após o término da injeção, o programa de monitoramento deve ser projetado para garantir que o armazenamento de CO2 atenda às condições ambientais e de segurança exigidas. Um programa de monitoramento abrange três domínios de monitoramento, a saber (i) o domínio subsuperficial (o reservatório), (ii) o domínio próximo à superfície (zonas rasas e solo) e (iii) o domínio atmosférico, incluindo poços, falhas e outras feições geológicas.
Tecnologias de captura de CO2
O CO2 pode ser capturado de grandes fontes de emissão estacionárias, como instalações de produção de gás natural (onde o CO2 já é separado de outros gases, como parte do processo), usinas de energia movidas a combustível fóssil, siderúrgicas, fábricas de cimento e algumas fábricas de produtos químicos . Ao contrário dos outros dois componentes do CCS, transporte e armazenamento geológico, o primeiro componente do CCS, ou seja, a captura de CO2 é quase inteiramente dependente da tecnologia e é o passo mais caro. A tecnologia para capturar CO2 dessas fontes está sendo adaptada da tecnologia de separação de CO2 atualmente usada em indústrias como a indústria de gás natural e produção de amônia (NH3) e também da tecnologia usada na indústria de separação de ar. Novas tecnologias também estão sendo desenvolvidas.
As principais tecnologias de separação para capturar CO2 atualmente são (i) usar um solvente líquido para absorver o CO2 (absorção), (ii) usar materiais sólidos para atrair o CO2 para a superfície, onde ele se separa de outros gases (adsorção) e (iii) usar membranas para separar o CO2 dos outros gases. Outras tecnologias incluem tecnologia de looping químico (um óxido metálico reage com o combustível, criando partículas metálicas, CO2 e vapor de água), processos de separação de baixa temperatura ou criogênicos (que dependem de diferentes temperaturas de mudança de fase para vários gases para separá-los) e sólidos regeneráveis secos processos.
As principais tecnologias concorrentes para captura de CO2 do uso de combustível fóssil são (i) captura pós-combustão (PCC) do gás de combustão de plantas baseadas em combustão, (ii) captura pré-combustão do gás de síntese em plantas baseadas em gaseificação e (iii) oxi combustão através da combustão direta de combustível com oxigênio. A maioria dos processos de combustão atuais usa ar, e o gás de combustão resultante normalmente contém baixas concentrações de CO2 (menos de 20%) e, portanto, são mais adequados para tecnologias de captura pós-combustão
Tecnologias de captura pós-combustão
A captura pós-combustão pode ser considerada uma forma de limpeza dos gases de combustão. O processo é adicionado ao back-end da planta, após os demais sistemas de controle de poluição. A integração do calor com a planta é necessária para que seja rentável.
O Electric Power Research Institute (EPRI) determinou em 2009 que existem mais de 50 conceitos de captura de CO2 pós-combustão em desenvolvimento que podem ser agrupados em vários tipos de processos físico-químicos. Esses grupos de tipo de processo são (i) absorção química, (ii) adsorção, (iii) membranas, (iv) biológico e (v) outros. Cada um desses diferentes grupos tem diferentes vantagens e desvantagens, bem como aplicabilidade em diferentes situações. Há desenvolvimentos consideráveis em relação aos dois primeiros grupos.
Processo de absorção química - Envolve uma ou mais reações químicas reversíveis entre CO2 e uma solução aquosa de um absorvente, como solvente à base de monoetanolamina (MEA) e aminas de alto desempenho (metildietanolamina ativada, aMDEA) etc. Ao aquecer o produto, a ligação entre o absorvente e o CO2 pode ser quebrada, produzindo um fluxo enriquecido em CO2. O processo de absorção química para separar o CO2 do gás de combustão é emprestado da indústria de processamento de gás. Processos à base de amina estão sendo usados comercialmente para a remoção de impurezas de gás ácido (CO2 e H2S) de fluxos de gás de processo. É, portanto, uma tecnologia comprovada e bem conhecida.
A fórmula de mono-etanol-amina é H2NCH2CH2OH. Amina é um grupo de compostos orgânicos, que podem ser considerados derivados de amônia (NH3) pela substituição de um ou mais átomos de H2 por radicais orgânicos. Os grupos substitutos (R) podem ser alquil, aril ou aralikl. Quando o (R) é um alquil, a amina é chamada de alcanolamina. Em geral, pode-se considerar que um grupo hidroxila serve para reduzir a pressão de vapor e aumentar a solubilidade em água, enquanto o grupo amino fornece a alcalinidade necessária em solução aquosa para absorver os gases ácidos. As acanolaminas removem o CO2 dos fluxos de gás residual por meio de uma reação exotérmica de CO2 com a funcionalidade amina da alcanolamina. As aminas de interesse comercial para capturar CO2 são solúveis em água.
As aminas são classificadas de acordo com o número de átomos de H2 de amônia que foram substituídos por radicais como (i) amina primária (RNH2) onde um átomo de H2 foi substituído, (ii) amina secundária (R2NH) onde dois átomos de H2 foram substituídos. substituído, e (iii) amina terciária (R3N) onde todos os três átomos de H2 foram substituídos.
As aminas primárias incluem monoetanolamina (MEA) e diglicolamina (DGA). MEA tem sido o solvente tradicional de escolha para absorção de CO2 e remoção de gases ácidos em geral. MEA é a menos cara das alcanolaminas. Sua cinética de reação é rápida e funciona bem em baixa pressão e baixa concentração de CO2. No entanto, existem várias desvantagens.
Primeiro, ele tem um alto calor de reação com o CO2, o que significa que um alto nível de energia deve ser fornecido na etapa de regeneração. Em segundo lugar, a absortividade de MEA com CO2 não é alta. No caso de alcanolaminas primárias e secundárias, a formação de carbamato (RNHCOO-) é a principal reação. A equação para a reação é CO2 + 2RNH2 =RNHCOO- + RNH3+. Nesta reação, dois mols de MEA devem ser usados para capturar um mol de CO2. Terceiro, a capacidade total de absorção superior do MEA não é alcançada na prática devido a problemas de corrosão. O efeito de corrosão é devido ao CO2 dissolvido e varia de acordo com as aminas usadas.
A concentração de MEA na fase aquosa na presença de O2 é limitada a 20% em peso. Além disso, MEA tem a pressão de vapor mais alta de qualquer uma das alcanolaminas e um alto arraste de solvente pode ocorrer durante a remoção de CO2 da corrente de gás e na etapa de regeneração. Para reduzir as perdas de solvente, geralmente é necessária uma lavagem com água da corrente de gás purificado. Além disso, o MEA reage irreversivelmente com impurezas menores, como COS e CS2 resultando na degradação do solvente. A formação de espuma do líquido absorvente MEA devido ao acúmulo de impurezas também pode ser uma preocupação.
Para os atuais sistemas absorvedores de MEA, as taxas de adsorção e dessorção são razoavelmente altas, portanto, uma boa cinética de reação. No entanto, a embalagem no absorvedor (contatores, para facilitar a transferência de massa eficiente) representa um custo significativo e seu consumo de energia também é significativo para a captura de CO2 dos gases de combustão. Além disso, a temperatura de decapagem não deve ser muito alta (cerca de 150 graus C). Caso contrário, pode ocorrer a dimerização do carbamato, deteriorando a capacidade de absorção do MEA.
As aminas secundárias incluem dietanolamina (DEA), diisopropilamina (DIPA). As aminas secundárias têm vantagens sobre as aminas primárias. Seu calor de reação com o CO2 é menor (360 calorias/grama) versus 455 calorias/grama) para aminas primárias. Isso significa que as aminas secundárias requerem menos calor na etapa de regeneração do que as aminas primárias. No entanto, tem todos os outros problemas das aminas primárias.
As aminas terciárias incluem trietanolamina (TEA) e metil-dietanolamina (MDEA). As aminas terciárias reagem mais lentamente com o CO2 do que as aminas primárias e secundárias, portanto, exigem maior taxa de circulação do líquido para remover o CO2 em comparação com as aminas primárias e secundárias. Isso pode ser melhorado através do uso de promotores. Uma grande vantagem das aminas terciárias é sua menor necessidade de calor para liberação de CO2 do solvente contendo CO2. As aminas terciárias apresentam menor tendência a formar produtos de degradação em uso do que as aminas primárias e secundárias, e são mais facilmente regeneradas. Além disso, as aminas terciárias têm taxas de corrosão mais baixas em comparação com as aminas primárias e secundárias. A principal desvantagem é que sua taxa de reação é muito lenta.
Um fluxograma típico do processo de absorção química para recuperação de CO2 do gás de combustão é mostrado na Figura 1. Durante a operação de absorção de amina, o fluxo de gás residual e a solução de amina líquida são contatados por fluxo em contracorrente em uma torre de absorção (ou absorvedor).
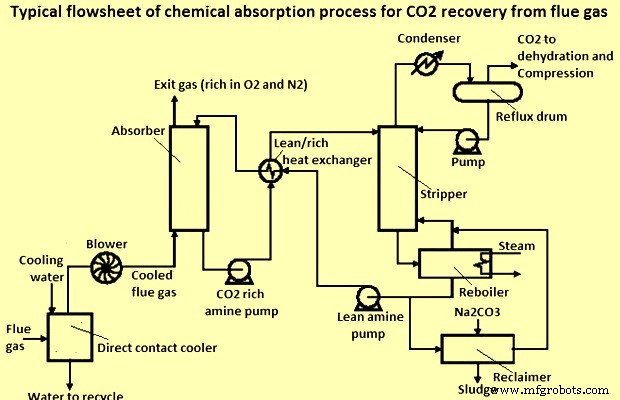
Fig 1 Fluxograma típico do processo de absorção química para recuperação de CO2 do gás de combustão
O gás de combustão que sai da chaminé é quente (cerca de 240 graus C) e à pressão atmosférica. O gás de combustão que entra no absorvedor em altas temperaturas pode levar à degradação do solvente e diminuição da eficiência de absorção. O gás de combustão deve ser resfriado até um ponto de orvalho da água de 50 graus C, entrando no absorvedor. O absorvedor geralmente opera a menos de 50 graus C. Isso é conseguido pulverizando água de resfriamento em um resfriador de contato direto.
O CO2 no gás de combustão é resfriado antes de entrar no absorvedor, onde reage com o carbonato de amônio para formar bicarbonato de amônio. O NH3 é liberado como um gás da solução solvente quando o CO2 é absorvido e a temperatura é mantida baixa para minimizar isso. Os gases que saem do absorvedor passam por uma lavagem com água para remover a amônia. O bicarbonato de amônio é aquecido no regenerador, separando o CO2. O solvente de carbonato de amônio é devolvido ao absorvedor. Água e NH3 são removidos do fluxo de CO2 que sai da coluna de stripper.
Um soprador é instalado para dar ao gás de combustão pressão suficiente para que ele passe pelo sistema de absorção-dessorção. O gás residual a ser purificado do CO2 normalmente entra no absorvedor na parte inferior, flui para cima e sai na parte superior, enquanto o solvente entra na parte superior do absorvedor, flui para baixo (em contato com o gás) e emerge na parte inferior. A diluição da amina circulante com água é realizada para reduzir a viscosidade do fluido circulante. Um fluido de viscosidade mais alta requer mais potência para bombear e fornecer circulação. A solução de amina líquida contendo o gás absorvido flui então para uma unidade de regeneração (stripper) onde é aquecida e os gases ácidos são liberados. A regeneração do solvente pode ser realizada a baixas pressões para aumentar a dessorção de CO2 do líquido. Alguma solução de amina é tipicamente transportada na corrente de gás ácido da etapa de regeneração e a solução de amina é recuperada usando um condensador, a fim de evitar perdas excessivas de solvente. A solução de amina pobre quente flui então através de um permutador de calor onde é contactada com a solução de amina rica da torre de contacto e a partir daí a solução de amina pobre é devolvida à torre de contacto de gás, isto é, absorvedor.
No caso do processo depurador de aminas, com aminas de alto desempenho (metildietanolamina ativada, aMDEA), o processo completo (aminas e compressão a 110 kg/sq cm de pressão) requer cerca de 1,6 toneladas de vapor de baixa pressão e 160 kWh de potência por tonelada de CO2 capturado.
Existem algumas limitações dos processos baseados em aminas e que resultaram em avanços tecnológicos. A tecnologia de depuração de amina no passado se concentrou na remoção de H2S (sulfeto de hidrogênio) para o setor de gás natural. No entanto, os requisitos são diferentes para a recuperação de CO2 do gás de combustão. Um desafio é a baixa pressão do gás de combustão para absorção de CO2. Além disso, impurezas no gás de combustão, como O2, óxidos de enxofre (SO2,SO3), óxidos de nitrogênio e material particulado, criam desafios especiais durante o processo de separação.
Em resumo, a recuperação de CO2 do gás de combustão requer uma quantidade significativa de processamento de pré-tratamento para evitar qualquer interferência na etapa de absorção do solvente. Isso aumenta o custo da captura de CO2. No entanto, melhorias significativas podem ser feitas no processo de absorção de solventes em termos de otimização das composições das aminas absorventes e dos contatores gás-líquido, a fim de gerenciar isso.
Absorção física – Para absorção física, o CO2 é fisicamente absorvido em um solvente de acordo com a Lei de Henry. A capacidade de absorção de solventes orgânicos ou inorgânicos para CO2 aumenta com o aumento da pressão e com a diminuição da temperatura. A absorção de CO2 ocorre em altas pressões parciais de CO2 e baixas temperaturas. Os solventes são então regenerados por aquecimento ou redução de pressão. A vantagem deste método é que requer relativamente pouca energia; mas o CO2 deve estar em alta pressão parcial.
Adsorção física sólida – Um processo de adsorção consiste em duas etapas principais, a saber (i) adsorção e (ii) dessorção. A viabilidade técnica de um processo é ditada pela etapa de adsorção, enquanto a etapa de dessorção controla sua viabilidade econômica. A adsorção requer uma forte afinidade entre um adsorvente e o componente a ser removido de uma mistura gasosa (neste caso, CO2). No entanto, quanto mais forte a afinidade, mais difícil é dessorver o CO2 e maior a energia consumida na regeneração do adsorvente para reutilização no próximo ciclo. Portanto, a etapa de dessorção deve ser cuidadosamente equilibrada em relação à etapa de adsorção para que o processo geral seja bem-sucedido.
Os processos de adsorção são bastante atrativos para o mecanismo de captura de CO2, apesar de suas desvantagens como baixa capacidade de adsorventes e influência de contaminantes como SO2 e H2O no processo de separação. Há também vantagens deste processo como disponibilidade, flexibilidade, operação totalmente automatizada do processo e produção de produto de alta pureza. A separação pode ser realizada por adsorção de oscilação de pressão (PSA) (Fig 2), adsorção de oscilação de pressão de vácuo (VPSA), adsorção de oscilação de temperatura (TSA), adsorção de oscilação de pressão-temperatura (PTSA) ou adsorção de oscilação elétrica (ESA) processos. Os leitos da instalação são preenchidos com adsorventes sólidos. A seletividade depende da diferença no equilíbrio de adsorção ou taxas de adsorção e da eficácia (concentração e recuperação) tem importância na configuração do ciclo, tempo de adsorção, pressão de adsorção e dessorção, temperatura durante o processo e tipo de adsorvente aplicado.
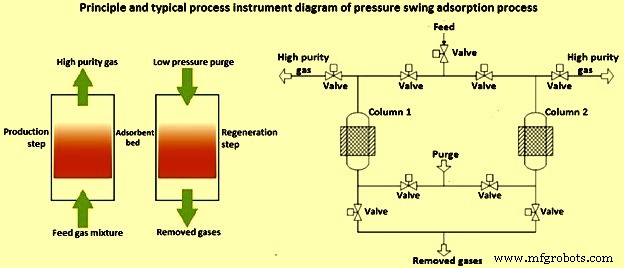
Fig 2 Processo de adsorção de oscilação de pressão
A principal vantagem da adsorção física sobre a absorção química é sua operação e regeneração simples e energeticamente eficientes, que podem ser alcançadas com um ciclo de oscilação de pressão ou de oscilação de temperatura (uma oscilação na pressão ou temperatura à medida que o processo passa por um ciclo de absorção-dessorção para conseguir a separação). A adsorção de oscilação de pressão é um processo comercial para separação de H2 de misturas de H2 e CO2 na produção de H2.
Houve avanços significativos no desenvolvimento de adsorventes para remoção de CO2 de gases de combustão. O material de adsorção primário utilizado tem sido zeólitos. Os zeólitos são mais eficazes para a separação de CO2 de espécies que são menos polares que o CO2, portanto, a presença de água e SOx em fluxos de gases de combustão representa um problema.
Novos adsorventes foram considerados e desenvolvidos, como carbonos, silicoaluminatos mesoporosos (por exemplo, estruturas de imidazolato zeolítico, ZIFs) e estruturas orgânicas metálicas (MOFs). Os adsorventes à base de carbono têm o potencial de serem regenerados pela aplicação de tensão elétrica (ESA). Novos materiais que estão sendo investigados incluem derivados de hidróxidos duplos em camadas (LDHs e LDOs). Outros avanços incluem a funcionalização dos poros do material adsorvente pela incorporação de aminas para aumentar a carga de CO2. Nesse caso, o CO2 é separado por meio de um processo de quimissorção.
Novos processos estão sendo desenvolvidos para lidar com fluxos de gases de combustão de alta umidade e impurezas. Estes incluem leitos adsorventes multicamadas. Os leitos multicamadas permitem o uso de adsorventes com alta seletividade de CO2, mas se degradam significativamente na presença de água.
Tecnologias de captura de pré-combustão
As tecnologias de captura de pré-combustão envolvem a remoção de poluentes e CO2 no tratamento a montante de combustíveis fósseis antes de sua combustão para recuperação de calor (via vapor) ou produção de energia elétrica ou H2.
Uma desvantagem da captura de C pós-combustão é a baixa concentração de CO2 nos gases de combustão, o que leva a uma penalidade de energia relativamente alta e alto custo de captura de C. A pré-combustão se esforça para reduzir essas penalidades descarbonizando o fluxo de processo rico em CO2 antes da combustão do combustível rico em H2 restante. Para alcançar a descarbonização de combustíveis de hidrocarbonetos, eles são primeiro convertidos em um syngas através da gaseificação de um combustível com O2 (ou ar). O gás de síntese é uma mistura de CO (monóxido de carbono), H2, CO2 e água, dependendo do processo de conversão e do combustível e outros componentes.
O gás de síntese é um produto intermediário, que pode então ser convertido para produzir (i) H2, (ii) energia elétrica integrada, usando a reação de deslocamento água-gás, ou (iii) geração poli, onde uma variedade de produtos de energia pode estar lá, incluindo energia, calor, H2 e synfuels e outros produtos químicos. O processo envolvido com cada um desses produtos de energia final é descrito abaixo.
Produção de H2 por reforma de metano – O método mais utilizado hoje para a produção de H2 é a reforma catalítica a vapor do metano (CH4). A reação de reforma da conversão de CH4 e H2 O para CO e H2 é endotérmico. A reação é realizada sobre um catalisador de Ni (níquel) em alta temperatura em um forno de queima direta alimentado por CH4. O catalisador é envenenado por S (enxofre), então qualquer S presente na alimentação deve ser removido. O gás de síntese, por sua vez, passa por um conversor catalítico de deslocamento de água, onde o CO reage exotermicamente com vapor para produzir H2 e um subproduto de CO2 . Esses subprodutos são então removidos do sistema. O gás de exaustão ainda contém um poder calorífico significativo, por isso é queimado para produzir vapor ou energia elétrica.
Gaseificação de carvão – As tecnologias de gaseificação podem produzir um fluxo de gás com alto teor de CO2 e pressão moderada. O carvão de alimentação é gaseificado em O2 (ou ar) para produzir um gás de síntese. O gás de síntese é resfriado a 200 graus C em resfriadores de gás de síntese gerando vapores de alta e baixa temperatura. Ele é então deslocado ainda mais em um reator de deslocamento de água e gás de baixa temperatura. O reator de deslocamento de gás de água é um reator catalítico em que o CO reage com vapor para produzir mais H2 e CO2. O gás é então resfriado a 35°C em preparação para a remoção do gás ácido. Aproximadamente 99% do H2S é removido do gás de síntese por absorção física e convertido em enxofre elementar. Uma unidade PSA pode ser usada para separar 85% do H2 do gás de síntese livre de S. O H2 sai em torno de 60 kg/sq cm e alta pureza (superior a 99,99%). O CO2 pode ser removido do gás de síntese a jusante do sistema de captura S. O gás de purga PSA é comprimido e queimado em um ciclo combinado de turbina a gás para produzir energia elétrica.
As tecnologias de gaseificação estão bem estabelecidas para a produção de H2. Plantas comerciais foram construídas e operadas com sucesso para produzir H2 para aplicações de refinaria e fabricação de produtos químicos (por exemplo, produção de NH3 e metanol) com base em uma variedade de matérias-primas de hidrocarbonetos.
Energia elétrica integrada – O gás de síntese com alto teor de H2 pode ser queimado em um turboexpansor para produzir energia elétrica em uma configuração de ciclo combinado. Se o gás de síntese for produzido usando gaseificação, o esquema é chamado de ciclo combinado de gaseificação integrada (IGCC). O IGCC permite que a eletricidade seja gerada com alta eficiência. Como o gás deve ser limpo para evitar danos à turbina a gás, o IGCC tem emissões ambientais muito baixas. Além disso, as plantas do IGCC usam menos água. Atualmente, o IGCC está sendo usado comercialmente em muitas plantas em todo o mundo por gaseificação de resíduos de petróleo para fornecer energia, H2 e vapor.
Os três principais tipos de gaseificadores de carvão são (i) leito móvel, (ii) leito fluidizado e (iii) fluxo arrastado. No entanto, a maioria dos gaseificadores considerados para captura de CO2 atualmente são baseados em gaseificadores de fluxo arrastado. A aplicação comercial do IGCC baseado em carvão tem sido limitada por seus custos relativamente altos, baixa disponibilidade de usinas e concorrência de usinas de geração de carvão pulverizado. O custo da captura de CO2 no IGCC depende fortemente do tipo de gaseificador.
Conforme mencionado acima, para permitir que o CO2 seja capturado, o gás combustível deve ser alimentado a um reator de deslocamento catalítico, onde a maior parte do CO é reagida pelo vapor para dar H2 e CO. Para o gaseificador de alimentação de pasta, vapor suficiente já está presente no o gás combustível da evaporação da água da pasta de carvão e do resfriamento de têmpera do gás do produto gaseificador. No entanto, para o gaseificador de alimentação seca, o vapor deve ser retirado do ciclo de vapor e adicionado à alimentação de gás combustível para o conversor de deslocamento.
Deve-se notar que o IGCC é mais caro para a geração de eletricidade do que a combustão convencional de carvão pulverizado, sem captura de CO2 em ambos os casos.
Poligeração – Syngas é um bom bloco de construção, pois pode ser usado para produzir uma ampla gama de produtos energéticos. A maior flexibilidade oferecida é a poligeração, na qual os 'syngas' podem produzir vapor, energia elétrica, H2 e produtos químicos (como metanol, líquidos de Fischer-Tropsch) em um único complexo de plantas.
Várias tecnologias de separação diferentes, incluindo tecnologias de solvente, adsorvente e membrana, podem ser aplicadas para separar o CO2 dos produtos da gaseificação.
Absorção – A tecnologia convencional é a absorção física em um processo de duas etapas que remove o H2S e depois captura o CO2. No entanto, o gás precisa ser resfriado após a reação de deslocamento água-gás e, em seguida, reaquecido antes de gerar energia. Isso reduz a eficiência e aumenta o custo.
Adsorção – Adsorventes podem ser usados para separar o CO2 dos fluxos de gases de combustão pós-combustão a jusante da reação de deslocamento de gás de água. Tanto a adsorção de oscilação de temperatura (TSA) quanto a adsorção de oscilação de vácuo/pressão (VSA/PSA) podem ser usadas para recuperar o CO2 do adsorvente. O CO2 está em baixa pressão quando recuperado via VSA/PSA e precisa ser compactado para armazenamento.
Membranas – Sistemas avançados de separação de gases baseados em membranas estão sendo desenvolvidos para combinar a reação de deslocamento de gás e a separação de H2 em uma única etapa. Os sistemas baseados em membrana empregam um reator de membrana de separação H2 de deslocamento de gás de água (HSMR) para deslocar o gás de síntese e extrair o H2. A temperatura máxima de cerca de 475 graus C garante uma cinética química rápida e um bom desempenho de equilíbrio de deslocamento de água e gás é obtido pela remoção contínua do produto H2.
Existem três classes principais de membranas inorgânicas permeáveis a H2, a saber (i) peneira molecular cerâmica, (ii) transporte de íons cerâmicos densos e (iii) metal denso.
Vantagens e desvantagens da pré-combustão (descarbonização) – As vantagens da pré-combustão (descarbonização) são (i) a separação de CO2 por absorção de solvente ou PSA é comprovada. O gás de exaustão vem a pressões elevadas e altas concentrações de CO2 reduzem significativamente os custos de captura, (ii) os custos de compressão são menores do que as fontes de pós-combustão, pois o CO2 pode ser produzido a pressões moderadas, (iii) a tecnologia oferece baixas emissões de SOx e NOx , (iv) o principal produto é o gás de síntese, que pode ser usado para outras aplicações ou produtos comerciais, e (v) uma ampla gama de combustíveis de hidrocarbonetos pode ser usada como matéria-prima, como gás, petróleo, carvão e coque de petróleo, etc. . As desvantagens são (i) o combustível de alimentação deve converter primeiro o combustível em syngas, (ii) turbinas a gás, aquecedores, caldeiras devem ser modificados para queima de H2, (iii) custos mais altos e maior risco tecnológico e (iv) requer grandes modificações nas plantas existentes para retrofit.
Combustão oxi-combustível
A combustão de oxi-combustível representa uma nova abordagem emergente para uma combustão de combustível fóssil mais limpa e com emissões próximas de zero. É realizado queimando o combustível em O2 puro em vez de ar. Ao eliminar o N2 (nitrogênio) no processo de combustão, a exaustão da corrente de gases de combustão é composta principalmente de água e CO2, sem N2. CO2 de alta pureza pode ser recuperado por condensação de água. No entanto, quando o combustível é queimado em O2 puro, a temperatura da chama é muito maior do que em um queimador de ar normal e o material convencional de construção do queimador não é capaz de suportar essa alta temperatura. Assim, ou o material de construção deve ser melhorado ou a temperatura da chama deve ser reduzida. O desenvolvimento de materiais resistentes a altas temperaturas tem sido lento porque é um grande empreendimento de P&D (pesquisa e desenvolvimento). Existem vários métodos que podem ser usados para moderar a temperatura da chama, sendo o mais comum a reciclagem de CO2. Na reciclagem de CO2, uma parte da corrente de gás de combustão rica em CO2 é reciclada de volta ao queimador para diminuir a temperatura da chama semelhante à de um queimador de ar normal. Outro método é usar injeção de água em vez de reciclagem de CO2 para controlar a temperatura da chama. Isso é muitas vezes referido como combustão de 'hidroxicombustível'. Efetivamente, essas duas opções permitem o uso contínuo de material refratário convencional até que um novo material resistente a altas temperaturas possa ser desenvolvido.
Um benefício primário da combustão de oxicombustível é o fluxo de CO2 de alta pureza que é produzido durante a combustão. Depois que os contaminantes são removidos, esse fluxo de CO2 é mais facilmente purificado e removido do que a captura pós-combustão. There are other benefits also such as reduction in NOx formation etc. When burning oil or coal, only two unit operations are needed for the combined removal of all other pollutants namely an electrostatic precipitator (ESP) or bag filter and a condensing heat exchanger (CHX)/reagent system. It is also possible to simplify the reagent system in the CHX to achieve total removal of SO2 with the CO2 stream for geologic storage. This further reduces the cost of unit operations for pollution abatement. The CHX increases the thermal efficiency of the boiler depending on the type of fossil fuel combusted, being the lowest for high rank bituminous coal and highest for natural gas.
Another benefit is the significant reduction in the size and capital cost of all plant equipment compared to conventional air-based combustion systems. This is due to the almost 5-fold decrease in the fire box volume and exit flue gas flow rates as N2 is eliminated in the combustion process.
The major disadvantage of oxy-fuel combustion is the high capital cost (primarily due to O2 requirements) and large electric power requirement inherent in conventional cryogenic air separation units required to generate O2. Oxy-fuel combustion is not currently used in typical large combustion systems because the air separation system is expensive and flue gas recycling is needed to be practiced in order to moderate flame temperature.
Processo de manufatura
- A sinergia de IoT celular e Bluetooth LE
- Armazenamento e manuseio da correia
- Criação e geração de imagens do Ciclocarbon
- Fibras de carbono:Passado, Presente e Futuro
- Os prós e contras dos anéis de fibra de carbono
- Braskem faz parceria com universidade para produção de plástico sustentável usando captura e uso de CO2
- Hiperconvergência e armazenamento secundário:Parte 2
- Fabricação de ferro por alto-forno e emissões de óxido de carbono
- Revestimento de carbono tipo diamante:uma inovação na fabricação de punções e matrizes
- Bolhas, cerveja e recuperação de CO2



