Preparação de micro / nanoesferas ocas de polianilina e sua capacidade de remoção de Cr (VI) de águas residuais
Resumo
As micro / nanoesferas ocas de polianilina (PANI) são obtidas através de uma simples polimerização de monômero em solução alcalina com Micelas Triton X-100 como moldes moles. As micro / nanoesferas ocas da PANI demonstram capacidade de remoção rápida e eficaz de Cromo (VI) (Cr (VI)) em uma ampla faixa de pH, e a capacidade de remoção máxima pode chegar a 127,88 mg / g em pH 3. Após tratamento com ácido, o micro / nanoesferas ocas de PANI usadas têm capacidade de remoção semelhante de Cr (VI) de águas residuais.
Histórico
O íon de metal pesado O cromo (VI) (Cr (VI)), proveniente do cromagem, curtimento de couro, acabamento de metais e indústrias têxteis, é seriamente perigoso para os ecossistemas e organismos vivos devido à sua carcinogenicidade e mobilidade [1,2,3] . Os íons Cr (VI) não tratados podem causar insuficiência renal, congestão pulmonar, dano gástrico, câncer de fígado, irritação da pele e assim por diante [4,5,6]. Em comparação com o Cr (VI), os íons Cr (III) são facilmente precipitados ou adsorvidos [7,8,9]. Assim, converter Cr (VI) em Cr (III) e precipitar Cr (III) em sólido são as técnicas comuns para a remoção de Cr (VI) da solução. Já os redutores tradicionais, como dióxido de enxofre, metabissulfito de sódio e sulfato ferroso, usados para a redução do Cr (VI), não são recicláveis e não podem ser reutilizados. Além disso, eles também levam à geração de produtos de resíduos secundários, levando a problemas ambientais crescentes [10, 11]. Portanto, é essencial explorar novos materiais para remoção de Cr (VI) do meio aquoso.
Desde que Rajeshwar e colaboradores relataram pela primeira vez que polímeros condutores poderiam converter Cr (VI) altamente tóxico em Cr (III) menos tóxico em 1993 [12], polímeros condutores, especialmente polianilina (PANI), têm sido amplamente preocupados [13,14, 15,16], devido à sua fácil síntese, baixo custo e mecanismo especial de dopagem / desdopagem de prótons. PANI, normalmente tem três estados de oxidação, que são pernigranilina (PB, que pertence à amina terciária aromática), esmeralda (EB, que pertence à amina secundária aromática) e leucoemeraldina (LB) [17, 18], contém unidades de benzenoide e quinonoide com abundantes grupos de aminas que podem fornecer elétrons para a redução de Cr (VI) [1, 10]. No entanto, PANI bulk e filme com baixa porosidade restringem sua aplicação na redução de Cr (VI). Recentemente, as micro / nanoesferas ocas de PANI têm recebido considerável atenção devido às suas amplas aplicações potenciais em supercapacitores [19, 20], campos de biossensores eletroquímicos [21] e assim por diante. Além disso, as micro / nanoesferas ocas da PANI com cavidade interna podem aumentar a área de superfície específica, melhorando assim a remoção da capacidade de Cr (VI) e a taxa de absorção. Recentemente, microesferas PANI ocas estão sendo preparadas usando métodos de molde rígido [19]; no entanto, eles envolvem procedimentos complexos de preparação e remoção, o que leva a uma reprodutibilidade pobre e torna bastante difícil reter a estrutura oca após a remoção do gabarito [22, 23]. Em comparação com os métodos de gabarito rígido, os métodos de gabarito flexível são mais baratos e eficazes. Mais importante, o molde macio pode ser removido facilmente com água e etanol [1, 24]. Portanto, um método de preparação simples, eficaz e de alto rendimento de micro / nanoesferas PANI ainda é desejável no campo da remoção de Cr (VI) tóxico.
Neste artigo, uma grande quantidade de micro / nanoesferas de PANI ocas reproduzíveis é sintetizada por uma polimerização de monômero simples em solução alcalina com micelas de Triton X-100 como modelos suaves. As micro / nanoesferas ocas reproduzíveis da PANI não são tóxicas e são seguras para os ecossistemas. Enquanto isso, as micro / nanoesferas ocas reproduzíveis de PANI têm alta capacidade de remoção de Cr (VI), que pode chegar a 127,88 mg / g em pH 3. O modelo de cinética de remoção de Cr (VI) e isoterma de absorção de micro / nanoesferas de PANI ocas estão em conformidade com pseudo- modelo de cinética de segunda ordem e modelo de isoterma de absorção de Langmuir, respectivamente. As micro / nanoesferas ocas da PANI não apenas removem Cr (VI) rapidamente, mas também podem ser facilmente regeneradas para reutilização.
Métodos
O objetivo do estudo
Para resolver o problema de que o íon de metal pesado Cr (VI) em águas residuais traz um perigo letal para os ecossistemas e organismos vivos, as micro / nanoesferas ocas reproduzíveis da PANI são preparadas por meio de uma polimerização de monômero simples em solução alcalina com micelas de Triton X-100 macias gabaritos, a fim de remover resíduos contendo Cr (VI).
Materiais
Anilina (Sinopharm Co. Ltd), hidróxido de sódio (NaOH, Sinopharm Co. Ltd), Triton X-100 (Alfa) e persulfato de amônio (APS, Sinopharm Co. Ltd) são de grau analítico e usados sem purificação adicional.
Síntese de Micro / Nanoesferas ocas de PANI
Micro / nanoesferas ocas de PANI foram preparadas por uma simples polimerização de monômero em solução alcalina com micelas de Triton X-100 como modelos. Em um processo de síntese típico, 32 mmol de anilina, 32 mmol de NaOH e 0,82 mmol de Triton X-100 foram diretamente dispersos em 20 mL de água desionizada com agitação magnética à temperatura ambiente por 20 min, então a solução de mistura foi resfriada no gelo. banho-maria por 5 min. Depois disso, a solução aquosa oxidante (20 mL) contendo 32 mmol APS pré-resfriada no banho de água gelada por 5 min foi adicionada à solução de mistura de anilina mencionada acima em uma porção, e a solução resultante foi agitada por mais 0,5 min para garantir a mistura completa e, em seguida, a reação foi realizada no banho de água gelada sem agitação por 12 h. Por fim, os produtos foram lavados e centrifugados com água desionizada e etanol até o filtrado ficar incolor e, em seguida, secos em estufa por 24h a 60 ° C.
Caracterização
A morfologia dos produtos PANI resultantes foi observada com microscópio eletrônico de varredura por emissão de campo (FESEM, Sirion 200) e microscópio eletrônico de transmissão (TEM, JEOL-2010). As estruturas da PANI preparada foram caracterizadas por difração de raios-X (XRD, Philips X'Pert) e espectroscopia de infravermelho com transformada de Fourier (FTIR, espectrofotômetro JASCO FT-IR 410). A concentração de Cr foi analisada por espectrômetro de emissão de plasma acoplado indutivamente (ICP) e espectroscopia de absorção de UV-Vis. O estado de oxidação do cromo adsorvido na nanoestrutura de PANI foi verificado usando espectroscopia de fotoelétrons de raios-X (XPS, ESCALAB 250). O potencial zeta e o tamanho de partícula foram obtidos por Zetasizer 3000HSa.
Remoção de Cr (VI) por esferas ocas de PANI
A solução de Cr (VI) foi preparada dissolvendo dicromato de potássio (K 2 Cr 2 O 7 ) em água desionizada. A solução estoque (2 mmol L −1 ) foi preparado dissolvendo 1,177 g de K 2 Cr 2 O 7 em 2.000 mL de água desionizada. Todas as soluções de trabalho com várias concentrações foram obtidas por diluições sucessivas. O pó PANI sintetizado (10 mg) foi disperso por ultrassom em 20 mL de solução de Cr (VI) (1,2 mmol L −1 ) com diferentes valores de pH, o qual foi ajustado com solução de NaOH e HCl. Após a reação por 3 h, a solução de reação foi centrifugada e os valores de pH do líquido sobrenadante foram ajustados na faixa de 7,5–8,5. Finalmente, as micro / nanoesferas ocas de PANI usadas foram separadas e enxaguadas várias vezes com água desionizada e secas. As capacidades de remoção de Cr (VI) das micro / nanoesferas ocas de PANI em diferentes valores de pH podem ser calculadas usando a seguinte equação:
$$ {q} _e =\ frac {\ left ({c} _0- {c} _e \ right) V} {m} $$ (1)
onde q e é a quantidade de remoção de Cr (VI) por grama de micro / nanoesferas ocas de PANI em equilíbrio (mg / g), V é o volume da solução (L), m é a massa das micro / nanoesferas ocas de PANI (g), e c 0 e c e são a concentração de Cr (VI) no início e no equilíbrio (mg / L), respectivamente.
Medição da cinética de remoção
Para os experimentos de cinética de remoção, foram realizados três conjuntos de experimentos, nos quais os valores de pH da solução de Cr (VI) foram 3, 4 e 5, respectivamente. O pó PANI sintetizado (10 mg) foi disperso por ultrassom em 20 mL de solução de Cr (VI) (1,2 mmol L −1 ) com diferentes valores de pH e a mistura foi agitada magneticamente. Em intervalos predeterminados, uma quantidade apropriada da solução de reação foi retirada e, em seguida, centrifugada. O líquido sobrenadante foi usado para analisar a concentração de Cr (VI) por espectroscopia de absorção de UV-Vis em comprimento de onda de 350 nm. Os gráficos cinéticos teóricos foram obtidos usando a equação de pseudo-segunda ordem:
$$ \ frac {t} {q_t} =\ frac {1} {k_2 {q} _e ^ 2} + \ frac {t} {q_e} $$ (2)
onde q e e q t são as quantidades de Cr (VI) removidas por micro / nanoesferas PANI ocas no equilíbrio e no tempo t (min) (mg / g), e k 2 é a constante de velocidade (g / mg min).
Remoção de medição isotérmica
Para os experimentos de isoterma de remoção, os processos de operação são os mesmos acima. Também fizemos três conjuntos de experimentos em diferentes valores de pH, 3, 4 e 5, respectivamente. Em cada experimento, o pó PANI sintetizado (10 mg) foi disperso por ultrassom em 20 mL de solução de Cr (VI) com diferentes concentrações sob agitação magnética. Quando a solução atingiu o equilíbrio de remoção, eles foram centrifugados e então analisados quanto à concentração de Cr (VI) remanescente por espectroscopia de absorção de UV-Vis. Os gráficos de Langmuir para a remoção de Cr (VI) por micro / nanoesferas ocas de PANI usando a equação de Langmuir:
$$ \ frac {c_e} {q_e} =\ frac {1} {q_m {k} _L} + \ frac {c_e} {q_m} $$ (3)
onde q m é a capacidade máxima de remoção (mg / g), q e são as quantidades de Cr (VI) no equilíbrio (mg / g), c e é a concentração de Cr (VI) no equilíbrio (mg / L), e k L é a constante de Langmuir.
Resultados e discussão
A PANI sintetizada foi obtida por polimerização de monômero com Triton X-100 Micelles como moldes moles. A morfologia via observação SEM e TEM é mostrada como Fig. 1. Micro / nanoesferas PANI abundantes podem ser observadas claramente a partir da imagem SEM de PANI na Fig. 1a. Com cuidado, um orifício na superfície das micro / nanoesferas é observado, conforme mostrado na imagem inserida da Fig. 1a, que indica que as micro / nanoesferas são ocas. Este resultado é posteriormente confirmado por meio da imagem TEM (Fig. 1b). Além disso, duas imagens mostram que o diâmetro dessas micro / nanoesferas está entre 0,5 e 2 μm.

a SEM e b Imagens TEM das micro / nanoesferas ocas de PANI sintetizadas
A estrutura molecular das micro / nanoesferas ocas de PANI sintetizadas é caracterizada por espectroscopia FTIR e difração de raios-X (XRD), mostrada na Fig. 2. Cinco picos característicos podem ser observados claramente na Fig. 2a. Os picos característicos em 1569 cm −1 e 1496 cm −1 são atribuídos à vibração de alongamento C-N do anel quinóide (Q) e anel benzenoide (B), respectivamente. O pico apareceu em 1298 cm −1 é devido à vibração de alongamento C-H com conjugação aromática [1]. Pico em 1142 cm −1 corresponde aos modos de alongamento N-Q-N e é um símbolo de deslocalização de elétrons em PANI [1]. Além disso, o pico de absorção em 824 cm −1 é característica das vibrações de flexão C-H fora do plano do anel de benzeno para-substituído [25]. Comparando os picos característicos do anel benzenoide e do anel quinóide, a intensidade de absorbância relativa do anel benzenoide é maior do que a do anel quinóide. Então, pode-se deduzir que as micro / nanoesferas ocas da PANI estão principalmente na forma esmeralda. A Figura 2b exibe o padrão de XRD de micro / nanoesferas ocas de PANI sintetizadas, que mostra alta cristalinidade incomum com picos de difração centrados em 20,2 ° e 25,4 °, correspondendo à periodicidade paralela e perpendicular às cadeias de polímero [25].
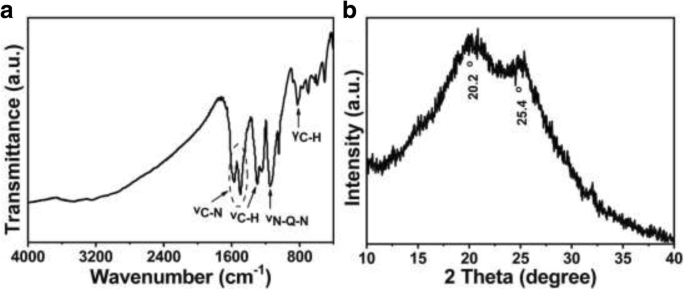
a Espectro FTIR e b Padrões de XRD das micro / nanoesferas ocas de PANI sintetizadas
A Figura 3 mostra os resultados da remoção de Cr (VI) em diferentes momentos, nos quais os valores de pH da solução de Cr (VI) são 3, 4 e 5, respectivamente. Visto na Fig. 3a, a cor da solução de Cr (VI) está ficando mais clara sob o tratamento com micro / nanoesferas PANI ocas com o aumento do tempo. Especialmente, o líquido relativamente claro é obtido após 90 min quando o pH é 3. E os resultados de que a concentração de Cr (VI) foi tratada por micro / nanoesferas PANI ocas são mostrados diretamente na Fig. 3b. Estes resultados indicam que as micro / nanoesferas ocas de PANI são candidatas eficientes para a remoção de Cr (VI) da solução em condições adequadas.
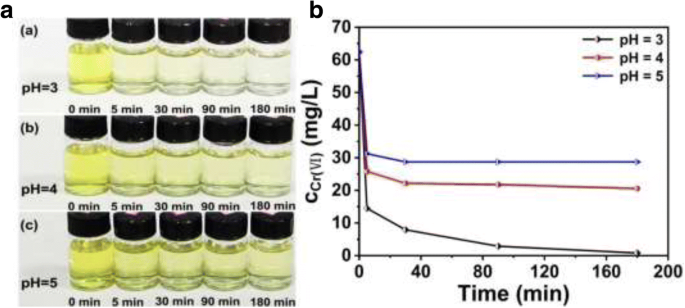
A solução de Cr (VI) após tratada com micro / nanoesferas ocas de PANI em tempos diferentes, pH da solução respectivamente a a 3, b 4 e c 5 (concentração inicial de Cr (VI):1,2 mmol / L (62,4 mg / L)). a As fotografias e b Concentração de Cr (VI) na solução final
O valor de pH da solução é um parâmetro importante que afeta as propriedades químicas do Cr (VI) em solução ou a protonação ou desprotonação da PANI. Portanto, as capacidades de remoção e redução de Cr (VI) da PANI sintetizada são estudadas em solução de diferentes pH, como mostrado na Fig. 4. A Figura 4a mostra as mudanças nas concentrações totais de Cr e Cr (VI) após o tratamento com cavidades PANI micro / nanoesferas em diferentes valores de pH, respectivamente. As capacidades de remoção de Cr (VI) das micro / nanoesferas ocas de PANI em diferentes valores de pH podem ser calculadas usando a Eq. (1). A relação correspondente entre as capacidades de remoção de Cr (VI) e os valores de pH é calculada a partir dos valores na Fig. 4a pela Eq. (1) e mostrado na Fig. 4b. A diminuição óbvia da concentração de Cr (VI) como a diminuição dos valores de pH de 12 para 1 mostra que as capacidades de remoção de Cr (VI) correspondentes das micro / nanoesferas ocas de PANI aumentam com o aumento da acidez. Especialmente, a capacidade de remoção de Cr (VI) mostra um rápido aumento quando o pH é inferior a 4. No entanto, a concentração total de Cr mostra um desempenho anormal quando o valor de pH está abaixo de 2, o que indica que a concentração de Cr (III) aumenta acentuadamente em a solução. Foi relatado que, em pH mais baixo (pH abaixo de 2), o Cr (III) reduzido existia predominantemente em Cr 3+ e a literatura relatou que a extensão da protonação das micro / nanoesferas ocas da PANI usada aumentou rapidamente com a diminuição do pH em pH ácido 1-2 [26, 27]. Portanto, os resultados do experimento acima podem ser atribuídos ao fato de que a repulsão eletrostática aumenta entre as microesferas PANI ocas utilizadas e o Cr (III) reduzido, que supera a interação de quelação entre eles, de modo que o Cr (III) entre em solução a partir da superfície de PANI, quando o pH está abaixo de 2. Quando o pH é superior a 2, a tendência de mudança da concentração total de Cr é semelhante à do Cr (VI) (Fig. 4a), indicando que a maior parte do Cr (III) reduzido é removido da solução. Afirma que as micro / nanoesferas ocas de PANI são boas candidatas à remoção de Cr (VI) quando o valor de pH estiver entre 2 a 4.
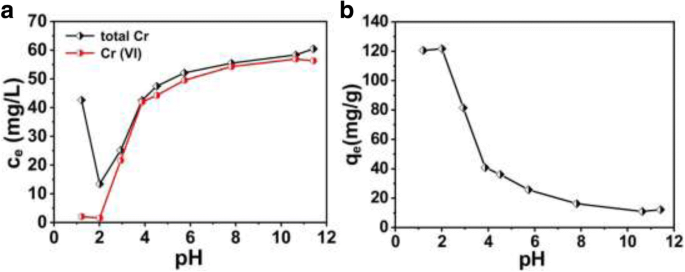
a As mudanças da concentração de Cr sob diferentes pH da solução, e b as capacidades de remoção de Cr (VI) correspondentes (concentração inicial de Cr (VI):1,2 mmol / L (62,4 mg / L))
As microesferas ocas de PANI após a reação com solução de Cr (VI) em pH 3, 4 e 5 são investigadas posteriormente. A Figura 5a-c mostra a análise de mapeamento de elemento das micro / nanoesferas PANI ocas usadas, nas quais o elemento Cr foi observado ao lado dos elementos C e N. Isso demonstra diretamente que os íons Cr foram adsorvidos de fato pelas micro / nanoesferas ocas da PANI. A Figura 5d mostra os espectros de XPS das microesferas ocas de PANI usadas em pH 3, 4 e 5, respectivamente, que exibem a energia de ligação do Cr 2p. Nos espectros de XPS, dois picos podem ser observados; o primeiro corresponde a 2p 1/2 , o último para 2p 3/2 . Comparando as três linhas do espectro XPS, a energia de ligação do Cr 2p 3/2 localiza-se em 577,4 eV e nada a ver com o valor do pH. Foi relatado que as bandas em 577,4 eV podem ser atribuídas ao Cr (III) por analogia com outros compostos de cromo [12, 28]. Assim, os Cr adsorvidos estão todos principalmente na forma de Cr (III).
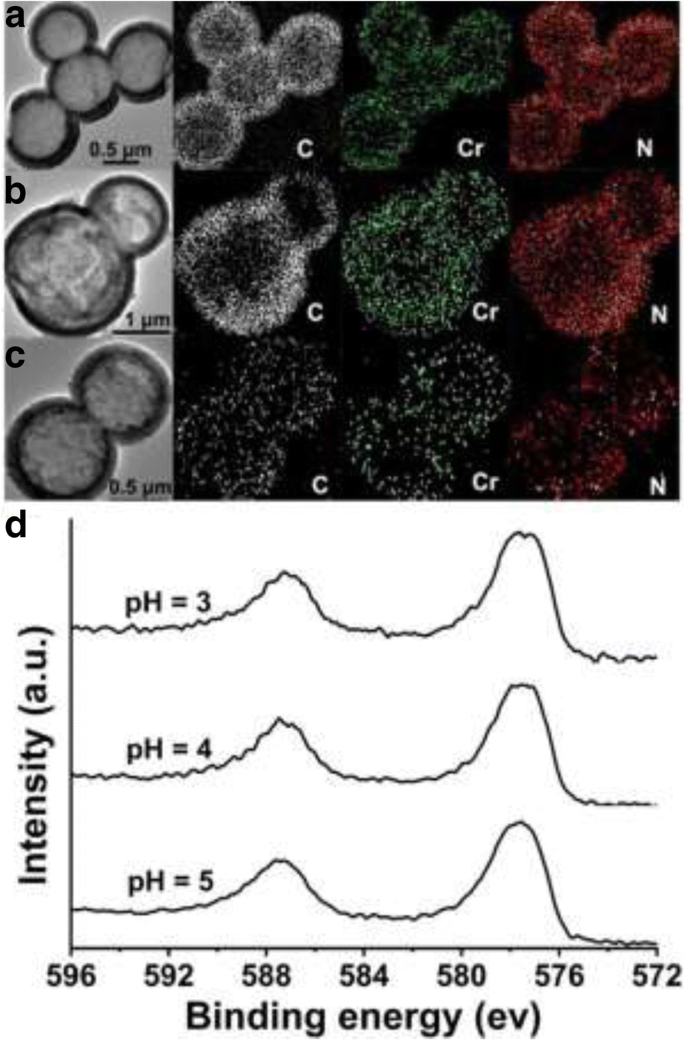
a - c Mapeamento de elemento e d Espectros de Cr 2p XPS das micro / nanoesferas ocas de PANI após a reação com Cr (VI) (concentração inicial de Cr (VI):1,2 mmol / L (62,4 mg / L); pH da solução respectivamente a 3, 4 e 5)
Com base em todos esses resultados, ele pode resumir o mecanismo de remoção de Cr (VI) com micro / nanoesferas de PANI ocas da seguinte forma:o Cr (VI) é absorvido na superfície de micro / nanoesferas de PANI (EB) intocadas ocas. Então, o Cr (VI) absorvido é todo reduzido a Cr (III). Enquanto isso, a PANI (EB) pura é oxidada na forma de pernigranilina (PB). Cr (VI) em solução existe na forma de íon cromato ácido (HCrO 4 - ) dentro da faixa de pH (2–6) [25]. Nesta faixa de pH, uma porção de EB PANI é protonada, e o grupo amina (-NH-) de suas moléculas existe como grupo amina (-NH 2 + -). Assim, Cr (VI) adsorvido por micro / nanoesferas ocas de PANI realiza-se através da interação eletrostática entre PANI de carga positiva e HCrO de carga negativa 4 - . O potencial zeta e o tamanho de partícula das amostras foram medidos com Zetasizer 3000HSa, e os resultados mostram que o potencial zeta é 38,6 mV e 32,9 mV, e o tamanho de partícula é de cerca de 990 nm e 630 nm para PANI antes e depois de Cr (VI) remoção em pH 3, respectivamente. Isso significa que PANI de antes e depois da remoção de Cr (VI) pode existir de forma estável na solução. Comparando a estrutura molecular de EB e PB PANI, pode-se descobrir que a solvatação de EB PANI de amina secundária aromática é maior do que a de PB PANI de amina terciária aromática, porque a amina secundária carrega um átomo de hidrogênio a mais do que a amina terciária [ 29]. Assim, o tamanho aparente de partícula de EB PANI é maior do que de PB PANI.
Como sabemos, a capacidade de remoção de Cr (VI) depende principalmente da área de superfície específica das micro / nanoesferas de PANI ocas. A área de superfície específica de micro / nanoesferas PANI ocas pode ser obtida por análise de adsorção-dessorção de nitrogênio (mostrado na Fig. 6), e a área de superfície BET pode ser calculada em 32,813 m 2 / g, indicando maior área de superfície específica de micro / nanoesferas PANI ocas.
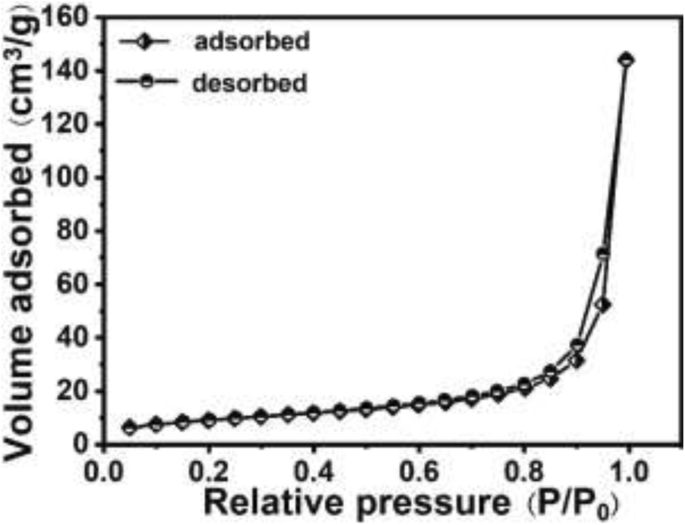
Isotermas de adsorção-dessorção de nitrogênio das micro / nanoesferas ocas de PANI sintetizadas
A Figura 7a mostra a relação entre a capacidade de remoção q t de Cr (VI) e o tempo t para solução com diferentes valores de pH. A capacidade de remoção aumenta rapidamente no estágio inicial (0 ~ 5 min) e, em seguida, continua a aumentar lentamente até o equilíbrio após cerca de 120 min. Indica que a remoção inicial ocorre na superfície das micro / nanoesferas ocas de PANI e, em seguida, prossegue para a parte interna [25].
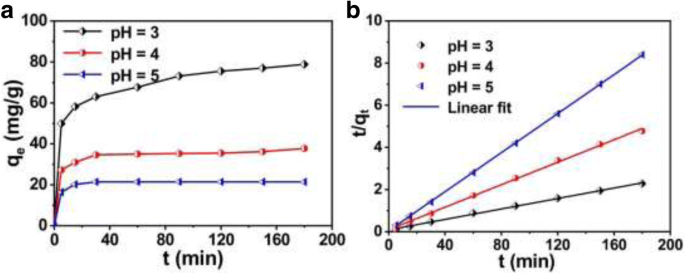
a Mudanças na concentração de Cr (VI) em momentos diferentes (concentração inicial de Cr (VI):1,2 mmol / L (62,4 mg / L), pH da solução respectivamente em 3, 4 e 5), e b os modelos de pseudo-segunda ordem na cinética de remoção de Cr (VI) com micro / nanoesferas PANI ocas
A fim de explorar a cinética de remoção de Cr (VI) com micro / nanoesferas ocas de PANI, alguns modelos contendo os modelos de pseudo-primeira e pseudo-segunda ordem são empregados para interpretar os dados do experimento. Aqui, a pseudo-segunda ordem é o modelo mais adequado para ajustar os dados experimentais, comparando os dados do experimento com esses modelos teóricos. A Figura 7b mostra os gráficos cinéticos teóricos de acordo com a equação de pseudo-segunda ordem. (2) O resultado mostra que t / q t versus t eram lineares e os coeficientes de correlação R 2 correspondem a 0,99788, 0,99817 e 0,99994, para pH 3, 4 e 5, respectivamente. Além disso, os valores de q e pode ser calculado a partir do declive, isto é, 80,654, 37,48 e 21,56 mg / g correspondendo ao valor de pH de 3, 4 e 5, respectivamente, que estão próximos dos valores experimentais mostrados na Fig. 7a.
As capacidades de remoção de Cr (VI) das micro / nanoesferas ocas da PANI também estão relacionadas à concentração de Cr (VI). Portanto, é importante investigar o efeito da concentração de Cr (VI) nas capacidades de remoção de micro / nanoesferas ocas de PANI. O experimento foi realizado em pH 3, 4 e 5, respectivamente, com várias concentrações iniciais de Cr (VI). A Figura 8a mostra as mudanças da capacidade de remoção de Cr (VI) ( q e (mg / g)) versus concentração de equilíbrio ( c e (mg / L)). Conforme mostrado na Fig. 8a, a capacidade de remoção aumenta mais rapidamente em concentrações mais baixas de Cr (VI) e tende a ser um valor constante em concentrações mais altas, ou seja, a capacidade máxima de remoção de Cr (VI) de micro / nanoesferas de PANI ocas é alcançada. Para descrever o resultado experimental da isoterma de remoção de Cr (VI), três modelos de isotermas importantes, que são os modelos de Langmuir, Freundlich e Temkin, são selecionados. No entanto, apenas o modelo de Langmuir pode ajustar os dados experimentais. A Figura 8b mostra os gráficos de Langmuir para a remoção de Cr (VI) por micro / nanoesferas PANI ocas da Eq de Langmuir. (3). O resultado mostra que c e / q e versus c e é linear em pH 3, 4 e 5, respectivamente (coeficiente de correlação R 2 =0,99950, 0,99875 e 0,99962 em pH 3, 4 e 5). Além disso, os valores de q m que é calculado a partir do declive são 25,61, 43,20 e 127,88 mg / g em pH 5, 4 e 3, respectivamente, que estão próximos dos valores experimentais mostrados na Fig. 8a. A isoterma de Langmuir é baseada na suposição de nenhuma interação entre o adsorvente de estrutura homogênea e a cobertura da monocamada. A remoção de Cr (VI) da solução na micro / nanosfera PANI oca corresponde ao modo monocamada. Pode-se afirmar que nenhuma adsorção adicional pode ocorrer quando os sítios ativos na superfície das micro / nanoesferas ocas da PANI são ocupados por Cr (VI).
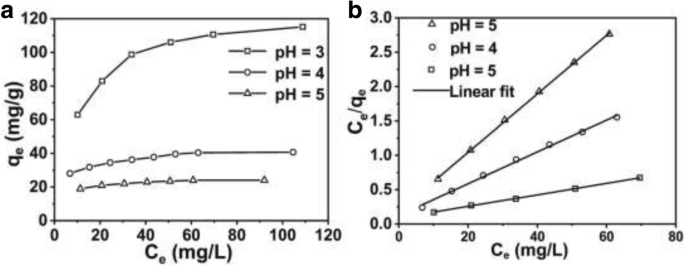
a A capacidade de remoção de Cr (VI) em diferentes concentrações de equilíbrio (pH da solução respectivamente em 3, 4 e 5), e b modelo isotérmico de remoção de Langmuir correspondente
A comparação da capacidade máxima de remoção de Cr (VI) das micro / nanoesferas ocas de PANI sintetizadas neste estudo com aquela relatada na literatura é mostrada na Tabela 1. Pode-se observar que as micro / nanoesferas ocas de polianilina apresentam maior Cr (VI ) capacidade de remoção do que a de muitos outros removedores. Esses resultados sugerem que as micro / nanoesferas ocas de PANI podem ser consideradas um material promissor para a remoção de Cr (VI) de solução aquosa.
Com base nos resultados acima mencionados, o processo de remoção de Cr (VI) pode ser explicado como segue. A solução inicial contém Cl - , H + , HCrO 4 - íons e assim por diante (Fig. 9a). Sob a condição de meio ácido, o estado de oxidação esmeralda dos íons PANI (EB) e Cr (VI) são oxidados e reduzidos ao estado de pernigranilina (PB) e Cr 3+ íons, respectivamente (Fig. 9b). O processo de reação principal pode ser demonstrado como segue em solução ácida [36]:
$$ 3 \ mathrm {PANI} \ \ left (\ mathrm {EB} \ right) +6 {\ mathrm {Cl}} ^ {\ hbox {-} 1} \ hbox {-} 6 {\ mathrm {e} } ^ {\ hbox {-} 1} \ a 3 \ mathrm {PANI} {\ left (\ mathrm {Cl} \ right)} _ 2 \ left (\ mathrm {PB} \ right) $$ (4) $$ 2 {{\ mathrm {H} \ mathrm {CrO}} _ 4} ^ {\ hbox {-} 1} \ kern0.5em +14 {\ mathrm {H}} ^ {+} \ kern0.5em +6 {\ mathrm {e}} ^ {\ hbox {-} 1} \ kern0.5em \ a 2 {\ mathrm {Cr}} ^ {3 +} \ kern0.5em + \ kern0.5em 8 {\ mathrm {H}} _2 \ mathrm {O} $$ (5)
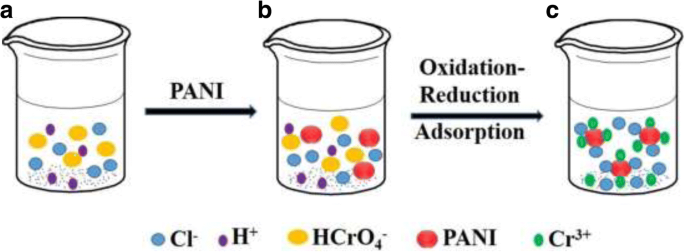
O diagrama esquemático da remoção de Cr (VI). a Águas residuais contendo Cr (VI) sob condições ácidas, b adicionar PANI a águas residuais contendo Cr (VI) e c água residual de remoção de Cr (VI)
Esta reação ocorre simultaneamente na superfície da PANI. O resultado Cr 3+ Os íons são absorvidos na superfície das micro / nanoesferas PANI (Fig. 9c). Como mencionado acima, as micro / nanoesferas PANI são esferas ocas, e a maioria das esferas ocas têm muitos orifícios, de modo que as superfícies externa e interna das micro / nanoesferas PANI podem absorver muito Cr 3+ íons por causa da estrutura oca (Fig. 1).
Foi relatado que a pernigranilina é instável em condições ambientais e facilmente reduzida ao estado de oxidação esmeralda em solução de ácido forte, como HCl e H 2 SO 4 [26]. Isso indica que as micro / nanoesferas ocas de PANI usadas podem ser facilmente regeneradas por meio de tratamento com ácido. A conversão entre a pernigranilina e o estado esmeralda pode ser mostrada como Esquema 1. Por exemplo, as micro / nanoesferas de PANI ocas usadas são posteriormente tratadas com HCl 1 M por 0,5 h e então reutilizadas para remoção de Cr (VI). Pode ser verificado na Tabela 2 que a capacidade de remoção das primeiras micro / nanoesferas ocas reutilizadas de PANI é provavelmente próxima da capacidade inicial de remoção de PANI [26, 37]. Pode-se concluir que as micro / nanoesferas ocas de PANI são um material reprodutível para remoção de Cr (VI).
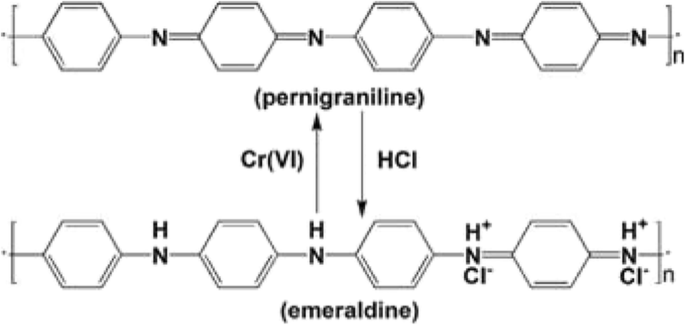
Ilustração esquemática da conversão entre pernigranilina e esmeralda de PANI
Conclusões
Uma grande quantidade de micro / nanoesferas PANI ocas foi fabricada por uma simples polimerização de monômero em solução alcalina com micelas Triton X-100 como modelos. As micro / nanoesferas ocas podem rápida e efetivamente remover Cr (VI) em uma ampla faixa de pH. Os dados da cinética de remoção são ajustados ao poço do modelo de pseudo-segunda ordem e a isoterma de remoção de Cr (VI) pode ser descrita pelo modelo de isoterma de Langmuir. A capacidade máxima de remoção das micro / nanoesferas ocas de PANI pode chegar a 127,88 mg / g em pH 3. Além disso, as micro / nanoesferas de PANI ocas utilizadas podem ser facilmente regeneradas por meio de tratamento com solução ácida, mantendo aproximadamente a mesma remoção de Cr (VI) capacidade. O presente trabalho indica que as micro / nanoesferas ocas de PANI são um material eficaz e reprodutível para a remoção de Cr (VI) tóxico de águas residuais.
Abreviações
- APS:
-
Persulfato de amônio
- B:
-
Anel benzenoide
- EB:
-
Esmeralda
- FESEM:
-
Microscópio eletrônico de varredura de emissão de campo
- FTIR:
-
Espectroscopia infravermelha com transformada de Fourier
- ICP:
-
Espectrômetro de emissão de plasma indutivamente acoplado
- LB:
-
Leucoemeraldine
- PANI:
-
Polianilina
- PB:
-
Pernigranilina
- Q:
-
Anel quinóide
- TEM:
-
Microscopia eletrônica de transmissão
- XPS:
-
espectroscopia de fotoelétrons de raios-X
- XRD:
-
Difração de raios X
Nanomateriais
- Ambos Tesla e Panasonic irão eliminar o cobalto de suas baterias
- A transmissão de esportes atrai mais espectadores (e capacidade da rede) em 2019
- Justificando a automação em sua fábrica:o que fazer, o que não fazer e conselhos dos especialistas
- Como a Ingram Micro traz valor do canal para parceiros e clientes
- Remoção adsortiva de íons de cobre (II) de solução aquosa usando um nanoadsorvente de magnetita de resíduos de escala de moinho:Síntese, caracterização, adsorção e modelagem cinética Estud…
- Preparação e propriedades magnéticas de nanopartículas de espinélio FeMn2O4 dopadas com cobalto
- Preparação de nanopartículas de mPEG-ICA carregadas com ICA e sua aplicação no tratamento de dano celular H9c2 induzido por LPS
- Em direção aos nanofluidos de TiO2 - Parte 1:Preparação e propriedades
- Preparação de Nanorods de Alumina a partir de Lodo de Alumina Contendo Cromo
- Preparação e desempenho fotocatalítico de fotocatalisadores de estrutura oca LiNb3O8



