Remoção adsortiva de íons de cobre (II) de solução aquosa usando um nanoadsorvente de magnetita de resíduos de escala de moinho:Síntese, caracterização, adsorção e modelagem cinética Estudos
Resumo
Neste estudo, o nanoadsorvente de magnetita (MNA) foi extraído de produtos residuais em escala de fábrica, sintetizado e aplicado para eliminar Cu 2+ a partir de uma solução aquosa. O produto residual em escala de moinho foi moído usando moagem convencional e impactado usando moinho de bolas de alta energia (HEBM) por 3, 5 e 7 horas de moagem. A este respeito, o MNA preparado foi investigado usando difração de raios-X (XRD), microscópio eletrônico de transmissão de alta resolução (HRTEM), microscopia eletrônica de varredura de emissão de campo - espectroscopia de raios-X dispersiva de energia (FESEM-EDS), UV-Vis espectroscopia, infravermelho com transformada de Fourier (FTIR), Brunauer – Emmett – Teller (BET) e potencial zeta. O tempo de moagem de MNA-7 h resultante exibiu uma estrutura cristalina com formas irregulares de 11,23 nm, área de superfície específica de 5,98 m 2 g −1 , magnetização de saturação, Sra. de 8,35 emug −1 , e carga de ponto isoelétrico em pH 5,4. A capacidade de adsorção ideal, q e de 4,42 mg.g −1 para a remoção de Cu 2+ íons foi obtido em 120 minutos de tempo de contato. Os dados experimentais foram mais bem ajustados ao modelo de isoterma de Temkin. Uma comparação entre os estudos cinéticos experimentais e os aspectos teóricos mostrou que a pseudo-segunda ordem combinou as tendências experimentais com um coeficiente de correlação de ( R 2 > 0,99). Além disso, a eficiência de regeneração de 70,87% foi alcançada após três ciclos de estudos de reutilização. O MNA oferece uma abordagem prática, eficiente e de baixo custo para reutilizar resíduos de escala de fábrica e fornecer separação ultrarrápida para remover Cu 2+ da água.
Introdução
A água é um dos mais valiosos recursos naturais baseados na natureza e desempenha um papel fundamental na existência de todos os seres vivos [1]. Com a revolução da economia mundial e a rápida expansão da industrialização contemporânea, os desafios da poluição da água tornam-se mais graves [2]. A nocividade do meio ambiente ecológico por meio de metais pesados está crescendo intensamente em todo o mundo devido ao enorme número de descargas provenientes de rotas industriais e populacionais. Os metais pesados não biodegradáveis são muito tóxicos e têm tendência a acumular-se nos órgãos humanos e outros organismos residentes, prejudicar a qualidade da água, desencadear várias dificuldades na vida aquática e causar inúmeras doenças e distúrbios [3,4,5] . Em particular, a liberação de águas residuais compreendendo íons cobre (II) (Cu 2+ ) resultante de vias antropogênicas em águas domésticas tornou-se problemático para a saúde pública e o meio ambiente [6,7,8]. Embora Cu 2+ é um importante oligoelemento no corpo humano e em várias rotas biológicas e no metabolismo dos animais [9], o enorme consumo em concentrações elevadas pode resultar em graves impactos toxicológicos, por exemplo convulsões, cólicas, vômitos ou, ao mesmo tempo, morte. Por exemplo, a contaminação devido ao Cu divalente inicia dramatização, queratinização, formigamento das mãos e pés e exibe influências carcinogênicas e mutagênicas [10-12]. Além disso, o consumo supérfluo de cobre irá provocar trauma oxidativo e síndromes neurodegenerativas agudas, incluindo esclerose lateral amiotrófica, distúrbio de Menkes, doença de Alzheimer e doença de Wilson [13, 14]. A poluição da água por Cu 2+ é considerado um dos problemas ambientais mais prevalentes desde Cu 2+ compostos estão contidos no excesso de atividades industriais [15]. Por outro lado, a deficiência de Cu 2+ na nutrição animal pode causar diarréia, anemia e distúrbios nervosos [16]. A Organização Mundial da Saúde (OMS) estipulou que o nível tolerável para Cu 2+ na água potável é de 2 mgL −1 [17, 18]. Além disso, a Agência de Proteção Ambiental dos Estados Unidos (USEPA) fixou a concentração máxima aceitável de cobre na água em 1,3 mgL −1 [19]. Assim, o nível de Cu 2+ na dieta diária, particularmente em água potável e esgoto, deve ser monitorado e reduzido a uma quantidade mínima antes de liberar para o ambiente [20].
Na tentativa de conter esses efeitos perigosos sobre o meio ambiente, vários métodos de remediação de efluentes têm sido utilizados, como precipitação [21], troca iônica [22], precipitação química, co-precipitação [23], processos de membrana [24, 25, 82 ], coagulação [26] e adsorção [3, 27–30] para remover Cu 2+ de águas residuais. Entre essas abordagens, a adsorção é fortemente desejável devido à sua extrema conveniência, custo-benefício, facilidade de operação, flexibilidade, procedimento de projeto simples, simplicidade, eficácia de remoção superior, maior praticidade e reciclabilidade [10, 31-33]. Portanto, o foco central foi mudado para explorar novos adsorventes compreendendo diversos grupos funcionais que poderiam acelerar Cu 2+ remoção.
Vários adsorventes podem ser aplicados para remover metais pesados da água por meio de adsorção, incluindo carvão ativado [34], biomassa agrícola [35], óxidos de metal [36], nanomateriais de sílica [37, 38], minerais de argila [31, 39, 40], outros [41]. No entanto, mais aplicações desses sorventes são restritas devido à sua condição complexa ou modificação de equipamentos específicos e baixa adsorção. Além disso, os adsorventes convencionais mostram recuperação fraca dos íons metálicos alvo de grandes volumes de solução devido a inadequações de difusão, capacidade de ligação mínima e insuficiência de sítios de superfície ativos [42]. Portanto, a necessidade de explorar um novo nano-absorvente de baixo custo com maior eficácia de adsorção, área de superfície adsortiva substancial, resistência de difusão mínima, capacidade de adsorção superior e separação rápida para enormes volumes de solução é indispensável.
Recentemente, vários novos absorventes foram utilizados, incluindo nanomateriais, materiais mesoporosos, nanotubos de carbono (CNT), materiais revestidos com íons e nanopartículas magnéticas [11, 43,44,45]. Dentre estes, os nanomateriais têm recebido grande atenção devido às suas características biológicas, físicas e químicas, conseqüência da grande relação superfície-volume, maior absorção de íons metálicos com capacidade de adsorção superior [46,47,48]. O nanossorvente magnético tem forte tendência de adsorver contaminantes de resíduos líquidos aquosos ou gasosos, e a aplicação desses sorventes magnéticos para desvendar muitos contratempos de contaminação ambiental tem ganhado atenção crescente nos últimos anos [11]. O adsorvente de magnetita é um precursor de baixo custo promissor com várias propriedades exclusivas, como sua alta área de superfície, superparamagnética, alta anisotropia, alta coercividade, baixa temperatura Curie altamente ativa, facilidade de separação, alta suscetibilidade magnética, excelente capacidade de reciclagem e reutilização, magnética propriedades de atração, entre outros [49, 50, 83]. Além disso, os NPs são considerados eficientes para sorção de alguns íons metálicos, ânions, ligantes, cátions e corantes, e sua aplicação é, portanto, atraente em um campo inovador de adsorção, recuperação ou eliminação de alguns íons [51,52,53] .
Diante disso, pode-se inferir que os estudos usando nanoadsorvente de magnetita de chips moídos industriais obtidos localmente usando a técnica de moagem de bolas de alta energia para remover Cu 2+ provenientes da água são bastante limitados e pouco aplicados, apesar do seu potencial impressionante. Nesse sentido, este estudo se concentra na síntese de um novo nanoadsorvente de magnetita (MNA) a partir de resíduos de escala de moagem usando o método de moagem de bolas de alta energia e sua aplicação como uma remoção econômica de íons de cobre (II) de metais pesados em água, a partir do modelo de uma solução aquosa. Além disso, o estudo da cinética de superfície do MNA reciclado de resíduos de escala de fábrica usado como adsorvente de metal no tratamento de águas residuais também foi investigado. A equação do modelo cinético da reação MNA foi cuidadosamente desenvolvida e estudada.
Materiais e métodos
Materiais e produtos químicos
Neste trabalho, as aparas de resíduos de escala de fábrica foram fornecidas pela fábrica de aço localizada em Terengganu, Malásia. A água desionizada (DI) usada no experimento em lote foi obtida a partir do sistema de refinamento Milli-Q water. O nitrato de cobre (Cu (NO 3 ) 2 ) foi adquirido da Aldrich (Chemical Industry Stock Co., Ltd., China) para a preparação de solução padrão de cobre (1000 ppm). Um pH 5-SS (spear pH Tester) foi empregado no experimento para medição de pH e agitação. O espectrofotômetro UV-Vis (HACH DR4000U) foi utilizado para analisar a concentração de cobre no comprimento de onda de 600 nm. A concentração inicial de cobre foi medida usando o procedimento padrão (APHA, 2005) [54], e o volume restante da amostra foi preservado em um resfriador a 4 ℃.
Síntese de magnetita nanoadsorvente (MNA)
Os chips de resíduos de escala de moagem bruta contêm partículas magnéticas e impurezas (partículas não magnéticas). As impurezas foram eliminadas para evitar a contaminação da amostra. A Figura 1 descreve o método usado para a síntese de nanoadsorvente de magnetita (MNA) a partir de chips moídos. Em primeiro lugar, os cavacos moídos foram extensivamente lavados com água DI e secos a 104 ℃ por 24 horas e, em seguida, triturados em tamanho de mícron usando uma máquina de fresagem convencional. Este procedimento foi realizado continuamente por 48 h, e a magnetita micro-dimensionada resultante (Fe 3 O 4 ) foi posteriormente limpo com a técnica de separação magnética (MST). O MST estimula a separação de partículas não magnéticas e magnéticas. Posteriormente, a magnetita mícron limpa foi seca em forno por 48 h a 104 ℃ e posteriormente transportada para um recipiente hermético. Além disso, as partículas magnéticas fortes foram separadas das fracas por uma técnica de separação por temperatura de Curie (CTST), conforme indicado na Fig. 1. Este método está de acordo com o procedimento adotado por [55-57]. As partículas magnéticas robustas separadas foram subsequentemente secas ao ar por 24 h e, em seguida, submetidas a um moinho de bolas de alta energia (HEBM) por três tempos de moagem diferentes de 3, 5 e 7 h para obter uma magnetita de tamanho nanométrico [58].

Procedimento de síntese de nanoadsorvente de magnetita usando o método HEBM
Caracterização do adsorvente de nano-magnetita preparado (MNA)
A morfologia estrutural do adsorvente sintetizado foi analisada com TEM / EDS usando Hitachi Co., Japão Modelo No. S3400N. O FTIR fornece informações sobre grupos funcionais existentes no adsorvente sintetizado. O aparelho Bruker-Tensor 27 IR com método padrão de pelotas KBr na faixa espectral 400–4000 cm −1 com 2 cm −1 resolução identificou espectros de FTIR do adsorvente de nanomagnetita. A técnica de difração de raios X (XRD) foi aplicada para analisar a estrutura cristalina e a fase do MNA sintetizado usando o difratômetro de raios X (XRD) Philips Expert Diffractometer com radiação Cu Kα (λ =0,154 nm) obtido na faixa 2θ de 20 a 80 ° com um tamanho de etapa de varredura de 2θ =0,033 com 5 s por etapa como a contagem. O espectro de XRD observado foi comparado com o banco de dados ICSD padrão. As composições estruturais e morfológicas da amostra de MNA foram obtidas por meio de microscopia eletrônica de varredura por emissão de campo (FESEM), JEM JEOL 2100, EUA, com microscópio eletrônico de transmissão de alta resolução (HRTEM). O Brunauer – Emmett – Teller (BET):Micromeritics II PLUS, EUA, foi conduzido para identificar a área de superfície específica do MNA por adsorção-dessorção de nitrogênio usando NOVA2020e analisador automático de área de superfície e porosidade. Antes da análise, o MNA foi desgaseificado a 100 ° C. As medições do potencial zeta foram realizadas usando um zeta sizer (Malvern ZS, UK). O zeta sizer forneceu uma titulação de vários valores de pH. A investigação das propriedades magnéticas da amostra em pó de MNA foi feita usando um magnetômetro de amostra vibratória (VSM) Modelo:LAKESHORE 7404, com um campo externo aplicado de 0–13 kOe (kG).
Estudos de Adsorção
Os testes de sorção foram realizados em sistema batch. Uma solução estoque de nitrato de cobre (Cu (NO 3 ) 2 ) (50 mgL −1 ) foi preparado e diluído para dar as concentrações adequadas. O pH foi ajustado usando 0,1 molL −1 HCl ou 0,1 molL −1 NaOH. As concentrações inicial e final de Cu 2+ foram determinados usando um espectrofotômetro ultravioleta-visível (UV-Vis) (Modelo:HACH DR4000U) a λ =600 nm, com base na curva de calibração preparada. Todos os testes de sorção foram realizados em frascos de 250 mL, aos quais foi adicionada a quantidade adequada de adsorvente e 100 mL da solução iônica. Os estudos cinéticos foram realizados usando concentração inicial de 1 mg / L de íon Cu (II) com 0,5 g de Fe 3 O 4 . A temperatura e o pH foram mantidos constantes em 25 ° C e pH 7, respectivamente. As concentrações iniciais de íons Cu (II) foram 10, 20, 30, 40, 50 mg / L em 200 mL. O pH foi variado em 2, 4 6, 8, 10 e 12 por adição de HCl e NaOH. Estudos preliminares demonstram que o processo de adsorção atingiu uma condição de equilíbrio em 180 min. Para estudar a dosagem que influenciava as capacidades de adsorção, foram utilizadas diferentes dosagens de MNA, variando entre 10 e 50 mg. A porcentagem de remoção (% RE ) e capacidade de adsorção ( q e ) de Cu 2+ os íons foram determinados usando as Eqs. 1 e 2, respectivamente [59, 60].
$$ \% RE =\ frac {{C_ {o} - C_ {e}}} {{C_ {o}}} \ vezes 100 $$ (1) $$ q_ {e} =\ frac {V} { m} \ left ({C_ {o} - C_ {e}} \ right) $$ (2)
onde C o e C e , representou as concentrações inicial e final (mgL −1 ) da solução, respectivamente. V é o volume da solução em litros, e m é a massa do adsorvente em gramas (g). q e (mg / g) é a quantidade de adsorbato por unidade de massa de adsorvente no tempo t.
Estudo cinético
Os experimentos foram conduzidos usando Jar Tester com 200 mL de solução de cobre a uma temperatura constante de 28 ℃ e pH 5,4. As amostras foram coletadas em um intervalo de tempo diferente em 0, 10, 20, 30, 40 e 50 min e analisadas usando UV-Vis. Os modelos cinéticos foram estudados usando Lagergren pseudo-primeira ordem e pseudo-segunda ordem. A pseudo-primeira ordem de Lagergren é representada na Eq. (3):
$$ q_ {t} =q_ {e} \ left ({1 - e ^ {{- k_ {1} t}}} \ right) $$ (3)
onde q e (mg / g) e q t (mg / g) são as quantidades de adsorvido no equilíbrio e no tempo t , respectivamente, e k 1 (min −1 ) é a constante de taxa de adsorção de pseudo-primeira ordem. Para a taxa de adsorção no mecanismo de segunda ordem, a equação da taxa cinética de pseudo-segunda ordem pode ser expressa como a Eq. (4):
$$ q_ {t} =\ frac {t} {{\ frac {1} {{k_ {2} q_ {e} ^ {2}}} + \ frac {t} {{q_ {t}}}} } $$ (4)
onde k 2 (gmg −1 .min −1 ) é a constante de taxa de equilíbrio de adsorção de pseudo-segunda ordem.
Estudo de regeneração
O MNA foi reivindicado novamente por abordagem de dessorção de solvente quando os locais de poros ativos atingiram o equilíbrio. O MNA foi separado por um ímã externo da solução aquosa e, subsequentemente, mergulhado na solução de HCL e misturado por 180 min a 26 ℃. O MNA resultante foi então lavado com água destilada para atingir pH neutro e então mantido por 1 h a 60 ℃. O MNA regenerado foi então reutilizado em conjunto com estudos anteriores [54, 55]. A eficiência de reutilização (RE%) foi calculada usando a Eq. 5:
$$ RE =\ frac {{q_ {reg}}} {{q_ {ori}}} \ vezes 100 \% $$ (5)
onde q reg e q ori são suas respectivas capacidades de adsorção por unidade de massa do adsorvente regenerado e original.
Análise estatística
Os dados experimentais foram submetidos a um delineamento inteiramente casualizado, e os dados obtidos foram analisados usando análise de variância (ANOVA) por um procedimento de modelo linear geral (GLM) no software SAS 9.4 Versão (SAS Institute Inc., Cary, NC , EUA). O teste de intervalo múltiplo de Duncan foi usado para separar as médias em p <0,05 nível de significância.
Resultados e discussão
Análise Estrutural e de Fase
Os resultados do exame de XRD das escalas do moinho de resíduos após MST e CTST são mostrados na Fig. 2a. Após o processo de MST (Fig. 2ai), o XRD confirmou a presença de wuestita (FeO) e magnetita (Fe 3 O 4 ) A difração de Bragg de wuestita foi observada a 2θ de 36,33 ° (111), 61,40 ° (044), 73,25 ° (113) conforme combinado com ICSD:98–001-2335. A fase de magnetita foi observada a 2θ de 35,61 ° (113) e 43,28 ° (004), concordou com a referência Fe 3 O 4 Arquivo ICSD 98–010-9826.
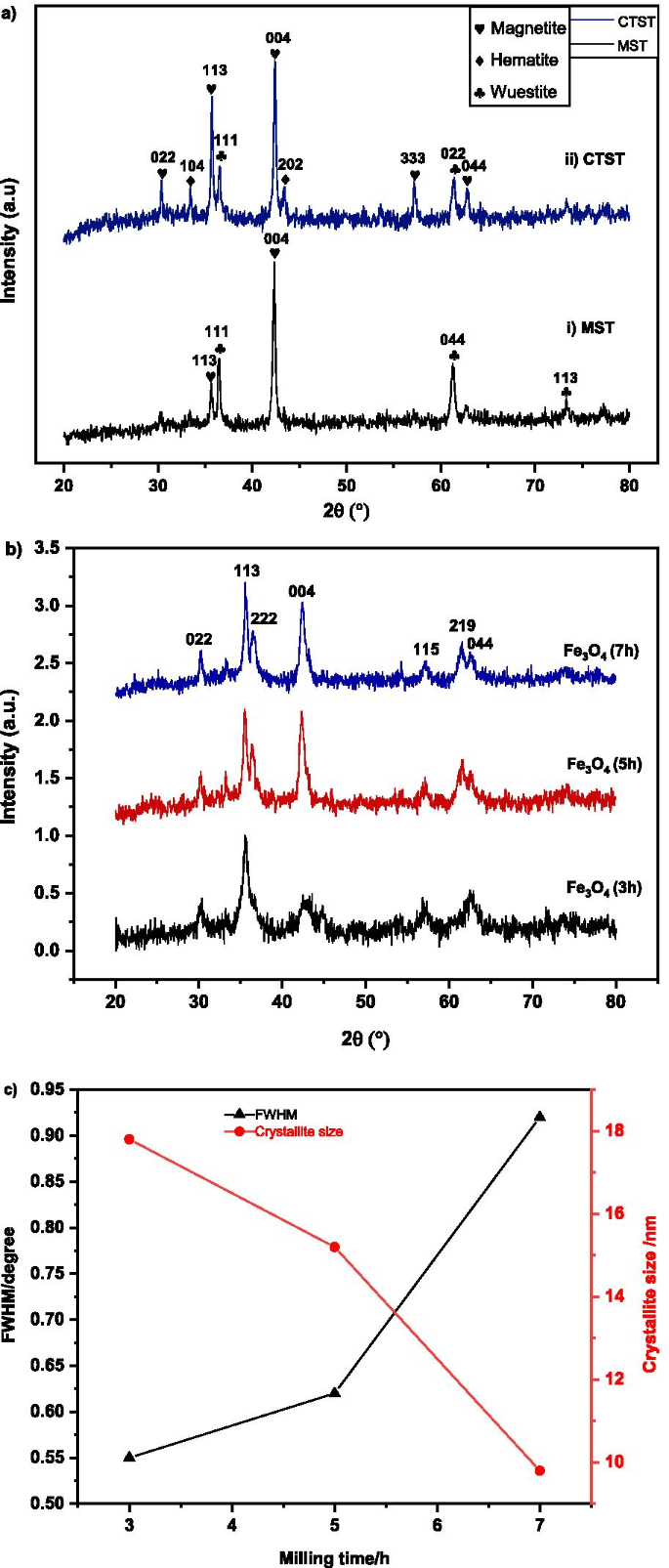
a Espectro de difração de raios-X em escala de moinho após passar por MST e CTST, b espectros indexados de magnetita em diferentes tempos de moagem de 3, 5 e 7 h, c A largura total na metade do máximo (FWHM) e o tamanho do cristalito do MNA com o tempo de moagem
Para o espectro de DRX após o processo de CTST (Fig. 2aii), foi observada a presença de magnetita, hematita e fase wuestita. O ângulo de difração de Bragg (2θ) de todos os picos foi essencial para identificar e concordar com o arquivo ICSD de referência 98-010-9826 para magnetita com os picos sendo 30,23 ° (022), 35,61 ° (113), 43,28 ° (004), 57,24 ° (333), 62,86 ° (044). Os picos de hematita também observados em 33,44 ° (104), 48,48 ° (202) conforme combinado com ICSD 98–004-6407); e ângulos de difração de wuestita de 36,33 ° (111) e 61,27 ° (022) conforme combinado com ICSD:98–001-2335. O resultado foi concordante e semelhante ao relatado na literatura anterior [84].
A Figura 2b ilustra os padrões de difração de XRD de escamas de pó de moinho após o processo de moagem de bolas de alta energia, em diferentes intervalos de tempo de 3, 5 e 7 h. Os espectros de difração da amostra sintetizada revelaram a presença de magnetita (Fe 3 O 4 ) fase com diâmetro nanométrico para todos os tempos de moagem. O ângulo de difração a 2θ de 30,24 °, 36,66 °, 36,57 °, 42,45 °, 57,26 °, 61,54 ° e 62,76 ° pode ser indexado a (022), (113), (222), (004), (224), (115) e (044) confirmando os picos de assinatura de uma célula unitária cúbica Fe 3 O 4 , respectivamente. Os espectros de XRD foram comparados ao ICSD de referência 98–01-11.241 de magnetita com um grupo espacial de Fd -3 m e parâmetro de rede ( a = b = c ) de 8,3440 Å. O adsorvente de nanomagnetita exibe alta pureza com aumento no tempo de moagem, conforme demonstrado na Fig. 2b. A alta energia gerada pela colisão da bola de aço nos frascos é responsável por quebrar a ligação do oxigênio e reduzir a hematita (Fe 2 O 3 ) para a magnetita (Fe 3 O 4 ) Estágio. Com o aumento do tempo de moagem, observou-se que a formação de magnetita nanocristalina foi determinada pelo alargamento dos picos de DRX. Conforme aumenta o tempo de moagem, o alargamento do pico de XRD aumenta, indicando a diminuição do tamanho das partículas. As intensidades de pico de DRX também diminuíram, com o aumento do tempo de moagem. O padrão está indicando a diminuição do tamanho das partículas das amostras [61]. À medida que o tamanho das partículas diminui, as deformações induzidas durante o processo de moagem resultaram em uma diminuição na intensidade do pico e no alargamento do pico de difração. O tamanho médio do cristalito D de amostras foi calculado usando a fórmula Debye-Scherrer como na Eq. (6) [62].
$$ D =\ frac {0.9 \ lambda} {{\ beta \ cos \ theta}} $$ (6)
onde D é o tamanho médio do cristalito, λ é o comprimento de onda do raio-X (0,1541 nm), β é a largura total na metade do máximo (FWHM), e θ é o ângulo de difração. Os espectros de XRD foram analisados automaticamente usando o software X’pert Highscore Plus. A relação de FWHM e tamanhos de cristalito são mostrados na Fig. 2c. A análise mostra que a mudança no pó de MNA microscópico com o aumento no tempo de moagem de 3, 5 e 7 h com a mudança de variação no FWHM e o tamanho médio do cristalito de MNA como mostrado na Fig. 2c. A tendência de variação do FWHM revelou que com o aumento do tempo de moagem a partir de 3, 5 e 7 h, o FWHM apresenta uma tendência de aumento. Com o aumento do tempo de moagem de 3, 5 e 7 h, o tamanho médio do cristalito diminuiu de um valor mínimo de 17,8 nm, 15,2 nm e 9,8 nm, respectivamente.
Composição Morfológica e Microestrutural
As micrografias HRTEM do MNA moído em diferentes tempos de moagem de 3, 5 e 7 h são apresentadas na Fig. 3. As micrografias mostram que as partículas de MNA exibem uma forma irregular durante os três períodos de moagem, conforme mostrado na Fig. 3. Além disso, um tamanho médio de partícula de MNA de 5,53 nm foi observado no tempo de moagem de 3 h em comparação com 14,45 nm (5 h) e 19,16 nm (7 h). Isto implica que um tamanho de partícula de MNA menor poderia ser alcançado em um tempo de moagem mais curto. O tamanho médio das partículas para 3, 5 e 7 h foi obtido na faixa de 10 a 22 nm. Conforme o tempo de moagem aumenta, a micro-deformação na amostra também aumenta [63]. Conseqüentemente, horas de moagem prolongadas produzirão mais tensão nas amostras. O aumento na deformação da rede com o tempo de moagem foi devido a um forte efeito de distorção causado pelo deslocamento e difusão do átomo na rede introduzida durante o processo de moagem. No entanto, efeitos de aglomeração foram observados na amostra de MNA conforme mostrado na Fig. 3, devido ao comportamento de atração magnética do pó de magnetita.

Imagens HRTEM com uma barra de escala de 20 nm de MNA em a 3 h b 5 he c 7 horas de tempo de moagem
Análise de propriedades magnéticas
As propriedades magnéticas das amostras foram investigadas usando um experimento VSM em temperatura ambiente. A resposta da magnetização ( M ) com o campo magnético externo aplicado ( H ) das amostras é mostrado na Fig. 4. A magnetização de saturação ( M s ), remanência ( M r ) e a coercividade ( H c ) das amostras são resumidos na Tabela 1. O valor de coercividade do MNA está na faixa de 200–270 G, a remanência entre 1,5 e 6,6 emu / ge os valores de magnetização de saturação entre 21 e 27 emu / g. Devido ao diâmetro do tamanho da partícula, que é inferior a 20 nm, as amostras têm uma propriedade superparamagnética. A partir dos parâmetros de magnetização (Tabela 1), isso indica que as amostras consistem em uma mistura dos compostos superparamagnéticos e ferromagnéticos que contribuem para o aumento da capacidade de adsorção. A amostra MNA-7 h mostra os parâmetros magnéticos mais elevados (Fig. 4) que contribuíram para a maior capacidade de adsorção do estudo de adsorção de Cu (Fig. 5).
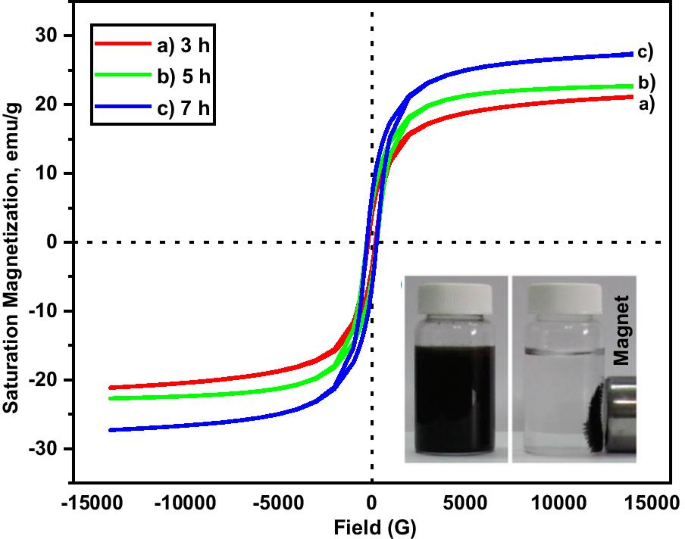
M-H gráfico de histerese de amostras em diferentes tempos de moagem a 3 h, b 5 he c 7 h
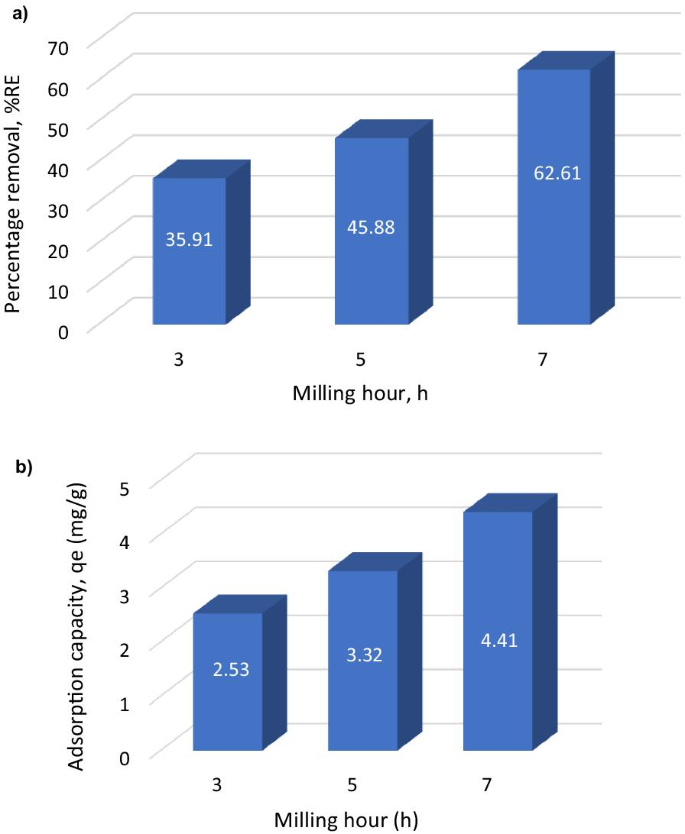
a O gráfico de barras da porcentagem de remoção; b capacidade de absorção / adsorção de metal de MNP em Cu 2+ em diferentes horas de moagem
Efeito dos parâmetros de adsorção
Uma análise adicional no estudo de adsorção em lote de MNA de 3, 5 e 7 h foi investigada. A Figura 5 mostra que o estudo de absorção foi realizado para o MNA em vários tempos de moagem de 3, 5 e 7 h. O gráfico mostra a maior capacidade de adsorção (metal captado) ( q e ) e maior porcentagem de remoção (% RE ) As horas de moagem do MNA-7 h mostram a maior capacidade de adsorção e a maior porcentagem de remoção da solução aquosa. Portanto, o MNA-7 h foi escolhido como o nanoabsorvente do MNA para posterior análise de absorção do lote em vários parâmetros de tempo de contato, concentração inicial, dosagem do absorvente, área de superfície, pH e temperaturas.
Análise da área de superfície
A adsorção de nitrogênio usando BET foi utilizada para avaliar a área de superfície e as características dos poros do MNA para 7 h de moagem. A Figura 6a mostra o resultado de BET para MNA-7 h com volume médio de poro de 0,011 cm 3 g −1 e área de superfície específica de 5,98 m 2 g −1 . O N 2 A curva de adsorção-dessorção de MNA-7 h encontra-se na curva de histerese do Tipo III (Fig. 6b), conforme previamente relatado por Sing et. al. (1985) [65]. Os resultados do BET descrevem as interações adsorvente-adsorvato das moléculas adsorvidas que estão agrupadas na superfície do MNA [66]. Portanto, a adsorção no tipo III revela que as moléculas de gás foram fisicamente adsorvidas no MNA [67].
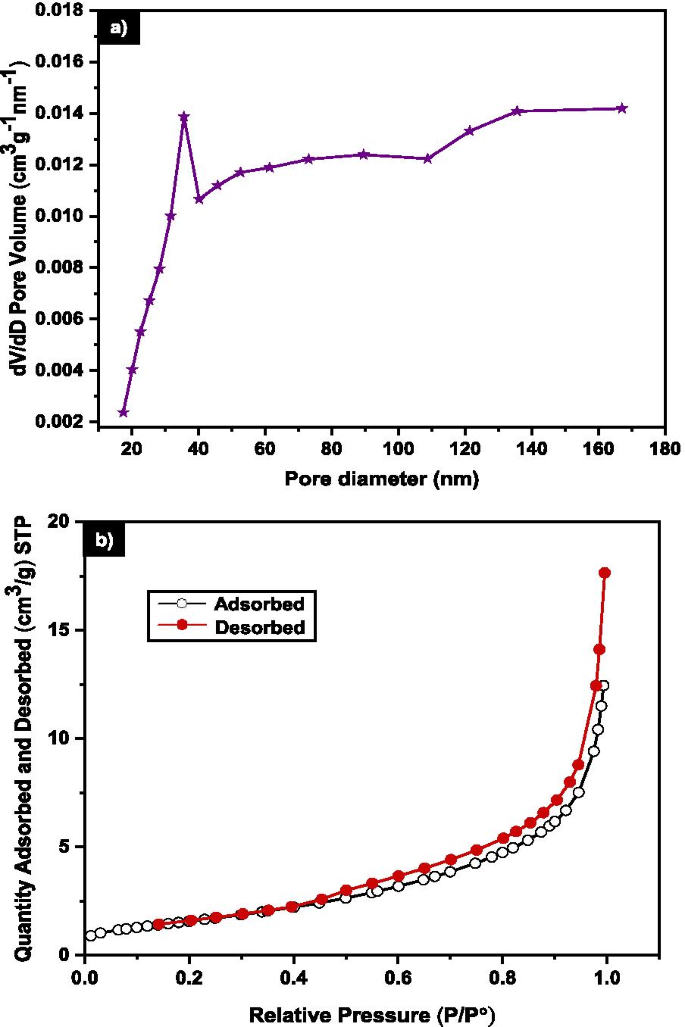
a Distribuição do diâmetro dos poros de 7 h MNA b Isoterma de adsorção-dessorção de nitrogênio
Análise EDS
Os constituintes elementares do MNA-7 h são ilustrados na Fig. 7. As análises FESEM e EDS revelaram a presença dos elementos Fe e O com porcentagem de 78,25% e 21,75%, respectivamente, para MNA-7 h antes do processo de adsorção (Fig. 7a). A Figura 7b mostra os espectros de EDS que mostram a presença do elemento Fe, Cu e O após o processo de adsorção. A existência de cobre no espectro mostra a adsorção de Cu 2+ por MNA. Essa tendência também está de acordo com os espectros exibidos nos estudos relatados por Lingamdinne et al. (2016) [64] como as nanopartículas de óxido de ferro foram utilizadas para a remoção adsortiva de metais pesados.
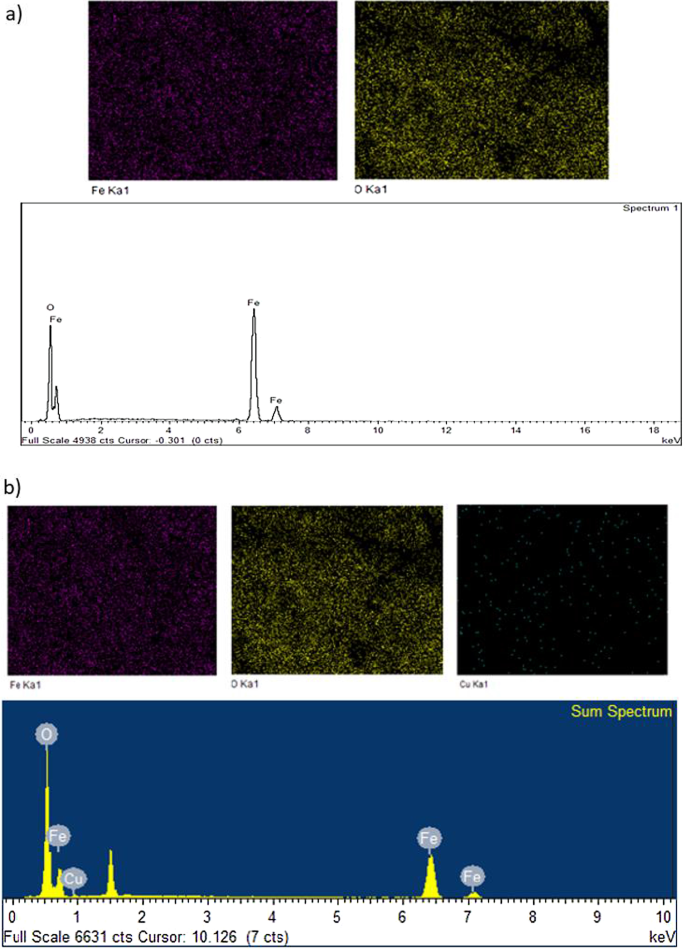
Análise de espectro EDS ( a ) antes da adsorção e ( b ) após a adsorção de íons Cu (II)
Análise FTIR
A confirmação adicional da adsorção de Cu em MNA-7 h também foi determinada por meio de uma análise de FTIR. O FTIR foi investigado para identificar o grupo funcional e ligação de Cu 2+ para o MNA. A Figura 8 mostra os espectros de FTIR do MNA-7 h antes e depois da adsorção de íons Cu (II). Os espectros de FTIR revelam uma banda de pico de características fortes do Fe 3 O 4 nanopartículas. Após a adsorção, o espectro FTIR revela as mudanças na intensidade das bandas na faixa de 500–600 cm −1 e 2800-3600 cm −1 que leva a Cu 2+ sorção. Além disso, as bandas de adsorção em 525 cm −1 e 576 cm −1 representam os sítios tetraédricos e octaédricos das nanopartículas de magnetita de banda Fe-O [68]. O espectro de adsorção forte e amplo em 3478 cm −1 corresponde ao grupo hidroxila (-OH) e traços da molécula de água na superfície do MNA [69]. A espectroscopia de FTIR revela que o MNA possui estrutura cristalina devido à presença de algumas substâncias químicas adsorvidas na superfície do MNA.
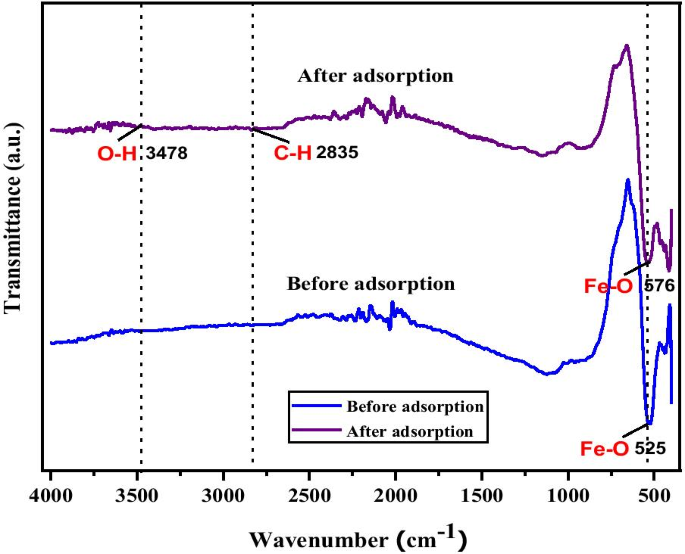
Os espectros de infravermelho da transformada de Fourier do MNA-7 h antes e depois da adsorção do íon Cu (II)
Análise de potencial Zeta
A Figura 9 mostra o potencial zeta de superfície de MNA-7 h. O potencial Zeta foi investigado para obter uma determinação precisa e precisa da carga de neutralização ocorrida no processo de adsorção. Os dados do potencial Zeta fornecem um valor mensurável para monitorar a dosagem de adsorvente ideal durante o processo de adsorção de Cu. Os resultados mostram que o ponto isoelétrico (pH pzc ) ocorreu em pH 5,4, o ponto em que Cu 2+ a adsorção em MNA ocorreu é ótima. Em uma solução aquosa, a superfície dos óxidos de ferro é coberta com OH - grupo, de modo que FeOH na superfície pode mudar para outros grupos funcionais Fe, como FeO ou FeOH 2 , devido ao processo de protonação ou desprotonação [70, 71]. O equilíbrio da protonação e desprotonação depende do pH da solução e do pH pzc do absorvente. Os resultados do potencial zeta sugerem que a adsorção foi eficiente em pH de 5,4.
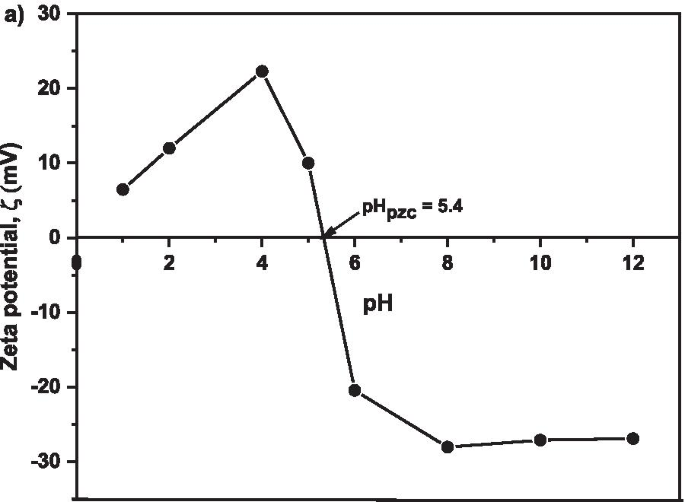
Potencial zeta para valores de pH de 1, 2, 4, 6, 8, 10 e 12 para MNA-7 h
Análise de adsorção em lote
Efeito do tempo de contato
Figure 10a shows the effect of contact time on adsorption capacity and rate of Cu 2+ uptake onto MNA after 250 min. It is evident that at longer contact time, the adsorption capacity reach equilibrium as the pH was kept at 5.4 and adsorbent dosage at 0.05 g. The maximum removal efficiency attained was 62.61% as shown in Fig. 10b. The Cu 2+ removal efficiency surges rapidly from the early first 5 min, and later slower and stable throughout the adsorption process. This is attributed to the fact that the rate of the adsorption capacity was high due to the abundant free binding and active sites of the Cu 2+ . Based on Fig. 10, it was noticed that the percentage removal and adsorption capacity increased rapidly with the increase in contact time at the initial stage. The contact time has a substantial influence on the efficacy of Cu 2+ removal and adsorption capacity. Increase in contact time from 0 to 240 min led to an increase in the removal efficiency of Cu 2+ from 0.81% to 62.61%. For contact time greater than 120 min, the removal efficiency of Cu 2+ remains steady, as the active sites has been saturated on the surface of the adsorbent. Similarly, the highest adsorption capacity of 4.41 mg/g was attained at 120 min of contact time. Thus, the equilibrium time was attained at 120 min.
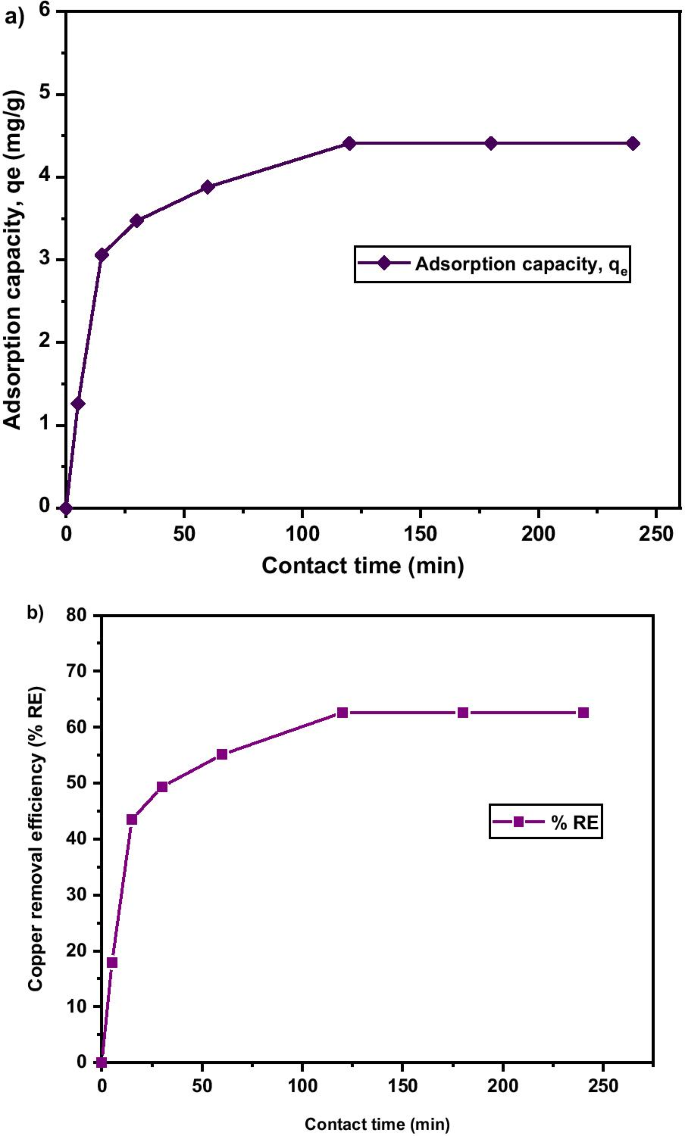
a Adsorption capacity; b Copper removal efficiency under various contact times of MNA-7 h (metal solution:200 mL; temperature:25 °C; initial pH:5.4; initial concentration:50 mg/L; adsorbent dosage:0.05 g)
The results of copper removal efficiency follow a definite trend (Table 2). It shows that the higher the time, the more the removal efficiency. There were significant differences (p < 0.05) among the removal efficiencies under varying contact times. Generally, as contact time progresses, the removal efficacy also improves. Table 3 shows the percentage of the copper removal at different adsorbent dosages. The result shows that as the time progresses, the removal percentage increases. 0.05 g adsorbent dosage recorded the highest copper removal efficiency (62.58 g) after 120 min contact time.
Effect of Initial Concentration
Figure 11 shows as the initial concentration increases, the equilibrium adsorption capacity also increases. Thus, the higher initial concentration due to 0.05 g adsorbent in the Cu 2+ solution to fill the active sites on the adsorbent and the quantity of copper adsorbed increases with the increase in Cu 2+ concentration [83]. The initial concentration of Cu 2+ increased from 10 mg/L to 50 mg/L with corresponding increase in adsorption capacity from 0.04 mg/g to 4.41 mg/g, which in turn provide a higher driving force for the ions from the solution to the adsorbents, resulting in more collisions between Cu 2+ and active sites on the MNA-7 h. Since nearly all the adsorption sites of MNA-7 h existed on their exterior, it is easy for the adsorbate to access these active sites, thereby facilitating a rapid attainment of equilibrium condition.
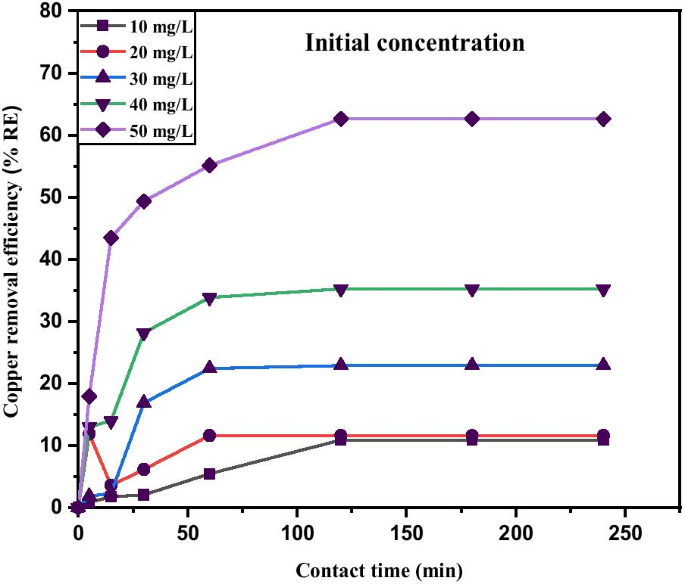
Copper removal efficiency under various initial concentration of MNA-7 h (metal solution:200 mL; temperature:25 °C; initial pH:5.4; adsorbent dosage:0.05 g)
Effect of MNA Dosage
Adsorbent dosage plays an important role during the adsorption process, as it controls the ability of the adsorbent for a given solution. The more the dosage, the more obtainable site for sorption to occur [67]. Figure 12a shows the adsorption capacity, q e of Cu 2+ with respect to different dosages of MNA-7 h at 0.05 g, 0.2 g, 0.5 g, and 0.8 g, respectively. The adsorption capacity was observed to be dependent on adsorbent dosage, which determines the availability of the active sites and the amount of the surface area for adsorption. This is due to the increase in surface area and the probability of collision and interaction between the particles of nano-adsorbent and Cu 2+ [72]. As shown in Fig. 12b, at 0.05 g dosage, 62.61% copper removal efficiency and 4.41 mg/g of adsorption capacity were recorded. The Cu 2+ removal increases sharply and becomes stable as the adsorbent dosage increases. As the adsorbent dosage increases, the larger surface interaction and the agglomeration effects develop. Thus, it causes a decrease in free specific area per unit mass of MNA surface, causing a reduction in contact surface with the adsorbate surface. This will lead to the decrease in q e and %RE. Besides, the decrease in q e and %RE , perhaps was due to the saturation of Cu 2+ in solution with respect to available adsorption binding sites [73]. Thus, a higher amount of adsorbent causes an aggregation which decreases the total surface area of the MNA, thereby leading to a decrease in adsorption capacity [74–76]. The aggregation could result to a decrease in total surface area of the adsorbent and an increase in diffusion path length [75].
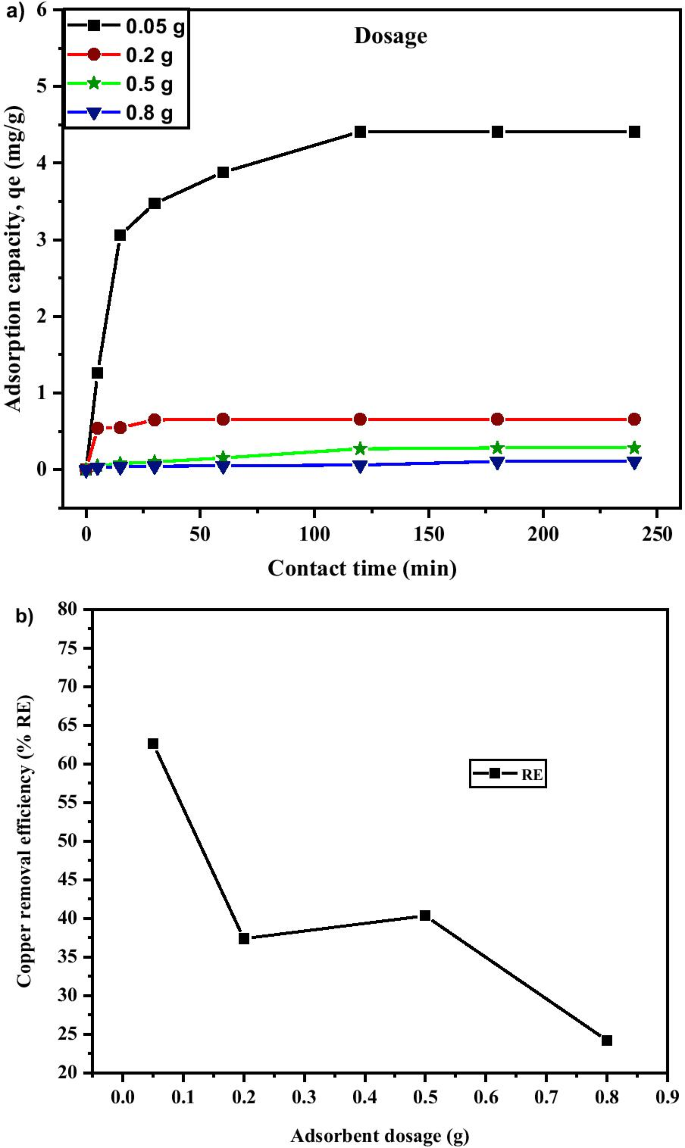
a Adsorption capacity; b Copper removal efficiency under various adsorbent dosage of MNA-7 h (metal solution:200 mL; initial concentration:50 mg/L; temperature:25 °C; initial pH:5.4)
Effect of pH
The removal of Cu 2+ from the aqueous solution through adsorption is highly dependent on the solution pH which determines the surface charge of the adsorbent and the adsorbate speciation [77]. Adsorption is regarded to be minimal at acidic state owing to higher concentration of H3 O + which competes with the positively charged ions for the actively binding site on the adsorbent surface, and this usually led to low contaminant removal [77, 78]. The influence of pH on the adsorption of Cu 2+ on MNA was evaluated between the pH range of (2–12). Figure 13 shows the effect of pH on the adsorption capacity and removal efficiency of Cu 2+ . It was observed that increase in pH from 2 to 5.4, results in an increase in adsorption capacity from 0.58 mg/g to 4.408 mg/g and percentage removal of copper from 10.71% to 62.61%, respectively. However, the equilibrium adsorption capacity of Cu 2+ is low at a strong acidic condition recording 0.58 mg/g at pH 2 due to the presence of a high percentage of H3 O + ion which competes with Cu 2+ at the sorption sites of MNA. Besides, when pH is higher than 5.4, the adsorption capacity decreases from 49.32% to 44.69%. At a higher pH, higher concentration of OH − causes a decrease in the adsorption rate. Figure 13a and b shows that pH has a significant impact on Cu 2+ adsorption capacity and removal percentage (%RE ) of Cu. The removal rate for Cu 2+ increases with an increase in pH, from 10.71% to 28.04% and to 62.61% when pH is at 2, 4 and 5.4, respectively, before declining to 49.32%, 42.56% and 44.69 at pH 8, 10 and 12, respectively (Fig. 13a).
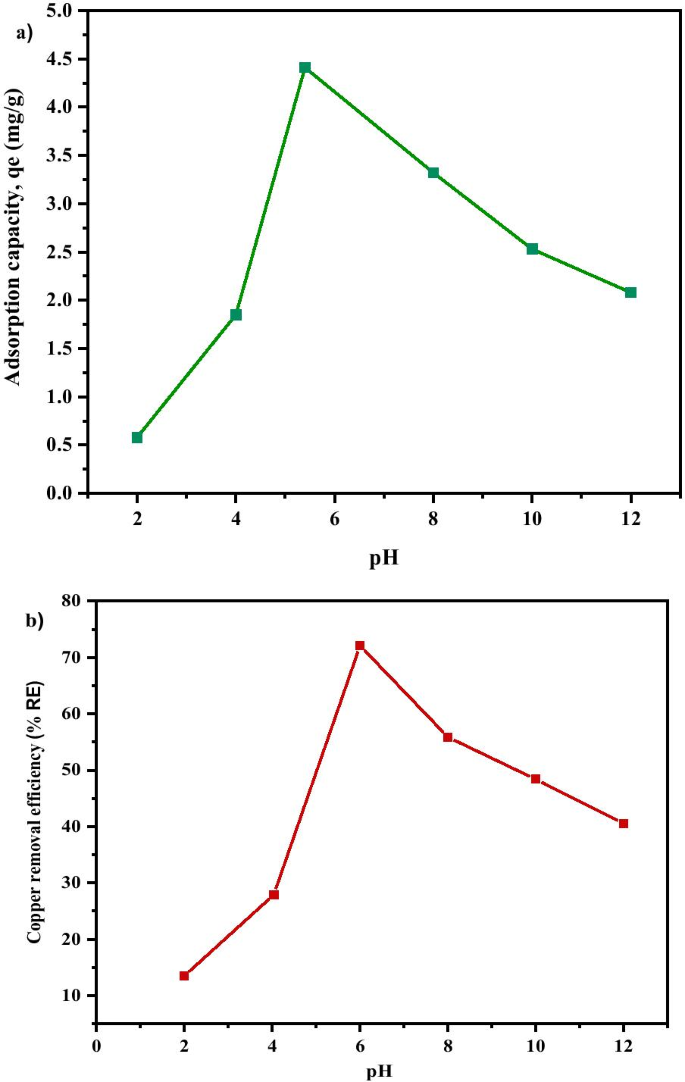
a Adsorption capacity; b copper removal efficiency under various pH of MNA-7 h (metal solution:200 mL; initial concentration:50 mg/L; temperature:25 °C; adsorbent MNA dosage:0.05 g)
Similarly, the adsorption capacity also increases from 10.71% to 62.61% with the increase in pH from 2 to 5.4 and decreases until it reaches pH 12. At pH 2 and 4, the amount of protonation of the adsorbent surfaces results in a decrease in Cu 2+ adsorption. The results also are in agreement with zeta potential graph as indicated in Fig. 9. Also, Fig. 9 describes the net charge of the MNA adsorbent surface at different pHs, with the point of zero charges (pHpzc ) As the pH increases, the H + ion is lower and causes the surface of the adsorbent to become negatively charged, with the increase in %RE of Cu 2+ , thereby increasing the electrostatic attraction force between the adsorbents in the solution [79]. Therefore, pH influences the surface zeta potential of MNA. The surface functionality of iron oxides varies depending on the nature of iron oxides and the pH value.
Copper Adsorption Kinetics
Kinetic studies are essential in the adsorption process to describe the uptake rate performance of MNA-7 h and influence the residual time for the entire adsorption process. The adsorption kinetics of Cu 2+ on MNA-7 h was determined using similar procedures to those used in the batch adsorption studies [55]. The Lagergren’s first-order kinetic model and second-order kinetic model for the removal of Cu 2+ at various initial concentrations from the aqueous solution using MNA at 0.05 g/L of the MNA dosage are shown in Fig. 14. The calculated q e values are in agreement with the theoretical values, and the graph shows good linearity with R 2 above 0.96. Therefore, the adsorption kinetics follows the pseudo-second-order model. The pseudo-second-order model represents the adsorption kinetics, involving donation or electron exchange between adsorbate and adsorbent. Table 4 shows the fitted parameter summary of Cu 2+ kinetics at different initial Cu 2+ concentrations (q e :mg/g, k 1 :min −1 , k 2 :g/mg/min) of MNA-7 h. For the parameters of initial concentration, C i (mg/L), adsorption capacity, q e (mg.g −1 ), k 2 is the rate constant of pseudo-first-order, k 2 is rate constant of pseudo-second-order, and the R 2 is the correlation coefficient. Two kinetic models:Lagergren’s first-order and pseudo-second-order order were applied to further study the rate of adsorption process for Cu 2+ . The kinetic parameters of pseudo-first-order and pseudo-second-order are presented in Table 4. According to Table 4, pseudo-second-order was best fitted for the adsorption of Cu 2+ . Pseudo-second-order revealed a higher correlation coefficient of R 2 = 0.999, for Cu 2+ removal.
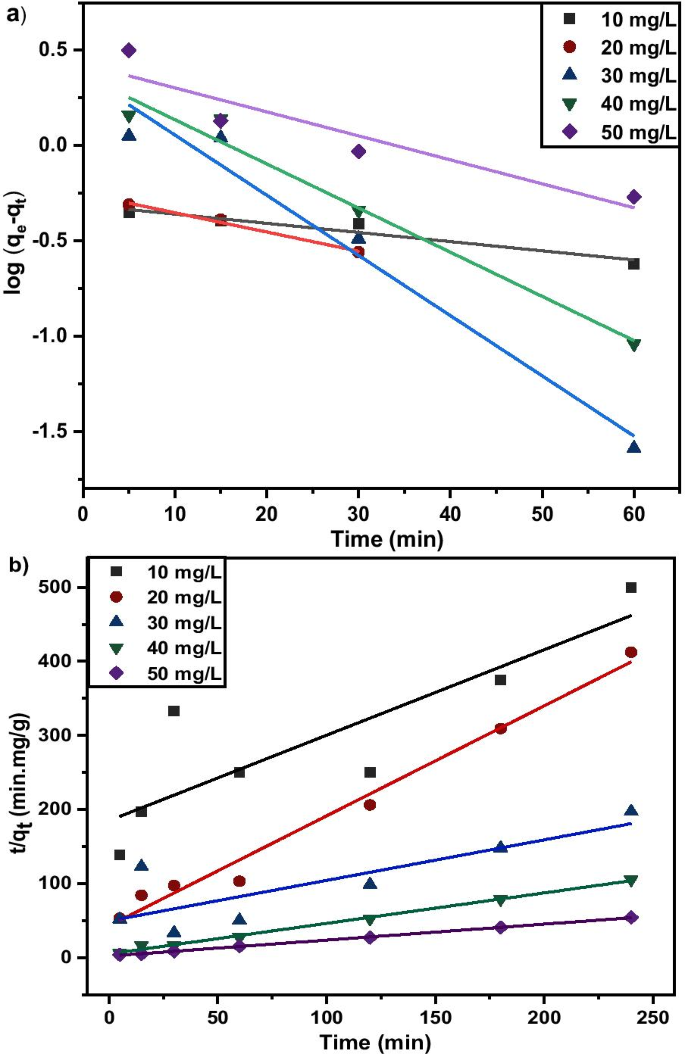
a Lagergren’s first-order kinetic model; b Pseudo-second-order kinetic model for the removal of Cu (II) ions at various initial concentrations from the aqueous solution using MNA at 0.05 g/L dosage of MNA-7 h
Copper Adsorption Isotherms
The adsorption isotherms experimental data were investigated using Freundlich isotherm model (Eq. 7) and Temkin isotherm model (Eq. 8). The adsorption isotherm is illustrated in Fig. 15a and b. The Freundlich isotherm is expressed as:
$$q_{e =} K_{F} \times C_{e}^{1/n}$$ (7) $$qe =B\log kt + B\log C_{e}$$ (8)
where q e is adsorbent capacity at equilibrium (mg/g); B :(RT /b ) is the Temkin constant related to heat of adsorption (J/mol) R is universal gas constant (8.314 J/mol K); T is absolute temperature (K); 1/b indicates the adsorption potential of the adsorbent; kt is equilibrium binding constant corresponding to the maximum binding energy (L/mg); and Ce is adsorbate concentration at equilibrium (mg/L). From the graph, the straight line emerged, and the values of q m and K L constants can be calculated using the slope and the intercept of the straight line. Freundlich and Temkin models was used to examine the relationship between the adsorbent and adsorbate. As shown in Fig. 15, the initial concentrate correlation coefficient with an R 2 value of 0.914 and manifested Temkin adsorption isotherm to be more favourable for the removal of copper. The synopsis of the isotherm parameter of Freundlich, Temkin parameter with correlation coefficient, R 2 for adsorption of Cu (II) on MNA-7 h at room temperature is depicted in Table 5. 1/n constant reciprocal implies natural sorption; therefore, the adsorption process is beneficial. The values of n, 1/n , K F , and R 2 for the current work are also presented in Table 5. Temkin isotherm adsorption plot shows maximum Cu 2+ removal by MNA-7 h at optimal conditions and reveals the feasibility of the process. The data prove that the Temkin model well fitted the experimental data than Freundlich based on the correlation coefficient, R 2 (Table 5). This could be due to the fact that the Temkin isotherm model considers the effect of indirect adsorbate on the adsorption process and assumes that the heat of the adsorption of molecules decreases linearly in the adsorption layer [80].
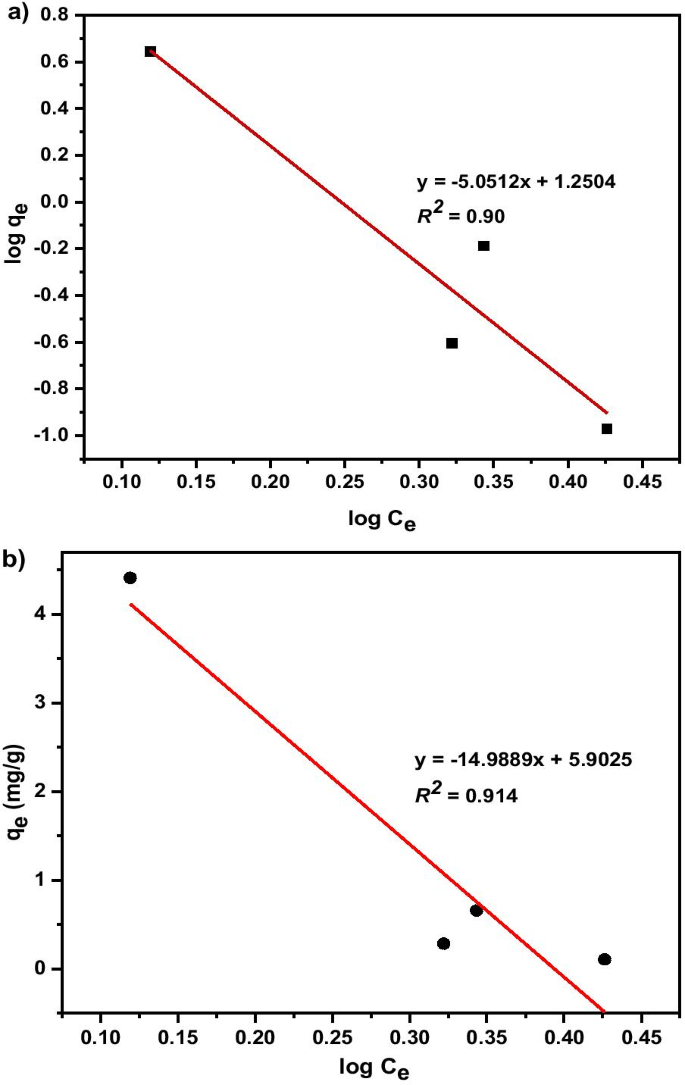
a Linearized Freundlich; b Linearized Temkin isotherm models for Cu 2+ adsorption by MNA-7 h at various adsorbent dosages:contact time 240 min; initial pH 5.4; temperatura do quarto
Regeneration and Desorption Study
The reusability of adsorbent is a prime issue since periodically regenerating adsorbent is strongly desirable for industrial applications [81]. In the reusability tests, the adsorption and desorption cycle of Cu 2+ onto MNA was repeated three times. The adsorption capacity of MNA was recycled, and the regeneration of the MNA of the adsorption–desorption cycle of Cu 2+ was repeated three times using the same MNA. The desorption process was studied for 3 cycles of MNA-7 h. The results proved that the magnetic nanoparticles have higher sustainability for industrial applications. The results also revealed that Cu 2+ could be desorbed from the adsorbent in the presence of deionized water as the desorbing agent. For repeated use of MNA, the adsorbed Cu 2+ were desorbed under suitable conditions. In this work, the percentage of desorption by MNA was obtained by 0.1 M HCl as shown in Table 6. Hence, MNA exhibits an enhanced recovery efficiency of 70.87%. Figure 16 displays the desorption efficiency of MNA. The adsorption capacity decreased by 10% during three adsorption–desorption cycles which indicates the stability and reusability of MNA.
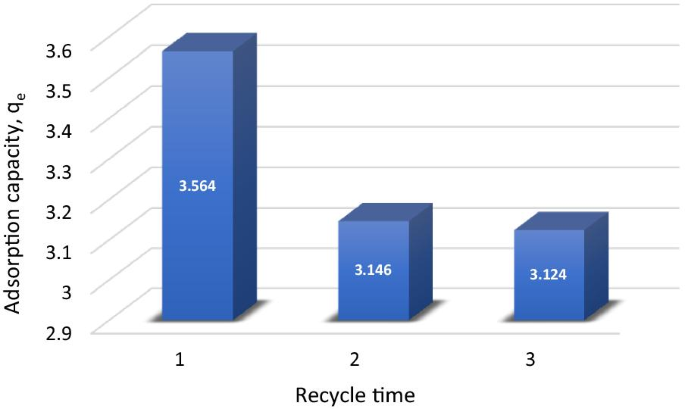
Desorption of copper onto MNA-7 h in three cycles
Conclusions
Novel magnetite nano adsorbent (MNA) from mill scale waste has been successfully synthesized via conventional milling technique and impacted by high-energy ball milling procedure at varying milling time. The high-energy ball milling (HEBM) at 3, 5 and 7 h successfully produced the MNA in the range of 10–25 nm, as confirmed by HRTEM. The HEBM technique was used to reduce the microcrystalline size to nano-sized particles showing the potentials of MNA as an efficient precursor for Cu 2+ removal in an aqueous solution.
VSM results showing the MNA-7 h possess the highest magnetization property and indicate the best absorbent, with the specific surface area of 5.98 m 2 g −1 and the average pore size of 8.01 nm thereby showing the better adsorption capacity. The adsorption of Cu 2+ on MNA-7 h was confirmed by EDS and FTIR analysis. For the adsorption studies, pH at 5.4, dosage of 0.05 g and 240 min of contact time, the highest adsorption capacity, q e and removal efficiency of 4.408 mgg −1 and 62.61% were achieved. Also, at the initial concentration of 50 mgL −1 Cu 2+ , the q e of 4.41 mgg −1 was recorded. The reusability efficiency of 70.87% was attained even after three cycles of reapplications and desorption. The Temkin adsorption isotherm fits best with a correlation coefficient, R 2 of 0.91. Based on these findings, it can be inferred that MNA is a promising precursor for Cu 2+ removal.
Disponibilidade de dados e materiais
The datasets generated during and/or analysed during the current study are available from the corresponding author on reasonable request.
Nanomateriais
- Síntese biogênica, caracterização e avaliação do potencial antibacteriano de nanopartículas de óxido de cobre contra Escherichia coli
- Hidrozincita com suporte de aerogel de sílica e hidrotalcita intercalada com carbonato para remoção de alta eficiência de íons de Pb (II) por reações de transformação de precipitação
- Esfoliação líquida de alta eficiência de nanofolhas de nitreto de boro usando solução aquosa de alcanolamina
- Preparação de nanoesferas poliméricas impressas com íons de paládio (II) e sua remoção de paládio (II) da solução aquosa
- Adepto verde na síntese e estabilização de nanopartículas de cobre:atividades catalíticas, antibacterianas, citotoxicidade e antioxidantes
- Síntese e caracterização de BiOCl modificado e sua aplicação na adsorção de corantes de baixa concentração de solução aquosa
- Síntese rápida de nanocristais de Pt e materiais La2O3 Pt / microporosos usando levitação acústica
- Platycodon saponins from Platycodi Radix (Platycodon grandiflorum) para a síntese verde de nanopartículas de ouro e prata
- Síntese e caracterização de nanoestruturas de cobre puro usando a arquitetura inerente da madeira como modelo natural
- Síntese fácil de nanofios de cobre ultralongos e finos e sua aplicação em eletrodos condutores transparentes flexíveis de alto desempenho



