Estratégia de sinterização hidrotérmica para material de ânodo LiNb3O8 estruturado poroso e oco
Resumo
LiNb de estrutura porosa e oca 3 O 8 o material do ânodo foi preparado por uma estratégia de sinterização hidrotermal assistida pela primeira vez. A evolução da fase foi estudada, e o mecanismo de formação da estrutura porosa e oca foi proposto. A formação da estrutura única pode ser atribuída à existência local da fase líquida devido à volatilização do elemento Li. Como material do ânodo, a capacidade de descarga inicial é 285,1 mAhg −1 a 0,1 C, a maior capacidade de descarga relatada até agora para LiNb 3 O 8 . Mesmo após 50 ciclos, a capacidade reversível ainda pode manter 77,6 mAhg −1 a 0,1 C, cerca de 2,5 vezes do LiNb 3 O 8 amostras preparadas por métodos tradicionais de estado sólido. A melhoria significativa da capacidade de armazenamento de Li pode ser atribuída à estrutura especial porosa e oca, que fornece uma alta densidade de locais ativos e canais paralelos curtos para rápida intercalação de Li + íons através da superfície.
Histórico
Nos últimos anos, muita atenção tem sido dada às estruturas ocas e porosas devido às suas aplicações difundidas em catálise, energia, engenharia ambiental, entrega de drogas e sistemas de sensores [1,2,3,4]. Em comparação com outras baterias de nova energia, as baterias de íon de lítio (LIBs) obtiveram sucesso comercial como a fonte de energia predominante para eletrônicos portáteis e mostram grande potencial em aplicações de grande escala devido à sua alta densidade de energia, longa vida útil e benignidade ambiental [5 ] Para obter alto desempenho eletroquímico, os eletrodos de LIBs sempre possuem estruturas abertas, que podem fornecer uma alta densidade de sítios ativos e canais paralelos para uma intercalação mais rápida de Li + íons através da superfície [6]. No entanto, é um desafio sintetizar os nanomateriais com estruturas abertas, incluindo arquiteturas porosas e ocas.
Para melhorar o desempenho do LIBs, as pessoas têm procurado materiais de eletrodo de alto desempenho, incluindo materiais de ânodo e cátodo. LiFePO 4 [7], LiCoO 2 [8], LiMn 2 O 4 [9], LiVPO 4 F [10], e vários materiais híbridos [11, 12] foram seriamente considerados candidatos para materiais catódicos. Para materiais anódicos, muitos materiais diferentes foram investigados como alternativas aos materiais anódicos à base de grafite, como óxidos de metal de transição (TMOs) [13], dissulfeto de molibdênio (MoS 2 ) e híbridos à base de grafeno [14]. Na literatura recente, o nióbio demonstrou ter desempenho eletroquímico superior [15]; alguns compostos tradicionais dopados com elemento Nb e novos compostos baseados em Nb estão bem desenvolvidos [16,17,18,19]. Os óxidos à base de Nb têm sido considerados materiais de ânodo promissores para LIBs com segurança aprimorada. Comparado com Li 4 Ti 5 O 12 (com uma capacidade teórica de 175 mAhg −1 ), Os óxidos à base de Nb têm uma capacidade teórica relativamente alta de 389 mAhg −1 . Além disso, é notável que os dois pares Nb redox, Nb 5+ / Nb 4+ e Nb 4+ / Nb 3+ , pode suprimir a formação de um filme de interface de eletrólito sólido (SEI) durante o ciclo [19]. LiNb 3 O 8 , um material bastante conhecido, sempre aparecem no processo de preparação do LiNbO 3 como uma fase de impureza devido à volatilização de Li [20]. Jian et al. introduzido pela primeira vez LiNb 3 O 8 material preparado por uma reação de estado sólido como um ânodo para LIBs. Verifica-se que o LiNb 3 conforme preparado O 8 amostra moída em moinho de bola com preto de acetileno (LiNb 3 O 8 -BM) melhorou amplamente as capacidades iniciais de descarga / carga (351 e 212 mAhg −1 ) do que aqueles do LiNb 3 conforme preparado O 8 amostra (250 e 170 mAhg −1 ) a 0,05 C; após 50 ciclos, a capacidade atingiu 150 mAhg −1 para LiNb 3 O 8 -BM a 0,1 C, apenas 30 mAhg −1 para LiNb 3 O 8 amostra [18]. LiNb poroso 3 O 8 nanofibras também exibiram capacidade aprimorada e ciclabilidade em virtude da alta área de superfície, pequenos nanocristais e estrutura porosa com a capacidade de descarga inicial de 241,1 mAhg −1 a 0,1 C [19]. Devido à dificuldade de obtenção de fase pura, como um novo material de ânodo com alta capacidade teórica, LiNb 3 O 8 raramente foi estudado.
Neste artigo, LiNb de estrutura porosa e oca 3 O 8 o material do ânodo foi preparado com sucesso por um processo de sinterização hidrotermal assistida. A evolução da fase foi estudada, e o mecanismo de formação da estrutura porosa e oca foi proposto. As propriedades morfológicas e eletroquímicas do LiNb 3 O 8 como o material do ânodo também foi estudado em detalhes.
Métodos
Preparação de Amostras
LiNb 3 O 8 os pós foram preparados pelo processo de sinterização hidrotérmica assistida. Monohidrato de hidróxido de lítio (LiOH · H 2 O, Aladdin, ACS, ≥98,0%) e pentóxido de nióbio (Nb 2 O 5 , Aladdin, AR, 99,9%) foram adquiridos como matérias-primas sem purificação adicional. Primeiro, 3,5 mmol de Nb 2 O 5 foi disperso em 35 ml de LiOH · H 2 O solução aquosa transparente (a proporção molar de Li:Nb =8:1) com agitação magnética por 1 h. Em seguida, a solução de suspensão foi colocada em um reator de autoclave de síntese hidrotérmica revestido de Teflon de 50 ml. Depois disso, o reator foi selado e mantido a 260 ° C por 24 h e, em seguida, resfriado até a temperatura ambiente naturalmente. Finalmente, os produtos preparados foram centrifugados e enxaguados com água desionizada e etanol. Após secagem em um forno a 60 ° C por 12 h, os pós brancos de Li-Nb-O foram coletados e calcinados em várias temperaturas de 500 a 800 ° C por 2 h com uma taxa de aumento de 5 ° C / min.
Caracterização
A característica de decomposição térmica do pó de Li-Nb-O foi estudada por um calorímetro termogravimétrico e diferencial de varredura (TG / DSC, Netzsch STA 409 PC / PG) desde a temperatura ambiente até 1200 ° C com uma taxa de rampa de 10 ° C / min sob N 2 atmosfera. As estruturas cristalinas dos pós calcinados foram analisadas usando difração de pó de raios-X (XRD; Bruker D8 Discover) com Cu Kα radiação. As morfologias dos pós calcinados foram caracterizadas por microscopia eletrônica de varredura (MEV; JSM-6700F). A análise de espectroscopia de fotoelétrons de raios-X (XPS) foi realizada em um instrumento Thermo-Fisher Escalab 250Xi.
Medições eletroquímicas
O LiNb 3 O 8 eletrodos foram preparados espalhando pasta de LiNb 3 O 8 pós, negro de fumo e fluoreto de polivinilideno (PVDF) com uma proporção de peso de 8:1:1 em uma folha de alumínio. Posteriormente, o eletrodo foi seco a 120 ° C em um forno a vácuo durante a noite. Os ânodos foram puncionados em discos com diâmetro de 16 mm. Para as medições eletroquímicas, células do tipo moeda CR2025 foram montadas em um porta-luvas cheio de argônio usando folha de lítio como contra-eletrodo e membrana microporosa de polipropileno (Celgard 2320) como separador para isolar os dois eletrodos e, em seguida, o 1,0-M LiPF 6 eletrólito foi dissolvido em uma mistura de carbonato de etileno e carbonato de dimetila (1:1 em volume). Os testes de carga-descarga galvanostática das células foram realizados usando um sistema de teste elétrico Land (Wuhan Land Electronics Co., Ltd., China) entre 0 e 3 V (vs. Li / Li + ) em diferentes densidades de corrente de 0,1–1 C (1 C =389 mAhg −1 ) As curvas de voltametria cíclica (CV) foram registradas em uma estação de trabalho eletroquímica (CHI604E, Shanghai Chenhua Instruments Co., Ltd., China) na faixa de voltagem de 1-3 V.
Resultados e discussão
A Figura 1 representa as curvas TG / DSC do pó obtido após a reação hidrotérmica sem calcinação adicional. A perda de peso do pó é muito pequena, cerca de 5%, mesmo quando a temperatura chega a 1100 ° C, mas a perda está ocorrendo ao longo de todo o processo de calcinação. Isso pode ser atribuído à evaporação do elemento Li devido à sua baixa temperatura de fusão, o que é confirmado pelos resultados de DSC com processo de reação endotérmica ao longo de todo o processo de calcinação. A 330 ° C, ocorre um pico endotérmico, que pode se originar da formação de LiNbO 3 . Uma reação exotérmica ocorre a 580 ° C resultante da reação entre LiNbO 3 e Nb 2 O 5 para formar LiNb 3 O 8 . Como visto na curva DSC, além de 1100 ° C, a reação exotérmica se torna forte devido à decomposição do LiNb 3 O 8 .
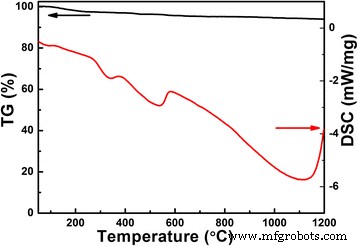
Curvas TG / DSC do pó Li-Nb-O da temperatura ambiente até 1200 ° C a uma taxa de aquecimento de 10 ° C / min em N 2
Os padrões de XRD de pós de Li-Nb-O calcinados em diferentes temperaturas são mostrados na Fig. 2. Pode ser visto que as fases principais são LiNbO 3 e Nb 2 O 5 a 500 ° C. Com o aumento da temperatura de calcinação, o pico de difração em 30,26 ° aparece, o qual pode ser indexado como o plano (410) do LiNb monoclínico 3 O 8 . A reação pode ser descrita pela Eq. (1) não Eq. (2) [21]:
$$ {\ mathrm {LiNb} \ mathrm {O}} _ 3+ {Nb} _2 {\ mathrm {O}} _ 5 \ a {\ mathrm {LiNb}} _ 3 {\ mathrm {O}} _ 8 $$ (1) $$ {\ mathrm {LiNb} \ mathrm {O}} _ 3 \ to {\ mathrm {LiNb}} _ 3 {\ mathrm {O}} _ 8+ {Li} _2 \ mathrm {O} \ uparrow $$ (2)
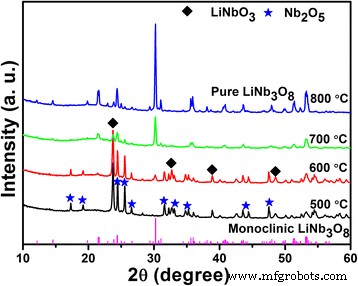
Padrões de XRD do pó Li-Nb-O calcinado em diferentes temperaturas por 2 h
A 700 ° C, o LiNb monoclínico 3 O 8 é a fase predominante com impureza quase insignificante. A fase pura do LiNb 3 O 8 é obtido a 800 ° C com todos os picos de difração indexados à fase monoclínica (cartão JCPDS nº 36–0307), um grupo espacial de P21 / a. Comparado com o método tradicional de estado sólido, a fase pura de LiNb 3 O 8 é mais facilmente obtido usando o processo de sinterização hidrotérmica assistida.
As imagens SEM do LiNb 3 O 8 pó calcinado a 800 ° C com diferentes ampliações são apresentados na Fig. 3. A estrutura porosa e oca que se assemelha a um favo de mel é formada por LiNb 3 O 8 nanopartículas com comprimento de vários micrômetros. A estrutura não é plana, com deformações óbvias, e até forma estruturas fechadas tipo tubby. É totalmente diferente da agregação de partículas que resulta das reações convencionais de estado sólido. O tamanho do LiNb 3 O 8 partícula tem cerca de 200 nm, como mostrado na Fig. 3c. O pequeno tamanho de partícula e a estrutura única são benéficos para a intercalação de íons [6]. A formação da estrutura única pode ser atribuída à volatilização do lítio durante o processo de calcinação, conforme comprovado pelos resultados do TG-DSC. Como a volatilização fácil do elemento Li, o excesso do elemento Li existente no pó migra facilmente para a superfície das partículas e se transforma em fase líquida. A existência local de fase líquida é propícia à formação de novo LiNb 3 O 8 partículas no local e também estimula a formação de redes entre as partículas.

a - c Imagens SEM do LiNb 3 O 8 pó com diferentes ampliações
Para confirmar ainda mais as composições elementares e o estado eletrônico, o LiNb de estrutura porosa e oca 3 O 8 os pós são analisados por XPS, como mostrado na Fig. 4. Os dados XPS foram calibrados usando C 1s como uma referência com a energia de ligação a 284,6 eV. Na Fig. 4a, dois picos em 207,1 e 209,8 eV correspondem a Nb 3d 5/2 e 3d 3/2 , respectivamente, indicando o Nb 5+ estado em LiNb 3 O 8 [22]. Os espectros XPS de O 1s na Fig. 4b podem ser deconvoluídos em dois picos a 530,3 e 532 eV. O primeiro é atribuído às ligações Nb-O, e o último está relacionado ao oxigênio não reticular [22, 23].
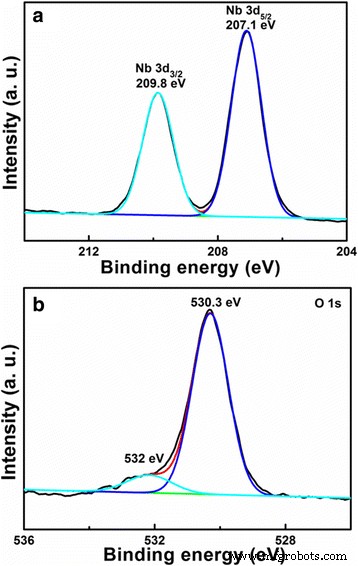
Espectro XPS de ( a ) Nb 3d e ( b ) O 1s para o LiNb3O8 estruturado poroso e oco
Para investigar o desempenho eletroquímico do LiNb preparado 3 O 8 amostra, foram realizados os testes de CV e ciclos de carga-descarga galvanostática. As três primeiras curvas CV de LiNb 3 O 8 pó a uma taxa de varredura de 0,1 mV / s na faixa de 3 ~ 1 V são mostrados na Fig. 5. No primeiro ciclo, dois picos pronunciados (inserção de Li) são observados em 1,13 e 1,30 V; o primeiro pode ser atribuído à redução parcial de Nb 4+ para Nb 3+ , enquanto o último pode estar relacionado à variação de valência total do Nb 5+ para Nb 4+ [18, 19]. Como visto na Fig. 5, os ciclos subsequentes são bastante diferentes do primeiro ciclo. O desaparecimento dos picos em 1,13 e 1,30 V implica que a transição de fase no primeiro ciclo é irreversível. Apenas os picos de oxidação (extração de Li) em 1,71 e 1,96 V permanecem estáveis após o ciclo, implicando na alteração da estrutura do LiNb 3 O 8 a amostra em ciclos subsequentes é reversível.
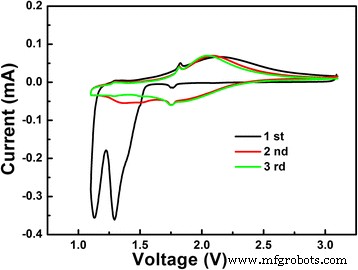
As três curvas CV iniciais do LiNb 3 O 8 pó a uma taxa de varredura de 0,05 mV / s entre as faixas de voltagem de 3–1 V
A Figura 6 mostra as curvas de descarga-carga do LiNb 3 O 8 pó a 0,1 C (aqui, 1 C =389 mAhg −1 ) entre 3 e 1 V no primeiro, segundo, décimo, trigésimo e quinquagésimo ciclos. Na primeira curva de descarga, dois platôs potenciais óbvios podem ser observados em aproximadamente 1,13 e 1,30 V, o que está em bom acordo com os resultados de CV que as reações de duas fases, Nb 4+ → Nb 3+ e Nb 5+ → Nb 4+ , tomar lugar. Porém, nos ciclos subsequentes, os platôs existentes no primeiro ciclo são substituídos por curvas inclinadas, implicando em reações diferentes entre o primeiro e os ciclos subsequentes. Ao mesmo tempo, a capacidade de descarga inicial do LiNb 3 O 8 a amostra é 285,1 mAhg −1 a 0,1 C, a maior capacidade de descarga relatada até agora para LiNb 3 O 8 materiais de ânodo [18, 19]. 4.4 Li por unidade de fórmula pode ser inserido no LiNb 3 O 8 material, correspondendo a uma composição de Li 5.4 Nb 3 O 8 . No entanto, a capacidade de carga no primeiro ciclo é 106,4 mAhg −1 , indicando que apenas 1,6 Li pode ser extraído reversivelmente. A grande perda de 2,8 Li é ambígua no momento.
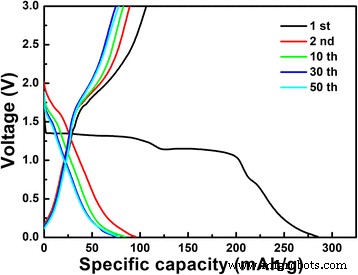
Perfis de carga-descarga galvanostática do LiNb 3 O 8 pó a 0,1 C entre 3 e 1 V
A Figura 7 mostra o desempenho de ciclismo do LiNb 3 O 8 amostra em diferentes taxas de corrente de até 50 ciclos. As capacidades de descarga inicial do LiNb 3 O 8 pó a taxas de 0,1, 0,5 e 1 C são 285,1, 250 e 228 mAhg −1 , respectivamente. A uma taxa atual de 0,1 C, a capacidade reversível ainda pode manter 77,6 mAhg −1 , cerca de 2,5 vezes do LiNb 3 O 8 amostras preparadas pelo método de estado sólido tradicional (cerca de 30 mAhg −1 a 0,1 C, Ref. [18]). A melhoria significativa da capacidade de armazenamento de Li pode ser atribuída à estrutura especial porosa e oca do LiNb 3 O 8 amostra, que fornece uma alta densidade de sites ativos e canais paralelos curtos para intercalação mais rápida de Li + íons através da superfície [6]. Quando as taxas aumentam para 0,5 e 1 C, as capacidades de descarga após 50 ciclos permanecem 39,7 e 29,4 mAhg −1 , respectivamente. Espera-se que a estabilidade da capacidade possa ser melhorada por modificação de superfície adequada no LiNb 3 O 8 material.
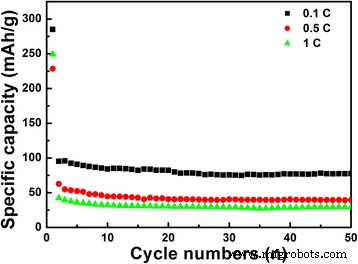
Desempenho de ciclismo do LiNb 3 O 8 pó em diferentes taxas de corrente de 0,1 C, 0,5 C e 1 C
Conclusões
Em resumo, LiNb de estrutura porosa e oca 3 O 8 o material do ânodo foi preparado com sucesso pela estratégia de sinterização hidrotermal assistida. A evolução da fase foi estudada, e o mecanismo de formação da estrutura porosa e oca foi proposto. A formação da estrutura única pode ser atribuída à existência local de fase líquida devido à volatilização de Li. Como o material do ânodo, a capacidade de descarga inicial é 285,1 mAhg −1 a 0,1 C, a maior capacidade de descarga relatada até agora para LiNb 3 O 8 . Após 50 ciclos, a capacidade reversível ainda pode manter 77,6 mAhg −1 , cerca de 2,5 vezes do LiNb 3 O 8 amostras preparadas por métodos tradicionais de estado sólido. A melhoria significativa da capacidade de armazenamento de Li pode ser atribuída à estrutura especial porosa e oca do LiNb 3 O 8 pó, que fornece uma alta densidade de sítios ativos e canais paralelos curtos para rápida intercalação de Li + íons através da superfície.
Nanomateriais
- Pó de metal refratário e seu processo de sinterização
- Um guia para construir e medir uma estratégia de manutenção enxuta
- Consertando uma estratégia de manutenção quebrada:Otimização de PM e FMEA
- TOTAL desenvolve estratégia de manutenção e inspeção
- Chave de inovação de material para 7nm e além
- Avanços na estratégia de transformação digital em petróleo e gás
- Nano e ânodo de bateria:uma revisão
- Os efeitos da relação Li / Nb na preparação e desempenho fotocatalítico de compostos Li-Nb-O
- Composto de MoS2 / Acetileno com poucas camadas como um ânodo eficiente para baterias de íon-lítio
- Preparação e desempenho fotocatalítico de fotocatalisadores de estrutura oca LiNb3O8



