Síntese de solução fácil de nanopartículas de fósforo vermelho para ânodos de bateria de íon de lítio
Resumo
O fósforo vermelho (RP) atraiu grande atenção como um material anódico para baterias de íon-lítio (LIBs) devido à sua alta capacidade específica teórica de 2596 mA h g - 1 e abundância de terra. No entanto, a preparação fácil e em larga escala dos nanomateriais de fósforo vermelho por meio de uma síntese de solução permanece um desafio. Aqui, desenvolvemos um método de solução simples e fácil para preparar nanopartículas de fósforo vermelho (RP NPs). PCl 3 reage prontamente com HSiCl 3 na presença de aminas à temperatura ambiente para produzir RP NPs amorfos com tamanhos de cerca de 100–200 nm em altos rendimentos. Quando usado como um ânodo para bateria recarregável de íon de lítio, o eletrodo RP NP exibe bom desempenho eletroquímico com uma capacidade reversível de 1380 mA h g - 1 após 100 ciclos a uma densidade de corrente de 100 mA g - 1 , e eficiências Coulombic atingindo quase 100% para cada ciclo. O estudo mostra que esta síntese de solução é uma abordagem fácil e conveniente para a produção em larga escala de materiais RP NP para uso em baterias de íon-lítio de alto desempenho.
Introdução
Há muito tempo que se percebeu que os combustíveis fósseis não são renováveis, são finitos e são prejudiciais ao meio ambiente. Baterias de íon de lítio recarregáveis (LIBs) com alta densidade de energia e longo ciclo de vida têm estimulado amplo interesse em pesquisas devido ao seu potencial como sistemas de armazenamento de energia eficientes e baratos [1,2,3]. As crescentes demandas por baterias de íon de lítio (LIBs) de baixo custo com alta densidade de energia e ciclo de vida longo exigem o desenvolvimento de novos materiais para eletrodos [4,5,6,7]. O ânodo de grafite tradicional, comumente usado em baterias de íon de lítio, é limitado em relação às suas baixas capacidades (372 mA h g - 1 ) [8, 9]. Para resolver este problema ou questão, uma grande quantidade de esforços têm sido dedicados para explorar e desenvolver materiais anódicos alternativos com capacidade substancialmente melhorada e eficiências coulombicas [10,11,12,13,14,15,16,17]. Entre uma ampla gama de materiais de ânodo de alta capacidade, o fósforo e seus compostos apresentam aplicações potenciais devido ao seu baixo custo, abundância e alta capacidade específica teórica (≈ 2600 mA h g - 1 ) [18,19,20,21,22].
O fósforo tem três alótropos, P branco, P preto e P vermelho [23]. White P é tóxico e quimicamente instável e não é adequado para aplicação em LIBs. Black P tem boa estabilidade termodinâmica e condutividade, mas o complexo processo de preparação limita suas aplicações em larga escala [24,25,26]. Entre esses três alótropos diferentes, o P vermelho é o candidato mais promissor [27] para a próxima geração de materiais anódicos de alta energia devido à sua estabilidade e abundância. No entanto, o P vermelho é afetado por sua baixa condutividade eletrônica (10 - 12 S m - 1 ) e mudança drástica de volume (300%) durante o processo de litiação-delitiação quando servido como ânodos para LIBs recarregáveis [28, 29].
Para contornar esses impedimentos, o P vermelho foi encapsulado em diferentes tipos de materiais hospedeiros de carbono [30,31,32,33,34,35,36] para melhorar substancialmente o desempenho eletroquímico dos ânodos P vermelho para LIBs. Por exemplo, Li et al. melhorou significativamente o armazenamento de lítio e o desempenho de armazenamento de sódio de P vermelho confinando P vermelho amorfo nanométrico em uma matriz de carbono mesoporosa (P @ CMK-3) via processo de vaporização-condensação-conversão [37]. Ruan et al. projetou uma nova estratégia para incorporar partículas vermelhas de P em um filme de carbono cross-link-estrutural (filme P-C) para uso como um ânodo livre de ligante flexível em LIBs, a fim de melhorar a condutividade eletrônica e acomodar a expansão de volume [38]. No entanto, a taxa de carregamento de P vermelho nos materiais compostos preparados pelo método de vaporização-condensação é tipicamente baixa, o que é desfavorável para a aplicação prática [39, 40]. Para este fim, o uso de nanopartículas ou nanoestruturas ocas de P vermelho preparadas por meio de controle de tamanho e engenharia de morfologia [41, 42] têm sido consideradas estratégias eficazes para acomodar a grande deformação induzida pela expansão de volume e evitar a pulverização do material. Por exemplo, Chang et al. desenvolveu uma síntese em larga escala de nanopartículas de fósforo vermelho (RPNPs) por meio da redução de PI 3 em iodobenzeno por etilenoglicol na presença de CTAB. Os eletrodos RPNP obtidos exibiram uma alta capacidade específica, longa vida útil e excelente capacidade de taxa como ânodos para LIBs [43]. Além disso, Zhou et al. relataram um método solvotérmico úmido para sintetizar nanoesferas ocas de fósforo vermelho com conchas porosas. Os eletrodos ocos de nanosfera P obtidos demonstraram altas capacidades e excelente desempenho em ciclos longos devido aos méritos das estruturas porosas e ocas [44]. Embora várias literaturas tenham relatado os métodos para a síntese em larga escala de fósforo vermelho, o desenvolvimento de um método fácil de alto rendimento e baixo custo para preparar o fósforo vermelho ainda é altamente desejável. Particularmente, a preparação do nanomaterial de fósforo vermelho por meio de uma síntese de solução permanece um desafio.
Aqui, relatamos uma abordagem fácil, rápida e inovadora baseada em solução para sintetizar RP NPs, empregando a reação à temperatura ambiente de PCl 3 com HSiCl 3 em CH 2 Cl 2 na presença de aminas. Esta nova solução fornece uma abordagem econômica para a produção em massa de nanopartículas de fósforo vermelho para uso em baterias de íon de lítio.
Métodos
Materiais
Triclorosilano (HSiCl 3 ) foi adquirido da TCI. n-Tripropilamina (Pr 3 N) foi obtido de Aladdin. Tricloreto de fósforo (PCl 3 ) foi adquirido na Sinopharm Chemical Reagent Co. Ltd. Diclorometano (CH 2 Cl 2 ) foi seco sobre CaH 2 antes de usar. Todos os outros reagentes químicos foram usados como recebidos sem purificação adicional.
Síntese de nanopartículas de fósforo vermelho
Em uma preparação típica, 0,55 mL de Pr 3 N e 0,5 mL de HSiCl 3 foram adicionados em 20 mL de CH anidro 2 Cl 2 . A solução incolor formada foi agitada magneticamente durante a noite à temperatura ambiente, durante a qual a cor se transformou em amarelo claro. E então 0,5 mL de PCl 3 foram adicionados à solução. Nanopartículas de fósforo vermelho (RP NPs) foram obtidas em vários segundos. Os produtos foram centrifugados, separados e lavados com CH 2 anidro Cl 2 , 1 M HF e água destilada para remover PCl 3 não reagido e sílica.
Medições eletroquímicas
As propriedades eletroquímicas das nanopartículas de fósforo vermelho como materiais anódicos em LIBs foram estudadas usando um conjunto de célula tipo moeda 2032 com folhas de metal de lítio servidas como contraeletrodos. As células CR2032 foram montadas em uma caixa de luvas cheia de argônio (ambas H 2 O e O 2 <0,1 ppm). O eletrodo de trabalho foi preparado pela mistura de material ativo (RP NPs), grafite condutiva e carboximetilcelulose de sódio (CMC) em uma proporção de peso de 5:3:2 em água desionizada para formar uma pasta homogênea, que foi então depositada em uma lâmina Folha de cobre. Após secagem a 80 ° C por 12 h em vácuo, a folha foi cortada em discos de 14 mm de diâmetro. O carregamento de massa total de materiais ativos no eletrodo foi de ~ 0,5 mg cm - 2 . O eletrólito era 1,0 M LiPF 6 em uma mistura de 1:1 ( v / v ) carbonato de etileno / carbonato de dietila (Shenzhen Kejingstar Technology Ltd., China). Os perfis de carga-descarga das meias-células foram registrados usando um dispositivo de teste de bateria Neware (Shenzhen, China) em um modo de corrente constante.
Caracterização
A difração de raios-X de pó (PXRD) foi realizada em um difratômetro de raios-X Bruker D8 com uma radiação Cu Kα (λ =1,5418 Å). Imagens de microscopia eletrônica de varredura (SEM) e espectros de espectroscopia dispersiva de energia (EDS) (pastilhas de silício como substrato) foram obtidas em um microscópio eletrônico de varredura de emissão de campo Hitachi (S-4800). Microscopia eletrônica de transmissão (TEM) e TEM de alta resolução (HR) foram realizados com um equipamento JEM-2100 (Japão). N 2 isotermas de adsorção foram coletadas a 77 K (analisador Micromeritics ASAP 2020) após desgaseificação a vácuo da amostra a 100 ° C por 10 h. A espectroscopia Raman (LabRAM Aramis, Horiba, equipada com laser de 633 nm) foi usada para investigar a estrutura de RP NPs. As medições de espectroscopia de fotoelétrons de raios X (XPS) foram registradas com um PHI 5000 VersaProbe. As análises termogravimétricas (TG) foram conduzidas em um analisador térmico STA449F3 (Netzche) simultâneo sob fluxo N 2 . As curvas I-V de RP NPs foram medidas usando o instrumento Biologic VMP3 da estação de sonda criogênica (CRX-4K, Lake Shore, EUA). Os testes de voltametria cíclica (CV) foram realizados em uma estação eletroquímica CHI650d (Shanghai Chenhua Instruments Inc., China).
Resultados e discussão
Síntese e caracterização de RPNPs
As nanopartículas de fósforo vermelhas (denotadas como RP NPs) foram sintetizadas por meio de um método de solução fácil, que é representado no Esquema 1. Descobrimos que o tricloreto de fósforo (PCl 3 ) reagiu prontamente com HSiCl pré-misturado 3 e tripropilamina (Pr 3 N) em CH 2 Cl 2 à temperatura ambiente para produzir laranja em pó em vários segundos. A cor da solução mudou para laranja muito rapidamente ao misturar uma solução de HSiCl 3 –Pr 3 N – CH 2 Cl 2 com PCl 3 , indicando a formação de RP NPs (Arquivo adicional 1:Figura S1). Postulamos que PCl 3 foram reduzidos por cloretos de oligossilano subvalentes para formar as nanopartículas de fósforo. Os cloretos de oligossilano foram formados pela reação de HSiCl 3 com tripropilamina (Pr 3 N) em CH 2 Cl 2 como resultados da reação de desproporcionamento de HSiCl 3 na presença de catalisadores de amina [45,46,47]. Nota-se que os intermediários oligossilanos pré-formados foram essenciais para a ocorrência da reação. Sem aminas (Pr 3 N), a reação de HSiCl 3 com PCl 3 não poderia ocorrer à temperatura ambiente. Da mesma forma, o Pr 3 N não conseguiu reagir com PCl 3 para produzir RP NPs à temperatura ambiente. O rendimento de RP NPs, com base na quantidade de átomos P em PCl 3 , foi de aproximadamente 38%, o que é muito maior do que a literatura relatada [43]. Além disso, esta abordagem de fase de solução utiliza PCl 3 de custo relativamente baixo em vez de PI 3 em iodobenzeno, que poderia ser mais econômica e facilmente escalonado para obter grandes quantidades de RP NPs. A cor dos RPNPs era laranja claro, diferindo da cor vermelha profunda do RP comercial (Arquivo adicional 1:Figura S2).
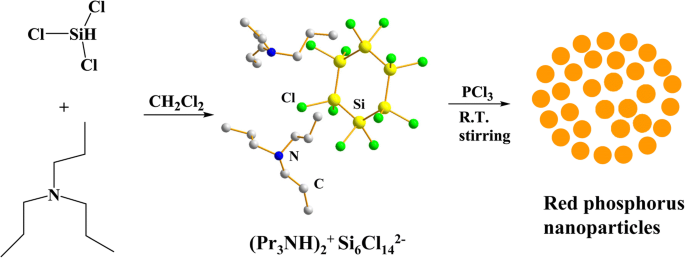
Ilustração esquemática do processo de síntese de RP NPs
A análise PXRD mostrou que o produto era fósforo vermelho. Como mostrado na Fig. 1a, os três picos de difração ampliados em 13-16 °, 25-38 ° e 47-65 °, consistentes com o padrão de XRD de RP comercial relatado na literatura [21, 36]. Imagens SEM mostram que a maioria dos RP NPs sintetizados exibiu forma esférica irregular com tamanhos de cerca de 100–200 nm de diâmetro. O padrão SAED correspondente de RP NPs (imagem de inserção da Fig. 2b) revelou que RP NPs eram de estrutura amorfa. Os espectros Raman de RP NPs apresentaram três picos enrugados entre 300 e 500 cm - 1 , que é consistente com o espectro Raman de RP comercial relatado na literatura [36]. Os três picos podem ser bem atribuídos aos modos de flexão de ligação (modo fundamental B1), vibrações de flexão de ligação (movimento de alongamento simétrico A1) e vibrações de alongamento (modo degenerado E1) de vermelho amorfo P (Fig. 1b). A análise gravimétrica térmica (TGA) de RPNPs na Fig. 3a mostra uma perda de peso acentuada entre 380 e 430 ° C sob uma atmosfera de nitrogênio devido à sublimação, enquanto o RP comercial mostra uma perda de peso acentuada entre 450 e 500 ° C. A depressão observada da temperatura de sublimação de RP NPs pode resultar de altas razões superfície-volume de nanopartículas [43, 48]. Para obter quantitativamente a informação da área de superfície, N 2 medições de sorção (Fig. 3b) foram realizadas. Os resultados revelaram que a área de superfície Brunauer – Emmett – Teller (BET) de RP NPs era de cerca de 37 m 2 g - 1 , que é muito maior do que o RP comercial.
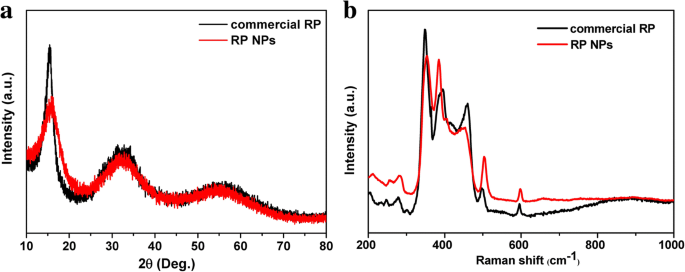
Caracterização de RPNPs. a Padrões de XRD de RPNPs e RP comercial. b Espectros Raman de RPNPs e RP comercial

Morfologia de RP NPs. a Imagens SEM de RP NPs. b Imagens TEM de RP NPs. A imagem inserida é o padrão SAED
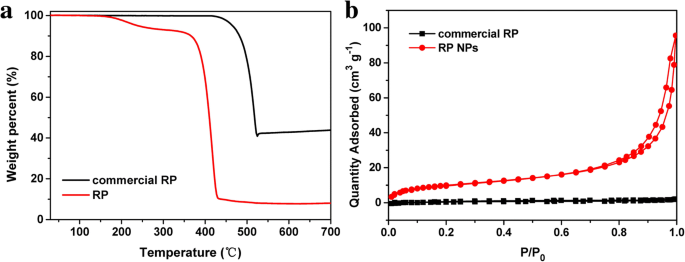
a TGA de RP NPs e RP comercial. b N 2 isotermas de adsorção de RP NPs e RP comercial
A fim de caracterizar ainda mais as estruturas, composições e estados químicos dos RP NPs preparados, medições de espectroscopia de raios-X de dispersão de energia (EDS) e espectroscopia de fotoelétrons de raios-X (XPS) foram realizadas (Fig. 4). O espectro de EDS mostra que RP NPs são quase completamente compostos de fósforo elementar. O espectro de pesquisa XPS (Fig. 4b) confirma ainda que P é o elemento dominante. O pico principal no espectro P 2p de XPS pode ser deconvoluído em dois picos em 129,74 e 130,74 eV, que correspondem ao 2p 3/2 e 2p 1/2 de P na ligação P – P, respectivamente, de acordo com a literatura anterior [49, 50]. Além disso, um pico fraco em 133,50 eV poderia ser atribuído à ligação P – O que foi possivelmente formada através da oxidação da superfície durante a exposição ao ar. Portanto, os resultados acima indicam que as nanopartículas preparadas são P amorfo vermelho. Além disso, as curvas de corrente-tensão (I-V) de RP NPs foram medidas, conforme mostrado no Arquivo adicional 1:Figura S3. A condutividade dos RPNPs é de cerca de 1,7 × 10 - 7 S m - 1 (0–2 V), que é 10 5 vezes maior do que o RP comercial (10 - 12 S m - 1 )
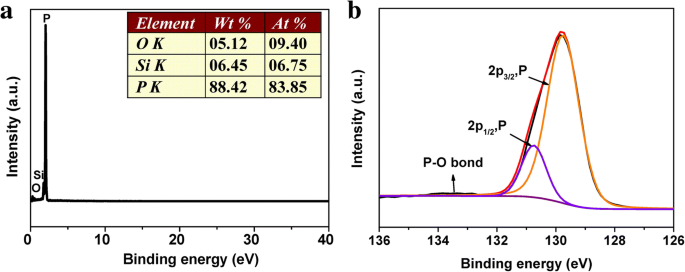
a Espectros EDS de RP NPs. b Espectro P 2p XPS de RP NPs
O desempenho eletroquímico dos RP NPs como materiais anódicos em LIBs foi testado em células tipo moeda CR2032 usando uma folha de metal de lítio como contra-eletrodo dentro das tensões operacionais de 0,01 a 2,5 V. A Figura 5a representa curvas CV típicas dos RP NPs em uma varredura taxa de 0,1 mV s - 1 . Há um amplo pico no primeiro ciclo de litiação, que é atribuído ao processo de ativação de inserção de íons Li no fósforo. Um par de picos redox localizados em 0,5–0,75 V e 1,0–1,25 V são atribuídos à litiação de P e à deslitiação de ligas P – Li [32, 51, 52], respectivamente. O desvio entre a primeira e as curvas catódicas subsequentes implica em perda de capacidade irreversível, que poderia ser atribuída à formação da interface de eletrólito sólido (SEI), bem como à ocorrência de reações colaterais nas superfícies do eletrodo, tais como reações colaterais de defeito locais, oxigênio de superfície e impurezas da água [36, 37, 53], um comportamento comumente observado para ânodos LIB. A Figura 5b mostra os perfis de tensão de descarga-carga típicos do eletrodo RP NPs para os primeiros 3 ciclos a uma densidade de corrente de 0,1 A g - 1 . A descarga curta aparente e os platôs de tensão de carga em torno de 0,7 V e 1,1 V são devidos à litiação e deslitiação dos componentes RP NPs, respectivamente, que concordam bem com os resultados de CV. O eletrodo forneceu uma descarga específica e capacidades de carga de 2818 e 1641 mA h g - 1 , respectivamente, para o primeiro ciclo, dando uma primeira eficiência coulômbica de 58,2%. A capacidade de carga diminuída pode ser atribuída à formação irreversível da membrana SEI. Observa-se que a eficiência coulômbica de RP NPs aumentou rapidamente para 100% após o segundo ciclo. Os RP NPs exibiram um declínio de capacidade óbvio nos primeiros 3 ciclos. A capacidade irreversível nas primeiras etapas descarga-carga resultou da decomposição do eletrólito, o que ocasionou a formação de SEI na superfície do eletrodo e o consumo de íon-lítio. Além disso, as nanopartículas possuem uma grande área superficial em contato com a solução eletrolítica, o que resultaria em mais reações colaterais, diminuindo a eficiência coulombica inicial no primeiro ciclo [54].
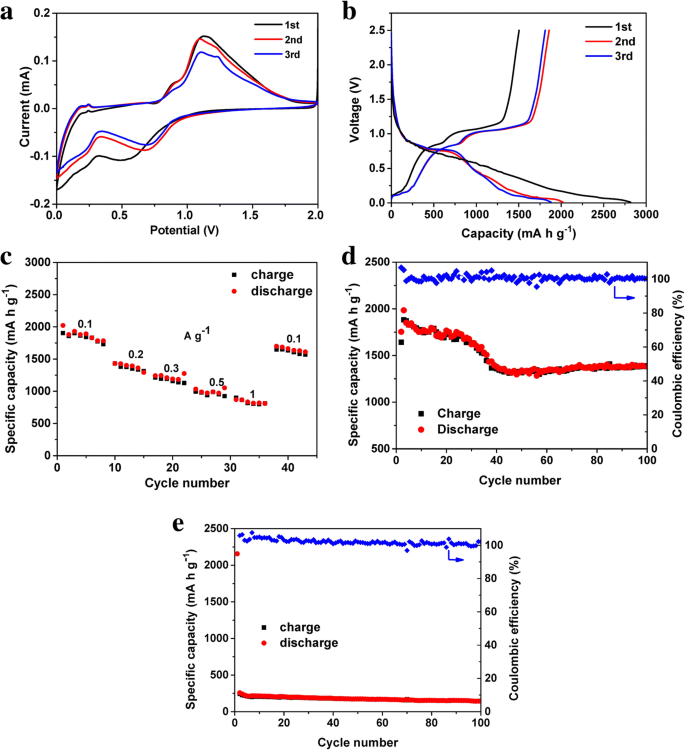
Desempenho eletroquímico de RPNPs. a Curvas CV dos RPNPs. b Perfis de tensão dos RPNPs. c Taxa de desempenho dos RPNPs em ciclos em diferentes densidades de corrente. d Desempenho de ciclagem de RPNPs a uma taxa de 0,1 A g - 1 . e Desempenho de ciclismo de RP comercial a uma taxa de 0,1 A g - 1
A taxa típica e desempenho de estabilidade de ciclo de longo prazo do eletrodo RP NPs são mostrados na Fig. 5c, d, respectivamente. RPNPs entregou as capacidades de carga específicas de 1801, 1430, 1245, 1227, 1184 e 871 mA h g - 1 nas taxas de 0,1, 0,2, 0,3, 0,5 e 1 A g - 1 , respectivamente. O eletrodo apresentou boa reversibilidade de taxa, com a capacidade de descarga específica recuperada para o valor inicial quando a densidade de corrente voltou a 0,1 A g - 1 após o ciclo em altas densidades de corrente. Os RP NPs finalmente mantiveram uma alta capacidade de descarga reversível de 1380 mA h g - 1 , isto é, a retenção de 89,1%, após 100 ciclos com eficiências coulombicas próximas de 100% ao longo das medições. Em comparação com RP comercial (Fig. 5e), RP NPs mostraram uma estabilidade de ciclo de longo prazo muito melhorada.
Conclusões
Em resumo, desenvolvemos uma nova abordagem de fase de solução fácil para sintetizar nanopartículas de fósforo vermelho através da reação de PCl 3 e HSiCl 3 na presença de aminas sob o meio ambiente. O RP NPs exibiu um desempenho eletroquímico muito melhor com alta capacidade reversível e estabilidade de ciclo de longo prazo do que o RP comercial quando servido como ânodo para bateria de íon de lítio recarregável. Os eletrodos RP NPs mantiveram uma alta capacidade de descarga reversível de 1380 mA h g - 1 (retenção de 89,1%) após 100 ciclos, com eficiência coulômbica próxima a 100% em cada ciclo. Este método de preparação simples abre caminho para a produção econômica de RP NPs como ânodos de alto desempenho para a indústria de baterias de íon-lítio.
Abreviações
- CH 2 Cl 2 :
-
Diclorometano
- CV:
-
Voltametria cíclica
- EDS:
-
Espectroscopia de energia dispersiva
- HSiCl 3 :
-
Triclorosilano
- PCl 3 :
-
Tricloreto de fósforo
- Pr 3 N:
-
n-tripropilamina
- PXRD:
-
Difração de raios-x de pó
- RP NPs:
-
Nanopartículas de fósforo vermelho
- SEM:
-
Microscopia eletrônica de varredura
- TEM:
-
Microscopia eletrônica de transmissão
- TG:
-
Termogravimétrico
- XPS:
-
espectroscopia de fotoelétrons de raios-X
Nanomateriais
- Nanocristais de estanho para bateria futura
- Nano e ânodo de bateria:uma revisão
- Síntese fácil e propriedades ópticas de pequenos nanocristais de selênio e nanorods
- Síntese fácil de nanopartículas de SiO2 @ C ancoradas em MWNT como materiais de ânodo de alto desempenho para baterias de íon-lítio
- Membranas compostas contendo nanopartículas de trocadores de íons inorgânicos para dessalinização eletrodialítica de glicerol
- Síntese fácil de compósito CuSCN colorido e condutor revestido com nanopartículas de CuS
- Crescimento direto de estruturas ZnO semelhantes a penas por uma técnica de solução fácil para aplicação de detecção de foto
- Nanopartículas de sílica para entrega de proteína intracelular:uma nova abordagem de síntese usando proteína fluorescente verde
- Método de pós-tratamento para a síntese de nanopartículas FePt-Fe3O4 binárias monodispersas
- Uma solução imersiva para baterias EV termicamente mais seguras



