Melhoria da ciclabilidade do ânodo de metal de lítio por meio da construção de um canal de íons interlamelar atômico para bateria de enxofre de lítio
Resumo
A migração uniforme de íons de lítio (Li) entre o separador e o ânodo de lítio é crítica para alcançar a deposição de Li de boa qualidade, o que é muito significativo para a operação de bateria de metal de lítio, especialmente para baterias de enxofre de lítio (Li-S). Os separadores comerciais, como polipropileno ou polietileno, podem ser preparados por processos úmidos ou secos, mas podem, de fato, causar porosidades abundantes, resultando na separação / revestimento irregular de íons de lítio e, finalmente, na formação de dendritos de lítio. Assim, construímos um canal de íons interlamelar atômico, introduzindo a montmorilonita em camadas na superfície do separador para orientar o fluxo de íons de Li e obter deposição de Li estável. O canal atômico interlamelar com espaçamento de 1,4 nm apresentou forte capacidade de absorção de eletrólitos e reserva de íons Li, promovendo rápida transferência de íons Li e resultando em deposição uniforme de íons Li no ânodo. Quando montado com o separador proposto, a eficiência coulômbica das baterias Li || Cu foi de 98,2% após 200 ciclos e um revestimento / decapagem estável mesmo após 800 h foi alcançado para as baterias simétricas Li || Li. É importante ressaltar que o separador proposto permite um aumento de capacidade específica de 140% após 190 ciclos com o emprego de baterias Li – S.
Introdução
Com a demanda cada vez maior por aplicações eletrônicas de alto desempenho, como veículos elétricos e sistemas portáteis, a pesquisa focada em dispositivos de armazenamento de energia com alta densidade de energia e ciclo de vida longo tem recebido grande atenção [1,2,3]. Especificamente, as baterias de metal de lítio (LMBs), como as baterias de enxofre de lítio (Li-S), são capazes de fornecer excelente desempenho de armazenamento de energia devido à alta densidade de energia, com potencial para aplicações práticas [4,5,6]. Notavelmente, o metal de Li tem sido empregado como um material de ânodo promissor, uma vez que tem alta capacidade teórica de armazenamento (~ 3860 mAh g −1 ), baixo potencial padrão (- 3,04 V vs. o eletrodo de hidrogênio padrão) e densidade de peso leve (0,53 g cm −3 ) No entanto, a existência de poros irregulares em separadores comerciais pode levar à má qualidade do lítio depositado, o que pode resultar na formação dendrítica e consumir mais metais de lítio e eletrólitos durante os processos repetidos de galvanização / decapagem [7, 8].
Consequentemente, os dendritos de Li poderiam formar o metal de Li “morto” quando eles são facilmente quebrados do coletor condutor, resultando em baixa eficiência de Coulomb (CE) e perda de capacidade irreversível [9, 10]. Além disso, dendritos de Li podem perfurar o separador e, assim, causar curto-circuito de LMBs, levando ainda mais à fuga térmica, incêndio e até mesmo possível explosão de baterias recarregáveis [11, 12]. Por causa de tais obstáculos, o uso de LMBs em baterias recarregáveis foi de fato limitado nos últimos 20 anos. Portanto, prevenir a formação de dendritos de lítio pode ser uma abordagem eficaz para explorar totalmente os recursos promissores dos LMBs [13]. Recentemente, pesquisadores propuseram vários métodos para resolver o problema acima, incluindo a otimização da composição do eletrólito [5, 14], a construção da camada de interfase de eletrólito sólido artificial (SEI) no ânodo de metal de Li [15], o desenvolvimento do ânodo de Li compósito tridimensional [ 16], e modificando o coletor [17, 18]. Embora essas estratégias tenham sido projetadas para estabilizar a camada SEI e / ou reduzir a densidade de corrente aplicada efetiva de metais de lítio, elas se concentraram principalmente em metais de lítio e eletrólitos. Até o momento, apenas alguns trabalhos foram conduzidos para abordar ou mitigar os desafios dos dendritos, modificando o separador [19]. Evidentemente, regular o separador pode ser um método novo e viável para inibir a formação de dendrito de lítio.
Entre os componentes dos LMBs, o separador não apenas desempenha um papel fundamental para segmentar os eletrodos anódicos e catódicos para evitar curto-circuito, mas também afeta diretamente o desempenho das baterias por meio da autorização de migração de íons de lítio [9, 20, 21]. Assim, foi relatado que a modificação simples do separador usando camada intermediária de eletrólito de polímero semissólido [22], grafeno [23] ou revestimento de superfície de alto módulo [24] pode efetivamente prevenir a formação de dendritos e, assim, melhorar o desempenho dos LMBs. Entre as abordagens relatadas anteriormente, no entanto, as camadas de barreira eram espessas (> 10 µm) e tinham alta carga de massa (vários miligramas), o que pode inevitavelmente impedir a rápida difusão de íons de lítio e reduzir a densidade de energia dos LIBs. Além disso, a maioria dos LMBs que usam esses separadores funcionais só podem circular com baixas densidades de corrente, por exemplo, menores que 2 mA cm −2 . Para melhorar a densidade de corrente crítica de LMBs, a adição de partículas inorgânicas dentro do separador para melhorar a estrutura porosa e aumentar a densidade de corrente crítica pode ser outro método eficaz. No entanto, a distribuição desigual dos poros no separador pode geralmente levar à difusão desordenada de íons Li durante o processo de galvanização / tira, levando à deposição desigual de íons Li e à formação de dendritos de Li [7]. Portanto, a microestrutura do separador com um canal de transferência de lítio uniforme é muito benéfica para eliminar o problema encontrado de dendrito durante os processos de carga / descarga.
Neste trabalho, com o objetivo de orientar a migração de íons Li de maneira uniforme através do separador, um separador composto modificado de montmorilonita à base de Li (Li-MMT) é fabricado por meio da construção de canais de íons interlamelares atômicos no separador de PP. O separador conforme preparado incorporado com espaçamento interlamelar (~ 1,4 nm) fornece locais ativos abundantes para difusão de íons de lítio e umedecimento de eletrólito [25]. Assim, o separador modificado é permitido atingir a deposição uniforme de íons de Li no ânodo de Li unificando a direção dos fluxos de Li, o que pode efetivamente eliminar os problemas de dendrito de Li nos processos de carga / descarga. Como resultado, o separador Li-MMT permite que as baterias Li || Cu forneçam 98,2% CE mesmo após 200 ciclos e garante que as baterias simétricas Li || Li atualizem o revestimento / decapagem estável por mais de 800 h a 1 mA cm -2 com capacidade de 1 mAh cm −2 . Além disso, as baterias com separadores Li-MMT @ PP também oferecem boa estabilidade de ciclo com 140% da capacidade específica aumentada em comparação com separadores PP após 190 ciclos a 0,5 mA cm −2 com carga de enxofre de 1,5 mg cm −2 .
Métodos Experimentais
Materiais e preparações
A montmorilonita (MMT), o fluoreto de polivinilideno (PVDF) e o hidróxido de lítio (LiOH) foram adquiridos à Aladdin. A N-metil pirrolidona (NMP) e ácido sulfúrico (H 2 SO 3 ) foram obtidos da Sinopharm Chemical Reagent Co., Ltd. O pó de enxofre (S) e o negro de acetileno (denotado como pó C) foram adquiridos a Alfa Aesar. Celgard 2500 foi usado como separador. O pó de Li-MMT foi preparado por meio de troca catiônica. Normalmente, 0,2 M H 2 SO 3 solução foi usada para converter os cátions dentro da camada intermediária de MMT para íons e, em seguida, a solução de LiOH foi usada para fazer a solução em PH =7, bem como converter os íons hidrogênio para os íons Li. A tecnologia de liofilização foi usada para coletar o pó de Li-MMT. Para a preparação do separador Li-MMT @ PP, apenas um lado do separador foi revestido com a pasta de Li-MMT que Li-MMT e pó de PVDF com proporção de massa de 9:1 foram uniformemente dispersos na solução de NMP e o carregamento de massa médio de Li-MMT tem apenas ~ 0,15 mg cm −2 .
Caracterização
O espectro de difração de raios-X (XRD) usando um difratômetro UltimaIV com radiação CuKα1 (λ =1,4506 Å) foi empregado para investigar a estrutura cristalina do pó de Li-MMT. Microscópio eletrônico de transmissão de alta resolução (HRTEM) foi usado para observar a intercamada de Li-MMT e o microscópio eletrônico de varredura (MEV, FEI NANOSEI 450) foi usado para analisar as morfologias de superfície.
Medições eletroquímicas
Para os testes de bateria Li || Cu e Li || Li, normalmente, as folhas de Cu foram primeiro lavadas com água deionizada e etanol três vezes para remover as possíveis impurezas. Em seguida, a folha de lítio foi cortada em círculos com área de 1 cm −2 para usar como fontes de Li. O eletrólito era 1 M de sal de lítio bistrifluorometanossulfonimida (LiTFSI) em uma mistura de 1,3-dioxaciclopentano (DOL) e 1,2-dimetoxietano (DME) (1:1 v / v) com 2% em peso de nitrato de lítio (LiNO 3 ) como aditivo. Para os testes de bateria Li – S, o cátodo S foi preparado através de nosso método anterior em que o pó C e S foram misturados e aquecidos a 155 ℃ por 24 h com uma razão de massa de 8:2 [26]. E então os pós dos compósitos C / S, C e PVDF com razão de massa de 8:1:1 foram uniformemente dispersos na solução de NMP para preparar o eletrodo de enxofre. A carga média de enxofre é de 1,5 mg cm −2 que foi revestido na folha de alumínio revestida com carbono. As baterias foram montadas por meio de bateria tipo moeda de aço inoxidável (CR2025) em um porta-luvas cheio de argônio. A folha de li foi usada como ânodo. 20 µL de eletrólito foram usados para umedecer o ânodo de lítio e 20 µL adicionais foram usados para umedecer o separador e o cátodo. Antes do teste, as baterias de Li – S montadas descansaram 12 he depois 0,2 mA cm −2 com 5 ciclos foi usado para ativar o desempenho da bateria. O sistema de teste eletroquímico foi o sistema de teste de bateria CT2001A (LAND Electronic Co., China). A tensão de corte foi de 1,7–2,7 V. A espectroscopia de impedância eletroquímica (EIS) foi testada pela estação de trabalho Eletroquímica (CHI660E, Chenhua Instruments Co., China).
Resultados e discussão
Para ilustrar o fluxo de íons de lítio através do separador de PP comercial, os esquemas são mostrados na Fig. 1a, b, em que a camada Li-MMT de ~ 5 µm foi uniformemente revestida no separador de PP para guiar o fluxo de íons de Li. É bem conhecido que o separador de PP comercial é tipicamente preparado por processos secos ou úmidos e, em seguida, o separador é esticado para gerar muitos vazios para permitir a passagem de íons de lítio. No entanto, o separador de PP comercial mostra caminhos desordenados e poros empilhados arbitrariamente (Fig. 1a), portanto, pode falhar em realizar a migração uniforme de íons de lítio e, finalmente, causar dendritos de lítio. Portanto, o canal de íon atômico Li-MMT foi empregado como o modulador para guiar o fluxo uniforme de íons de Li (Fig. 1b) e alcançar a deposição uniforme de Li. A estrutura cristalina do MMT é tipicamente composta de camadas carregadas negativamente (NCLs) separadas por espaço intercamada (> 1 nm), que hospeda os íons cátions trocáveis, como Li + , Na + , Mg 2+ , Ca 2+ , etc. Portanto, o método de troca catiônica é necessário para converter os cátions hospedeiros em íons Li [25]. A estrutura básica dos NCLs é uma camada T-O-T típica, onde "T" representa a folha tetraédrica e "O" representa a folha octaédrica [25]. Com a estrutura intercamada única de Li-MMT, o eletrólito pode efetivamente penetrar na camada de Li-MMT, resultando no transporte desimpedido de íons Li, conseguindo assim a difusão eficiente de íons [7, 25]. A morfologia de Li-MMT é mostrada na Fig. 1c, d, que mostra claramente a estrutura de nano folha 3D típica com arquitetura próxima e arbitrariamente empilhada. De acordo com a imagem HRTEM, a estrutura em camadas de Li-MMT pode ser observada e mostra um espaço entre camadas de ~ 1,39 nm.
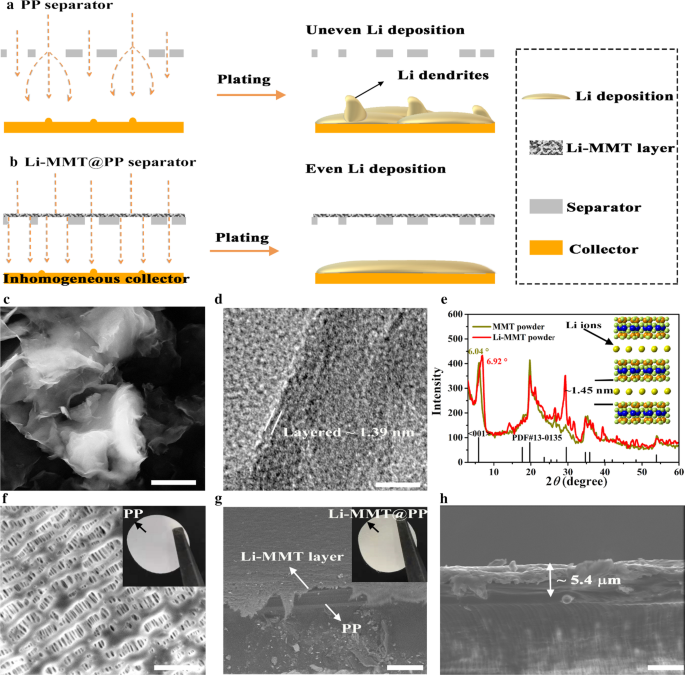
Preparação e caracterização de pós Li-MMT e separador Li-MMT @ PP. a , b Esquemas de conceitos de design com diferentes separadores. c Imagem SEM de Li-MMT. d Imagem HRTEM de Li-MMT. e Espectro de XRD. f Imagem SEM do separador PP, a imagem ótica inserida é o separador PP. g Imagem SEM do separador Li-MMT @ PP e h perfil cruzado correspondente, a imagem óptica inserida em g é o separador Li-MMT @ PP. Barra de cicatriz: c 1,5 µm, d 5 nm, f 2,5 µm, g 25 µm, h 5 µm
A medição precisa do espaço entre camadas de Li-MMT é mostrada na Fig. 1e. O MMT bruto com os cátions indeterminados em seu interlayer apresenta um pico em torno de 6,04 °. Após a troca iônica, o pico localizado a 6,92 ° é capaz de confirmar a mudança de cátions indeterminados para íons Li. Uma vez que os cátions dentro do MMT bruto são altamente variáveis em tamanho e distribuição, enquanto os íons Li são menores do que outros cátions [25], fazendo com que a distância entre camadas diminua gradualmente. De acordo com a lei de Bragg, o espaçamento entre camadas de Li-MMT pode ser estimado em ~ 1,4 nm, o que pode fornecer um amplo canal para o transporte de íons de lítio e umedecimento de eletrólito. A morfologia porosa do separador PP é apresentada na Fig. 1f. Após o revestimento da camada de Li-MMT, pode-se constatar que a porosidade do separador Li-MMT @ PP diminui significativamente (Fig. 1g), o que é benéfico para o movimento regular de íons. Neste trabalho, a pasta de Li-MMT foi revestida em uma máquina de revestimento, que apresenta potencial para produção em larga escala. A espessura revestida é de apenas 5 µm (Fig. 1h) com aumento de massa desprezível.
Beneficiado do canal de íon interlamelar atômico acima mencionado, o separador Li-MMT @ PP é eficaz para regular a deposição de Li e suprimir o crescimento de dendrito de Li em escala atômica por meio da orientação do fluxo de íon de Li. As medições de Brunner – Emme – Teller (BET) mostram a distribuição do tamanho dos poros do pó de Li-MMT no escopo de 1–3 nm (arquivo adicional 1:Fig. S1). Conforme mostrado na Fig. 2a, a bateria Li || Cu foi empregada para estudar o CE. Verificou-se que o separador Li-MMT @ PP pode fornecer a bateria Li || Cu com alto CE e excelente estabilidade, mesmo ao longo de 200 ciclos na densidade de corrente de 1 mA cm −2 com capacidade de 1 mAh cm −2 . Durante os testes, pode-se observar que todos os CE apresentam uma tendência ascendente nos primeiros 5 ciclos, ocasionada pela passivação superficial da deposição de Li. No entanto, a CE média mais alta nos primeiros 5 ciclos do separador Li-MMT @ PP destaca as vantagens de que o metal Li depositado sofre uma reação lateral inferior com o eletrólito líquido quando acoplado ao separador Li-MMT @ PP. Com o plaqueamento / decapagem reduplicativo, a deficiência do separador PP é gradualmente exposta de que a bateria Li || Cu montada dura apenas ~ 50 ciclos e seu CE diminui drasticamente para 60% e quase zero após 150 ciclos. Pelo contrário, a bateria CE de Li || Cu montada com o separador Li-MMT @ PP ainda oferece ciclos estáveis com baixo potencial excessivo (Fig. 2b) e a bateria ainda mantém 98,2% CE após 200 ciclos, indicando o Li depositado o metal é mais uniforme e nenhum dendrito de lítio é produzido após a regulação da camada de Li-MMT.
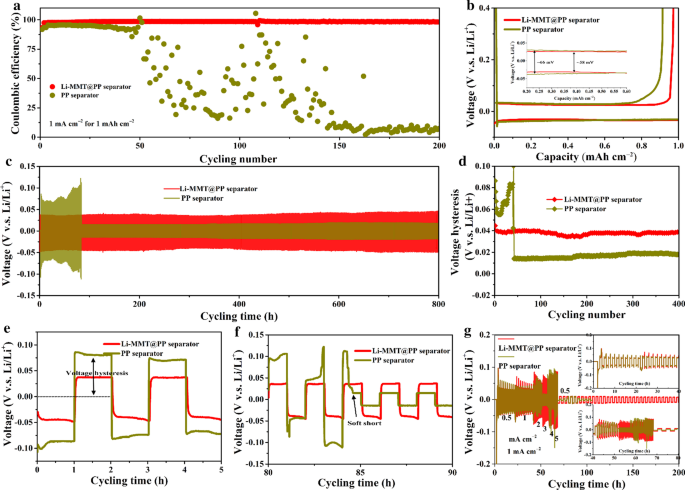
Desempenho eletroquímico de baterias simétricas Li || Cu e Li || Li. a Curvas CE e b curvas de tensão correspondentes. c Perfis de tensão-tempo das baterias simétricas Li || Li usando Li-MMT @ PP ou separador PP a 1 mA cm −2 com capacidade de 1 mAh cm −2 . d Histerese de tensão de baterias simétricas Li || Li. e , f Os perfis de ampliação parcial de c . g Os desempenhos de taxa de baterias simétricas Li || Li
Para investigar melhor as vantagens do separador Li-MMT @ PP na estabilidade do ciclo de ânodos de metal de Li, baterias de Li || Li simétricas com vários separadores também são fabricadas. Conforme mostrado na Fig. 2c, quando a capacidade de ciclagem é 1 mAh cm −2 a uma densidade de corrente de 1 mA cm −2 , a bateria com o separador Li-MMT @ PP oferece uma excelente estabilidade de ciclo com patamares de tensão estáveis ao longo de 400 ciclos (900 h) (Fig. 2d). Em nítido contraste, a bateria com o separador PP exibe forte histerese de tensão nos estágios iniciais. O overpotential é quase duas vezes maior do que o separador Li-MMT @ PP (Fig. 2e). Após o Li plaqueamento / decapagem por mais de 84 horas, uma queda repentina de tensão é observada para a bateria com o separador de PP (Fig. 2f), que pode ser atribuída à conexão elétrica entre os eletrodos, resultando no “curto suave”. Portanto, os desempenhos de taxa da bateria simétrica de Li foram posteriormente usados para avaliar a densidade de corrente na supressão dos dendritos de Li. Conforme mostrado na Fig. 2g, o separador Li-MMT @ PP sob a densidade de corrente, mesmo tão alta quanto 5 mA cm −2 ainda exibe comportamentos normais de chapeamento / striping. O separador PP apresenta flutuações de tensão significativas à medida que a densidade da corrente se aproxima de 3 mA cm −2 . Especialmente quando a densidade da corrente é aumentada para 5 mA cm −2 , a tensão se torna extremamente instável, indicando que a superfície do ânodo de Li sofre graves dendritos de Li. Em comparação com trabalhos anteriores (Arquivo adicional 1:Tabela S1), o separador modificado Li-MMT mostra vantagens competitivas para suprimir efetivamente os dendritos de Li.
A correlação de íons Li através do separador antes e após o revestimento da camada Li-MMT é proposta na Fig. 3a. Após a troca catiônica, a camada intermediária de Li-MMT fornece o sítio ativo para Li. O espaçamento entre camadas de 1,4 nm serve como um canal de íons de lítio exclusivo para permitir o fluxo regular de íons de lítio durante os processos de galvanização / decapagem. No entanto, para o separador de PP, os caminhos desordenados (Fig. 3b) e os poros empilhados arbitrariamente não permitirão a migração uniforme de íons Li como através do separador, levando à deposição heterogênea de íons Li nos processos eletroquímicos, e causando a formação de dendritos de lítio. Assim, as morfologias de ânodos de metal de Li após 20 ciclos são investigadas para esclarecer ainda mais o efeito do separador Li-MMT @ PP na supressão de dendritos de Li. Como mostrado na Fig. 3c, e, após o revestimento da camada de Li-MMT, a deposição uniforme e densa de Li é realizada e nenhuma formação de dendrito de Li é observada na superfície do ânodo, mesmo após 20 ciclos. É importante ressaltar que o ânodo de metal de Li ainda retém uma estrutura relativamente densa e compacta com superfície livre de dendritos, destacando as vantagens da camada de Li-MMT para comportamento favorável de revestimento / decapagem de Li livre de dendritos. No entanto, para a célula com separador de PP, o ânodo de metal de Li exibe dendritos de Li em forma de fio óbvios após os ciclos (Fig. 3d), e empilha de forma frouxa Li musgoso com uma estrutura altamente porosa (Fig. 3f).
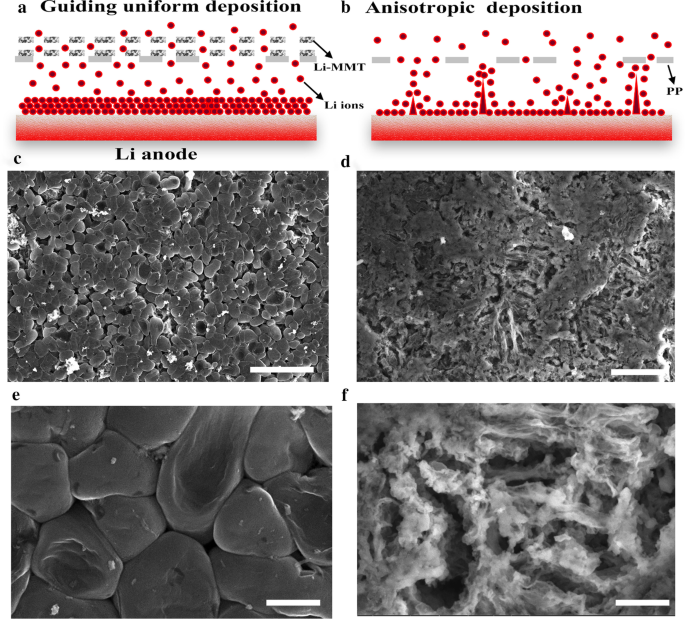
Imagens SEM do ânodo de Li acoplado com Li-MMT @ PP ou separador PP após 20 ciclos a 1 mA cm −2 com capacidade de 1 mAh cm −2 . a , b Ilustração do mecanismo dos separadores Li-MMT @ PP ou PP. c , e Separador Li-MMT @ PP. d , f Separador PP. Barras de escala: c 25 µm, d 10 µm, e , f 2,5 µm
Para demonstrar o potencial do separador Li-MMT @ PP na aplicação prática de baterias de metal Li, o cátodo S com carregamento S de 1,5 mg cm −2 foi empregado como eletrodo. A interface eletroquímica montada com diferentes separadores foi investigada pela medição de espectroscopia de impedância eletroquímica (EIS). Como mostrado na Fig. 4a, normalmente, todos os separadores exibem semicírculos deprimidos em altas frequências, que correspondem à resistência de transferência de carga interfacial. Embora possamos ver que a resistência de transferência de carga da bateria montada com o separador Li-MMT @ PP é ligeiramente maior do que a do separador PP, o desempenho da bateria não foi afetado após a ativação de baixa densidade de corrente, que foi reivindicada na seção experimental. Durante as regiões de baixa frequência, as linhas inclinadas apresentam a difusão do íon de lítio dentro dos materiais ativos. A Figura 4b mostra os patamares de tensão do cátodo composto C / S montado com separadores Li-MMT @ PP ou PP entre 1,7 e 2,8 V (V.S. Li / Li + ) Os testes de voltametria cíclica (CV) foram realizados e apresentados no Arquivo Adicional 1:Fig. S2. Embora a maior concentração de polissulfetos gere apenas ligeiramente maior concentração de polarização do que o separador PP, a área de pico do separador Li-MMT @ PP é muito maior do que a do separador PP, indicando que mais polissulfetos são gerados ao usar a camada de revestimento Li-MMT . De acordo com os mecanismos de reação do cátodo S, a bateria Li – S exibe dois platôs típicos durante os processos de carga / descarga. No primeiro estágio antes do ponto de joelho, o separador Li-MMT @ PP oferece uma alta capacidade de descarga de ~ 400 mAh g −1 com histerese de tensão desprezível. No entanto, para o separador PP, apenas ~ 210 mAh g −1 capacidade é observada, indicando que polissulfetos de cadeia longa parcialmente liberados (especialmente para o Li 2 S 8 ) não estão envolvidos na reação redox subsequente para contribuir com a capacidade. A maior capacidade de descarga durante o primeiro platô implica que a camada Li-MMT pode evitar efetivamente o transporte de polissulfetos de cadeia longa solúveis para a superfície do ânodo de Li. Nas segundas etapas de conversão, obviamente, para o separador de PP, pequenas quantidades de polissulfetos de cadeia curta são formadas devido à existência de efeito vaivém dentro do eletrólito à base de éter, o que foi confirmado por nosso trabalho anterior [26]. Em contraste, o separador Li-MMT @ PP é racionalmente projetado para que a superfície Li-MMT tenha forte capacidade de ancoragem para polissulfetos para evitar o transporte de polissulfetos [25]. As excelentes propriedades de adsorção garantem que os polissulfetos sejam impedidos de espalhar a superfície do ânodo de Li e passivar a superfície de Li, permitindo que a bateria Li – S montada com o separador Li-MMT @ PP tenha uma alta capacidade de descarga de 1283 mAh g −1 . Ciclos de longo prazo com boa estabilidade são os principais objetivos das baterias comerciais. A ciclabilidade de longo prazo dos separadores Li-MMT @ PP é mostrada na Fig. 4c. Nos primeiros 20 ciclos, pode-se observar que as capacidades do separador Li-MMT @ PP e PP apresentam uma tendência típica de diminuição. Isso ocorre porque, no processo de descarga inicial, polissulfetos abundantes precipitariam do interior do material do cátodo C / S e se depositariam na superfície do material do cátodo [26], resultando na perda de capacidade. No entanto, após estabilizar o ânodo de metal de lítio, os benefícios do separador Li-MMT @ PP são revelados de que a retenção da capacidade de descarga mantém 100% durante os ciclos subsequentes e o CE também é 100%.
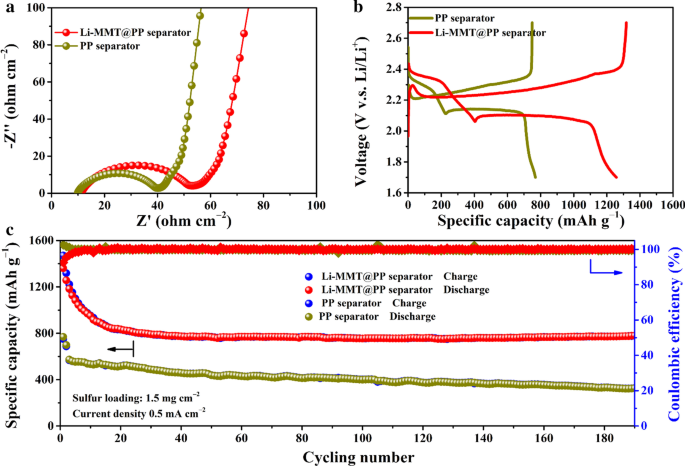
Desempenho eletroquímico de baterias Li – S com diferentes separadores. a Resultados do EIS. b Os platôs de carga / descarga com separador Li-MMT @ PP ou PP. c Desempenho de ciclagem de longo prazo a 0,5 mA cm −2 com carga de enxofre de 1,5 mg cm −2
Conclusões
Em resumo, o canal de íons interatômicos (Li-MMT) foi construído no separador de PP poroso para modular o fluxo de íons de Li e, em seguida, orientar a deposição uniforme de íons de Li no ânodo de Li durante a eletrodeposição / decapagem. Devido ao amplo espaço entre camadas (~ 1,4 nm) de Li-MMT, o separador Li-MMT @ PP garante muito a ciclabilidade do ânodo de metal Li, unificando a direção do fluxo de íons de lítio, resultando na deposição uniforme de íons Li no superfície do ânodo, formando assim um ânodo de lítio livre dendrítico. Quando montado com o separador Li-MMT @ PP, a bateria Li – S exibe uma notável capacidade reversível de 776 mAh g −1 (quase 1,4 vezes maior do que o separador PP) com 100% CE após 190 ciclos na densidade de corrente de 0,5 mA cm −2 com a carga de enxofre de 1,5 mg cm −2 .
Disponibilidade de dados e materiais
Todos os dados estão totalmente disponíveis sem restrição.
Abreviações
- Li:
-
Lítio
- Li – S:
-
Enxofre de lítio
- PP:
-
Polipropileno
- PE:
-
Polietileno
- MMT:
-
Montmorilonita
- CE:
-
Eficiência Coulombic
- LMBs:
-
Baterias de metal de lítio
- SEI:
-
Interfase de eletrólito sólido
- Li-MMT:
-
Montmorilonita à base de Li
- PVDF:
-
Fluoreto de polivinilideno
- LiOH:
-
Hidróxido de lítio
- NMP:
-
N-metil pirrolidona
- H 2 SO 3 :
-
Ácido sulfúrico
- C:
-
Acetileno preto
- XRD:
-
Difração de raios X
- HRTEM:
-
Microscópio eletrônico de transmissão de alta resolução
- LiTFSI:
-
Sal de lítio bistrifluorometanossulfonimida
- DOL:
-
1,3-dioxaciclopentano
- DME:
-
1,2-Dimetoxietano
- LiNO 3 :
-
Nitrato de lítio
- EIS:
-
Espectroscopia de impedância eletroquímica
- NCLs:
-
Camadas carregadas negativamente
- BET:
-
Brunner – Emmet – Teller
- CV:
-
Voltametria cíclica
Nanomateriais
- Nanocristais de estanho para bateria futura
- Nano e ânodo de bateria:uma revisão
- O rearranjo atômico de poços quânticos múltiplos baseados em GaN em gás misto H2 / NH3 para melhorar propriedades estruturais e ópticas
- Investigações da sorção de íons de metal pesado usando nanocompósitos de biocarvão modificado com ferro
- Efeito de diferentes ligantes no desempenho eletroquímico do ânodo de óxido de metal para baterias de íon-lítio
- Composto de aerogel de carbono ativado revestido com polianilina para bateria de lítio-enxofre de alto desempenho
- Transformação da lama de Si em estrutura de nano-Si / SiOx por difusão interna de oxigênio como precursor para ânodos de alto desempenho em baterias de íon de lítio
- Síntese assistida por humate de nanocompósitos MoS2 / C via co-precipitação / rota de calcinação para baterias de íon de lítio de alto desempenho
- Revisão:Filtros de Metal Poroso e Membranas para Separação Óleo-Água
- Tornos CNC para metal



