Nanorods de ouro revestidos com BSA para terapia fototérmica NIR-II
Resumo
A segunda janela próxima ao infravermelho é considerada a janela ótica ideal para imagens médicas e terapia por sua capacidade de penetração no tecido profundo. A preparação dos nanobastões de ouro com absorção de longo comprimento de onda e baixa citotoxicidade ainda é um desafio. Uma série de nanobastões de ouro com grande proporção foi sintetizada. Pode ser observada forte absorção de plasma na segunda janela do infravermelho próximo de 1000 a 1300 nm. A biocompatibilidade dos nanobastões de ouro sintetizados é dramaticamente melhorada através do revestimento por albumina de soro bovino (BSA), enquanto as propriedades ópticas dos quais permanecem. O camundongo portador de tumor de câncer de mama pode ser bem tratado pelos nanobastões de ouro preparados com a intensidade de luz NIR-II tão baixa quanto 0,75 W / cm 2 . Em resumo, esses resultados demonstram a viabilidade do uso de baixa dose de iluminação para tratar o tumor na região NIR-II por meio de nanopartículas de gould de grande proporção de aspecto.
Introdução
Nanopartículas de ouro têm despertado grande interesse em pesquisas biomédicas como a brilhante biocompatibilidade e a baixa citotoxicidade. Por exemplo, as nanopartículas de ouro com alta eficiência de atenuação de raios-X foram consideradas promissoras para o diagnóstico de tumor baseado em tomografia computadorizada (TC) [1, 2]. Além disso, as nanopartículas de ouro exibem excelentes propriedades ópticas, que são conhecidas como efeito de ressonância plasmônica de superfície (SPR). As nanopartículas de ouro podem converter de forma eficiente a energia do fóton em energia térmica para a terapia do câncer na presença de luz de ressonância de plasma de superfície [3, 4]. Portanto, várias nanopartículas de ouro com tamanho e morfologia ajustáveis foram desenvolvidas para ablação fototérmica de tumores, por exemplo, nanobastões de ouro, nanoconchas de ouro e nanocages de ouro [5,6,7]. Em particular, os nanobastões de ouro (AuNR) com formato e tamanho anisotrópico ajustáveis têm sido amplamente estudados desde sua excelente estabilidade fototérmica, biocompatibilidade e forte absorção na região NIR [8]. É bem conhecido que a luz infravermelha próxima pode penetrar nos tecidos biológicos de forma mais eficaz do que a luz visível, pois quanto maior o comprimento de onda da luz, menor a perda de espalhamento da luz [9]. Além disso, as nanopartículas em forma de bastonete foram encontradas com permeabilidade tumoral dramaticamente melhorada e maior tempo de circulação sanguínea, resultando em maior acúmulo de tumor [10, 11]. No entanto, a desvantagem significativa para a aplicação de nanobastões de ouro à terapia fototérmica (PTT) é a irradiação do laser de alta potência, que induziria a danos elevados no tecido normal (exposição de intensidade de luz máxima permitida) [12]. Foi provado que o PTT na segunda janela do infravermelho próximo (NIR-II, 1000–1700 nm) tem uma profundidade de penetração no tecido muito maior do que no NIR-I (700–1000 nm), como a dispersão de luz muito menor no NIR -II [13,14,15,16,17]. Portanto, espera-se que a nanoplataforma de PTT no NIR-II atinja um tratamento de tumor mais eficaz com PTT e tenha um grande potencial de aplicação clínica para uma terapia de tumor mais complexa. Porém, a preparação dos nanobastões de ouro com absorção de longo comprimento de onda e baixa citotoxicidade ainda é um grande desafio. Aqui, relatamos a síntese de nanobastões de ouro pelo método sem sementes com picos de absorção na segunda janela da janela do infravermelho próximo (1000–1300 nm). A modificação da superfície foi introduzida por meio de revestimento com BSA para reduzir a citotoxicidade. A razão de aspecto dos nanobastões de ouro preparados (AuNR @ BSA) foi caracterizada por microscópio eletrônico de transmissão (TEM) e espalhamento dinâmico de luz (DLS). O modelo de camundongo com tumor de câncer de mama foi usado para testar o efeito terapêutico fototérmico de AuNR @ BSA. Descobrimos que o tumor poderia ser bem tratado com intensidade de luz tão baixa quanto 0,75 w / cm 2 .
Materiais e métodos
Materiais
Cloreto de ouro tri-hidratado (HAuCl 4 · 3H 2 O) (99,9%), brometo de hexadecil trimetil amônio (CTAB) (99%), ácido nítrico (GR, 65-68%) e solução de peróxido de hidrogênio (GR, 30%) foram recebidos de Shanghai Aladdin biológico technology Co. Ltd . Boro-hidreto de sódio (NaBH 4 ) (97%) e nitrato de prata (AgNO 3 ) (99,8%) foram recebidos da Shanghai Lingfeng Chemical Reagent Co. Ltd. O ácido clorídrico (HCl) (38%) foi recebido da Dongguan Dongjiang Chemical Reagent Co. Ltd. A hidroquinona (99%) foi recebida da Energy Chemical. A albumina de soro bovino (98%) foi obtida da Sigma-Aldrich. Hidróxido de sódio (AR, 96%) foi recebido da Greagent.
O meio RPMI 1640 e a penicilina-estreptomicina foram adquiridos da HyClone. A solução tamponada com fosfato (PBS) foi adquirida à Corning. A pancreatina foi adquirida na Coolaber. O soro fetal bovino (FBS) foi adquirido da Gibco. As células 4T1 foram fornecidas pelo Centro de Pesquisa de Óptica Biomédica e Imagem Molecular do Instituto de Tecnologia Avançada de Shenzhen, Academia Chinesa de Ciências. A Dojindo Chemical Technology (Shanghai) Co., Ltd forneceu o Cell Counting Kit-8 (CCK-8) para o teste de proliferação celular e toxicidade. A água ultrapura Millipore foi usada ao longo do experimento.
Preparação de Nanopartículas AuNR @ CTAB
A síntese de nanobastões de ouro é conduzida da seguinte forma:0,4 mL de HAuCl 4 (aq) (10 mM) e 10 mL de CTAB (aq) (0,1 M) foram adicionados a 23-33 µL de AgNO 3 (aq) (100 mM). Em seguida, 10-30 µL de HCl (1,2 M) e 525 µL de hidroquinona aquosa (0,1 M) foram adicionados à solução de crescimento sob mistura suave. A cor da solução de crescimento mudou de laranja para um amarelo muito claro. Após 15 min de agitação, 10–40 µL de NaBH gelado recém-preparado 4 (aq) (10 mM) solução foi injetada na solução de crescimento. A mistura foi agitada durante 30 s e envelhecida durante 18 h à temperatura ambiente. O AuNR @ CTAB foi então lavado por PBS duas vezes.
Preparação de AuNR @ BSA
Primeiro, adicionamos uma certa quantidade de CTAB para ajustar sua concentração na solução AuNR @ CTAB para 1 mM e, em seguida, o ultrassom dissolve completamente o CTAB. 3 mL de AuNR @ CTAB são adicionados lentamente a 3 mL de solução de BSA (10 mg / mL), e a solução mista é sonicada por 30 min. Após centrifugação a 9500 × r por 40 min, o sobrenadante foi substituído por 6 mL de solução de BSA (5 mg / mL) e, em seguida, o pH foi ajustado para 11-12 com hidróxido de sódio (2 M), agitado por pelo menos 18 h. Depois disso, o AuNR @ BSA sintetizado foi centrifugado a 9500 × r por 40 min, depois lavado duas vezes com PBS e dissolvido em PBS para uso posterior.
Caracterizações de Nanopartículas AuNR @ CTAB e AuNR @ BSA
A análise morfológica dos nanobastões de ouro foi obtida por Beijing Zhongke Baice Co., Ltd. através do microscópio eletrônico Talos F200X para obter imagens TEM. Zetasizer Nano ZS (Malvern, Reino Unido) foi usado para estudar a distribuição de tamanho e potencial zeta de várias nanopartículas por DLS. O espectro de absorção de UV-Vis foi determinado pelo espectrofotômetro ultravioleta-visível UV-2700 (SHIMADZU, Japão).
Para a caracterização da morfologia de AuNR @ BSA dentro do tumor, 100 µL de AuNR @ BSA (OD =25 a 1064 nm) foram injetados nos locais do tumor com irradiação de cerca de 10 min, após o que os tumores tratados foram coletados. O tumor não tratado foi coletado como controle. Os tumores coletados foram incubados em solução de glutaraldeído a 2,5% (Coolaber.co., Pequim, China) para microscopia eletrônica de transmissão (Beijing Zhongke Baice Co., Ltd). O padrão de espectroscopia de infravermelho com transformada de Fourier (FT-IR) e os padrões de difração de raios-X (XRD) de amostras de AuNR foram obtidos por Beijing Zhongke Baice Co., Ltd.
Medição do desempenho fototérmico de AuNR @ CTAB e AuNR @ BSA
A solução de nanorod de ouro foi diluída para OD diferente em 1064 nm (0,5, 1, 1,5 e 2), e o PBS foi usado como um controle em branco. Os nanobastões de ouro (500 µL) foram irradiados com um laser de 1064 nm (Haoliangtech, Shanghai, China) a uma intensidade de potência de 0,35–1 W / cm 2 por 30 min. A temperatura foi registrada com um termovisor infravermelho (FLUKE TI25).
Fotoestabilidade de AuNR @ BSA
Para testar a fotoestabilidade, os espectros de absorção de AuNR @ BSA foram medidos em função do tempo de irradiação. Os AuNR @ BSA (OD =1) foram irradiados sob laser NIR (1064 nm, 0,5 w / cm 2 ) De 0 a 10 min, o espectro foi registrado a cada minuto. O teste de ciclo fototérmico também foi realizado como a solução AuNR @ BSA (0,5 mL) irradiada a cada 10 minutos com irradiações de laser ligadas e desligadas (1064 nm, 0,5 W / cm 2 ), e a mudança de temperatura foi registrada.
Cultura celular
Linhagem de células de câncer de mama murino (células 4T1) foi cultivada em RPMI 1640 contendo 10% de FBS e 100 U / mL de penicilina ou 100 µg / mL de estreptomicina. O ambiente de cultura é 37 ° C, e a condição de umidificação é 5% CO 2 .
In Vitro Avaliação da Citotoxicidade de Nanopartículas de Ouro
O ensaio CCK-8 foi usado para identificar a citotoxicidade de nanobastões de ouro. As células 4T1 foram pré-semeadas em placas de 96 poços (5 × 10 3 por poço) e incubados por 24 h. Posteriormente, 10 μL de várias concentrações de AuNR @ CTAB e AuNR @ BSA foram adicionados e incubados por mais 24 h. Após lavagem com PBS duas vezes, 10 μl de solução de CCK-8 foram adicionados a cada poço e incubados por 40 min, seguido pela medição da absorbância a 450 nm com um leitor de microplaca.
Para fototoxicidade, as células 4T1 foram pré-semeadas em uma placa de 96 poços (5 × 10 3 por poço) e incubadas por 24 h, então as células foram irradiadas com laser NIR (1064 nm, 0,75 W / cm 2 , 10 min) e posteriormente incubado por 24 h. Depois disso, 10 μL de solução de CCK-8 foram adicionados a cada poço e incubados por mais 40 min a 37 ° C. Em seguida, um leitor de microplacas foi utilizado para detectar a absorbância de cada poço a 450 nm.
Modelo de rato com tumor
Todos os ratinhos BALB / c foram adquiridos de Beijing Vital River Laboratory Animal Technology Co. Ltd. Todos os procedimentos de experiências com animais foram realizados seguindo os procedimentos padrão aprovados pelo Comité de Tecnologia Avançada de Shenzhen da Academia Chinesa de Ciências. O modelo de tumor foi estabelecido pela injeção subcutânea de células 4T1 (2 × 10 6 ) na parte de trás dos ratos. Os estudos em animais foram conduzidos quando o volume do tumor atinge aproximadamente 100 mm 3 .
In Vivo Circulação de Sangue e Biodistribuição
Para medição do tempo de circulação, primeiro, 200 μL de AuNR @ BSA foram injetados por via intravenosa na veia da cauda de camundongos BALB / c e, em seguida, 20 μL de sangue foram coletados a 0,25, 2, 4, 6, 8, 12, 36 e 48 h, e diluído com 30 μL de PBS para obter 50 μL de amostra de sangue. Cerca de 400 μL de HNO 3 concentrado (grau cromatográfico) foi adicionado, a tampa foi apertada e digerida a 90 ° C durante 2 h. Após resfriar à temperatura ambiente, 150 μL H 2 O 2 (grau cromatográfico) foi lentamente adicionado e, em seguida, aquecido a 90 ° C por 1 h sem cobertura. Ao final, a solução foi diluída para 5 mL com água ultrapura. A concentração de íon Au foi medida por espectroscopia de emissão óptica com plasma indutivamente acoplado (ICP-OES) após passar por filtro de seringa de náilon de 0,44 mm.
Para medida de biodistribuição, cerca de 200 μL de AuNR @ BSA foram injetados por via intravenosa na veia da cauda de camundongos BALB / c. Após 24 h, o camundongo foi morto e o coração, fígado, baço, pulmão e rim foram retirados e secos em estufa a 80 ° C. Antes da digestão, cada órgão foi pesado, 800 μL de HNO concentrado 3 (GR) foi adicionado e aquecido a 90 ° C durante 2 h. Após resfriar à temperatura ambiente, 200 μL H 2 O 2 (GR) foi adicionado lentamente gota a gota, aquecido a 90 ° C durante 1 h e, em seguida, a solução foi diluída para 10 mL por água ultrapura. Finalmente, a concentração de íon Au foi medida por ICP-OES após passar pelo filtro de seringa de náilon de 0,44 mm.
Eficiência do tratamento fototérmico
A fim de avaliar o efeito terapêutico térmico de AuNR @ BSA, os camundongos portadores de tumor com tumores 4T1 foram divididos aleatoriamente em quatro grupos com o volume do tumor de cerca de 100 mm 3 :(1) AuNR @ BSA, (2) AuNR @ BSA + Laser; (3) Somente laser (4) Controle de branco. Um termovisor infravermelho foi usado para registrar a imagem térmica infravermelha do local do tumor. O volume do tumor e o peso corporal dos camundongos foram registrados antes e após o tratamento, respectivamente. O volume do tumor pode ser calculado de acordo com a equação normal (volume =largura 2 × comprimento / 2). Duas semanas depois, os ratos foram mortos e os tumores isolados.
Análise de dados
O software estatístico SPSS 16.0 foi utilizado para a análise dos dados. Os dados das medidas foram expressos em média ± d, a comparação entre os grupos foi feita por análise de variância e a comparação dos dados de contagem foi realizada pelo teste Qui-quadrado. P <0,05 foi considerado estatisticamente significativo.
Resultados e discussão
Síntese e caracterização de AuNR @ CTAB
Verificou-se que quanto menores os nanobastões de ouro, melhor é a farmacocinética e menor a citotoxicidade [18]. No entanto, o pico de absorção de SPR de nanobastões de ouro está altamente relacionado à razão de aspecto, quanto maior a razão de aspecto, menor a energia do pico de SPR. A fim de sintetizar AuNR com grande proporção de aspecto, entretanto, manter o tamanho o menor possível, os parâmetros de síntese foram otimizados, como a concentração de surfactante, o pH da solução de crescimento e a concentração do agente redutor. O NaBH 4 (aq) é um tipo de agente redutor forte que forma o núcleo de Au via nucleação de explosão de LaMer, seguido por rápida fixação aleatória de íons de Au e maturação intrapartícula [19]. Como a quantidade molar de NaBH 4 aumentando, o pico máximo de absorção de nanobastões de ouro sofre um deslocamento para o azul de 1223 para 865 nm (Fig. 1C). O pH da solução de crescimento também é um parâmetro chave para controlar o crescimento dos nanobastões de ouro, que é ajustado através da quantidade de ácido clorídrico [20]. O pico máximo de absorção de nanobastões de ouro foi gradualmente desviado para o vermelho de 871 para 1070 nm, enquanto aumentava a quantidade de ácido clorídrico (Fig. 1D). Além disso, Ag + é considerado capaz de controlar a direção de crescimento dos nanobastões de ouro, e quanto menor o Ag + concentração o comprimento de onda de absorção mais longo do pico SPR poderia ser realizado (Fig. 1E). No final, os nanobastões de ouro sintetizados são em vinho tinto, como mostrado na Fig. 1B. Portanto, considerando a eficiência de síntese dos nanobastões de ouro e a disponibilidade de fonte de luz laser, escolhemos os nanobastões de ouro com pico máximo de absorção em 1064 nm para o tratamento fototérmico de tumores.
As fotopropriedades de AuNR @ CTAB em diferentes condições de síntese. a A preparação do AuNR @ CTAB. b A imagem de nanobastões de ouro revestidos de CTAB (AuNR @ CTAB), c Espectros de UV-vis de AuNR @ CTAB preparado com variação de NaBH 4 concentração, d Espectros de UV-vis de AuNR @ CTAB preparado com concentração variável de HCl e Espectros de UV-vis de AuNR @ CTAB preparado com variação de AgNO 3 concentração
Síntese e caracterização de AuNR @ BSA
O brometo de cetiltrimetilamônio (CTAB) é o composto mais amplamente usado para a síntese de nanobastões de ouro com comprimentos e proporções de aspecto precisos. No entanto, CTAB tem citotoxicidade significativa quando a concentração é superior a 1–10 μM. A aplicação dos nanobastões de ouro revestidos com CTAB (AuNR @ CTAB) em biomedicina tem sido bastante restrita [21]. Além disso, a estabilidade coloidal de nanobastões de ouro revestidos com CTAB em solução aquosa é dramaticamente afetada pela temperatura, que é fácil de ser cristalizada em baixas temperaturas [22]. Dada a redução da citotoxicidade do CTAB e a melhoria de sua estabilidade, várias abordagens têm sido propostas para substituir o CTAB durante o processo de síntese dos nanobastões de ouro ou para funcionalizar os nanobastões de ouro revestidos com CTAB. Usando polímeros, peptídeos, surfactantes e lipídios para modificar a superfície das nanopartículas, a maioria dessas estratégias usa moléculas tioladas ou forças de interação eletrostática para se ligar à superfície do ouro [23]. As proteínas são as opções mais promissoras como as vantagens da estabilidade coloidal, biocompatibilidade e posterior funcionalização. [26]
Os nanobastões de ouro embrulhados em CTAB e BSA são representados na Fig. 2A. O pico máximo de absorção de AuNR @ BSA é de cerca de 1064 nm, que é cerca de 30 nm desviado para o vermelho em comparação com o de AuNR @ CTAB (Fig. 2B). O potencial zeta dos nanobastões de ouro mudou de positivo para negativo por meio da substituição do revestimento CTAB por BSA (arquivo adicional 1:Fig. S1). A partir dos espectros FTIR do AuNR @ BSA e AuNR @ CTAB (arquivo adicional 1:Fig. S2), podemos encontrar dois picos característicos de 1649 cm −1 e 1539 cm −1 no caso de AuNR @ BSA, que foram atribuídos às bandas vibracionais amida I e amida II de BSA. O espalhamento dinâmico de luz (DLS) também foi aplicado para analisar o tamanho hidrodinâmico do AuNR @ CTAB e AuNR @ BSA; além disso, a morfologia de AuNR @ BSA e AuNR @ CTAB foi caracterizada por microscopia eletrônica de transmissão (TEM), como mostrado na Fig. 2C, D. Dois picos podem ser claramente encontrados na medição da intensidade de espalhamento de DLS, um com tamanho hidrodinâmico de cerca de 3,10 ( ± 0,85) nm e o outro cerca de 57,45 (± 24,22) nm para AuNR @ CTAB. No entanto, no caso de AuNR @ BSA, os picos mudam para 8,64 (± 3,80) nm e 89,24 (± 42,24) nm. Podemos descobrir que a forma do AuNR permanece semelhante após o revestimento com BSA, exceto que as extremidades se tornam ligeiramente arredondadas (Fig. 2C, D). Para aplicações de terapia in vivo, o tamanho crítico das nanopartículas é limitado a menos de 100 nm [25]. Além desse tamanho, a capacidade das nanopartículas de penetrar nos tumores será limitada; portanto, os nanobastões de ouro apresentados seriam um candidato ideal à terapia tumoral [24]. Conforme mostrado no arquivo adicional 1:Fig. S3, os picos característicos de Au podem ser claramente observados no padrão de XRD, a partir dos planos (111), (200), (220) e (311) das nanopartículas de Au.
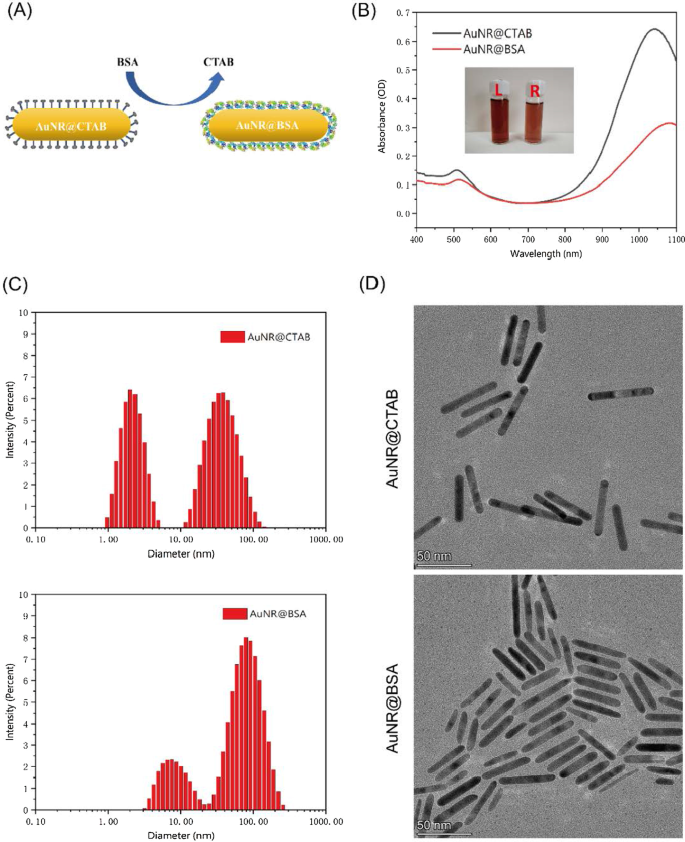
Caracterização de AuNR @ BSA e AuNR @ CTAB. a Preparação de AuNR @ BSA. b Espectros de UV-Vis de AuNR @ CTAB (L) e AuNR @ BSA (R). c A medição de intensidade DLS de AuNR @ CTAB e AuNR @ BSA. d As imagens TEM de AuNR @ CTAB e AuNR @ BSA
In Vitro Efeito fototérmico de nanobastões de ouro
O laser de diodo de 1064 nm como a fonte de luz NIR-II mais econômica é considerado o comprimento de onda ideal para terapia fototérmica. Portanto, a nanoplataforma de ouro NIR-II ideal para terapia fototérmica eficiente é considerada como caracterizada como forte absorção de SPR em 1064 nm, alta eficiência fototérmica e excelente estabilidade fototérmica. Para investigar o efeito fototérmico do AuNR @ BSA preparado, PBS e diferentes OD (=0,5, 1, 1,5, 2) de AuNR @ BSA foram excitados a 1064 nm com intensidade de luz de 0,35 a 1 W / cm 2 por 30 min. Um termovisor foi usado para registrar as mudanças de temperatura a cada 5 minutos, conforme mostrado na Fig. 3A. O efeito fototérmico de AuNR @ BSA e AuNR @ CTAB com a mesma absorvância (OD =1) é significativamente maior do que o de PBS. Pudemos descobrir que a temperatura subiu rapidamente nos primeiros 5 min e depois permaneceu em cerca de 80 ° C pelo resto do tempo, conforme ilustrado na Fig. 3A. O aumento da temperatura induzida pela fototérmica para PBS principalmente causado pela absorção harmônica de água em 1064 nm. A temperatura máxima em função da intensidade da luz é ilustrada na Fig. 3B. Verificou-se que a temperatura térmica fotoinduzida de AuNR @ CTAB e AuNR @ BSA na absorbância de cerca de 1 é proporcional à intensidade da luz. O aumento da temperatura é muito mais rápido para AuNR @ CTAB e AuNR @ BSA do que para PBS, pois a intensidade do laser aumenta. Além disso, a Fig. 3C mostra que sob as mesmas condições de irradiação (1064 nm, 0,75 W / cm 2 ), a temperatura fototérmica máxima é dramaticamente aumentada conforme a absorbância de ambos AuNR aumenta. As propriedades fototérmicas do AuNR revestido com BSA são um pouco melhores do que as do revestido com CTAB. Não há mudança significativa na temperatura fototérmica máxima de AuNR @ BSA (OD =1, 61,1 ° C) dentro de três ciclos de irradiação (0,5 W / cm 2 , 10 min), o que indica a excelente estabilidade fototérmica do AuNR @ BSA preparado (Fig. 3D). A Figura 3E representa a imagem da temperatura fototérmica de AuNR @ CTAB (OD =1), AuNR @ BSA (OD =1) e PBS sob irradiação de laser durante 10 min. A temperatura máxima do PBS é 44,5 ° C, enquanto a temperatura máxima do AuNR é de 85,5 ° C. Os resultados acima demonstraram que o AuNR @ BSA sintetizado possui características de absorção adequadas, eficiência de conversão fototérmica e fotoestabilidade na faixa NIR-II como um excelente agente terapêutico fototérmico.
Avaliação in vitro do efeito fototérmico de AuNR @ BSA. a A temperatura fototérmica de AuNR @ BSA e AuNR @ CTAB em função do tempo de irradiação do laser (absorbância SPR de cerca de 1, 1064 nm, 1 W / cm 2 ) b Aumento da temperatura desencadeada por NIR de PBS, AuNR @ CTAB (OD =1) e AuNR @ BSA (OD =1) em função da intensidade de irradiação do laser (1064 nm, 0,35 a 1 W / cm 2 ) c Aumento de temperatura disparado por NIR de AuNR @ BSA e AuNR @ CTAB com absorvância diferente para irradiação de laser de 10 min (1064 nm, 1 W / cm 2 ) d Conversão fototérmica de AuNR @ BSA (OD =1) sob três ciclos de irradiação (1064 nm, 0,5 W / cm 2 ) e Imagem térmica de PBS, AuNR @ CTAB (OD =1), AuNR @ BSA (OD =1) sob irradiação com laser NIR (1064 nm, 1 W / cm 2 ) em um intervalo de tempo de 5 e 10 min. (média ± DP, n =3)
In vitro Citotoxicidade e toxicidade fototérmica de nanobastões de ouro
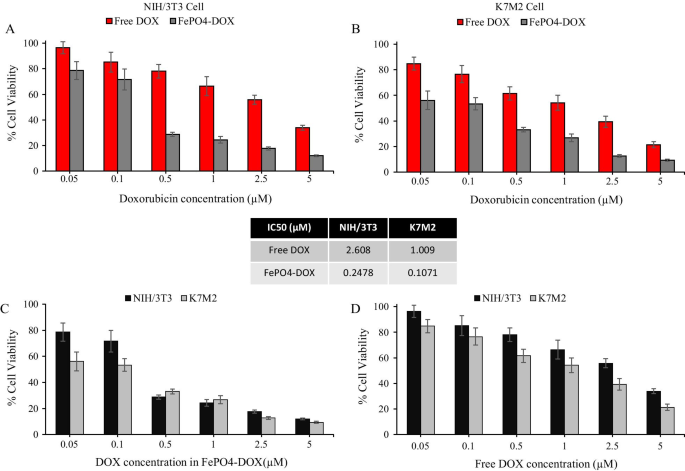
A análise de CCK-8 foi realizada para quantificar a citotoxicidade de AuNR @ CTAB e AuNR @ BSA em células 4T1 em diferentes concentrações. Mesmo sem irradiação de laser, o AuNR @ CTAB já exibe citotoxicidade significativa em concentração muito baixa (absorvância de cerca de 0,05), portanto, a aplicação biológica do qual é muito restrita. No entanto, o AuNR @ BSA demonstra excelentes perspectivas de aplicação biológica, por exemplo, a viabilidade celular ainda está na faixa aceitável como a absorvância AuNR @ BSA atinge cerca de 1 (Fig. 4A). Estimulado pela estabilidade promissora e alta eficiência de conversão fototérmica de AuNR @ BSA, a toxicidade fototérmica foi conduzida em células tumorais 4T1 in vitro com intensidade de luz de cerca de 0,75 W / cm 2 por 10 min. Toxicidade fototérmica significativa foi encontrada em absorbância em torno de 1 com taxa de sobrevivência celular em torno de 20%; no entanto, cerca de 100% de sobrevivência celular foi encontrada para experimentos sem radiação (Fig. 4B, Arquivo adicional 1:Fig. S4). Estes resultados in vitro indicam que o tratamento fototérmico AuNR @ BSA na região NIR-II pode matar eficazmente as células cancerosas em relativa intensidade de radiação.
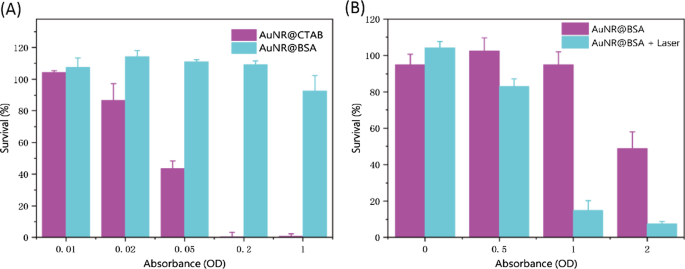
Citotoxicidade in vitro e toxicidade fototérmica de nanobastões de ouro. a Viabilidade celular de células 4T1 incubadas com várias concentrações de AuNR @ CTAB e AuNR @ BSA. b Viabilidade celular de células 4T1 incubadas com várias concentrações de AuNR @ BSA sem e com irradiação a laser NIR (1064 nm, 0,75 W / cm 2 , 10 min). (média ± DP, n =3)
In Vivo Estudos de Biodistribuição
O tempo de circulação sanguínea é essencial para a entrega bem-sucedida dos medicamentos baseados em nanopartículas [24]. O tempo de circulação sanguínea de AuNR @ BSA foi monitorado pela concentração de Au via ICP-OES e descobriu-se que era de cerca de 1,5 h (meia-vida) (Fig. 5A). A biodistribuição in vivo de AuNR @ BSA também foi medida pela concentração de Au em diferentes órgãos (Arquivo adicional 1:Fig. S5). Conforme mostrado na Fig. 5B, AuNR @ BSA foram altamente acumulados no fígado e baço após 24 h de injeção intravenosa devido à sua forte fagocitose como um órgão do sistema reticuloendotelial (RES) [27, 28]. Esses resultados mostram que AuNR @ BSA pode se acumular efetivamente no fígado e no baço. AuNR @ BSA tem aplicações potenciais em doenças relacionadas ao fígado e baço.
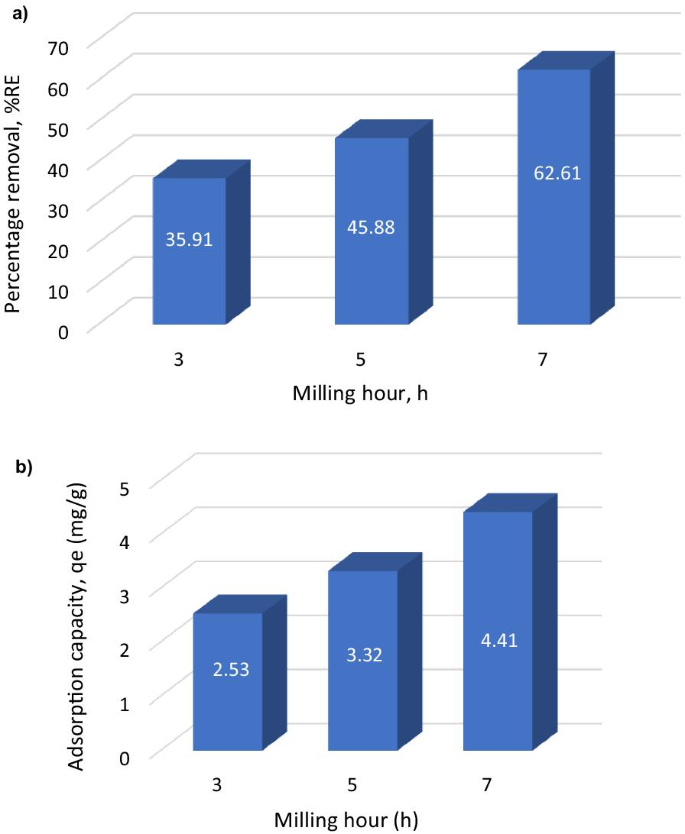
A biodistribuição de AuNR @ BSA no sangue e órgãos. a A concentração de Au no sangue em função do tempo via injeção intravenosa de AuNR @ BSA. b A biodistribuição de AuNR @ BSA em vários órgãos
In Vivo Tratamento fototérmico de infravermelho próximo de nanobastões de ouro
O excelente desempenho fototérmico do AuNR @ BSA nos encoraja a buscar a terapia fototérmica in vivo em camundongos BALB / c portadores de tumor. AuNR @ BSA foi injetado in situ no tumor e, em seguida, a luz foi introduzida para terapia fototérmica 10 minutos depois (1064 nm, 0,75 W / cm 2 ) A variação da temperatura in vivo foi monitorada por um termovisor. As mudanças de temperatura antes e depois do tratamento são representadas na Fig. 6D. A temperatura do local do tumor era de cerca de 63,9 ° C em 10 min de irradiação e manteve pouca flutuação a esta temperatura (Fig. 6D). Em contraste, não há mudança de temperatura observável para o grupo de controle na mesma condição de irradiação (grupo AuNR @ BSA, grupo PBS, grupo laser). Após a terapia fototérmica, o volume do tumor e o peso corporal dos camundongos foram monitorados a cada dois dias durante 14 dias. Conforme apresentado na Fig. 6A, B, o tumor do grupo AuNR @ BSA_laser foi completamente inibido e deixado como crostas queimadas no local do tumor original, enquanto o dos grupos de controle cresceu relativamente rápido e fora de controle (grupo AuNR @ BSA, Grupo PBS, grupo laser). As crostas são a pele queimada, o que prova diretamente que o processo PPT pode causar excesso de calor local no local do tumor com AuNR @ BSA injetado. O efeito fototérmico é muito eficiente, pois observamos que os tumores sólidos no grupo AuNR @ BSA + laser diminuem rapidamente dois dias após o tratamento. Para capturar ainda mais as alterações tumorais após o tratamento, ao final da observação de 14 dias, os camundongos foram mortos e os tumores isolados. Como mostrado na Fig. 6C, o tamanho do tumor do grupo de tratamento com AuNR @ BSA_laser foi totalmente suprimido, enquanto todos os outros grupos apresentaram crescimento descontrolado. Imagens de camundongos do grupo (AuNR @ BSA + laser) mostraram que os tumores não continuaram a crescer após o tratamento de 14 dias (Fig. 6E). Portanto, considerando a capacidade terapêutica ideal e nenhuma citotoxicidade óbvia, AuNR @ BSA para terapia de irradiação de laser de segunda janela no infravermelho próximo é um candidato ideal para PTT disparado por luz in vivo. Isso mostra claramente que a hipertermia simples usando a terapia NR-II atual pode inibir efetivamente o crescimento do tumor (arquivo adicional 1).
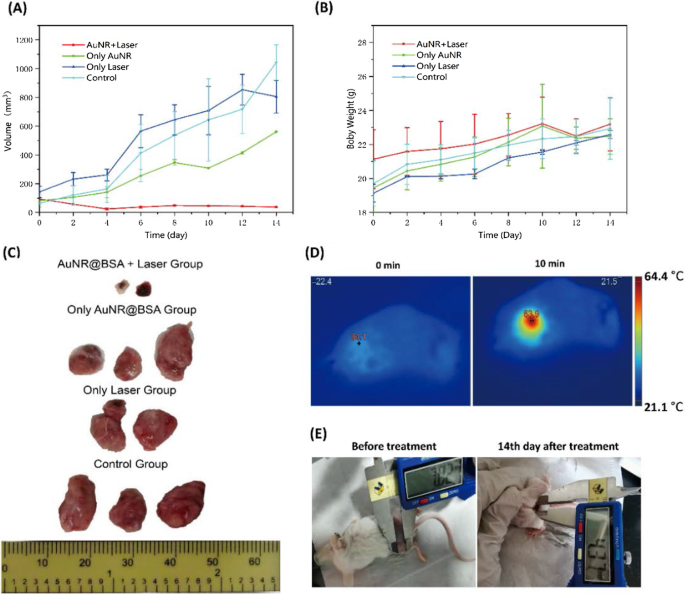
Tratamento fototérmico de camundongos com tumor. a Volume tumoral em função do tempo em diferentes condições de tratamento. b Mudanças no peso corporal de camundongos com tumores em função do tempo, pós-tratamento. c Fotografias de tecidos tumorais em diferentes grupos após tratamento de 14 dias. d Imagens termográficas infravermelhas de camundongos com tumor expostos a um laser de 1064 nm (0,75 W / cm 2 , 10 min) aos 10 min pós-injeção intratumoral de AuNR @ BSA. e Imagens de camundongos do grupo AuNR @ BSA_laser após o tratamento. (média ± DP, n =2)
Além disso, TEM foi considerado para o tumor isolado após o tratamento fototérmico e o tumor não tratado. O AuNR pôde ser observado no tecido tumoral após tratamento fototérmico. Ele forneceu evidências adicionais de que os nanobastões de ouro ainda apresentam excelente fotoestabilidade no ambiente de tecido tumoral (Fig. 7).
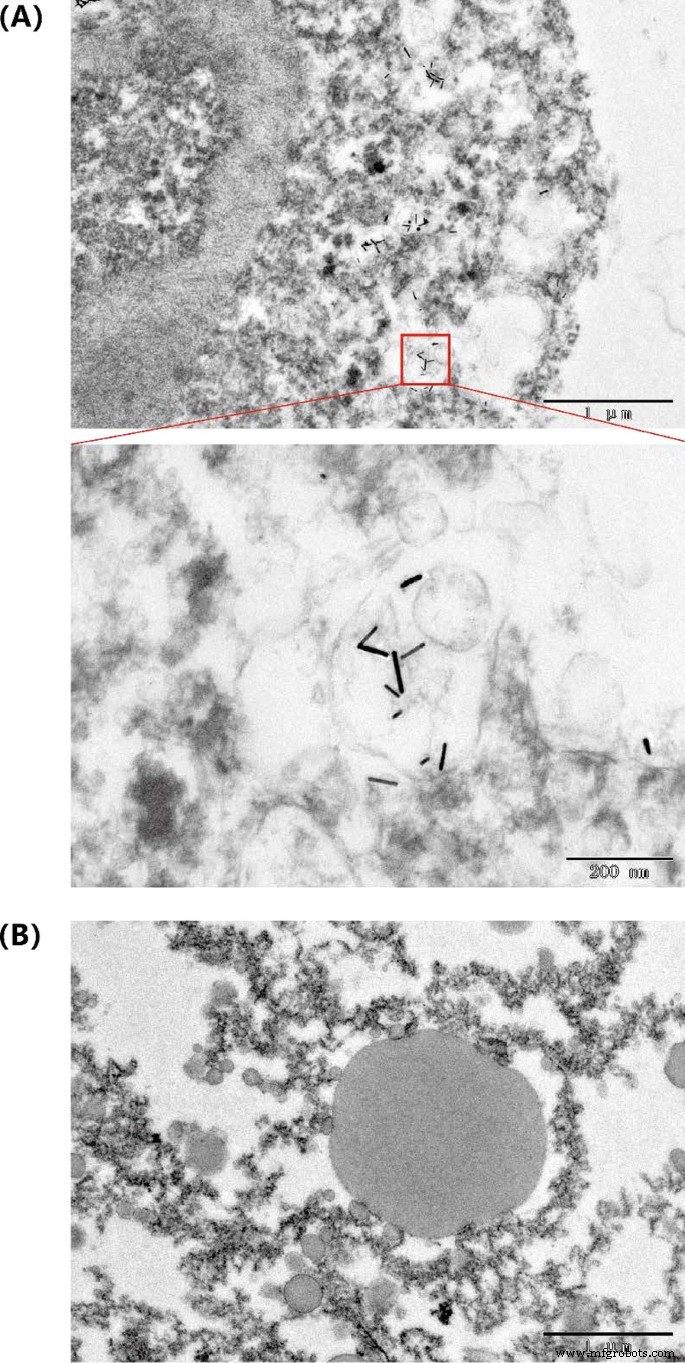
Micrografia eletrônica de transmissão de AuNR @ BSA em tecido tumoral a Tumor tratado. b Tumor não tratado
Conclusão
Aqui, sintetizamos o AuNR @ BSA com o máximo de absorção de SPR na segunda janela do infravermelho próximo para terapia fototérmica, como suas excelentes propriedades fototérmicas e biocompatibilidade. A biocompatibilidade do AuNR relatado foi significativamente melhorada pelo revestimento com albumina de soro bovino, e as propriedades fototérmicas não foram afetadas. A biodistribuição do AuNR @ BSA injetado por via intravenosa indica que grandes quantidades de AuNR se acumularam no fígado e no baço. The TEM image of AuNR@BSA inside tumor reveals that the high in vivo photostability of the AuNR and suggests that once upon injection, several phototreatment might be applied to reach the desired therapy outcomes. The excellent photothermal conversion of the reported AuNR was able to sufficiently inhibit tumor growth even under low light irradiation. The PTT of AuNR@BSA combined with other treatment strategies, such as immunotherapy and chemotherapy, would be promising for developing a useful tool for personalized, safe, and effective tumor treatment.
Disponibilidade de dados e materiais
The data set used and/or analyzed in this study can be obtained from the corresponding author upon reasonable request. All data generated or analyzed during this study is included in this published article.
Nanomateriais
- Nanopartículas plasmônicas
- Nanopartículas de ouro para sensores quimio
- TPE de nível médico usado para bola de terapia premiada
- Nanopartículas multifuncionais de ouro para aplicações diagnósticas e terapêuticas aprimoradas:uma revisão
- Nanopartículas para terapia do câncer:progresso e desafios atuais
- Estruturas Metálicas-Orgânicas de Meio Ambiente como Sistema de Administração de Medicamentos para Terapia de Tumor
- Síntese e desempenho in vitro de nanopartículas de ferro-platina revestidas com polipirrole para terapia fototérmica e imagem fotoacústica
- Nanomontagens de ácido 5-aminolevulínico-esqualeno para fotodetecção e terapia de tumor:estudos in vitro
- Biocompatível de ácido 5-aminolevulínico / vesículas etossômicas carregadas com nanopartículas de Au para terapia fotodinâmica / fototérmica sinérgica transdérmica in vitro de cicatrizes hip…
- Plataforma para tecnologias quânticas usando ouro



