Nanocompósitos de poli (N-isopropilacrilamida) -pirrol com luz quase infravermelha disparada termicamente para terapia quimio-fototérmica do câncer
Resumo
A terapia combinada baseada em nanocompósitos multifuncionais tem sido considerada uma abordagem promissora para melhorar a eficácia terapêutica do câncer. Aqui, relatamos poli ( N multifuncional direcionado -isopropilacrilamida) (PNIPAM) nanocompósitos à base de terapia quimio-fototérmica sinérgica para células de câncer de mama. Para aumentar a temperatura de transição, foi adicionado ácido acrílico (AAc) no processo sintético da PNIPAM, mostrando que a temperatura crítica inferior intrínseca da solução foi alterada para 42 ° C. Para gerar o efeito fototérmico sob irradiação de laser infravermelho próximo (NIR) (808 nm), nanopartículas de polipirrol (ppy) foram uniformemente decoradas em PNIPAM-AAc. O ácido fólico (FA), como um ligante direcionado ao câncer, foi conjugado com sucesso nos grupos carboxila excedentes na rede PNIPAM. A liberação da droga de nanocompósitos PNIPAM-ppy-FA foi eficientemente desencadeada em resposta à mudança de temperatura por irradiação com laser NIR. Também confirmamos que PNIPAM-ppy-FA foi internalizado em células de câncer de mama MDA-MB-231 por endocitose mediada por receptor de folato e eficácia terapêutica do câncer significativamente aumentada com tratamento de combinação de efeitos quimio-fototérmicos. Portanto, nosso trabalho incentiva uma maior exploração de agentes nanocarreadores multifuncionais para abordagens terapêuticas sinérgicas para diferentes tipos de células cancerosas.
Introdução
O sistema de entrega de drogas (DDS) é um dos métodos poderosos de administração de um composto farmacêutico para obter um efeito terapêutico na terapia do câncer [1]. Embora o objetivo do DDS seja entregar o fármaco ativo e se acumular na área desejada, o DDS convencional costuma ser acompanhado por graves efeitos colaterais e eficiência terapêutica ineficiente [2, 3]. Para superar esses obstáculos, uma variedade de nanocarreadores, que têm a capacidade de responder a estímulos internos ou externos específicos, incluindo temperatura, luz, pH, campo elétrico, oxidação-redução, atividade enzimática e concentração de antígeno, foram desenvolvidos para DDS e usado para induzir a liberação sustentada e controlada do fármaco [4,5,6].
Um dos vários estímulos, o nanocarreador termo-responsivo é uma abordagem poderosa para melhorar o tratamento do câncer, porque as drogas em nanopartículas podem ser liberadas a uma determinada temperatura [7]. Além disso, a vantagem das nanopartículas termossensíveis poderia ser combinada com outros estímulos para induzir a erradicação completa do câncer [8, 9]. Como uma nanopartícula termo-responsiva, poli ( N -isopropilacrilamida) (PNIPAM) tem recebido mais atenção, pois exibe uma transição de fase em uma temperatura de solução crítica mais baixa (LCST) em torno de 32 ° C [10, 11]. Abaixo do LCST, toda a rede de polímero em PNIPAM existe em um estado dilatado devido às ligações de hidrogênio. Por outro lado, PNIPAM transita para o estado hidrofóbico e as ligações de hidrogênio são reduzidas, resultando em um colapso da rede polimérica acima do LCST [12, 13]. Comparado a outras nanopartículas, o nanocarreador baseado em PNIPAM tem a vantagem de alta eficiência de encapsulação de fármaco, capacidade de liberação controlada de fármaco e boa biocompatibilidade [14]. No entanto, devido à liberação espontânea do fármaco na temperatura corporal, o nanocarreador baseado em PNIPAM não é suficiente para uso em DDS avançado. Para superar isso, os estudos anteriores adicionaram os ácidos orgânicos (por exemplo, ácido vinilacético, acrílico e alilacético) no processo sintético de PNIPAM, resultando na redução dos efeitos colaterais pela liberação contínua do fármaco [15].
Recentemente, uma série de estudos se concentraram em novas abordagens terapêuticas em que a integração de dois ou mais estímulos desencadeou nanopartículas para aumentar a eficácia terapêutica do câncer [16,17,18]. Por exemplo, a terapia fototérmica (PTT) exibe várias vantagens, como controle preciso da luz em tumores, penetração não invasiva e baixa toxicidade para células normais [19, 20]. Para combinar as nanopartículas com PTT, os agentes fototérmicos (por exemplo, nanobastões de ouro, nanotubos de carbono, polipirrol (ppy) e óxido de grafeno) devem ser uniformemente encapsulados em nanopartículas baseadas em PNIPAM [21,22,23]. O estudo anterior fabricou os nanobastões de ouro revestidos de sílica mesoporosa com uma concha PNIPAM termo e responsiva ao pH e explorou ainda mais as aplicações de terapia do câncer in vivo [24]. No entanto, esses nanocompósitos baseados em PNIPAM requerem um processo sintético de várias etapas. Além disso, uma vez que os nanocompósitos não tinham uma porção de direcionamento contra células cancerosas específicas, eles poderiam causar efeitos colaterais graves em outros órgãos ou tecidos normais. Em nosso relatório anterior, desenvolvemos um sistema de liberação controlada bidirecional usando as propriedades sensíveis ao pH e termossensíveis do PNIPAM [15]. Nanogéis de PNIPAM foram copolimerizados com conteúdo de ácido acrílico (AAc) para controle eficiente de LCST. Para melhorar o direcionamento do câncer e a eficácia terapêutica, desenvolvemos a terapia de combinação de direcionamento do câncer usando efeito quimio e fototérmico (Esquema 1). Com o aumento da temperatura pela irradiação do laser NIR, as drogas dos nanocompósitos termo-responsivos do PNIPAM foram liberadas e o efeito fototérmico foi subsequentemente ativado. Devido ao ácido fólico conjugado (FA), os nanocompósitos baseados em PNIPAM exibiram eficácia terapêutica significativamente melhorada em relação às células de câncer de mama MDA-MB-231.
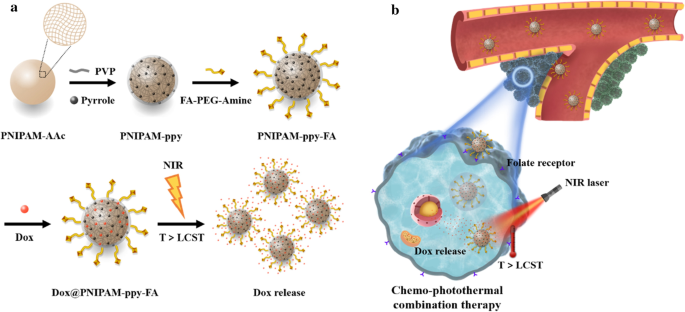
Ilustração esquemática de a síntese de luz NIR e nanocompósitos Dox @ PNIPAM-ppy-FA termicamente acionados e b aplicativo para terapia de combinação quimio-fototérmica aprimorada em células de câncer de mama
Materiais e métodos
Materiais
NIPAM, N, N ′-Metilenobisacrilamida (MBA), persulfato de potássio (KPS, 99%), N- (3-Dimetilaminopropil) - N Cloridrato de ′-etilcarbodiimida (EDC) e N -Hidroxissuccinimida (NHS) foram adquiridos da Sigma-Aldrich (St. Louis, MO, EUA). A polivinilpirrolidona (PVP) e o pirrol (98%) foram obtidos na Alfa Aesar (Ward Hill, MA, EUA). O AAc foi adquirido da Dae Jung Chemicals &Materials. Co. Ltd (Coréia). FA-PEG-amina (FA-PEG-NH 2 , MW:5 kDa) foi fornecido por Nanocs, Inc. (New York, NY, USA). O cloridrato de doxorrubicina (Dox) foi obtido na Tokyo Chemical Industry. Co. Ltd (Tóquio, Japão). Todos os produtos químicos e materiais foram usados comercialmente sem purificação adicional.
Síntese de nanopartículas PNIPAM-AAc decoradas com ppy
A PNIPAM termo-responsiva copolimerizada com nanopartículas de AAc foi sintetizada de acordo com relatório anterior [15]. 1,13 g de monômero NIPAM, 0,077 g de MBA e 0,136 g de AAc foram dissolvidos em 100 mL de água desionizada e adicionados em um frasco de fundo redondo de três tubuladuras de 250 mL. Após 30 min, a temperatura da reação foi aumentada para 80 ° C e agitação vigorosa durante 1 h. Para induzir a polimerização, KPS (1,5 mg) foi adicionado à mistura, seguido por agitação durante 4 h. A mistura foi dialisada contra uma membrana de diálise de 12-14 kDa de corte de peso molecular (MWCO) em água desionizada por 7 dias para remover monômero não reagido, iniciador, íons dispensáveis e nanopartícula de PNIPAM-AAc foi obtida por liofilização por 48 h. Para funcionalizar o efeito fototérmico, o ppy foi decorado com nanopartículas PNIPAM-AAc [25]. PVP (50 e 100 mg) e monômero de pirrol (50 e 100 μL) foram adicionados rapidamente em 10 mg / mL de solução de PNIPAM-AAc e foram agitados por 12 h em temperatura ambiente. Em seguida, KPS (3,4 mg) foi inserido na solução de PNIPAM-AAc e foi adicionalmente agitado durante 14 h. O PNIPAM-AAc decorado com ppy foi centrifugado três vezes com água destilada. O PNIPAM-ppy-5 e o PNIPAM-ppy-10 foram obtidos por liofilização por 48 h.
Síntese de nanocompósitos PNIPAM-ppy direcionados para câncer
Para obter nanocompósitos PNIPAM-ppy direcionados ao câncer (PNIPAM-ppy-FA), 10 mg de PNIPAM-ppy foram dissolvidos em solução salina tamponada com fosfato (PBS, 10 mL, pH 5,5) e ultra-sônicos por 5 min. EDC (15 mg, 0,078 mmol) e NHS (15 mg, 0,13 mmol) foram adicionados à solução de PNIPAM-ppy. Após 1 h, FA-PEG-NH 2 (5 mg) foi adicionado e foi adicionalmente agitado durante a noite. FA-PEG-NH não reagido 2 , EDC e NHS em solução de PNIPAM-ppy foram removidos por uma membrana de diálise (MWCO 6–8 kDa) e os nanocompósitos PNIPAM-ppy-FA foram liofilizados por 48 h.
Síntese de nanocompósitos PNIPAM-ppy-FA carregados com drogas anticâncer
10 mg de PNIPAM-ppy-FA foram dissolvidos em água desionizada e ultra-sônicos por 5 min. 0,5 mg / mL Dox foi adicionado em gotas à solução de PNIPAM-ppy-FA, agitando vigorosamente à temperatura ambiente. O Dox não carregado foi removido por centrifugação (14.000 rpm, 10 min) e foi purificado com água desionizada. PNIPAM-ppy-FA carregado com Dox (Dox @ PNIPAM-ppy-FA) foi obtido por liofilização durante 48 h.
Caracterização de NIR e nanocompósitos PNIPAM-ppy-FA termo-responsivos
Microscopia eletrônica de transmissão (TEM, JEOL-2100F, JEOL, Japão) foi usada para caracterizar o tamanho, morfologia e distribuição dos nanocompósitos PNIPAM-ppy-FA. Para medição de TEM, as amostras foram preparadas colocando uma gota da solução de amostra em água desionizada (concentração:1 g / L) em uma grade de cobre de malha 200 revestida com carbono. A distribuição de tamanho e a carga superficial dos nanocompósitos PNIPAM-ppy-FA, que foram dissolvidos em água desionizada e ultra-sônicos por 5 min, foram medidos usando um Zetasizer Nano Z (Malvern Instruments, Reino Unido). A modificação da superfície e ligação química dos nanocompósitos PNIPAM-ppy-FA foram confirmadas por espectroscopia de infravermelho com transformada de Fourier (FT-IR). Os espectros FT-IR foram registrados nas pelotas de KBr usando um instrumento Nicolet iS50 (Thermo Fisher Scientific, Inc., EUA) no intervalo de 400–4000 cm −1 com uma resolução de 4 cm −1 . A propriedade óptica e a capacidade de carga Dox em nanocompósitos PNIPAM-ppy-FA foram observadas por espectroscopia UV-Vis (UV 1800, Shimazu, Japão).
Propriedade fototérmica e fotoestabilidade de NIR e nanocompósitos PNIPAM-ppy-FA termo-responsivos
A propriedade fototérmica de nanocompósitos PNIPAM-ppy-FA carregados com Dox (Dox @ PNIPAM-ppy-FA) foi avaliada por detecção em tempo real de mudanças de temperatura. Dox @ PNIPAM-ppy-FA foi dissolvido em solução aquosa com diferentes concentrações de 0,05, 0,1 e 0,2 mg / mL e foi irradiado por 20 min usando um laser NIR de 808 nm (MDL-N-808, CNI Optoelectronics Tech. Co. Ltd., China) a uma densidade de potência de 2 W / cm 2 . A influência da densidade de potência do laser NIR foi estudada por irradiação do laser NIR por 20 min com uma densidade de potência de 1, 2 e 3 W / cm 2 , respectivamente. Além disso, para investigar a estabilidade fototérmica contra o laser NIR, a solução Dox @ PNIPAM-ppy-FA (0,1 mg / mL) foi exposta por 15 min e após processo de resfriamento natural por cinco vezes. Durante a irradiação do laser NIR, a temperatura da solução Dox @ PNIPAM-ppy-FA foi medida por um termopar ligado a um termômetro digital (DTM-318, Tecpel Co., Taiwan) a cada 60 s por 15 min.
NIR e liberação de medicamento termo-responsivo de nanocompósitos PNIPAM-ppy-FA
Para estudar os perfis de liberação de Dox por resposta térmica, soluções de Dox @ PNIPAM-ppy-FA (1 mg / mL) foram preparadas em frascos de 5 mL e foram então agitadas a 25, 37 e 50 ° C. Em um tempo de liberação definido (0–72 h), o sobrenadante de cada amostra foi coletado por centrifugação e substituído por um volume igual de meio fresco. A quantidade de Dox liberada de nanocompósitos PNIPAM-ppy-FA foi estimada por medição de espectroscopia UV-Vis em 480 nm. Além disso, o comportamento de liberação de Dox via solução de Dox @ PNIPAM-ppy-FA (1 mg / mL) respondeu a estímulos laser NIR foi vigorosamente agitado a 37 ° C e foi irradiado por 10 min em pontos de tempo pré-determinados (1, 2, 3 , 4 e 5 h). Como controle, foi utilizada a solução Dox @ PNIPAM-ppy-FA sem irradiação com laser NIR. O Dox liberado foi determinado pelo método mencionado.
Análise de citotoxicidade de nanocompósitos PNIPAM-ppy-FA
A citotoxicidade dos nanocompósitos PNIPAM-ppy-FA incluindo PNIPAM-ppy-FA e Dox @ PNIPAM-ppy-FA foi verificada usando o ensaio MTT. As células A549 e MDA-MB-231 foram semeadas em placas de 96 poços a uma densidade de 1 × 10 4 células por poço em 200 µL de meio RPMI 1640 contendo 10% de FBS e 1% de penicilina-estreptomicina e foram incubadas a 37 ° C em atmosfera umidificada com 5% de CO 2 . Após 1 dia, 200 µL de nanocompósitos PNIPAM-ppy-FA com várias concentrações (20–100 µL) foram tratados em cada célula e a placa foi incubada por 24 h. As células foram lavadas com DPBS e o meio foi então substituído por meio fresco com agente MTT (0,5 mg / mL). Após outra incubação durante 4 h, o meio foi cuidadosamente removido e 200 µL de DMSO foram adicionados a cada poço para dissolver os cristais de formazan roxos internalizados. A absorção foi medida a 595 nm usando um leitor de microplaca iMark ™ (Bio-rad, Hercules, CA, EUA).
Análise de absorção celular de nanocompósitos PNIPAM-ppy-FA
Para avaliar a capacidade de direcionamento para células cancerosas específicas de nanocompósitos PNIPAM-ppy-FA, células A549 e MDA-MB-231 foram semeadas em uma placa de 8 poços (ibidi, Munique, Alemanha) a uma densidade de 2 × 10 4 células / mL e foram incubadas por 24 h. As células foram então incubadas com nanocompósitos PNIPAM-ppy-FA (60 µg / mL) durante 6 h. Posteriormente, as células foram lavadas duas vezes com DPBS para remover os nanocompósitos restantes e fixadas com paraformaldeído 4% por 15 min. Após tratamento com 0,1% Triton-X por 15 min à temperatura ambiente, as células foram finalmente coradas por Alexa Fluor 488 faloidina (1:200, Invitrogen, EUA) por 1 dia a 4 ° C e 4,6-diamidino-2- fenilindol (DAPI, Thermo Fisher Scientific, EUA) por 10 min, respectivamente. As imagens de captação celular foram observadas usando microscopia confocal de varredura a laser (CLSM, LSM 710, Carl Zeiss, Alemanha).
Efeitos anticâncer aprimorados de nanocompósitos PNIPAM-ppy-FA via irradiação a laser NIR
A eficácia terapêutica aprimorada usando NIR e PNIPA-ppy-FA termo-responsivo em células de câncer de mama foi investigada por ensaio de MTT. MDA-MB-231 (1 × 10 4 células / mL) foram semeadas em placas de 96 poços e foram incubadas por 24 h. As células foram então lavadas com DPBS e nanocompósitos PNIPAM-ppy-FA e Dox @ PNIPAM-ppy-FA em várias concentrações (20, 40, 60, 80 e 100 μg / mL) foram adicionados a cada poço de uma maneira dependente da concentração . Após incubação durante a noite, o meio foi removido, seguido pela adição de meio fresco. Para os grupos de irradiação a laser NIR, as células foram tratadas com 5 W / cm 2 por 5 min. Em seguida, MDA-MB-231 foram lavados com DPBS e o meio fresco incluindo solução de MTT foi adicionado. Após 4 h, o meio foi cuidadosamente removido e 200 μL de DMSO foram adicionados a cada poço. Finalmente, a absorbância a 595 nm foi medida por um leitor de microplaca iMark ™ para determinar a viabilidade celular. Como outro método para observação dos efeitos terapêuticos do câncer, foi realizado o ensaio de vivos e mortos. PNIPAM-ppy-FA e Dox @ PNIPAM-ppy-FA (60 μg / mL) foram tratados em MDA-MB-231. Após 24 h, o MDA-MB-231 foi exposto com ou sem irradiação a laser NIR (5 W / cm 2 , 5 min) e foram corados com calceína AM e homodímero-1 de etídio. Após 30 min, as células foram lavadas várias vezes com DPBS. As imagens vivas / mortas foram obtidas usando microscopia de fluorescência invertida (Olympus Ix73, Japão).
Resultados e discussão
Síntese e caracterização de NIR e nanocompósitos PNIPAM-ppy direcionados ao câncer com resposta térmica
Para a geração de nanocompósitos baseados em PNIPAM termo-responsivos, nanopartículas PNIPAM-AAc foram fabricadas por um método de polimerização radical [15]. Para controlar LCST via irradiação de laser NIR, o ppy foi coberto pela reação de polimerização em PNIAPM-AAc conforme preparado. O PNIPAM-ppy-FA direcionado ao câncer foi sintetizado por conjugação química de FA-PEG-NH 2 ao grupo carboxila em PNIPAM-AAc. De acordo com as imagens TEM na Fig. 1a, a morfologia, o tamanho e a dispersão de PNIPAM-AAc, PNIPAM-ppy e PNIPAM-ppy-FA foram observados. O PNIPAM-AAc preparado exibiu a forma homogênea com um diâmetro médio de 274,32 ± 11,62 nm. Após decoração do ppy, PNIPAM-ppy e PNIPAM-ppy-FA apresentaram tamanhos semelhantes com 275,99 ± 11,41 e 285,77 ± 17,92 nm. O tamanho do PNIPAM-ppy-FA carregado com Dox aumentou ligeiramente de 285,77 ± 17,92 para 290,73 ± 12,28 nm, indicando que as drogas anticâncer foram carregadas em nanocompósitos PNIPAM-ppy-FA [26]. Curiosamente, em comparação com PNIPAM-AAc, a presença do ppy dentro dos nanocompósitos PNIPAM-ppy-FA foi claramente exibida por pequenos pontos pretos. Além disso, devido à cadeia de PEG, os nanocompósitos PNIPAM-ppy-FA foram bem dispersos em solução aquosa sem agregação [27]. Os diâmetros hidrodinâmicos médios de PNIPAM-AAc, PNIPAM-ppy, PNIPAM-ppy-FA e Dox @ PNIPAM-ppy-FA foram medidos por análise DLS (Arquivo adicional 1:Fig. S1). Os diâmetros de PNIPAM-AAc, PNIPAM -ppy, PNIPAM-ppy-FA e Dox @ PNIPAM-ppy-FA foram 432, 450,7, 468,6 e 486,7 nm, respectivamente. Devido aos diferentes métodos analíticos, o diâmetro de cada nanocompósito era maior do que o do TEM, mas o tamanho da partícula e a distribuição dos nanocompósitos PNIPAM-ppy-FA exibiram uma tendência semelhante.
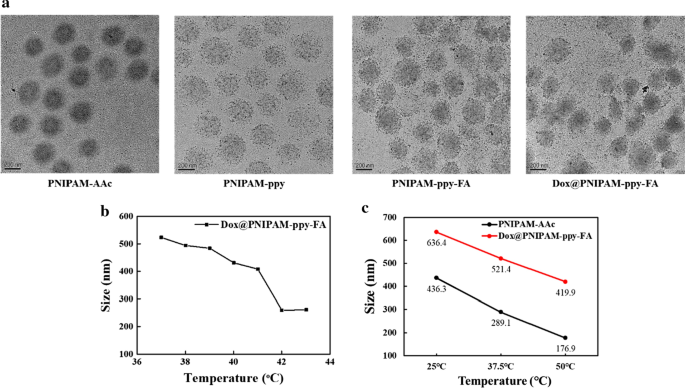
a Imagens TEM de nanocompósitos PNIPAM-AAc, PNIPAM-ppy, PNIPAM-ppy-FA e Dox @ PNIPAM-ppy-FA. b Análise LCST de Dox @ PNIPAM-ppy-FA por DLS. c Diâmetros médios de PNIPAM-AAc e Dox @ PNIPAM-ppy-FA dependendo das diferentes condições de temperatura (a 25 ° C, 37,5 ° C e 50 ° C)
Para investigar a influência do ppy polimerizado em PNIPAM-AAc, os valores LCST de PNIPAM-AAc e Dox @ PNIPAM-ppy-FA foram medidos por diferentes temperaturas (Fig. 1b). Comparado com nosso trabalho anterior [15], o LCST de Dox @ PNIPAM-ppy-FA foi ligeiramente menor do que o de PNIPAM-AAc (42 ° C). Esta diferença pode ser causada pelos grupos carboxila reduzidos em PNIPAM-AAc devido a ppy polimerizado e ligante de direcionamento de câncer conjugado [28]. Subseqüentemente, monitoramos a mudança de tamanho de partícula dependendo da temperatura na Fig. 1c. Para isso, os diâmetros de PNIPAM-AAc e Dox @ PNIPAM-ppy-FA foram medidos na faixa de temperatura de 25 a 50 ° C. À medida que a temperatura aumentava, o PNIPAM-AAc diminuía de 436 para 177 nm. Além disso, o tamanho de Dox @ PNIPAM-ppy-FA foi bastante reduzido de 630 para 420 nm, indicando que ppy decorado em nanocompósitos PNIPAM não afetou altamente para aplicações de DDS controlado e termo-responsivo [27].
Os valores de potencial zeta de PNIPAM-AAc, PNIPAM-ppy, PNIPAM-ppy-FA e Dox @ PNIPAM-ppy-FA exibiram a mudança de superfície dos nanocompósitos antes e depois da modificação (Fig. 2a). O potencial zeta de PNIPAM-AAc era - 37,1 ± 1,61 mV devido aos grupos carboxila em AAc [29]. Os valores de PNIPAM-ppy e PNIPAM-ppy-FA aumentaram para - 29,6 ± 0,96 e - 15,6 ± 0,26 mV, indicando que polipirrol carregado positivamente e FA-PEG-NH 2 foram introduzidos com sucesso em nanocompósitos PNIPAM-ppy-FA [27]. Devido ao Dox carregado negativamente, o potencial zeta de Dox @ PNIPAM-ppy-FA mudou para cargas mais negativas (- 28,6 ± 0,23 mV). Como mostrado na Fig. 2b, a síntese bem-sucedida de PNIPAM-AAc, PNIPAM-ppy e PNIPAM-ppy-FA foi confirmada por espectroscopia FT-IR. O espectro de PNIPAM-AAc mostrou os picos de vibração de alongamento de C-N e CH 2 entre 1100 e 1200 cm −1 e os picos de C =O, N – H e COOH foram observados em 1545, 1645 e 1750 cm −1 , que pertencia ao PNIPAM-AAc [15]. O polipirrol em PNIPAM-ppy e PNIPAM-ppy-FA demonstrou os picos adicionais em 935 e 1050 cm -1 foram observados [30]. No espectro de PNIPAM-ppy-FA, os novos picos de vibração apareceram em 1107 e 2880 cm −1 , que é atribuído ao C – O – C da cadeia PEG. Este resultado indicou a conjugação química bem-sucedida de FA-PEG-NH 2 [31]. No entanto, o ligante de direcionamento de FA não foi detectado por FT-IR, porque sua estrutura era semelhante ao PEG. Para confirmar a presença de FA em nanocompósitos PNIPAM, PNIPAM-AAc, PNIPAM-ppy e PNIPAM-ppy-FA foram realizados por espectroscopia UV-Vis (Fig. 2c). Enquanto os espectros de PNIPAM-AAc e PNIPAM-ppy (sem FA) não mostraram nenhum pico de absorção, PNIPAM-ppy-FA mostrou o pico adicional em 280 nm, que foi distinto em FA [32]. Este resultado apoiou que as moléculas de FA foram enxertadas em nanocompósitos baseados em PNIPAM.
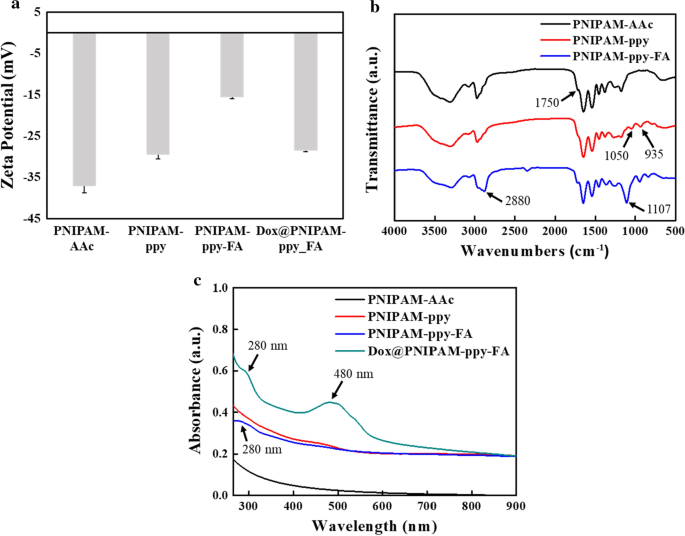
a Análise do potencial Zeta de PNIPAM-AAc, PNIPAM-ppy, PNIPAM-ppy-FA e Dox @ PNIPAM-ppy-FA. b Espectros FT-IR de PNIPAM-AAc, PNIPAM-ppy e PNIPAM-ppy-FA. c Espectros de UV-Vis de PNIPAM-AAc, PNIPAM-ppy, PNIPAM-ppy-FA e Dox @ PNIPAM-ppy-FA
Propriedade fototérmica de nanocompósitos PNIPAM-ppy-FA via irradiação a laser NIR
Para usar nanocompósitos baseados em PNIPAM para terapia fototérmica, a propriedade óptica dos nanocompósitos PNIPAM-ppy-FA foi examinada por espectroscopia UV-Vis. Conforme mostrado na Fig. 2c, PNIPAM-AAc não mostrou qualquer absorbância na região NIR (λ =700-1000 nm). No entanto, os espectros de PNIPAM-ppy, PNIPAM-ppy-FA e Dox @ PNIPAM-ppy-FA obviamente mostraram a absorvância forte na mesma faixa devido às nanopartículas de ppy polimerizadas. Esses resultados de absorbância demonstraram que os nanocompósitos PNIPAM-ppy-FA podem converter a luz NIR em calor [26]. Em seguida, avaliamos a propriedade fototérmica dos nanocompósitos PNIPAM-ppy-FA por irradiação com laser NIR (Fig. 3). Para otimizar o efeito fototérmico, PNIPAM-FA (sem pirrol), PNIPAM-ppy-5-FA (ppy 50 μL) e PNIPAM-ppy-10-FA (ppy 100 μL) foram preparados na mesma concentração (0,1 mg / mL ) e, em seguida, foram expostos a irradiação de laser NIR de 808 nm a uma densidade de 2 W / cm 2 por 20 min (Fig. 3a). A temperatura do PNIPAM-ppy-10-FA aumentou para 14,5 ° C, que foi 2 vezes mais alta do que a do PNIPAM-ppy-5-FA. Como controle, PNIPAM-FA sem ppy foi irradiado, mas a temperatura aumentou de forma desprezível (2,4 ° C). Portanto, escolhemos PNIPAM-ppy-10-FA para investigar experimentos fototérmicos adicionais. Para observar as mudanças de temperatura por concentração, o laser NIR foi irradiado para PNIPAM-ppy-FA em diferentes concentrações (0,05, 0,1 e 0,2 mg / mL). Na Fig. 3b, dependendo da concentração, a temperatura aumentou para 10, 14,5 e 18 ° C, respectivamente. Além disso, a solução PNIPAM-ppy-FA (0,1 mg / mL) foi irradiada com várias densidades de potência do laser (1–3 W / cm 2 ) na Fig. 3c. Como esperado, o aumento da temperatura do nanocompósito era altamente dependente da potência do laser. Posteriormente, observamos a estabilidade fototérmica dos nanocompósitos PNIPAM-ppy-FA na Fig. 3d. Embora a irradiação com laser NIR tenha sido realizada repetidamente pelo menos 5 vezes, a temperatura foi continuamente aumentada para 33 ° C, mostrando que o nanocompósito PNIPAM-ppy-FA era um nanocarreador adequado como terapia fototérmica.
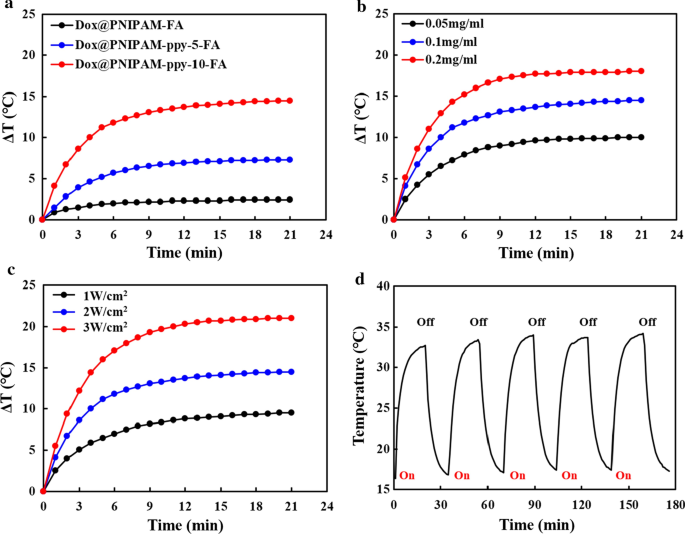
Desempenho fototérmico de nanocompósitos PNIPAM-ppy-FA. a Análise de temperatura de Dox @ PNIPAM-ppy-5-FA e Dox @ PNIPAM-ppy-10-FA sob irradiação de laser NIR de 808 nm (2 W / cm 2 ) b Análise de temperatura de diferentes concentrações de Dox @ PNIPAM-ppy-FA sob irradiação NIR de 808 nm (2 W / cm 2 ) c Efeito fototérmico de Dox @ PNIPAM-ppy-FA com várias densidades de potência (1, 2 e 3 W / cm 2 ) (D) Curva de temperatura de Dox @ PNIPAM-ppy-FA ao longo de cinco ciclos liga / desliga usando irradiação a laser NIR (2 W / cm 2 )
NIR e liberação de droga com resposta térmica de nanocompósitos PNIPAM-ppy-FA
Para avaliar os perfis de liberação do fármaco via NIR e resposta térmica, analisamos as propriedades de encapsulação e liberação dos nanocompósitos Dox @ PNIPAM-ppy-FA. Inicialmente, medimos os espectros de absorção de UV-Vis do PNIPAM-ppy-FA carregado com a droga e um forte pico de absorção foi observado perto de 480 nm (Fig. 2c). Este resultado indicou que Dox foi carregado com sucesso em nanocompósitos PNIPAM-ppy-FA. A eficiência de carregamento Dox dos nanocompósitos PNIPAM-ppy-FA foi calculada para 15% usando a curva de calibração Dox (dados não mostrados). Na Fig. 4a, o perfil de liberação de Dox de PNIPAM-ppy-FA foi estudado em diferentes temperaturas. Observamos o comportamento de liberação de Dox por 72 h a 25 ° C, 37 ° C e 50 ° C e a liberação cumulativa de Dox de PNIPAM-ppy-FA foi de 15%, 42% e 67%, respectivamente. Uma vez que LCST de PNIPAM-ppy-FA diminuiu ligeiramente para 42 ° C, a liberação cumulativa à temperatura corporal foi considerada relativamente maior do que a temperatura ambiente. Uma grande quantidade de Dox foi liberada, no entanto, o Dox liberado não afetou a eficiência terapêutica, porque os nanocompósitos Dox @ PNIPAM-ppy-FA puderam ser internalizados apenas em células positivas para receptor de folato, conforme descrito anteriormente [26, 32]. Acima da LCST (50 ° C), a quantidade de Dox dos nanocompósitos PNIAPM-ppy-FA foi liberada quatro vezes maior do que a temperatura ambiente, sugerindo que os nanocompósitos PNIPAM-ppy-FA poderiam ser usados em sistema de liberação controlada de drogas por meio de resposta térmica. Além disso, investigamos o comportamento de liberação desencadeada por luz NIR de nanocompósitos PNIPAM-ppy-FA na Fig. 4b. A solução Dox @ PNIAPM-ppy-FA (1 mg / mL) foi exposta ao laser NIR (3 W / cm 2 ) irradiação por 10 min e esta operação foi repetida a cada 1 h. Durante 6 h, a quantidade total de Dox via irradiação com laser NIR atingiu 35%, enquanto o perfil de liberação de Dox sem irradiação com laser NIR mostrou cerca de 5% e 15% (25 ° C e 37 ° C). Este resultado mostrou que a irradiação com laser NIR resultou em uma temperatura mais alta do que LCST de nanocompósitos e induziu a liberação de Dox dos nanocompósitos PNIPAM-ppy-FA.
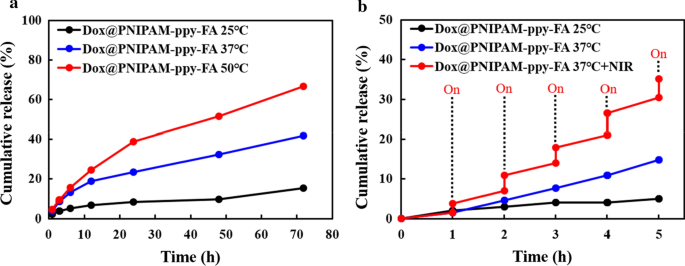
a Perfis de liberação Dox cumulativos de Dox @ PNIPAM-ppy-FA via resposta térmica e b Irradiação de laser NIR de 808 nm
Análise de citotoxicidade e absorção celular de nanocompósitos PNIPAM-ppy-FA
De acordo com a literatura, a citotoxicidade dos nanocompósitos PNIPAM-ppy-FA foi investigada para células de câncer de pulmão e mama (Arquivo adicional 1:Fig. S2) [33, 34]. Independentemente das concentrações da amostra, após incubação com PNIPAM-ppy-FA por 24 h, ambas as viabilidades celulares foram observadas (> 85%). Portanto, nossos nanocompósitos PNIPAM-ppy-FA não mostraram citotoxicidade como um nanocarreador para aplicações de entrega de drogas [35, 36]. Para investigar se PNIPAM-ppy-FA poderia entregar seletivamente às células cancerosas, examinamos os sinais fluorescentes de nanocompósitos intracelulares PNIPAM-ppy-FA usando microscopia confocal de varredura a laser (arquivo adicional 1:Fig. S3). Os comportamentos de captação celular das linhas de células PNIPAM-ppy-FA e Dox @ PNIPAM-ppy-FA foram avaliados em receptor de folato negativo (A549) e positivo (MDA-MB-231) [37]. Após incubação de células de câncer de mama MDA-MB-231 com Dox @ PNIPAM-ppy-FA, forte fluorescência vermelha foi observada, mostrando que Dox @ PNIAPM-ppy-FA foram internalizadas em lisossomas de células MDA-MB-231. Em constante, quando PNIPAM-ppy-FA e Dox @ PNIPAM-ppy-FA foram tratados com células A549, os sinais Dox não foram observados. Essas imagens confocais demonstraram que os nanocompósitos de PNIAPM-ppy-FA podem ser internalizados seletivamente em células cancerosas superexpressas de receptor de folato através da via de endocitose mediada por receptor, conforme descrito anteriormente [38, 39].
Efeitos quimio-fototérmicos anticâncer de NIR e nanocompósitos termossensíveis PNIPAM-ppy-FA
Para confirmar a eficácia terapêutica da combinação in vitro de nanocompósitos PNIPAM-ppy-FA, os nanocompósitos PNIPAM-ppy-FA foram avaliados em células MDA-MB-231 com ou sem irradiação de laser NIR e as viabilidades celulares foram avaliadas por ensaio MTT na Fig. 5a . Para terapia fototérmica, as células de câncer de mama MDA-MB-231 com PNIPAM-ppy-FA foram incubadas por 12 h e foram subsequentemente expostas ao laser NIR (5 W / cm 2 , 5 min). A viabilidade celular das células do câncer de mama MDA-MB-231 diminuiu para 70-90%, dependendo das concentrações de PNIPAM-ppy-FA. Para confirmar o único efeito quimioterapêutico, nanocompósitos PNIPAM-ppy-FA carregados com Dox foram tratados. Observamos que as viabilidades diminuíram para 50% devido à liberação de Dox dos nanocompósitos, correspondendo ao perfil de liberação na Fig. 4. Curiosamente, após a irradiação do laser NIR nas células MDA-MB-231 com nanocompósitos Dox @ PNIPAM-ppy-FA, o a viabilidade celular diminuiu drasticamente até 24%, que foram maiores do que os dos grupos de controle (PNIPAM-ppy-FA com irradiação a laser NIR, Dox @ PNIPAM-ppy-FA sem irradiação a laser NIR). Este resultado indicou um efeito de sinergia ideal da terapia de combinação quimio-fototérmica mediada por irradiação a laser NIR. Além disso, para observar diretamente a eficiência terapêutica em células cancerosas, o ensaio vivo / morto foi realizado na Fig. 5b. Como um grupo de controle, observamos a viabilidade de apenas células MDA-MB-231 com ou sem irradiação a laser NIR (5 W / cm 2 , 5 min) e a maioria das células apresentou fluorescência verde (células vivas). Demonstrou que a irradiação com laser NIR não afetou evidentemente a viabilidade celular. Além disso, as células MDA-MB-231 com PNIPAM-ppy-FA sob irradiação com laser NIR apresentaram algumas fluorescências vermelhas (células mortas), indicando efeito terapêutico fototérmico causado pelos nanocompósitos PNIPAM-ppy-FA. Apesar de não haver irradiação de laser NIR em células MDA-MB-231 com Dox @ PNIPAM-ppy-FA, foi observada uma fluorescência vermelha esporádica, indicando quimioterapia. Além disso, quando as células MDA-MB-231 foram tratadas com nanocompósitos e irradiação com laser NIR, a maioria das células cancerosas exibiu um pouco de fluorescência vermelha [39, 40]. Estes resultados apoiaram os efeitos terapêuticos sinérgicos da terapia quimio-fototérmica via irradiação a laser NIR e nanocompósitos Dox @ PNIPAM-ppy-FA termo-responsivos.
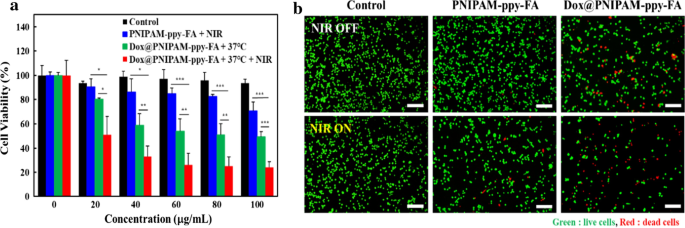
a Análise quantitativa da viabilidade de células de câncer de mama MDA-MB-231 tratadas com PNIPAM-ppy-FA e Dox @ PNIPAM-ppy-FA com diferentes concentrações e com ou sem irradiação a laser NIR de 808 nm. b Imagens de fluorescência de ensaio vivo / morto em células MDA-MB-231 após o tratamento de nanocompósitos PNIPAM-ppy-FA e Dox @ PNIPAM-ppy-FA (60 μg / mL) com ou sem irradiação a laser NIR. As células vivas e mortas são coradas com Calcein AM (verde) e homodímero de Ethidium-1 (vermelho). Barras de escala são 200 μm
Conclusão
Nós construímos com sucesso um NIR direcionado ao câncer e nanocompósitos PNIPAM-ppy-FA termo-responsivos para terapia de combinação quimio-fototérmica. Para induzir a liberação controlada e o efeito fototérmico via irradiação com laser NIR de 808 nm, as nanopartículas de ppy foram uniformemente decoradas em PNIPAM-AAc pelo método de polimerização. PNIPAM-ppy-FA carregado com Dox mostrou efeito fototérmico e fotoestabilidade significativos. Além disso, Dox @ PNIPAM-ppy-FA mostrou propriedades favoráveis de transição termossensível em diferentes condições e a liberação do fármaco dos nanocompósitos PNIPAM-ppy-FA pode ser controlada por luz NIR e resposta térmica. Estudos in vitro verificaram que os nanocompósitos PNIPAM-ppy-FA mostraram excelente biocompatibilidade e eficácia terapêutica aprimorada para células de câncer de mama. Esta eficácia anticâncer aumentada por meio de nanocompósitos contribuiu para as seguintes razões:(1) captação celular específica de nanocompósitos em endocitose mediada por receptor de folato, (2) liberação de Dox acumulada de PNIPAM-ppy-FA via NIR e resposta térmica, e (3) ) efeito terapêutico sinérgico por combinação quimio-fototérmica. Portanto, nosso nanocompósito PNIPAM-ppy-FA poderia ser potencialmente usado como um nanocarreador multifuncional para abordagens terapêuticas sinérgicas para diferentes tipos de câncer com efeitos colaterais reduzidos.
Disponibilidade de dados e materiais
Os dados e a análise no presente trabalho estão disponíveis com os autores correspondentes mediante solicitação razoável.
Abreviações
- PTT:
-
Terapia fototérmica
- NIR:
-
Próximo ao infravermelho
- FA:
-
Ácido fólico
- FA-PEG-NH 2 :
-
Amina FA-PEG
- LCST:
-
Temperatura crítica mais baixa da solução
- PNIPAM:
-
Poli ( N -isopropilacrilamida)
- ppy:
-
Polipirrol
- TEM:
-
Microscopia de transmissão
- UV – Vis:
-
Espectroscopia ultravioleta-visível
Nanomateriais
- Nanopartículas para terapia do câncer:progresso e desafios atuais
- Nanorods de ouro revestidos com BSA para terapia fototérmica NIR-II
- Estruturas Metálicas-Orgânicas de Meio Ambiente como Sistema de Administração de Medicamentos para Terapia de Tumor
- Administração de medicamentos baseados em células para solicitações de câncer
- Nanocompósitos de poli (N-isopropilacrilamida) magnético:efeito do método de preparação nas propriedades antibacterianas
- Síntese fácil de nanocompósitos magnéticos funcionalizados por superfície para adsorção efetivamente seletiva de corantes catiônicos
- Síntese mediada por sementes de nanobastões de ouro de razão de aspecto ajustável para imagens fotoacústicas no infravermelho próximo
- Nanosensibilizador magnético modificado por aptâmero para imagens de ressonância magnética in vivo de câncer que expressa HER2
- Síntese fácil em um vaso de pontos de carbono de polidopamina para terapia fototérmica
- Carbon Dots @ Platinum Porfirina Composto como Nanoagente Teranóstico para Terapia Eficiente Fotodinâmica do Câncer



