Nanomedicina lipossomal:Pedidos de entrega de drogas na terapia do câncer
Resumo
O aumento da prevalência do câncer, uma doença em que o crescimento celular rápido e incontrolável causa complicações e disfunção dos tecidos, é uma das preocupações sérias e tensas de cientistas e médicos. Atualmente, o diagnóstico do câncer e principalmente seu tratamento eficaz têm sido considerados um dos maiores desafios da saúde e da medicina no século passado. Apesar dos avanços significativos na descoberta e distribuição de medicamentos, seus muitos efeitos adversos e especificidade e sensibilidade inadequadas, que geralmente causam danos a tecidos e órgãos saudáveis, têm sido grandes barreiras para seu uso. A limitação na duração e quantidade da administração desses agentes terapêuticos também é um desafio. Por outro lado, a incidência de células tumorais resistentes aos métodos típicos de tratamento do câncer, como a quimioterapia e a radioterapia, evidencia a intensa necessidade de inovação, aprimoramento e desenvolvimento das propriedades dos fármacos antitumorais. Os lipossomas têm sido sugeridos como candidatos adequados para a administração de drogas e tratamento do câncer em nanomedicina devido à sua capacidade de armazenar drogas com diferentes características físicas e químicas. Além disso, a alta flexibilidade e potencial da estrutura do lipossoma para modificação química pela conjugação de vários polímeros, ligantes e moléculas é um fator importante para os lipossomas, não apenas para aumentar seus méritos farmacológicos, mas também para melhorar a eficácia dos medicamentos anticâncer. Os lipossomas podem aumentar a sensibilidade, especificidade e durabilidade desses agentes anti-células malignas no corpo e fornecer benefícios notáveis para serem aplicados em nanomedicina. Revisamos a descoberta e o desenvolvimento de lipossomas com foco em suas aplicações clínicas para tratar diversos tipos de câncer e doenças. Como as propriedades dos medicamentos lipossomais podem ser melhoradas e suas oportunidades e desafios para a terapia do câncer também foram considerados e discutidos.
Resumo gráfico
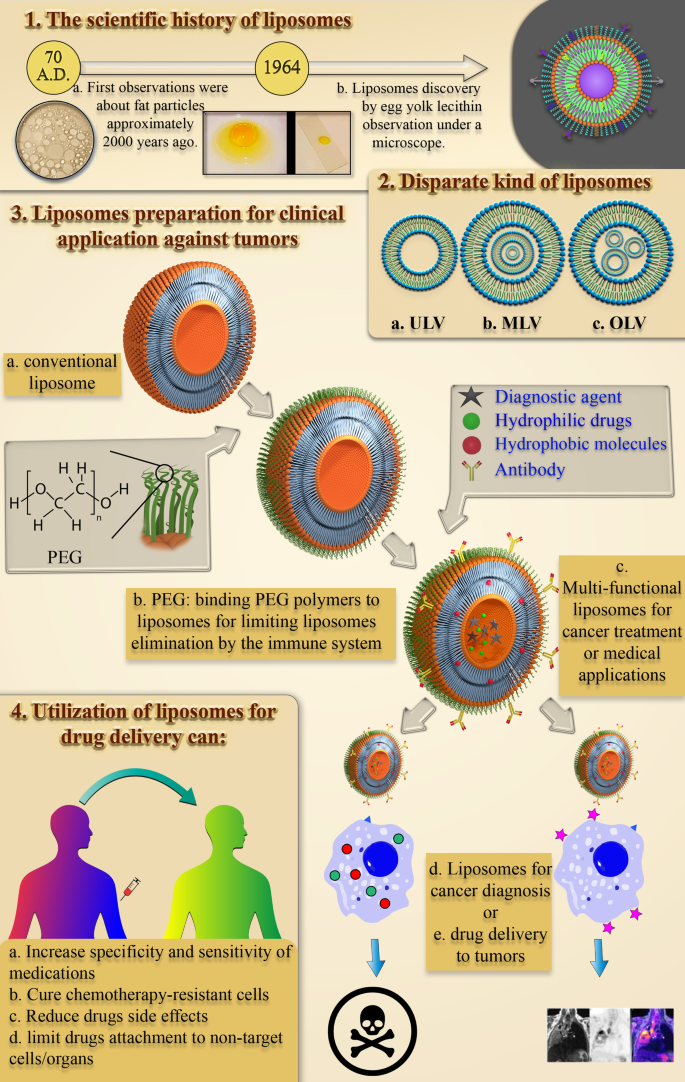
Introdução
O câncer, uma doença em que as células saudáveis do corpo saem do estado normal e se dividem de maneira descontrolada, é reconhecido como um grande desafio médico no século atual. Essa complicação é causada pelo acúmulo de carcinógenos ambientais ou mutações genéticas [1] e é reconhecida como um grande desafio médico no século atual. Milhões de pessoas morrem todos os anos devido ao câncer, e o número de novos pacientes e a taxa de mortalidade estão crescendo continuamente [2]. De acordo com relatórios da Organização Mundial da Saúde (OMS), o câncer foi a segunda causa de mortalidade em 2018, e uma estimativa mostrou que cerca de 9,6 milhões de pessoas morreram de vários tipos de câncer naquele ano. Em 2018, 1 em cada 6 mortes foram causadas aproximadamente por câncer. Cerca de 70% das mortes por câncer ocorrem em países em desenvolvimento e de baixa renda. No entanto, a incidência e a taxa de letalidade do câncer em países desenvolvidos também devem ser consideradas [3].
A quimioterapia com agentes antitumorais é conhecida por ser um importante tratamento para o câncer [4]. A quimioterapia com medicamentos gratuitos é limitada devido à falta de sensibilidade e especificidade adequadas. Como resultado, esta limitação impediu o tratamento preciso devido aos efeitos colaterais e inibiu o esforço do efeito antitumoral suficiente [5]. A quimioimunoterapia, um tratamento combinado concomitante, também foi sugerida como um método eficaz e promissor para a terapia do câncer, tratando explicitamente as células tumorais resistentes aos medicamentos convencionais. Nos últimos anos, uma variedade de tratamentos convencionais e avançados foram descobertos e aplicados para tratar o câncer. Por exemplo, para reduzir os efeitos colaterais de drogas anticâncer convencionais, especificamente agentes de quimioterapia, vários nanomedicamentos [6], incluindo nanopartículas virais (VNPs) [7, 8], pontos quânticos [9], nanomateriais de polímero [10] e lipossomas [11] foram aplicados.
Entre os diferentes nanomedicamentos, os lipossomas como nanopartículas esféricas (NPs) possuem uma estrutura particular. A presença de duas fases aquosa e orgânica no constituinte do lipossoma permite o aprisionamento de ambos os tipos de agentes hidrofílicos e hidrofóbicos e cria uma vantagem notável para o lipossoma em relação a muitos nanocarreadores. Uma das maneiras de aumentar as propriedades de especificidade, biodisponibilidade e biocompatibilidade dos medicamentos antitumorais é aprisioná-los em diversos tipos de lipossomas [5]. Nas últimas duas décadas, esforços significativos foram feitos para explorar os lipossomas para fins terapêuticos. Alguns desses medicamentos, como DaunoXome® e Caelyx®, foram aprovados para aplicações gerais e clínicas, enquanto outros estão em fase final de produção e aprovação [12].
Geralmente, existem diferentes tipos de lipossomas terapêuticos, tais como imunolipossomas e lipossomas sensíveis ao pH. Os imunolipossomas são um grande grupo de dispositivos nanomédicos, também conhecidos como sistemas de entrega de drogas direcionadas (DDSs), que têm demonstrado efeitos anti-malignos significativos em estudos e pesquisas [13]. Os lipossomas sensíveis ao pH também são conhecidos como um grupo de lipossomas polimórficos, nos quais a estrutura e as moléculas constituintes são alteradas pela mudança do pH, levando à liberação de seu conteúdo de fármaco [14]. Além disso, os lipossomas, como outras nanomedicinas, têm potencial para serem utilizados para reparo e regeneração de tecidos, imagens e diagnóstico, além de sistemas de liberação de medicamentos. O uso de lipossomas em vários aspectos simplifica a identificação, gerenciamento e tratamento de doenças e cânceres [15].
Neste artigo, é apresentado um resumo das descobertas sobre a descoberta e estrutura dos lipossomas, várias propriedades dos lipossomas e drogas lipossomais para o tratamento do câncer no mercado e seu desenvolvimento. Por fim, será concluído um relatório sobre as oportunidades e desafios da utilização dos nanomedicamentos lipossomais, que podem ser destacados como questões cruciais a serem percebidas nas pesquisas futuras dos cientistas, levando à remoção das limitações e fortalecendo os pontos positivos.
Texto Principal
A história científica dos lipossomas:descoberta e definição
Demorou cerca de 1950 anos desde os primeiros estudos sobre a estrutura e o comportamento de pequenas partículas de lipídios em um ambiente aquoso até a primeira nanopartícula de entrega de fármaco à base de lipídios aprovada pelo FDA dos EUA. O processo de estudar o comportamento dos lipídios e das partículas de gordura no aqua começou com as primeiras observações de Plínio, o Velho, quase 2.000 anos atrás [16]. No final do século XVII, a descoberta da célula por Anthonie Van Hook levantou muitas questões sobre a estrutura das células [17]. Então, Gorter e Grendel descobriram a presença de bicamadas fosfolipídicas nas membranas celulares [18]. Posteriormente, Singer e Nicolson descreveram posteriormente o modelo de membrana em mosaico de duas camadas para explicar o comportamento dos fosfolipídios da membrana celular [19]. Essas observações e hipóteses científicas atraíram a atenção de outros cientistas para NPs derivados de gordura. Na década de 1960, Alec D. Bangham, que estudou o efeito dos lipídios, principalmente dos fosfolipídios, no processo de coagulação do sangue no Instituto Babraham [20, 21], observou acidentalmente os primeiros lipossomas e ficou surpreso ao ver a formação de partículas esféricas espontâneas no água [22]. Posteriormente, Gerald Weissmann, um visitante do laboratório de Alec Bangham que estava ciente dos resultados da pesquisa de Bangham, chamou a Mesofase Esmética observada por Alec de "lipossomas" em vez de "banghossomos" e ganhou o Prêmio Nobel [22]. A história científica da descoberta de lipossomas está resumida na Fig. 1.
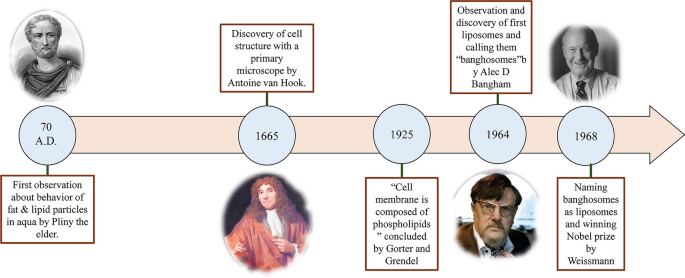
Diagrama de observações que levaram à descoberta dos lipossomas. As tendências históricas e científicas do estudo do comportamento de partículas de lipídios e gorduras na água e as observações que levaram à descoberta dos lipossomas, junto com imagens dos cientistas envolvidos no evento, Plínio, o Velho [23], Anthonie Van Hook [24], Alec D. Bangham [25] e Gerald Weissmann [26], respectivamente, da esquerda para a direita
Quais estruturas são conhecidas como nanopartículas lipossomais atualmente?
Há um intenso esforço para definir NPs lipossomais e descobrir suas propriedades de maneira razoável. Hoje em dia, os lipossomas são definidos como fragmentos de formação espontânea e esféricos que consistem em uma membrana de bicamada lipídica e um núcleo hidrofílico.
Os lipossomas variam em tamanho na faixa de cerca de 10 nm a 2500 nm (ou 2,5 µm) [15]. No entanto, a maioria dos lipossomas administrados para a entrega de drogas têm, tipicamente, cerca de 50 a 450 nm de tamanho. Definitivamente, lipossomas com dimensões muito maiores também podem ser utilizados para aplicações médicas [27]. Além disso, os lipossomas são compostos principalmente por fosfolípidos. Os fosfolipídios são um tipo de lipídios, que são curiosamente semelhantes aos triglicerídeos. Na estrutura dos fosfolipídios, existe um pólo hidrofílico e duas cadeias hidrofóbicas. Assim, os fosfolipídios são considerados moléculas anfifílicas.
A membrana de lipossoma de fosfolipídios inclui principalmente fosfatidilcolina (PC), esfingomielina (SM), fosfatidilserina (PS) e fosfatidiletanolamina (PE), que são anfifílicos e têm uma forte tendência para formar estruturas particulares na água [28]. A razão física para esse fenômeno é a co-presença de uma cabeça hidrofílica (molécula de fosfato) e duas caudas hidrofóbicas (ácidos graxos) nos fosfolipídios. O grupo fosfato interage com H 2 Moléculas O polares, enquanto as caudas hidrofóbicas escapam das moléculas de água e interagem umas com as outras [29]. Nesse caso, as cadeias apolares são colocadas opostas uma à outra e formam uma bicamada, criando um espaço lipofílico entre elas. Consequentemente, esta estrutura parcial lipofílica dos lipossomas pode ser aplicada para armazenar agentes e materiais hidrofóbicos. Além disso, a seção hidrofílica do fosfolipídeo é então direcionada para as moléculas de água por meio de forças moleculares, como ligações de hidrogênio, Van der Waals, etc., que aparecem entre elas. Isso leva à formação de uma área hidrofílica dentro dos lipossomas. A estrutura da molécula de lecitina, como um fosfolipídeo natural que é abundante na gema de ovo e capaz de formar lipossomas em água e em várias regiões de um lipossoma, é mostrada na Fig. 2.
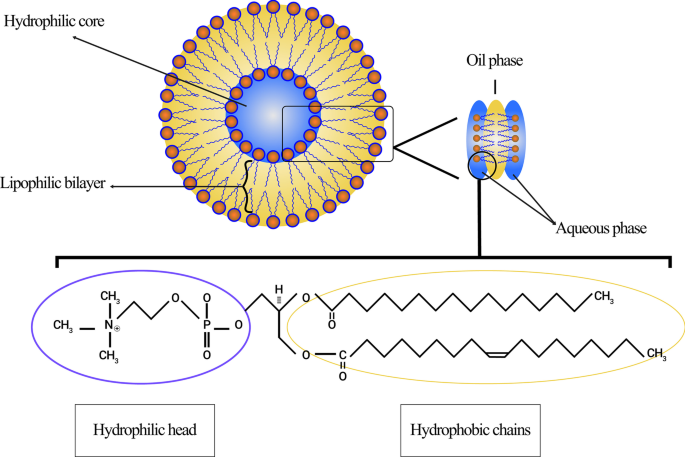
Figura esquemática dos lipossomas originados da lecitina. Diferentes regiões de lipossomas, incluindo núcleo hidrofílico e bicamada hidrofóbica, são demonstradas. A estrutura da molécula de lecitina, seu pólo hidrofílico e cadeias hidrofóbicas são especificadas
Da mesma forma, a estrutura esférica dos lipossomas após a dissolução em água, dependendo do tipo de moléculas, da temperatura do meio aquoso, da concentração molar e da presença de outras substâncias, como íons, determina sua forma final [30]. Os atributos físicos e químicos predominantes de um lipossoma são as propriedades líquidas dos lipídios que os compõem, especialmente os fosfolipídios e as outras moléculas que os compõem. Essas propriedades incluem permeabilidade, densidade de carga superficial e tamanho geral [31].
Classificação de tipos diferentes de lipossomas
Desde a descoberta dos lipossomas, essas estruturas sempre foram utilizadas como parte essencial de pesquisas biológicas, biofísicas, bioquímicas ou farmacêuticas.
Hoje, os lipossomas podem ser categorizados com base em seu tamanho, o número de sua bicamada fosfolipídica, procedimento de síntese e mecanismo de preparação. Em termos de tamanho, os lipossomas podem ser divididos em três grupos:pequeno, médio e grande. Considerando o número de camadas de membrana, elas podem ser vesículas unilamelares (ULVs), vesículas oligolamelares (OLVs) e vesículas multilamelares (MLVs). A este respeito, os ULVs são lipossomas compostos por uma bicamada de fosfolipídios medindo cerca de 50 a 250 nm, enquanto os MLVs são muito maiores, cerca de 0,5-1,5 µm, e incluem várias membranas de bicamada de fosfolipídios [32]. Diferentes métodos de síntese causam margens entre esses dois grupos. Em termos de aplicação, os ULVs também possuem um grande ambiente hidrofílico internamente, o que os torna adequados para o aprisionamento de drogas hidrofílicas. As pequenas vesículas unilamelares (SUVs), como as ULVs, são compostas por uma bicamada fosfolipídica, mas em termos de dimensão, têm menos de 100 nm de tamanho [33, 34]. Do ponto de vista morfológico, os OLVs são lipossomas compostos por duas a cinco vesículas que podem ter tamanhos idênticos ou diferentes. Na estrutura das OLVs, as vesículas estão todas encerradas em uma grande bicamada fosfolipídica, sem estar dentro uma da outra. Os OLVs geralmente são cerca de 0,1–1 µm [33,34,35]. Em contraste com ULVs, MLVs não são ideais para a entrega de substâncias hidrofílicas. MLVs são principalmente explorados para a entrega de agentes hidrofóbicos [36]. Diferentes tipos de lipossomas são ilustrados na Fig. 3.
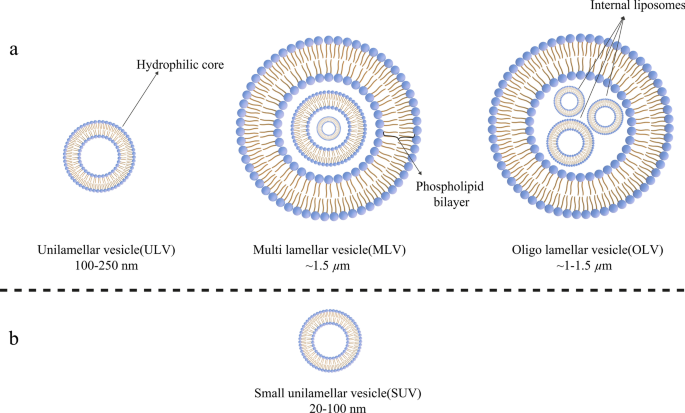
Classificação dos lipossomas de acordo com vários critérios: a Os lipossomas são divididos em três categorias em termos de tamanho; b A estrutura da pequena vesícula unilamelar (SUV), como um membro das vesículas unilamelares (ULVs), que tem um tamanho pequeno perceptível
Métodos de preparação de lipossomas e desenvolvimento de suas novas gerações
Em contraste com as nanopartículas de ouro como NPs duras, os lipossomas são NPs suaves [37] e podem ser sintetizados por meio de diferentes métodos. Por exemplo, MLVs e ULVs têm mecanismos distintos de preparação. Na maioria desses métodos, um solvente particular (como clorofórmio ou metanol, etc.) é usado para resolver lipídios destinados a formar membranas de lipossomas (com a razão molar desejada) em um frasco de fundo redondo (RBF). Por exemplo, apertar a mão é o procedimento primário para sintetizar MLVs [38]. Durante este procedimento, que também é conhecido como hidratação de filme lipídico, os lipídeos são adicionados a um solvente orgânico. Em seguida, o solvente é evaporado por um dispositivo rotativo e o produto sólido é lipolisado. Em última análise, os lipossomas são sintetizados seguindo métodos de hidratação e extrusão [39]. Outros métodos de síntese de lipossomas incluem sonicação, evaporação de fase reversa, célula de pressão francesa, liofilização e extrusão de membrana [38, 40].
Além disso, os lipossomas também podem ser ordenados em diferentes categorias com base em sua descoberta e desenvolvimento ao longo do tempo. Os lipossomas de primeira geração são geralmente denominados lipossomas convencionais ou clássicos. Os problemas, que foram observados ao usar lipossomas convencionais como NPs terapêuticos, foram identificados tão rapidamente in vivo. Um dos primeiros problemas examinados foi a limitação do aprisionamento do fármaco nos lipossomas. Em outras palavras, muitos medicamentos não foram capazes de ser armazenados dentro dos lipossomas de primeira geração [41]. Junto com o grande desejo de pesquisar a estrutura e propriedades dos lipossomas, como estabilidade, eficácia terapêutica e, a possibilidade de aplicações clínicas, esses desafios levaram ao desenvolvimento de lipossomas de segunda geração por meio da alteração de lipídios constituintes, carga superficial, peso líquido, e volume total [42]. Para ser preciso, os lipossomas de segunda geração são sintetizados principalmente pela adição de alguns polímeros hidrofílicos a lipossomas convencionais para o aumento de sua vida útil em fluidos corporais para torná-los candidatos apropriados para sistemas de distribuição de drogas. Este tipo de lipossoma pode ser dividido em dois grupos:lipossomas de longa circulação não específicos ou lipossomas de longa circulação direccionados para o ligando [43].
Os arqueossomos, como uma nova geração de lipossomas, são constituídos pelo lípido da membrana arquea e por análogos de fosfolípidos sintéticos. Na última década, esforços extensos e consideráveis foram feitos para investigar o potencial dos arqueossomos para serem empregados na distribuição de drogas e vacinas. Os núcleos estruturais dos lípidos do tipo arquea são moléculas de diéter ou tetraéter com cadeias fittanil saturadas que contêm cerca de 20 a 40 carbonos. Essas cadeias de carbono se ligam às ligações de éter dos carbonos sn-2,3 da espinha dorsal do glicerol encontrado em arqueol ou caldarqueol. Como mencionado acima, essas partículas também podem ser amplamente utilizadas na administração de medicamentos para complicações neoplásicas, alergias e infecções, bem como vacinas [44].
Avaliação das características do biomaterial e propriedades físico-químicas dos lipossomas
Conforme mencionado anteriormente, apesar dos avanços generalizados nas ciências médicas, o tratamento de algumas doenças, especialmente o câncer, ainda enfrenta desafios formidáveis devido aos agentes e métodos terapêuticos ineficientes. Ajustar a dose do medicamento injetado para influenciar os tumores é uma questão tensa devido à estreita janela terapêutica dos agentes anticâncer. Em outras palavras, um pequeno distanciamento entre a dose terapêutica e a tóxica, bem como sensibilidade e especificidade inadequadas, têm criado uma grande demanda por procedimentos corretivos avançados [42].
Além disso, a utilização de nanomateriais para entrega de drogas aos tecidos tem chamado a atenção recentemente. Biocompatibilidade e biodegradabilidade são duas características essenciais das características do biomaterial para a disponibilidade de nanomateriais em sistemas de distribuição. A biocompatibilidade é necessária para inibir os NPs terapêuticos de danificar os tecidos e sistemas do corpo e, a biodegradabilidade é urgente para quebrar os NPs em compostos não tóxicos e removê-los simplesmente dos órgãos [15]. Após a detecção dos lipossomas, os cientistas começaram a aplicá-los como nanomateriais para a entrega de drogas. Como mencionado, os lipossomas possuem duas propriedades de biomateriais necessárias para fins terapêuticos:biocompatibilidade e biodegradabilidade [36]. Além disso, os NPs lipossômicos têm outras características que os tornam adequados para essa finalidade. Por exemplo, devido à estrutura específica dos lipossomas, ambos os grupos de fármacos hidrofílicos (solúveis em água) e hidrofóbicos (solúveis em lípidos) podem ser encapsulados neles. Além disso, a presença de uma membrana de bicamada fosfolipídica em lipossomas protege os agentes armazenados em lipossomas de vários fenômenos e danos, como degradação enzimática, inativação biológica por estruturas imunológicas e alterações químicas in vivo. Este ponto tem duas vantagens significativas:primeiro, a estrutura das moléculas aprisionadas no lipossoma é preservada antes de atingir o tecido-alvo, e nenhuma modificação é feita nele e, segundo, outros tecidos saudáveis e não-alvo são protegidos da exposição ao droga devido à membrana do lipossoma e, não pode ser influenciada por esses agentes [42]. Os lipossomas também podem ser aplicados para a entrega de materiais genéticos, como DNA, RNA, etc. e, para fins de terapia gênica. Os lipossomas utilizados para este fim podem ser compostos por lipídios catiônicos, aniônicos, neutros e fosfolipídios ou uma mistura deles [45]. Alguns agentes de diagnóstico e imagem, como pontos de carbono, podem ser utilizados para detecção de câncer e imagem na combinação de lipossomas ou isoladamente [46]. Embora os pontos de carbono sejam parcialmente aprovados para aplicação clínica e explorados em investigações, a citotoxicidade permanece uma barreira desafiadora para sua ampla aplicação [47]. A estrutura geral de NPs de drogas lipossomais é mostrada na Fig. 4.
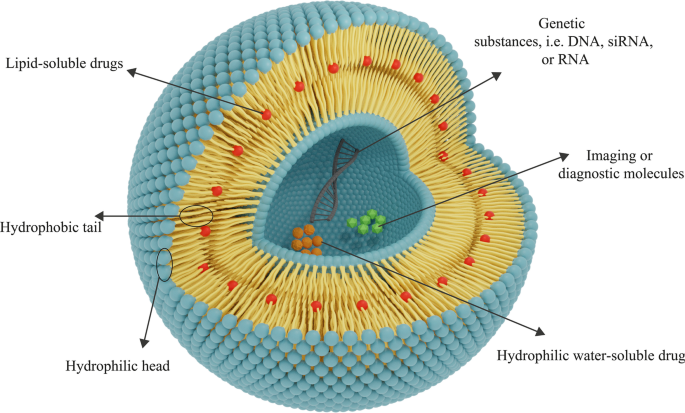
A estrutura geral dos lipossomas consiste em camadas de fosfolípidos. Dependendo da hidrofilia-hidrofobicidade de uma droga, o tipo apropriado de lipossomas para sua entrega será determinado. As drogas hidrofílicas são aprisionadas no núcleo hidrofílico central e as drogas hidrofóbicas são colocadas na área lipofílica. Os lipossomas também podem ser utilizados para a entrega de genes
Os fosfolipídios formadores de membrana presentes nos lipossomas são compostos não tóxicos e podem ser sintetizados em uma ampla gama de tamanhos. Os atributos físico-químicos dos lipossomas dependem de seus constituintes. Assim, lipossomas com as propriedades desejadas podem ser sintetizados pela adição de certos compostos, como colesterol, polietilenoglicol (PEG), etc. Além disso, a membrana dos lipossomas é impermeável a moléculas gigantes, o que ajuda a reter melhor o material dentro do lipossoma [48 ] Todas as características mencionadas do lipossoma o apresentam como um nanomaterial apropriado para exploração na distribuição de agentes terapêuticos para o tratamento de várias doenças, especialmente câncer.
Gregory Gregoriadis, como um dos pesquisadores pioneiros neste campo, propôs a hipótese do uso de lipossomas para os sistemas de liberação de drogas e afirmou que os compostos de drogas poderiam ser aprisionados em lipossomas [49]. O biomaterial apropriado e as propriedades físico-químicas dos lipossomas foram relatados. Por exemplo, uma pesquisa sobre lipossomas contendo o fármaco antitumoral citosina arabinosídeo usado em modelos animais mostrou um aumento significativo na vida de camundongos com leucemia L1210 [50]. Ao aplicar lipossomas, uma dose suficiente da forma ativa do fármaco pode ser entregue ao local alvo de uma maneira protegida [42].
Aumento da especificidade e sensibilidade de NPs lipossomais para usos terapêuticos
Como mencionado anteriormente, o uso de várias moléculas e polímeros possibilita a alteração da estrutura e da membrana dos lipossomas, e por meio disso, novas funcionalidades podem ser adicionadas aos lipossomas ou suas propriedades podem ser modificadas [51]. Tanto o prolongamento da circulação dos lipossomas no sangue como o aumento da sua capacidade de acumulação no tecido tumoral específico ou local patológico através do efeito EPR são as primeiras características importantes que devem ser tidas em consideração devido à elevada taxa de eliminação dos lipossomas. A conjugação de moléculas de PEG a membranas de lipossomas por meio de conjugação química tem sido usada sequencialmente para adicionar esta funcionalidade aos lipossomas [52]. A importância e o papel dos polímeros de etilenoglicol no aumento da meia-vida dos lipossomas, especialmente os NPs terapêuticos lipossomais em fluidos corporais, como o sangue, foram expressos há cerca de 20 anos [53].
Abuchowski e McCoy fizeram as primeiras tentativas de estender a meia-vida dos lipossomas na corrente sanguínea, conjugando PEG à sua estrutura. Como resultado, seus esforços geralmente aumentavam o tempo de circulação dos lipossomas e sua meia-vida na corrente sanguínea [54]. Após alguns meses, outros pesquisadores investigaram a possibilidade de reduzir a alta velocidade de depuração dos lipossomas pelas células do sistema de fagocitose mononuclear (MPS). Ao ligar o PEG às moléculas superficiais dos lipossomas [53], espera-se que a circulação dos lipossomas no sangue melhore. Há uma infinidade de artigos neste campo. Além disso, ao contrário dos lipossomas convencionais, os lipossomas revestidos com PEG demonstraram propriedades farmacodinâmicas independentes da dose [55]. Entre vários polímeros, as moléculas de PEG são um dos polímeros que podem ser ligados à superfície do lipossoma para prolongar a sua vida em prateleira in vivo. Outros polímeros também podem ser usados para este propósito [56]. A Figura 5 demonstra como as moléculas de polímero PEG podem proteger o lipossoma de anticorpos e também prolongar sua vida na corrente sanguínea.
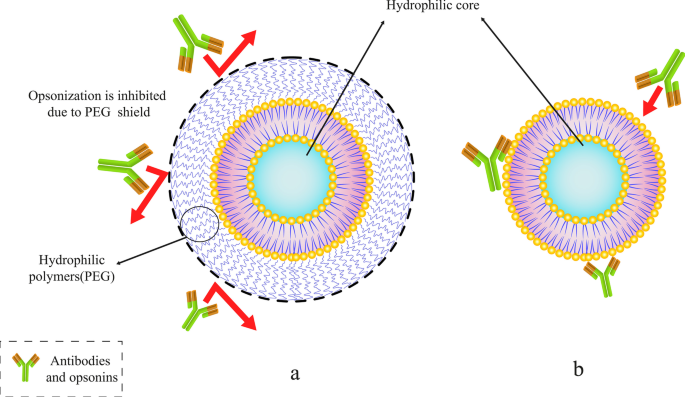
Conjugar um polímero específico, como polietilenoglicol (PEG), a lipossomas. a Lipossomas PEGuilados com proteção de moléculas de polímero PEG. b Lipossoma convencional preso por anticorpos e opsoninas
Como mencionado, é digno de nota que outras moléculas podem ser exploradas para prolongar a circulação de lipossomas além do PEG. Além disso, os polímeros de polioxazolinas estão entre as substâncias usadas para modificar a membrana dos lipossomas para aumentar sua meia-vida. Nesse sentido, Woodle et al. foram o primeiro grupo a aplicar poli [2-etil-2-oxazolina] (PEOZ) para sintetizar lipossomas furtivos. Seus resultados testemunharam uma redução na eliminação e absorção de poli [2-etil-2-oxazolilado] PETOXilado-lipossomas injetados em ratos por células hepático-esplênicas [57]. Seus resultados indicaram que a conjugação de outros polímeros, como poli [2-etil-2-oxazolina] e poli [2-mtil-2-oxazolina] (PMOZ) poderia ter efeitos semelhantes ao PEG no aumento da meia-vida e no prolongamento da circulação de lipossomas in vivo. Eles também compararam a bio-distribuição de lipossomas conjugados com PEG-, PEOZ- e PMOZ em vários órgãos e sistemas. As consequências também demonstraram que a bio-distribuição de todos esses lipossomas no sangue e no baço era quase a mesma, mas no fígado a distribuição de PMOZ era muito menor do que nos outros [57].
Pain et al. moléculas de dextrano ligadas à superfície de ULVs. Seus resultados mostraram que os lipossomas conjugados com dextrana, em comparação com os lipossomas convencionais, tinham uma circulação mais estendida e menor absorção e captação pelo fígado e baço. Esta consequência testificou que as moléculas de dextrano, além de prolongar a vida útil dos lipossomas no corpo, também poderiam ser aplicadas para aumentar a estabilidade e regular a taxa de liberação do fármaco dos lipossomas [58].
A segunda questão que deve ser observada é a fluidez e estabilidade dos lipossomas. Outros lípidos, incluindo colesterol, podem ser usados na estrutura dos lipossomas. O colesterol pode ocasionalmente ser substituído por alguns compostos na bicamada fosfolipídica para aumentar algumas propriedades do lipossoma. No entanto, foi comprovado que a modificação do conteúdo da bicamada do lipossoma e a substituição de algumas das moléculas de fosfolipídios por certos compostos, especialmente o colesterol, podem reduzir a fluidez dos lipossomas [59]. Além disso, a presença de colesterol na membrana dos lipossomas aumenta a estabilidade de sua estrutura (tanto em experimentos in vivo quanto in vitro). Também reduz a permeabilidade e a possibilidade de vazamento de substâncias aprisionadas. O colesterol é um esteróide hidrofóbico que interage com as cadeias hidrofóbicas entre as bicamadas fosfolipídicas para estabilizar sua estrutura quando presente na membrana dos lipossomas. Esta ação do colesterol é substancial quando se explora lipossomas clinicamente in vivo porque evita que o lipossoma se converta em lipoproteína de alta densidade (HDL) e lipoproteína de baixa densidade (LDL) no corpo. Além disso, as estruturas lipídicas presentes no sangue e nos fluidos intracelulares podem ter uma impressão nos lipossomas. Lipoproteínas como LDL e HDL afetam os lipossomas injetados e causam a transferência de lipídios e o rearranjo de suas membranas. Eles também reduzem drasticamente a estabilidade de NPs lipossomais contendo drogas [12]. É perceptível que outros materiais, como DNA e outras moléculas utilizadas na membrana de lipossomas para aplicações terapêuticas, devem ser ancorados ao colesterol na membrana. Adicionar várias substâncias às membranas dos lipossomas é uma forma de criar características positivas nos lipossomas [42].
As terceiras características essenciais que devem ser consideradas são a sensibilidade e especificidade dos lipossomas para uma identificação precisa e ligação específica às células alvo. Pela ligação de compostos, como anticorpos monoclonais, F ab fragmentos e outras moléculas conjugativas, como transferrina e folato, é possível aumentar a especificidade dos lipossomas, resultando em ligação específica às células tumorais [60]. Além disso, o aumento da especificidade e sensibilidade de nanocarreadores de drogas, especificamente lipossomas, foi investigado anteriormente. Por exemplo, Mohammad J. Akbar et al. estudaram lipossomas conjugados com peptídeo-PEG-lipídio para tratar câncer de pulmão de células pequenas (SCLC). Os seus resultados mostraram que a ligação do péptido antagonista do receptor do péptido de libertação de gastrina (GRPR) aos lipossomas pode aumentar a especificidade e a acumulação destes lipossomas em células que expressam GRPR. Eles também alegaram que esses lipossomas ligados a peptídeos poderiam ser aplicados para tratar células de câncer de pulmão devido à regulação positiva de genes que expressam GRPR nelas [61].
Eventualmente, medicamentos e drogas foram adicionados aos lipossomas PEGuilados por causa de suas propriedades apropriadas, e agora, essas estruturas lipossomais foram estabelecidas para utilização clínica-industrial [62]. Os anticorpos também foram usados em estudos iniciais para aumentar a capacidade dos lipossomas de se ligarem às células-alvo [63]. Neste caso, a endocitose mediada por receptor foi realizada por lipossomas para entrar na célula [64]. Enquanto isso, vários métodos foram desenvolvidos para ligar anticorpos a lipossomas [65]. Os estudos sobre os lipossomas conjugados com anticorpos provaram que a toxicidade dos fármacos anticancerígenos contra as células tumorais em cultura aumenta com a conjugação dos anticorpos nas superfícies dos lipossomas [66]. Quando os anticorpos foram aplicados na superfície dos lipossomas de PEG, a relíquia de anticorpos para anexar aos seus receptores alvo foi velada por polímeros de PEG, especialmente quando as cadeias laterais anexadas ao PEG eram longas [67]. Portanto, o uso simultâneo de PEG e anticorpo para medicamentos de lipossomas e suas desvantagens devem ser considerados pelos cientistas.
O quarto fator importante na aplicação terapêutica dos lipossomas é o estudo da liberação dos fármacos neles aprisionados. O ajuste dos lipossomas para a liberação de drogas dentro deles afetadas pelas condições anormais dos tecidos danificados é uma das questões cruciais na administração clínica de lipossomas. Além disso, o uso de compostos sensíveis à temperatura, pH ou um metabólito específico na superfície dos lipossomas que podem se ligar ao tecido e à superfície da membrana das células-alvo é um método para liberar esses medicamentos com precisão. A utilização deste método pode resultar no efeito específico dos lipossomas na superfície da membrana das células-alvo e também na liberação do conteúdo da droga dentro delas [68].
The releasing rapidity of compounds entrapped in liposomal NPs is the fifth substantial criterion for adjusting the dose of drugs available at the target site. One of the essential objects that should be considered for the proper usage of all kinds of drug delivery systems, including liposomes, is the releasing rate of drugs and regulation. With regard to liposomal drug delivery systems and NPs, it is worth mentioning that the encapsulated substances in the liposomes are not biologically available and can only be bioavailable while it is released from the initial state. Therefore, drug-containing liposomes can provide the ability to increase the concentration of bioavailable drugs for cancerous tissues and to improve the quality of treatment and therapeutic efficacy can be achieved on condition that the rate of drug release from the liposome is adjusted [69]. Furthermore, it has been proven that changing the liposome bilayer content and replacing some phospholipids with certain compounds, especially steroid molecules like cholesterol, can decrease the permeability and unintended leakage of the compounds stored in them [70]. Consequently, this advantage can be exploited to adjust the release rate of the encapsulated compound. Once released, the drugs must penetrate sufficiently into the cell and make the necessary physiological-biochemical changes to exert their impact.
As it is mentioned earlier, various compounds, including aptamers, can be conjugated to liposomes. In this regard, Mohammad Mashreghi et al. applied anti-epithelial cell adhesion molecule (anti-EpCAM) as an aptamer to functionalize Caelyx® liposomes. Their experiment outcomes determined that functionalization of Caelyx® with this aptamer could enhance the merits of this liposomal drug and made it a viable option for cancer treatment [71]. Figure 6 shows the structure of different types of liposomes that are used in vitro or for clinically scientific purposes schematically.
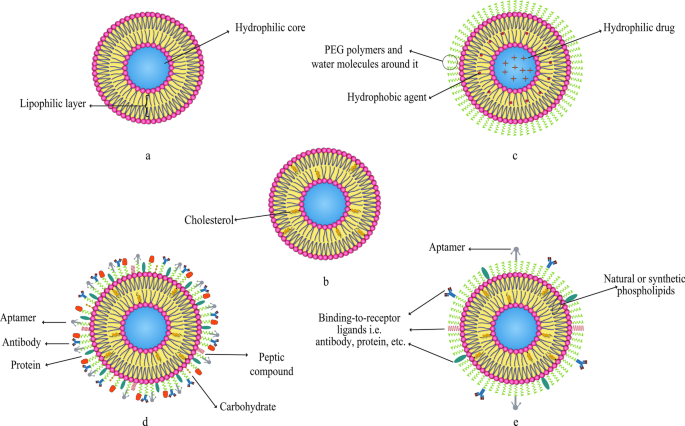
Various kinds of liposomes. a Conventional liposome; b cholesterol-conjugated liposome; c PEGylated or stealth liposome; d ligand-targeted liposome; e multi-functional liposome
The passage of drugs through lysosomes to enter cells (which have low pH and many degrading enzymes) is the sixth most important factor for the practical application of conjugated medicines to liposomes. To protect therapeutic agents from unwanted conversions in extracellular and intracellular space, cell-penetrating peptides are attached to the liposome surface [72].
On Liposomal Drugs Pharmacology:Pharmacokinetics and Pharmacodynamics
The assessment of pharmacological attributes, as an essential part of medicine and pharmaceutical science, is required not only to gain a better understanding of liposomes pros and cons as drug carriers but also to confirm and evaluate them in clinical trials. The pharmacological properties of liposomal drugs and their interactions with the body can be examined in two various aspects:pharmacokinetic (the effect of the body on therapeutic compounds) and pharmacodynamics (how medications act and impact the body and cellular pathways) [73]. In general, the utilization of liposomes for drug delivery in cancer treatment or other disorders requires the elevation of these agents' effectiveness on the one hand, and reducing their toxicity toward normal tissues on the other hand. Subjects such as the proper administration route of NP-based drugs, their circulation in the bloodstream and half-life, their biological distribution in tissues, and their cellular metabolism, as well as their elimination, metabolization and clearance, have been studied in the field of pharmacokinetics [74]. The pharmacokinetics of liposomes primarily study the bioavailability of liposome-conjugated drugs in various body fluids and tissues. Indeed, the study of chemical decomposition and biological excretion, and liposome uptake and purification are also considered in pharmacokinetics. The results of studies on pharmacological advantages of using liposomal drugs (regardless of the type of liposomes applied in the DDS) instead of free drugs showed that:
Primarily, liposome can modify the drug release profile to a sustained release, and consequently, reduce the requirement for constant injection. Secondly, it can extend the presence of the drug in the bloodstream and body fluids, and as a consequence, increase its half-life. Thirdly, it has the potential to lead to better bio-distribution in cancerous tissues while reducing drug influences on healthy tissues due to limited particle size to cross the Endothelium of healthy capillaries. Ultimately, it reduces drug metabolism and inactivation in plasma before reaching the target tissue, in addition to its positive effect on the clearance of drug metabolites [75, 76].
However, some changes are required in the pharmacokinetics of liposomes to increase their solubility, specificity, and sensitivity. These modifications enable them to overcome chemotherapy-resistant cells, enhance the efficacy and half-life. Moreover, their toxicity or unintended metabolic compounds product as a result of their metabolization should be decreased by these modifications [77].
After consuming liposomal drugs administration, they enter the body and circulate in the bloodstream with a specific half-life. Their size and formative composition determine the half-life of liposomal medications. Moreover, rapid clearance of liposomal drugs from the body can reduce their duration of action and therapeutic index. As aforesaid, appending hydrophilic polymers such as PEG to liposomes is able to decrease their clearance rate and solve this challenge [78]. Also, it is possible to adjust the fluidity and drug-release rate of the liposome membrane by adding cholesterol molecules.
The application of liposomes for drug delivery may lead to some changes in drug pharmacokinetics [79]. The ability of liposomes to change the pharmacokinetic properties of the various drugs and medications is one of their significant benefits in drug delivery systems [80]. Concerning the process of liposome clearance and elimination, it is obvious that liposomal structures are affected by plasma proteins after being administered. For instance, after injection of liposomal nanoparticles opsonins are adsorbed on the surface of the liposomes. Opsonins are plasma protiens which mostly include immunoglobulins and fibronectin [42]. Opsonins presence on the surface of liposomes will result in their elimination by MPS, as one of the significant elimination section of various drugs from blood and body fluids. They also clear liposomes through the attachment of some receptors such as complement C3b and Fc to opsonins-liposomes complex [81]. Various tissues and cells such as liver kupffer cells, macrophages present in the spleen, bone marrow, and lymph nodes are involved in the clearance of liposomal NPs [82].
According to the International Union of Pure and Applied Chemistry (IUPAC) definition, pharmacodynamics refers to the study of the pharmacological impact of compounds on living systems and the biochemical and physiological consequences of these effects [83]. The increased elusion to identify therapeutic agents when encapsulated in liposomes has been recognized as one of the pharmacodynamical benefits of liposomes utilization [84].
Furthermore, the physicochemical characteristics have significant influences on the pharmacology of liposomal drugs. The particle size, electrical charge of membrane, and the composition of membrane lipids are some of these physicochemical properties that can affect the pharmacokinetics and pharmacodynamics of the agents. Firstly, there is a direct relationship between the particle size of nanoparticles, including liposomes, and their clearance rate. By increasing the size of NPs, their elimination rate by the immune system and MPS cells will also enhance [85]. Secondly, it is worth mentioning that the net charge of liposome membranes is a consequence of the electrical charge of phospholipids and their other constituting particles that made them up. As a result, a rise in the membrane charge is associated with enhanced clearance rates of these agents [86]. The composition of membrane lipids and other structural features (such as hydrophilic core radius) also remarkably affect the pharmacokinetics of liposomal drugs [87].
More importantly, it has been hypothesized that different types of liposomes exhibit distinct drug kinetics/dynamics depending on their various structures. The drug release rate also rests on the number of phospholipid bilayers and the content of loaded drug compounds. It is also contingent upon the hydrodynamic diameter, total volume, and other pharmacokinetic properties as well [88].
Administration Route of Liposomal Drugs
Like many different drugs, NP-based liposomal medicines can be administered from a wide variety of routes. In other words, oral consumption [89] and distinct injection methods such as intravenous (I.V.) administration and various local injections are among the common administration routes of liposomal drugs [90]. The usage of nanoparticles, including liposomes, for drug delivery via oral administration has been highlighted as an effective strategy since the nanoparticles increase the bioavailability of medicines, improve their interaction with cells, and prevent any modifications in the molecular structure of the drug due to enzymes and gastric juices in the gastrointestinal tract. Moreover, they have the ability not only to enhance the release of remedial molecules into the mucosal and epidermal layer but also to protect drugs from unwanted changes during the first pass effect [89]. Intravenous injection is used as the primary administration route for many liposomal drugs approved by the FDA or other authorities [42]. On the other hand, subcutaneous (S.C.), intradermal (I.D.), intraperitoneal (I.P.), and intramuscular (I.M.), classified under the title of the local injection, are also utilized for administration of liposomal drugs [90,91,92].
Liposomal Drugs Fate In Vivo and Their Targeting Mechanism of Action
Following administration of the liposomal drugs, they reach the pathological lesions at the target site through the bloodstream and accumulate there. The mechanism of action of liposomal drugs on tumors starts with their accumulation at the target site, uptake of them by tumor cells, and the release of free drugs [93]. Subsequent to entering the body, liposomal drugs reach the tumors through various targeting mechanisms of action and then interact with cells in different ways [94]. In general, tumor-targeting mechanisms are divided into two categories:passive and active targeting. Passive targeting refers to the mechanisms in which liposomes are spontaneously accumulated at the tumor site and interact with target cells without the presence of a specific ligand [95]. The effect of enhanced permeability and retention (EPR) has been suggested as the most critical passive targeting mechanism. To be precise, the spontaneous accumulation of therapeutic NPs and liposomal drugs at the tumor site is called the EPR effect [96]. This phenomenon can be assigned to the leaky nature of tumor tissue vessels, unlike normal tissue capillaries, which makes them permeable to molecules and NPs. Consequently, This ultimately leads to the accumulation of drug compounds in these tissues and the effect of EPR [97]. The ultimate fate of the drug in the intracellular fluid and cytoplasm of tumor cells depends on several factors such as release mechanism, nanocarrier constituents, and molecule structure [98]. In healthy tissue, the number and the shape of capillaries are proportionate and normal, respectively. However, in cancerous organs, unlike healthy tissue, the number and the structure of capillaries are higher and deformed, respectively, because of the angiogenesis process. Moreover, the tumor capillaries structure is destroyed, and the endothelial phalanx cells are diminished. As a result, the volume of plasma fluid leaking into the intercellular space will be enhanced. In healthy tissue, however, capillary phalanx cells retain cellular tight adhesions, preventing NPs, small molecules, and liposomal drugs from seeping into the intercellular space [99]. The EPR effect in cancerous capillaries and their difference with normal and healthy tissue vessels are illustrated in Fig. 7.
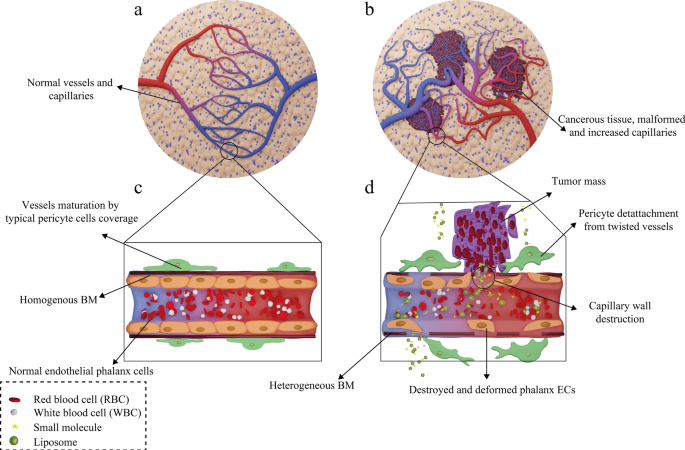
Mechanism of action of the drug-containing liposomes on tumor cells via EPR effect. a Healthy tissue and its normal capillaries; b cancerous tissue with increased-deformed vessels; c structure of normal and healthy vessel; d destructions and deformed capillary in tumor tissue
On the other hand, active targeting has attracted considerable attention as one of the targeting mechanisms of action owing to its appropriate effectiveness and high specificity. Active targeting includes various types and is also generally aimed to reduce the off-target impacts of liposomal NPs on healthy cells and non-target tissues [95]. In this method, molecules such as monoclonal antibodies, small molecules, signal peptides, vitamins, particular carbohydrates, glycolipids, or aptamers are generally utilized for surface modification of liposomes [100, 101]. Moreover, active targeting can be split into various subtypes according to diverse features. For instance, it can be classified into two general categories:
- 1.
Targeting tumor cell and cancer tissue receptors:This method relies on conjugating specific molecules to the membrane surface of liposomes, making them able to bind to special or overexpressed receptors on cancer cells [102]. In cancer cells, upregulation of different genes causes an increase in the expression of specific cell surface receptors in response to enhanced metabolic demands for rapid cell proliferation [103]. In active targeting, particular molecular modifications can be applied for targeting specifically the overexpressed surface receptors of cancer cells, such as folate receptor (FR), transferrin receptor (TfR), or Epidermal growth factor receptor (EGFR) [95]. In this regard, the role of folate receptors in cancer cells is to increase folic acid uptake [104], whereas transferrin receptors bind to transferrin (as a free molecule with 80 kDa weight in serum) and cause endocytosis of this monomeric glycoprotein to occur [105]. Moreover, EGFR receptors are a class of tyrosine kinases involved in cellular processes such as tissue differentiation and repair. The expression of this receptor in cancer cells is significantly increased due to its involvement in processes such as angiogenesis, cell proliferation, and metastasis [106].
- 2.
Utilizing tumor microenvironment as the target:In this method, changes in the surface of liposomes are exploited to enable them to target signal peptides or other receptors in the microenvironment of cancer cells. In other words, this active targeting mechanism can inhibit the growth of tumor cells and metastasis, prevent genotypic and phenotypic variations in neovascular endothelial cells, and control drug resistance [107]. Furthermore, some receptors in the tumor microenvironment, such as Vascular endothelial growth factor (VEGF), Vascular cell adhesion protein (VCAM), matrix metalloproteases, and integrin, are targeted in this mechanism [95].
Cellular Uptake of Therapeutic NPs and the Effect of Liposomal Drugs on Targeted Cells:Actions and Interactions
As it is mentioned earlier, liposomes are able to target tumor cells either passively or actively. After the liposome reaches the cancerous cells and the tumor environment through the targeting mechanism, it can release its therapeutic content and exert its effects by means of various mechanisms. Consequently, lipid composition, the surface charge of the membrane, type of cancer, type of target cells, as well as the presence of specific ligands on the liposome membrane, can influence the cell-liposome interaction [108].
Figure 8 illustrates different types of liposomes interactions with target cells. After being injected into the body, drug-containing liposomes travel to different tissues through blood vessels and eventually reach their target cells based on their surface ligands. These liposomes can bind to cellular receptors via these ligands, which is called specific absorption [42]. Albeit, receptor-free liposomes can also adhere to the target cell surface through molecular attractions, electrostatic forces, and molecular interactions called non-specific absorption. Following liposomes binding to the cell, the therapeutic agent is released into the cytoplasm, and its effects may be produced in different ways. The liposomal nanocarriers can be entirely fused to the plasma membrane of the cell and release the drug. Drug compounds are also able to be released from the liposome into the cell and to enter the cell through micropinocytosis or passive diffusion without the occurrence of fusion. Liposomes may directly interact with the cell or exchange lipid fragments with the cell membrane through protein-mediated processes. At the same time, the drug may act on the cell and exert the therapeutic effects of the liposomal drug. However, some liposomes are capable of entering through endocytosis (specific or nonspecific). In particular, liposomes penetrating the cell via this passage can have various destinies. It is possible for them to combine with lysosomes. In such cases, lysosomal enzymes affect the structure of the drug by reducing the pH of the phagolysosome sac. Ultimately, liposomes release the drug by fusing it to the cell membrane or endocytosis, and after that, medications exert their therapeutic effect [42, 62]. All possible ways for the liposome to penetrate the cell and exert its effect are depicted and compared in Fig. 8.
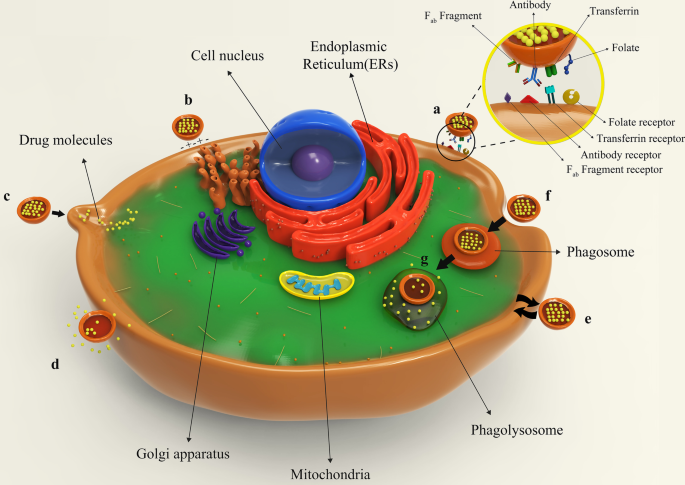
Binding of liposomes to the target cell. a Specific attachment via ligand-receptor interaction; b non-specific absorption of liposomes through intramolecular-electrostatic forces; c the attachment and fusion of liposome to the cell membrane and drug release; d liposome arrival to the target cell and drug release without fusion; e exchange lipid fragments between the cell membrane and liposome through protein-mediated processes; f endocytosis of liposome by target cell; g lysosomal digestion of liposome in the cell cytoplasm
On the other hand, NP-based medications can undergo endocytosis, pinocytosis, or phagocytosis by the target cells. Endocytosis is known as the process in which compounds outside the cell space approach the cell membrane and then enter the cell as a vesicle [109]. Pinocytosis, also recognized as fluid endocytosis, occurs when small molecules or suspensions are introduced into a cell through a vesicle by creating an invagination in the cell membrane. Moreover, pinocytosis vastly occurs in human cells to absorb fat droplets. In an immunological study, Yuriko Tanaka et al. reported that liposome-coupled antigens pinocytosis can be performed by antigen processing cells (APC). This report had proved that liposomes can undergo pinocytosis mechanisms [110]. In phagocytosis, particles larger than 0.5 μm are engulfed by immune cells, it may also occur for liposomes (especially for MLVs and liposomes larger than 500 nm). For example, Jitendra N. Verma et al. confirmed the occurrence of phagocytosis on liposomes by a study on the phagocytosis of liposomes with malarial antigens by macrophages [111].
Kaposi's Sarcoma, One Instance of Successful Liposomal Drugs Applications
Kaposi's sarcoma is a progressive multifocal anti-proliferative cancer primarily known as endometrial sarcoma. This cancer is more common in HIV patients whose immune system is weakened. Furthermore, it has been commonly seen in skin tissue and may also involve other tissues. Hence, this disorder is generally referred to as skin mucosal sarcoma [112]. To treat this disease, modified long-circulating liposomes can be helpful. In this regard, liposomes passively target tumor cells. Moreover, the effect of EPR and specific binding increases the concentration of the therapeutic drug in cancer tissues 5 to 11 times higher than normal skin [113]. For this purpose, Doxorubicin is used for the treatment of this disease. Correspondingly, entrapment of the doxorubicin into liposomes (which was PEGylated to prolong its half-life) prevents normal tissues from being exposed to the drug. It also reduces drug uptake by these healthy doxorubicin-sensitive tissues such as the heart [114].
Additionally, the liposomal form of doxorubicin, Doxil, is a type of anthracycline drug which is approved for clinical administration by US-FDA. It is used to treat AIDS-related Kaposi sarcoma and multiple myeloma [115]. Doxil has better therapeutic efficacy and less toxicity than free doxorubicin, which can be attributed to its ability to target tumors indirectly. It is also passive targeting due to leakage of tumor vessels and the EPR effect [116]. Moreover, the Doxil unilamellar liposomes are < 100 nm in size and have been used to treat various cancer types [42]. Analyses have also proved that free doxorubicin concentration is lower than that of Doxil at the target tissue site [117]. In this regard, Ogawara et al. investigated the effect of Doxil (formed by binding doxorubicin to PEG liposomes) on cancer cells in male mice and showed that PEG liposomal doxorubicin or Doxil1 had been effective on both doxorubicin-resistant and doxorubicin-sensitive C26 cell groups [118]. This can highlight the significance of the exploitation of liposomal NPs. Because they can be consumed to overcome the resistance of cancer cells to common chemotherapy agents at low costs without time-consuming research works to discover new clinical therapeutic compounds [119]. The application of nanoparticles, such as liposomes, to deliver doxorubicin to tumor tissues has been widely investigated. Entrapment of ATP-binding cassette transporter superfamily B member 1 (ABCB1) substrate doxorubicin into liposomes can increase drug uptake and enhance its intracellular distribution within cancer cells, especially ABCB1-expressing cancer cells [120]. The simple structure of Doxil is illustrated in Fig. 9.
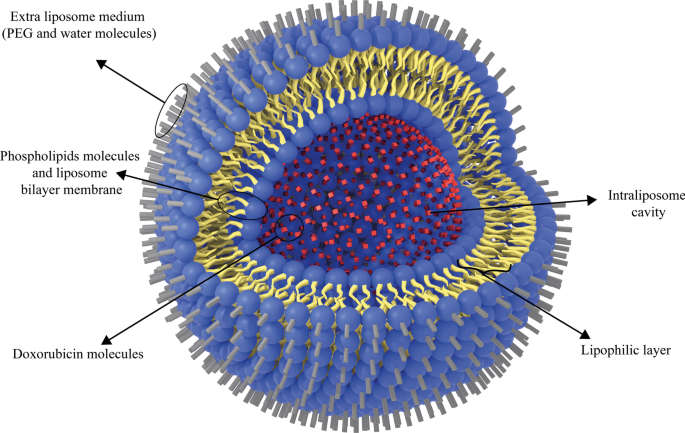
The schematic structure of Doxil drug. Doxorubicin drug molecules are entrapped in the hydrophilic cavity of unilamellar PEGylated liposomes
Furthermore, liposomal nanomaterials can be exploited for the treatment of infectious diseases. Systemic fungal infection is one of the most challenging conditions that is usually treated with amphotericin B, which is highly toxic to kidney cells. For this purpose, the usage of liposome-entrapped amphotericin B can reduce the toxicity of this drug compared to its free form [48]. Unilamellar liposomes have been used to entrap this agent. It has proven that liposomal amphotericin B is more effective than the free drug form [121]. Based on the formulation, these liposomes also alter the bio-distribution of amphotericin B, such as anticancer drugs, which in turn not only arrange the mechanism of action but also increase the effective dosage concentration at the target tissue [122]. AmbiSome, liposomal form amphotericin B, is approved for public administration too. Other approved liposomal drugs, from anti-fungal medications to cancer therapeutic agents, are summarized in Table 1.
Although the application of liposomal NPs to treat cancer has been touted as a viable solution for drug delivery and affecting tumor cells, drug delivery to cancerous tissues in the central nervous system (CNS) has remained a significant challenge. In addition, drug delivery to central nervous system cells faces many turbulences owing to a blood–brain barrier (BBB). However, this problem can be partially solved by developing new methods and using lipid-based compounds [136].
Liposomal Nanoparticles in the Investigational Phase for Therapeutic Purposes
Liposomal siRNA
RNA is a type of genetic molecule with a variety of functions, including translation and transcription processes. The discovery of small-interfering RNA (siRNA) is a significant advance in biology in the last decade [137]. Synthetic siRNAs can be utilized to target oncogenes and their mRNAs. Furthermore, siRNAs can be applied for targeting genes contributing to the carcinogenesis, proliferation, and metastasis of tumor cells or their resistance to standard chemotherapies and radiation [138]. Therefore, it has been considered a modern method for cancer therapy. On the other hand, the nanoparticles used to deliver siRNA must possess properties such as biodegradability, great bio-distribution, low toxicity, etc. All of these features can be offered by liposomes making this popular drug delivery system a promising candidate for this purpose [28]. siRNAs bound to neutral lipid-based NPs are well isolated from these liposomes. They also influence ephrin type-A receptor 2 (EphA2), focal adhesion kinase (FAK), neuropilin-2, Interleukin 8 (IL-8), and TROJAN Mobile Remote Receiving System/erythroblast transformation-specific (TMRRS/ERG), Elongation factor 2 kinase (EF2K) or Bcl-2 pathways. Following the occurrence of this mechanism, a suitable antitumor effect has been observed against ovarian, colon, and breast cancer cells, etc. [139, 140]. Numerous studies have been conducted on siRNA delivery by liposomes, and in most of them, the cationic lipid Dioleoyl-3-trimethylammonium propane (DOTAP) has been widely expended in the structure of liposomes. Due to DOTAP high positive charge, this cationic lipid can be toxic to cells. It can stimulate cellular hemolysis and reduce ultimate biocompatibility as well. This has challenged the application of this lipid in the composition of liposomes applied for siRNA delivery [141].
Liposomal Curcumin Nanoparticles
Curcumin-conjugated liposomes are another instance of liposomal nanoparticle usage. Curcumin is a natural polyphenolic and hydrophilic compound that is abundant in the Curcuma longa plant and can be mainly prepared from turmeric extraction. Nowadays, the anticancer effect of curcumin has been well indicated against many tumor cells, such as breast cancer, liver carcinoma, and prostate cancer, etc. [142]. The primary mechanism of action of curcumin against cancer cells is to interfere with the translation of proteins such as Bcl-xl and regulate apoptosis by influencing their process, controlling the release of reactive oxygen species (ROS) and cytochrome, regulating molecular factors such as cyclin affecting the cell cycle. On the other hand, curcumin can damage the nuclear and mitochondrial DNA structure of liver cancer cells, thereby disrupting their function [143]. In comparison with free curcumin, the application of liposomal curcumin improves pharmacokinetics and pharmacodynamics while reducing the dosage required to target tumors. Matheus Andrade Chave et al. explored curcumin-containing liposomes by inserting curcumin molecules into the MLV liposome [144]. The synthesis of liposomal curcumin and curcumin structure are described in Fig. 10.
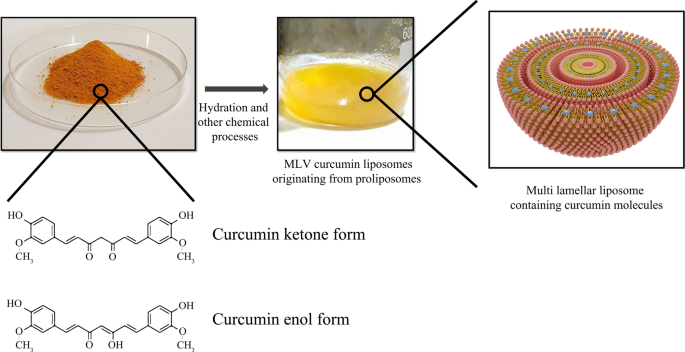
An overview of curcumin powder and liposomal curcumin synthesis. Chemical reactions performed for liposomal curcumin production and curcumin molecule structure in various forms are simply demonstrated
In addition, liposomes prepared for therapeutic research applications can be synthesized by employing various methods. For example, Qiao Wang et al. exploited the ultrasonication and lipid film-hydration method to synthesize daidzein long-circulating liposomes (DLCL) [145]. Xiaoyuan Ding et al. also used the film hydration method for the synthesis of aptamer and Au-NPs (Apt-Au)-modified Morin pH-sensitive liposome. Their outcomes showed high biocompatibility and insignificant toxicity of these liposomal structures and highlighted these liposomes as a viable option for selective targeting of tumors [146].
Other Liposomal NPs in the Investigational Phase
Several liposomal drugs have been synthesized and utilized in various medications at the investigational phase. For instance, CPX-1 was produced by entrapping the antitumor agents, Irinotecan and floxuridine (1:1 molar ratio) in liposomes, and was designed to treat advanced colorectal cancer. This therapeutic nanoparticle is in phase II research status [128]. Lipovaxin-MM is another momentous liposomal nanoparticle in phase I research prepared by placing melanoma antigens in liposomes and mainly administrated for immunotherapy of malignant melanoma. This agent is also under investigation [128].
Conclusion
As spherical structures in liquids, liposomes can be applied as a promising option for cancer therapy and drug delivery, as well as imaging, and disease management. By reviewing liposomes pros and cons, scientists will be able to improve them in future research works.
Some opportunities and challenges in liposomes utilization are described in the following. One of the convenient features of liposomes is their morphological similarity to cells (presence of phospholipids), as well as increasing the effectiveness of the drugs. As a negative point, liposomal phospholipids may sometimes undergo hydrolysis or oxidation reactions which may be problematic. Other pros of liposomes include increased stability of the encapsulated drug in it, reduced contact of sensitive tissues with therapeutic molecules, decreased drug toxicity, improved pharmacokinetic and pharmacodynamics properties, the ability to regulate the rate of drug release, and the potential of their structure to accept the desired chemical modification. In contrast to these opportunities, there are some challenges such as leakage or unintended entrapment of drugs, low liposome bioactivity, decreased-solubility, rapid clearance of conventional liposomes from the blood by the reticuloendothelial system (RES), and problems caused by continuous intravenous administration or local injection.
Besides examining the advantages and disadvantages of liposomes, we should take their proper targeting mechanism of action into account. Passive targeting is considered a beneficial mechanism due to the abundant clinical evidence and experience. It also increases the circulation time of liposomal drugs. The problem of this mechanism lies in its non-specific drug delivery and its physiological barriers. In contrast, beneficial features of active targeting include increased specificity in drug delivery, the possibility of overcoming chemotherapy-resistant tumor cells, and reduced off-target effects. However, the difficulty in identifying accurate binding sites on cancer cells and the lack of adequate evidence of its former utilization have led to some ups and downs in its application.
Liposomes are reasonable candidates for elevating the effectiveness of current anticancer agents and preventing the incidence of drug resistance. Future research in this area should be focused on further investigation into the properties of liposomal structures. To probe about drug entrapment in therapeutic nanoparticles, including liposomes, much more detailed examinations will be required.
Abreviações
- WHO:
-
World Health Organization
- VNPs:
-
Viral nanoparticles
- NPs:
-
Nanopartículas
- US FDA:
-
United States Food and Drug Administration
- DDSs:
-
Drug delivery systems
- PC:
-
Fosfatidilcolina
- SM:
-
Sphingomyelin
- PS:
-
Phosphatidylserine
- PE:
-
Phosphatidylethanolamine
- ULVs:
-
Unilamellar vesicles
- OLVs:
-
Oligo lamellar vesicles
- MLVs:
-
Multilamellar vesicles
- SUVs:
-
Small unilamellar vesicles
- RBF:
-
Round-bottom flask
- LNs:
-
Liposomal nanoparticles
- MPS:
-
Mononuclear phagocytosis system
- PEG:
-
Polietileno glicol
- PEOZ:
-
Poly [2-ethyl 2-oxazoline]
- PETOXylated:
-
Poly [2-ethyl-2-oxazolylated
- PMOZ:
-
Poly [2-methyloxazoline]
- HDL:
-
High-density lipoprotein
- LDL:
-
Low-density lipoprotein
- SCLC:
-
Small cell lung cancer
- GRPR:
-
Gastrin-releasing peptide receptor
- Anti-EpCAM:
-
Anti-epithelial cell adhesion molecule
- IUPAC:
-
International Union of Pure and Applied Chemistry
- I.V.:
-
Intravenous
- S.C.:
-
Subcutaneous
- I.D.:
-
Intradermal
- I.P.:
-
Intraperitoneal
- I.M.:
-
Intramuscular
- EPR:
-
Permeabilidade e retenção aprimoradas
- fR:
-
Folate receptor
- TfR:
-
Transferrin receptor
- EGFR:
-
Epidermal growth factor receptor
- VEGF:
-
Vascular endothelial growth factor
- VCAM:
-
Vascular cell adhesion protein
- APC:
-
Células apresentadoras de antígeno
- ABCB1:
-
ATP-binding cassette transporter superfamily B member 1
- HSPC:
-
Hydro soy phosphatidylcholine
- DSPG:
-
1,2-Distearoyl-sn-glycero-3-PG
- DOPC:
-
Dioleoylphosphatidylcholine
- DPPG:
-
1,2-Dipalmitoyl-sn-glycero-3-phosphoglycerol
- DSPC:
-
1,2-Distearoyl-sn-glycero-3-phosphocholine
- AML:
-
Acute myeloid leukemia
- ALL:
-
Acute lymphocytic leukemia
- DSPE:
-
1,2-Distearoyl-sn-glycero-3-phosphoethanolamine
- DOPE:
-
Dioleoylphosphatidylethanolamine;
- EPG:
-
Esterified propoxylated glycerols;
- DMPC:
-
1,2-Dimyristoyl-sn-glycero-3-phosphocholine
- DOPS:
-
1,2-Dioleoyl-sn-glycero-3-phospho-L-serine
- POPC:
-
1-Palmitoyl-2-oleoyl-sn-glycero-3-phosphocholine
- DMPG:
-
1,2-Dimyristoyl-sn-glycero-3-phosphoglycerol
- MPEG:
-
Methoxypolyethylene glycols.
- CNS:
-
Central nervous system
- BBB:
-
Blood–brain barrier
- siRNA:
-
Small-interfering RNA
- EphA2:
-
Ephrin type-A receptor 2
- FAK:
-
Focal adhesion kinase
- IL-8:
-
Interleukin-8
- TMRRS/ERG:
-
TMRRS/ERG TROJAN Mobile Remote Receiving System/erythroblast transformation-specific
- EF2K:
-
Elongation factor 2 kinase
- DOTAP:
-
Dioleoyl-3-trimethylammonium propane
- ROS:
-
Espécies que reagem ao oxigênio
- DLDC:
-
Daidzein long-circulating liposomes
- RES:
-
Reticuloendothelial system
Nanomateriais
- Seleção correta da bomba Vital para aplicações de tratamento de sementes
- Nanofibras e filamentos para entrega aprimorada de drogas
- Nanopartículas para terapia do câncer:progresso e desafios atuais
- Estruturas Metálicas-Orgânicas de Meio Ambiente como Sistema de Administração de Medicamentos para Terapia de Tumor
- Administração de medicamentos baseados em células para solicitações de câncer
- Peixe-zebra:um sistema de modelo em tempo real promissor para a entrega de medicamentos neuroespecíficos mediada por nanotecnologia
- Nanopartículas lipídicas de PLGA rastreadas com 131I como transportadores de administração de drogas para o tratamento quimioterápico direcionado do melanoma
- Tratamento UV de filmes de malha nanowire de cobre flexível para aplicações de condutor transparente
- Nanocarriers à base de nucleosídeo-lipídio para entrega de sorafenibe
- Micro-robôs impressos em 3D prometem entrega de medicamentos



