Estudo in vitro da influência das nanopartículas de Au nas linhas celulares HT29 e SPEV
Resumo
Modelos de cultura de células são ferramentas excelentes para potencial toxicidade de nanopartículas e investigações fundamentais na pesquisa do câncer. Assim, as informações sobre a toxicidade potencial do AuNP e os efeitos na saúde humana são necessárias para o uso de nanomateriais em ambientes clínicos. O objetivo de nossa pesquisa é examinar os efeitos dos AuNPs nas linhas celulares de origem epitelial:contínuas e oncogênicas. Foram utilizadas linha celular epitelial de rim porcino embrionário (SPEV) e linha celular de carcinoma colorretal (HT29). Nas culturas de teste, a proliferação celular, necrose / apoptose e geração de esferóides multicelulares foram avaliados. Demonstramos que as concentrações de AuNP de 6-12 μg / ml reduziram a proliferação de células SPEV e HT29 e aumentaram o número de células nos estágios iniciais e finais de apoptose e necrose. Foi demonstrado que pequenas concentrações de AuNPs (1-3 μg / ml) estimulam a formação de esferóides multicelulares por células HT29 e SPEV. No entanto, concentrações mais altas de AuNP (6–12 μg / ml) tiveram efeitos citotóxicos e anti-coesivos na célula em suspensão. A grande sensibilidade à ação dos AuNPs foi demonstrada pela linha de HT29 (6 μg / ml) em comparação às células SPEV (12 μg / ml). Este estudo experimental do efeito de AuNPs em linhas de células SPEV e HT29 justificará sua aplicação adicional no tratamento anticâncer mediado por AuNP.
Histórico
A produção e investigação das nanopartículas de ouro (AuNPs) não têm apenas alto potencial para ampla aplicação terapêutica de ouro [1, 2], mas também os tornam adequados para aplicações biomédicas específicas, como terapias alvo [3, 4]. Relatórios recentes demonstraram que o uso de AuNPs oferece uma oportunidade para novas terapias antitumorais com um risco reduzido de desenvolvimento de resistência. Assim, vários estudos comprovaram a atividade antitumoral de nanopartículas contra câncer de mama, fígado, estômago, cólon e pulmão [5, 6].
Sabe-se que as nanopartículas (NPs) podem modular o destino celular, induzir ou prevenir mutações, iniciar a comunicação célula-célula e modular a estrutura celular [7, 8]. Além disso, AuNPs têm vantagens sobre outros NPs de metal devido à sua biocompatibilidade e atividade antitumoral [8,9,10,11,12]. Os efeitos citotóxicos e genotóxicos dos AuNPs estão associados à sua forma, tamanho, carga, concentração, tempo de interação, etc. [12,13,14]. Assim, informações sobre sua toxicidade potencial e efeitos na saúde humana são necessárias para o uso de nanomateriais em ambientes clínicos.
Atualmente, apesar do grande sucesso na terapia direcionada, o problema da entrega seletiva de AuNPs no tecido-alvo permanece sem solução. Alguns estudos observaram diferentes taxas de captação de NPs por células epiteliais de origem diferente [15, 16]. No entanto, faltam investigações para explicar esse fenômeno, embora possam ajudar a atingir o direcionamento seletivo de tecido de AuNPs. As diferenças anatômicas ou fisiológicas entre os diferentes epitélios podem explicar as diferenças nas taxas de captação e transporte de AuNPs. Em particular, a taxa de absorção pode ser influenciada pelas propriedades da membrana plasmática das células e pela ligação das nanopartículas às glicoproteínas e proteoglicanos da superfície celular, bem como pela capacidade das células para o transporte vesicular [17]. Assim, levando em consideração a impossibilidade de interação exclusivamente seletiva de nanopartículas com células-alvo, o estudo comparativo das características de sua interação com células normais e oncogênicas a fim de evitar consequências indesejáveis da terapia do câncer é tópico [8,9,10].
Embora os modelos in vivo sejam valiosos para avaliar a toxicidade biológica de nanopartículas, os modelos de cultura de células são altamente úteis para estudos pré-clínicos fisiológicos e toxicológicos. Atualmente, as culturas de células são amplamente utilizadas em vários campos da biologia, medicina, medicina veterinária e biotecnologia. O uso de culturas de células permite explorar processos biológicos que são difíceis e às vezes impossíveis de estudar ao nível dos organismos. Um papel importante das culturas de células é desempenhado na biotecnologia na produção de muitas vacinas, sistemas de teste e substâncias biologicamente ativas. As culturas de células são utilizadas para diagnosticar doenças de várias etiologias, como objetos de teste ao testar novos agentes farmacológicos, terapêuticos e cosméticos, bem como aditivos alimentares [18].
Neste trabalho em modelos de cultura de células, tentamos examinar as características dos efeitos dos AuNPs das células epiteliais de origem de linha celular contínua e oncogênica. A cultura em monocamada de células epiteliais SPEV (linha inoculada epitelial de rim porcino embrionário) e células HT-29 (linha celular de carcinoma do cólon) podem ser consideradas como um modelo de tecidos epiteliais normais e cancerosos quando a terapia antitumoral com AuNPs é aplicada. Vários ensaios tradicionais de citotoxicidade, incluindo adesão, proliferação, necrose / apoptose e esferóides multicelulares, foram empregados para validar a citotoxicidade celular de AuNPs.
Métodos
Cultura de células SPEV
As células SPEV foram cultivadas em frascos de plástico em DMEM (Sigma, EUA) com 5% de FCS ( v / v ) (HyClone, EUA) suplementado com penicilina / estreptomicina (PAA, Áustria) e anfotericina B (5 μg / ml) (5% CO 2 , 95% de umidade) conforme relatado por [19]. A concentração de semeadura era 0,5–2 × 10 4 células / cm 2 . O meio de cultura foi substituído a cada 2 dias. As células foram passadas em 100% de confluência [20]. A linha de células SPEV cresceu e preservou a estrutura morfológica inicial da monocamada durante as passagens em série sem evidência de degeneração celular em cultura.
Cultura de células HT29
As células HT29 foram cultivadas em frascos de plástico (Nunc, Dinamarca) em meio RPMI-1640 (Sigma, EUA) com 10% de FCS ( v / v ) (HyClone, EUA) suplementado com 2 mM de L-glutamina (Sigma, EUA) e 40 mg / ml de gentamicina (Sigma, EUA) sob condições padrão (5% CO 2 , 95% de umidade) [21]. A densidade celular ideal era 0,5–4,0 × 10 4 células / cm 2 . As células foram gentilmente cedidas a nós pelo Banco de Linhas de Células de Tecido Humano e Animal do Instituto RE Kavetsky de Patologia Experimental, Oncologia e Radiobiologia NAS da Ucrânia.
Manipulações com AuNPs
AuNPs foram gentilmente cedidos pelo Instituto de Bioquímica e Fisiologia de Plantas e Microorganismos da Academia Russa de Ciências. AuNPs foram sintetizados pelo método do citrato [22]. O tamanho médio das nanopartículas foi de 15 nm. A concentração inicial de ouro foi de 57 μg / ml. Os resultados da microscopia eletrônica de campo escuro, imagem de AuNPs de 15 nm e espectros de extinção de AuNPs de 15 nm (b) são mostrados na Fig. 1 (Fig. 1a; observe o diagrama da distribuição de tamanho) [23]. AuNPs foram introduzidos nas células por difusão passiva a 37 ° C. As concentrações investigadas foram 1, 3, 6 e 12 μg / ml. As células sem AuNPs nas mesmas condições foram consideradas como controle.
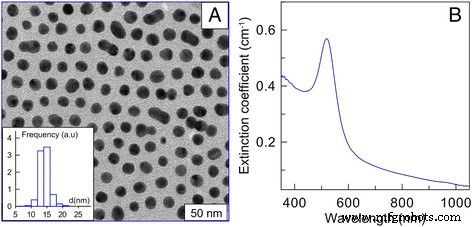
Resultados de microscopia eletrônica de campo escuro, a imagem de AuNPs de 15 nm (nota –– diagrama da distribuição de tamanho), b espectros de extinção de AuNPs de 15 nm
Células de adesão e proliferação
O estado morfofuncional das culturas de células foi avaliado pelas propriedades adesivas e atividade proliferativa. As propriedades adesivas das células SPEV e HT29 foram avaliadas visualmente usando um microscópio invertido; o número de células aderidas e achatadas foi contado 30, 60, 120, 180 e 1440 min após o início da cultura.
A dinâmica de proliferação de células SPEV e HT29 foi estudada por 1-4 dias. Para examinar o incremento do número de células nas culturas estudadas aos termos de investigação, estas foram enzimaticamente (1:1 (solução de tripsina 0,25%:EDTA, PAA)) destacadas do plástico e o número de células foi contado. O número total de células cultivadas foi contado pelo método tradicional na câmara de Goryaev.
Processos apoptóticos / necróticos
Os processos apoptóticos e necróticos em células SPEV e HT29 expostas a AuNPs foram investigados em 4 dias com Anexina-V (BD, EUA), corantes 7-Amino-Actinomicina (7AAD) (BD) usando um FACS Calibur Becton-Dickinson. Os resultados foram analisados com o software WinMDI v.2.8.
Esferóides multicelulares
Os esferóides multicelulares (MSs) foram gerados para estimar o impacto in vitro de AuNPs no potencial de migração e agregação das células investigadas. O sistema modelo esferóide (3-D) de células SPEV e HT29 foi cultivado pelo método convencional, que foi relatado por [24] e modificado em nosso laboratório [25]. Resumidamente, a suspensão de células foi contada usando azul de tripano e um número igual de células (5 × 10 4 células / cm 2 ) foram plantados em meio de cultura totalmente suplementado. A geração de MS foi alcançada manipulando cultura de células com 0,24% de carboximetilcelulose (CMC) em placas de 24 poços revestidas com 1% de ágar com rotação (80 rpm) por 24 h. Depois disso, a cultura de células 3-D foi mantida em condições padrão. Para investigar a dependência do tamanho e do número de MSs na concentração de AuNP, os MSs foram gerados na presença de AuNPs. O cultivo posterior foi conduzido por 48 h com rotação constante das placas. No estágio seguinte, imagens de micro foto foram feitas pelo método de campo escuro com um microscópio Carl Zeiss Stemi 2000. A morfologia da MS foi estudada com a ajuda do programa Axio Vision Release 4.7 (Zeiss). Este programa permite medir as dimensões geométricas de agregados celulares. Em seguida, calculou-se o volume de todos os EMs que estavam nos arquivos. Foi usado com a seguinte fórmula: V =0,4 × a × b 2 , onde a e b –– diâmetros geométricos de MSs [24]. Para análise estatística, todos os agregados de células foram agrupados por tamanho de 1 × 10 −4 mm 3 para 1 × 10 −2 mm 3 com incremento de 1 × 10 −3 mm 3 . O número de MS e a mediana dos volumes de MS foram estimados para cada grupo.
Análise estatística
Uma análise de variância de fator único e t de Student foram utilizados testes para processamento estatístico dos dados com o pacote de software Statistica 8. O limite de significância foi de 0,05. Os resultados são apresentados como médias e erros padrão (M ± SE).
Resultados
Efeito de AuNPs na adesão de células SPEV e HT-29
A adesão celular é um indicador do estado funcional das células e é necessária para o crescimento posterior da cultura. Quando a adesão terminou, as células tornaram-se achatadas e ganharam morfologia apropriada. As propriedades adesivas das células SPEV são apresentadas na Fig. 2.
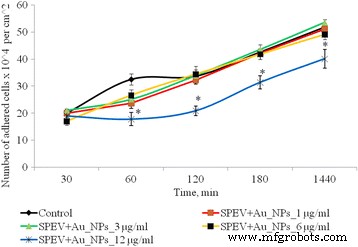
Dinâmica de adesão de células SPEV após exposição de AuNPs, * p ≤ 0,05 é significativo em comparação com o controle
Após 1 h de cultivo de células SPEV com AuNPs a 1, 3 e 6 μg / ml, o número de células aderidas foi menor em relação ao valor de controle. A porcentagem de células achatadas em amostras com AuNPs para essas concentrações não diferiu significativamente do controle. A adesão foi retardada após 1 h de incubação com AuNPs a 12 μg / ml. O número de células aderidas por centímetro quadrado foi reduzido em 1,8 vezes em relação ao controle. Esta tendência de adesão persistiu por todos os períodos de teste. Após 24 horas de observação, o número de células aderidas foi menor em relação ao controle em 1,3 vezes. Ao mesmo tempo, a incubação de AuNPs em pequenas concentrações (1 e 3 μg / ml com células tumorais (HT29) não teve efeito significativo na quantidade de células adesivas. O aumento da concentração de AuNP para 6 e 12 μg / ml levou à diminuição do número de células tumorais na fração adesiva em 1,16 e 1,28 vezes, respectivamente, (Fig. 3). Os dados obtidos podem ser influenciados por diversos processos. Um deles é o efeito citostático / citotóxico dos AuNPs na fração de adesão do tumor e linhas de células embrionárias, o que leva à morte celular, transição para apoptose ou necrose. O outro processo é a redução da adesão celular, sob a influência de AuNPs e transferência de células para a fração de suspensão. Notavelmente, ambos os processos podem ser realizados simultaneamente. e cada um pode contribuir para a diminuição do número de células vivas na fração de adesão.
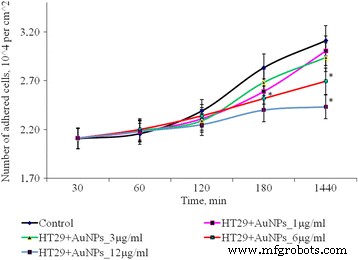
Dinâmica de adesão de células HT29 após exposição de AuNPs, * p ≤ 0,05 é significativo em comparação com o controle
Efeito de AuNPs na proliferação de células SPEV e HT-29
O efeito de AuNPs dentro do intervalo de concentração de 1–12 μg / ml em processos proliferativos em cultura de células SPEV foi estudado (Fig. 4). Nos dias 2–4 de cultivo com AuNPs a 1, 3 e 6 μg / ml, o número de células não diferiu significativamente do controle. No dia 4 de cultivo com AuNPs a 3 e 6 μg / ml, esse índice diminuiu 1,15 e 1,23 vezes, respectivamente, em comparação com o controle. A redução no número de células em 1,5 vezes (dias 2 e 3) e 1,15 vezes no dia 4 de cultura com AuNPs a 12 μg / ml foi observada na cultura SPEV versus o controle. Assim, a concentração de AuNP, 12 μg / ml, desacelerou o crescimento celular dentro do período de tempo observado.
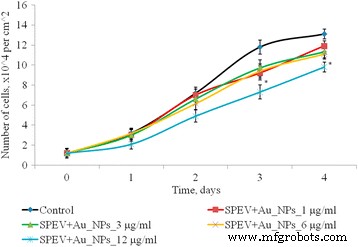
Proliferação de células SPEV após exposição de AuNPs, * p ≤ 0,05 é significativo em comparação com o controle
O efeito de AuNPs em concentrações de 1 a 12 μg / ml sobre o número de células HT 29 em uma cultura em monocamada é mostrado na Fig. 5. Durante os primeiros 3 dias de incubação, o número de células no controle e na presença de AuNPs não foi estatisticamente diferente. No 4º dia de cultivo, notou-se diminuição dose-dependente do número de células na cultura 2D. Assim, após 4 dias de cultivo, para baixas concentrações de AuNPs (1 e 3 μg / ml), o número de células HT 29 não é significativamente diferente em comparação com o controle. Mas em concentrações mais altas de AuNP (6-12 μg / ml), o número de células HT29 foi menor do que o controle em 1,33 e 1,44 vezes, respectivamente.
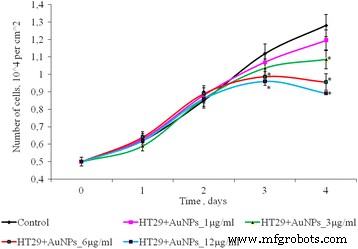
Proliferação de células HT29 após exposição de AuNPs, * p ≤ 0,05 é significativo em comparação com o controle
Efeito de AuNPs em processos apoptóticos / necróticos em células SPEV e HT-29
As células SPEV e HT-29 na presença de AuNPs foram cultivadas durante 4 dias nas condições padrão. O cultivo de células SPEV e HT29 com AuNPs a 1 e 3 μg / ml e os índices de processos apoptóticos / necróticos não diferiram significativamente do controle (Tabelas 1 e 2).
A cultura com AuNPs a 6–12 μg / ml aumentou a porcentagem de células de anexina V + / 7AAD +, anexina V- / 7AAD + e anexina V + / 7AAD, bem como reduziu a porcentagem de células vivas. O número de Annexin V + / 7AAD + As células SPEV foram maiores do que o valor de controle em 7,8 ± 0,7% ( p ≤ 0,05) com 12 μg / ml de AuNPs. O número de Annexin V + / 7AAD + As células HT 29 foram maiores do que o valor de controle em 3,2 ± 0,4% ( p ≤ 0,05) com 6 μg / ml de AuNPs e 4,8 ± 0,6% ( p ≤ 0,05) com 12 μg / ml de AuNPs.
Efeito de AuNPs na geração de esferóides multicelulares de células SPEV e HT29
Para determinar a dependência do tamanho e número de esferóides multicelulares (MSs) na concentração de AuNP, MSs foram gerados em várias concentrações de AuNPs durante 48 h. Nossos dados demonstraram a capacidade de variedade das células HT29 e SPEV para formar esferóides multicelulares sob as mesmas condições do microambiente (Figs. 6 e 7).
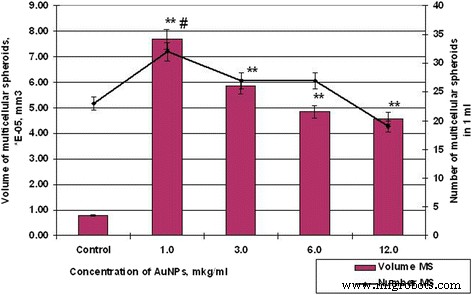
Número e volume de células MS SPEV após incubação com AuNPs, # p ≤ 0,01 (para número de MSs); ** p ≤ 0,01 (para o volume de MSs)
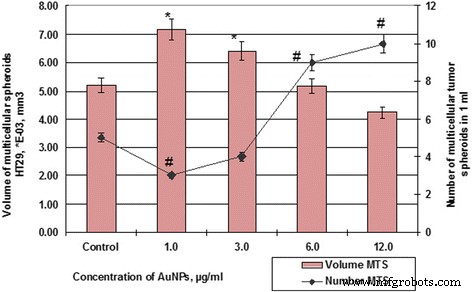
Número e volume de células MS HT29 após incubação com AuNPs. # p ≤ 0,01 (para número de MSs); ** p ≤ 0,01 (para o volume de MSs)
Portanto, se as amostras de controle de células HT29 por 48 h formaram esferóides com volume médio de 5,19 × 10 −3 mm 3 , o esferóide de volume médio de células SPEV foi 0,79 × 10 −5 mm 3 . Ao mesmo tempo, a influência de AuNPs nas células HT29 e SPEV teve a mesma tendência. A presença de AuNPs no microambiente celular estimulou a formação de esferóides multicelulares em ambas as culturas. Assim, quando a concentração de AuNPs foi de 1 e 3 μg / ml de volume de MSs para SPEV aumentou 9,7 e 7,4 vezes, respectivamente, em comparação com o controle (Fig. 6), as mesmas concentrações de AuNP também estimularam um volume crescente de MSs para HT29 por 1,4 e 1,2 vezes, respectivamente (Fig. 7).
O aumento adicional da concentração de AuNP levou à diminuição do volume médio de MSs em ambas as culturas. A elevação na concentração de AuNP de 1 para 12 μg / ml diminuiu o volume de HT29 MSs de 7,18 × 10 −3 mm 3 para 4,24 × 10 −3 , em 1,69 vezes, segundo o controle. Quanto ao SPEV, quando a concentração de AuNPs foi aumentada de 1 para 12 μg / ml, o volume de MSs diminuiu de 7,69 para 4,58 × 10 −5 mm 3 , em 1,68 vezes, conforme controle. No entanto, o aumento da concentração de AuNP coincide com a redução no volume de MSs e está correlacionado com o aumento no número de esferóides em cultura de células HT29 (Figs. 6 e 7). O número de HT29 MSs aumentou de 3 para 10 por campo de visão na concentração de AuNP de 1 para 12 μg / ml. Ao mesmo tempo, o número de MSs SPEV diminuiu de 32 para 19, respectivamente.
Os dados obtidos (Figs. 6 e 7) demonstram que AuNPs são capazes de influenciar interações coesas no sistema célula a célula. Nossos dados mostram que pequenas concentrações de AuNPs (1-3 μg / ml) estimularam a formação de esferóides multicelulares de células embrionárias e tumorais. No entanto, concentrações mais altas de AuNP (6–12 μg / ml) tiveram efeitos citotóxicos e anti-coesivos na célula em suspensão. Este processo contribuiu para a formação de um maior número de HT29 MSs com a diminuição do volume médio. Quanto ao SPEV, a alta concentração de AuNPs pode ter um efeito citostático que reduz o número de células na fração adesiva e o número de MSs em suspensão. Anteriormente, os autores relataram que as nanopartículas de carbono reduzem a adesão das células ao substrato, estimulam a transferência das células para a suspensão e levam à formação de esferóides multicelulares [25, 26]. Na literatura, existem dados sobre a capacidade do AuNP de quebrar a estrutura dos microfilamentos de actina / miosina e diminuir a proliferação, adesão e diferenciação celular [27]. Nossos dados confirmaram essa suposição.
Discussão
Avaliamos os efeitos dos AuNPs na proliferação, necrose / apoptose e formação de esferóides multicelulares de origem contínua e oncogênica de células epiteliais. Foi demonstrado que os AuNPs a 6–12 μg / ml reduziram o número de células SPEV e HT29 e aumentaram o número de células nos estágios iniciais e finais de apoptose e necrose. As pequenas concentrações de AuNPs estimulam a formação de esferóides multicelulares pelas células HT29 e SPEV. No entanto, concentrações mais altas de AuNP tiveram efeitos citotóxicos e anti-coesivos nas células em suspensão. A grande sensibilidade à ação de AuNPs foi demonstrada pela linha de HT29 (6 μg / ml) em comparação com as células SPEV (12 μg / ml).
Os efeitos dos AuNPs na morfologia celular e no citoesqueleto só recentemente receberam mais atenção, e o mecanismo subjacente e as consequências futuras não foram investigados em profundidade [28,29,30]. A este respeito, é importante para todos os novos tipos de AuNP avaliar sua via de captação endocítica e localização intracelular em função do tempo. Para diferentes tipos de AuNPs, os efeitos foram descritos como dependentes da concentração intracelular de AuNP e como transitórios, onde após divisões celulares recorrentes, as concentrações de AuNP intracelulares diminuem exponencialmente e os efeitos não são mais observados. Além disso, a possível fuga endossômica dos AuNPs deve ser avaliada. Como os defeitos do citoesqueleto foram descritos como claramente dependentes das concentrações de AuNP, uma ampla faixa de concentração de partículas deve ser testada para tentar avaliar a capacidade máxima de carregamento celular sem quaisquer efeitos. Além disso, como o citoesqueleto também está envolvido em muitas vias de sinalização intracelular, ainda precisa ser investigado se a ruptura do citoesqueleto induzida por AuNPs leva a efeitos secundários [31].
Como os NPs têm certas dimensões físicas, o volume intracelular que ocupam pode levar a alterações na morfologia celular ou afetar a estrutura da rede do citoesqueleto celular [28, 29, 31]. Os efeitos posteriores também podem ser devido às altas demandas da postura de NP sobre a maneira endocítica celular. Foi descrito que AuNPs têm um efeito profundo na morfologia de vários tipos de células, como células de pulmão de carcinoma humano A549 [32]. AuNPs também foram descritos como tendo um efeito dependente da concentração nas fibrilas de actina de fibroblastos dérmicos humanos [33, 34]. Mironava et al. [35, 36] mostraram ainda que os filamentos do citoesqueleto são interrompidos em função do tempo de exposição de AuNP, concentração e tamanho dos NPs, embora os níveis de expressão da proteína de actina ou β-tubulina não tenham sido afetados.
O tipo de célula usado também é de grande importância, pois diferentes tipos de células, mesmo quando intimamente relacionados, podem reagir de maneira bastante diferente para o mesmo tipo de nanomateriais [37, 38]. De preferência, os tipos de células que estão mais envolvidos nas (futuras) aplicações biomédicas dos NPs devem ser testados (por exemplo, células epiteliais, endoteliais) ou células múltiplas que são derivadas das diferentes camadas germinativas. Ao investigar os efeitos citotóxicos, o uso de tipos de células cancerígenas deve ser minimizado, pois podem levar a resultados aberrantes [39]. As células cancerosas têm várias características específicas e vias de sinalização intracelular alteradas que são destinadas a aumentar a proliferação e manter a viabilidade celular, o que as tornará menos propensas a alguns efeitos citotóxicos mediados por NP.
Em nossa opinião, a ligação de AuNPs a grupos funcionais de superfície (por exemplo, proteínas transmembrana) de células pode ser reversível ou irreversível, resultando em lesões estruturais temporárias ou permanentes [40, 41]. Implicações potenciais de mudanças nas propriedades biomecânicas (por exemplo, dureza e elasticidade), adesividade e propriedades elétricas de superfície das células são perceptíveis. Assim, as mudanças na dureza ou elasticidade podem influenciar a flexibilidade estrutural da superfície, a produção de energia mecânica para a divisão celular e a motilidade celular. Quanto à adesividade, o microambiente celular é normalmente composto de matriz extracelular com moléculas específicas que permitem que as células adiram ao seu entorno [42]. A carga superficial, sem dúvida, desempenha um papel importante nas interações entre as células e seus arredores.
Os outros autores também relataram que os NPs estão preferencialmente localizados nas mitocôndrias e causam estresse oxidativo, bem como potencializam danos estruturais [40]. Um artigo recente de Pan et al. descreve que AuNPs de 1,4 nm induzem necrose via estresse oxidativo e dano mitocondrial em células Hela [43]. O acúmulo de nanopartículas no meio celular após a biodegradação não é seguro porque pode romper organelas e até mesmo causar mutações genéticas.
As alterações que ocorrem nas células durante a apoptose são semelhantes para a maioria dos tipos de células. Em células apoptóticas, há mudanças na composição lipídica da membrana plasmática:transferências de fosfatidilserina da parte citoplasmática da bicamada para o lado externo, causando ativação da cascata de caspases, condensação da cromatina e distúrbio da cadeia de transporte de elétrons na mitocôndria e, eventualmente, interrompendo a síntese de ATP. A morte celular programada pode ser desencadeada por estímulos fisiológicos mediados por receptores resultantes de distúrbios genéticos, exposição a fatores químicos ou físicos, bem como por outras alterações nas células. Observamos que esse efeito ocorre com 6–12 μg / ml de AuNPs.
Agregados multicelulares (esferóides, corpo embrióide) representam um nível intermitente entre células em crescimento em monocamada e cultura de tecidos. Os esferóides são modelos objetivos do crescimento e organização tridimensional celular, das interações célula a célula e da influência das condições microambientais, por exemplo, concentração de AuNP, na intensidade de proliferação, bem como na adesividade celular e formação de microagregados. A formação de MS é um método de cultura bem estabelecido tanto para tumor quanto para linhagens de células embrionárias [24, 44, 45]. Em nosso trabalho, a formação e o crescimento de esferóides são alcançados pela adição de CMC como parte da matriz extracelular artificial e revestimento de superfície com 1% de ágar que inibiu a adesão celular à superfície e estimulou a agregação celular. Nessas condições, a cultura de MS pode ser realizada até os agregados formarem necrose central, devido ao crescimento limitado da massa celular ou diferenciação espontânea das células embrionárias.
Na literatura, há informações sobre a interação AuNPs com linhagem de células de câncer de cólon e linhas de células embrionárias [46, 47]. De acordo com esses dados, a exposição até mesmo a concentrações muito baixas de AuNPs pode ter um efeito prejudicial sobre as células precursoras neurais embrionárias humanas e HT29 por enfatizar a proliferação celular, diferenciação e morte celular por apoptose.
Existem dados publicados que o efeito de AuNPs é baseado na acumulação da fase G0 / G1, depleção da fase S e G2 / M, bem como nos níveis reduzidos de ATP em células de carcinoma escamoso oral humano (HSC-3) [48]. A regulação do ciclo celular pode ser abordada pela violação de contatos focais de células com substrato e transferência de células para a fração suspensa em cultura 2D e contatos de inibição célula a célula na junção de lacuna em cultura 3D [48,49,50]. Devido ao tamanho nanométrico de AuNPs (próximo a 15 nm), ele não pode ser centros de coesão para as células. Ao mesmo tempo, a intercalação de AuNPs na membrana celular [51], a influência no potencial zeta de AuNP da membrana celular [32] e a influência na formação de contatos célula a célula / célula a superfície obviamente podem desencadear o mecanismo de necrose / apoptose , efeito citotóxico e interrupção do ciclo celular. A violação dos contatos focais das células com o substrato e a transferência das células para a fração suspensa é uma forma de regulação do ciclo celular [48, 49]. Pequenas concentrações de AuNPs não exerceram efeito citotóxico estatisticamente significativo nas células. No entanto, concentrações mais altas de AuNP tiveram efeitos citotóxicos e anti-coesivos nas células em suspensão. Esse processo contribuiu para a formação de um maior número de MSs com a diminuição do volume médio. Supomos que o AuNP se forma em contatos coesos de células e os compromete. Assim, nossos experimentos sobre os efeitos de AuNPs em linhas de células SPEV e HT29 apóiam sua aplicação adicional no desenvolvimento de terapias contra o câncer mediadas por AuNP.
Embora estudos futuros sejam necessários para confirmar os efeitos anticâncer nos estudos em animais in vivo. No entanto, nossa profunda convicção é que, se conhecermos a natureza da substância e sua possível influência negativa, seremos capazes de evitar os efeitos prejudiciais do AuNP e usar seu potencial biotecnológico positivo. Nossa investigação pode ser aplicada de forma bastante confiável em materiais eficazes para o contexto de tratamento anticâncer com o máximo de vantagem para a medicina.
Conclusões
Nossos resultados apóiam a noção de que AuNPs induzem citotoxicidade dependente da dose em células SPEV e HT29. Além disso, este relatório demonstra pela primeira vez que 15 nm AuNPs em concentrações de 6-12 μg / ml reduziram a proliferação de células SPEV e HT29 e aumentou o número de células nos estágios iniciais e finais de apoptose e necrose. Além disso, foi demonstrado que pequenas concentrações de AuNPs (1–3 μg / ml) estimulam a formação de esferóides multicelulares. No entanto, concentrações mais altas de AuNP tiveram efeitos citotóxicos e anti-coesivos nas células em suspensão. A grande sensibilidade à ação de AuNPs foi demonstrada pela linha de HT29 (6 μg / ml) em comparação com as células SPEV (12 μg / ml).
Nanomateriais
- Nanopartículas de ouro para sensores quimio
- Nanopartículas multifuncionais de ouro para aplicações diagnósticas e terapêuticas aprimoradas:uma revisão
- Nanopartículas para terapia do câncer:progresso e desafios atuais
- Preparação e propriedades magnéticas de nanopartículas de espinélio FeMn2O4 dopadas com cobalto
- Preparação de nanopartículas de mPEG-ICA carregadas com ICA e sua aplicação no tratamento de dano celular H9c2 induzido por LPS
- Biossegurança e capacidade antibacteriana do grafeno e do óxido de grafeno in vitro e in vivo
- Síntese e desempenho in vitro de nanopartículas de ferro-platina revestidas com polipirrole para terapia fototérmica e imagem fotoacústica
- Promoção do crescimento celular SH-SY5Y por nanopartículas de ouro modificadas com 6-mercaptopurina e um peptídeo penetrador de neurônio
- Influência da rigidez elástica e adesão da superfície no salto de nanopartículas
- Uma metodologia de duas etapas para estudar a influência da agregação / aglomeração de nanopartículas no módulo de Young de nanocompósitos poliméricos



