Biossegurança e capacidade antibacteriana do grafeno e do óxido de grafeno in vitro e in vivo
Resumo
Nos últimos anos, nanopartículas de grafeno (G) e óxido de grafeno (GO) começaram a ser aplicadas na modificação da superfície de implantes cirúrgicos. No entanto, a biossegurança e a capacidade antibacteriana de G e GO ainda não estão claras. Neste estudo, a biossegurança de G e GO in vitro foi avaliada por co-cultura com células-tronco mesenquimais da medula óssea (BMSCs) e a biossegurança in vivo foi observada por meio do implante de materiais no tecido muscular de camundongos. Os resultados de biossegurança mostraram que 10 μg / ml foi a concentração crítica de segurança para G e GO. Quando a concentração foi superior a 10 μg / ml, a citotoxicidade de G e GO mostrou-se dose-dependente.
Os resultados antibacterianos mostraram que G apresentou a capacidade antibacteriana com concentração igual e superior a 100 μg / ml; GO apresentou capacidade antibacteriana com concentração igual e superior a 50 μg / ml. O efeito antibacteriano de G e GO foi de forma dependente da dose in vitro.
A concentração de GO ou G entre 50 e 100 μg / ml pode ser a melhor faixa para manter o equilíbrio entre citotoxicidade e capacidade antibacteriana. Nosso estudo revela que o G e o GO têm potencial para uso clínico, com boa biossegurança e propriedades antibacterianas em uma determinada faixa de concentração.
Histórico
Nos últimos anos, os implantes cirúrgicos são amplamente usados para tratar fraturas ósseas e outras doenças, mas o implante precisa de boa biossegurança e propriedades antibacterianas para evitar rejeição e infecção. Na verdade, o tratamento ortopédico de defeitos ósseos infecciosos ainda é um grande problema. Sobre o aspecto das bactérias, Staphylococcus aureus é o patógeno mais comum em ortopedia e implantes ortopédicos [1]. Devido ao defeito ósseo e à infecção [2], o tratamento é difícil e os pacientes precisam de muito tempo para serem curados. Se a ferida não cicatrizar, o último tratamento é a amputação do membro [3, 4].
O bom tratamento do defeito ósseo infeccioso deve satisfazer simultaneamente o controle da infecção e a reconstrução da solicitação de reparo do defeito ósseo. Com o desenvolvimento da engenharia de tecido ósseo, um número crescente de aplicações de biomateriais são utilizadas na área de tratamento ortopédico. A taxa de cura de infecções nos ossos pode, portanto, ser bastante melhorada. Esses materiais incluem principalmente osso heterogêneo [5], biocerâmica [6] (como hidroxiapatita [7] e fosfato de cálcio [8]), polímeros [9, 10], materiais proteicos (como fibras de colágeno [11]), e assim por diante. Ao lado desses materiais, Beatriz Pelaz et al. revelou a importância e a perspectiva promissora da nanotecnologia em implantes [12]; entre essas nanopartículas, o grafeno e seus derivados são outros materiais inéditos para atender aos requisitos de reparo ósseo.
O grafeno é bidimensional, com uma ou algumas camadas de átomos de carbono em uma estrutura em favo de mel [13,14,15]. É amplamente utilizado em materiais compósitos [16, 17], sensores [18, 19], energia [16, 20] e outros campos devido às suas excelentes propriedades físicas. O óxido de grafeno é um material de grafeno funcionalizado por superfície que está em uma camada de átomos de carbono conectada com uma extensão infinita bidimensional dos grupos tensoativos de base contendo oxigênio e sua forma de óxido de grafeno [21]. O grafeno (G) e seus derivados têm causado grande preocupação na área biomédica devido à sua estrutura bidimensional única, bem como por propriedades físicas e químicas específicas [22]. Grafeno funcionalizado e seus derivados têm muitas funções, como carga de drogas [23], antibacteriana [24], bioimagem [25, 26] e terapia do câncer [27].
Sobre o aspecto da capacidade antimicrobiana, Li et al. revelou que o mecanismo antimicrobiano de G é causado principalmente por transferência de carga [28] e migração bacteriana. Bactérias transferidas para a superfície de nanofolhas afiadas, que dilaceram as bactérias pelas bordas afiadas [29]. Além disso, Tu et al. também demonstraram outro potencial mecanismo antimicrobiano que o G pode penetrar nas células, levando à extração de grandes quantidades de fosfolipídios das membranas celulares [30]. Assim, G e óxido de grafeno (GO) possuem bioatividade e capacidade antimicrobiana, o que atende aos requisitos para serem qualificados como materiais de reparo ósseo.
No entanto, com a produção e aplicação em grande escala, as questões de biossegurança do grafeno são particularmente importantes. Os trabalhadores podem sofrer com a exposição a nanopartículas (NPs) por meio de vários meios, incluindo inalação, contato cutâneo e vias gastroentéricas. Andrea Prodi et al. sugeriu uma abordagem gradual para avaliar a exposição a NP para proteção adicional [31]. Exceto para avaliação, biossegurança e biocompatibilidade são outros pontos-chave da pesquisa. Kan Wang et al. demonstraram a biocompatibilidade do GO, que exibe toxicidade para células de fibroblastos humanos quando a dose é inferior a 20 μg / ml, mas exibe citotoxicidade óbvia quando a dose é superior a 50 μg / ml, com redução significativa da adesão celular [32]. No momento, uma visão mais consistente confirma que G e GO têm um efeito tóxico sobre as bactérias, mas em desacordo com o efeito tóxico sobre as células [33,34,35,36]. A função e toxicidade de G e GO ainda precisam de um estudo mais específico. Beatriz Pelaz et al. levantou uma questão, “como reduzir os riscos e aumentar os benefícios são vitais para o desenvolvimento de nanomedicamentos seguros e eficazes”, o que lembra e incentiva o estudo para a combinação dos riscos potenciais de G e GO e capacidade antibacteriana in vivo e in vitro [12] .
As células-tronco mesenquimais da medula óssea (BMSCs) são células-tronco adultas multipotentes. Eles se tornaram uma importante fonte de células para reparar defeitos ósseos na engenharia de tecidos [37, 38]. Além disso, a interação entre grafeno e derivados e células-tronco ainda carece de pesquisas [39, 40].
Portanto, este estudo pesquisou o efeito de G e GO em tecidos musculares de camundongos BMSCs in vitro, Staphylococcus aureus , com o objetivo de investigar a citotoxicidade e capacidade antibacteriana de G e GO in vivo e in vitro e promover a pesquisa de nanomedicina e nanotoxicidade de nanomateriais de carbono.
Resultados
Citotoxicidade G e GO
G e GO Citotoxicidade in vitro
Ao microscópio eletrônico, nanopartículas G ou GO apresentaram formato irregular com o tamanho de 30,41 ± 5,59 nm, e aglomeração de partículas pôde ser encontrada (Fig. 1a, b). Após 7 dias de cultura, a morfologia da célula foi alterada para a forma de fuso (Fig. 1c). Nódulos de cálcio foram formados após cultura com meio de diferenciação osteogênica (fig. 1d). O acúmulo de óleo foi formado após a diferenciação adipogênica (Fig. 1e).
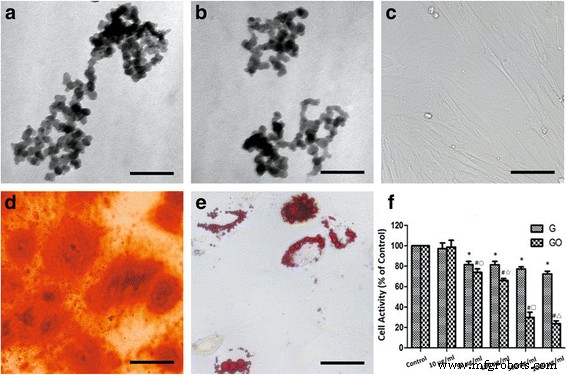
Citotoxicidade G e GO ( a , b). Imagens TEM de G ( a ) e GO ( b ) mostrou a nano-rede formada. c Citomorfologia de BMSCs. d Vermelho de alizarina para deposição de cálcio. e Óleo vermelho O para lipídio. f Atividade celular após o tratamento G e GO, * P <0,01 com grupo de controle, # P <0,01 com grupo de controle, ○ P <0,05 com grupo G 50 μg / ml, ☆, □, △ P <0,01 com a mesma concentração do grupo G. r 2 (G) =0,843, r 2 (GO) =0,939. Barras de escala a , b 200 nm, c , d 100 μm, e 50 μm. r , coeficiente de correlação
Quando a concentração foi superior a 10 μg / ml, G ou GO inibiu o crescimento de BMSCs. A citotoxicidade foi maior no grupo de 1000 μg / ml e mostrou-se de maneira dose-dependente. Quando a concentração foi superior a 10 μg / ml, a citotoxicidade do grupo GO foi maior do que o grupo G na mesma concentração. A diferença foi mais significativa com o aumento da concentração (fig. 1f).
Sob a observação de MEV, quando a concentração de G ou GO era de 10 μg / ml, as BMSCs estavam em bom estado com boa adesão e forma. Quando a concentração de G era superior a 50 μg / ml, as células mudaram, incluindo diminuição do tamanho, aumento da secreção da superfície e extensão das microvilosidades da superfície celular. Quando a concentração de GO era superior a 50 μg / ml, as BMSCs estavam encolhidas e deformadas e a maioria das células estava morta. Esses resultados indicaram que o GO tinha maior citotoxicidade para BMSCs em comparação com G na mesma concentração (Fig. 2).
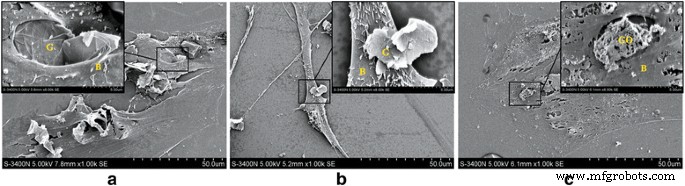
Imagens SEM de co-cultura de G, GO e BMSCs. a Grupo G, 10 μg / ml. As células estão em boas condições. b Grupo G, 50 μg / ml. O tamanho da célula diminui, a secreção da superfície aumenta e os microvilosidades na superfície da célula tornam-se longos. c Grupo GO, 50 μg / ml. BMSCs encolhem e deformam. G grafeno, óxido de grafeno GO, B BMSCs
Sob a observação de TEM, descobrimos que G ou GO poderia entrar em BMSCs e se depositar no interior da célula. E quando a concentração era superior a 50 μg / ml, alterações no microambiente celular, incluindo desordem da estrutura celular e bagunça de microvilosidades, foram encontradas, indicando a maior citotoxicidade do GO em comparação com o grupo G (Fig. 3).
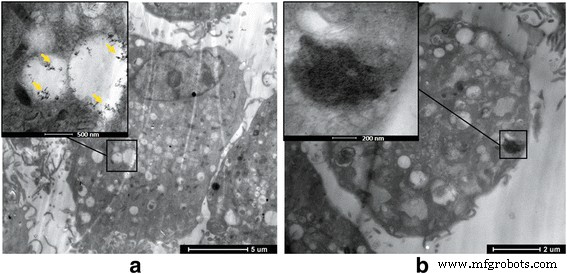
Imagens TEM de co-cultura de G, GO e BMSCs. a Grupo G. b GO group. Tanto G quanto GO podem levar a distúrbios da estrutura celular e bagunça de microvilosidades na superfície celular; GO causa alterações no microambiente celular de alta citotoxicidade
Com base no resultado da observação SEM e TEM, descobrimos que 10 μg / ml era a concentração crítica de segurança para G e GO. Quando a concentração de GO foi superior a 10 μg / ml, o GO apresentou maior citotoxicidade para BMSCs em comparação com G.
G e GO Citotoxicidade In Vivo
Para analisar a citotoxicidade de G e GO in vivo, selecionamos tecido esquelético para representar e simular a circunstância do transplante local em ortopedia. O resultado da coloração HE do tecido esquelético no grupo controle e no grupo G apresentou estrutura normal com miofibrilas musculares paralelas ao eixo vertical. Em corte transversal, a seção miofibrilar apresentada como manchas finas e núcleo localizava-se na borda das células. As alterações mencionadas acima também podem ser encontradas em células esqueléticas normais, indicando que G tem pouca toxicidade para os tecidos musculares.
Ao contrário, no grupo GO, as linhas transversais das fibras musculares no corte longitudinal estavam fraturadas e não nítidas, revelando atrofia e necrose do músculo. Assim, o GO apresentou maior toxicidade aos animais (Fig. 4).
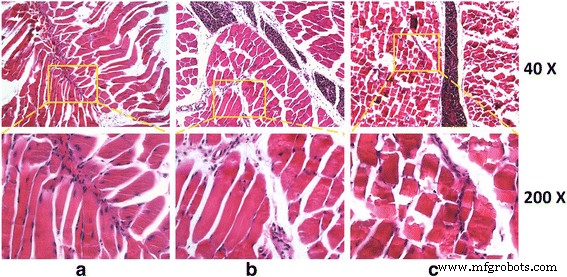
Secções de tecido manchadas com coloração HE. a O controle representa o tecido não lesado. b Grupo G. Células esqueléticas presentes como uma faixa reta. As miofibrilas musculares são paralelas ao longo do eixo, as linhas transversais são claras e a seção transversal é composta por blocos irregulares. A seção miofibrilar se apresenta como manchas finas; núcleo está localizado na borda. c GO group. As linhas transversais das fibras musculares na seção longitudinal são fraturadas e não estão claras
Propriedades antibacterianas G e GO
Capacidade antibacteriana in vitro
No experimento de bacteriostose in vitro, a intensidade de fótons da ROI de G ou GO mostrou-se dose-dependente. E a intensidade do fóton diminuiu de acordo com o aumento da concentração. Quando comparado ao grupo G na mesma concentração, o grupo GO apresentou menor intensidade de fótons (fig. 5).
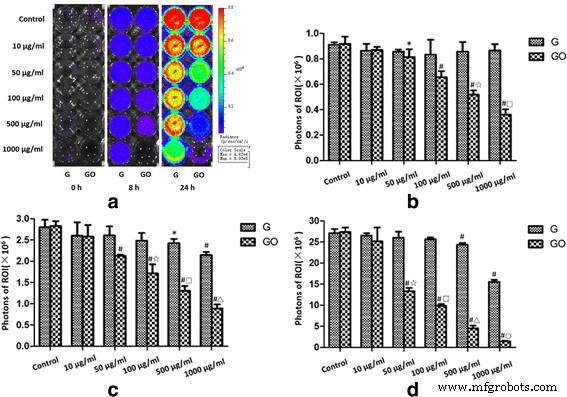
Monitoramento de intensidade de bioluminescência de S . aureus em vitro. G e GO mostram uma maneira dependente da dose na capacidade antibacteriana in vitro. a Bioluminescência de Xen-29 com imagem in vitro após 0, 8 e 24 h de incubação a 37 ° C, com variações na cor representando a intensidade da luz (Bin M (8), FOV12, f1, 15 s). b PI =0 h, r 2 (GO-0 h) =0,924. c PI =8 h, r 2 (G-8 h) =0,584, r 2 (GO-8 h) =0,960. d PI =24 h, r 2 (G-24 h) =0,616, r 2 (GO-24 h) =0,943. * P <0,01 com grupo de controle, # P <0,01 com grupo de controle, ☆, □, △, ○ P <0,01 com a mesma concentração do grupo G. r , coeficiente de correlação
Às 0, 8 e 24 h, quando as concentrações de G eram 100, 500 e 1000 μg / ml, G mostrou a capacidade de inibição do crescimento de Xen-29 em comparação com o grupo controle. No entanto, a intensidade do fóton nos grupos de 10 e 50 μg / ml não apresentou diferença significativa em comparação com o grupo controle.
Quando as concentrações de GO foram de 50, 100, 500 e 1000 μg / ml, às 0, 8 e 24 h, o GO apresentou efeito de inibição do crescimento em relação ao Xen-29. Da mesma forma, a intensidade do fóton nos grupos de 10 e 50 μg / ml não apresentou diferença estatisticamente significativa em comparação com o grupo controle.
Os resultados mostraram que o G apresentou capacidade antibacteriana com concentração superior a 100 μg / ml, e o GO apresentou capacidade antibacteriana com concentração superior a 50 μg / ml. A capacidade antibacteriana de G ou GO era dependente da dose. GO teve capacidade antibacteriana mais forte em comparação com G na mesma concentração.
Capacidade antibacteriana in vivo
No experimento de bacteriostose in vivo, o grupo GO apresentou valores de intensidade de fótons (PI) significativamente mais baixos em 0 e 24 h. O valor do IP foi diminuído em comparação com o grupo G e o grupo controle. No entanto, o valor de IP do grupo G não foi estatisticamente significativamente diferente em comparação com o grupo controle (fig. 6). Os resultados mostraram que o GO mostrou uma forte capacidade antibacteriana, mas o G não mostrou nenhuma capacidade antibacteriana óbvia in vivo na concentração de 100 μg / ml.
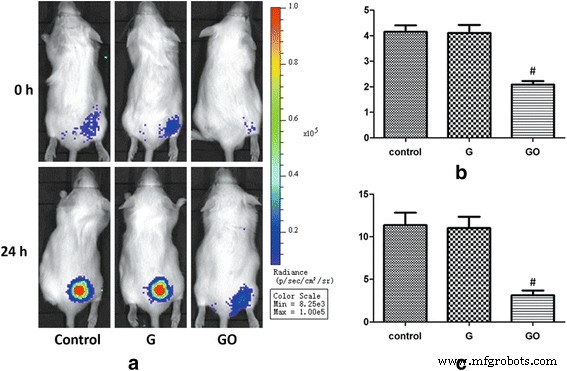
Monitoramento de intensidade de bioluminescência de S . aureus na Vivo. GO mostra uma maneira dependente da dose na capacidade antibacteriana in vivo. a Bioluminescência de Xen-29 com imagens in vivo após 0 e 24 h de incubação, com variações na cor representando a intensidade da luz (Bin M (8), FOV12, f1, 60 s). b PI =0 h, # P <0,01 com grupo controle. c PI =24 h, # P <0,01 com grupo controle
Discussão
Com o desenvolvimento da engenharia de tecidos, um número crescente de aplicações de biomateriais são utilizadas no campo do tratamento ortopédico [41]. Uma boa biossegurança é necessária para biomateriais. G e GO têm sido amplamente utilizados na área médica por sua segurança e propriedades físicas e químicas exclusivas. No aspecto da capacidade antibacteriana, G e GO são as boas substâncias antibacterianas. Os principais mecanismos antibacterianos são a transferência de carga [28, 29] e a penetração nas células [30]. Assim, a capacidade antibacteriana de G e GO poderia atender aos requisitos para materiais de reparo ósseo abaixo dos limites seguros.
Neste estudo, para identificar as propriedades de biossegurança, observamos efeito citotóxico de G e GO sobre as BMSCs por meio de MEV e TEM, sendo esse efeito apresentado de forma dose-dependente. Além disso, o GO teve maior efeito citotóxico. Sobre o aspecto das propriedades antibacterianas, observamos ainda que G e GO tinham propriedades antibacterianas como uma forma dependente da dose, e o efeito GO foi significativamente melhor do que G in vivo. Em conclusão, a concentração na faixa de 50 ~ 100 μg / ml pode ser melhor para manter o equilíbrio entre o efeito citotóxico menor e a capacidade antibacteriana principal.
Esta pesquisa demonstrou que tanto G quanto GO apresentam efeito citotóxico para BMSCs e células esqueléticas e a toxicidade de GO é maior que G. Um grande número de estudos tem demonstrado a toxicidade de nanocélulas G e suas propriedades físicas e químicas do material (como tamanho, forma e grupos funcionais de superfície) em direção às células [35, 42, 43]. Além disso, os pesquisadores descobriram que o G puro pode induzir citotoxicidade por meio do esgotamento do potencial da membrana mitocondrial (MMP) e do aumento das espécies reativas de oxigênio intracelular (ROS) [12], portanto, desencadeando a apoptose pela ativação da via mitocondrial [34, 44] . Porém, o fenômeno de que a citotoxicidade do GO é superior ao G pode estar associado aos grupos contidos na superfície do GO [45]. Os pesquisadores descobriram que a citotoxicidade do GO está diretamente relacionada ao conteúdo sérico. Hu W et al. demonstraram que o GO tem uma forte capacidade de adsorção que poderia adsorver proteínas séricas para formar inclusões proteicas [46], demonstrando a maior base citotóxica do GO em comparação com G. Nossos experimentos confirmaram as conclusões mencionadas acima. Além disso, a toxicidade animal é outro indicador importante da avaliação da segurança biológica de G e GO. Neste estudo, foi encontrada resposta patológica grave em tecidos musculares no grupo GO, indicando sua maior toxicidade em comparação com o grupo G.
Em segundo lugar, as propriedades antibacterianas estão de acordo com as alterações de dose de G e GO; A concentração de GO de 50 ~ 100 μg / ml pode equilibrar melhor a toxicidade biológica e a capacidade antibacteriana. Nossos estudos demonstraram que tanto a toxicidade biológica quanto a capacidade antibacteriana apresentam-se de forma dose-dependente. Portanto, algum intervalo de concentração pode manter o equilíbrio entre a toxicidade biológica menor e a capacidade antibacteriana principal.
Os resultados mostraram que tanto G quanto GO apresentaram alguma toxicidade biológica para BMSCs e tecidos musculares, mas no grupo GO, a capacidade antibacteriana foi significativa in vivo. Com base nos resultados anteriores de toxicidade G e GO, descobrimos que a concentração de 50 ~ 100 μg / ml pode ser a melhor para manter o equilíbrio entre a toxicidade biológica menor e a capacidade antibacteriana principal, fornecendo assim novas evidências em relação à biossegurança e antibacteriano capacidade de G e GO in vivo e in vitro em trabalho clínico.
Embora o GO tenha muito efeito tóxico, a toxicidade pode ser evitada por modificações do GO [47, 48]. Ao mesmo tempo, os materiais GO modificados podem ser degradados e eliminados no corpo [49]; assim, uma nova direção de pesquisa da modificação para GO é sugerida. Além disso, os efeitos de G e GO em outros órgãos ou tecidos importantes ainda precisam de mais pesquisas para se chegar à medicina holística. Enquanto isso, se o GO causa danos por estresse oxidativo às bactérias e a presença de mecanismo antibacteriano adicional, é necessário um estudo mais aprofundado. Antes da aplicação na engenharia de tecidos, os mecanismos de toxicidade G e GO e as formas modificadas de reduzir a toxicidade ainda precisam de mais esclarecimentos.
Métodos
Animais
Ratos Sprague-Dawley (SD) machos e camundongos Balb / C machos foram adquiridos no Instituto Pasteur do Irã e mantidos sob a condição de luz / escuridão de 12 h a 25 ° C. Ratos SD com a idade de 4 semanas foram usados para o isolamento das BMSCs. Camundongos Balb / C foram usados para experimentos com animais in vivo. Todos os animais foram criados no Centro de Animais de Laboratório da Fourth Military Medical University, e as operações estavam seguindo o Animal Experimental Surgery Standard do Xijing Hospital. Todos os experimentos com animais foram aprovados pelo Comitê de Uso e Cuidado Institucional de Animais da Quarta Universidade Médica Militar.
Grafeno e óxido de grafeno
G ou GO (camadas 1-2) (Hengqiu Graphene Technology, China) foram respectivamente adicionados em etanol absoluto (usado para teste de microscópio eletrônico de transmissão, TEM), tampão PBS (usado para experimentos de células in vitro) e solução salina (usado para experimentos com animais in vivo) para preparar a solução G ou GO (o resultado do teste de espectroscopia Raman foi fornecido pela Hengqiu Graphene Technology). A concentração inicial da solução G ou GO foi de 1 mg / ml. A solução G ou GO foi dispersa usando ultrassom 2 h antes dos experimentos.
Citotoxicidade
Cultura de células
O meio de cultura de células continha 10% de soro fetal bovino (Gibco, Carlsbad, Califórnia, EUA), DMEM / F12 (Corning, NY, EUA), 100 U / ml de penicilina e 100 U / ml de estreptomicina (Sigma, St. Louis, Missouri, EUA). As BMSCs foram extraídas de ratos machos com 4 semanas de idade pelo método de cultura de medula óssea [50]. Após a execução do rato, o fêmur e a tíbia foram removidos em condições assépticas. A cavidade medular foi lavada com meio de cultura de células; em seguida, a mistura foi centrifugada a 1500 rpm por 10 min para coletar a medula óssea. A medula óssea foi ressuspensa com meio de cultura de células e inoculada em frascos de cultura de células revestidos de gelatina a 37 ° C e 5% de dióxido de carbono em incubadora de células. O meio nos frascos de cultura de células foi trocado após 48 horas e as células não aderentes foram removidas; em seguida, o meio de cultura foi trocado uma vez a cada 48 h. Células de terceira a quinta passagem foram usadas para os próximos experimentos.
A diferenciação osteogênica e a diferenciação adipogênica em BMSCs foram realizadas com meio de diferenciação (Cyagen, CA, EUA). Após 2 semanas de indução da diferenciação, as células foram fixadas com solução de formaldeído a 4% por 30 min; em seguida, foi realizada a coloração com vermelho de alizarina para diferenciação osteogênica e a coloração com vermelho de óleo para diferenciação adipogênica.
Atividade celular
A concentração da suspensão de BMSC foi ajustada para 5 × 10 4 / le as células foram cultivadas em uma placa de 96 orifícios com 100 μl em cada orifício. Após 24 h, o meio foi substituído por meio de cultura de células contendo G ou GO nas concentrações de 0 (como grupo controle), 10, 50, 100, 500 e 1000 μg / ml. Após 24 h de cultura, 10 μl de alamarBlue (Bio-rad, Hercules, CA, EUA) foram adicionados a cada orifício por mais 4 h de cultura. A microplaca (Bio-rad, Hercules, CA, EUA) foi usada para detectar os valores de OD (densidade óptica) em 570 e 600 nm e, em seguida, a calculadora colorimétrica alamarBlue® (Bio-rad, Hercules, Califórnia, EUA) foi usada para avaliar a taxa de proliferação celular.
Caracterização usando SEM
As BMSCs foram semeadas em uma placa de vidro fina de 24 furos com 0,17 mm de espessura e 14 mm de diâmetro. Após 24 h de cultivo, o meio foi substituído por meio de cultura celular contendo G ou GO nas concentrações de 0 (como grupo controle), 10, 50, 100, 500 e 1000 μg / ml. As células continuaram a cultura durante 24 horas e o sobrenadante foi removido posteriormente. As células foram fixadas com solução de glutaraldeído 2,5% por 24 horas. Em seguida, as células foram observadas em microscópio eletrônico de varredura (Hitachi S-4800 SEM, JPN) após desidratação e douramento.
Caracterização usando TEM
As suspensões G e GO foram ajustadas para 50 μg / ml. As células foram co-cultivadas com G ou GO por 24 horas e então digeridas por 0,25% de tripsina. O sobrenadante foi removido após centrifugação a 1000 rpm durante 10 min. As células foram fixadas com solução de glutaraldeído 2,5% por 24 he cortes foram observados por microscopia eletrônica de transmissão (FEI Tecnai G2 TEM, EUA).
Toxicidade e identificação do tecido muscular
Para analisar a citotoxicidade de G e GO in vivo, selecionamos tecido esquelético para representar e simular a circunstância do transplante local em ortopedia. G ou GO foram respectivamente injetados nos tecidos do músculo femoral medial de camundongos Balb / C. Os camundongos foram mortos após 7 dias, e os tecidos musculares injetados com G ou GO foram fixados com solução de formaldeído neutro a 10% por 24 h. Após a desidratação do álcool, o tecido foi envolto em parafina e fatiado para a realização da coloração por hematoxilina e eosina (HE). Fatias foram observadas sob microscópio invertido (microscópio invertido Leica DMI6000B, RBT).
Capacidade antibacteriana
Cultura bacteriana
Selecionamos o Xen-29 para cultura por sua reação luminescente. Xen-29 era uma bactéria bioluminescente de Staphylococcus aureus (Caliper, LS, EUA) derivado de ATCC-12600. As bactérias foram cultivadas em meio Luria Bertani (LB, Sigma, St. Louis, MO, EUA) contendo 200 μg / ml de canamicina (Sigma, St. Louis, MO, EUA) a 37 ° C. Uma única colônia foi coletada em caldo LB a 37 ° C com agitação por 2–3 h na velocidade de 200 rpm. Quando a absorvância a 600 nm atingiu 0,5 (aproximadamente equivalente a 1,44 × 108 cfu / ml) em comparação com a absorvância em branco de caldo LB, as bactérias foram usadas para o próximo experimento.
Imagem bioluminescente
Para apresentar a imagem bioluminescente, usamos o sistema de imagem macroscópica óptica CCD refrigerado IVIS Lumina II (Caliper, LS, EUA). O sinal bioluminescente bacteriano foi convertido em intensidade de fótons (PI). O software Living Image® 4.2 (Caliper, LS, EUA) foi utilizado para quantificação de IP em regiões de interesse (ROI). A fim de evitar o movimento dos camundongos no processo de imagem, os camundongos foram anestesiados para evitar a instabilidade do sinal recebido.
Capacidade antibacteriana in vitro
Xen-29 foi adicionado à placa de 24 orifícios e a concentração em cada orifício foi 10 7 cfu. Em seguida, a suspensão G ou GO foi adicionada para ajustar a concentração em 0 (controle), 10, 50, 100, 500 e 1000 μg / ml. O volume constante em cada orifício foi de 500 μl. Para analisar a capacidade antibacteriana de G e GO, o IP bacteriano na ROI foi medido sequencialmente em 0, 8 e 24 horas após a intervenção.
Capacidade antibacteriana in vivo
Com base nos resultados do experimento acima, o grupo de 100 μg / ml foi escolhido para identificar a capacidade antibacteriana. A suspensão de Xen-29 (200 μl) foi injetada nos tecidos do músculo femoral medial de camundongos Balb / C. PI de ROI foi detectado em 0 e 24 horas após a operação.
Análise de dados
Todos os dados foram apresentados como média ± desvio padrão (DP). t do aluno teste foi utilizado para comparação entre G e GO com a mesma concentração. A análise de variância (ANOVA) unilateral foi usada para comparar as diferenças entre G e GO com diferentes concentrações, respectivamente. P <0,05 foi considerado estatisticamente significativo.
Conclusões
Em conclusão, G e GO têm algum efeito citotóxico biológico de forma dose-dependente. G e GO têm propriedades antibacterianas e funcionam também como forma dependente da dose; as propriedades antibacterianas do GO são significativamente melhores do que o G in vivo. A concentração de 50 ~ 100 μg / ml pode ser melhor para manter o equilíbrio entre a toxicidade biológica menor e a maior capacidade antibacteriana. Além disso, as modificações do GO para reduzir a toxicidade precisam ser esclarecidas para contribuir com as aplicações de G e GO em nanomedicina.
Abreviações
- BMSCs:
-
Células-tronco mesenquimais da medula óssea
- G:
-
Grafeno
- GO:
-
Óxido de grafeno
- HE:
-
Hematoxilina e eosina
- LB:
-
Luria Bertani médium
- NPs:
-
Nanopartículas
- PI:
-
Intensidade do fóton
- ROS:
-
Espécies que reagem ao oxigênio
- SEM:
-
Microscópio eletrônico de varredura
- TEM:
-
Microscopia eletrônica de transmissão
Nanomateriais
- Grafeno em alto-falantes e fones de ouvido
- Síntese biogênica, caracterização e avaliação do potencial antibacteriano de nanopartículas de óxido de cobre contra Escherichia coli
- Compostos de grafeno e polímero para aplicações de supercapacitor:uma revisão
- Nanotubos de titanato Nanocompósitos de óxido de grafeno decorado:Preparação, Retardância de Chama e Fotodegradação
- Biossegurança e capacidade antibacteriana do grafeno e do óxido de grafeno in vitro e in vivo
- Avaliação de estruturas de grafeno / WO3 e grafeno / CeO x como eletrodos para aplicações de supercapacitor
- Preparação de moagem de esferas em uma etapa de nanoescala CL-20 / óxido de grafeno para sensibilidade e tamanho de partícula significativamente reduzidos
- Uma análise comparativa in vivo de nanopartículas de óxido de cobre e zinco biossintetizadas por vias de administração intraperitoneal e intravenosa em ratos
- Redução aprimorada da condutividade do próton e da permeabilidade do metanol por meio da biomembrana de óxido de grafeno sulfonado eletrolítico de alginato de sódio
- Propriedades das nanopartículas de óxido de zinco e sua atividade contra micróbios



