Um Método Simples Assistido por Ablação a Laser para Fabricação de Substrato SERS Superhidrofóbico em Filme de Teflon
Resumo
Com alta sensibilidade no nível de uma única molécula, o espalhamento Raman aprimorado por superfície (SERS) é considerado uma tecnologia de detecção óptica ultrassensível com amplas possibilidades de aplicação em muitos campos. No entanto, a fabricação complicada e o preço inacessível do substrato SERS ainda são um obstáculo no caminho para serem amplamente utilizados na indústria. Neste trabalho, os espectros SERS em um filme comercial de Teflon gravado a laser (PTFE) com microarray gravado são investigados. A molhabilidade da superfície do filme modulada por gravação a laser faz com que o microarray tenha a capacidade de diminuir a área de contato na superfície do filme durante a evaporação da água. A imagem SEM da área gravada aponta que o processo de gravação gerado por micro / nanoestruturas é crucial para sua propriedade superhidrofóbica. As moléculas de sondagem (ou seja, azul de metileno e rodamina6G) foram utilizadas para investigar com o limite de detecção (1 × 10 −14 M). Além disso, a biomolécula (albumina de soro bovino) foi utilizada para demonstrar seus benefícios em aplicações biológicas. As intensidades medidas dos espectros Raman neste PTFE com microarray gravado a laser demonstram seu valor potencial para um substrato SERS. Nosso trabalho neste substrato SERS simples e barato com alta sensibilidade tem um grande valor comercial e muita aplicação em muitos campos.
Histórico
O espalhamento Raman intensificado por superfície (SERS) já despertou grande interesse do público desde sua descoberta em 1974, pois é uma técnica espectroscópica ultrassensível promissora para obter a impressão digital vibracional de características moleculares, mesmo no caso de solução superdiluída [1, 2,3,4,5]. O enorme campo eletromagnético próximo à superfície do metal é o fator intensificado dominado no SERS, que vem da oscilação coletiva de elétrons livres excitada pela luz, chamada plasmon de superfície. Como resultado, os fortes sinais moleculares Raman obtidos são principalmente derivados daquelas moléculas que estão localizadas nas nano-lacunas ou fendas, os chamados pontos quentes, perto da superfície do metal onde o campo eletromagnético é muito intensificado.
Em trabalhos anteriores, as várias nanopartículas de morfologia Ag ou Au foram introduzidas para se depositar no vidro ou wafer de silício, a fim de fabricar o substrato SERS [6,7,8,9]. Infelizmente, o vidro, o wafer de silício e outros substratos frequentemente usados são hidrofílicos, então as nanopartículas dispersas no solvente são livremente dispersas nos substratos após a evaporação, resultando na distância entre as nanopartículas tão grande que é difícil formar um campo eletromagnético maior Aprimoramento. Considerando a difusão do soluto, existe um método que pode ser esperado para conseguir concentrar os solutos em uma pequena área, obrigando as nanopartículas a serem densamente compactadas e as moléculas a entrarem nas áreas de pontos quentes, o que poderia atingir os objetivos de aprimoramento os sinais Raman das moléculas. Conseqüentemente, a linha de pensamento fornece outra abordagem para fabricar os substratos SERS impactantes. Recentemente, com base na concepção, vários substratos hidrofóbicos ou superidrofóbicos já foram relatados como substratos SERS ativos, graças ao alto aprimoramento e reprodutibilidade aprimorada, como o substrato de arranjo de micro-pilares cilíndricos de Si decorado com Ag-NP, arranjo de nanopartículas de óxido de zinco revestido de prata substrato superhidrofóbico, e assim por diante [10, 11]. A razão é que a superfície superhidrofóbica pode efetivamente reunir os solutos dissolvidos na solução em uma pequena faixa após a evaporação da água. No entanto, muitos substratos super-hidrofóbicos causam a perda de solutos por causa de suas micro / nanoestruturas inerentes [12, 13]. Enquanto isso, o processo de fabricação desses substratos costuma ser demorado e complexo, e esses substratos geralmente são caros. Normalmente, leva várias horas para que toda a água se volatilize em temperatura ambiente, limitando a detecção e análise rápidas em aplicações práticas. Por conta dessas desvantagens, é um desafio popularizar amplamente o substrato SERS super-hidrofóbico no mundo real.
Neste trabalho, um método assistido por ablação a laser foi proposto para fabricar o substrato SERS sobre Teflon (PTFE). A molhabilidade da superfície é alterada pela tecnologia de gravação a laser. Ao projetar um padrão de gravação a laser adequado e definir os parâmetros apropriados de gravação, um tipo de substrato de PTFE superhidrofóbico com microarranjos é obtido. Os microarrays são hidrofóbicos e circundados pela área superhidrofóbica, que é gerada a partir da gravação a laser.
Graças ao substrato especial, os solutos dissolvidos na água podem ser coletados com sucesso nos pequenos círculos hidrofóbicos após a evaporação do solvente, levando apenas 10 minutos. Semelhante às placas de 24 poços em laboratório biológico, o substrato SERS desenvolvido com poços virtuais pode detectar convenientemente as moléculas e suas concentrações. Além disso, o substrato SERS obtido custa apenas 20 RMB e todo o processo de fabricação leva 20 minutos. Em suma, é fabricado um substrato SERS ativo, confiável, prático e de baixo custo, que pode realizar uma evaporação rápida sem afetar os resultados de detecção neste trabalho.
Métodos e Experimento
Material
Nitrato de prata (99,99%), PVP (Mw =58.000, K29-32), boro-hidreto de sódio (NaHB 4 ), etilenoglicol (EG), azul de metileno (MB) e Rhodamine6G (R6G) foram adquiridos à Shanghai Aladdin bioquímica Polytron Technologies Inc. (Shanghai, China). A albumina de soro bovino (BSA) foi adquirida à Sigma-Aldrich (Taufkirchen, Alemanha). Todos os produtos químicos foram usados como recebidos sem purificação ou tratamento adicional. Água desionizada de alta pureza (18,25 MΩ · cm) foi produzida usando Aquapro AWL-0502-H (Aquapro International Company LLC., Dover, DE, EUA). Teflon conforme adquirido (PTFE) foi usado diretamente, que está amplamente disponível no mercado online, e o tamanho era 50 × 30 × 5 mm.
A Síntese de Nanopartículas de Ag
As nanopartículas de Ag foram sintetizadas de acordo com um método de síntese anterior. No processo de experimento, a solução EG foi introduzida para dissolver o sólido ou pó. No início, 6 mL de uma solução de EG foram adicionados a um frasco de 100 mL e, em seguida, o frasco foi movido para um banho de óleo a uma temperatura de 165 ° C sob agitação durante 1 h. A seguir, 0,08 mL de um NaHB 4 solução (0,0015 mg / mL), 1,5 mL de uma solução de PVP (20 mg / mL) e 0,4 mL de um AgNO 3 solução (48 mg / mL) foram respectivamente adicionados ao frasco anterior por sua vez por agitação durante 20 min. Posteriormente, o colóide cinza de prata foi obtido. As nanopartículas de Ag podem ser obtidas da solução por centrifugação e lavadas com etanol mais de quatro vezes. Ao final, a amostra foi dispersa na água para posterior experimentação. Usando a água deionizada, as nanopartículas de Ag conforme preparadas seriam preparadas em diferentes concentrações de colóide de prata e as concentrações foram estimadas em 1,19 × 10 −11 , 1,19 × 10 −12 , 1,19 × 10 −13 , 1,19 × 10 −14 e 1,19 × 10 −15 M.
A Fabricação de PTFE Gravado
O PTFE original adquirido foi enxaguado com água e etanol por mais de três vezes. Em seguida, o PTFE original lavado foi gravado pelo CO 2 máquina de gravação a laser com base no projeto CAD mostrado no arquivo adicional 1:Figura S1 usando gravação a laser (a potência de saída:16–24%, a velocidade de gravação:35–75 mm / s, o comprimento da etapa de gravação:0,02–0,10 milímetros).
Caracterização
A morfologia da superfície do PTFE gravado e original foi obtida por MEV (TESCAN MIRA 3 FE). Cinco microlitros de solução aquosa de nanopartículas de Ag foram despejados no PTFE original e PTFE gravado respectivamente, e então o processo de evaporação em temperatura ambiente e as imagens do ângulo de contato estático com a água foram obtidos usando câmera de alta velocidade (Phantom V 7.3). O valor do ângulo de contato estático com a água foi medido por um tipo de software comercial de régua.
Duas gotas de solução de 5 μL Ag foram colocadas no PTFE original e no PTFE gravado, respectivamente. Posteriormente, seriam levados ao forno (70 ° C). Após a evaporação, as nanopartículas de Ag agregadas nas duas superfícies foram caracterizadas ao microscópio óptico e ao MEV, respectivamente. Outra gota de 5 μL de solução aquosa coloidal de Ag foi colocada no PTFE gravado, e as imagens de SEM de agregados de nanopartículas de Ag foram obtidas após a evaporação à temperatura ambiente.
Em uma análise SERS típica, a solução aquosa de Ag com a mesma concentração e volume (5 μL) foi depositada no substrato de PTFE original e no substrato de PTFE gravado, respectivamente, para formar um embasamento aprimorado. Então, 5 μL de solução aquosa de MB e R6G com diferentes concentrações molares (10 −9 , 10 −11 , 10 −12 , 10 −13 , e 10 −14 M) foi colocado no substrato aprimorado como uma sonda e seco no forno de secagem (70 ° C), e a atividade SERS foi medida com o espectrógrafo Raman com um laser He-Ne de 633 nm (10 mW). Conforme relatado, as moléculas poderiam manter a atividade SERS nesta temperatura [12]. Cinco microlitros de solução aquosa de BSA com diferentes concentrações (20, 2, 0,2, 0,02 e 0,002 μg / mL) foram colocados no substrato aprimorado e secos no forno (40 ° C), e a atividade SERS foi medida com o Espectrógrafo Raman com laser He-Ne de 633 nm (10 mW). Para manter a bioatividade do BSA, a temperatura de evaporação foi ajustada para 40 ° C [14]. Os sinais foram obtidos com uma varredura a cada 20 s em todas as medições.
Resultados e discussão
O processo do experimento é mostrado na Fig. 1. A molhabilidade da superfície de PTFE original foi alterada por tratamento a laser usando o design CAD mostrado no arquivo adicional 1:Figura S1, levando a um resultado que toda a superfície tornou-se super-hidrofóbica, exceto para estes não tratados áreas, que eram a superfície hidrofóbica (o diâmetro do círculo:0,5 mm, lacuna:0,8 mm). A fotografia do PTFE gravado é mostrada no arquivo Adicional 1:Figura S2. Posteriormente, uma gota de solução coloidal de Ag (5 μL) foi colocada no PTFE gravado e evaporado no forno (70 ° C). Cerca de 10 minutos depois, as nanopartículas de Ag puderam ser agregadas no círculo (superfície hidrofóbica) devido à propriedade altamente repulsiva da superfície super-hidrofóbica, e então o substrato SERS ativo foi obtido. Em primeiro lugar, a Rodamina6G (R6G) e o azul de metileno (MB) atuaram como as moléculas de sonda para investigar o desempenho SERS do substrato SERS fabricado. Uma gota de solução molecular foi jogada no PTFE gravado cobrindo as nanopartículas de Ag previamente depositadas. Por causa da repelência à água da estrutura superhidrofóbica, a gota molecular se tornaria cada vez mais espessa no processo de evaporação, o que enriqueceria as moléculas para as áreas de pontos quentes na lacuna entre as nanopartículas de forma eficaz. Curiosamente, a evaporação de alta temperatura não só poderia acelerar a evaporação do solvente para obter uma análise rápida sem influenciar os resultados do experimento, mas também dificilmente teria um efeito adverso na agregação de solutos a 70 ° C.
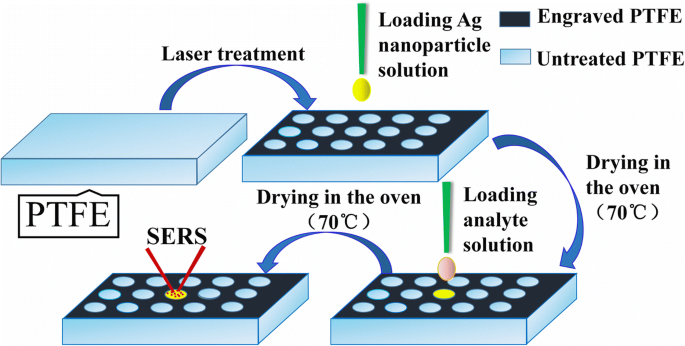
O diagrama esquemático do processo experimental
Para explicar melhor a razão pela qual o PTFE gravado é melhor do que o PTFE original na capacidade de enriquecer solutos, as imagens de SEM e os perfis de evaporação usando uma câmera de vídeo de alta velocidade dos dois tipos de substratos de PTFE são obtidos e mostrados na Fig. 2. Como o PTFE foi gravado, o laser destruiria e removeria a superfície lisa do PTFE original, o que poderia alterar a rugosidade da superfície e permitir que micro / nanoestruturas apareçam no PTFE. Na Fig. 2a, para PTFE gravado, todas as superfícies dos círculos não tratados mostram uma superfície relativamente lisa, mas a área gravada é embelezada com micro / nanoestruturas, o que transforma o PTFE em PTFE superhidrofóbico. Enquanto isso, as imagens do ângulo de contato mostram que o ângulo de contato estático com a água do PTFE gravado é muito maior do que o original e o valor do ângulo (PTFE gravado) é 151,8 °, conforme mostrado na parte inferior da Fig. 2a, que já atingiu o valor do ângulo de contato estático exigido pela estrutura superhidrofóbica [15]. A câmera de vídeo de alta velocidade foi usada para observar e registrar o processo de evaporação em que uma gota de solução colóide de 5 μL Ag evaporou no PTFE original e gravado à temperatura ambiente (R.T.), respectivamente. Como os processos de evaporação demoravam muito, os perfis de evaporação do início e do final do processo de evaporação foram capturados respectivamente para explicar intuitivamente o processo, mostrado na Fig. 2b (PTFE original) e na Fig. 2c (PTFE gravado). Para o PTFE original, durante a evaporação, a superfície de contato entre a solução e a superfície do substrato quase não diminui. Em contraste, existe uma diminuição relativamente óbvia sobre a superfície de contato para PTFE gravado, como mostrado na Fig. 2c. A razão é que a repelência à água das micro / nanoestruturas reduz gradualmente a gota na área do círculo hidrofóbico durante o R.T. evaporação, contribuindo para a diminuição da área de contato. Comparando as Fig. 2b e c, pode-se observar diretamente que as nanopartículas de Ag no PTFE fabricado foram coletadas em uma área muito menor do que o PTFE original. É importante destacar que a superfície super-hidrofóbica especial (a distribuição alternada da superfície hidrofóbica e super-hidrofóbica) não deixa a solução fixar nas texturas micro ou nanoescala e a maioria dos solutos seriam coletados nestes círculos após a evaporação, conforme mostrado em Arquivo adicional 1:Figura S3. Dito de outra forma, a superfície superhidrofóbica especial pode evitar as desvantagens dos materiais superhidrofóbicos gerais de que os analitos permanecem nas micro / nanoestruturas após a evaporação, causando a perda de solutos e um enfraquecimento dos sinais SERS.
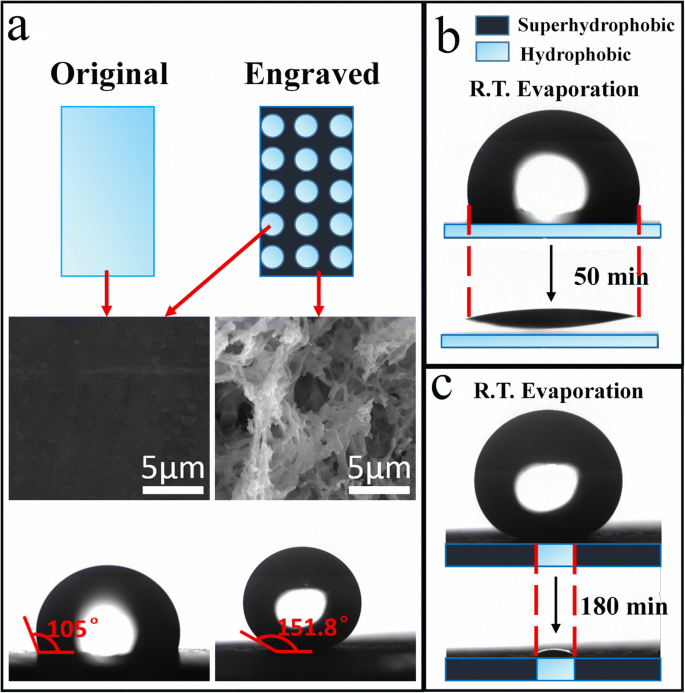
a As imagens SEM da superfície do substrato sobre o PTFE original e PTFE gravado e as imagens de ângulo de contato estático correspondentes; b Perfis de evaporação da solução no PTFE original; c Perfis de evaporação da solução no PTFE gravado
A fim de observar visualmente que as nanopartículas de Ag se reuniram mais densamente no PTFE gravado em comparação com o PTFE original sob evaporação de alta temperatura (70 ° C), existem imagens de microscópio óptico e imagens de SEM com diferentes múltiplos, como mostrado na Fig. 3, respectivamente. A imagem SEM das nanopartículas de Ag preparadas é mostrada no arquivo adicional 1:Figura S4 [16]. Devido ao efeito do anel do café, depois que toda a água evaporou completamente, a maioria das nanopartículas de Ag se reuniria na borda e as nanopartículas restantes seriam dispersas no meio, o que ocupa a maior parte da área para o PTFE original, conforme mostrado na Fig. 3a –G. Com relação ao PTFE gravado, após o processo de evaporação em ambiente de alta temperatura, as nanopartículas de Ag se acumularam no pequeno círculo e não houve efeito de anel de café, conforme mostrado na Fig. 3h-k. Deve ser apontado que a área final de agregação das nanopartículas de Ag no PTFE gravado é quase 25 vezes menor do que o PTFE original, comparando as Fig. 3a e h. Para reduzir o tempo de evaporação, a amostra foi levada ao forno. Notavelmente, a evaporação em alta temperatura pode tornar as nanopartículas mais compactas em comparação com o R.T. evaporação conforme mostrado no arquivo adicional 1:Figura S5. Uma possível explicação é que a rápida evaporação pode fazer com que as nanopartículas de Ag se juntem mais rapidamente. No entanto, a temperatura de evaporação não pode ser elevada demais porque a estrutura das moléculas do analito pode ser deteriorada em temperaturas de aquecimento muito altas, resultando em sinais SERS reduzidos. Devido à rápida evaporação, pode-se economizar muito tempo para preparar o substrato SERS. Resumindo, o substrato fabricado pode enriquecer com eficiência os solutos em uma área muito menor dentro de 10 min para 5 μL de solução de Ag.

a - c As imagens do microscópio óptico e d - g as imagens SEM da agregação de nanopartículas de Ag no PTFE original com diferentes múltiplos. h , i As imagens do microscópio óptico e j , k as imagens SEM da agregação de nanopartículas de Ag no PTFE gravado com diferentes múltiplos. As pequenas caixas laranjas representam a área ampliada e a linha pontilhada branca circunda a área do remate de acumulação de nanopartículas de Ag
Uma vez que a capacidade de detecção de gravação de PTFE depende altamente da hidrofobicidade da superfície, do tamanho da área de detecção e da concentração inicial de nanopartículas de Ag, investigamos esses parâmetros fabricando o substrato de PTFE designado. A intensidade do pico Raman principal em 1322 cm −1 de MB (1 × 10 −9 M) é obtido nos vários substratos SERS. Investigamos o efeito do comprimento da etapa gravada, a potência de saída, a velocidade de gravação e o tamanho do diâmetro do círculo na hidrofobia da superfície. Deve ser apontado que o comprimento da etapa gravada, a potência de saída, a velocidade de gravação e o diâmetro do círculo restringiriam um ao outro e influenciam a capacidade de detecção do substrato. Para entender mais claramente como cada fator afeta a capacidade de detecção, as três variáveis permanecem as mesmas e uma delas é alterada.
Conforme mostrado na Fig. 4a, o ângulo de contato (linha vermelha) e a intensidade Raman (linha preta) diminuem com o aumento do comprimento do passo de gravação. A razão é que quanto menor o comprimento da etapa de gravação, mais densas são as micro / nanoestruturas. Com a ajuda de micro / nanoestruturas mais densas fora dos círculos, os solutos podem ser enriquecidos com sucesso nesses pequenos círculos, e então a capacidade de detecção do substrato é melhorada. Devido à limitação da precisão da máquina de gravação a laser, 0,02 mm é o comprimento mínimo do passo de gravação neste trabalho. Conforme mostrado na Fig. 4b, com o aumento da potência de saída, o ângulo de contato aumenta, mas a intensidade Raman mostra uma tendência de primeiro aumento e depois diminuição. Com o aumento da potência de saída, o PTFE original foi destruído e ablacionado pelo forte laser, levando a mais micro / nanoestruturas na superfície do substrato. Devido à presença de mais micro / nanoestruturas, a superfície do substrato torna-se mais hidrofóbica, conforme evidenciado pelo aumento do ângulo de contato. Notavelmente, a micro ou nanoestrutura supérflua teve um efeito adverso no aumento dos sinais Raman moleculares. A razão é que as micro / nanoestruturas suficientes tornam o substrato super-hidrofóbico, que é capaz de enriquecer os analitos no círculo hidrofóbico, mas os fragmentos de PTFE supérfluos são fáceis de cobrir os pequenos círculos hidrofóbicos conforme o aumento da potência do laser. Posteriormente, os solutos permanecem nas micro / nanoestruturas após o processo de evaporação causando a perda de solutos, o que leva ao enfraquecimento da intensidade Raman. Pode-se concluir que o PTFE gravado fabricado pelo laser de saída de 20% é o substrato SERS ideal.
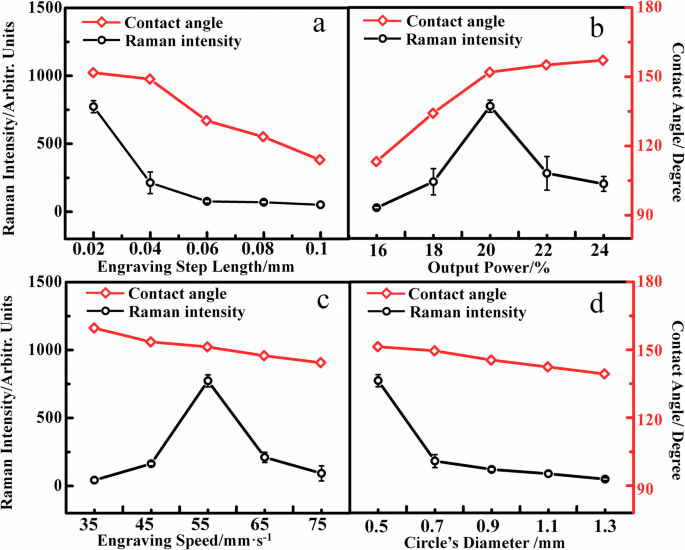
a A relação entre o ângulo de contato, intensidade Raman e a velocidade de gravação (a potência de saída:20%; a velocidade de gravação:55 mm / s; o diâmetro do círculo:0,5 mm; a concentração de Ag:1,19 × 10 −12 M). b A relação entre o ângulo de contato, intensidade Raman e a potência de saída (o comprimento da etapa de gravação:0,02 mm; a velocidade de gravação:55 mm / s; o diâmetro do círculo:0,5 mm; a concentração de Ag:1,19 × 10 - 12 M). c A relação entre o ângulo de contato, a intensidade Raman e a velocidade de gravação (o comprimento da etapa de gravação:0,02 mm; a potência de saída:20%; o diâmetro do círculo:0,5 mm; a concentração de Ag:1,19 × 10 −12 M) d A relação entre o ângulo de contato, a intensidade Raman e o diâmetro do círculo (o comprimento da etapa de gravação:0,02 mm; a potência de saída:20%; a velocidade de gravação:55 mm / s; a concentração de Ag:1,19 × 10 - 12 M)
Na Fig. 4c, o ângulo de contato diminui e a intensidade Raman aumenta e, em seguida, diminui à medida que aumenta a velocidade de gravação. Comparado com o ângulo de contato na Fig. 4b e Fig. 4c, conclui-se que o efeito da velocidade de gravação na superfície do PTFE é oposto ao da potência de saída. A razão é que com o aumento da velocidade do laser, o tempo de exposição do ponto do laser na superfície do PTFE torna-se menor, causando menos ablação do PTFE original. Portanto, menos micro / nanoestruturas são produzidas, levando à diminuição do ângulo de contato. De acordo com a relação entre a intensidade Raman e a velocidade de gravação, o substrato SERS produzido pela velocidade do laser de 55 mm / s possui a melhor capacidade de detecção. Assim, 55 mm / s foi escolhido como a velocidade de gravação no experimento. Como é mostrado na Fig. 4d, o ângulo de contato e a intensidade Raman diminuiriam com o aumento do diâmetro do círculo. Como o círculo é o PTFE não tratado, essas áreas mantêm sua propriedade de umedecimento original, um estado hidrofóbico. Quando uma gota de solução é pingada no substrato de PTFE gravado, a gota tende a permanecer no círculo hidrofóbico. Devido à repelência da água na estrutura superhidrofóbica ao lado do círculo, a gota no PTFE gravado tem um ângulo de contato bastante grande. Com o aumento do diâmetro do círculo, a área de contato entre a gota e a superfície aumenta e a gota lentamente se torna plana, em vez de um esferóide. Como o volume da gota nos diferentes substratos é o mesmo, o ângulo de contato diminui gradualmente. O efeito muda a superfície de gravação de PTFE de superhidrofóbico para hidrofóbico, o que pode afetar o enriquecimento dos solutos, levar à perda de solutos e, finalmente, enfraquecer os sinais Raman. Ao mesmo tempo, com o aumento do diâmetro do círculo, as nanopartículas de Ag se dispersariam em uma região maior, o que aumentaria a lacuna entre as nanopartículas de Ag e, em seguida, enfraqueceria os sinais SERS. Por outro lado, devido ao aumento do diâmetro do círculo, os analitos são dispersos em uma área maior, dificultando a detecção do SERS. Para resumir, a intensidade Raman da molécula enfraqueceria com o aumento do diâmetro do círculo. Devido à limitação da precisão da máquina de gravação a laser, 0,5 mm é o diâmetro mínimo do círculo.
Nesse ínterim, a concentração inicial de nanopartículas de Ag também afeta a intensidade SERS mostrada no arquivo adicional 1:Figura S6. Com o aumento da concentração de nanopartículas de Ag, a intensidade Raman aumenta dramaticamente e então tende a se estabilizar. Com o aumento das nanopartículas de Ag, existem mais “pontos quentes” no substrato, levando ao aumento dos sinais Raman. A discussão mais detalhada foi fornecida nas informações de apoio. Para salvar as nanopartículas de Ag, o 1,19 × 10 −12 A solução de colóide M Ag é escolhida como a concentração inicial de nanopartículas de Ag. Para resumir, neste trabalho, o comprimento da etapa de gravação de 0,02 mm, a potência de saída de 20%, a velocidade de gravação de 55 mm / s, o diâmetro do círculo de 0,5 mm e o 1,19 × 10 −12 Foram escolhidas nanopartículas de M Ag.
A fim de realizar várias detecções no mesmo substrato, o PTFE gravado foi feito nas placas de 24 poços (Fig. 5a), que eram semelhantes às placas de 24 poços para cultura de células. O substrato obtido pode conseguir detectar substâncias diferentes simultaneamente no mesmo PTFE gravado. Enquanto isso, as micro / nanoestruturas na superfície de PTFE gravada poderiam atuar como poços virtuais entre duas gotículas diferentes, o que poderia impedir que as diferentes gotículas se fundissem. Para explicar melhor as vantagens do substrato de PTFE gravado com microarranjos, o PTFE original foi escolhido para comparação. Os espectros SERS de moléculas MB são mostrados na Fig. 5b. A intensidade do sinal SERS do MB obtido nos microarrays é um grande aumento óbvio em comparação com o PTFE original. Já se sabe que as nanopartículas de Ag que evaporam no substrato original tendem a se difundir em uma área muito maior do que no PTFE gravado de acordo com a Fig. 3. Portanto, as nanopartículas de Ag, que estão dispersas no PTFE original, estão longe de uns aos outros, mesmo no limite, contribuindo com os sinais errantes de Raman. No entanto, em termos de PTFE com microarranjos, isso poderia fazer com que nanopartículas massivas se reunissem e a distância reduzida entre as nanopartículas pode aumentar os sinais de SERS. Conforme relatado anteriormente [17,18,19], quanto menor for o tamanho da lacuna, mais forte é o campo eletromagnético da lacuna entre as duas nanopartículas. Por outro lado, o PTFE gravado tem a capacidade de concentrar as moléculas do analito em soluções aquosas superdiluídas, enquanto o PTFE original não, causando mais moléculas dentro da área de foco do ponto de laser incidente no PTFE gravado em comparação com o PTFE original. Enquanto isso, devido ao efeito de condensação superhidrofóbica, o substrato pode ajudar as moléculas a serem entregues nas áreas de pontos quentes [20]. Vale ressaltar que a alta probabilidade de adquirir sinais SERS de moléculas é outro fator muito importante de substratos SERS ativos. Para provar que a probabilidade de detectar as moléculas MB no PTFE gravado é maior do que no PTFE original, as medições de mapeamento sistemático são realizadas e a concentração de moléculas é 1 × 10 −9 M, conforme mostrado no Arquivo Adicional 1:Figura S7. A Fig. 5c, d mostra os espectros de moléculas MB e moléculas R6G, respectivamente, que são coletadas nos substratos SERS de PTFE gravados. É ilustrado que os sinais Raman das moléculas MB são gradualmente enfraquecidos com a diminuição da concentração molecular, enquanto os principais picos podem ser distinguidos e a concentração limite de detecção é 1 × 10 −14 M, como mostrado na Fig. 5c. Além disso, a consequência análoga é encontrada pelos espectros R6G como mostrado na Fig. 5d. Para provar a utilização do PTFE gravado em aplicações biológicas, uma proteína, albumina de soro bovino (BSA), foi usada para testar o desempenho do substrato SERS desenvolvido. O BSA com várias concentrações foi detectado na água, e os espectros Raman foram mostrados na Fig. 5e. Além disso, o limite de detecção de MB, R6G e BSA detectado em vários substratos ou usando métodos diferentes está listado no arquivo adicional 1:Tabela S1.
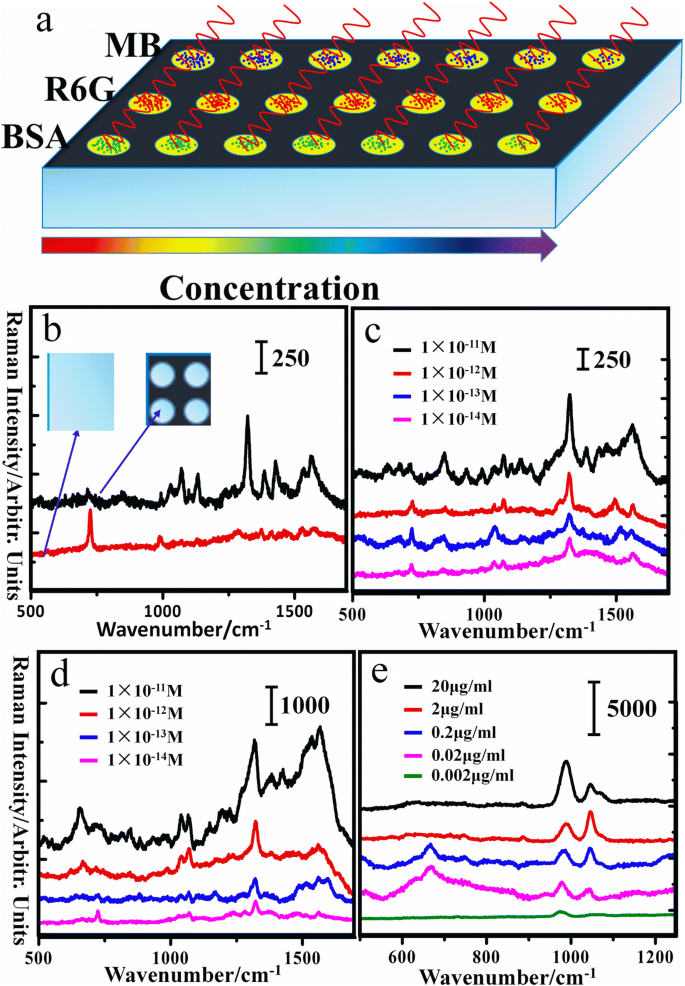
a O esboço esquemático da detecção de substância no PTFE gravado. b Espectros SERS de moléculas MB com a mesma concentração (1 × 10 −9 M) foi obtido em PTFE original e PTFE gravado, respectivamente. c , d , e e Espectros SERS de moléculas MB, moléculas R6G e BSA com várias concentrações, respectivamente
Conclusão
Em resumo, um substrato SERS de baixo custo, ativo e super-hidrofóbico foi fabricado gravando o PTFE por meio dos parâmetros e padrão de gravação adequados, o que poderia atingir as detecções múltiplas em um mesmo substrato. Ao comparar as imagens do ângulo de contato e perfis de evaporação do PTFE original e gravado, o PTFE gravado possui a melhor hidrofobicidade e consegue diminuir a área de contato na superfície do substrato. Além disso, a imagem SEM da área gravada revela a razão pela qual o PTFE gravado possui a melhor hidrofobia devido às micro ou micro / nanoestruturas. Além disso, o PTFE com microarrays poderia contribuir para coletar as nanopartículas de Ag em uma área muito pequena em comparação com o PTFE original pelas imagens SEM obtidas sobre a agregação de nanopartículas de Ag nos dois substratos, levando à produção de um grande número de pontos quentes na superfície de PTFE gravada. A intensidade dos espectros MB Raman (10 −9 M) obtido no PTFE gravado é uma grande melhoria em comparação com o PTFE original. Deve ser apontado que a concentração mais baixa de R6G e MB é 1 × 10 −14 M detectado no substrato SERS super-hidrofóbico fabricado. Enquanto isso, fica provado que o substrato pode ser usado para detectar o BSA (0,002 μg / mL). Resumindo, neste trabalho, uma espécie de substrato SERS barato, altamente sensível e ativo possui um grande valor comercial e pode ser utilizado em diversos campos.
Abreviações
- BSA:
-
Albumina sérica bovina
- EG:
-
Etilenoglicol
- MB:
-
Azul de metileno
- NaHB 4 :
-
Boro-hidreto de sódio
- PTFE:
-
Teflon
- R.T .:
-
Temperatura do quarto
- R6G:
-
Rhodamine6G
- SEM:
-
Microscópio eletrônico de varredura
- SERS:
-
Espectro Raman aprimorado de superfície
Nanomateriais
- Método de fabricação de moléculas artificiais ganha prêmio de melhor pôster
- Nanofios de silício amorfo cultivados em filme de óxido de silício por recozimento
- Método de pós-tratamento para a síntese de nanopartículas FePt-Fe3O4 binárias monodispersas
- Fabricação e caracterização de novo composto de suporte de catalisador anódico de nanofibra de carbono Tio2 para célula de combustível de metanol direto via método de eletrofiação
- Um ânodo de filme Fe2O3 nanocristalino preparado por deposição de laser pulsado para baterias de íon-lítio
- Fabricação de Hierárquicas ZnO @ NiO Core – Shell Heteroestruturas para melhorar o desempenho fotocatalítico
- Por que o corte a laser é adequado para a fabricação de chapas metálicas?
- Filme Sensor para Aeroespacial
- O desafio do método 5S para a indústria 4.0
- Corte a laser:a escolha certa para sua próxima fabricação de metal



