MicroRNA-133a-3p restaurado ou PSAT1 esgotado restringe o aneurisma intracraniano induzido por danos às células endoteliais por meio da supressão da via GSK3β / β-catenina
Resumo
Não está claro sobre o papel funcional do microRNA-133a-3p (miR-133a-3p) no aneurisma intracraniano (IA). Portanto, o objetivo do presente estudo foi investigar o papel regulador do miR-133a-3p na regulação da IA induzida por lesão endotelial vascular através da sinalização de fosfoserina aminotransferase 1 (PSAT1) / glicogênio sintase quinase 3β (GSK3β) / β-catenina caminho. Tecidos de arteríola intracraniana normal e tecidos IA foram coletados de pacientes com trauma cerebral e IA. A expressão de miR-133a-3p, PSAT1, GSK3β e β-catenina em tecidos foi determinada por RT-qPCR e análise de western blot. As células endoteliais (ECs) do IA humano foram cultivadas e tratadas com miR-133a-3p mimetizador e si-PSAT1 para determinar suas funções na migração de células endoteliais, apoptose e proliferação. A expressão de miR-133a-3p, PSAT1, GSK3β, β-catenina, Ki-67, CyclinD1, Bax e Bcl-2 em ECs foi testada por RT-qPCR ou análise de Western blot. Além disso, o modelo de rato IA foi estabelecido para detectar as alterações patológicas e a expressão de miR-133a-3p, PSAT1, GSK3β, β-catenina, VEGF e MMP-9 em tecidos IA in vivo. A expressão de miR-133a-3p foi relacionada ao número e tamanho de IA. A expressão de MiR-133a-3p foi extinta e a expressão de PSAT1, GSK3β e β-catenina foi aumentada em IA. O miR-133a-3p restaurado e o PSAT1 esgotado aliviaram a mudança patológica; redução da expressão de PSAT1, GSK3β e β-catenina em IA; suprimiu a apoptose e a proliferação e migração avançadas de ECs de IA, bem como a expressão de VEGF e MMP-9 reduzida em tecidos de IA in vivo. Nosso estudo sugere que a superexpressão de miR-133a-3p ou a regulação negativa de PSAT1 restringe o dano às células endoteliais e avança a proliferação das células endoteliais por meio da inibição da via GSK3β / β-catenina em IA. MiR-133a-3p pode ser um marcador candidato potencial e alvo terapêutico para IA.
Apresentação da hipótese
No presente estudo, podemos especular que o eixo miR-133a-3p / PSAT1 pode afetar a IA induzida por dano às células endoteliais através da modulação da via GSK3β / β-catenina.
Teste da hipótese
Para verificar essa hipótese, coletamos amostras clínicas, células endoteliais (CEs) do IA humano e estabelecemos modelos de IA de ratos para elucidar as funções do miR-133a-3p e PSAT1 no processo de IA.
Implicações da hipótese
Nosso estudo confirma nossa hipótese de que a superexpressão de miR-133a-3p ou a regulação negativa de PSAT1 restringem o dano às células endoteliais e avançam a proliferação das células endoteliais por meio da inibição da via GSK3β / β-catenina em IA. Essas descobertas fornecem um novo insight sobre uma nova terapia-alvo para IA.
Introdução
O aneurisma intracraniano (IA) é um tipo de distúrbio cerebrovascular, caracterizado por artéria protuberante não convencional no cérebro, bem como hemorragia subaracnoide (HSA) causada por ruptura IA, acompanhada de alta letalidade e morbidade [1]. Por ser uma doença destrutiva, a patogênese da IA não foi esclarecida [2]. IA é uma forma familiar rara, mas geralmente acredita-se que seja o resultado de lesão vascular adquirida causada por hipertensão, tabagismo e outros fatores de risco tradicionais [3]. Enrolamento endovascular ou clipagem microcirúrgica têm sido utilizados para prevenir a futura ruptura de aneurisma não rompido em pacientes com alto risco de ruptura [4]. Embora um progresso significativo tenha sido feito na operação cirúrgica de IA, a recuperação pós-operatória pobre ainda é apresentada em pacientes com IA [5]. A difícil situação do tratamento de IA torna necessário explorar mais o mecanismo e encontrar uma nova estratégia terapêutica.
MicroRNAs (MiRNAs) são uma classe de RNAs não codificantes que modulam a expressão de genes alvo via inibição da tradução no nível pós-transcricional ou mediação da degradação do mRNA [6]. Foi revelado que miR-133a-3p como um inibidor de tumor em várias neoplasias malignas e a superexpressão de miR-133a-3p pode inibir o crescimento de células de câncer colorretal (CRC) [7]. Um estudo anterior afirmou que, à luz do bloqueio da glutaminólise mediada por autofagia, o miR-133a-3p suprime ainda mais a metástase e o crescimento do câncer gástrico [8]. Além disso, um estudo apresentou que o miR-133a-3p participa da regulação do desenvolvimento cardíaco e da hipertrofia cardíaca [9]. Um estudo demonstrou que a regulação positiva de miR-195-5p diminui a angiogênese e a resistência à cisplatina no câncer de ovário por meio da supressão da via de sinalização GSK3β / β-catenina dependente da fosfoserina aminotransferase 1 (PSAT1) [10]. Outro estudo relatou que o miR-365 reprime a invasão celular e o crescimento no carcinoma espinocelular do esôfago (ESCC) por meio da modulação do PSAT1 [11]. PSAT1 é uma enzima envolvida na biossíntese de serina; é originalmente purificado do cérebro de ovelhas e tem níveis elevados em muitos tecidos [12]. Foi documentado que PSAT1 medeia a progressão do ciclo celular no câncer de mama por meio da modulação da via de sinalização GSK3β / β-catenina [13]. Liu et al. assinala também que o PSAT1 exerce uma função no desenvolvimento do ESCC e prevê uma fraca sobrevivência; portanto, pode ser um alvo promissor para a terapêutica anticâncer [14]. Dadas as análises mencionadas, esperava-se que este estudo fizesse contribuições para uma nova abordagem para o papel funcional do eixo miR-133a-3p / PSAT1 / GSK3β / β-catenina em IA.
Materiais e métodos
Declaração de Ética
O estudo foi aprovado pelo Comitê de Revisão Institucional do Primeiro Hospital de Ensino da Universidade de Medicina Tradicional Chinesa de Tianjin. Todos os participantes assinaram um termo de consentimento livre e esclarecido. Todos os experimentos com animais foram avaliados com o Guia para o Cuidado e Uso de Animais de Laboratório pelos Comitês Internacionais.
Assuntos de estudo
De janeiro de 2016 a março de 2018, foram selecionados os casos de HAS por AI tratados na neurocirurgia do Primeiro Hospital Universitário da Universidade de Tianjin de Medicina Tradicional Chinesa. As amostras patológicas de 75 casos de IA obtidas por microcirurgia foram coletadas e classificadas como grupo IA, incluindo 29 homens e 46 mulheres com idades entre 31 e 55 anos, com idade média de 44,98 ± 6,79 anos. Pacientes com traumatismo cranioencefálico tratados na neurocirurgia ao mesmo tempo no Hospital Universitário da Universidade de Tianjin de Medicina Tradicional Chinesa foram selecionados como grupo controle. Além disso, 75 casos de tecidos normais da arteríola intracraniana foram acumulados por operação traumática ou descompressão interna, incluindo 43 homens e 32 mulheres com idades entre 34-56 anos, com uma idade média de 48,14 ± 8,68 anos. Os pacientes foram excluídos se tivessem histórico de hipertensão, diabetes ou tumores. Não houve diferença marcante em gênero e idade entre o grupo IA e o grupo de controle (ambos P > 0,05).
Tratamento e preservação de amostras
Após a ressecção cirúrgica, algumas das amostras dos dois grupos foram fixadas com formaldeído, desidratadas com álcool gradiente de baixa a alta concentração e incluídas em parafina. Em seguida, as amostras foram fatiadas para coloração por hematoxilina-eosina (HE) e coloração imunohistoquímica. Algumas amostras foram rapidamente colocadas em tanques de nitrogênio líquido e então transferidas para um refrigerador criogênico - 80 ° C para a detecção de análise de western blot e reação em cadeia da polimerase quantitativa de transcrição reversa (RT-qPCR). Algumas amostras foram fixadas com glutaraldeído para observação em microscópio eletrônico, e algumas amostras foram utilizadas para isolamento de CEs.
Observação ao microscópio eletrônico
As amostras foram fixadas com glutaraldeído a 3% e, a seguir, fixadas novamente com tetróxido de ósmio a 1%. As amostras foram desidratadas com acetona, embebidas em Epon812 e fatiadas em seções semi-finas com espessura de 3 μm. Por fim, as amostras foram duplamente tingidas com acetato de uranila e citrato de chumbo e observadas em microscópio eletrônico de transmissão H-600IV (Hitachi, Tóquio, Japão).
Coloração HE
As seções de parafina preparadas foram cozidas a 60 ° C por 30 min. Após as etapas acima terem sido concluídas, as fatias de tecido foram fixadas em xileno, desidratadas com álcool absoluto gradiente e limpas com solução salina tamponada com fosfato (PBS). As fatias de tecido foram tingidas com hematoxilina, tratadas com amônia por alguns segundos, tingidas com eosina por 2 min, desidratadas e depuradas. Em seguida, as fatias de tecido foram gotejadas com goma neutra e seladas com lamínula. Finalmente, um microscópio (Nikon, Tóquio, Japão) foi adotado para observação e gravação.
Coloração imunohistoquímica
O kit de imunohistoquímica foi produzido pela Zymed Laboratories (San Francisco, CA, EUA). As fatias de parafina foram desparafinadas e hidratadas, e as fatias de parafina foram imersas em solução de xileno por 5 min × 3 vezes. As fatias foram colocadas em álcool 100% absoluto por 3 min × 2 vezes e, a seguir, embebidas em álcool 95–75% por 3 min. Após a desparafinação, as fatias foram incubadas com peróxido de hidrogênio a 3% por 15 min para eliminar a atividade da peroxidase endógena. As fatias foram gotejadas com solução de bloqueio e incubadas com solução de trabalho de soro de cabra normal por 15 min, em seguida, sondadas com anticorpo primário contra metaloprotease de matriz (MMP) -9 (5 μg / mL) e fator de crescimento endotelial vascular (VEGF) (1:250 , Abcam, Cambridge, MA, EUA) (PBS para controle negativo (NC)) e incubado por 1–2 h. As fatias foram sondadas novamente com solução de trabalho de anticorpo secundário de biotinilação por 30–60 min. As fatias foram adicionadas com fluido de trabalho de estreptavidina / peroxidase marcado por peroxidase de rábano, gotejado com solução de diaminobenzidina (DAB) recém-preparada, contracorada e bloqueada. A imagem foi conhecida pelo sistema de imagem Nikon SPOT FlexTM. A área de expressão da proteína MMP-9 e VEGF foi avaliada por software de análise quantitativa imunohistoquímica. Cinco campos visuais de alto poder foram detectados aleatoriamente na área de acúmulo de células positivas em cada amostra, e a absorbância média de cada tela foi usada como o valor médio para análise estatística.
Isolamento e cultura de CEs
Os CEs foram isolados de tecidos normais de arteríola intracraniana e tecidos IA e cultivados. O tecido foi cortado em 3 mm 2 fragmentos e incubados durante 25 min em 0,1% de colagenase B / 0,1% de dispase (Roche, Basel, Suíça). O tecido foi descolado, triturado por 2 min por uma pipeta de 2 mL e filtrado por uma peneira de 100 Ìm (BD Biosciences, NJ, EUA) para isolar os CEs. A suspensão celular foi centrifugada e então ressuspensa em meio de cultura MV2 contendo fatores de crescimento e 20% de soro fetal bovino (PromoCell, Heidelberg, Alemanha). Em seguida, as células foram semeadas em placas revestidas com fibronectina (Sigma Aldrich Inc., St. Louis, MO, EUA) com uma densidade de 10 4 células / cm 2 (1 μg / cm 2 ) e cultivado por 1 dia com 5% de CO 2 . No dia seguinte à semeadura, as células foram enxaguadas com PBS para remover as células não ligadas e colocadas em um meio fresco. Ao atingir cerca de 80-100% de confluência, as culturas foram expostas a imunoseparação por Ulex europaeus Agglutinin I (UEA) -coated (Vector Laboratories, Ltd., Peterborough, UK) grânulos (Dynabeads M-450 Tosylactivated, Oxoid, Hampshire, UK) para obter ECs puros. ECs ligados aos grânulos revestidos com lectina foram acumulados com um concentrador de partículas magnéticas, enquanto as células não ligadas foram removidas por meio de lavagem com meio basal duas vezes. Células UEA-positivas foram ressuspensas em meio de cultura e semeadas em placas revestidas com fibronectina para melhorar sua adesão e crescimento. As culturas tornaram-se confluentes em 4–6 dias.
Identificação de ECs
Os ECs foram identificados por coloração imunocitoquímica com um anticorpo CD31 de superfície celular e um antígeno relacionado ao fator FVII. As células foram limpas duas vezes com PBS, fixadas com 4% de paraformaldeído, incubadas com 3% de H 2 O 2 por 10-15 min para eliminar a atividade da peroxidase endógena e, em seguida, incubado com Triton X-100 0,1% por 10 min para células perfuradas. As células foram gotejadas com anticorpo primário específico:Fator VII (1:200), CD31 (1:400, Roche, Basel, Suíça) e incubadas a 4 ° C durante a noite. Em seguida, as células foram gotejadas com imunoglobulina G (1:50) marcada com anticorpo secundário à peroxidase de rábano. As células foram incubadas a 37 ° C por 45 min e desenvolvidas por DAB evitando a luz por 4 min. Em seguida, o desenvolvimento da cor foi encerrado com água destilada e a fotografia observada ao microscópio. As células foram observadas sob o microscópio de fluorescência invertida de diferença de fase, e as células positivas e o número total de células foram contados aleatoriamente em 10 campos visuais. A taxa de células com coloração positiva =(o número de células positivas / o número total de células) × 100%. O grupo NC correspondente foi estabelecido e o anticorpo primário foi substituído por PBS, e as outras etapas foram realizadas como acima.
Agrupamento e transfecção de células
Para estudar os efeitos entre miR-133a-3p e PSAT1 em ECs de IA, os ECs foram agrupados em grupo de controle (ECs vasculares normais sem qualquer transfecção), grupo IA (ECs vasculares de IA sem qualquer transfecção), grupo NC mimetizador (transfectado com miR -133a-3p mímico NC), grupo mímico miR-133a-3p (transfectado com miR-133a-3p mímico), pequeno grupo RNA de interferência (si) -NC (transfectado com si-PSAT1 NC), grupo si-PSAT1 (transfectado com si-PSAT1) e grupo miR-133a-3p mimetizador + superexpressão (oe) -PSAT1 (transfectado com miR-133a-3p mimetizador e oe-PSAT1). Entre eles, mímico NC, mímico miR-133a-3p, si-PSAT1, si-NC e oe-PSAT1 foram concebidos e compostos por GenePharma Co., Ltd. (Xangai, China). A transfecção foi realizada estritamente de acordo com as instruções da Lipofectamine TM Reagente de transfecção 2000 (Thermo Fisher Scientific, MA, EUA).
Citometria de fluxo
O meio na placa de cultura foi descartado e as células foram enxaguadas duas vezes com PBS. As células foram separadas por 0,25% de tripsina, centrifugadas a 800 rpm por 5 min e suspensas com 1 × tampão de ligação, e a densidade celular foi ajustada para 1 × 10 7 células / mL. A suspensão de células (100 μL) foi incubada com 5 μL de iodeto de propídio (PI, 20 μg / mL) e anexina V-FITC por 20 min, depois misturada com 400 μL de tampão de ligação 1 ×. O citômetro de fluxo (classificador de células BD FACSArial I) foi utilizado para detectar a apoptose celular em 1 h. Os resultados foram que o quadrante inferior esquerdo (Q4) no mapa de dispersão mostrou células vivas saudáveis (FITC - / PI - ), o quadrante inferior direito (Q3) como as células apoptóticas iniciais (FITC + / PI - ), e o quadrante superior direito (Q2) eram as células apoptóticas tardias e apoptóticas (FITC + / PI + ); taxa de apoptose =porcentagem de apoptose precoce (Q3) + porcentagem de apoptose tardia (Q2).
Ensaio de 3- (4, 5-Dimetiltiazol-2-Yl) -2, 5-difeniltetrazólio (MTT)
As células foram destacadas com tripsina para preparar a suspensão celular. As células foram contadas sob um microscópio invertido. A concentração de células foi ajustada para 5 × 10 4 células / mL. As células foram semeadas em uma placa de cultura de 96 poços. Após 48 h, as células foram incubadas com 20 μL de solução de MTT por 4 h. O MTT em cada poço foi dissolvido com 150 μL de dimetilsulfóxido. O valor de densidade óptica (OD) de ECs foi medido no comprimento de onda de 570 nm. A taxa de proliferação de CEs foi calculada à luz do valor de DO.
Teste Scratch
As células em cada grupo foram semeadas em uma placa de 24 poços com 2 × 10 5 células / poço. Três poços paralelos foram colocados em cada grupo. Quando atingiu cerca de 90% de confluência, o plano de crescimento celular foi riscado com uma ponta de micropipeta descartável esterilizada de 1 mL; cada poço foi riscado uma vez e o comprimento do risco e a profundidade de cada poço eram consistentes. Após a raspagem, as células flutuantes foram removidas, o meio de cultura foi substituído por um novo e o espaçamento da raspagem foi observado ao microscópio após 24 horas de cultura. A área de cicatrização da ferida arranhada foi enumerada pelo software National Instrument Vision Assistant 8.6. A migração celular =área de cicatrização / área inicial da ferida por arranhão × 100%.
Animais de experiência e estabelecimento de modelos de ratos IA
Oitenta e quatro ratos Sprague-Dawley (SD) com 7 semanas de idade e pesando de 180 a 200 g (Centro de Animais de Laboratório, Academia de Ciências Médicas Militares, Pequim, China) foram selecionados. Os ratos foram alojados no centro experimental de animais. As condições de alimentação foram controladas a 22–25 ° C e 50–60% de umidade com luz natural. Todos os ratos foram alimentados em gaiolas de rato padrão com 4 ratos por gaiola. Os ratos foram alimentados com água potável sanitária urbana e ração comum para ratos. As almofadas foram trocadas a cada 3 dias, e a gaiola foi lavada e esterilizada. Os ratos IA foram modelados de acordo com a referência [15]. O aneurisma roto foi identificado quando os seguintes sintomas ocorreram em ratos [16]:1, diminuição da atividade de comer ou beber realizada por uma perda de peso (cerca de 10% de perda de peso) ao longo de 24 horas; 2, flexão do tronco e membros anteriores durante o levantamento; 3, andar de lado em postura normal; 4, inclinando-se para o lado em repouso, nenhuma atividade espontânea. Os ratos com esses sintomas foram sacrificados 3 meses após a operação. Os tecidos IA foram obtidos durante a operação e perfundidos com PBS, e o corante azul contendo ácido glutâmico foi perfundido na artéria cerebral.
Tratamento e intervenção de ratos IA
Os 84 ratos acima foram separados aleatoriamente em 7 grupos com 12 ratos em cada grupo. Os métodos de tratamento foram os seguintes:grupo normal (nenhuma modelagem foi realizada); Grupo IA (estereotáxica injetada com 100 μL de mistura de PBS e Lipofectamina 2000); imitar grupo NC (injeção estereotáxica com mistura de 100 μL de miR-133a-3p imitar NC e Lipofectamina 2000); grupo miR-133a-3p mimetizador (injeção estereotáxica com 100 μL de mistura de miR-133a-3p mimetizador e Lipofectamine 2000); grupo si-NC (injeção estereotáxica com mistura de 100 μL de si-PSAT1 NC e Lipofectamina 2000); grupo si-PSAT1 (injeção estereotáxica com mistura de 100 μL de si-PSAT1 e Lipofectamina 2000); e miR-133a-3p mimetizador + grupo oe-PSAT1 (injeção estereotáxica com 100 μL de mistura de miR-133a-3p mimetizador e oe-PSAT1 e Lipofectamine 2000). Todas as injeções acima foram realizadas uma vez por dia, e esses ratos foram criados em um laboratório de animais livre de patógenos específicos (SPF) por 12 semanas. Após 12 semanas, os ratos de cada grupo foram anestesiados e a cavidade torácica foi aberta conforme descrito acima. Do ventrículo esquerdo entubado na aorta, o sangue foi liberado cortando a cava. Ao mesmo tempo, 30 mL de solução salina contendo heparina sódica (37 ° C) foram perfundidos através do duto e, em seguida, 10% de poliformaldeído / tampão de fosfato 0,1 M (pH 7,4) foi lentamente injetado no cérebro através do duto. Depois que a perfusão foi fixada, o cérebro foi aberto. O anel arterial na base do crânio foi separado e removido ao microscópio cirúrgico, as alterações dos aneurismas foram observadas ao microscópio e as características patológicas foram pesquisadas. O mímico NC, o mímico miR-133a-3p, si-NC, si-PSAT1 e oe-PSAT1 foram compostos por Shanghai Sangon Biotechnology Co., Ltd. (Shanghai, China).
Detecção de hemodinâmica
A taxa de fluxo de sangue no final da artéria carótida comum esquerda de ratos foi testada antes de 3 dias da operação e 12 semanas após o tratamento de intervenção. O método foi o seguinte:os ratos foram colocados na estrutura do animal da máquina de anestesia para inalação e os parâmetros de fluxo foram ajustados. Depois que os ratos respiraram de forma estável e não houve nenhuma reação óbvia quando a cauda dos ratos foi tocada, os ratos foram fixados na mesa de operação experimental com elástico. O cabelo do pescoço do rato foi raspado com um barbeador elétrico. O detector de ultrassom Doppler colorido foi ligado e a velocidade do fluxo sanguíneo no final da artéria carótida comum esquerda foi medida e os dados registrados depois que a sonda foi esfregada com o agente de acoplamento apropriado. Após a medição, os ratos foram cuidadosamente colocados de volta na gaiola para manter o trato respiratório desobstruído até que os ratos acordassem após a anestesia.
RT-qPCR
O RNA total foi extraído com base no kit de extração de RNA total simples de RNA (TIANGEN Biotechnology Co., Ltd., Pequim, China). O RNA de alta qualidade foi confirmado por análise ultravioleta e eletroforese de desnaturação de formaldeído, e o RNA foi reversamente transcrito em DNA complementar pelo kit de reagentes PrimeScript RT. A reação de PCR foi realizada por SYBR Permix Ex Taq II (Takara, Dalian, Liaoning, China). Os iniciadores de PCR foram concebidos e compostos por Beijing ComWin Biotech Co., Ltd. (Pequim, China) (Tabela 1). U6 foi selecionado como um parâmetro interno para miR-133a-3p, PSAT1, GSK3β, β-catenina, Bax, Bcl-2, Ki-67 e CyclinD1 com gliceraldeído fosfato desidrogenase (GAPDH) como um parâmetro interno. Os dados foram medidos por 2 −ΔΔCt .
Análise de Western Blot
As proteínas totais foram extraídas de células e tecidos, e as amostras de proteínas foram quantificadas pelo Bicinchoninic Acid Protein Assay Kit (Beyotime Institute of Biotechnology, Shanghai, China). As amostras foram misturadas com 1/4 do volume de tampão de amostra 5 × e fervidas por 5 min. O gel de separação a 10% e o gel concentrado a 5% foram selecionados para eletroforese. A membrana foi incubada em leite em pó desnatado a 5% por 60 min. A membrana foi anexada com o anticorpo primário PSAT1 (1:500), GSK3β (1:500), β-catenina (1:5000), Bax (1:1000), Bcl-2 (1:1000), CyclinD1 (1:200), Ki-67 (1:5000), MMP-9 (1 μg / mL), VEGF (1:1000) (todos da Abcam, Cambridge, MA, EUA). Em seguida, a membrana foi incubada com anticorpo secundário (1:2000) por 60 min. A membrana foi imersa na solução de reação de eletroquimioluminescência (Instituto Beyotime de Biotecnologia, Xangai, China) por 1 minuto e, em seguida, coberta com filme plástico após a remoção do fluido. A membrana foi exposta por raio X, e o resultado foi observado após o desenvolvimento e fixação. GAPDH (1:10000, Abcam) foi usado como um controle de carregamento, e a imagem da proteína foi analisada pelo software ImageJ2x.
Ensaio do gene Dual Luciferase Reporter
A relação alvo entre miR-133a-3p e PSAT1 e o sítio de ligação entre miR-133a-3p e PSAT1 3 ′ região não traduzida (3′UTR) foram previstos por um site de bioinformática (https://cm.jefferson.edu/rna22 / Pré-computado /). A sequência da região do promotor PSAT1 3′UTR contendo o sítio de ligação miR-133a-3p foi amplificada e clonada no plasmídeo pGL3-luciferase básica (Takara Bio Inc., Otsu, Shiga, Japão) para construir o plasmídeo de tipo selvagem (WT) ( PSAT1-WT) de PSAT1 3′UTR, enquanto o plasmídeo recombinante PSAT1-MUT mutante (MUT) foi formulado por mutação do sítio de ligação miR-133a-3p em PSAT1-WT com kit de mutação pontual (Takara Bio Inc., Otsu, Shiga , Japão). Os ECs vasculares na fase de crescimento logarítmico foram semeados em uma placa de 96 poços. Quando a confluência está atingindo cerca de 70%, os plasmídeos PSAT1-WT e PSAT1-MUT foram misturados com os plasmídeos mímicos de NC e miR-133a-3p pela Lipofectamine 2000 e co-transfectados em ECs vasculares. As células foram recolhidas e lisadas 48 h após a transfecção e a atividade da luciferase foi verificada por um kit de detecção de luciferase (Promega Corporation, Madison, WI, EUA).
Análise estatística
Todos os dados foram explicados pelo software SPSS 21.0 (IBM Corp., Armonk, NY, EUA). Os dados de enumeração foram indicados por taxa ou porcentagem, e a análise foi determinada pelo teste do qui-quadrado ou teste de Fisher. Os dados de medição submetidos à distribuição normal foram transmitidos por média ± desvio padrão. A comparação entre dois grupos foi conduzida por t teste, enquanto a comparação entre vários grupos foi analisada por análise de variância unilateral (ANOVA) seguida pelo teste post hoc de Tukey. A P valor <0,05 foi considerado significativo.
Resultados
Dados gerais de pacientes com AI
Conforme demonstrado na Tabela 2, foram comparados os dados gerais do grupo IA e do grupo controle. As informações específicas estão listadas na Tabela 2.
A expressão de miR-133a-3p está relacionada ao número e tamanho de IA
Ao analisar a relação entre a expressão de miR-133a-3p e as características clínico-patológicas de IA, foi detalhado na Tabela 3 que, à luz da expressão relativa média de miR-133a-3p em IA, 75 casos de IA foram distribuídos em dois grupos:grupo de alta expressão miR-133a-3p ( n =47) e grupo de expressão baixa miR-133a-3p ( n =28). A relação entre miR-133a-3p e diferentes parâmetros clínico-patológicos foi analisada estatisticamente pelo teste do qui-quadrado ou teste de Fisher. Os resultados mostraram que a expressão do miR-133a-3p não estava relacionada à idade, sexo, forma e posição do aneurisma (todos P > 0,05), mas associado ao número e tamanho do aneurisma (ambos P <0,05).
A expressão de MiR-133a-3p é recusada e a expressão de PSAT1, GSK3β e β-catenina é aumentada em tecidos IA
A expressão de miR-133a-3p em IA foi determinada por RT-qPCR, e os resultados revelaram que em relação aos tecidos de arteríolas intracranianas normais (o grupo de controle), a expressão de miR-133a-3p foi reduzida nos tecidos de IA (o Grupo IA) ( P <0,05) (Fig. 1a). A análise de RT-qPCR e western blot manifestou que a expressão de PSAT1, GSK3β e β-catenina foi aumentada nos tecidos IA em relação àquela nos tecidos de arteríolas intracranianas normais (todos P <0,05) (Fig. 1a – c).
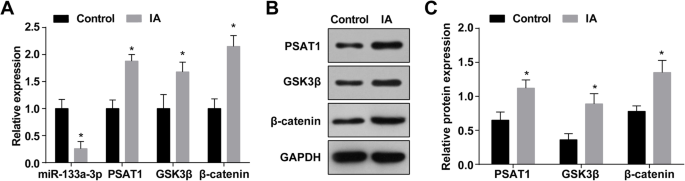
A expressão de MiR-133a-3p está diminuída e a expressão de PSAT1, GSK3β e β-catenina está aumentada em tecidos IA. a Expressão de miR-133a-3p, PSAT1, GSK3β e β-catenina no grupo IA e no grupo normal. b Banda de proteína da expressão de PSAT1, GSK3β e β-catenina. c Expressão da proteína de PSAT1, GSK3β e β-catenina no grupo IA e no grupo normal por ensaio de western blot. n =75, * P <0,05 vs. o grupo de controle. Os dados de medição foram descritos como média ± desvio padrão, e as comparações entre dois grupos foram realizadas por amostra independente t teste
Alterações patológicas de aneurisma e expressão de MMP-9 e VEGF em tecidos IA
Observando diretamente o tecido das arteríolas intracranianas normais e os tecidos IA, foi apresentado que, no grupo controle, os vasos nos tecidos arteriais eram vermelho vivo e nenhuma placa aterosclerótica óbvia e trombo lateral foram encontrados no lúmen. O tumor dos tecidos do aneurisma do grupo IA era principalmente marrom ou vermelho escuro, e a aparência era escrotiforme ou fusiforme, e a textura era principalmente dura. Quando o tumor foi aberto, apareceu placas ateroscleróticas brancas ou vermelho-escuras na parede do tumor de algumas amostras de tumor, que eram achatadas, redondas ou de formato oval. Em algumas amostras de tumor, havia trombo mural na cavidade tumoral e a textura do trombo era macia. A espessura da parede do tumor diminuiu gradualmente a partir do colo do tumor, alguns dos quais tinham apenas uma membrana de fibra fina no topo do tumor, e alguns deles tinham até se rompido. A fenda do aneurisma rompido estava localizada no topo do tumor ou próximo a ele.
A coloração HE mostrou que, sob o microscópio de luz, a espessura da parede dos tecidos normais da arteríola intracraniana era uniforme; a estrutura anatômica das camadas interna, média e externa estava clara e intacta; a morfologia das células em cada camada era normal; o sarcolema das células adjacentes freqüentemente se formou intimamente; e as células inflamatórias da parede eram raras. No grupo IA, as protrusões locais formadas na cavidade vascular lateral distal no topo da bifurcação da artéria intracraniana na parede do aneurisma tornaram-se obtusas e menores, e os CEs locais foram perdidos. Um pequeno número de amostras mostrou uma migração da camada de células do músculo liso para a camada íntima e proliferação de células miogênicas da íntima. Os CEs diminuíram ou até desapareceram. A camada de células endoteliais era composta por células miointimais hiperplásicas e CEs dispostos linearmente, ou por CEs apoptóticos e células sanguíneas aderidas ao lúmen. Seu vacúolo degenerou e apresentou interrupção de continuidade. Alguns deles foram descolados junto com a membrana basal, e as fibras de colágeno da íntima foram aumentadas. A aterosclerose estava alterada e a parede da arteríola estava obviamente mais fina e preenchida com um grande número de tecidos da escada conectiva. Infiltração celular inflamatória e difusão parcial foram observadas em todas as camadas, principalmente nas membranas média e externa. Depósitos de cristais de lipídios e colesterol foram observados em algumas células. Algumas das paredes do tumor foram completamente ou localmente adelgaçadas e expandidas para fora (Fig. 2a, b).
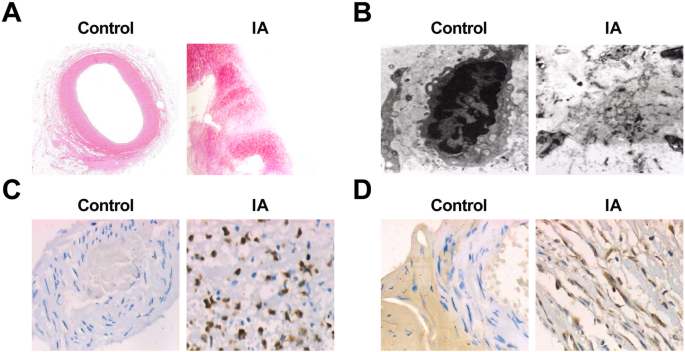
Alterações patológicas do aneurisma e a expressão de MMP-9 e VEGF em IA. a Seções de tecido de arteríolas intracranianas normais no grupo de controle sob coloração HE (10 ×). b Secções de tecido IA tingidas com HE (× 10). c Ultraestrutura de tecidos de arteríolas intracranianas normais no grupo de controle sob um microscópio eletrônico (× 10.000). d Ultraestrutura de tecidos IA sob um microscópio eletrônico (× 10.000). e Expression of MMP-9 in the control group and the IA group by immunohistochemical staining (× 200). f Expression of VEGF in the control group and the IA group by immunohistochemical staining (× 200)
The sections of the normal intracranial arterioles tissues and IA tissues were observed by an electron microscope, and it performed that in normal intracranial arterioles tissues, the matrix fibers of the cerebral vascular wall could be seen clearly, and there was no endothelial injury, cell pyknosis, or degeneration. In the IA tissues, obvious endothelial cell injury, cell pyknosis, or vacuole degeneration were observed, the number of middle smooth muscle cells was declined, most of the nucleus pyknosis was appeared, and chromatin aggregation and apoptotic bodies could be seen. Some cells showed swelling of the mitochondria and disappearance of normal internal structure. The extracellular matrix that formed the cytoskeleton was blurred and showed amorphous floc. There were many fragments in the missing parts of the cells (Fig. 2c, d).
Immunohistochemical staining was utilized to test MMP-9 and VEGF expression, and the results revealed that there was no expression of MMP-9 and VEGF in 75 cases of the control group. It existed 60 cases of positive expression of MMP-9 in the 75 cases of IA samples. MMP-9 positive expression appeared in the inner and the outer membranes of IA wall, but the expression was not uniform. The positive expression was mainly characterized by a brownish yellow cytoplasm. The positive expression of VEGF was 66 cases in 75 cases of IA samples. In the wall of IA, there was a high positive expression in the middle and the outer membranes and a low positive expression in the intima. The positive expression was also mainly characterized by a brownish yellow cytoplasm (Fig. 2e, f). The expression of MMP-9 and VEGF in the two groups is shown in Table 4.
Identification of Vascular ECs
The expression of factor VIII and CD31 in ECs were analyzed by immunohistochemical staining. The results reported that vascular ECs reacted positively to factor VIII and CD31-related antigen antibodies, and the positive rate was 95%. In addition, there were a large number of brown particles in the cytoplasm, and the fifth passage of cells of brown staining was dramatically higher than the primary passage of cells (Fig. 3a, b).
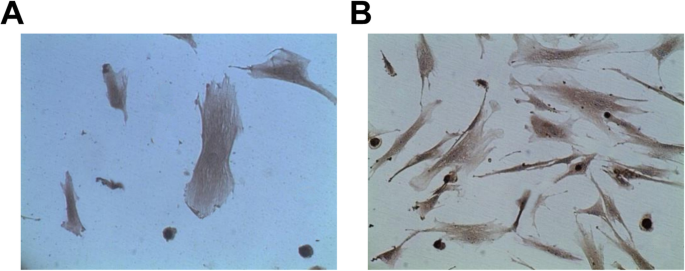
Vascular ECs react positively to FVIII and CD31 related antigen antibodies. a Identification of ECs by CD31. b Identification of ECs by FVII
Upregulation of miR-133a-3p and Downregulation of PSAT1 Suppress Apoptosis and Advance Proliferation and Migration of ECs in IA
Flow cytometry, RT-qPCR, and western blot analysis were adopted for observing the apoptosis and Bax and Bcl-2 expression in ECs of IA after treated with miR-133a-3p mimic or si-PSAT1. It was indicated that compared to the control group, the apoptosis rate of cells and Bax expression was elevated in the IA group and the Bcl-2 expression was decreased (all P <0.05). The cell apoptosis and Bax and Bcl-2 expression in the IA group, mimic NC group, and si-NC group had no significant change (all P> 0.05). By comparison with the si-NC group and mimic NC group, the apoptosis rate of cells in the si-PSAT1 group and miR-133a-3p mimic group was suppressed, the Bax expression was declined, and the Bcl-2 expression was raised (all P <0.05). Versus the miR-133a-3p mimic group, the apoptosis rate and Bax expression were enhanced, and the Bcl-2 expression was reduced in the miR-133a-3p mimic + oe-PSAT1 group (all P <0.05) (Fig. 4a–e).
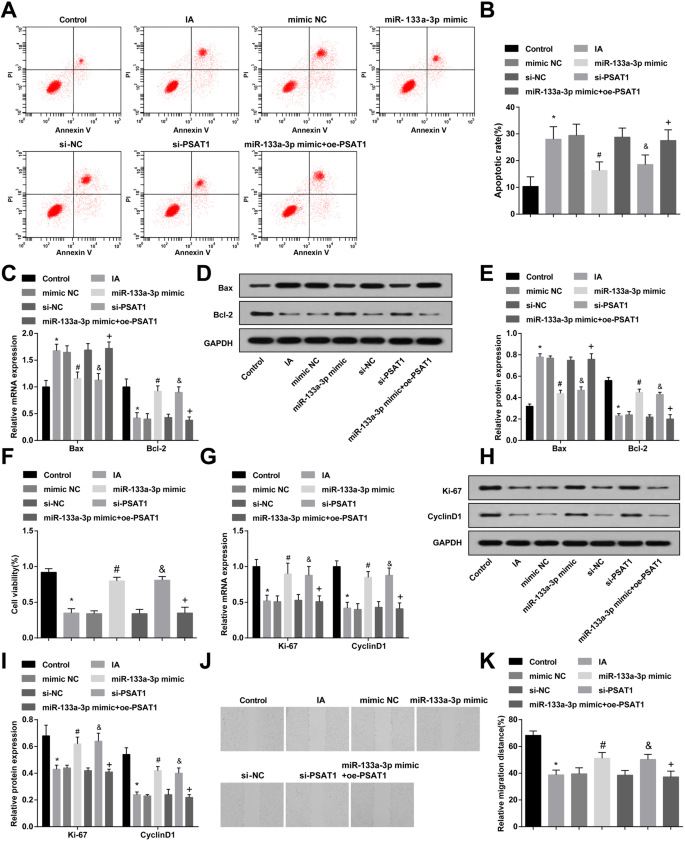
Highly expressed miR-133a-3p and lowly expressed PSAT1 inhibit apoptosis and promote proliferation and migration of IA ECs. a Detection of apoptosis of ECs by flow cytometry. b Detection of apoptosis rate of ECs in each group. c Bax and Bcl-2 expression in ECs detected by RT-qPCR. d Protein band of Bax and Bcl-2 expression. e Bax and Bcl-2 protein expression in ECs detected by western blot analysis. f MTT assay was used to detect proliferation activity of ECs in each group. g RT-qPCR was used to detect the expression of Ki-67 and CyclinD1 in each group of ECs. h Protein band of Ki-67 and CyclinD1 expression. eu Ki-67 and CyclinD1 protein expression in ECs detected by western blot analysis. j Detection of the migration of ECs in each group by scratch test. k Statistical results of endothelial cell migration in each group. N =3, *P <0.05 vs. the control group. #P <0.05 vs. the mimic NC group. &P <0.05 vs. the si-NC group. +P <0.05 vs. the miR-133a-3p mimic group. Measurement data were depicted as mean ± standard deviation; data were assessed by one-way analysis of variance followed by Tukey’s post hoc test
MTT assay, RT-qPCR, and western blot analysis were utilized to observe the proliferation and the expression of Ki-67 and CyclinD1 in ECs of IA after treated with miR-133a-3p mimic or si-PSAT1. It was displayed that in contrast to the control group, the proliferation activity and Ki-67 and CyclinD1 expression were reduced in the IA group (all P <0.05). There was no significant difference in the proliferation activity and Ki-67 and CyclinD1 expression of the IA group, mimic NC group, and si-NC group (all P> 0.05). In relation to the si-NC group and the mimic NC group, the proliferation activity and Ki-67 and CyclinD1 expression were heightened in the si-PSAT1 group and the miR-133a-3p mimic group (all P <0.05). In comparison to the miR-133a-3p mimic group, the proliferation activity and Ki-67 and CyclinD1 expression were reduced in the miR-133a-3p mimic + oe-PSAT1 group (all P <0.05) (Fig. 4f, i).
The migration of ECs in each group after treatment with miR-133a-3p mimic or si-PSAT1 for 24 h was observed by scratch test. It was revealed that the migration of cells in the IA group was inhibited relative to that in the control group (P <0.05). There was no markedly change in cell migration of the IA group, the si-NC group, and the mimic NC group (all P> 0.05). Compared to the si-NC group and the mimic NC group, the cell migration in the si-PSAT1 group and the miR-133a-3p mimic group was elevated (both P <0.05). Versus the miR-133a-3p mimic group, the cell migration was declined in the miR-133a-3p mimic + oe-PSAT1 group (P <0.05) (Fig. 4j, k).
Restored miR-133a-3p and Depleted PSAT1 Reduce PSAT1, GSK3β, and β-Catenin Expression in ECs of IA
RT-qPCR was used to detect miR-133a-3p expression in ECs of IA; it was yielded that compared to the control group, miR-133a-3p expression in the IA group was reduced (P <0.05). miR-133a-3p expression in the IA group, mimic NC group, and si-NC group did not change markedly (P> 0.05). MiR-133a-3p expression in the miR-133a-3p mimic group was enhanced relative to that in the mimic NC group (P <0.05). In contrast with the si-NC group, there was no distinct change in miR-133a-3p expression in the si-PSAT1 group (P> 0.05). Versus the miR-133a-3p mimic group, miR-133a-3p expression was showed no significant difference in the miR-133a-3p mimic + oe-PSAT1 group (P> 0.05) (Fig. 5a).
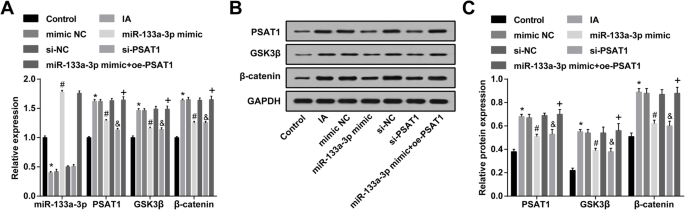
Upregulation of miR-133a-3p and downregulation of PSAT1 decrease PSAT1, GSK3β, and β-catenin expression in ECs of IA. a miR-133a-3p, PSAT1, GSK3β, and β-catenin expression in ECs detected by RT-qPCR. b Protein bands of PSAT1, GSK3β, and β-catenin. c PSAT1, GSK3β, and β-catenin protein expression in ECs in each group detected by western blot analysis. N =3, *P <0.05 vs. the control group. #P <0.05 vs. the mimic NC group. &P <0.05 vs. the si-NC group. +P <0.05 vs. the miR-133a-3p mimic group. Measurement data were depicted as mean ± standard deviation, and data were assessed by one-way analysis of variance followed by Tukey’s post hoc test
The expression of PSAT1, GSK3β, and β-catenin in ECs of IA was tested by western blot analysis and RT-qPCR. It was indicated that in relation to the control group, PSAT1, GSK3β, and β-catenin expression in the IA group was raised (all P <0.05). PSAT1, GSK3β, and β-catenin expression in the IA group, mimic NC group, and si-NC group did not change dramatically (all P> 0.05). PSAT1, GSK3β, and β-catenin expression in the miR-133a-3p mimic group and si-PSAT1 group was degraded relative to that in the mimic NC group and si-NC group (all P <0.05). In relation to the miR-133a-3p mimics group, PSAT1, GSK3β, and β-catenin expression was elevated in the miR-133a-3p mimic + oe-PSAT1 group (all P <0.05) (Fig. 5a–c).
Upregulating miR-133a-3p and Downregulating PSAT1 Alleviate the Pathological Changes of IA Tissues
By testing the hemodynamic changes of rats after modeling, we monitored the blood flow velocity of rats in each group 3 days before operation and 12 weeks after intervention treatment. It was performed that there was no obvious difference in blood flow velocity in each group 3 days before operation (P> 0.05). After 12 weeks of intervention, the blood flow velocity of rats in the IA group depressed relative to that in the normal group (P <0.05). There was no distinct difference in the degree of decrease of blood flow velocity in the IA group, mimic NC group, si-NC group, and miR-133a-3p mimic + oe-PSAT1 group (all P> 0.05). By comparison with the si-NC group and the mimic NC group, the blood flow velocity was heightened in the miR-133a-3p mimic group and the si-PSAT1 group (both P <0.05). In contrast to the miR-133a-3p mimic group, the blood flow velocity was declined in the miR-133a-3p mimic + oe-PSAT1 group (P <0.05) (Fig. 6a).
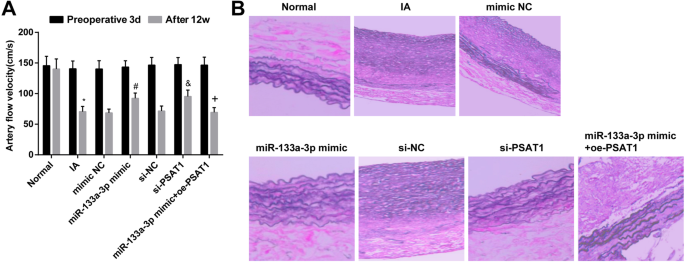
Upregulated miR-133a-3p and downregulated PSAT1 alleviate the pathological changes of IA tissues. a Hemodynamic changes at each time point after successful modeling in rats. b Changes of IA tissue after transfection. n =12, *P <0.05 vs. the normal group. #P <0.05 vs. the mimic NC group. &P <0.05 vs. the si-NC group. +P <0.05 vs. the miR-133a-3p mimic group. Measurement data were depicted as mean ± standard deviation, and data were assessed by one-way analysis of variance followed by Tukey’s post hoc test.
The changes of IA tissues were verified by HE staining. The results displayed that in the normal group, the elastic fibers in the middle layer of intracranial vascular tissue were neat, the normal elastic protein wave-like structure was appeared, and there was no broken and degradation. In relation to the normal group, the lumen of intracranial vascular tissue was enlarged, the normal elastic protein wave-like structure was disappeared, the elastic fiber in the middle layer of local elastic protein vessel was broken, and some of the elastic fibers were completely degraded in the IA group. There was no distinct change in the morphology of IA tissues in the si-NC group, mimic NC group, IA group, and miR-133a-3p mimic + oe-PSAT1 group. In contrast with the si-NC group and the mimic NC group, the wave structure of elastic protein in intracranial vascular tissue of rats in the miR-133a-3p mimic group and the si-PSAT1 group was existed, and the local elastic protein vascular structure was slightly disordered, but there was no fracture and dissolution (Fig. 6b).
Highly Expressed miR-133a-3p and Lowly Expressed PSAT1 Reduce PSAT1, GSK3β, β-Catenin, VEGF, and MMP-9 Expression in IA Tissues in Vivo
The expression of miR-133a-3p in IA tissues in vivo was tested by RT-qPCR, it was suggested that in relation to the normal group, miR-133a-3p expression was declined in the IA group (P <0.05). miR-133a-3p expression in the IA group, mimic NC group, and si-NC group did not change obviously (all P> 0.05). MiR-133a-3p expression in the miR-133a-3p mimic group was elevated relative to that in the mimic NC group (P <0.05). By comparison with the si-NC group, there was no marked change in miR-133a-3p expression in the si-PSAT1 group (P> 0.05). Versus the miR-133a-3p mimic group, miR-133a-3p expression showed no significant difference in the miR-133a-3p mimic + oe-PSAT1 group (P> 0.05) (Fig. 7a).
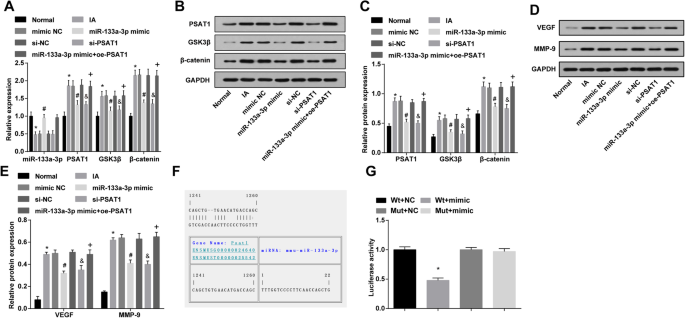
Overexpression of miR-133a-3p and low expression of PSAT1 decrease PSAT1, GSK3β, and β-catenin, VEGF and MMP-9 expression in IA tissues in vivo and PSAT1 is a target gene of miR-133a-3p. a Detection of miR-133a-3p, PSAT1, GSK3β, and β-catenin expression in IA tissues of rats in each group by RT-qPCR. b Protein bands of PSAT1, GSK3β, and β-catenin. c Detection of PSAT1, GSK3β, and β-catenin protein expression in IA tissues of rats in each group by western blot analysis. d Protein bands of VEGF and MMP-9. e Detection of VEGF and MMP-9 protein expression in IA tissues of rats in each group by western blot analysis. f Prediction of the target site of PSAT1 binding to the corresponding miR-133a-3p by Target Scan. g Result of dual luciferase reporter gene assay. a - e , n =12; f - g , N =3, *P <0.05 vs. the normal group/the Wt + NC group. #P <0.05 vs. the mimic NC group. &P <0.05 vs. the si-NC group. +P <0.05 vs. the miR-133a-3p mimic group. Measurement data were depicted as mean ± standard deviation, and data were assessed by one-way analysis of variance followed by Tukey’s post hoc test
The expression of PSAT1, GSK3β, and β-catenin in IA tissues in vivo was tested by western blot analysis and RT-qPCR. It was appeared that in contrast with the normal group, PSAT1, GSK3β, and β-catenin expression in the IA group was increased (all P <0.05). PSAT1, GSK3β, and β-catenin expression in the IA group, mimic NC group, and si-NC group did not change markedly (all P> 0.05). PSAT1, GSK3β, and β-catenin expression in the miR-133a-3p mimic group and si-PSAT1 group was decreased compared with that in the mimic NC group and si-NC group (all P <0.05). Versus the miR-133a-3p mimic group, PSAT1, GSK3β, and β-catenin expression was enhanced in the miR-133a-3p mimic + oe-PSAT1 group (all P <0.05) (Fig. 7a–c).
Western blot analysis was used to verify the VEGF and MMP-9 expression in IA tissues in vivo; the results perceived that by comparison with the normal group, VEGF and MMP-9 expression in the IA group were enhanced (both P <0.05). VEGF and MMP-9 expression in the IA group, mimic NC group, and si-NC group did not change obviously (all P> 0.05). In relation to the mimic NC group and si-NC group, VEGF and MMP-9 expression in the miR-133a-3p mimic group and si-PSAT1 group were declined (all P <0.05). Versus the miR-133a-3p mimic group, VEGF and MMP-9 expression were elevated in the miR-133a-3p mimic + oe-PSAT1 group (all P <0.05) (Fig. 7d, e).
PSAT1 Is a Target Gene of miR-133a-3p
The online prediction software (https://cm.jefferson.edu/rna22/Precomputed/) was utilized to forecast and analyze the target site of PSAT1 binding to the miR-133a-3p, and the sequence of 3′UTR region combined by PSAT1 and miR-133a-3p. In order to prove that the predicted binding site of miR-133a-3p resulted in a change in the luciferase activity, the mutation sequence and the wild sequence of PSAT1 3′UTR deleting miR-133a-3p binding site were devised. Luciferase activity was verified by co-transfection of miR-133a-3p mimic and WT (Wt-miR-133a-3p/PSAT1) or MUT (Mut-miR-133a-3p/PSAT1) recombinant plasmids in vascular ECs. The results revealed that miR-133a-3p mimic had no distinct effect on luciferase activity in the Mut-miR-133a-3p/PSAT1 group (P> 0.05), while the luciferase activity in the Wt-miR-133a-3p/PSAT1 group was markedly declined (P <0.05) (Fig. 7f, g).
Discussion
IA is an abnormal dilatation of the intracranial artery, which weakens the arterial wall through continuously pushing outwards the vascular wall, which results in a higher risk of aneurysm rupture [17]. In a study conducted by Liu et al., it has shown that some miRNAs are involved in modulating the cell proliferation of vascular smooth muscle cells, which is closely associated with IA [18]. Also, a recent study has provided a proof that circulating miRNAs can be used as a new biomarker to assess the possibility of IA occurred in high-risk individuals [19]. It is customarily considered that PSAT1 may be involved in schizophrenia spectrum conditions and alters serine metabolism [20]. The current study was designed to explore the regulatory role of miR-133a-3p modulated vascular endothelial injury and triggered IA through modulating the PSAT1/GSK3β/β-catenin signaling pathway.
In this present study, the relationship among miR-133a-3p expression and clinicopathological features of IA was analyzed, and the results demonstrated that the expression of miR-133a-3p was not related to age, gender, shape, and position of aneurysm but associated with the number and size of aneurysm. Some scholars considered that the shear stress of regional blood flow in the arterial wall induced the induction of monocyte chemoattractant protein-1 (MCP-1) and macrophage inflammatory protein 1α (MIP-1α) expression by fibroblasts and vascular ECs within the vascular wall. The highly reactive chemotactic factors MCP-1 and MIP-1α made an aggregation of macrophagocyte in the vascular wall and mediated inflammatory response, then, induced the excitation of nuclear transcription factor c-Jun and then regulated the activation of activated protein 1 (AP-1), then activated MMP-9 promoter in its structural domain to raise MMP-9 mRNA expression, and finally induced the dissolution of extracellular matrix of vascular wall, causing the formation of intracranial aneurysm [21,22,23]. Saito et al. [24] found that MMP-9 positive cells were mainly from the middle and the outer membranes of the artery macrophages, which certified that MMP-9 expressed by macrophages mediated the degeneration of the arterial wall, leading to the formation of arterial aneurysm. The above studies have indicated that MMP-9 was linked to the formation of IA. The results of our study revealed that MMP-9 was upregulated in IA; thus, we speculated that mR-133a-3p might be involved in the occurrence and development of IA by regulating the PSAT1/GSK3β/β-catenin pathway and further regulating MMP-9. In our study, we found that restoring miR-133a-3p reduced the expression of PSAT1, GSK3β, β-catenin, and MMP-9 in intracranial aneurysm tissues. We will carry out relevant research in the future study to verify our findings.
Our study has provided substantial evidence in relation to the notion that miR-133a-3p expression was decreased and the PSAT1, GSK3β, and β-catenin was elevated in IA. Emerging evidence has suggested that miR-133a-3p plays a suppressive role in different kinds of tumors. Recent study has presented that miR-133a-3p expression was dramatically degraded in breast cancer tissues in contrast with that in non-cancer tissues [25]. Another study has purported that miR-133a-3p expression is declined in advanced prostate cancer (PCa) tissues relative to that in the adjacent normal tissues or benign prostate lesion tissues, especially in bone metastatic PCa tissues [26]. The promoting effect of PSAT1 in other types of diseases are found in some literatures. It is reported that PSAT1 expression was remarkably heightened in non-small cell lung cancer (NSCLC) and forecasted poor clinical outcome of NSCLC patients [27]. Furthermore, PSAT1 is considered as the highest upregulated gene in CRC tumors as well as highly expressed in chemoresistant disease patients [28]. It has been manifested that GSK3β activity was elevated in cancerous tissues [29]. Moreover, the phosphorylation level of GSK3β as well as the expression of nuclear β-catenin are also enhanced, suggesting that GSK3β/β-catenin pathway may be participated in osteopontin regulation [30].
Other results emerged from our data suggested that upregulation of miR-133a-3p and downregulation of PSAT1 suppressed apoptosis and advanced proliferation and migration of IA ECs, reduced VEGF, and MMP-9 expression in IA tissues. It has been suggested previously that the over-expression of miR-133a-3p retrains the invasion, growth, and mitosis of oral squamous cell carcinoma cells by targeting collagen type I alpha 1 (COL1A1) [31]. It is reported that highly expressed miR-133a-3p can repress the propagation of ESCC cells, advance cell apoptosis, and decline the migration and invasion of ESCC cells by targeting COL1A1 [32]. Another study has verified that transient upregulation of miR-133a-3p suppresses the migration, invasion, and growth abilities of gallbladder carcinoma cells through directly targeting recombination signal-binding protein Jκ [33]. In like manner, this study suggests that miR-133a-3p exerts its role in IA through targeting PSAT1. It is displayed that PSAT1 overexpression boosts ESCC cell growth and matrigel invasion in vitro, and injection of mice with ESCC cells with high expression of PSAT1 induces tumor formation in vivo [14]. Other study also has reported that PSAT1 is highly expressed and forecasts a poor clinical outcome of patients, as well as enhances cell tumorigenesis and proliferation in vivo and in vitro [13]. Prior research generally confirms that PSAT1 advances cell cycle progression, proliferation, and tumorigenesis through loss- and gain-of-function experiments [27]. It has been indicated that MMPs are composed of a series of enzymes which cleaves protein substrates on the basis of a conserved mechanism referring activation of an active site-bound water molecule through a Zn 2+ ion [34]. MMP-9 is a distinct protease which push forward an immense influence on many biological processes [35]. A study has contended that MMP-9 is elevated in the aneurysm groups compared to the control group [36]. Vascular endothelial growth factor-A (VEGF-A) is recognized as the key modulator of endovascular differentiation of trophoblast [37]. A study has revealed that silenced PSAT1 expression suppresses VEGF, β-catenin, and GSK3β phosphorylation expression [10].
Conclusion
To briefly conclude, our study confirms our hypothesis that overexpression of miR-133a-3p or downregulation of PSAT1 restrain endothelial cell damage and advance endothelial cell proliferation via inhibiting the GSK3β/β-catenin pathway in IA. These findings provide a new insight in a novel target therapy for IA. These findings underscore the role of miR-133a-3p in IA in relation the PSAT1/GSK3β/β-catenin pathway. However, a conclusion about the effects of miR-133a-3p and PSAT1 cannot be made clearly due to limited known researches on this. It needs to be monitored rigorously and reported appropriately in the future clinical trials.
Disponibilidade de dados e materiais
Not applicable
Abreviações
- miR-133a-3p:
-
MicroRNA-133a-3p
- IA:
-
Intracranial aneurysm
- PSAT1:
-
Phosphoserine aminotransferase 1
- GSK3:
-
β-glycogen synthase kinase 3β
- SAH:
-
Subarachnoid hemorrhage
- MiRNAs:
-
MicroRNAs
- CRC:
-
Colorectal cancer
- ESCC:
-
Esophageal squamous cell carcinoma
- HE:
-
Hematoxylin-eosin
- PBS:
-
Phosphate buffer saline
- MMP:
-
Matrix metalloprotease
- VEGF:
-
Vascular endothelial growth factor
- NC:
-
Negative control
- DAB:
-
Diaminobenzidine
- FBS:
-
Soro fetal bovino
- UEAI:
-
Ulex europaeus agglutinins I
- PI:
-
Propidium iodide
- FITC:
-
V-fluorescein isothiocyanate
- DMSO:
-
Dimetilsulfóxido
- OD:
-
Optical density
- SD:
-
Sprague-Dawley
- SPF:
-
Specific pathogen-free
- GAPDH:
-
Glyceraldehyde phosphate dehydrogenase
- BCA:
-
Bicinchoninic acid
- 3′UTR:
-
3′ Untranslated region
- WT:
-
Wild type
- MUT:
-
Mutant
- ANOVA:
-
Analysis of variance
- NSCLC:
-
Non-small cell lung cancer
- VEGF-A:
-
Vascular endothelial growth factor-A
Nanomateriais
- O amplificador emissor comum
- Preparação de nanopartículas de mPEG-ICA carregadas com ICA e sua aplicação no tratamento de dano celular H9c2 induzido por LPS
- A administração de nanopartículas de artesunato aumenta a eficiência antitumoral ao ativar a apoptose celular mediada por mitocôndrias
- Controlando o crescimento de seleneto de índio de alta uniformidade (In2Se3) Nanofios por meio do processo de recozimento térmico rápido em baixa temperatura
- Síntese fácil de óxido de estanho mesoporoso semelhante a buraco de minhoca via auto-montagem induzida por evaporação e propriedades aprimoradas de detecção de gás
- Projeto e ajuste da função de trabalho do grafeno via tamanho, modificação, defeitos e dopagem:um estudo da teoria do primeiro princípio
- Uma investigação em uma célula solar de silício cristalino com camada de silício preta na parte traseira
- Ajuste do modo de movimento deslizante de nanotubos de carbono por meio de grupos hidroxila
- Absorção de luz efetiva usando grades de pirâmide dupla-face para célula solar de silício de filme fino
- O efeito da apoptose nas células cancerosas do fígado de nanopartículas de ouro modificadas com ácido litocólico



