Progresso da pesquisa de hidrogel termossensível em terapia tumoral
Resumo
Em comparação com as estratégias tradicionais de terapia tumoral, o hidrogel como sistema de reservatório de drogas pode realizar a liberação de drogas sob demanda e a capacidade de penetração nos tecidos profundos. Ele também exibe grande retenção no local do tumor para aumentar a permeabilidade e o efeito de retenção do tratamento do tumor. Isso pode superar significativamente a resistência do medicamento e os efeitos colaterais graves. O hidrogel composto inorgânico / orgânico tem atraído grande atenção devido aos seus efeitos combinados, potencializando os efeitos terapêuticos contra vários tipos de tumores. O hidrogel injetável in situ pode restringir com segurança os medicamentos nos locais das lesões sem vazamento e garantir melhor biossegurança. Além disso, o hidrogel possui macroporos interconectados que podem fornecer espaço suficiente para o transporte de nutrientes, atividade celular e interações célula-célula. A terapia térmica é uma estratégia eficaz para terapia tumoral devido à sua mínima invasividade e alta seletividade. Como a temperatura do local pode ser controlada com precisão e ajuda a evitar os riscos de destruir o sistema imunológico do corpo e eliminar as células normais, a terapia térmica exibe resultados de tratamento significativos. No entanto, quando a temperatura celular atinge aproximadamente 43 ° C, causa a inativação celular a longo prazo. Com base nesses méritos, a formulação de hidrogel termossensível com funções adaptativas mostra excelente eficácia, capacidade ilimitada de penetração no tecido e poucos efeitos colaterais deletérios. Além disso, o hidrogel termossensível tem propriedades físicas únicas sob estímulos externos, que é o sistema de entrega de drogas ideal para liberação sob demanda no tratamento de tumores. Este artigo fará uma revisão do estado do hidrogel termossensível em aplicações clínicas para terapia do câncer.
Introdução
Nos últimos anos, os pesquisadores têm focado sua atenção em biomateriais 3D, uma vez que os macroporos reticulados fornecem espaço suficiente para o transporte de nutrientes, atividade celular e interações célula-célula [1]. Como o carreador ideal de drogas, o hidrogel tem invasividade mínima. Pode formar os formatos desejados para atender aos requisitos de locais de lesões irregulares na terapia do câncer [2]. O hidrogel tradicional é geralmente fabricado por meio de interação física ou ligação química do polímero constituinte, que tem efeitos mínimos em sua função [3]. O hidrogel como sistema de liberação de drogas deve responder a estímulos endógenos / exógenos, garantindo assim a liberação sob demanda do medicamento nos locais da lesão e reduzindo os efeitos colaterais desnecessários nos tecidos normais [4]. O nanomaterial inorgânico funcional incorporado ao hidrogel pode superar significativamente os limites intrínsecos, que tem outras propriedades fascinantes e melhora notavelmente a eficácia terapêutica responsiva a estímulos [5,6,7].
A terapia térmica tem as vantagens de controle da temperatura local e invasividade mínima, que se tornou uma nova abordagem terapêutica após quimioterapia, radioterapia e intervenção cirúrgica no tratamento atual do tumor [8]. Com base na termoterapia mediada por material inorgânico de hidrogel com característica física única sob certos estímulos, é a plataforma de entrega de agente ideal para terapia de dose de droga sob demanda em locais de lesão [9,10,11]. Em comparação com as abordagens terapêuticas sinérgicas tradicionais (quimio / radioterapia, quimioterapia / terapia fotodinâmica e terapia fotodinâmica / fototérmica), o hidrogel termossensível carregado com drogas antitumorais. Isso pode ajudar a penetrar os medicamentos nos tecidos profundos, formar os formatos desejados para preencher os tecidos irregulares e promover a cicatrização de feridas [12]. Além disso, o aquecimento moderado da temperatura pode melhorar os resultados da quimioterapia, melhorando a permeabilidade da citomembrana para aumentar a captação celular de drogas e controlar a liberação da droga do hidrogel. Quando a temperatura celular ultrapassa 41 ° C, ocorre a desnaturação das proteínas e a inativação temporária das células, que perduram por várias horas. Quando a temperatura atinge aproximadamente 43 ° C, causa a inativação celular em longo prazo [13]. Além disso, a injeção de hidrogel termossensível in situ nos locais da lesão pode evitar o risco de acúmulo de drogas no fígado e baço para melhorar os resultados da terapia e garantir uma melhor biossegurança in vivo [14].
O benefício do hidrogel termossensível na clínica pode facilitar a administração, melhorar a eficácia terapêutica na região da lesão e reduzir danos desnecessários aos tecidos normais, melhorando assim a adesão do paciente. Este artigo irá resumir alguns hidrogéis termossensíveis para melhorar o tratamento de doenças e tornar o estado atual do hidrogel em aplicação clínica.
Hipertermia magnética hidrogel
É bem conhecido que a concentração de dopagem de nanopartículas inorgânicas no hidrogel pode inevitavelmente afetar as propriedades intrínsecas do hidrogel, que geralmente apresentam dependência da dose [15]. A alta concentração de agentes aumentaria a eficácia terapêutica. No entanto, desnecessariamente, ele deteriora as propriedades reológicas do hidrogel, resultando em liberação rápida, tratamento descontrolado e efeitos colaterais graves nos tecidos normais [16].
É um desafio fabricar hidrogel de nanopartículas de alto desempenho, que deve equilibrar as propriedades intrínsecas do hidrogel e associar as funções associadas ao processo de carregamento de nanopartículas inorgânicas. Esta contradição é muito óbvia no projeto de hidrogel magnético na termoquimioterapia sinérgica para tratamento pós-cirúrgico altamente eficiente [17]. Essa deficiência seria superada de forma eficaz, fornecendo boas propriedades reológicas e eficiência de aquecimento suficiente. Isso é baseado em glicol-quitosana, poli (etilenoglicol) telecélico difuncional (DT-PEG) e óxido de ferro com domínio de vórtice ferromagnético (FVIOs) como matérias-primas (Fig. 1) [18]. Comparado com o hidrogel magnético tradicional, o hidrogel magnético obtido supera os efeitos colaterais e exibe propriedades reológicas notáveis e alta capacidade de conversão de aquecimento em um campo magnético alternado [19]. Além disso, este hidrogel magnético auto-adaptável regula a droga de uma maneira sustentável a longo prazo. Tem como alvo direto os locais da lesão. A hipertermia magnética pode promover a internalização de um medicamento, eventualmente causa apoptose das células cancerosas e reduz o tamanho do tumor. O hidrogel incorporado com FVIO tem as características de autocura, gelificação rápida e capacidade de autoconfirmação, que podem satisfazer a termoquimioterapia sinérgica e fornecer uma estratégia alternativa para abordar a necessidade clínica não atendida. Este trabalho reforça a promessa potencial para a precisão dos locais de injeção. Aumenta a eficiência da hipertermia magnética para o tratamento de tumor de xenoenxerto.
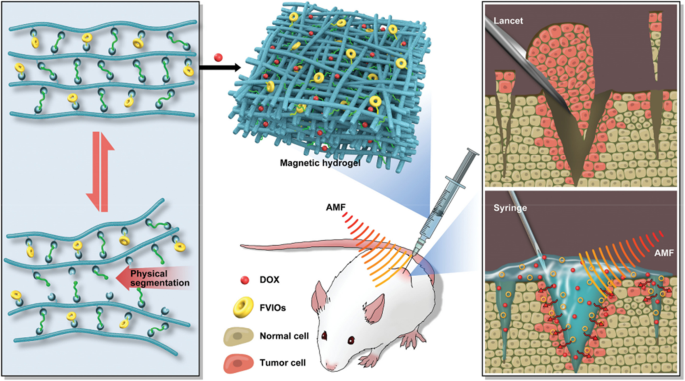
Ilustra hidrogel magnético funcionalizado com FVIO com funções adaptativas ideais para prevenção de recorrência pós-operatória de câncer de mama [18]. Copyright 2019 Adv. Healthcare Mater
Hidrogel de absorção de luz no infravermelho próximo
A terapia fototérmica (PTT) tem atraído grande atenção devido às suas vantagens imbatíveis no tratamento do câncer, incluindo o tratamento de controle e resultados satisfatórios na erradicação do câncer [20,21,22]. Porém, o PTT convencional tem pouca penetração no local das lesões profundas, trazendo efeitos deletérios na terapia. A quimioterapia e a estratégia sinérgica de PTT podem ser uma boa candidata para aumentar a eficácia terapêutica do tumor [23].
Vários materiais fototérmicos têm sido amplamente explorados como transportadores de entrega de drogas ou reagentes de acoplamento para terapia do câncer, incluindo estruturas metal-orgânicas e pontos de carbono [24,25,26,27]. Dentre esses materiais, os pontos de polímero conjugado (Pdots) são biomateriais biocompatíveis, degradáveis, atóxicos e de fácil funcionalização. Estes são pequenos em tamanho e extraordinárias propriedades fotofísicas [28,29,30,31]. Mais importante ainda, os Pdots com fortes propriedades de absorção óptica e fotoestabilidades na janela de luz do infravermelho próximo (NIR) são agentes satisfatórios para PTT e imagem fotoacústica (PAI) [32,33,34]. Iohexol é um agente de contraste eficiente e seguro aprovado pela Food and Drug Administration para imagens de tomografia computadorizada (TC) corporal [35]. No entanto, o tempo de Iohexol para imagens de TC é muito curto e essa deficiência inevitável limita o Iohexol amplamente usado na clínica [26]. Ralar iohexol em hidrogel termossensível à base de Pdots-DOX pode superar com sucesso esta desvantagem de iohexol para melhorar a capacidade de imagens de TC. Isso torna o hidrogel um excelente candidato usado na teranóstica do câncer.
Com base nesses méritos, Men et al. introduziu uma plataforma multifuncional de entrega de drogas Pdots @ hidrogel com boa biodegradabilidade, forte capacidade de absorção de NIR, alta eficiência de conversão fototérmica e liberação de drogas de controle, capacidade de imagem bem satisfeita de CT / PA / fluorescência e resultados terapêuticos de tumor aprimorados (Fig. 2) [ 36]. O sistema de hidrogel Pdots-DOX-iohexol @ mediado por luz NIR obtido exibe fortes efeitos fototérmicos. Alcançou quimioterapia de controle de dose por irradiação de luz NIR de intervalo, penetração superior no tecido e invasão mínima no tratamento do câncer, inibindo assim o crescimento do tumor. Mais importante ainda, a modalidade de nanoengenharia para o Pdots-DOX-iohexol @ hidrogel possui excelente capacidade de imagem CT / FL / PA e alta biocompatibilidade para detecção de câncer. Portanto, o conceito de integração de vários agentes diagnósticos / terapêuticos em um sistema pode ser potencialmente aplicado a várias perspectivas de terapia de doenças na clínica.
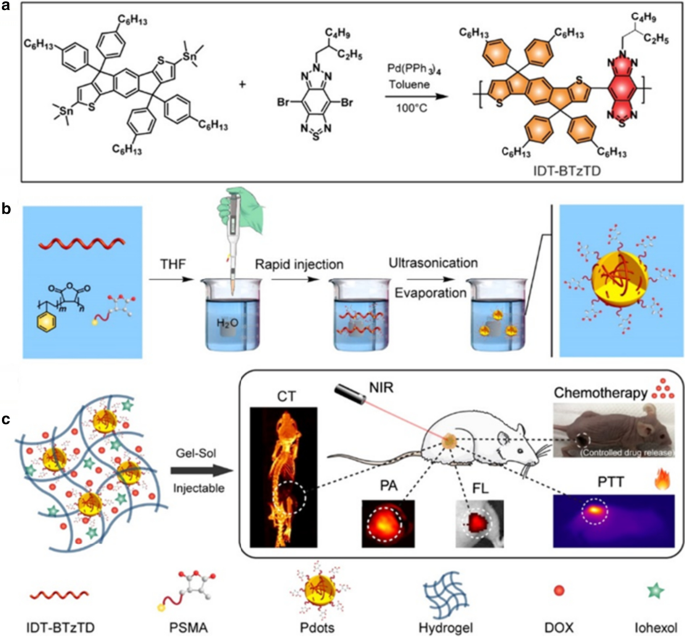
a Esquema da fabricação do polímero conjugado IDT - BTzTD. b Esquema da fabricação de IDT - BTzTD Pdots. b Esquema dos Pdots - DOX - iohexol @ hidrogel para terapia quimio-fototérmica sinérgica guiada por imagem trimodal FL / PA / CT [36]. Copyright 2020 ACS Appl. Mater. Interfaces
Hidrogel bifuncional de efeitos fototérmicos
Atualmente, o tratamento de tumores ósseos depende principalmente de intervenção cirúrgica e abordagens sinérgicas de quimio / radioterapia, o que melhora significativamente a taxa de sobrevida dos pacientes [37]. No entanto, a intervenção cirúrgica sempre causa defeitos ósseos. Ele remove as células tumorais de forma incompleta, tornando os tecidos ósseos difíceis de curar por si próprios, e as células cancerosas residuais se proliferam em vários dias. Portanto, é importante desenvolver um biomaterial com terapia tumoral e simultaneamente promover a regeneração óssea após a cirurgia.
O hidrogel injetável como uma abordagem alternativa promissora pode formar os formatos desejados para preencher os tecidos com defeitos. Seus componentes são muito semelhantes aos tecidos ósseos para melhorar a capacidade osteogênica [38]. O hidrogel injetável aplicado na engenharia de tecido ósseo deve ser lento o suficiente para atender à manipulação cirúrgica e, simultaneamente, ser rápido o suficiente para realizar a estabilidade e a função após a injeção in vivo [39]. Para resolver esses problemas, Luo e seus colegas forneceram um novo hidrogel injetável bifuncional. Este hidrogel usou polidopamina (PDA) para modificar a nano-hidroxiapatita (n-HA) e imobilizar a cisplatina (DDP) para fabricar partículas de PHA-DDP. Em seguida, foram introduzidas partículas de PHA-DDP no Schiff com base no sistema de reação entre a quitosana (CS) e o alginato de sódio oxidado (OSA) (Fig. 3) [40]. A nano-hidroxiapatita (n-HA) desempenhou um papel importante na formação óssea, que é o principal material inorgânico nos tecidos ósseos e é composta por elementos de cálcio e fósforo [41]. O PDA inspirado em mexilhões como o candidato ideal para agentes fototérmicos tem boa biocompatibilidade e biodegradabilidade e tem grupos funcionais abundantes. O PDA inspirado em mexilhões se deposita facilmente em várias substâncias, como o carregamento de drogas antitumorais (cisplatina, DDP) por meio de ligações de hidrogênio ou outras interações [42,43,44]. Além disso, o n-HA foi modificado em PDA para obter o n-HA decorado com PDA (PHA), melhorando a adesão e proliferação celular [45].
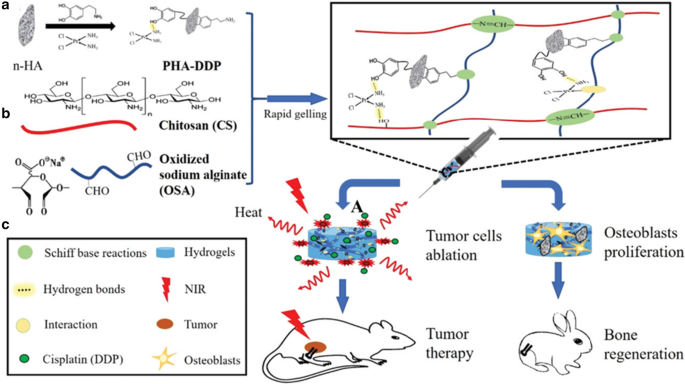
Ilustração esquemática da formação de hidrogéis bifuncionais OSA-CS-PHA-DDP e bioaplicação [40]. Copyright 2019 Macromol. Biosci
O hidrogel injetável OSA-CS-PHA-DDP obtido com sucesso tem excelentes efeitos fototérmicos de PDA de inibir o crescimento do tumor via hipertermia local sob irradiação a laser. Além disso, efeitos fototérmicos suaves podem melhorar a permeabilidade da citomembrança para aumentar a absorção celular de drogas antitumorais. Eles podem destruir as interações de ligações de hidrogênio entre o DDP e o PDA para melhorar a liberação do medicamento e aumentar os efeitos do tratamento do tumor. Mais importante, o abundante grupo funcional de PDA pode promover a proliferação e adesão de células-tronco mesenquimais ósseas e facilitar ainda mais a formação de novo tecido ósseo. Este hidrogel bifuncional integra o tratamento do tumor com a regeneração óssea com base nessas propriedades. Ele mostra uma abordagem promissora para defeitos ósseos relacionados a tumor na clínica.
Hidrogel de agarose responsivo a PTT / PDT
A vascularização do tumor tem pouca integridade da estrutura, resultando em suprimento insuficiente de oxigênio nas regiões do tumor. Condição de hipóxia causando um microambiente tumoral ácido, aumentando a produção de ácido láctico por meio da glicólise anaeróbica [46]. Assim, a hipóxia e o baixo pH são as características comuns do microambiente tumoral, comprometendo gravemente a eficácia terapêutica.
A terapia fototérmica destrói os tecidos tumorais com base na hipertermia local mediada por agentes fototérmicos sob irradiação a laser [47]. Assim, vários tipos de agentes fototérmicos foram desenvolvidos para satisfazer o desempenho do PTT [48]. No entanto, a maioria deles ainda apresenta algumas desvantagens na aplicação clínica, como não degradabilidade, baixa biossegurança e progresso de síntese complexa. O ácido húmico (HA) tem excelente capacidade de conversão fototérmica e imagem fotoacústica (PA), que é extraída da humificação bioquímica de matéria animal e vegetal e tem atraído cada vez mais atenção no PTT [49]. Enquanto isso, a terapia fotodinâmica (PDT) é outra estratégia eficaz para terapia tumoral, utilizando as espécies reativas de oxigênio (ROS) geradas a partir de moléculas de oxigênio na presença de fotossensibilizadores (PS) sob excitação a laser [50]. O cloro e6 tem alto rendimento de produção de ROS e baixa toxicidade no escuro, o que tem sido amplamente utilizado em PDT [51]. Porém, o microambiente de hipóxia intrínseca pode comprometer os efeitos terapêuticos durante o progresso da PDT.
O hidrogel de agarose LMP derrete na temperatura acima de 65 ° C e a transição sol-gel começa na temperatura abaixo de 25 ° C durante o processo de resfriamento, que exibe grande potencial para administração de medicamento sob demanda, regulando com precisão várias temperaturas [7, 52 ] Portanto, o hidrogel de agarose LMP racionalizado e funcionalizado é uma abordagem promissora para obter alta biodisponibilidade do medicamento e melhorar o resultado terapêutico por meio de uma única injeção. Como a Fig. 4 é mostrada, Hou et al. forneceu uma nova abordagem “co-aprisionada” ao incorporar simultaneamente SH, Ce6 e MnO 2 nanopartículas em agarose de baixo ponto de fusão (LMP) e a agarose obtida @ SH / MnO 2 / O hidrogel híbrido Ce6 foi usado com sucesso para melhorar o PTT / PDT por meio da melhora do ambiente de hipóxia tumoral [53]. Em seguida, o hidrogel híbrido sintetizado foi injetado nas áreas tumorais, exibindo excelente biocompatibilidade e biodegradabilidade, principalmente quando foi precisamente introduzido nas mais íntimas. Além disso, MnO 2 e Ce6 pode ser continuamente permeado para o ambiente circundante amaciando e hidrolisando o hidrogel híbrido. Mais importante, o SH, como absorvedor de luz, converte a luz em térmica sob irradiação de laser, portanto, o próprio hidrogel pode ser aplicado no PTT. Além do mais, MnO 2 liberado do hidrogel pode catalisar H 2 excessivo O 2 em tecidos tumorais para gerar oxigênio, o que pode melhorar os resultados do PDT ao ser exposto a laser de 660 nm e atenuar o ambiente de hipóxia tumoral. Esta agarose multifuncional @ SH / MnO 2 / O hidrogel híbrido Ce6 foi injetado nos locais do tumor sem entrar no sistema circulatório, o que ajuda a evitar risco biológico potencial e ser eliminado pelo sistema imunológico do corpo. Portanto, ele atinge “uma injeção, múltiplas terapias” e nos inspira a explorar abordagens baseadas em hidrogel adequadas para várias terapias de doenças na clínica.
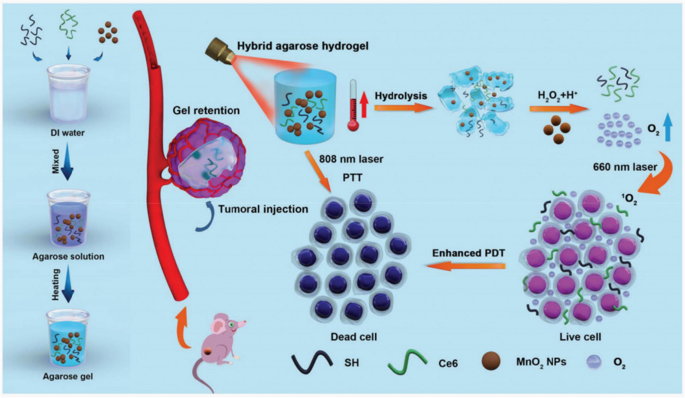
Diagrama esquemático do processo de síntese e princípio de funcionamento da agarose @ SH / MnO 2 / Hidrogel Ce6. A inibição tumoral eficaz foi alcançada por meio de terapia tumoral fotoinduzida intensificada com base no alívio da hipóxia tumoral [53]. Copyright 2020 Biomater Sci
Perspectivas
A terapia térmica tem as vantagens de invasividade mínima e alta seletividade, que é uma estratégia eficaz para terapia tumoral na clínica [54, 55]. Comparada com as abordagens convencionais, a terapia térmica pode controlar com precisão a temperatura local e evitar efetivamente efeitos colaterais desnecessários, como danos a problemas normais e destruição do sistema imunológico do corpo [56]. Quando a temperatura da célula atinge 41 ° C, a célula torna-se temporariamente inativa e causa desnaturação das proteínas, e essa condição dura várias horas. Como a temperatura chega a 43 ° C, pode causar a inativação das células a longo prazo. Embora a terapia térmica tenha alcançado um progresso muito interessante no campo da terapia tumoral, ainda há uma falta de agentes fototérmicos ou transportadores de drogas seguros e eficazes com boa biocompatibilidade e biodegradabilidade.
O hidrogel é o candidato ideal para carreador de fármacos com boa biocompatibilidade e biodegradabilidade no tratamento tumoral atual. A incorporação de inorgânico / orgânico ao hidrogel atraiu amplamente a atenção devido aos seus efeitos cooperativos que podem aumentar os efeitos da terapia contra o tumor. Entre os vários hidrogel responsivo, o hidrogel termossensível pode controlar de forma precisa e contínua a liberação do fármaco por meio do estímulo da temperatura nos tecidos tumorais. Em comparação com os métodos de injeção percutânea e intravenosa, a localização precisa do hidrogel para administração injetada dentro dos agentes tem melhor biossegurança in vivo [57].
Conclusões
Apesar dos méritos significativos do hidrogel, a aplicação clínica tem sido limitada devido à biodistribuição insatisfatória, baixa biocompatibilidade e baixa capacidade de penetração do tumor. Neste artigo, o hidrogel termossensível tem as vantagens de melhor biocompatibilidade, excelente capacidade de inibição de tumor e nenhum efeito colateral desnecessário. Esses méritos promoverão ainda mais sua aplicação na clínica para o tratamento de várias doenças.
Disponibilidade de dados e materiais
Não aplicável.
Abreviações
- DT-PEG:
-
Poli (etilenoglicol) telecélico difuncional
- FVIOs:
-
Óxido de ferro de domínio de vórtice ferromagnético (FVIOs)
- PTT:
-
Terapia fototérmica
- Pdots:
-
Pontos de polímero
- NIR:
-
Próximo ao infravermelho
- PAI:
-
Imagem fotoacústica
- CT:
-
Tomografia computadorizada
- PDA:
-
Polidopamina
- N-HA:
-
Nano-hidroxiapatita (n-HA)
- DDP:
-
Imobilizar cisplatina
- CS:
-
Quitosana (CS)
- OSA:
-
Alginato de sódio oxidado
- DDP:
-
Cisplatina
- HA:
-
Ácido húmico
- HA:
-
Ácido húmico
- PDT:
-
Terapia fotodinâmica
- ROS:
-
Espécies reativas de oxigênio
- PS:
-
Fotossensibilizadores
- LMP:
-
Baixo ponto de fusão
- SH:
-
Humato de sódio
- Ce6:
-
Cloro e6
- MnO 2 :
-
Óxido de manganês
Nanomateriais
- AI apoia projeto de pesquisa de iluminação inteligente
- Acelerando a detecção precoce da doença com nanobiotecnologia
- Pesquisadores da IBM levam para casa o prêmio de inovação para pesquisa de semicondutores
- O Conselho Europeu de Pesquisa financia pesquisas em dispositivos de molécula única por manipulação de átomos
- Nanopartículas para terapia do câncer:progresso e desafios atuais
- Nanorods de ouro revestidos com BSA para terapia fototérmica NIR-II
- Ajustando a toxicidade de espécies reativas de oxigênio na terapia avançada de tumor
- Estruturas Metálicas-Orgânicas de Meio Ambiente como Sistema de Administração de Medicamentos para Terapia de Tumor
- Progresso em nanoestruturas baseadas em óxidos de ferro para aplicações em armazenamento de energia
- Um breve relatório de progresso sobre células solares de perovskita de alta eficiência



