Formação rápida de nanofibra Ag por meio da redução livre de H2 assistida por nanopartículas de Pt de polímeros contendo Ag +
Resumo
Redes unidimensionais baseadas em nanoestruturas de Ag têm atraído atenção significativa como materiais condutores transparentes de próxima geração. Nanofibras de Ag (NFs) com razões de aspecto altas diminuem a densidade numérica necessária para a percolação; portanto, eles formam películas condutoras transparentes qualitativamente superiores. Este estudo relata um novo método para fabricar rapidamente Ag NFs via H 2 assistido por nanopartículas de Pt - redução gratuita de AgNO 3 de estado sólido . Nossos resultados indicaram inicialmente que os polímeros podem ser uma fonte de gás hidrogênio na presença de nanopartículas de Pt; Ag NFs com proporções acima de 10 5 foram obtidos aqui aquecendo AgNO 3 - contendo NFs de polímero em um curto período de tempo e em um ambiente ao ar livre. Nosso método não apenas reduziu com sucesso a quantidade de resíduo de polímero frequentemente encontrado em NFs fiados, mas também criou um sistema de redução autossustentável eficaz que não requer um suprimento externo de gás de redução. As redes Ag NF obtidas foram altamente condutoras e transparentes. Além disso, o mecanismo de formação do Ag NF foi investigado. Demonstramos que o método proposto apresenta alto potencial para a produção de altos rendimentos de Ag NFs de forma simples e rápida.
Introdução
Filmes transparentes condutores são amplamente usados como eletrodos transparentes em telas de cristal líquido, células solares, janelas inteligentes, telas sensíveis ao toque [1,2,3,4,5,6], aquecedores de filme transparente [7,8,9,10,11] e materiais de proteção contra ondas eletromagnéticas [12,13,14]. O mais recente material condutor transparente, óxido de índio e estanho (ITO), tem excelente condutividade e transparência na região visível [15]. No entanto, com a crescente demanda por materiais condutores flexíveis nos últimos anos, a falta de flexibilidade do ITO e a escassez de In levaram à pesquisa de alternativas viáveis. Numerosos candidatos, como nanotubos de carbono [1, 7, 16], grafite [8, 17, 18], polímeros condutores [19, 20] e nanofios metálicos (NWs) [3,4,5, 9,10,11 ], foram amplamente estudados. Em particular, as redes Ag NW [3, 4, 9] parecem ser alternativas promissoras. Além da excelente condutividade, elasticidade e flexibilidade derivadas das propriedades metálicas do Ag, um diâmetro do fio menor que os comprimentos de onda da luz visível garante alta transparência da rede. Em comparação com o ITO, as redes Ag NW têm os benefícios de uma faixa mais ampla de comprimento de onda com transparência excessivamente alta [21]. Essas propriedades podem ser aplicadas a sistemas fotovoltaicos para melhorar a eficiência de conversão de células solares.
Atualmente, a abordagem de poliol [22, 23] é a rota mais promissora para sintetizar Ag NWs. Os Ag NWs sintetizados por este processo baseado em solução podem ser facilmente dispersos para formar uma rede. No entanto, os pontos de contato entre os NWs influenciam fortemente as propriedades das redes. A alta resistência de contato aumenta muito a resistência da folha, enquanto a fraca ligação piora as propriedades mecânicas quando a rede é deformada. Estudos anteriores indicaram que NWs mais longos poderiam produzir filmes condutores transparentes qualitativamente melhores porque dobrar o comprimento dos NWs diminui a densidade numérica necessária para percolação por um fator de quatro [24]. No entanto, os métodos de síntese existentes limitaram o comprimento de Ag NWs a várias dezenas de micrômetros e as relações de aspecto a 10 2 –10 3 ; portanto, os problemas causados pelos pontos de contato permanecem um desafio.
Em comparação com Ag NWs, as nanofibras de Ag (NFs) têm aproximadamente o mesmo tamanho em diâmetro, mas são muito mais longas (geralmente várias dezenas de milímetros) e têm relações de aspecto mais altas que podem chegar a 10 5 –10 6 . No entanto, existem poucos relatos sobre a síntese de Ag NFs. Embora Ag + - contendo NFs precursores podem ser produzidos em massa através de eletrofiação [2] e blow-spinning [25], os desafios enfrentados nesta síntese incluem a redução de Ag + para formar Ag NFs contínuos e a decomposição dos polímeros isolantes residuais provenientes da solução precursora. Recentemente, Lin et al. relataram um método para reduzir o nitrato de prata (AgNO 3 ) NFs por irradiação UV [6]. Uma rede Ag NF em grande escala foi obtida após 3 h de irradiação UV para reduzir Ag + . No entanto, o processo de redução foi relativamente longo e a decomposição de polímeros residuais continuou a ser um problema. No entanto, o efeito catalítico das nanopartículas metálicas [26, 27] nos deu a inspiração de que os polímeros podem ser usados de forma eficaz na presença de nanopartículas metálicas específicas.
Este estudo relata um método simples para a fabricação de Ag NFs. Nossos resultados indicam que os polímeros podem ser uma fonte de gás hidrogênio na presença de nanopartículas de Pt; obtivemos Ag NFs com altas razões de aspecto aquecendo AgNO 3 - contendo NFs de polímero. As redes Ag NF resultantes eram altamente condutoras e transparentes. Este método proposto tem alto potencial para produzir altos rendimentos de Ag NFs de uma maneira simples e rápida.
Experimental
O procedimento experimental para a fabricação das redes Ag NF é ilustrado na Fig. 1. Nanopartículas de Pt foram depositadas em uma superfície de 18 x 18 mm 2 substrato de vidro de microcobertura com uma espessura de 120-170 µm usando um sistema de pulverização catódica de magnetron (SC-701HMCII, SANYU ELECTRON Co., Ltd.) a 23 ° C (Fig. 1a). A pureza do alvo Pt era de 99,99%. A pressão e a taxa de deposição foram 1,5 Pa e 2,5 Å / s a 25 mA, respectivamente, e foram determinadas a fim de se obter uma distribuição homogênea das nanopartículas em uma quantidade precisa. O tempo de deposição foi de 4 s, após o que a espessura do Pt depositado foi de 1 nm. Notavelmente, esta espessura não resultou em um filme de Pt contínuo, mas em ilhas descontínuas (nanopartículas). Este fenômeno é conhecido como estágio inicial de crescimento do filme de metal fino [28,29,30]. Essas nanopartículas de Pt são cruciais na fabricação de Ag NFs, conforme discutido em detalhes nas seções posteriores. Após a deposição das nanopartículas de Pt, um AgNO eletrofiado 3 / álcool polivinílico (PVA) / polivinilpirrolidona (PVP) - rede NF misturada foi depositada no substrato aplicando tensão de 20 kV ao AgNO 3 / Solução aquosa de PVA / PVP por 5 min a uma distância de coleta de 15 cm (Fig. 1b). Uma seringa com agulha de 0,41 mm de diâmetro interno foi conectada a uma microbomba. A taxa de fluxo da microbomba foi ajustada para 0,05 mL / h. A solução bombeada era composta de AgNO 3 (pó, pureza de 99,8%), PVA (grau de polimerização:1500), PVP e água desionizada em uma proporção em peso de 10:8,5:4:100 em% em peso. A viscosidade da solução era de 277 mPa s. Os pesos moleculares de PVA e PVP são 6,6 × 10 4 g / mol e 4 × 10 4 g / mol, respectivamente. O PVA é um material polimérico comum usado para eletrofiação, enquanto o PVP é usado como um agente de proteção molecular. Finalmente, as amostras foram aquecidas ao ar a 250 ° C por 30 min para reduzir o AgNO 3 a Ag na presença de nanopartículas de Pt (Fig. 1c). Os produtos foram medidos usando o método de quatro sondas e analisados por microscopia de força atômica (AFM:Dimension Icon, Bruker Japan Co., Ltd.), difração de raios-X (XRD:Smart Lab, Rigaku Co., Ltd.), campo - microscopia eletrônica de varredura de emissão (FE-SEM:SU-70, HITACHI Co., Ltd.), microscopia eletrônica de transmissão de varredura de campo escuro anular de alto ângulo (HAADF-STEM:Talos F200X, FEI Co., Ltd.), dispersiva de energia Raio-X (EDX) e espectrometria Raman (RAMANtouch, Nanophoton Co., Ltd.).
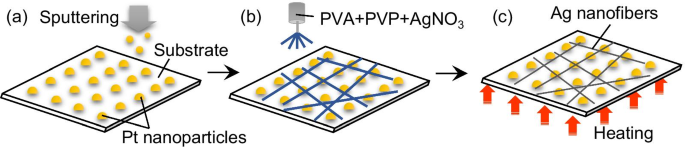
Esquema mostrando o processo de fabricação da rede Ag NF: a Pt sputtering, b eletrofiação do AgNO 3 / PVA / PVP-rede NF mista e c aquecimento ao ar
Resultados e discussão
A Figura 2a mostra os estados das amostras durante o experimento. Cada amostra é marcada com uma linha tracejada. As ilustrações da esquerda para a direita são do substrato de vidro preparado, o vidro após a pulverização catódica de Pt, a rede NF após a eletrofiação, a amostra após o aquecimento (as porções amarelas são eletrodos de Au no tamanho de 18 × 1,5 mm 2 usado para medição de resistência), e um filme de Ag de 15 nm de espessura depositado em um substrato de vidro para referência. A Figura 2b mostra uma imagem AFM de Pt depositada a 2,5 Å / s por 8 s em um substrato de vidro. Foi confirmada a formação de um filme descontínuo com superfície rugosa e grande número de pequenos orifícios com diâmetro de 10–20 nm e profundidade de 2–3 nm. A profundidade foi altamente consistente com a espessura de filme desejada. As nanopartículas de Pt foram distribuídas em clusters com um tamanho médio no plano de 32 nm. Isso pode ser devido ao fato de metais com alto ponto de ebulição possuírem altos valores de supersaturação e pequenos núcleos críticos, e se condensam facilmente [31]. Acreditamos que as nanopartículas de Pt se distribuam de forma mais dispersa quando a espessura do filme é de 1 nm. Após o aquecimento, a amostra apresenta alta transparência na região visível (Fig. 2c). A longa rede percolada por NF é claramente ilustrada na visão ampliada da micrografia SEM (Fig. 2c). A fração de área da rede, medida pela aplicação de limites à micrografia SEM usando software de análise de imagem (WinROOF2015, MITANI Corporation), é de aproximadamente 47%. A análise HAADF-STEM (Fig. 2d) demonstra que os NFs tinham várias dezenas de nanômetros de diâmetro e tinham uma microestrutura policristalina. Os NFs eletrofiados abrangeram o substrato; portanto, seu comprimento era de aproximadamente 18 mm ou mais. Portanto, a relação de aspecto das NFs presentes atingiu uma ordem de 10 5 ou ainda maior. Todos os picos no padrão de XRD (Fig. 2e) estão em boa concordância com aqueles da estrutura cúbica centrada na face de Ag, indicando que Ag NFs foram obtidos com sucesso e finamente cristalizados. Os resultados da análise de EDX (Fig. 2f – i) indicam que a rede era composta por Ag NFs, sem distribuição relacionada a C nas NFs. Além disso, Pt não foi detectado, provavelmente porque estava presente em apenas uma pequena quantidade. Os elementos detectados de Si, O, Na, Al e K (Fig. 2i) originaram-se do substrato de vidro e, portanto, podem ser ignorados. As curvas de corrente-tensão medidas (Fig. 2j) demonstram que as redes Ag NF formadas têm propriedades metálicas e suas resistências de folha são tão baixas quanto várias dezenas de Ω / sq, que é comparável àquelas de ITOs disponíveis comercialmente. A presente rede Ag NF pode ser facilmente aplicada a um substrato de filme como um eletrodo transparente flexível (por exemplo, consulte o arquivo adicional 1:Fig. S1).
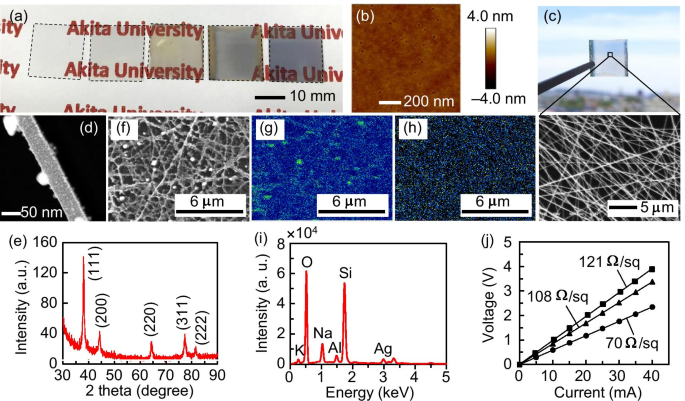
a Estados dos espécimes durante o experimento. b Imagem AFM de Pt pulverizada em um substrato de vidro. c Imagens ópticas e FE-SEM da amostra após o aquecimento. d Imagem HAADF-STEM de Ag NF. e Padrão de XRD de Ag NF. Resultados da análise EDX da rede Ag NF: f Imagem SEM, g Ag, e h Mapeamentos de distribuição C e i análise qualitativa da área indicada em ( f ) j Curvas de corrente-tensão das amostras medidas usando o método de quatro sondas
Como resultado, o papel das nanopartículas de Pt e a importância do aquecimento no ar, ao invés do vácuo, foram questionados. Portanto, esses aspectos são discutidos nos próximos parágrafos.
O objetivo inicial da deposição de nanopartículas de Pt era melhorar o processo de eletrofiação para que mais AgNO 3 / PVA / PVP NFs podem ser depositados no substrato de vidro isolado. Curiosamente, quando aquecemos o AgNO 3 / PVA / PVP NFs com nanopartículas de Pt a 250 ° C, obtivemos Ag NFs. Os resultados da análise de XRD e EDX (Fig. 2e-i) apoiam fortemente esta nova descoberta. É altamente improvável que o Ag tenha sido produzido pela decomposição térmica do AgNO 3 após aquecimento a 250 ° C devido à decomposição do AgNO 3 ocorre em temperaturas acima de 500 ° C [32]. Portanto, é mais provável que o Ag tenha sido produzido a partir da redução do hidrogênio do AgNO 3 . Além disso, o gás hidrogênio provavelmente veio do PVA e do PVP usados nos experimentos. No entanto, até o momento, não há relatos de que o gás hidrogênio possa ser gerado diretamente a partir da decomposição térmica do PVA ou PVP. A maioria dos relatórios indicou que o principal produto de decomposição do PVA a aproximadamente 200 ° C é H 2 O [33,34,35,36]. Postulamos que as nanopartículas de Pt são o fator decisivo para o processo de redução. O Pt tem sido objeto de muitas pesquisas e é bem conhecido como um catalisador de reações químicas.
A discussão acima é resumida pelas Eqs. (1) e (2) abaixo.
$$ {\ left [{\ mathrm {CH}} _ {2} \ mathrm {CHOH} \ right]} _ {n} \ begin {array} {c} \ stackrel {\ mathrm {Pt}} {\ to } \\ {\ mathrm {in ~ air}} \ end {array} {\ mathrm {CO}} _ {2} + {\ mathrm {H}} _ {2} + {\ mathrm {H}} _ { 2} \ mathrm {O} $$ (1)
e
$$ {\ mathrm {H}} _ {2} + {\ mathrm {Ag}} ^ {+} \ to \ mathrm {Ag} + {\ mathrm {H}} ^ {+}. $$ (2)
Os principais componentes do PVA ([CH 2 CHOH] n ) e PVP ([C 6 H 9 NÃO] n ) são semelhantes e o PVA é responsável pela maior parte da solução de eletrofiação; portanto, nos concentramos no PVA na discussão a seguir. As reações mostradas nas Eqs. (1) e (2) foram propostas com base em nossa especulação porque é significativamente desafiador provar que o PVA produz gás hidrogênio via decomposição térmica na presença de nanopartículas de Pt. No entanto, de acordo com nossos resultados experimentais e outras considerações abrangentes, essas reações parecem mais prováveis de ter ocorrido. Para verificar o efeito catalítico das nanopartículas de Pt, outras nanopartículas metálicas também foram depositadas (semelhante ao processo mostrado na Fig. 1a), e os experimentos foram repetidos. Conforme mostrado na Tabela 1, nanopartículas de Ag e Au foram depositadas em substratos de vidro. Suas espessuras foram restritas a 1 nm, que é um tamanho semelhante ao das nanopartículas de Pt. Substratos de vidro sem qualquer deposição de nanopartículas também foram preparados para comparação. Para garantir a reprodutibilidade dos resultados experimentais, pelo menos quatro corpos-de-prova foram preparados para cada tipo de nanopartícula metálica. Essas peças de teste foram então submetidas a eletrofiação (Fig. 1b) e aquecimento (Fig. 1c) nas mesmas condições que as usadas para as nanopartículas de Pt. A comparação das resistências da folha antes e depois do aquecimento demonstra que apenas as resistências da folha das peças de teste com nanopartículas de Pt foram grandemente reduzidas de serem isoladas para medir várias dezenas a centenas de Ω / sq. Este resultado implica que o AgNO 3 componente alterado para Ag. Portanto, concluímos que as nanopartículas de Pt desempenham um papel crítico no sucesso da fabricação de Ag NFs. Devido à presença de nanopartículas de Pt, os materiais poliméricos isolantes (PVA e PVP) não só se decompõem termicamente, mas também produzem gás hidrogênio de forma eficaz que pode reduzir o AgNO 3 .
A redução de íons metálicos usando gases redutores é geralmente realizada sob vácuo. Portanto, o tamanho da amostra é limitado pela câmara de vácuo e uma quantidade significativa de tempo é gasta criando o vácuo. Felizmente, nosso método não requer um ambiente de vácuo porque descobrimos que um ambiente ao ar livre é mais adequado para a fabricação de Ag NFs altamente condutores. Por exemplo, a Fig. 3a mostra uma amostra (preparada pelos mesmos processos mostrados na Fig. 1a, b) após aquecimento sob vácuo (usando uma taxa de fluxo de 200 sccm de gás Ar e uma pressão de 130 Pa a 250 ° C por 30 min ) Ao contrário dos espécimes aquecidos ao ar, as peças aquecidas sob vácuo eram translúcidas e de cor marrom claro. Notavelmente, suas resistências de folha eram tão altas quanto vários milhares de Ω / sq, o que é uma a duas ordens de magnitude maior do que aquelas aquecidas no ar. Os resultados da análise de EDX (Fig. 3b-e) indicam que uma quantidade significativa de C está presente nos NFs, enquanto o Si, O, Na e Al detectados (Fig. 3e) vieram do substrato de vidro e, portanto, foram ignorados. A análise espectroscópica Raman (Fig. 3f) demonstra que esses átomos de carbono têm uma estrutura amorfa. Dois picos Raman característicos em aproximadamente 1325 e 1583 cm −1 foram detectados, que são consistentes com os picos relatados em outro lugar [6]. Além disso, conforme mostrado na Fig. 3f, um aumento na linha de base do espectro Raman foi detectado devido à fluorescência, o que implica uma alta possibilidade de resíduos orgânicos (polímeros). Portanto, os corpos de prova aquecidos sob vácuo apresentaram resistências de folha muito grandes.
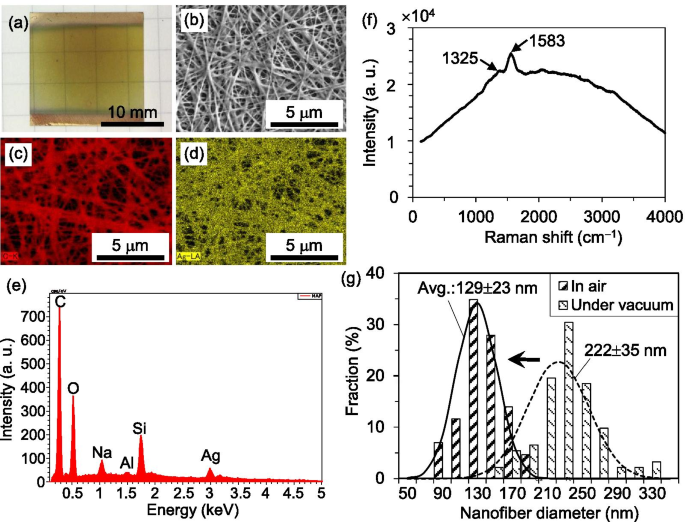
Amostra após aquecimento sob vácuo com a imagem ótica e resultados de análise EDX: b SEM, c C e d Mapeamentos de distribuição de Ag; e análise qualitativa da área indicada em ( b ); e f o espectro Raman. g Histogramas do diâmetro NF após aquecimento ao ar e sob vácuo
A Figura 3g exibe os histogramas do diâmetro NF após aquecimento ao ar e sob vácuo. Os diâmetros foram medidos usando a função de medição de SEM. Sob cada condição de aquecimento, mais de 40 NFs foram selecionados aleatoriamente para as observações SEM (com ampliação de 5000 ×) e medições subsequentes. Em comparação com aqueles aquecidos sob vácuo, o diâmetro médio dos NFs após o aquecimento ao ar é aproximadamente 100 nm mais fino. Isso pode ser o resultado da oxidação de carbonos amorfos e sua liberação através da fase de vapor (CO 2 ) A remoção de carbonos amorfos dos NFs talvez tenha reduzido muito as resistências da folha. A discussão acima pode ser explicada pela seguinte reação química:
$$ {\ left [{\ mathrm {CH}} _ {2} \ mathrm {CHOH} \ right]} _ {n} \ begin {array} {c} \ stackrel {\ mathrm {Pt}} {\ to } \\ {\ mathrm {no ~ vácuo}} \ end {array} \ mathrm {C} + {\ mathrm {H}} _ {2} + {\ mathrm {H}} _ {2} \ mathrm {O }. $$ (3)
O produto preferido da decomposição térmica do PVA é H 2 O durante o aquecimento sob vácuo; portanto, C não pode ser oxidado por oxigênio, e carbonos amorfos residuais são produzidos. Em contraste, conforme expresso na Eq. (1), a presença de ar durante o aquecimento fornece o oxigênio necessário para a oxidação dos carbonos. Portanto, um ambiente ao ar livre é mais adequado para a fabricação de Ag NFs altamente condutores.
Além de fornecer um método de fabricação simples, consideramos se o método proposto poderia ser mais eficiente e com economia de energia. A Figura 4 mostra as medições in situ da resistência da folha. A amostra foi pré-aquecida sob vácuo (usando uma taxa de fluxo de 200 sccm de gás Ar e pressão de 130 Pa a 250 ° C por 30 min) de modo que sua resistência inicial da folha fosse de aproximadamente 6340 Ω / sq. A amostra foi então aquecida de 150 a 250 ° C ao ar. O perfil da temperatura de aquecimento é representado na Fig. 4 pela linha contínua, enquanto a resistência da folha é representada pela linha pontilhada. A resistência da folha aumentou quase linearmente conforme a amostra foi aquecida de 150 a 200 ° C por causa do aumento na resistividade elétrica conforme a temperatura aumentou. No entanto, a 200 ° C, a resistência da folha começou a diminuir rapidamente, embora a temperatura de aquecimento continuasse a aumentar. Após aproximadamente 55 min, a resistência da folha caiu de 6420 Ω / sq para aproximadamente 400 Ω / sq e, em seguida, a tendência decrescente começou a saturar. Este fenômeno pode ter sido causado pela oxidação de carbonos amorfos e sua liberação, como discutido acima. Portanto, a temperatura de aquecimento pode ser reduzida para aproximadamente 200 ° C para a fabricação de Ag NFs. Esse progresso não é apenas útil para economizar energia, mas também amplia a gama de opções para substratos resistentes ao calor.
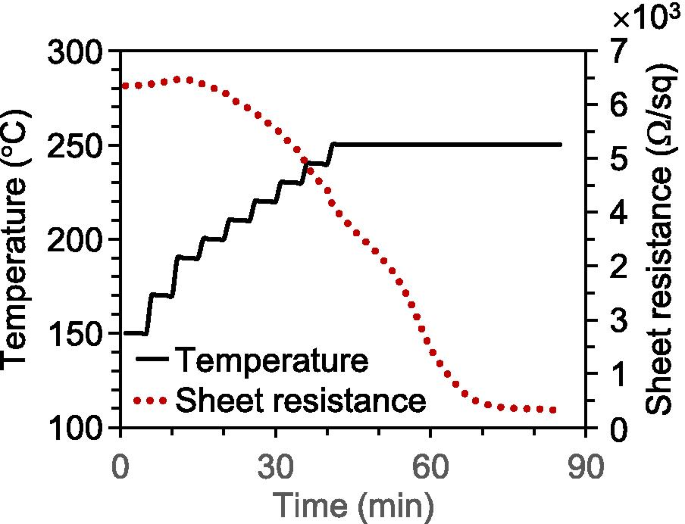
Variação na resistência da folha com temperatura e tempo de aquecimento
Conclusões
Em resumo, um método simples para fabricar Ag NFs via redução assistida por nanopartículas de Pt de AgNO 3 foi proposto, e o mecanismo foi investigado. Embora o método precise ser melhorado ainda mais, ele tem alto potencial para produzir altos rendimentos de Ag NFs com altas taxas de aspecto e filmes transparentes condutores de uma maneira simples, rápida e econômica. Nanopartículas de Pt podem ser depositadas em um substrato por deposição a vácuo ou usando um líquido de dispersão de Pt comercial. Em teoria, a maioria dos sais de prata, como cloreto de prata, sulfeto de prata e fluoreto de prata, podem ser reduzidos; portanto, a fonte de Ag + não está limitado a AgNO 3 . Além disso, prevemos que os outros metais do grupo da platina, como Pd e Rh, podem produzir o mesmo efeito catalítico do Pt por causa de suas propriedades químicas semelhantes.
Disponibilidade de dados e materiais
Todos os dados gerados ou analisados durante este estudo estão incluídos neste artigo e seu arquivo de informações complementares.
Abreviações
- AFM:
-
Força atômica microscópica
- AgNO 3 :
-
Nitrato de prata
- EDX:
-
Raio-X de energia dispersiva
- FE-SEM:
-
Microscopia eletrônica de varredura por emissão de campo
- HAADF-STEM:
-
Microscopia eletrônica de transmissão de varredura de campo escuro anular de alto ângulo
- ITO:
-
Óxido de índio estanho
- NW:
-
Nanowire
- NF:
-
Nanofibra
- PVA:
-
Álcool polivinílico
- PVP:
-
Polivinilpirrolidona
- XRD:
-
Difração de raios X
Nanomateriais
- Controle de Polarização Terahertz Completo com Largura de Banda Ampliada via Metasurfaces Dielétricos
- Influência das Condições de Formação de Nanomateriais Pd / SnO2 nas Propriedades dos Sensores de Hidrogênio
- Evolução morfológica de Si com padrão de poço (001) Substratos impulsionados pela redução de energia de superfície
- Controlando o crescimento de seleneto de índio de alta uniformidade (In2Se3) Nanofios por meio do processo de recozimento térmico rápido em baixa temperatura
- Fabricação e caracterização de novo composto de suporte de catalisador anódico de nanofibra de carbono Tio2 para célula de combustível de metanol direto via método de eletrofiação
- Eficácia antitumoral aprimorada e farmacocinética de Bufalin via lipossomas PEGuilados
- Redução aprimorada da condutividade do próton e da permeabilidade do metanol por meio da biomembrana de óxido de grafeno sulfonado eletrolítico de alginato de sódio
- Reação de redução de oxigênio no nanocatalisador de PtCo:envenenamento por ânion (Bi) sulfato
- Ajuste do modo de movimento deslizante de nanotubos de carbono por meio de grupos hidroxila
- Síntese in situ de nanopartículas bimetálicas de cobre e tungstênio via plasma térmico reativo de radiofrequência (RF)



