Óxido de grafeno funcionalizado com quitosana assistido por micro-ondas como nanossistema de administração intracelular controlada de drogas para atividade antitumoral sinérgica
Resumo
Para alcançar uma melhor eficácia antitumoral, é urgente melhorar a eficiência da administração de drogas anticâncer no direcionamento das células cancerosas. Neste trabalho, nanofolhas de óxido de grafeno funcionalizado com quitosana (ChrGO) foram fabricadas por meio de redução assistida por micro-ondas, as quais foram empregadas no nanossistema de entrega intracelular de fármaco anticâncer em células de câncer de mama. A pesquisa de carga e liberação de drogas indicou que a adriamicina pode ser eficientemente carregada e liberada a partir das nanofolhas ChrGO. Menor liberação de droga durante a entrega e melhor biocompatibilidade de ChrGO / adriamicina melhora significativamente sua segurança e eficácia terapêutica em células BT-474 com superexpressão de HER2. Além disso, ChrGO / adriamicina em combinação com trastuzumabe exibiu atividade antitumoral sinérgica em células BT-474, que demonstrou eficácia terapêutica superior em comparação com cada medicamento sozinho. As células tratadas com trastuzumabe (5 μg / mL) ou ChrGO / adriamicina equivalente (5 μg / mL), cada uma provocou 54,5% e 59,5% de morte celular, respectivamente, enquanto o tratamento combinado com trastuzumabe e ChrGO / adriamicina resultou em uma dramática célula de 88,5% morte. A terapia de duplo direcionamento apresentou maior apoptose, indicando eficácia terapêutica superior devido à presença de diferentes mecanismos de ação. O tratamento combinado de ChrGO / adriamicina e trastuzumabe em células BT-474 induziu a parada do ciclo celular e apoptose, o que acabou levando à morte de células cancerosas aumentadas. Este trabalho forneceu uma fabricação fácil assistida por microondas de ChrGO como um nanossistema de distribuição intracelular de drogas controlada e direcionada, que se espera seja uma nova terapia promissora para o tratamento de células de câncer de mama com superexpressão de HER2.
Introdução
O receptor HER2 é um membro da família do receptor EGFR que medeia o crescimento e a diferenciação das células cancerígenas e é altamente superexpresso em 20-30% dos cânceres de mama humanos, levando a um fenótipo de tumor metastático e prognóstico ruim [1]. HER2 também é superexpresso em aproximadamente 20% dos cânceres gástricos humanos [2]. O trastuzumabe, um anticorpo terapêutico monoclonal humanizado, demonstra vantagens terapêuticas promissoras como terapia de primeira linha em pacientes com câncer de mama com superexpressão de HER2 [3]. No entanto, a taxa de resposta geral ao trastuzumabe permanece modesta:15-30% quando tratado como terapia única e 50-75% quando usado em tratamento combinado com drogas quimioterápicas [4]. Entre os pacientes que respondem ao trastuzumabe, a maioria deles eventualmente progride após a resposta inicial e adquire resistência ao longo do tempo após o tratamento contínuo [5]. Assim, é essencial e necessário desenvolver novas terapias adicionais para pacientes com superexpressão de HER2 para melhorar as taxas de sobrevida geral.
As antraciclinas ainda funcionam como a espinha dorsal do tratamento do câncer. Para os agentes antraciclínicos, o inibidor da topoisomerase II adriamicina tem sido amplamente utilizado para tratar muitos cânceres, como câncer de mama, pulmão e linfóide [6]. A adriamicina tem eficácia efetiva no tratamento de pacientes com câncer de mama com superexpressão de HER2, devido à proximidade entre o gene HER2 e o gene topoisomerase II [7]. Apesar do benefício clínico observado com terapias baseadas em antraciclinas no câncer de mama, a disfunção cardíaca restringiu aplicações terapêuticas mais expansivas. No ensaio clínico, o trastuzumabe em combinação com adriamicina demonstrou eficácia significativa, enquanto a cardiotoxicidade altamente dependente da dose foi um problema que deve ser resolvido [8]. A liberação sustentada de agentes quimioterápicos no tecido do câncer alvo é reconhecida como uma boa solução para reduzir as doses necessárias para a eficácia terapêutica e melhorar os perfis de segurança [9]. Para alcançar uma melhor eficácia antitumoral, mas menos efeitos colaterais, há uma necessidade urgente de melhorar a eficiência da administração de drogas anticâncer visando células cancerosas.
Os nanomateriais à base de óxido de grafeno (GO) têm demonstrado grande promessa na distribuição controlada de agentes quimioterápicos [10]. Numerosos estudos têm demonstrado que a toxicidade do GO está associada à sua funcionalização de superfície [11]. Recentemente, agentes ambientalmente amigáveis, como quitosana e PEG, foram relatados para funcionalizar o GO com grupo funcional de superfície menos tóxico [12, 13]. A estabilidade coloidal das nanopartículas em meios biológicos é crucial para o desenvolvimento de um sistema de entrega de drogas eficaz e seguro para uso clínico [14]. Nanofolhas funcionalizadas GO ganharam grande atenção em aplicações biomédicas devido às suas propriedades, como biocompatibilidade e estabilidade. Como um excelente candidato para biomaterial à base de grafeno, a estabilidade coloidal de GO ou rGO é importante para controlar o desempenho de carreadores de drogas. O GO funcionalizado com poli (etilenoglicol) exibiu uma propriedade coloidal melhorada em meios de cultura de células [15]. P. Khanra relatou um novo método para a redução simultânea e bio-funcionalização do GO usando células de levedura como biocatalisador redutor [16, 17]. Avinav G apresentou uma biossíntese de um vaso único de GO utilizando extrato de levedura durante um processo de autoclave [18]. O tratamento de sonicação de folhas GO de tamanho micrométrico por horas resultou em nanofolhas GO, que mostraram maior estabilidade coloidal em comparação com GO de tamanho micrométrico regular [19]. Embora os estudos anteriores tenham demonstrado o alto potencial do GO para biomateriais, as nanofolhas bio-funcionalizadas de GO com quitosana por redução assistida por micro-ondas usando extrato de levedura livre de células não foram estudadas até agora. Para este propósito, uma nova estrutura de óxido de grafeno funcionalizado com quitosana (ChrGO) foi construída por um sistema de síntese de microondas fácil que utiliza extrato de levedura como redutor. Além disso, a funcionalização efetiva do GO com quitosana biocompatível fornece uma plataforma potencial para o carregamento e entrega eficiente do fármaco. Os estudos de carregamento e liberação de drogas demonstraram que a adriamicina foi carregada e liberada com eficiência nas nanofolhas ChrGO. Os compósitos ChrGO / adriamicina mostraram atividade antitumoral significativa de maneira dependente da concentração. Particularmente, o tratamento combinacional com ChrGO / adriamicina e trastuzumab resultou em um efeito de inibição do crescimento aumentado em células BT-474 em comparação com a monoterapia. A eficácia antitumoral sinérgica desses agentes foi revelada ser mediada pela interrupção do ciclo celular e apoptose, o que acabou levando à morte das células cancerosas. Este trabalho relatou uma rota promissora para a produção rápida e econômica de compósitos ChrGO, que administrou agentes quimioterápicos de maneira controlada espaço-temporalmente para o tratamento eficiente do câncer (Esquema 1).
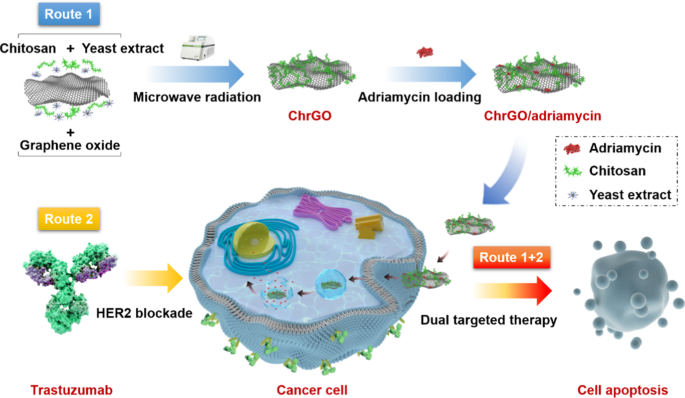
Biofuncionalização assistida por micro-ondas e redução de óxido de grafite como nanossistema de distribuição controlada de drogas para terapia de duplo direcionamento em células BT-474 com superexpressão de HER2
Materiais e métodos
Materiais
O pó de grafite foi obtido na Qingdao Huatai Tech (Qingdao, China). O quitosano e a adriamicina foram adquiridos à Aladdin Co., Ltd. (Shanghai, China). O trastuzumab foi adquirido à Hoffmann-La Roche Ltd (Basel, Suíça). Roswell Park Memorial Institute-1640 (RPMI-1640), meio Eagle modificado de Dulbecco (DMEM) e soro fetal bovino (FBS) foram adquiridos da Invitrogen Corporation (Camarillo, EUA). Amicon ® Filtros ultracentrífugos foram adquiridos da Merck Millipore. CellTiter 96 ® kit de ensaio de proliferação celular em solução aquosa e Caspase-Glo ® O kit do sistema de ensaio 3/7 foi obtido da Promega Corporation (Madison, EUA). A levedura de padeiro seco foi obtida da AB / Mauri Co., Ltd. BT-474 e as linhas celulares Cos-7 foram obtidas do Cell Bank of Chinese Academy of Sciences (Shanghai, China). O meio Luria-Bertani foi adquirido da Sangon Biotech Co., Ltd. Todos os produtos químicos eram de qualidade analítica e estavam disponíveis comercialmente sem purificação adicional.
Redução assistida por micro-ondas do GO funcionalizado com quitosana
O óxido de grafite (GO) foi preparado a partir de flocos de grafite nativa usando um método de Hummer modificado [14]. Para obter uma única camada de GO nanométrico, o GO foi esfoliado com uma sonda ultrassônica (Scientz, China) operando a 800 W por 8 h. Por fim, o GO esfoliado foi disperso em água desionizada para uso posterior. As nanofolhas parcialmente reduzidas de quitosana – GO (ChrGO) foram sintetizadas através da redução assistida por micro-ondas de GO com solução aquosa de quitosana usando um sistema de síntese de micro-ondas. O extrato de levedura livre de células foi usado para a biossíntese de ChrGO via redução assistida por micro-ondas. Primeiro, as células de levedura armazenadas foram ativadas por inoculação em meio Luria-Bertani e agitação a 135 rpm por 18 h a 25 ° C. As células de levedura ativadas foram transferidas para uma solução de sacarose a 2% com agitação a 135 rpm por mais 6 h a 25 ° C. Em seguida, 6 mL de extrato de levedura livre de células foram obtidos por separação centrífuga a 2.000 rpm por 5 min. Em seguida, 50 mg de quitosana foram dissolvidos em 25 mL de solução de ácido acético a 2% (v / v) e misturados com extrato de levedura [20]. Uma solução de GO de 5 mg foi adicionada sob agitação magnética vigorosa. Finalmente, a solução preparada foi transferida para o equipamento de síntese de microondas NOVA-2S (PreeKem Scientific Instruments, China) para a reação de microondas. O esquema de aquecimento para o sistema de micro-ondas envolveu o aquecimento a 80 ° C por 5 min e a manutenção da temperatura por mais 5 min. O ChrGO obtido foi purificado com um filtro MWCO de 100 kDa (Millipore, EUA) e liofilizado para uso posterior.
Caracterizações
Imagens de microscopia eletrônica de transmissão (TEM) de GO nanométricos foram obtidas em um microscópio eletrônico de transmissão JEM-2100 com uma tensão de aceleração de 200 kV (JEOL, Japão). Os espectros de ultravioleta-visível (UV-Vis) foram obtidos usando um espectrofotômetro UV / Vis / NIR Lambda 950 (Perkin-Elmer, EUA). Os espectros de infravermelho de transformada de Fourier (FTIR) foram coletados usando um espectrômetro FTIR Vertex 70 de 4000 a 400 cm -1 com amostras preparadas como pelotas de KBr (Bruker, Alemanha). Os espectros Raman foram registrados usando um microscópio Raman Senterra R200-L com um comprimento de onda de excitação de 532 nm (Bruker Optics, Alemanha). Os padrões de difração de raios X (XRD) foram examinados por um difratômetro Bruker D8 Advance (Bruker, Alemanha). Os elementos de superfície foram registrados usando espectroscopia de fotoelétrons de raios-X (XPS) Kratos AXIS Ultra DLD com radiação monocromática Al Ka (1486,6 eV) (Shimadzu, Japão). A análise termogravimétrica (TGA) foi conduzida em um PerkinElmer Pyris 1 TGA a uma taxa de aquecimento de 5 ° C / min de 30 a 800 ° C em uma atmosfera de nitrogênio (PerkinElmer, EUA). A carga superficial dos compósitos foi medida por um instrumento Malvern Zeta Nano ZS-90 (Malvern, Reino Unido).
Carregamento e liberação de drogas
Quatro miligramas de nanopartículas de ChrGO foram suspensos em 20 mL de solução aquosa de adriamicina (0,4 mg / mL). Após sonicação por 0,5 h, a agitação foi realizada no escuro por 24 h, evitando a luz. A adriamicina não carregada foi removida por filtração por centrifugação através de filtros Amicon MWCO de 50 kDa (Millipore, EUA) e lavada com solução salina tamponada com fosfato (PBS, pH 8,0) até o sobrenadante ficar incolor. A concentração de adriamicina foi determinada usando uma curva de concentração de adriamicina padrão por espectrometria UV-Vis a 490 nm com um SpectraMax ® Leitor de microplaca M5 (Molecular Devices, EUA). A quantidade de adriamicina carregada em ChrGO foi determinada com uma absorbância de UV-Vis medindo a concentração da perda de adriamicina no sobrenadante de Amicon ® Filtro centrífugo Ultra-15 mL.
As características de liberação de adriamicina de ChrGO foram estudadas. O ChrGO carregado com adriamicina foi submerso em 10 mL de solução tampão de PBS. Em intervalos especificados, 2 mL de solução de adriamicina liberada separada de ChrGO foram coletados por filtração por centrifugação através de filtros Amicon MWCO de 50 kDa (Millipore, EUA). O volume da solução ChrGO / adriamicina foi mantido constante pela adição de 2 mL de solução tampão PBS fresca após cada amostragem. A quantidade de adriamicina liberada de ChrGO foi medida por uma absorbância UV-Vis a 490 nm por um SpectraMax ® Leitor de microplaca M5 (Molecular Devices, EUA). Os estudos de liberação foram investigados em diferentes soluções de pH (valores de pH 5 e 7,4).
Análise de biocompatibilidade e ensaio de eficácia terapêutica
As células BT-474 e Cos-7 foram mantidas em RPMI-1640 suplementado com 10% de FBS ou DMEM suplementado com 10% de FBS, respectivamente, e cultivadas em uma atmosfera umidificada de 5% de CO 2 a 37 ° C. O ensaio de biocompatibilidade de GO e ChrGO foi realizado em células BT-474 ou Cos-7 por meio de ensaio de citotoxicidade celular. As células foram colocadas em placas planas de 96 poços a uma densidade de 3 × 10 4 células por poço e pré-incubadas por 18 h antes do tratamento com GO e ChrGO. Em seguida, as diluições dos agentes testados foram adicionadas às células e incubadas por mais 24 horas. A viabilidade das células foi determinada por CellTiter 96 ® uma solução aquosa. A absorbância foi medida a 490 nm por um SpectraMax ® Leitor de microplaca M5 (Molecular Devices, EUA).
A eficácia dos complexos ChrGO / adriamicina isoladamente ou em combinação com trastuzumabe na proliferação de células BT-474 foi investigada por ensaio de inibição de proliferação [16]. As células BT-474 foram semeadas em placas planas de 96 poços a uma densidade de 1 × 10 4 células por poço e incubadas por 24 h. Em seguida, os complexos ChrGO / adriamicina sozinhos ou em tratamento combinado com trastuzumabe foram introduzidos nas células BT-474 no meio de cultura. Após incubação de 96 h, as células viáveis foram determinadas por CellTiter 96 ® uma solução aquosa. A absorbância foi medida com um SpectraMax ® Leitor de microplaca M5 a 490 nm (Molecular Devices, EUA). Os dados foram analisados com ANOVA de um fator. p <0,05 foi considerado estatisticamente significativo.
Análise do ciclo celular e ensaio de apoptose
Para a análise do ciclo celular, as células BT-474 foram semeadas em placas de seis poços a uma densidade de 5 × 10 5 células por poço e podem aderir por 16 h. As células foram tratadas com complexos ChrGO / adriamicina isoladamente ou em combinação com trastuzumabe por 24 h. Células BT-474 foram colhidas e fixadas com etanol 70% (v / v) a 4 ° C por 24 h. As células fixadas de BT-474 foram coradas com solução de iodeto de propídio (15 μg / mL) contendo ribonuclease A (10 μg / mL) a 25 ° C por uma hora. Em seguida, as células foram analisadas com citômetro de fluxo (BD Biosciences, EUA). Para o ensaio de apoptose, células BT-474 foram semeadas em placas de 96 poços de parede branca a uma densidade de 2 × 10 4 células por poço e podem aderir por 18 h. As células foram tratadas com complexos ChrGO / adriamicina, trastuzumab sozinho ou em tratamento de combinação por 24 h. Em seguida, o meio de cultura foi descartado e 100 µL de Caspase-Glo ® 3/7 de reagente foi adicionado a cada poço e incubado à temperatura ambiente por 2 h. A luminescência foi medida por um SpectraMax ® Leitor de microplaca M5 (Molecular Devices, EUA). Os resultados foram analisados por ANOVA de um fator. p <0,05 foi considerado estatisticamente significativo. Todos os estudos foram realizados de acordo com as diretrizes e regulamentos relevantes.
Resultados e discussão
Síntese e caracterização
A morfologia das folhas GO sintetizadas foi caracterizada por microscopia eletrônica de transmissão (TEM). A Figura 1a revela a distribuição de tamanho uniforme de nanofolhas GO abaixo de 100 nm, com um tamanho médio de aproximadamente 45 nm. A alta densidade de elétrons do GO exibiu melhor contraste em comparação com a quitosana, que é pouco visível devido à sua baixa densidade de elétrons e natureza hidratada [21]. Devido à maior área de superfície, GO em nanoescala ou folhas GO reduzidas têm sido amplamente utilizadas como transportadores de drogas [22]. O padrão de difração de elétrons de área selecionada (SAED) na Fig. 1c exibe os anéis concêntricos, que demonstram a presença de uma natureza policristalina correspondente ao óxido de grafeno [23].

a Imagem TEM de baixa ampliação de nanofolhas GO, b imagem TEM de alta resolução de nanofolhas e c um padrão SAED típico de nanofolhas GO
Para estabilizar nanofolhas GO em solução fisiológica, nanofolhas GO funcionalizadas com quitosana foram preparadas por redução assistida por micro-ondas usando um sistema de micro-ondas [24]. O GO-quitosano reduzido resultante (ChrGO) foi analisado por espectrometria UV-Vis. A Figura 2a mostra os espectros de UV-Vis de GO e ChrGO. GO exibiu um pico de absorção acentuado em 230 nm e um ombro em 300 nm, que é atribuído ao π - π * transição de ligações C =C aromáticas e n - π * transição de ligações C =O, respectivamente [25, 26]. Depois que a quitosana foi enxertada em GO, o pico em 230 nm mudou para o vermelho para 270 nm para ChrGO, e o ombro em 300 nm obviamente desapareceu, o que foi atribuído à restauração parcial da conjugação eletrônica entre os átomos de carbono aromáticos [27]. Uma solução preta de ChrGO sintetizado é mostrada na Fig. 2b, que indica a formação de óxido de grafeno parcialmente reduzido (p-rGO). Ambas as nanofolhas GO e ChrGO estavam bem dispersas em H 2 desionizado O. A estabilidade coloidal dos derivados de GO ou GO em solução aquosa é muito importante para sua aplicação biomédica. Os resultados sugerem que a quitosana foi conjugada com GO após a redução.
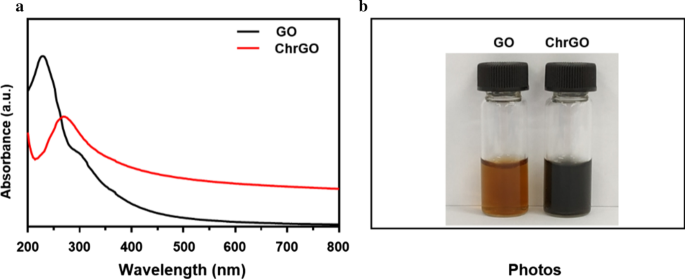
a Espectro UV-Vis das nanofolhas GO e ChrGO em solução aquosa, b fotografias de nanofolhas GO e ChrGO sintetizado
A espectroscopia FTIR foi realizada para caracterizar a estrutura de GO, quitosana e ChrGO (Fig. 3a). Os picos característicos de GO estavam situados em 3440 cm −1 e 1376 cm −1 , correspondendo às ligações O – H e C – OH, respectivamente. O pico em 1072 cm −1 foi atribuído à vibração de alongamento de C – N – C. Visivelmente, os picos das moléculas de quitosana em 2912 cm −1 e 2848 cm −1 foram atribuídos às vibrações de alongamento do CH 3 - e –CH 2 - [28, 29]. O p-rGO funcionalizado com quitosana resultou em novas ligações, o que levou a novos picos nos espectros de ChrGO. Há uma diminuição significativa nas intensidades da banda C =O em 1636 cm −1 no ChrGO comparado ao GO, o que sugere que o processo de redução removeu os grupos contendo oxigênio do GO [30]. O espectro FTIR de ChrGO confirmou a conjugação bem-sucedida de quitosana em GO. Além disso, a espectroscopia Raman foi usada para caracterizar as propriedades eletrônicas e a estrutura do grafeno. A banda G é atribuída ao E 2g fônons de sp 2 domínios de carbono, enquanto a banda D é atribuída à vibração de sp 3 domínios de átomos de carbono e átomos de carbono desordenados. A intensidade da banda D indica as características de distúrbios e defeitos nas folhas de carbono [31]. A redução das nanofolhas GO também foi analisada na razão do sinal da banda D versus G [32]. O espectro Raman representativo de GO mostra dois picos característicos da banda D (1341 cm −1 ) e a banda G (1591 cm −1 ) na Fig. 3b. Mudança na intensidade relativa de I D / I G valor ilustra a mudança no estado de conjugação eletrônica do GO no processo de redução [33]. O deslocamento da banda D mostra a funcionalização bem-sucedida do GO reduzido. O valor de I D / eu G aumenta de 0,99 (GO) para 1,12 (ChrGO), o que é atribuído à introdução de sp3 defeitos após funcionalização e recuperação incompleta da estrutura característica do grafeno [34]. Esta observação está de acordo com o relatório anterior e sugere a formação de grafeno funcionalizado com quitosana [16].
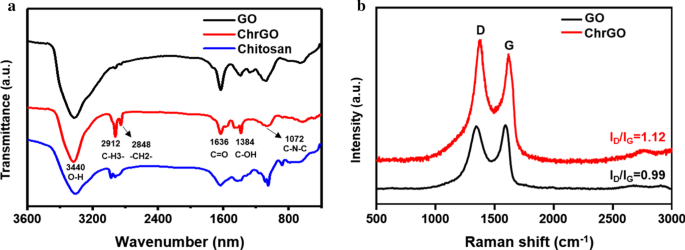
a Espectros de FTIR de GO, ChrGO e quitosana, b Espectros Raman de GO e ChrGO
A composição da superfície de ChrGO foi confirmada por XPS. A varredura completa do espectro XPS de ChrGO mostra três picos em 284, 399 e 533 eV, que são atribuídos a C1s, N1s e O1s (Fig. 4a), respectivamente. A análise elementar relativa exibiu um aumento nos níveis de oxigênio e nitrogênio do ChrGO, com uma diminuição associada no conteúdo de carbono em comparação com o GO. Os espectros C1s de alta resolução de ChrGO mostrados na Fig. 4b exibem quatro picos separados, correspondendo a C – C ou C =C ( sp 2 , 284,7 eV), C-O (epóxi / hidroxilas, 286,4 eV), C =O ( sp 3 , 288,2 eV) e ligações O =C – O (carboxilatos, 289,1 eV). O aparecimento de um pico de amida em ChrGO fornece evidências para a funcionalização da quitosana no GO [35]. Os grupos funcionais hidrofílicos abundantes na superfície tornaram ChrGO altamente solúvel em uma solução aquosa, o que é consistente com os resultados de FTIR. As biomoléculas como aminoácidos redutores e ácido alfa-linolênico no extrato de levedura podem ter um papel significativo na fabricação assistida por microondas de ChrGO [20].
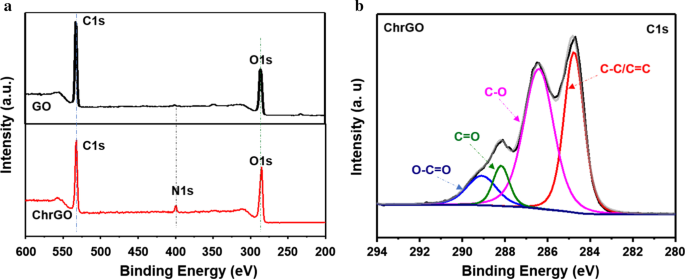
a Pesquise os espectros XPS de GO e ChrGO, b espectros de alta resolução de C1s
O padrão de difração de raios-X (XRD) de GO e ChrGO é apresentado na Fig. 5a. Nos espectros GO XRD, o pico principal em 11,0 ° e o pico fraco em 20,7 ° apresentam claramente a estrutura de grafite. A característica pico de difração em 11,0 ° correspondendo ao (001) plano de GO, que mostra a síntese bem-sucedida de GO [36]. A pequena saliência entre 20 ° e 24 ° mostra as porções grafíticas, que são atribuídas ao grafite puro não oxidado [37]. Com a funcionalização da quitosana, o pico (001) do GO desaparece, enquanto o pico de difração ampla a 21,4 ° torna-se proeminente. Essa mudança pode ser atribuída à redução do GO, onde a redução torna o pack do rGO mais apertado do que o GO. O reflexo (002) da amostra de ChrGO é muito amplo, sugerindo que a amostra está muito mal ordenada ao longo da direção de empilhamento, o que pode ser atribuído à redução incompleta de GO [33]. Os comportamentos de decomposição de GO, quitosana e ChrGO foram estudados por análise de gravidade térmica (TGA) [38]. As curvas TGA de ChrGO, GO e quitosana são mostradas na Fig. 5b, que foram medidas em uma atmosfera de nitrogênio. GO começou a perder peso abaixo de 100 ° C, o que foi atribuído à eliminação de água livre adsorvida na estrutura empilhada [39]. O GO perdeu 42% de seu peso na faixa de 191–231 ° C, que estava relacionado à decomposição de grupos contendo oxigênio lábil. A taxa de perda de peso de ChrGO em 100–250 ° C é significativamente menor do que GO, e é óbvio que ChrGO mostrou um padrão de decomposição diferente em comparação com GO. A eliminação térmica de ChrGO e quitosana pura ocorreu de 250 a 440 ° C, que está relacionada à despolimerização e pirólise de grupos funcionais mais estáveis, como unidades glicosídicas de quitosana e grupos carboxila [40]. Comparado com GO, ChrGO foi termicamente estável e deu uma grande perda de peso de 36% no primeiro estágio de decomposição a 250–440 ° C, enquanto que pouca perda de peso é exibida para o GO. A perda de peso significativa na região de alta temperatura de 450-800 ° C foi devido à degradação térmica do esqueleto de carbono, que poderia ser atribuída aos resíduos de quitosana e biomoléculas do extrato de levedura, como aminoácidos [41].
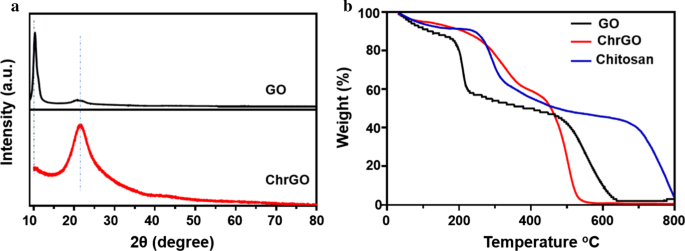
a Padrões de XRD de GO e ChrGO, b Curvas TGA de GO, quitosana e ChrGO
A carga superficial de GO e ChrGO foi medida por um instrumento Malvern Zeta Nano ZS-90, que é um parâmetro importante de estabilidade coloidal. A densidade de carga superficial mais alta em nanofolhas GO cria uma dispersão coloidal mais estável [42]. Conforme mostrado no arquivo adicional 1:Fig. S1, o potencial zeta do GO diminuiu monotonicamente de -10,7 mV em pH 3 para -35,5 mV em pH 11, o que confirmou a carga negativa na superfície das nanofolhas GO. O valor do potencial zeta para ChrGO foi comparativamente menor do que o potencial de GO em qualquer pH variando de 3 a 11. Nanofolhas ChrGO exibiram estabilidade em toda a faixa de valores de pH, enquanto coloides GO reduzidos foram relatados como menos estáveis em água desionizada devido a aumentou π - π empilhamento nas superfícies desoxigenadas [43]. Embora alguns grupos de amina livre estivessem presentes na superfície da quitosana [44], um potencial zeta mais alto de ChrGO não foi alcançado. O menor valor do potencial zeta de ChrGO pode ser atribuído às abundantes moléculas de aminoácidos negativos do extrato de levedura, o que aumenta a estabilidade coloidal em solução fisiológica [20]. A superfície carregada negativamente do ChrGO os torna potencialmente aplicáveis para o carregamento e entrega da droga.
Biocompatibilidade de ChrGO As-Sintetizado
A biocompatibilidade do ChrGO como sintetizado é importante para suas aplicações na distribuição de drogas. A citotoxicidade celular de ChrGO e GO foi investigada por ensaio de citotoxicidade. Células Cos-7 e células BT-474 foram incubadas na presença de ChrGO ou GO por 24 h. Os resultados da citotoxicidade celular são apresentados na Fig. 6. Pode-se concluir que ChrGO não apresentou citotoxicidade celular óbvia para células Cos-7 e BT-474. Mesmo na concentração de 100 μg / mL, a viabilidade celular estava acima de 90%. No entanto, o GO exibiu citotoxicidade celular significativa de maneira dose-dependente, com apenas 73,0 ± 0,5% e 71,0 ± 0,5% de sobrevivência celular para as células Cos-7 e BT-474 na concentração de 100 μg / mL, respectivamente. Os resultados demonstraram que a quitosana funcionalizada na superfície do GO apresentou grande baixa citotoxicidade e melhor biocompatibilidade. Foi relatado que a funcionalização da superfície do GO com macromoléculas atenua notavelmente seus efeitos citotóxicos [45]. Hu et al. relataram que o soro fetal bovino em meio celular diminuiu acentuadamente a citotoxicidade celular do GO em células A549 de câncer de pulmão de células não pequenas [46].
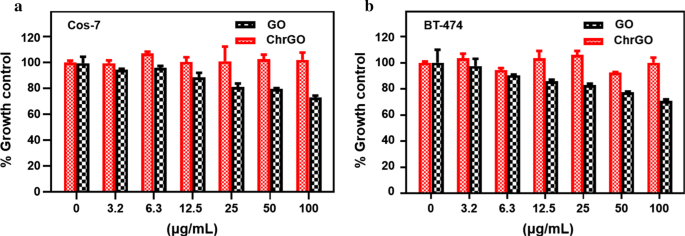
Biocompatibilidade de GO e ChrGO. Concentrações variáveis de nanopartículas foram cultivadas com a Células Cos-7 e b Células BT-474, e seu efeito na viabilidade celular foi determinado
Carregamento e liberação da droga
A aplicação biomédica potencial de ChrGO como um carreador de drogas é medida pelo comportamento de carga e liberação de drogas. As características estruturais dos derivados de grafeno são altamente eficazes para a administração de drogas aromáticas devido à sua grande área de superfície específica. A adriamicina é um dos quimioterápicos de tumor primário contra uma variedade de malignidades hematológicas e tumores sólidos e é freqüentemente usada como um medicamento modelo para avaliar os sistemas de distribuição de medicamentos derivados de grafeno [47]. A capacidade de carga de adriamicina nas nanofolhas ChrGO foi verificada pelo pico de absorvância UV-Vis característico da adriamicina a 490 nm. Como esperado, a eficiência máxima de carregamento da adriamicina ligada às nanofolhas ChrGO foi tão alta quanto 169,8%, o que foi parcialmente atribuído à grande área de superfície das nanofolhas ChrGO. Os nanocompósitos de ChrGO / adriamicina carregados com adriamicina foram facilmente dispersos em um tampão fisiológico, exibindo uma solução transparente com uma cor levemente avermelhada.
Para explorar o perfil de liberação de adriamicina dos complexos ChrGO / adriamicina, os diferentes valores de pH de PBS foram introduzidos para imitar ambientes de células tumorais. Arquivo adicional 1:A Fig. S2 mostra os perfis de liberação cumulativa de adriamicina do ChrGO / adriamicina em pH 5 e 7,4. A adriamicina liberada de ChrGO / adriamicina foi caracterizada por uma liberação rápida inicial e, em seguida, um estágio de liberação mais lenta em solução de PBS de pH 5,0. A liberação cumulativa de adriamicina foi de 6,5% nas primeiras 3 horas e, em seguida, apresentou um aumento lento para 26,7% em 96 horas em pH 5,0. Em contraste, a porcentagem de adriamicina do ChrGO / adriamicina aumentou mais lentamente e foi menor em pH 7,4, exibindo uma porcentagem de liberação de adriamicina de 2,5% nas primeiras 3 h para 7,4% em 96 h. Estudos anteriores mostraram os perfis de liberação de drogas do GO funcionalizado muito lentamente em um meio com pH 7,4 [48]. A protonação dos grupos carboxila no ChrGO diminui o empilhamento π – π, a ligação H e as interações eletrostáticas entre a adriamicina e o ChrGO, facilitando a liberação da adriamicina no meio acético [49]. A sensibilidade ao pH dá potencial de ChrGO / adriamicina para entrega de droga específica ao local, o que subsequentemente aumenta a citotoxicidade nas células tumorais.
Eficácia terapêutica dos complexos ChrGO / Adriamicina
A eficácia terapêutica dos complexos ChrGO / adriamicina em células de câncer BT-474 com superexpressão de HER2 foi investigada pelo ensaio de inibição de proliferação. A superexpressão do receptor HER2 tem um papel fundamental na transformação das células de câncer de mama BT-474. O tratamento com trastuzumab sozinho, um anticorpo monoclonal anti-HER2, resulta na inibição significativa do crescimento das células BT-474 [50]. As shown in Fig. 7a, after treatment with ChrGO/adriamycin complexes, the cell viability of BT-474 cells was decreased significantly, demonstrating a dosage-dependent toxic effect. Besides, when compared to free adriamycin, the ChrGO/adriamycin complexes demonstrated a less effective performance in killing BT-474 cells, which was ascribed to the gradual diffusion of loaded adriamycin rather than direct treatment with free adriamycin [51]. However, the therapeutic efficacy of the ChrGO/adriamycin complexes was close to that of free adriamycin as their concentration of ChrGO/adriamycin complexes increased, which can be explained by the sustained adriamycin release from the ChrGO carrier.
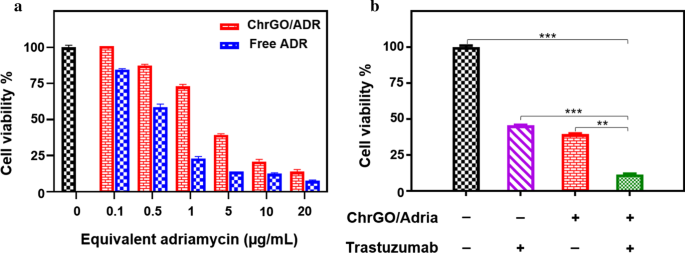
a In vitro cell viability of BT-474 cells incubated with concentrations of free adriamycin and adriamycin loaded in ChrGO/adriamycin complexes, b cytotoxicity of ChrGO/adriamycin complexes (5 μg/mL) in combination with trastuzumab (5 μg/mL) in BT-474 cells. Adria:adriamycin. **p < 0.01, ***p <0,001
To study whether trastuzumab, an anti-HER2 monoclonal antibody, could improve the antitumour activity of equivalent amounts of adriamycin loaded on ChrGO, BT-474 cells were treated with trastuzumab alone or in combination with ChrGO/adriamycin. Treatment with trastuzumab alone produced a significant inhibition of BT-474 proliferation, which is consistent with a previous report [52]. The combined therapy with trastuzumab and ChrGO/adriamycin resulted in an enhanced cell growth inhibition effect, as shown by a reduction of 88.5% compared with a reduction of 54.5% with trastuzumab alone (5 μg/mL) and 59.5% with equivalent ChrGO/adriamycin alone (5 μg/mL) versus the negative control (Fig. 7b). The results suggest that the ChrGO system may be effectively used to develop composites for combination therapies, and the combined treatment of ChrGO/adriamycin and trastuzumab resulted in a modest, but significant, reduction of cell viability compared to each drug alone.
Cell Cycle Analysis and Apoptosis
To determine whether the ChrGO/adriamycin complexes have effects on cell cycle progression, a cell cycle assay of ChrGO/adriamycin complexes alone or in combination treatment with trastuzumab was performed on BT474 cells. As shown in Fig. 8a, flow cytometry analysis revealed that trastuzumab alone increased the cell population in the G0/G1 phase. Treatment with ChrGO/adriamycin alone mediated a significant reduction in the number of G0/G1 cells and accumulation in S phase and G2/M phase compared to control cells. Besides, ChrGO/adriamycin combined with trastuzumab mediated S phase arrest, accompanied by a significant decrease in the number of cells in the G0/G1 phase. While ChrGO/adriamycin is most active in the S phase of the cell cycle, ChrGO/adriamycin treatment with trastuzumab can cause an increase in G0/G1 phase compared to ChrGO/adriamycin alone. A previous report showed that trastuzumab can cause cell arrest in the G1 phase [53]. Adriamycin inhibits cell proliferation and DNA replication, ultimately leading to cell cycle arrest [54].
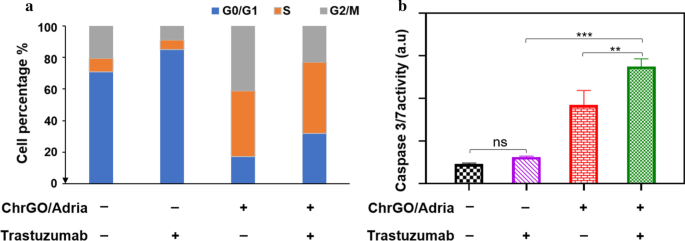
a Cell cycle analysis after treatment with ChrGO/adriamycin alone or in combination with trastuzumab in BT-474 cells, b effect of ChrGO/adriamycin (5 μg/mL) plus trastuzumab (5 μg/mL) on induction of apoptosis in BT-474 cells. Adria:adriamycin. **p < 0.01, ***p <0,001
To assess the effects of ChrGO/adriamycin on apoptotic molecules, BT-474 cells were treated for 48 h with either ChrGO/adriamycin, trastuzumab, or a combinational treatment of both agents. For the visualization of apoptosis, caspase 3/7 activity has been extensively used as an apoptosis-specific marker due to its activity related to the process of apoptosis [55]. As observed from Fig. 8b, compared to the negative control, treatment with ChrGO/adriamycin (5 μg/mL) alone significantly increased the caspase 3/7 activity. However, trastuzumab (5 μg/mL) alone did not significantly increase caspase 3/7 expression, suggesting that trastuzumab does not induce apoptosis. In contrast, treatment with ChrGO/adriamycin (5 μg/mL) plus trastuzumab (5 μg/mL) significantly increased caspase 3/7 activity compared to that with each drug alone. The dual-targeted therapy showed higher apoptosis, indicating superior therapeutic efficacy due to the presence of different mechanisms of action. Similar to other studies, adriamycin amplifies the apoptotic response in HER2-overexpressing cancer cells [56]. In conclusion, ChrGO/adriamycin combined with trastuzumab induces cell cycle arrest and apoptosis, which ultimately results in augmented cell death.
Conclusões
In the present work, the chitosan-functionalized graphene oxide nanosheets were structured with microwave-assisted reduction, which demonstrated biocompatibility and good dispersion stability. The as-prepared nanocomposites showed high efficiency of drug encapsulation and delivery. The ChrGO/adriamycin nanosheets displayed significant growth inhibition of BT-474 in a dose-dependent manner. The combined treatment of ChrGO/adriamycin and trastuzumab resulted in superior therapeutic efficacy in BT-474 cells compared to that with each agent alone. The results are favourable for the development of intracellular nanocarriers to deliver drugs in a controlled manner, which is expected to improve the therapeutic effect on HER2-overexpressing cancer therapies.
Disponibilidade de dados e materiais
The datasets supporting the conclusions of this current study are available from the corresponding authors upon reasonable request.
Abreviações
- ChrGO:
-
Chitosan-functionalized graphene oxide
- EGFR:
-
Receptor do fator de crescimento epidérmico
- HER2:
-
Human epidermal growth factor receptor-2
- GO:
-
Graphene oxide
- DMEM:
-
Dulbecco's modified Eagle medium
- FBS:
-
Fetal bovine serum
- TEM:
-
Microscopia eletrônica de transmissão
- UV–Vis:
-
Ultraviolet–visible
- FTIR:
-
Fourier transform infrared
- XRD:
-
Difração de raios X
- XPS:
-
espectroscopia de fotoelétrons de raios-X
- TGA:
-
Thermogravimetric analysis
- PBS:
-
Phosphate-buffered saline
- SAED:
-
Selected-area electron diffraction
- TGA:
-
Gravimetric analysis
Nanomateriais
- Nanofibras e filamentos para entrega aprimorada de drogas
- Nanopartículas de FePO4 biocompatíveis:entrega de drogas, estabilização de RNA e atividade funcional
- Estruturas Metálicas-Orgânicas de Meio Ambiente como Sistema de Administração de Medicamentos para Terapia de Tumor
- Administração de medicamentos baseados em células para solicitações de câncer
- Peixe-zebra:um sistema de modelo em tempo real promissor para a entrega de medicamentos neuroespecíficos mediada por nanotecnologia
- Nanopartículas lipídicas de PLGA rastreadas com 131I como transportadores de administração de drogas para o tratamento quimioterápico direcionado do melanoma
- Nanotecnologia:do Sistema de Imagem In Vivo à Entrega Controlada de Medicamentos
- Nanopartículas de sílica para entrega de proteína intracelular:uma nova abordagem de síntese usando proteína fluorescente verde
- Avaliação de estruturas de grafeno / WO3 e grafeno / CeO x como eletrodos para aplicações de supercapacitor
- Investigação sobre as características físico-químicas de um sistema baseado em nanolipossomas para administração dupla de medicamentos



