Avaliação quantitativa da internalização celular de nanopartículas poliméricas dentro das células cancerosas da laringe e células do sistema imunológico para a entrega aprimorada de drogas
Resumo
A tradução clínica de nanomedicina à base de poli (ácido lático-co-glicólico) (PLGA) é limitada, em parte devido à baixa eficiência de entrega resultante de fagocitose não específica por fagócitos. Compreender a interação das nanopartículas entre as células cancerosas e as células do sistema imunológico ainda é algo difícil de entender. Neste estudo, uma investigação quantitativa sobre a internalização celular de partículas fluorescentes de PLGA (100 nm, 500 nm e 1 µm) contra células de carcinoma da laringe com ou sem monócitos / macrófagos em sistemas de monocultura ou co-cultura foi realizada pela primeira vez. Partículas de PLGA em concentrações de 5–20 µg / mL mostram biocompatibilidade superior, exceto para 500 nm e partículas de PLGA de 1 µm a 20 µg / mL reduzem ligeiramente a viabilidade celular. A observação microscópica descobriu que todos os três tamanhos de partículas são efetivamente ingeridos por células cancerosas e macrófagos; no entanto, o exame de fluorescência quantitativa revelou que o índice de captação de células cancerosas (fluorescência de partícula intracelular média por célula cancerosa normalizada para a de por macrófago) é substancialmente diminuído para todas as partículas de PLGA em co-culturas em comparação com aquele em monoculturas (1,35-1,05, 1,50–0,59 e 1,4–0,47 para partículas de 100 nm, 500 nm e 1 µm, respectivamente). A análise quantitativa usando citometria de fluxo confirmou ainda mais o índice de absorção reduzido de células cancerosas em co-culturas, mas contagens de partículas mais altas por macrófago. Também foi descoberto que a formação de células gigantes multinucleadas por meio da fusão de macrófagos aumentou após o tratamento com PLGA, o que poderia ser mais explorado como uma abordagem potencial para a administração de medicamentos para tumores. No geral, essas descobertas fornecem novos insights sobre a interação de nanopartículas imunológicas com células cancerosas, o que pode facilitar a aplicação de nanocarreadores baseados em PLGA para o tratamento de carcinoma de laringe.
Introdução
O câncer é uma das principais causas de mortalidade em todo o mundo, com cerca de 10 milhões de novos casos de morte relatados em 2018 [1]. O carcinoma de laringe (células cancerosas surgem da laringe) é a segunda malignidade mais comum dos carcinomas de células escamosas de cabeça e pescoço (CECP), sendo responsável por cerca de 180.000 novos casos e 95.000 mortes em 2018 [2]. Atualmente, drogas direcionadas são desenvolvidas como um tratamento opcional para desafios introduzidos por terapias tradicionais, como cirurgia, radioterapia e quimioterapia [3]. Esforços científicos foram acelerados para melhorar o direcionamento e a eficácia do medicamento e reduzir os efeitos colaterais indesejados pelo desenvolvimento, por exemplo, de novos nanotransportadores de medicamento ( i.e. , microagulhas), drogas anticâncer personalizadas e sistemas terapêuticos de administração direcionada a anticorpos [4].
Nanocarriers têm sido amplamente utilizados para carregar drogas anticâncer, como cisplatina, paclitaxel e docetaxel para melhorar sua solubilidade em água, biodisponibilidade e estabilidade para melhor entrega e eficácia da droga [3, 4]. Em geral, a distribuição de drogas com base em nanopartículas (NP) permite a distribuição de uma ampla gama de outras substâncias ( por exemplo , proteínas, anticorpos, vacinas e ácidos nucléicos) para regiões específicas do corpo em modelos animais e pacientes [4, 5]. No entanto, o chamado efeito de maior permeabilidade e retenção (EPR) resultou em uma eficiência de direcionamento consideravelmente variável entre os diferentes tipos de câncer [6]. Evidências recentes sugerem que a deposição de nano-portadores de drogas (aqui NPs de ouro) em tumores depende preferencialmente do processo de transcitose [7], um tipo de transporte transcelular biológico, no qual as substâncias / NPs são transferidas através das células de um lado para o outro incluindo os cursos de endocitose, transferência vesicular e exocitose. Deve, no entanto, ser observado que os resultados contraditórios em relação aos mecanismos de entrega de drogas direcionadas enfatizam a importância crítica para a compreensão da base da interação celular com nano-drogas ou NPs utilizando múltiplas estratégias experimentais que variam de cultura de células in vitro a cultura de tecidos ex vivo e estudo animal in vivo.
Numerosos nanocarriers como lipossomas, albumina NPs (NPs), sílica NPs e poli (ácido láctico-co-glicólico) (PLGA) foram clinicamente empregados para tratar diferentes tipos de câncer incluindo carcinoma de laringe [4]. NPs com base polimérica, como micelas e PLGA, possuem grande potencial em aplicações biomédicas por causa de suas formulações versáteis de nano-droga por meio de mistura simples ou conjugação covalente, excelente capacidade de automontagem, alta capacidade de carga de droga e biocompatibilidade [8, 9 ] Por exemplo, nanocarreadores de PLGA revestidos com polietilenoglicol (PEG) carregados com doxorrubicina e indocianina verde permitem a terapia quimio-fototérmica sinérgica para câncer de mama [10]. Além disso, estudos in vitro e in vivo mostraram que micelas carregadas com cisplatina exibem excelente atividade anticâncer contra tumores ortotópicos de HNSCC ( i.e. , SAS-L1 e HSC-2) [11]. Embora vários nano-fármacos com base polimérica, como PLGA e micelas, tenham sido aprovados para uso clínico ou estejam sendo avaliados em ensaios clínicos [4, 6], muitos mais nano-fármacos poliméricos estão sob investigação pré-clínica com diferentes células cancerígenas de cabeça e pescoço linhas e modelos de tumor de xenoenxerto de animais [11,12,13,14].
A evidência científica destacou a importância das respostas imunológicas do hospedeiro aos nano-portadores de drogas, porque uma vez que esses NPs entram no corpo, eles se tornam inevitavelmente reconhecidos pelo sistema imunológico. Os macrófagos são considerados a primeira linha de defesa celular do hospedeiro, especializando-se na neutralização e eliminação de alérgenos, microrganismos e partículas estranhas ( por exemplo , nanotransportadores) por meio de fagocitose e consequente iniciação de respostas imunes. A maioria dos nanotransportadores concebidos de forma inovadora falhou na entrega direcionada para regiões doentes específicas ou tumores in vivo devido ao acúmulo eficiente de NPs no sistema de fagócitos mononucleares (MPS), como células de Kupffer no fígado e macrófagos de polpa vermelha no baço [15]. Portanto, compreender os mecanismos de captação celular de NPs por células do sistema imunológico, como monócitos e macrófagos, é crucial, pois determina o tempo de vida de nanocarreadores em tecidos e fluidos biológicos relevantes. O sistema emergente de co-cultura de células in vitro tem, portanto, gradualmente atraído cada vez mais atenção nos campos da nanomedicina e da toxicologia, devido à crescente demanda por resultados mais significativos que possam refletir melhor a condição in vivo [16]. De fato, foi comprovado que os sistemas de co-cultura exibem uma situação realista ao simular estados de tecidos saudáveis e doentes [17] e têm sido utilizados de forma confiável em estudos de captação celular e absorção de drogas NP [18,19,20,21]. A utilização de co-cultura de células cancerígenas e modelos de células imunológicas geralmente oferece uma plataforma adequada para sondar as rotas de absorção e os mecanismos desses nanomateriais em células, o que pode facilitar o projeto de nanocarreadores que são melhor direcionados para células cancerosas enquanto reduzem simultaneamente a fagocitose NP. Portanto, é de importância essencial determinar a eficiência de captação e o destino de NPs em células cancerosas na presença de células imunes. A maioria dos nanocarreadores foi projetada para ter diâmetros de 50–200 nm para aproveitar o efeito EPR e prolongar a circulação sanguínea, enquanto NPs maiores (> 500 nm) são relatados como eliminados de forma eficiente pelo MPS [6]. PLGA, um nano-portador aprovado pela FDA, em diferentes tamanhos (100, 500 e 1000 nm) foi, portanto, selecionado para investigar as capacidades de captação de UM-SCC-17A (uma linha de células de carcinoma escamoso de laringe clássica) [22] e THP- 1 (uma linha de células monocíticas humanas agudas). Vários estudos in vitro aplicaram nanocarreadores PLGA para entregar drogas para matar células cancerosas HNSCC em monoculturas [12, 13, 23], este é o primeiro estudo a investigar a eficiência de captação e o mecanismo de captação de NP por células do sistema imunológico e células de câncer de laringe de forma síncrona em um modelo de co-cultura empregando diferentes tamanhos de PLGA, o que pode fornecer uma base fundamental para o desenvolvimento de uma nova nanomedicina segura por projeto para terapia de HNSCC.
Materiais e métodos
Materiais
Três partículas PLGA comercializadas (Sigma-Aldrich) com diferentes tamanhos, incluindo 100 nm, 500 nm e 1000 nm, foram usadas neste estudo. Todas as partículas foram carregadas com fluoróforos verdes com excitação óptica e comprimentos de onda de emissão (ex / em) de 460 nm e 500 nm. Todas as partículas foram recebidas na forma de pó e suspensas em água destilada com concentração final de 10 mg / mL para posterior aproveitamento. Os diâmetros hidrodinâmicos e os potenciais zeta de três partículas foram realizados por dispersão de luz dinâmica (DLS) conduzida com um instrumento Malvern Zeta Sizer Nano (Malvern Instruments Ltd., Malvern, Reino Unido). As suspensões de estoque de cada partícula foram 1:100 diluídas em 80 µl de água destilada para medição DLS. Seguindo a indicação do fabricante, foram obtidas 3 medições repetidas para cada partícula.
Culturas de células de UM-SCC-17A e THP-1 e exposição a partículas
A linha de células de carcinoma da laringe humana UM-SCC-17A e a linha de células de monócitos / macrófagos humanos THP-1 adquirida da Sigma-Aldrich, EUA e Shanghai Hengya Biotechnology Company (Shanghai, China), respectivamente, foram usadas para construir o modelo in vitro em este estudo. Células UM-SCC-17A e células THP-1 foram cultivadas em meio de cultura de células DMEM [22] ou RPMI-1640 suplementado com 10% de FBS (Gibco, Alemanha) e solução de penicilina-estreptomicina a 1% (Gibco, Alemanha) em 37 ° C com 5% de CO2. As células THP-1 foram expostas a soluções 100 nM de Phorbol 12-miristato 13-acetato (PMA) (Sigma, EUA) por 72 h antes da semeadura das células para se diferenciar em macrófagos. Ambas as células foram passadas usando 0,5% de tripsina-EDTA a cada 3 dias, e a morfologia celular foi verificada todos os dias para garantir a saúde das células.
As células foram semeadas em placas de 24 poços na densidade de 0,1 × 10 6 células / poço para células monoculturais para ensaio WST-1 e LDH, ou em lamínula de vidro estéril em placas de 24 poços para microscopia fluorescente. Para o modelo de co-cultura, as células UM-SCC-17A foram primeiro semeadas em placas de 24 poços a uma densidade de 50.000 / poço durante a noite e, em seguida, adicionadas com 50.000 células THP-1 / poço. As partículas foram suspensas em 500 µl de meio de cultura de células respectivo para células UM-SCC-17A e THP-1 monoculturadas ou meio de cultura de células misto 1:1 para células co-cultivadas e expostas a amostras de células por 24 h com final concentrações de 5, 10 e 20 µg / mL para WST-1 e ensaio de LDH ou 10 µg / mL para microscopia fluorescente.
Para a medição FACS, as células foram semeadas em placas de 12 poços da mesma maneira como descrito antes a uma densidade de 250.000 células / poço, ou 125.000 células / poço cada para o modelo de co-cultura. As células foram cultivadas em 1 mL de meio de cultura de células durante a noite e expostas a partículas de PLGA a uma concentração final de 10 µg / mL por 24 h.
Ensaio de viabilidade celular
A viabilidade celular foi determinada pelo kit de reagente de proliferação celular WST-1 (Roche, Alemanha) de acordo com as instruções do fabricante. Resumidamente, a solução WST-1 foi diluída 1:10 em qualquer meio de cultura de células respectivo para monocultura UM-SCC-17A ou THP-1, ou meio de cultura de células misto 1:1 para células co-cultivadas. O sobrenadante foi drenado após a exposição e as células foram incubadas com 500 µl de solução de trabalho de ensaio WST-1 a 37 ° C durante 30 min. As amostras foram coletadas e centrifugadas a 14.000 rpm por 10 min para remover as partículas. A absorbância (valor OD) das soluções foi medida sob o comprimento de onda de 450 nm usando Infinite ® F200 (Tecan, EUA). Os valores de absorbância foram corrigidos subtraindo o valor de uma amostra em branco contendo apenas a solução de trabalho WST-1, e as viabilidades celulares relativas foram comparadas com a amostra de controle não tratada.
Ensaio de vazamento de membrana celular
A liberação de lactato desidrogenase (LDH) foi medida usando um kit comercial de detecção de citotoxicidade (LDH) (Roche, Alemanha) para determinar a citotoxicidade por partículas de PLGA. O sobrenadante das células foi coletado 24 h após a exposição, centrifugado a 14.000 rpm por 10 min e 1:10 diluído em 200 µl de meio de cultura de células completo. O controle positivo foi definido como a liberação total de LDH por incubação das células com 0,2% de Triton X-100 a 37 ° C por 15 min e 1:50 diluído em 200 µl de meio de cultura de células completo. As amostras foram incubadas com 100 soluções de trabalho de ensaio de LDH durante 30 min à temperatura ambiente e a reação foi interrompida usando 50 µl de HCl a 1%. A absorbância no comprimento de onda de 492 nm foi medida usando Infinite®F200 (Tecan, EUA), e as concentrações relativas de LDH foram calculadas de acordo com a seguinte equação
$$ {\ text {Relativo}} \; {\ text {LDH}} \; {\ text {concentração}} =\ left ({{\ text {sample}} \; {\ text {OD}} {- } {\ text {blank}} \; {\ text {OD}}} \ right) / \ left ({{\ text {positivo}} \; {\ text {control}} \; {\ text {OD} } {-} {\ text {blank}} \; {\ text {OD}}} \ right) \ vezes 5 \ vezes 100 \%. $$
Microscopia de fluorescência
As células foram visualizadas por coloração Hoechst para localização das partículas ao microscópio de fluorescência. As células foram lavadas com PBS por 3 vezes após 24 h de exposição das partículas e incubadas com formaldeído a 4% por 10 min em temperatura ambiente. Depois de fixadas com formaldeído, as células foram incubadas com 200 µl de solução de coloração contendo 1:1000 diluído Hoechst e 1% de BSA em PBS por 30 min. Em seguida, as lamínulas foram movidas para uma lâmina de vidro de cabeça para baixo e mantidas com uma gota de agente anti-fade de fluorescência DAKO para visualização. Quatro canais ópticos foram definidos com um microscópio de fluorescência, incluindo campo claro para morfologia celular, DAPI para núcleos celulares e GFP para partículas. Os tempos de exposição do canal de partículas para cada imagem fluorescente foram registrados e usados para homogeneização da intensidade de fluorescência em diferentes partículas, e as partículas intracelulares foram calculadas pela intensidade de fluorescência usando áreas selecionadas aleatoriamente por ImageJ (https://imagej.nih.gov/ij /). O índice de absorção em diferentes partículas foi comparado entre células UM-SCC-17A monoculturadas ou co-cultivadas. Resumidamente, a intensidade média de fluorescência (MFI) de partículas internalizadas foi calculada em, por exemplo, 50 células para cada tipo de célula, que foi determinada como o valor de subtração entre a intensidade de fluorescência total ( I total ) de uma área específica e a autofluorescência ( I auto ) de área de mesmo tamanho na equação da região livre de partículas [24, 25]. O índice de captação de células cancerosas foi determinado pelo MFI de UM-SCC-17A normalizado para aquele de células THP-1 em qualquer modelo de monocultura ou co-cultura. O cálculo foi realizado seguindo a equação abaixo:
$$ {\ text {uptake}} \; {\ text {index}} =\ frac {{I _ {{{\ text {total1}}}} - I _ {{{\ text {auto1}}}} \ left ({{\ text {MFI}} _ { {{\ text {UM}} - {\ text {SCC}} - 17A}}} \ right)}} {{I _ {{{\ text {total2}}}} - I _ {{{\ text {auto2} }}} \ left ({{\ text {MFI}} _ {{{\ text {THP}} - 1}}} \ right)}} $$
Classificação de células ativadas por fluorescência (FACS)
A classificação de células ativadas por fluorescência (FACS) foi realizada para medir a capacidade de absorção de três partículas. As células foram lavadas com PBS por três vezes para remover o meio celular e as partículas dissociativas 24 h após a exposição e incubadas com 200 µl de tripsina-EDTA 0,5% (Gibco, Alemanha) a 37 ° C por 4 min para remover as células da placa . Em seguida, a reação foi interrompida pela adição de 2 ml de meio de cultura de células completo e a suspensão de células foi movida para um tubo de vidro para medição FACS e centrifugada por 5 min a 300 × G, 4 ° C. O sobrenadante foi descarregado suavemente e as células foram suspensas em 200 µl de PBS e preservadas em gelo. Células vivas foram primeiro separadas de detritos e células mortas usando dispersão direta (FSC-A) no lado (SSC-A). Em seguida, as células co-cultivadas foram analisadas usando canal APC versus FSC-A para separar células UM-SCC-17A de macrófagos com base no tamanho das células. Um total de 30.000 células foi analisado para cada amostra, e a intensidade média de fluorescência para cada célula foi calculada e normalizada entre diferentes partículas. Enquanto isso, após 24 horas de incubação de partículas com células, o sobrenadante da cultura de células, tampão de lavagem (três vezes lavagem para remover as partículas residuais fixadas à superfície da célula) e células (digestão tripsinizada) foram coletados para medir a intensidade fluorescente usando uma microplaca leitor (Infinite®F200, Tecan). Por esta abordagem, a porcentagem de partículas ingeridas pelas células pode ser determinada para cada grupo, por exemplo, cerca de 30.000 partículas expostas a uma única célula em 12 poços / placa (250.000 células no total) a uma dosagem de 5 µg de 100 nm Partículas de PLGA, resultando em uma média de 13.000 partículas internalizadas por células individuais, que é cerca de 43% da dose aplicada entregue às células. Esta porcentagem entregue pode ainda ser usada para calcular as contagens de partículas no sistema de co-cultura para cada tipo de células em FACS.
Quantificação da fusão celular
A fusão de macrófagos com células gigantes multinucleadas (MGC) foi definida como uma célula gigante morfologicamente contendo dois ou mais núcleos dentro de um citoplasma normal, que podem ser identificados de forma clara e sincrônica em imagens de campo claro e imagens fluorescentes após a coloração, conforme registrado na literatura [26]. . A porcentagem de fusão celular foi calculada pelo número de núcleos MGC (contagem manual) normalizados para a contagem total de células, que foi determinada com uma abordagem automatizada no ImageJ (https://imagej.nih.gov/ij/).
Análise estatística
O software GraphPad V8.0 (GraphPad Software Inc., San Diego, CA, EUA) foi usado para análise estatística e visualização dos resultados. Seguindo ANONA unilateral, o método Holm − Sidak ou o teste t foi realizado para comparar resultados de múltiplos grupos ou resultados de dois grupos, respectivamente. Todos os experimentos foram realizados com triplicações independentes, e os dados foram apresentados como média ± desvio padrão (STD). Resultados com p valor <0,05 (*) e p <0,01 (**) foram considerados significativos.
Resultados e discussão
Caracterização de partículas de poli (ácido lático-co-glicólico)
Micrografias de fluorescência de partículas de PLGA (Fig. 1a, b, c) exibiram intensidade fluorescente robusta e nenhuma diminuição significativa nos sinais de fluorescência ao longo de 14 d após a preparação (Arquivo adicional 1:S1), sugerindo uma distribuição de tamanho relativamente homogênea e alta fluorescência estabilidade. Conforme denotado pelo fornecedor, 100, 500 e 1000 nm de partículas de PLGA mostraram os tamanhos de cerca de 80,6 ± 19,3 nm, 542,6 ± 128,3 nm e 951,9 ± 237,5 nm (Fig. 1d, e, f), respectivamente. De acordo com as medições do potencial zeta, as cargas superficiais médias nas partículas foram - 20,6 ± 5,3, - 17 ± 4,6 e - 16,5 ± 3,5 com índice de polidispersidade de 0,057, 0,056 e 0,062 para 100, 500 e 1000 partículas nm, respectivamente, as quais indicaram seus padrões altamente monodispersos. Todas as partículas foram submetidas a vórtex e sonicadas em banho-maria por 5 min para eliminar amplamente a agregação de partículas. No entanto, pequenos picos correspondentes a partículas de 100 e 1000 nm foram observados com diâmetros de cerca de 4-6 µm por causa da agregação de partículas inevitável em quantidades muito pequenas (cerca de 3-4%).
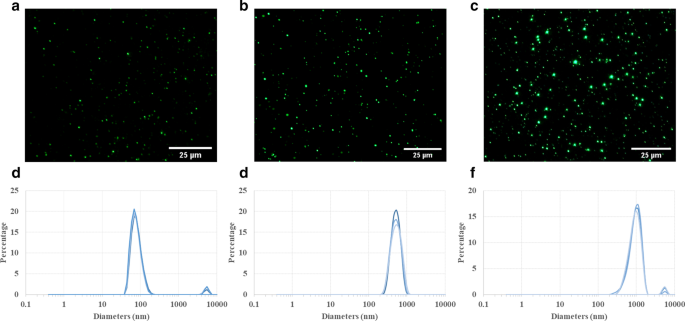
Caracterização de partículas PLGA. Micrografias de fluorescência mostram os diferentes tamanhos ( a 100 nm, b 500 nm e c 1 µm) de partículas PLGA. Essas partículas podem ser detectadas em Microscopia Óptica Olympus exibindo distribuições de tamanho de partícula relativamente uniforme em suspensão de água. Medidas de espalhamento dinâmico de luz (DLS) exibem a distribuição de tamanho ponderada por volume para 100 nm ( d ), 500 ( e ), 1 µm ( f ) Partículas PLGA. Apesar de uma pequena parte da agregação de partículas (picos menores:3–4%) em suspensões de PLGA de 100 nm e 1 µm, a distribuição geral do tamanho de partícula é bastante homogênea por causa do estreito pico principal
Avaliação da viabilidade celular e citotoxicidade
Devido à sua excelente biocompatibilidade e biodegradabilidade, as partículas de PLGA foram aprovadas pelo FDA e pela Agência Européia de Medicina para aplicações biomédicas [27, 28]. Partículas de PLGA têm sido, portanto, usadas atualmente na clínica e são amplamente aplicadas em estudos pré-clínicos como nanocarreadores que distribuem drogas para tumores ou regiões doentes específicas. No entanto, a eficiência de direcionamento e eficácia terapêutica das partículas de PLGA são impedidas, pelo menos parcialmente, pelo sistema imunológico. Por exemplo, a fagocitose de alta partícula por células de Kupffer no fígado restringiu enormemente os nano-fármacos transportadores de entrar no local do tumor [15]. Portanto, é de vital importância estabelecer modelos in vitro avançados para estudar a interação entre células cancerosas, células imunes e partículas para melhor mimetizar a situação in vivo de entrega de drogas. UM-SCC-17A é uma linha de células de carcinoma escamoso de laringe única isolada da amostra de câncer de laringe primária [29]. No entanto, informações sobre sua eficiência de absorção celular in vitro em sistemas de co-cultura ( por exemplo , a co-incubação de macrófagos e células cancerosas) ainda é insuficiente, uma questão que precisa ser tratada para melhorar a capacidade de previsão de respostas in vivo. Além disso, foi comprovado que o tamanho de partícula e o revestimento da superfície desempenham um papel importante na capacidade de entrega a tumores sólidos, locais doentes e células cancerosas em modelos animais e culturas de células [30,31,32,33]. Aqui, aplicamos, portanto, três tamanhos de PLGA a células de carcinoma UM-SCC-17A para investigar os efeitos do tamanho de partícula na captação celular e distribuição intracelular em sistemas de monocultura e co-cultura.
Este estudo determinou a viabilidade celular usando o método WST-1 (4- [3- (4-iodofenil) -2- (4-nitrofenil) -2H-5-tetrazolio] -1,3-benzeno dissulfonato) para monocultura THP-1 e células UM-SCC-17A, bem como uma co-cultura de ambos os tipos de células. Apesar de nenhuma morte celular óbvia ter ocorrido em grupos tratados com 100 e 500 nm de PLGA em todas as concentrações testadas, 500 nm e 1 µm de partículas de PLGA na concentração mais alta (20 µg / mL) reduziram significativamente a viabilidade celular na monocultura UM-SCC-17A células (Fig. 2a). Como esperado, a viabilidade das células THP-1 não foi significativamente afetada após 24 h de incubação com todos os três tipos de PLGA em concentrações de 5–20 µg / mL (≥ 95% de viabilidade em comparação com células não tratadas, cuja viabilidade é considerada 100% , Fig. 2b). Idêntica aos resultados das células UM-SCC-17A de monocultura, a viabilidade celular no sistema de co-cultura não foi alterada pela presença de partículas de 100 e 500 nm de PLGA nas três dosagens aqui utilizadas, embora tenha diminuído significativamente no grupo tratado com 20 µg / mL 1 µm PLGA (Fig. 2c).
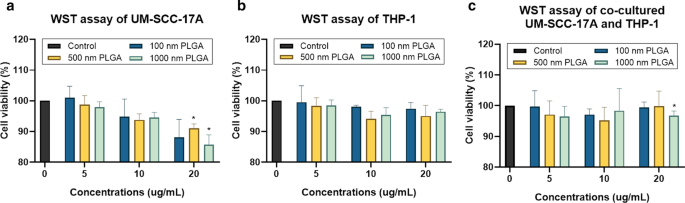
Determinação da viabilidade celular em células de monocultura e co-cultura utilizando o ensaio WST. UM-SCC-17A ( a ) e células THP-1 ( b ), e células UM-SCC-17A e THP-1 co-cultivadas ( c ) foram tratados com várias concentrações (5-20 µg / mL) de partículas de PLGA em três tamanhos
A avaliação da citotoxicidade das partículas utilizando o ensaio de LDH é determinar o vazamento da membrana celular medindo a quantidade de LDH extracelular [9]. A liberação dessa enzima citoplasmática no sobrenadante da cultura celular é característica de lesão da membrana celular, levando à morte celular irreversível. Apesar do ligeiro aumento dos níveis de LDH com dosagens mais altas em células de monocultura UM-SCC-17A tratadas com várias doses de 1 µm de PLGA, nenhuma citotoxicidade distinta para as células foi observada, mesmo na concentração mais alta de 20 µg / mL (Fig. 3a) . Não surpreendentemente, todos os três tamanhos de PLGA usados aqui em várias dosagens foram incapazes de induzir a liberação substancial de LDH no sobrenadante, indicando os efeitos tóxicos insignificantes para células THP-1 de monocultura, que também é altamente consistente com os resultados de viabilidade celular descritos acima (Fig . 3b). Nos experimentos de co-cultura, todas as partículas com diferentes concentrações mostraram excelente biocompatibilidade para ambas as células em termos de níveis de LDH liberados (Fig. 3c). Em geral, a ampla faixa de tamanho de partícula, de 100 nm a 1 µm, que foi usada aqui cobre os tamanhos típicos de nanotransportadores (50–200 nm), como lipossomas, micelas, dendrímeros, polímeros e minicélulas. Esta faixa também cobre partículas de tamanho sub-mícron (partículas de 500 nm podem ainda ser consideradas como NPs, por exemplo, partículas com tamanhos de cerca de 500 nm têm as mesmas vias de depuração no pulmão que as de NPs em 10–100 nm [34] e tamanho de mícron de 1 µm. Nenhuma dessas partículas de PLGA mostrou qualquer citotoxicidade óbvia para as células THP-1 e / ou UM-SCC-17A em sistemas de monocultura e co-cultura, exceto para as partículas de 500 nm e 1 µm de PLGA na concentração mais alta contra UM-SCC- 17A e células de co-cultura (mas mais de 85% das células sobreviveram), indicando que são favoráveis para aplicações em sistemas de distribuição de drogas.
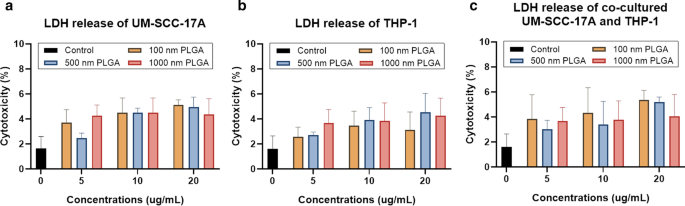
Determinação da citotoxicidade para células de monocultura e co-cultura usando o ensaio de LDH. UM-SCC-17A ( a ) e células THP-1 ( b ), e células co-cultivadas ( c ) foram tratados com partículas de PLGA. Nenhuma morte celular significativa foi observada após 24 h de incubação de partículas (com diferentes tamanhos e concentrações usadas aqui) e células em sistemas de monocultura e co-cultura
Capacidades de absorção celular de PLGA em sistemas de monocultura e cocultura
A Figura 4 mostra a morfologia celular (Fig. 4a, d, g), núcleos celulares e NPs de 100 nm (Fig. 4b, e, h) e imagens ampliadas mescladas (Fig. 4c, f, i) em monocultura e co- sistemas de cultura. Nenhuma partícula foi observada nas células não tratadas do grupo de controle (arquivo adicional 1:S2). Grandes aglomerados de NPs de PLGA de 100 nm de tamanho grande foram observados no citoplasma das células de monocultura de macrófagos (Fig. 4c). Enquanto isso, a monocultura UM-SCC-17A exibiu uma excelente capacidade de absorção de 100 nm PLGA, comprovada pelos sinais de fluorescência verde brilhante observados dentro da membrana celular (Fig. 4f). Para ilustrar melhor o acúmulo intracelular de partículas PLGA em células THP-1 ou UM-SCC-17A e partículas extracelulares nas co-culturas, sobreposições de imagens de campo claro com imagens de fluorescência foram aplicadas como no arquivo adicional 1:S3). No sistema de co-cultura, ambos os tipos de células são diferenciáveis em termos de morfologia e tamanho da célula nas imagens de campo claro, em que os macrófagos exibiram uma forma redonda e tamanho pequeno, enquanto as células cancerosas exibiram um tamanho grande e forma alongada. No entanto, as células cancerosas mostraram ingestão celular insuficiente devido à alta captação de 100 nm PLGA pelos macrófagos no sistema co-cultivado. Isso é esperado porque os macrófagos são considerados um tipo eficiente e específico de células imunes para realizar a função de fagocitose para limpar microorganismos estranhos, alérgenos e partículas. Da mesma forma, a Fig. 5 e a Fig. 6 mostram a análise qualitativa da capacidade de absorção celular de partículas de PLGA de 500 nm e 1 µm em culturas de células únicas ou mistas, respectivamente. É digno de nota que ambas as morfologias celulares não foram alteradas após o tratamento com diferentes tamanhos de partículas de PLGA na concentração de 10 mg / mL usada aqui (Fig. 4a, d, g, Fig. 5a, d, g, e Fig. 6a, d, g). Partículas de PLGA de 500 nm e 1 µm exibiram intensidade de fluorescência mais forte em células UM-SCC-17A únicas (Fig. 5e, f, e Fig. 6e, f) do que em células THP-1 únicas (Fig. 5b, c, e Fig. . 6b, c). Em incubações de co-cultura (Fig. 5h, i, e Fig. 6h, i), há aparentes diminuições de sinal nas células cancerosas, nas quais a intensidade da fluorescência da partícula foi menor do que a dos macrófagos. Os macrófagos fagocitaram todos os tipos de partículas de forma rápida e eficaz para que as células cancerosas não pudessem ingerir partículas suficientes no sistema de co-cultura. Para quantificar o efeito da fagocitose na capacidade de captação pelas células cancerosas para diferentes tamanhos de partículas de PLGA, foi realizada uma análise óptica semiquantitativa. Resumidamente, as intensidades de fluorescência de partícula foram calculadas com base em, por exemplo, 50 células carregadas de partículas individuais para atingir um valor médio para ambos os tipos de células, e o índice de captação de células cancerosas foi determinado pela média da intensidade fluorescente de partícula intracelular por câncer célula normalizada à dos macrófagos (Fig. 7). Na monocultura, o índice de captação de células cancerosas para PLGA 100 nm foi encontrado em cerca de 1,34 ± 0,19, sugerindo que as células cancerosas ingeriram mais partículas do que aquelas ingeridas por macrófagos na cultura de uma única célula (Fig. 7). Isso não é surpreendente devido ao alto nível de viscosidade das partículas de PLGA e ao tamanho maior das células cancerosas da laringe. Da mesma forma, 500 nm e 1 µm de PLGA também foram amplamente internalizados por células cancerosas com índices de absorção de aproximadamente 1,5 ± 0,25 e 1,4 ± 0,31, respectivamente, em monocultura. Os índices de absorção para partículas grandes diminuíram substancialmente (0,59 ± 0,12 e 0,47 ± 0,1) na presença de macrófagos em sistemas de co-cultura. Enquanto isso, capacidades de internalização celular idênticas para ambos os tipos de células após 24 h de incubação de partículas de PLGA de 100 nm na cultura de células mistas. Overall, the results accumulated here suggested that the ingestion of particles by cancer cells and macrophages might depend on different routes of uptake pathway in single-cell culture and co-culture environment. Moreover, the presence of macrophages reduced the cellular internalization of PLGA particles by cancer cells particularly for large ones, a biological event that has been observed in in vivo nanomedicine drug delivery studies [3, 15].
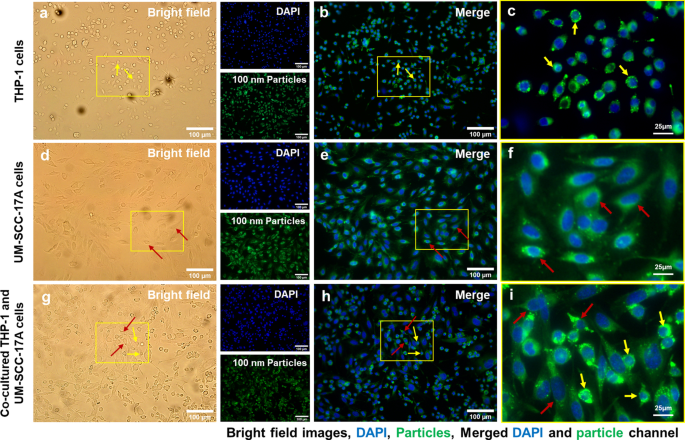
Microscopic examination of cellular internalization of 100 nm PLGA nanoparticles in monoculture and co-culture cells. Single type of cells or mixed cells was treated with 100 nm PLGA nanoparticles for 24 h at 37 °C at a concentration of 10 µg/mL. Cells were observed under bright-field (a , d , g ) and fluorescent channels (b, e, and h) with particles observed at the green channel and cell nuclei in the blue channel after stained with Hoechst. Massive cellular uptake of 100 nm PLGA nanoparticles can be visualized in magnified images (c , f , i ) for monoculture THP-1 macrophages (yellow arrows) and laryngeal cancer cells UM-SCC-17A (red arrows). In the co-culture system, 100 nm PLGA nanoparticles were still highly ingested by macrophages but less efficient for cancer cells compared to single cultured cells
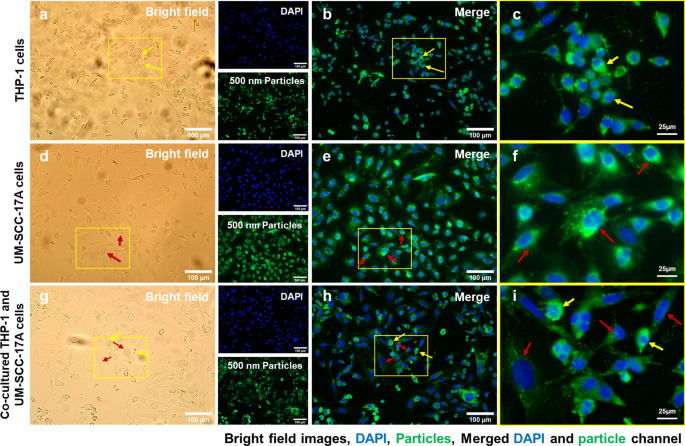
Microscopic examination of cellular internalization of 500 nm PLGA nanoparticles in monoculture and co-cultured cells. Single type of cells or mixed cells was treated with 500 nm PLGA nanoparticles for 24 h at 37 °C at a concentration of 10 µg/mL. Cells were observed under bright-field (a , d , g ) and fluorescent channels (b , e , h ) with particles observed at the green channel and cell nuclei in the blue channel after stained with Hoechst. Massive cellular ingestion of 500 nm PLGA nanoparticles can be visualized in magnified images (c , f , i ) for monoculture THP-1 macrophages (yellow arrows) and laryngeal cancer cells UM-SCC-17A cells (red arrows). In the co-culture system, 500 nm PLGA nanoparticles were still highly uptake by macrophages, while cancer cells had inadequate particle internalization
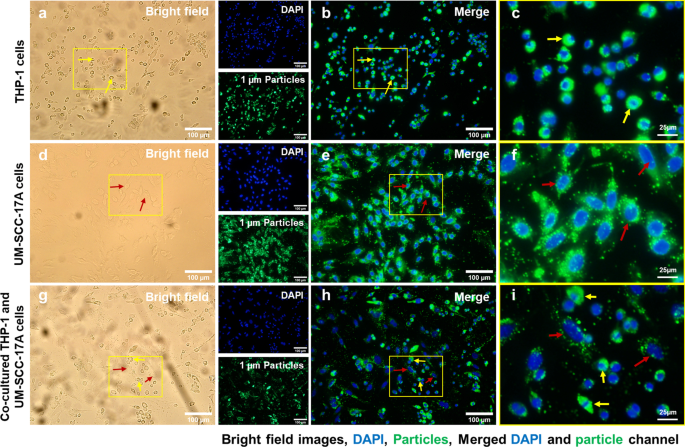
Microscopic examination of cellular internalization of 1 µm PLGA particles in monoculture and co-culture cells. Single type of cells or mixed cells was treated with 1 µm PLGA particles for 24 h at a concentration of 10 µg/mL. Cells were observed under bright-field (a , d , g ) and fluorescent channels (b , e , h ) with particles observed at the green channel and cell nuclei in the blue channel after stained with Hoechst. A large amount of particle uptake and tremendous accumulation of 1 µm PLGA particles can be visualized in magnified images (c , f , i ) for monoculture THP-1 (yellow arrows) and UM-SCC-17A laryngeal cancer cells (red arrows). In the co-culture system, 1 µm PLGA particles were still efficiently uptake by macrophages, while cancer cells had insufficient particle ingestion
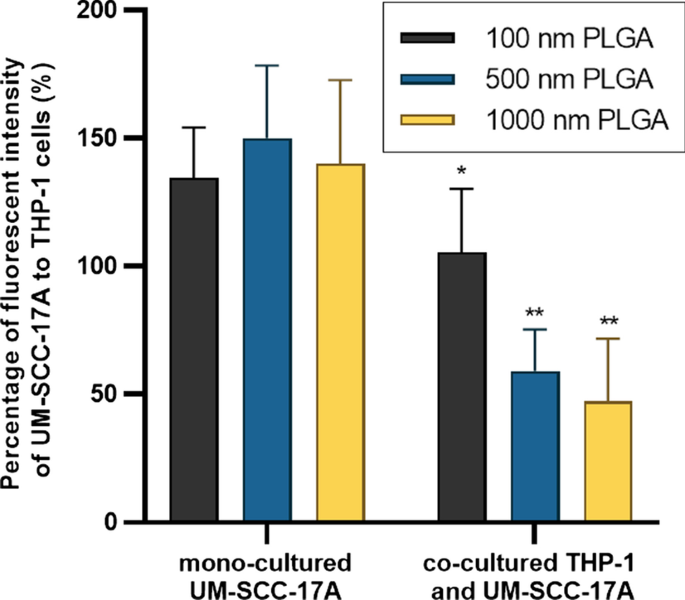
Quantitative analysis of PLGA particle internalization in UM-SCC-17A cells in monoculture and co-culture systems. The percentage of particle fluorescent intensity in UM-SCC-17A cells normalized to that in THP-1 cells for solely and mixed cultured cells
Quantification of cellular uptake by flow cytometry
Flow cytometry is widely used to determine of particle-cell interplay in a quantitative manner, for example, the size-dependent uptake of polystyrene particles with sizes ranging from 20 to 1000 nm by dendritic cells in vivo [35]. FACS was thus utilized for analysis of the percentage of NP-positive cells and particle number in those NP-positive cells in monoculture and co-culture systems. Then, average NP counts in a single cell were calculated by determining the total fluorescence intensity in particle-laden cells normalized to the fluorescence of total applied dose. For example, about 70% of 500 nm PLGA was deposited in the cancer cells, whereas the residual was kept in the supernatant of cell cultures (Additional file 1:S4). This fluorescence intensity measured by a Tecan reader was then compared to the average/total FACS signals (FITC signal values of P5 and P6 in Fig. 8,) to estimate the particle number in the co-culture system. As seeded in the co-cultured cells, about half of the cells were recognized as macrophages and the rest were considered as cancer cells. It was observed that approximately 13,000 of single 100 nm PLGA particles accumulated in cancer cells and 9700 particles in macrophages (Fig. 8i) in the monoculture, consistent with the above microscopic examinations. A much lower particle number (164 ± 30 and 45 ± 15) was ingested by monocultured cancer cells for 500 nm and 1 µm PLGA, with a slightly lower particle count in the respective macrophages (Fig. 8i). The number of particles ingested by single cells is in great agreement with the literature records [24]; for instance, an average 2500 of gold NPs coated with cetyltrimethylammonium bromide were deposited in epithelial cells, while PEG-modified gold NPs only had a few tens per cell [36]. In co-culture systems, unexpectedly, there is a slight increase of 100 nm particle number in cancer cells, despite a higher enhancement of NP internalization by macrophage. Comparing to the uptake index in the single-cell to mixed cell culture, it also reduces about 25% for 100 nm PLGA particles. The uptake indices were found to significantly decline with around 2.5 and 3 folds reduction in co-cultured system for 500 nm and 1 µm PLGA, respectively (Fig. 8i). Generally, it was found that the existence of macrophages largely affects the uptake ability of cancer cells especially for large particles, which is also in excellent agreement with the above observations.
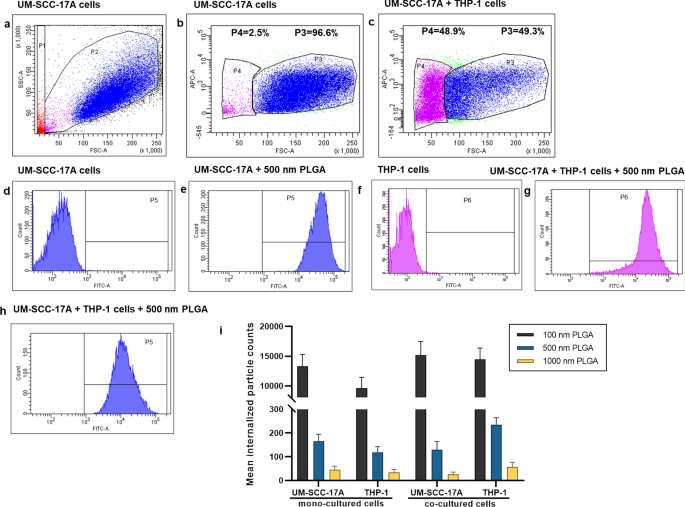
Particle uptake quantification in monoculture UM-SCC-17A cells and co-culture with THP-1 cells by flow cytometry. Grating strategy to identify respective cell populations in mixed cell culture (a - h ) Gating is showing one representative experiment of cells exposure to 500 nm PLGA particles. With initial live gating in the y-axis with a side scatter (SSC-A) and x-axis with a forward scattering (FSC-A), P2 a were further gated with FSC-A versus APC-A to differentiate the THP-1 cells in P4 c from UM-SCC-17A cell population in P3 (monoculture cells (b ) and mixed cells (c )). The cell population of P3 further displayed as counts versus FITC plots (P5) in non-exposed cells (d ), monoculture cells (e ), and co-cultured cells (h ) Also, P6 is the counts versus FITC-A plot originated from P4 population in non-exposed cells (g ) and co-cultured cells (f ) Both types of cells efficiently ingested the 500 nm PLGA indicated by the solid histogram completed shifted to the right side of the x -axis, indicating particles are taken up by all exposed cells. Quantification of particle-laden numbers (i ) in both types of cells for mono-culture and co-culture systems
Currently, different uptake pathways by cancer cells in ingesting particles with different sizes and surface modifications like clathrin-mediated endocytosis, caveolae-mediated endocytosis, clathrin- and caveolae-independent endocytosis, micropinocytosis, and macropinocytosis have been claimed in the literature [37]. For instance, it has been proved that iron oxide aggregates with a size of < 200 nm are taken up by MCF-7 cells through the clathrin-mediated endocytosis, whereas larger aggregates tend to be ingested via macropinocytosis [38]. Another study has demonstrated that 100 nm plain polystyrene particles tended to be taken up mainly through macropinocytosis, whereas the internalization of carboxylated polystyrene particles prefer to occur via the clathrin-mediated endocytic route [25]. Phagocytosis is a classical uptake pathway for immune cells such as neutrophils, dendritic cells, and most importantly monocytes/macrophages. The uptake pathways tightly depend on various parameters of drug delivery vesicles, e.g. , the particle size, chemical composition, surface modification, proteins in the culture environment, as well as cell type. Usually, multiple uptake pathways can be involved in particle ingestion such as the caveolae-mediated endocytosis, clathrin-mediated endocytosis, and macropinocytosis, which has been found to participate in cellular internalization of 300–400 nm chitosan NPs in human HeLa cells [39]. It has also been observed that 63 nm cholesterol-modified pullulan NPs enter into the human hepatocellular carcinoma (HepG2) cells via macropinocytosis and clathrin-mediated endocytosis [40]. Several previous studies showed that PLGA particle cell uptake involves different endocytic pathways, in which clathrin-independent endocytosis is the main route responsible for the internalization of PLGA in in vitro models [23, 24, 37]. Nevertheless, once they entered into the cells, PLGA particles applied here were highly potentially entrapped by the endo-lysosomal system consisting of early endosomes, recycling endosomes, late endosomes, and lysosomes [41]. It should be noted, however, that there is a lack of studies showing the cellular uptake mechanisms in co- or tri-cultured systems in vitro, a notion that has to be probe in the future.
Induction of cell fusion by PLGA NPs
Extensive scientific evidence has shown that the fusion of monocytes/macrophages into multinucleated giant cells (MGCs) occurred in a broad range of biological processes [42, 43]. Generally, implantation of biomaterials into the body causes a foreign body response characterized by the fusion of macrophages into MGCs and fibrotic encapsulation [44]. A wide type of human and murine primary cells like alveolar macrophages, splenic macrophages, microglia, bone-marrow-derived macrophages, and blood monocytes, as well as cell lines such as RAW264.7 and UG3 were also frequently observed to form MGCs in vitro [26, 45]. It is well-known that the macrophages form a fusogenic phenotype when they are unable to ingest foreign materials via phagocytosis because of the large size of particles or implants. So far, it is unclear whether in vitro macrophage cell fusion relates to the particle size in the range 100–1000 nm, which can be easily phagocytized. Here, the cell fusions were observed in all groups by microscopic examination (Fig. 9). The cellular fusion was confirmed only when multiple nuclei were found to share the same cytoplasm in both fluorescence images and bright-field images. Spontaneous formation of giant cells by THP-1 cells was occurred in the control group without particle treatment (Fig. 9a), with a fusion percentage of about 10% of the total cells (Fig. 9h), as reported in the literature [46]. Size-dependent cellular fusion was found for 100 and 500 nm PLGA particles, whereas 1 µm PLGA-induced insignificant enhancement of fusions in monoculture. This may be due to the small number of 1 µm PLGA particles exposed to cells (approximately 60 particles exposed to each cell at a concentration of 10 µg/mL). When the macrophages were co-cultured with cancer cells, the percentages of MGC formation were increased in all groups in comparison with the corresponding monoculture groups. In particular, there is a significant increment of cellular fusion for 1 µm PLGA (19%) in the mixed cell culture. The most prominent increase in fusion occurred in co-cultured 500 nm PLGA particles, which might be attributed to the large size of particles and sufficient particle numbers ingested per cell.
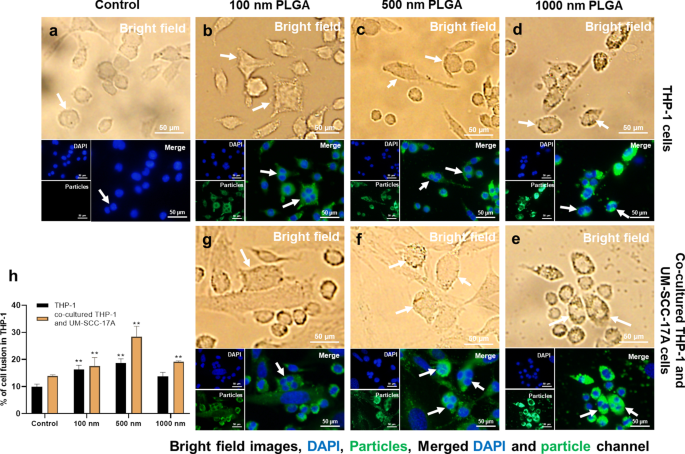
Visualization and quantification of THP-1 cell fusion in monoculture and co-culture systems. Cell fusion occurred in all groups including the control group without particle treatment for THP-1 cells (a ) Monocultured (b , c ) 100 nm and 500 nm NP-induced significant cell fusion compared to 1 µm PLGA group (d ), which has a slightly higher level than that of the control group. In co-cultured systems, 100 nm (g ) and 1 µm (e ) PLGA had an identical percentage of cellular fusion, which is apparently smaller than that of 500 nm group (f ) Quantification of cell fusion for all groups after 24 h incubation was displayed in h
The molecular machinery involved in macrophage fusion has been widely probed, achieving substantial progress [43]. For example, the formation of macrophage fusion receptors CD47and CD44 together allowed mediating the process of macrophage fusion, and subsequent the differentiation of giant cells [42] and miR-223 delivery by a NP vesicle permitted attenuating it [47]. Hence, further study should focus on the determination of key molecules in regulating particle-induced macrophage fusion and the dominant receptors expressed in the giant cell membrane. Another important concern is the fate of MGCs. It is believed that MGCs fused with particles or stimuli might subsequently experience the process of apoptosis or necrosis [48]. This may lead to the release of undigested particles or other giant materials to the other cells in vitro or biological tissues in vivo, further inducing the long-term inflammatory response or granulomas. On the other hand, the macrophage fusion itself may be benefit for NP drug delivery, for example, in tumorous tissues, the re-release of drugs from macrophages to the cancer cells might represent an enhanced tumor killing ability. More importantly, future nanomedicine study should address how to exploit the application of macrophage fusion for nanocarrier drug delivery to improved disease diagnosis and therapy. This is because not only macrophages an abundant type of immune cells in the body with the excellent uptake ability of nano-drugs, but also they may be used in targeted gene delivery for repair of injured tissues.
Conclusion
To the best of our knowledge, this study first reported the competitive cellular uptake of PLGA particles with sizes ranging from 100 nm to 1 µm in co-cultured UM-SCC-17A laryngeal cancer cells and THP-1 monocytes/macrophages. The data collected here proved that immune cells may alter/lower the particle internalization by cancer cells in vitro, which is similar to the previous findings in in vivo nanocarrier drug delivery studies. Size-dependent and cell culture-related macrophage cellular fusion caused by PLGA particles has also been demonstrated here. Future studies should probe the uptake mechanism in co-cultured systems and design novel approaches to achieve a higher uptake index for laryngeal cancer cells in the presence of phagocytes. Moreover, elaborate evaluation of intracellular trafficking and fate of nano-drug-carriers in co- or tri-cultured systems in 3D, which better mimic the in vivo conditions, is needed prior to the utilization of animal studies in vivo and even in clinical trials.
Disponibilidade de dados e materiais
All data generated or analyzed during this study are included in this published article [and its supplementary information files].
Abreviações
- PLGA:
-
Poly(lactic-co-glycolic acid)
- HNSCC:
-
Head and neck squamous cell carcinoma
- EPR:
-
Enhanced permeability and retention
- NPs:
-
Nanopartículas
- ICG:
-
Indocyanine green
- MPS:
-
Mononuclear phagocyte system
- LDH:
-
Lactate dehydrogenase
- FACS:
-
Fluorescence-activated cell sorting
- MGC:
-
Multinucleated giant cells
- DLS:
-
Dynamic light scattering
Nanomateriais
- Nanofibras e filamentos para entrega aprimorada de drogas
- Demonstração de um biossensor flexível à base de grafeno para detecção sensível e rápida de células cancerosas do ovário
- Nanopartículas para terapia do câncer:progresso e desafios atuais
- Nanopartículas de FePO4 biocompatíveis:entrega de drogas, estabilização de RNA e atividade funcional
- Administração de medicamentos baseados em células para solicitações de câncer
- Nanopartículas lipídicas de PLGA rastreadas com 131I como transportadores de administração de drogas para o tratamento quimioterápico direcionado do melanoma
- Bioflavonóide direcionado ao receptor de folato Nanopartículas de quitosana carregadas com genisteína para efeito anticâncer avançado em cânceres cervicais
- Comparação entre o ácido fólico e a funcionalização baseada no peptídeo gH625 de nanopartículas magnéticas Fe3O4 para internalização celular aprimorada
- Potencial antiproliferativo e de desencadeamento de apoptose de nanopartículas lipídicas direcionadas à base de paclitaxel com internalização celular aprimorada por receptores de transferrina - u…
- Influência de Mg Doping em Nanopartículas de ZnO para Avaliação Fotocatalítica Aprimorada e Análise Antibacteriana



