Emissão de infravermelho próximo Cr3 + / Eu3 + Co-dopado com galogermanato de zinco Nanopartículas luminescentes de persistência para imagem celular
Resumo
Nanopartículas luminescentes emissoras de infravermelho próximo (NIR) foram desenvolvidas como agentes potenciais para bioimagem. No entanto, falta sintetizar nanopartículas uniformes com luminescência longa para imagens de longo prazo. Aqui, demonstramos a síntese de Zn estruturado em espinélio 3 Ga 2 Ge 2 O 10 :Cr 3+ (ZGGO:Cr 3+ ) e Zn 3 Ga 2 Ge 2 O 10 :Cr 3+ , Eu 3+ (ZGGO:Cr 3+ , Eu 3+ ) nanopartículas por um método sol-gel em combinação com uma subsequente calcinação livre de atmosfera redutora. As amostras foram investigadas por meio de caracterizações detalhadas por técnicas combinadas de XRD, TEM, STEM, difração de elétrons de área selecionada, espectroscopia de excitação por fotoluminescência (PLE) / fotoluminescência (PL) e análise de PL dependente da temperatura. As nanopartículas monocristalinas são solução sólida homogênea, possuindo forma cúbica uniforme e tamanho lateral de ~ 80-100 nm. Após excitação UV a 273 nm, ZGGO:Cr 3+ , Eu 3+ exibiu uma banda de emissão NIR em 697 nm ( 2 E → 4 A 2 transição de distorção Cr 3+ íons em galogermanato), na ausência de Eu 3+ emissão. A luminescência persistente NIR da amostra pode durar mais de 7200 se ainda manter intensidade intensa. Eu 3+ a incorporação aumentou a intensidade de luminescência persistente e o tempo de pós-luminescência de ZGGO:Cr 3+ , mas não afetou significativamente a estabilidade térmica. O ZGGO obtido:Cr 3+ , Eu 3+ -NH 2 nanopartículas possuíam uma excelente capacidade de imagem para células in vitro.
Histórico
Materiais luminescentes persistentes podem emitir por um longo tempo até horas após a interrupção da excitação [1]. Principalmente devido aos seus grandes interesses de pesquisa, os fósforos têm sido comercializados como materiais de visão noturna ou escura para uma ampla gama de aplicações, como sinalização de segurança, sinalização de rota de emergência, marcadores de identificação ou diagnósticos médicos [2]. Os fósforos de longa persistência típicos são os emissores de cores primárias comercializados, como o vermelho Y 2 O 2 S:Eu 3+ , Mg 2+ , Ti 4+ ou CaS:Eu 2+ , Tm 3+ , Ce 3+ [3, 4], o SrAl 2 verde O 4 :Eu 2+ , Dy 3+ ou MgAl 2 O 4 :Mn 2+ [5, 6], e o CaAl azul 2 O 4 :Eu 2+ , Nd 3+ ou SrMgSi 2 O 6 :Eu 2+ , Dy 3+ [7, 8] fósforos. Embora muitos sucessos tenham sido feitos em fósforos persistentes visíveis, a investigação e o desenvolvimento de fósforos persistentes na região do infravermelho próximo (NIR) (~ 700–2500 nm) são insuficientes. Nos últimos anos, as aplicações potenciais de fósforos persistentes mostrando luminescência vermelha ou NIR se expandiram de sinais de segurança de visão noturna para sistemas de imagem in vivo [1, 9, 10].
Materiais luminescentes persistentes com fotossensibilizadores anexados como um agente in vivo foram inicialmente testados por Chen e Zhang para terapia fotodinâmica [11]. Então, Scherman et al. relatou um trabalho marcante na bioimagem in vivo com o fósforo emissor de NIR de Ca 0,2 Zn 0,9 Mg 0,9 Si 2 O 6 :Eu 2+ , Mn 2+ , Dy 3+ [12]. Logo depois, dois novos fósforos emissores de NIR de CaMgSi 2 O 6 :Eu 2+ , Mn 2+ , Pr 3+ e Ca 2 Si 5 N 8 :Eu 2+ , Tm 3+ com melhor desempenho foram desenvolvidos pelo mesmo grupo [13, 14]. Recentemente, Cr 3+ - fósforos persistentes de galato dopado com emissão NIR e pós-luminescência longa, incluindo espinélio ZnGa 2 O 4 :Cr 3+ e suas variantes, como Zn 3 Ga 2 Ge 2 O 10 :Cr 3+ , Zn 3 Ga 2 GeO 8 :Cr 3+ , Yb 3+ , Er 3+ e ZnGa 2 - x (Ge / Sn) x O 4 :Cr 3+ , foram preparados por um método de estado sólido [1, 9, 10, 15,16,17,18,19,20,21]. As amostras de disco de cerâmica exibiram tempo de pós-luminescência de até 360 h na região NIR, mas os materiais volumosos são inadequados para bioimagem in vivo. Nanopartículas luminescentes de longa persistência que emitem NIR de ZnGa 2 O 4 :Cr 3+ [22, 23], ZnGa 2 O 4 :Cr 3+ , Sn 4+ [19,20,21] e Zn 2,94 Ga 1,96 Ge 2 O 10 :Cr 3+ , Pr 3+ [9] foram sintetizados por um método sol-gel em combinação com uma subsequente calcinação livre de atmosfera redutora. A luminescência persistente do pó das nanopartículas exibe luminescência NIR brilhante na janela de transparência biológica com um tempo de pós-luminescência superlongo. A PEGilação melhora muito a biocompatibilidade e a solubilidade em água das nanopartículas, que possuem grande potencial para aplicação de bioimagem in vivo de longo prazo com alto SNR sem a necessidade de excitação in situ. Acredita-se que íons selecionados de um grupo que consiste em íons alcalino-terrosos, íons lantanídeos e Li + co-dopagem com Cr 3+ em galato de zinco e galogermanato de zinco produziria luminescência persistente NIR notável [1]. Eu 3+ em hospedeiros óxidos sempre exibe uma emissão vermelha em ~ 700 nm decorrente do 5 D 0 - 7 F 4 intra-4 f transição eletrônica após curta excitação de UV na banda de transferência de carga (CT) em 250 nm [24]. Por outro lado, Cr 3+ é um centro luminescente favorável em sólidos por causa de suas emissões de banda estreita (geralmente em 700 nm) devido ao spin proibido 2 E- 4 A 2 transição, ou uma emissão de banda larga (650–1600 nm) devido ao spin permitido 4 T 2 - 4 A 2 transição [1, 20]. Em vista disso, Cr 3+ / Eu 3+ galato de zinco co-dopado e galogermanato de zinco produziria intensa luminescência NIR persistente, devido a que a banda de transferência de carga (CTB) de O 2− -Eu 3+ sobrepõe-se ao CTB de O 2− -Ga 3+ , e a emissão em ~ 700 nm de 5 D 0 - 7 F 4 transição de Eu 3+ sobrepõe-se ao de 2 E- 4 A 2 transição de Cr 3+ . Além disso, eu 3+ íons substituindo Ga 3+ íons em sítios octaédricos distorcidos podem render força de campo de cristal hospedeiro adequada em torno de Cr 3+ íons, afetando assim a emissão de NIR. Neste trabalho, Zn 3 Ga 2 Ge 2 O 10 :Cr 3+ , Eu 3+ (denominado como ZGGO:Cr 3+ , Eu 3+ ) nanopartículas foram sintetizadas por um método sol-gel em combinação com uma subsequente calcinação livre de atmosfera redutora, que seria usada como nanossondas promissoras para bioimagem futura. As amostras foram investigadas por meio de caracterizações detalhadas por técnicas combinadas de difratometria de raios-X (XRD), microscopia eletrônica de transmissão (TEM), STEM, difração de elétrons de área selecionada (SAED), excitação de fotoluminescência (PLE) / espectroscopia de fotoluminescência (PL) e temperatura análise de PL dependente. Nas seções a seguir, relatamos a síntese, caracterização e aplicação do ZGGO:Cr 3+ , Eu 3+ nanopartículas.
Experimental
Síntese
As fontes de metal inicial são Zn (NO 3 ) 2 · 6H 2 O, Cr (NÃO 3 ) 3 · 9H 2 O, Ga 2 O 3 , Eu 2 O 3 , e GeO 2 foram todos os produtos 99,99% puros adquiridos da Sinopharm (Xangai, China). Os outros reagentes são de qualidade analítica e foram adquiridos na Shenyang Chemical Reagent Factory (Shenyang, China). Zn (NÃO 3 ) 2 · 6H 2 O e Cr (NÃO 3 ) 3 · 9H 2 O foram dissolvidos em água desionizada. Ga 2 O 3 e Eu 2 O 3 foram dissolvidos em solução de ácido nítrico. GeO 2 e ácido etilenodiaminotetracético (EDTA) foram dissolvidos em hidróxido de amónio diluído. À solução de mistura, a solução de EDTA foi adicionada lentamente sem qualquer precipitação, e a razão molar de íons metálicos totais para EDTA foi mantida a 1:2. A razão molar do átomo de Zn:Ga:Ge:Cr:Eu foi fixada em 3:1,984:2:0,01:0,006. A solução final foi agitada vigorosamente à temperatura ambiente durante 1 h, depois aquecida em um forno a 85 ° C para a evaporação lenta da água até a solução se tornar um sol que finalmente se tornou um gel. O gel obtido foi aquecido a 200 ° C durante 3 h para formar materiais pretos porosos. Finalmente, os materiais porosos foram moídos e recozidos sob fluxo O 2 gás (200 mL / min) em temperaturas selecionadas por 2 h.
Funcionalização de superfície
O ZGGO:Cr 3+ , Eu 3+ o pó foi moído durante 30 min, depois 150 mg da amostra obtida foram adicionados a 50 mL de solução de NaOH 0,1 mol / L. Após sonicação durante 1 h, a suspensão foi vigorosamente agitada durante 24 h à temperatura ambiente. A solução colóide resultante foi centrifugada a 1000 rpm durante 10 min para remover partículas de grande tamanho e o sobrenadante foi centrifugado a 10.000 rpm durante 10 min para recolher o precipitado. O ZGGO obtido:Cr 3+ , Eu 3+ Nanopartículas de -OH foram lavadas três vezes com água desionizada.
Dez miligramas de ZGGO:Cr 3+ , Eu 3+ Nanopartículas de -OH foram dispersas em 4 mL de dimetilformamida (DMF) com o auxílio de sonicação por 10 min. Em seguida, 40 μl de 3-aminopropil-trietoxissilano (APTES) foram adicionados sob agitação vigorosa por 24 h em temperatura ambiente. O ZGGO obtido:Cr 3+ , Eu 3+ -NH 2 nanopartículas foram coletadas por centrifugação a 10.000 rpm por 10 min e lavadas com DMF três vezes para remover APTES que não reagiram.
Imagem celular
As células Hek293T foram cultivadas em DMEM com 10% de FBS e semeadas em placas de cultura de 35 mm por 2 h em um CO 2 incubadora. O ZGGO obtido:Cr 3+ , Eu 3+ -NH 2 as nanopartículas foram dispersas em meio celular (50 mg / mL), as quais foram excitadas por 10 min por uma lâmpada UV de 254 nm e então movidas para placas de cultura tratadas por 1 h. Após a remoção do meio celular, foi adicionado 0,1 mL de formaldeído-PBS a 1% e as células foram coradas com 0,5 mL de corante DAPI no escuro por 10 min. Finalmente, as células foram lavadas com PBS várias vezes para posterior caracterização.
Todos os estudos envolvendo animais foram aprovados pelo comitê de uso e cuidado de animais da universidade.
Técnicas de caracterização
A identificação da fase foi realizada por XRD (modelo SmartLab; Rigaku, Tóquio, Japão) operando a 40 kV / 40 mA usando radiação Cu Kα filtrada por níquel e uma velocidade de varredura de 6,0 ° 2 θ / min. Morfologias dos produtos foram observadas via TEM (modelo JEM-2000FX; JEOL, Tóquio). A fotoluminescência dos fósforos foi analisada com um fluorospectrofotômetro FP-8600 (JASCO, Tóquio). Os sinais de luminescência persistentes foram obtidos usando Horiba JY FL3-21. As imagens de decaimento da pós-luminescência foram gravadas em uma sala escura usando um Kodak In-Vivo Imaging System FX Pro. A imagem das células foi conduzida por um microscópio confocal de varredura a laser (LEICA TCS SP2, Alemanha).
Todos os estudos envolvendo animais foram aprovados pelo comitê de uso e cuidado de animais da universidade.
Resultados e discussão
A pureza de fase das amostras foi investigada pela primeira vez por XRD. A Figura 1 (acima) mostra os padrões de XRD do ZGGO conforme preparado:Cr 3+ e ZGGO:Cr 3+ , Eu 3+ calcinados a 1000 ° C, os quais foram identificados juntamente com o Zn estruturado em espinélio 3 Ga 2 Ge 2 O 10 [1, 9]. A estrutura cristalina do Zn 3 Ga 2 Ge 2 O 10 é o mesmo com o de ZnGa 2 O 4 (JCPDS No. 38-1240), que é a solução sólida de ZnGa 2 O 4 e Zn 2 GeO 4 . Na estrutura do Zn 3 Ga 2 Ge 2 O 10 , Ge desempenha o papel de substituição de Ga, propício à formação de armadilhas, enquanto ZnGa 2 O 4 é a estrutura cristalina dominante [1]. Existem dois tipos de cátions em uma célula de uma unidade; Zn 2+ e Ga 3+ são circundados por quatro e seis ânions de oxigênio, formando um tetraedro e um octaedro, respectivamente (Fig. 1, abaixo). Cálculos dos dados de difração produzindo as constantes de células para ZGGO:Cr 3+ são um = b =~ 0,8335 nm, próximo ao do espinélio ZnGa 2 O 4 ( a = b =~ 0,8335 nm, JCPDS No. 38-1240). Devido aos raios iônicos maiores de Eu 3+ (para coordenação sêxtupla, \ ({r} _ {{\ mathrm {Eu}} ^ {3+}} \) =0,0947 nm e \ ({r} _ {{\ mathrm {Ga}} ^ {3+} } \) =0,062 nm) [25], um valor maior de a = b =~ 0,8336 nm foi observado para ZGGO:Cr 3+ , Eu 3+ . A análise de alargamento de perfil da reflexão de (311) Bragg foi conduzida aplicando a equação de Scherrer para tamanhos médios de cristalito de 83 ± 6 nm para ZGGO:Cr 3+ e ZGGO:Cr 3+ , Eu 3+ amostras. Na Fig. 1 (acima), também descobrimos que os produtos resultantes calcinados a 900 ° C são a mistura da fase espinélio (JCPDS No. 38-1240) e romboédrica (JCPDS No. 11-0687), indicando uma temperatura de calcinação de ≥ 1000 ° C é necessário para produzir espinélio Zn 3 Ga 2 Ge 2 O 10 em uma fase de forma pura.
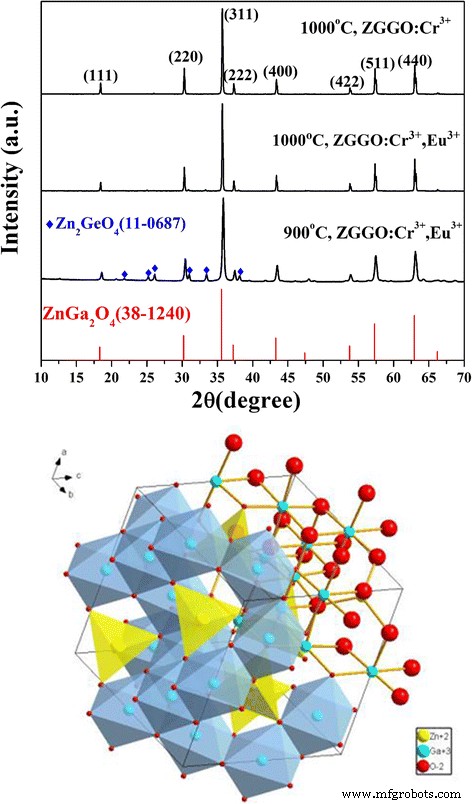
Padrões de XRD do ZGGO conforme preparado:Cr 3+ e ZGGO:Cr 3+ , Eu 3+ e a estrutura cristalina do espinélio ZnGa 2 O 4
A Figura 2 (à esquerda) mostra a morfologia TEM para ZGGO:Cr 3+ , Eu 3+ partículas, indicando claramente que consistem inteiramente em partículas cúbicas, com tamanhos laterais de ~ 80-100 nm. Os cantos agudos e as franjas de rede bem resolvidas sugerem sua excelente cristalinidade, enquanto os espaçamentos de ~ 0,29 nm correspondem bem à (220) planície de ZnGa estruturado em espinélio 2 O 4 ( d (220) =~ 0,29 nm, JCPDS No. 38-1240) (inserção na Fig. 2). Como os tamanhos de partícula estão próximos aos tamanhos médios de cristalito calculados a partir dos dados de XRD, as amostras obtidas podem ser monocristalinas. A análise SAED (Fig. 2 (direita)) confirmou ainda que as nanopartículas em análise são monocristalinas. As nanopartículas investigadas aqui são soluções diretas de estado sólido, em vez de uma mistura mecânica. O mapeamento elementar de Zn, Ga, Ge, Cr e Eu fornece evidências desta solução sólida, conforme revelado na Fig. 3 para ZGGO:Cr 3+ , Eu 3+ . Não apenas cada partícula contém Zn, Ga, Ge, Cr e Eu, mas todos os elementos são igualmente distribuídos entre as partículas.

TEM, imagem HR-TEM (esquerda) e padrão SAED (direita) do ZGGO:Cr 3+ , Eu 3+ nanopartículas

Morfologia das partículas STEM (imagem de campo claro, a primeira imagem) e mapeamento elementar de ZGGO:Cr 3+ , Eu 3+ nanopartículas
A Figura 4 mostra os espectros de excitação do ZGGO:Cr 3+ e ZGGO:Cr 3+ , Eu 3+ pó à temperatura ambiente. O espectro de excitação monitorado em 697 nm cobre uma região espectral muito ampla (de 200 a 650 nm) e consiste em quatro bandas de excitação principais com pico em 273, 328, 410 e 569 nm, respectivamente. A banda de excitação em 273 nm é atribuída à banda de transferência de carga de O 2− -Ga 3+ em ZnGa 2 O 4 hospedeiro, enquanto as bandas posteriores se originam das transições internas de Cr 3+ , incluindo a banda de 328 nm originada do 4 A 2 → 4 T 1 ( te 2 ) transição, a banda de 410 nm originada do 4 A 2 → 4 T 1 ( t 2 e ), e a banda de 569 nm originada do 4 A 2 → 4 T 2 ( t 2 e ) [19, 20]. Incorporação da Eu 3+ não alterou significativamente as posições das bandas PLE, mas aumentou significativamente as intensidades das transições internas de Cr 3+ , com I 410 / eu 273 aumentando de 0,18 para 0,56. Os resultados acima indicam que Eu 3+ a incorporação conduz à excitação da luz visível. No entanto, a banda de excitação mais forte em 273 nm também revelou que a banda de transferência de carga de O 2− -Ga 3+ é o comprimento de onda de excitação mais eficaz. A excitação do pó a 273 nm deu uma banda de emissão NIR a 697 nm (Fig. 5) devido ao 2 E → 4 A 2 transição em distorcido Cr 3+ íons em galogermanato, na ausência de Eu 3+ emissão.
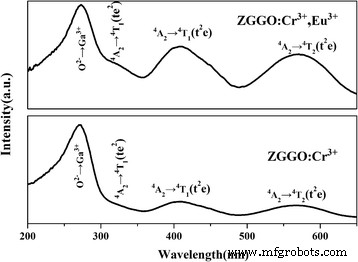
Espectros de excitação por fotoluminescência (PLE) de ZGGO:Cr 3+ e ZGGO:Cr 3+ , Eu 3+ pós
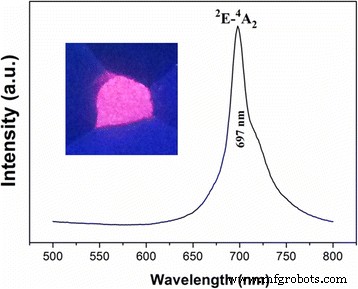
Espectros de fotoluminescência (PL) de ZGGO:Cr 3+ , Eu 3+ pós
As curvas de decaimento de luminescência persistente NIR de ZGGO:Cr 3+ e ZGGO:Cr 3+ , Eu 3+ nanopartículas foram monitoradas a 697 nm após iluminação de luz UV de 254 nm (lâmpada de xenônio como fonte de luz) por 5 min em temperatura ambiente, conforme mostrado na Fig. 6. O resultado demonstra que a luminescência persistente NIR do ZGGO:Cr 3 + a amostra pode durar mais de 7200 se ainda manter uma intensidade apreciável. A intensidade de luminescência persistente de ZGGO:Cr 3+ , Eu 3+ aumenta com a incorporação de Eu 3+ íon. Acredita-se que íons lantanídeos co-dopam com Cr 3+ no galogermanato de zinco produziria notável luminescência persistente NIR, devido ao seu importante papel no aumento da quantidade de defeitos anti-sítio, que são responsáveis pela luminescência persistente de Cr 3+ no hospedeiro galogermanato de zinco [1]. Por outro lado, luminescência persistente NIR de ZGGO:Cr 3+ , Eu 3+ a amostra pode durar mais do que ZGGO:Cr 3+ , indicando que Eu 3+ a incorporação pode aumentar o tempo de pós-luminescência. A Figura 7 mostra imagens de decadência de pós-luminescência NIR de ZGGO:Cr 3+ , Eu 3+ pós obtidos por um Kodak In-Vivo Imaging System FX Pro em momentos diferentes após a interrupção da irradiação UV, confirmando ainda que a luminescência pode durar mais de 120 min e manter uma intensidade de emissão NIR intensa.
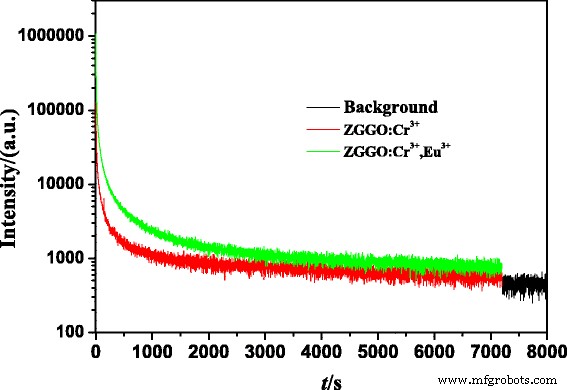
Curvas de decaimento de luminescência persistente NIR de ZGGO:Cr 3+ e ZGGO:Cr 3+ , Eu 3+ pós monitorados a 697 nm após iluminação de luz UV de 254 nm por 5 min

Imagens de decadência de pós-luminescência NIR de ZGGO:Cr 3+ , Eu 3+ pós obtidos por um Kodak In-Vivo Imaging System FX Pro em momentos diferentes após a interrupção da irradiação UV
Para avaliar o desempenho da aplicação de fósforo, especialmente para aplicações de alta potência, a estabilidade térmica é um parâmetro chave. Para avaliar o comportamento de têmpera térmica dos fósforos neste trabalho, os espectros de PL foram analisados em temperaturas variando de 298 a 573 K (Fig. 8). Para todas as amostras, a elevação da temperatura produziu uma diminuição nas intensidades de emissão em 697 nm. Para obter uma imagem mais abrangente do comportamento de têmpera térmica e estimar o valor de sua energia de ativação ( E a ), a equação de Arrhenius (Eq. (1)) foi empregada da seguinte forma [26,27,28]:
$$ {I} _ {\ mathrm {T}} =\ frac {I_0} {1 + c \ exp \ left (- \ frac {E _ {\ mathrm {a}}} {kT} \ right)} $$ (1)
onde eu 0 e eu T são as intensidades das temperaturas inicial e final, respectivamente; c é a constante de taxa; E a é a energia de ativação; e k é a constante de Boltzmann (8,629 × 10 −5 eV K −1 ) A Figura 8 mostra o In ( I 0 / eu T - 1) vs 10.000 / T linhas de relacionamento para a banda de emissão centrada em 697 nm para ZGGO:Cr 3+ e ZGGO:Cr 3+ , Eu 3+ . Energias de ativação semelhantes foram calculadas: E a =0,23 eV para ZGGO:Cr 3+ e E a =0,25 eV para ZGGO:Cr 3+ , Eu 3+ . A probabilidade de que ocorra uma transição não radiativa por unidade de tempo ( α ) pode ser definido de acordo com a Eq. (2) da seguinte forma [29]:
$$ \ alpha =s \ \ exp \ left (- \ frac {E _ {\ mathrm {a}}} {kT} \ right) $$ (2)
onde s é o fator de frequência (s −1 ), k é a constante de Boltzmann, e T é a temperatura. Pode ser visto que uma energia de ativação mais baixa ( E a ) leva a uma probabilidade maior ( α ) de uma transição não radiativa. Por causa da energia de ativação semelhante, ZGGO:Cr 3+ e ZGGO:Cr 3+ , Eu 3+ exibiu estabilidade térmica fechada, indicando Eu 3+ a incorporação não afetou significativamente a estabilidade térmica. No entanto, as bandas laterais de fônon associadas (PSBs) centradas em 670 nm tornaram-se dominantes em uma temperatura mais alta, induzindo, assim, picos de emissão aumentados.
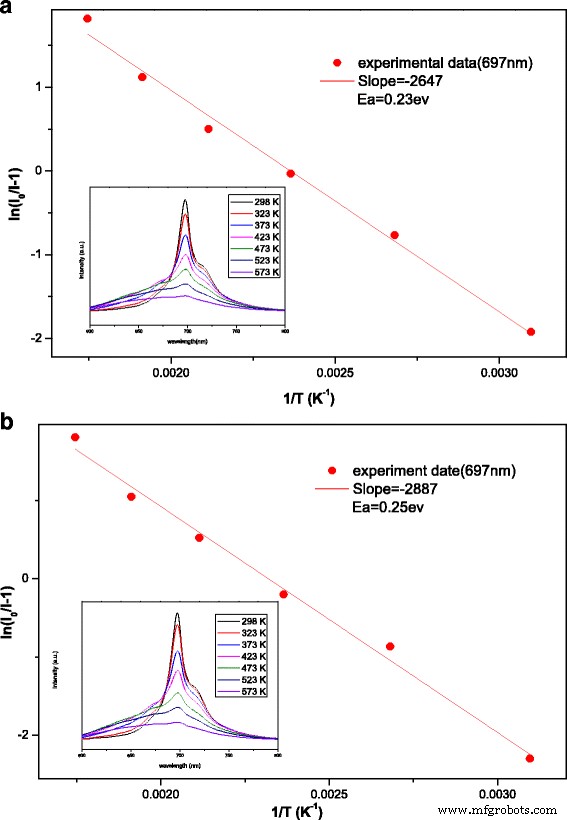
Energia de ativação de extinção térmica para bandas de emissão em a ZGGO:Cr 3+ e b ZGGO:Cr 3+ , Eu 3+ pós. As inserções mostram a dependência da temperatura correspondente dos espectros PL de 298 a 573 K
Nós também investigamos os espectros de excitação e emissão de PL da dispersão aquosa de ZGGO:Cr 3+ , Eu 3+ (Fig. 9). Comparado com o ZGGO:Cr 3+ , Eu 3+ pó, a dispersão aquosa exibiu quase o mesmo perfil das curvas de excitação e emissão de PL, exceto a intensidade de excitação relativamente fraca a 300 e 600 nm. A intensidade enfraquecida é provavelmente devido ao efeito de extinção da vibração O – H da água.
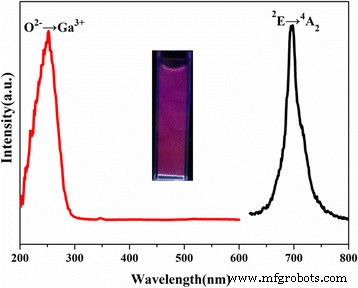
Espectro de excitação e emissão de ZGGO:Cr 3+ , Eu 3+ solução aquosa à temperatura ambiente. A inserção mostra as fotos digitais do ZGGO:Cr 3+ , Eu 3+ solução aquosa sob irradiação de luz UV 254 nm
As células Hek293T foram empregadas aqui para teste de imagem in vitro. O ZGGO obtido:Cr 3+ , Eu 3+ -NH 2 as nanopartículas foram dispersas em meio celular (50 mg / mL), as quais foram excitadas por 10 min por uma lâmpada UV de 254 nm e então movidas para placas de cultura tratadas por 1 h. A Figura 10 (esquerda, cor vermelha) mostra a imagem de luminescência celular coletada em um microscópio confocal de varredura a laser na ausência de excitação. O sinal de luminescência pós-luminescência das células Hek293T ainda era forte o suficiente para ser medido com precisão após 1 h, embora os sinais de luminescência pós-luminescência diminuíssem gradualmente ao longo do tempo. Para comparação, a imagem de luminescência celular foi coletada em um microscópio confocal de varredura a laser por outro modo das mesmas células coradas com 0,5 mL de corante DAPI (à direita na Fig. 10, excitação simultânea). Os sinais de imagem semelhantes sugeriram que o ZGGO:Cr 3+ , Eu 3+ -NH 2 nanopartículas possuíam uma excelente capacidade de imagem para células in vitro.
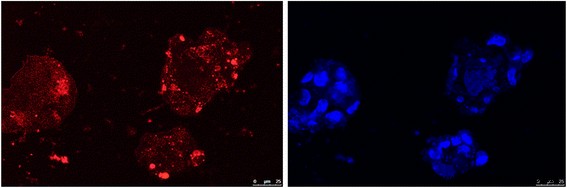
Imagem LSCM (esquerda, cor vermelha) de células Hek293T incubadas com ZGGO:Cr 3+ , Eu 3+ -NH 2 nanopartículas por 1 h. A imagem certa (cor azul) é a aparência das mesmas células coradas com 0,5 mL de corante DAPI. Barra de escala =25 μm
Conclusões
Neste trabalho, ZGGO estruturado em espinélio:Cr 3+ e ZGGO:Cr 3+ , Eu 3+ nanopartículas foram sintetizadas por um método sol-gel em combinação com uma subsequente calcinação livre de atmosfera redutora. As amostras foram investigadas por meio de caracterizações detalhadas por técnicas combinadas de XRD, TEM, STEM, SAED, espectroscopia PLE / PL e análise de PL dependente da temperatura. As nanopartículas com forma cúbica uniforme e tamanho lateral de ~ 80-100 nm são de solução única cristalina e homogênea. A excitação do pó a 273 nm deu uma banda de emissão NIR a 697 nm devido ao 2 E → 4 A 2 transição em distorcido Cr 3+ íons em galogermanato, na ausência de Eu 3+ emissão. NIR luminescência persistente do ZGGO:Cr 3+ , Eu 3+ pode durar mais de 7200 se ainda manter intensidade intensa. A intensidade de luminescência persistente de ZGGO:Cr 3+ e o tempo de pós-luminescência aumenta com a incorporação de Eu 3+ íon. No entanto, eu 3+ a incorporação não afetou significativamente a estabilidade térmica. Finalmente, o ZGGO obtido:Cr 3+ , Eu 3+ -NH 2 nanopartículas possuíam uma excelente capacidade de imagem para células in vitro.
Nanomateriais
- Cientistas da IBM são os primeiros a demonstrar motores brownianos para nanopartículas
- Nanopartículas de ouro para sensores quimio
- Nanopartículas para terapia do câncer:progresso e desafios atuais
- Nanopartículas carregadas de drogas de Donepezila emulsificadas com Donepezila direcionada para o cérebro
- Nanotecnologia:do Sistema de Imagem In Vivo à Entrega Controlada de Medicamentos
- Estudo in vitro da influência das nanopartículas de Au nas linhas celulares HT29 e SPEV
- Novel Biocompatible Au Nanostars @ PEG Nanopartículas para imagens In Vivo CT e propriedades de depuração renal
- Síntese e desempenho in vitro de nanopartículas de ferro-platina revestidas com polipirrole para terapia fototérmica e imagem fotoacústica
- Comparação entre o ácido fólico e a funcionalização baseada no peptídeo gH625 de nanopartículas magnéticas Fe3O4 para internalização celular aprimorada
- Método de marcação de células da microscopia adaptado para uso em imagens de corpo inteiro



