Nanopartículas multifuncionais aumentadas por ultrassom com foco de baixa intensidade para a integração de imagens de ultrassom e terapia sinérgica de câncer de mama metastático
Resumo
Acredita-se que a metástase do câncer de mama tenha um efeito negativo em seu prognóstico. Beneficiando-se das notáveis características de penetração profunda e não invasivas, a terapia sonodinâmica (SDT) demonstra toda uma série de potenciais que levam ao tratamento do câncer. Para aliviar a limitação da monoterapia, uma nanoplataforma multifuncional foi explorada para realizar a eficiência do tratamento sinérgico. Aqui, estabelecemos um novo nanossistema multifuncional que encapsula clorina e6 (Ce6, para SDT), perfluoropentano (PFP, para imagem de ultrassom) e docetaxel (DTX, para quimioterapia) em uma estrutura núcleo-casca de PLGA bem projetada. As nanopartículas sinérgicas Ce6 / PFP / DTX / PLGA (CPDP NPs) apresentam excelente biocompatibilidade e estabilidade principalmente para permitir sua aplicação posterior. Após a irradiação de ultrassom focalizado de baixa intensidade (LIFU), a imagem de ultrassom aprimorada pode ser revelada tanto in vitro quanto in vivo. Mais importante, combinadas com LIFU, as nanopartículas exibem capacidade antitumoral intrigante por meio de espécies de oxigênio reativas citotóxicas induzidas por Ce6, bem como liberação de DTX para gerar uma eficiência terapêutica combinada. Além disso, esta estratégia de tratamento ativa uma forte capacidade anti-metastática pela qual os nódulos metastáticos pulmonares foram significativamente reduzidos. Os resultados indicam que a nanoplataforma orientada para SDT combinada com quimioterapia pode ser fornecida como uma abordagem promissora na elevação da terapia sinérgica eficaz e na supressão da metástase pulmonar do câncer de mama.
Introdução
O câncer de mama tem assombrado as mulheres há anos como um dos tumores malignos mais ameaçadores. Devido à alta heterogeneidade e alta capacidade metastática, é relatado que a metástase à distância do câncer de mama foi responsável por mais de 90% de sua mortalidade, enquanto a taxa de sobrevida em 5 anos de pacientes avançados ou metastizados é de apenas 26%, resultando em um resultado clínico ruim [1,2,3]. A caracterização negativa do câncer de mama tem dificultado a cura completa, fazendo com que a estratégia de tratamento seja mais desafiadora na eliminação do tumor primário e também da metástase à distância.
As abordagens terapêuticas tradicionais, como cirurgia e quimioterapia, ainda são consideradas eficazes no tratamento do câncer de mama [4]. Entre todas as drogas quimioterápicas, docetaxel (DTX) está desempenhando um papel significativo no tratamento do câncer de mama metastático (MBC) e câncer de mama avançado (ABC) [5]. Como a droga antitumoral de primeira linha sintetizada pelas substâncias químicas do teixo, o efeito antitumoral do DTX é obtido principalmente pela destruição da mitose e da proliferação celular [6]. Devido à sua ampla eficiência antitumoral, o DTX está se tornando um dos agentes quimioterápicos mais eficazes no tratamento do câncer de mama [7]. No entanto, o agente quimioterápico geralmente induz efeitos indesejáveis, bem como toxicidade para todo o corpo, o que restringe muito a eficácia terapêutica [8]. Além disso, diferentes estágios clínicos e diversas condições pessoais revelam que uma única abordagem terapêutica pode não ser eficiente o suficiente para atender a todas as expectativas no tratamento do câncer de mama. Portanto, há uma necessidade urgente de conter o efeito colateral tóxico e aumentar a eficácia do tratamento do DTX nos requisitos de aplicação futuros.
O ultrassom foi explorado pela primeira vez no diagnóstico clínico devido às suas vantagens extraordinárias, como ausência de radiação, não invasividade e custo-benefício [9, 10]. Apesar das características únicas mencionadas acima, ele também ganhou muita atenção nas perspectivas terapêuticas baseadas em materiais nanoestruturados [11]. A terapia sonodinâmica foi inicialmente realizada pela cavitação e "efeito de sonoporação" desencadeados por ultrassom. A geração de ROS durante este processo induz a citotoxicidade em direção às células cancerosas de forma eficaz, levando a um rápido dano ao DNA e apoptose das células tumorais [9]. Ao contrário do emprego superficial de terapia fotodinâmica (PDT), SDT recebe um resultado terapêutico mais agradável no tratamento de tumores profundos por ultrassom focalizado de baixa intensidade (LIFU), que possui méritos para prevenir lesão térmica indesejável durante o tratamento [12, 13]. Como um dos fundamentos do SDT, os sonossensibilizadores têm sido explorados em várias terapias tumorais [14]. O cloro e6 (Ce6) foi originalmente empregado como um fotossensibilizador comum, mas sua desejável capacidade terapêutica e excelente afinição ao tecido tumoral o tornaram capaz de ser aplicado também como um sonosensibilizador [15]. Jogado como uma segunda geração da família do cloro, o Ce6 tem despertado uma grande atenção no tratamento de tumores por sua desejável geração de ROS [16]. No entanto, a única aplicação de Ce6 tem despertado instabilidade e toxicidade cutânea indesejável, o que tem limitado a extensa exploração do SDT.
Nos últimos anos, o desenvolvimento da nanotecnologia tem desempenhado um papel muito importante em muitos campos, incluindo biossensorio, poluição ambiental e degradação de contaminantes [17,18,19,20,21,22,23]. Nanopartículas baseadas em nanotecnologia têm muitas vantagens, como menor diâmetro, maior área de superfície externa e menor resistência à difusão interna [24]. Anteriormente, as nanopartículas estiveram envolvidas na aplicação de vários materiais, como MOF [25], dióxido de titânio [26] e grafeno [21]. A tendência de rápido crescimento da nanotecnologia combinada com o tratamento do câncer também foi amplamente explorada, abrindo um caminho viável para a promoção de uma estratégia terapêutica combinada [27]. Para realizar aplicações terapêuticas tumorais eficazes, as nanopartículas delicadamente projetadas são definidas principalmente para melhorar a eficiência de transporte do agente de quimioterapia tóxico por meio do efeito de permeabilidade e retenção aprimorada (EPR), permitindo um acúmulo aumentado no local do tumor [28, 29]. Além disso, o efeito colateral indesejado também pode ser diminuído por meio do encapsulamento da quimioterapia. Foi relatado que o perfluoropentano (PFP) possui uma excelente capacidade de transformação da fase líquida para a fase gasosa sob irradiação, o que poderia ser aplicado como uma nova sonda molecular de ultrassom, especialmente em tratamento e imagem ultrassônica [30]. Mais importante ainda, a fase líquida inicial permite que o PFP seja prontamente encapsulado em vários materiais [31]. Além disso, o encapsulamento de PFP pode melhorar muito a capacidade de imagem de ultrassom no local do tumor de acordo com o efeito EPR mencionado acima e evitar a limitação de tamanho provocada por microbolhas de tamanho micrométrico maiores. Exceto para imagens de tumor, a combinação de múltiplas abordagens terapêuticas é de enorme valor no tratamento de câncer orientado por nanossistemas. Especificamente, as práticas, incluindo a integração da terapia sonodinâmica e quimioterapia, colocaram ênfase para revolucionar as eficiências terapêuticas tradicionais. Xu et al. [32] demonstraram que, devido ao SDT, um resultado terapêutico aprimorado pode ser revelado com drogas quimioterápicas e, portanto, levou à ativação da apoptose de células tumorais direcionadas à mitocôndria. Esse padrão revela o tratamento sinérgico, que é altamente preocupado em futuras utilizações.
Aqui, com as inspirações mencionadas acima, pretendemos exercer as nanopartículas tudo-em-um (CPDP NPs) para estabelecer um sistema diagnóstico e terapêutico, que é realizado pela terapia sinérgica orientada para SDT combinada com quimioterapia, bem como o aprimorado imagem de ultrassom. Devido à excelente segurança e estabilidade metabólica ideal como um nanocarreador desejável, o PLGA o tornou favorável na exploração de várias capacidades antitumorais [33, 34]. Portanto, nesta estratégia, usando PLGA como o material da camada externa, PFP poderia melhorar significativamente a imagem de ultrassom por meio de sua capacidade de deslocamento de fase acionada por LIFU, enquanto Ce6, um sonossensibilizador de segunda geração desejável, também poderia ser exposto a LIFU para induzir a geração de ROS. Além disso, acompanhados pela liberação de DTX, tanto a quimioterapia quanto o SDT serão realizados para atingir uma terapia sinérgica em última instância. É importante ressaltar que a estrutura core-shell de CPDP NPs pode ser administrada de forma constante sem ferir tecidos ou células normais e também permite que as nanopartículas tenham uma eficiência de encapsulação relativamente maior [35]. Além disso, o conteúdo poderia ser bem protegido nesta estrutura núcleo-casca [36,37,38], especialmente para PFP, que pode ser efetivamente transformado de líquido em gás devido à existência da estrutura. Usando essa estrutura núcleo-casca, a estratégia sinérgica pode ser demonstrada simultaneamente de uma forma mais estável. Em primeiro lugar, a estratégia sinérgica ajuda a reduzir significativamente o efeito colateral do DTX por encapsulamento eficaz, que é de grande importância para aliviar o sofrimento no tratamento de tumores malignos e agressivos; em segundo lugar, em comparação com a quimioterapia única, a combinação de SDT e quimioterapia tem se mostrado uma estratégia promissora para fortalecer a eficiência terapêutica. Em terceiro lugar, a imagem de ultrassom aprimorada realizada pela PFP otimizou a estratégia de diagnóstico e também ajudou a verificar a eficácia antitumoral. Por último, mas não menos importante, todo o sistema é seguro e estável com excelente biocompatibilidade. Ressalta-se que nesta estratégia, as metástases pulmonares, bem como o crescimento do tumor, foram notavelmente inibidos tanto in vitro quanto in vivo. Em conclusão, a estratégia sinérgica demonstrou uma eficácia de tratamento produtiva contra tumor maligno de mama e sua metástase à distância e, combinada com sua capacidade de imagem de ultrassom, pode se tornar a estratégia de tratamento promissora em aplicações clínicas futuras.
Materiais e métodos
Materiais
PLGA-COOH (Mw 12.000 Da) foi adquirido de Jinan Daigang Biomaterial Co., Ltd (Jinan, China). O perfluoropentano (PFP) e a agarose foram obtidos na Sigma-Aldrich Co., Ltd. (St. Louis, MO). O cloro e6 (Ce6) foi adquirido da Melone Pharmaceutical Co., Ltd. (Dalian, China). O kit de ensaio de citotoxicidade Cell Counting Kit-8 (CCK-8) foi obtido de Dojindo Molecular Technologies (Tóquio, Japão). O diacetato de 2 ', 7' -diclorodi-hidrofluoresceína (H2DCFDA) foi adquirido na MedChemExpress Co., Ltd. (NJ, EUA). O iodeto de propídio (PI) foi obtido da Solarbio Science and Technology Co. Ltd. (Pequim, China). A anexina V-FITC / PI foi obtida na BD Biosciences (EUA). O docetaxel (DTX) foi adquirido na MedChemExpress Co., Ltd. (NJ, EUA). Todos os outros reagentes eram produtos analíticos puros sem purificações adicionais. O meio Roswell Park Memorial Institute 1640 (DMEM), soro fetal bovino e tirisina foram adquiridos da Gibco (ThermoFisher Scientific, EUA) e espectrofotômetro UV (UV-Vis, Hitachi, Japão).
Síntese de CPDP NPs
As nanopartículas de Ce6-PFP-DTX / PLGA (CPDP NPs) foram preparadas por um método de emulsão dupla W / O / W de acordo com o relatório anterior [39, 40]. Resumidamente, 2 mg de Ce6 foram primeiramente dissolvidos em 500 μL de metanol. Em seguida, 50 mg de PLGA-COOH e docetaxel (2 mg) foram dissolvidos em 4 mL de diclorometano e, em seguida, a solução anterior foi adicionada simultaneamente. Em seguida, 200 μL de PFP foram adicionados à solução acima. Em conseqüência, a mistura foi disparada por uma sonda ultrassônica (Sonics &Materials Inc., EUA) para ganhar uma primeira emulsão (5 s ligado e 5 s desligado, 3 min). Para adquirir a segunda emulsão, 8 mL de uma solução de poli (álcool vinílico) (PVA) (p / v =4%) foram adicionados à emulsão acima, usando a mesma sonda ultrassônica por 2 min. Depois de adicionar 10 mL de álcool isopropílico a 2% na emulsão final, a solução foi misturada mecanicamente à temperatura ambiente por pelo menos 4 h para tornar o diclorometano totalmente volatilizado. Finalmente, CPDP NPs foram centrifugados por três vezes (12.000 rpm, 5 min) e, em seguida, coletados e armazenados a 4 ° C para uso posterior. Os PDP NPs foram preparados da mesma maneira, exceto para Ce6. Todos os processos experimentais foram operados acima do gelo e conduzidos estritamente no escuro.
Caracterização de CPDP NPs
O tamanho de partícula e o potencial zeta de CPDP NPs e PDP NPs foram realizados pelo instrumento Malvern Zetasizer Nano (Malvern, Reino Unido). A morfologia foi caracterizada por microscopia eletrônica de transmissão (TEM) e microscopia óptica. Para avaliar a estabilidade, CPDP NPs foram dissolvidos em solução tamponada com fosfato (PBS) e medidos nos tamanhos de 7 dias, respectivamente. Cada amostra foi medida em triplicado. A eficiência de encapsulamento de CPDP NPs foi calculada através da seguinte fórmula:
Eficiência de encapsulamento (%) =(Peso do DTX de carregamento ou Ce6 / Peso do DTX total ou Ce6) × 100%. Para verificar o encapsulamento dos vários materiais, os espectros de UV-Vis de várias amostras foram investigados (UH5300, Hitachi). O encapsulamento efetivo também foi analisado por TEM.
Taxa de liberação de drogas de CPDP NPs
Para avaliar a capacidade de liberação de drogas de Ce6 e DTX em NPs de CPDP, duas soluções com diferentes pHs (solução tampão de fosfato, PBS:7,4, solução tampão de acetato, ABS:5,6) foram utilizadas para testar a eficiência de liberação cumulativa. Resumidamente, CPDP NPs foram inicialmente dispersos com 1 mL de PBS ou ABS após a mistura ter sido selada em um saco de diálise (PM:10.000); toda a solução foi então transferida para um frasco de vidro (volume total:150 mL) no qual 149 mL de PBS ou ABS foram adicionados para manter o volume total da solução em 150 mL. A garrafa de vidro foi então colocada em um agitador de temperatura constante a 37 ° C, e em diferentes períodos (0,5, 1, 2, 4, 8, 12, 24, 48, 72 h), a solução foi coletada e imediatamente suplementada com a mesma volume do meio. Cada grupo foi repetido três vezes. Finalmente, as concentrações de Ce6 e DTX foram medidas por Synergy Hybrid Multi-Mode Read (BioTek, EUA) a 403 e 229 nm, respectivamente, e a taxa de liberação da droga em cada ponto de tempo foi calculada.
Imagem de ultrassom in vitro
Para investigar a capacidade ultrassônica de NPs de CPDP, a emulsão (1 mg / mL) foi inicialmente acionada por um equipamento transdutor de ultrassom focado de baixa intensidade (LIFU) (Ronghai Ultrasonic Medical Engineering Research Center, Chongqing, China), e o padrão de condução foi definido como 50% do ciclo de trabalho, duração de pulso de 1 s sob diferentes intensidades (1–2 W / cm 2 ) para tempos de duração diferentes. Para imagens de ultrassom, CPDP NPs irradiados foram adicionados ao modelo de agarose preparado anteriormente, respectivamente, usando instrumento de diagnóstico de ultrassom Philips EPIQ5 (frequência de sonda:12 MHz, MI:0,06) para observar imagens 2D e CEUS de CPDP NPs. Enquanto isso, o software ImageJ foi aplicado para analisar o valor da escala de cinza de cada grupo.
Captação celular e geração de ROS in vitro de CPDP NPs por irradiação LIFU
A linha celular de câncer de mama murino 4T1 foi obtida do banco de células de Shanghai da Chinese Academy of Sciences (Shanghai, China) e incubada em meio RPMI 1640 misturado com 10% de FBS e 1% de estreptomicina / penicilina a 37 ° C em 5% de CO 2 incubadora umidificada.
As células 4T1 foram incubadas primeiro como condição anterior a uma densidade de 1 × 10 4 células por placa para testar a absorção celular usando CLSM em diferentes intervalos de tempo (1 h, 2 h, 4 h, 8 h). Para verificar a geração de ROS, as células foram separadas nos seguintes 5 grupos:controle, CPDP NPs, LIFU, Ce6 + LIFU, CPDP NPs + LIFU. Após cultura convencional de 24 h, o meio foi substituído por CPDP NPs (200 μL, 0,8 mg / mL) ou solução Ce6 (200 μL), respectivamente, e as células foram co-incubadas por mais 3 h. Em seguida, irradiação LIFU (2 W / cm 2 , 120 s) foi conduzido, respectivamente, de acordo com os diferentes grupos. Após a co-incubação e o tratamento LIFU, 100 μL de solução diluída de DCFH-DA foram adicionados e cada grupo foi cultivado na incubadora anterior por 15 min. Um microscópio confocal de varredura a laser (CLSM) foi usado para confirmar o resultado da produção de espécies reativas de oxigênio, e as intensidades de fluorescência correspondentes foram medidas pelo software ImageJ.
Citotoxicidade in vitro e capacidade de tratamento combinada de NPs de CPDP
Um ensaio de CCK-8 foi aplicado para avaliar a citotoxicidade de NPs de CPDP. Resumidamente, células de câncer de mama murino 4T1 foram incubadas em uma placa de 96 poços, com uma densidade de 1 × 10 4 por poço por 24 h. Em seguida, CPDP NPs foram diluídos com meio RPMI 1640 sem soro em várias concentrações (0,0.2,0.4,0.6,0,8 mg / mL, n =3), com ou sem irradiação LIFU (2 W / cm 2 , 120 s). Após mais 24 horas de processo de co-cultivo, foi realizada a viabilidade celular das células 4T1.
Para avaliar a eficiência da apoptose celular do tratamento combinado, as células 4T1 foram co-cultivadas como anteriormente por 24 horas e, em seguida, separadas em cinco grupos a seguir:(1) controle (sem quaisquer tratamentos), (2) LIFU (apenas com exposição LIFU a 2 W / cm 2 ), (3) CPDP NPs (apenas com solução de CPDP NPs a 0,8 mg / mL), (4) PDP NPs + LIFU e (5) CPDP NPs + LIFU. Após várias coincubações de nanopartículas (200 μL) e exposição LIFU, cada grupo foi tratado com anexina V (5 μL) e coloração dupla com iodeto de propídio (5 μL) por 20 min e analisados por meio de um protocolo de citometria de fluxo.
Inibição in vitro da metástase celular
Para investigar a inibição da capacidade metastática das células, o ensaio de cicatrização de feridas e o ensaio transwell foram desenvolvidos. Para o ensaio de cicatrização de feridas, as células 4T1 foram convencionalmente cultivadas como anteriormente na placa de 6 poços. Após o crescimento das células a uma confluência de 80%, uma ponta de pipeta (10 μL) foi aplicada para conduzir um arranhão artificial ao longo do centro da placa de 6 poços. Em seguida, as células foram tratadas nos mesmos grupos mencionados acima. Após uma coincubação contínua por 24 horas, as células foram lavadas com PBS 3 vezes e observadas em microscopia óptica (Olympus, Japão).
Para o ensaio transwell, o compartimento superior da câmara transwell (Corning, San Diego, EUA) foi aplicado principalmente para imitar a matriz extracelular in vivo. Células 4T1 a uma densidade de 1 × 10 5 as células por poço foram semeadas na câmara superior em um meio RPMI 1640 sem soro, enquanto o compartimento inferior foi preenchido com um meio de cultura completo misturado com FBS a 10%. Em seguida, as células foram separadas da mesma forma que os grupos acima e tratadas por 24 horas, respectivamente. Em seguida, as células da superfície inferior foram fixadas com paraformaldeído e coradas com violeta cristal. Os resultados foram observados em microscopia de luz (Olympus, Japão).
Imagem de ultrassom In Vivo
Ratinhos BALB / c fêmeas saudáveis (4 semanas) e ratinhos Kunming (4 semanas) foram obtidos no Ningxia Medical University Laboratory Animal Center. Todos os experimentos com animais foram conduzidos de acordo com as diretrizes aprovadas pelo Comitê de Revisão de Ética em Bem-Estar Animal da Ningxia Medical University. Para estabelecer o modelo de tumor de camundongos, camundongos BALB / c foram inoculados com células de câncer de mama 4T1 (1 × 10 7 / mL) no flanco direito. Depois que o tamanho do tumor cresceu para 60-80 mm 3 , Camundongos BALB / c foram injetados com CPDP NPs (200 μL, 1 mg / mL) através da veia da cauda por via intravenosa. 24 h depois, os locais dos tumores dos camundongos foram conduzidos com LIFU (2 W / cm 2 , 120 s) e, a seguir, as imagens 2D e CEUS foram adquiridas por meio do instrumento de ultrassom diagnóstico por ultrassom Philips EPIQ5 citado anteriormente. A análise da escala de cinza foi medida pelo software ImageJ.
Eficiência terapêutica sinérgica in vivo de NPs de CPDP
Após a inoculação das células cancerígenas 4T1, o tamanho do tumor foi registrado a cada dois dias, e o volume do tumor foi calculado pela fórmula como:Volume =1/2 × Comprimento × Largura 2 . O tamanho do tumor e o peso corporal dos camundongos foram registrados a cada 2 dias, enquanto as imagens do crescimento do tumor foram registradas a cada 3 dias. Quando o volume do tumor atingiu 60-80 mm 3 , camundongos com tamanho de tumor semelhante foram divididos aleatoriamente nos mesmos cinco grupos:controle, LIFU, CPDP NPs, PDP + LIFU e CPDP NPs + LIFU ( n =3). Cada grupo foi injetado por via intravenosa com vários NPs (200 μL) através da veia da cauda, exceto para o grupo de controle (200 μL de PBS em vez disso). Vinte e quatro horas depois, o local do tumor foi exposto com irradiação LIFU (2 W / cm 2 ) por 120 s. Toda a administração do SDT foi repetida a cada 3 dias e durou 18 dias. O peso corporal e o volume do tumor dos camundongos foram medidos e calculados. Após o tratamento, os camundongos foram mortos e os tecidos tumorais enviados para H&E, TUNEL e PCNA para posterior análise histológica.
Biossegurança de CPDP NPs In Vivo
Para investigar a biossegurança de nanopartículas de CPDP in vivo, camundongos Kunming fêmeas saudáveis ( n =3) foram separados nos seguintes 4 grupos:controle, 5 mg / mL, 10 mg / mL e 20 mg / mL. Os CPDP NPs (200 μL) foram injetados através da veia da cauda do camundongo; então, os ratos tiveram livre acesso a comida e água sem qualquer administração adicional. O peso corporal dos camundongos foi medido a cada 2 dias. Após 30 dias, os camundongos foram mortos e as amostras de sangue coletadas para análises de células sanguíneas e bioquímica. Os principais órgãos (coração, fígado, baço, pulmão e rim) foram coletados e investigados para coloração H&E, respectivamente.
Inibição In Vivo da Metástase Pulmonar
Para avaliar a inibição da metástase pulmonar de cada grupo, todo o processo foi conduzido observando o número de nódulos metastáticos no pulmão, bem como uma avaliação histológica de coloração H&E. Depois que todos os camundongos foram sacrificados, os tecidos pulmonares foram removidos e fixados; em seguida, fotografias de nódulos de câncer foram tiradas e os tecidos pulmonares foram posteriormente analisados com coloração H&E.
Análise estatística
Os dados de medição foram todos realizados 3 vezes e expressos como média ± desvio padrão (SD) e analisados por ANOVA unilateral ou um t de Student padrão teste através do software SPSS (versão:19.0), enquanto p valor <0,05 foi considerado estatisticamente significativo.
Resultados
Caracterização de CPDP NPs e eficiência de liberação de drogas
Um método de emulsão dupla foi aplicado na fabricação de NPs de CPDP, que encapsulou tanto o material de deslocamento de fase PFP, o sonosensibilizador Ce6 e o quimio-droga DTX simultaneamente. Quando disperso em PBS ou água desionizada, a solução apresentou uma aparência cinza claro. CPDP NPs exibiu uma forma esférica homogênea e uma estrutura núcleo-casca clara, sendo observada por meio de microscopia óptica ou microscopia eletrônica de transmissão (Fig. 1a, b). Os diâmetros médios de CPDP NPs e PDP NPs foram 249,5 ± 77,46 nm e 246,6 ± 81,01 nm, e os potenciais zeta de superfície médios foram - 18,47 ± 0,55 mV e - 3,987 ± 0,66 mV, respectivamente (Fig. 1c, d). O tamanho dos NPs do CPDP garantiu que ele pudesse ser acumulado no local do tumor de forma passiva por meio do efeito EPR [40]. A carga diferente entre CPDP NPs e PDP NPs é principalmente devido ao Ce6 carregado negativamente [41]. Além disso, o potencial zeta negativo de NPs de CPDP indicou uma menor adsorção de proteínas plasmáticas, verificando a estabilidade relativa das nanopartículas. As distribuições de tamanho de partícula foram mantidas entre uma faixa de 249,5 e 385,1 nm em 7 dias (Fig. 1e), demonstrando a estabilidade relativa de NPs de CPDP. De acordo com a curva padrão, a eficiência de encapsulamento do DTX e Ce6 foi de 83,84 ± 1,39% e 60,54 ± 3,79%, respectivamente.
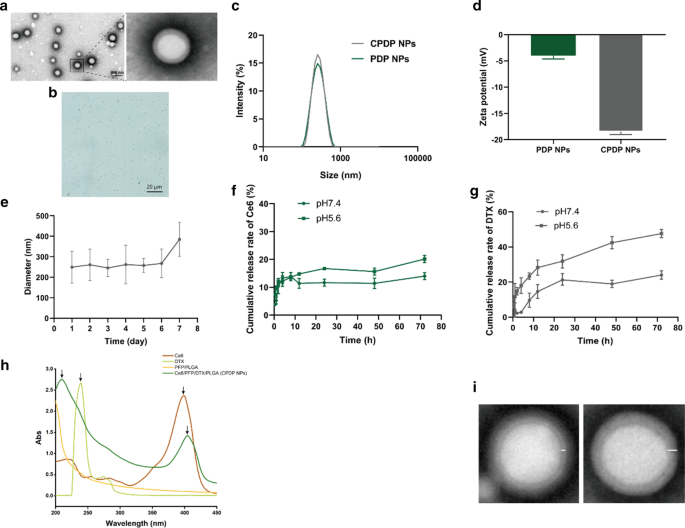
a TEM (barra de escala:500 nm) e b imagem de microscópio de luz de CPDP NPs (barra de escala:20 μm). c Distribuição de tamanho e d potencial zeta de PDP NPs e CPDP NPs. e A distribuição de tamanho de NPs de CPDP em 7 dias. f A taxa de liberação de Ce6 e g a taxa de liberação de DTX sob diferentes condições (pH 7,4 e pH 5,6, n =3). h O espectro UV-Vis de Ce6, DTX, PFP / PLGA e CPDP NPs, respectivamente. As setas de CPDP NPs mostram os picos característicos de Ce6 e DTX, indicando o encapsulamento efetivo de ambos os materiais. eu O resultado TEM de duas nanopartículas. A nanopartícula PFP / PLGA exibe a casca fina e o núcleo redondo (à esquerda). A nanopartícula CPDP encapsulada em Ce6 e DTX mostra a casca muito mais espessa e o núcleo oval (direita)
Como a eficiência de liberação de droga de Ce6 e DTX de CPDP NPs indicada na Fig. 1f, g, um aumento de quase duas vezes no índice de liberação de DTX foi registrado em pH 5,5 em comparação com nanopartículas dissolvidas em pH 7,4, o que indicou a liberação de droga razoável taxa de DTX pode ser alcançada de forma eficaz em um microambiente tumoral ácido. Os resultados acima em todos exibiram os delicados NPs de CPDP projetados podem exercer uma liberação de fármaco quimioterápico estável e oportuna no ambiente de tumor ácido, e também fundamentalmente desejável para ser preparado para SDT.
Como o UV-Vis exibiu, DTX e Ce6 revelaram picos de absorção únicos em 229 nm e 403 nm, respectivamente, e ao contrário, PFP / PLGA não mostrou nenhum dos picos. Deve-se notar que o espectro de NPs CPDP exibiu os picos semelhantes ambos perto dos dois comprimentos de onda acima, enquanto o resto mostrou a mesma tendência do espectro PFP / PLGA, indicando o encapsulamento bem-sucedido dos vários materiais (Fig. 1h). Para verificar ainda mais o encapsulamento eficaz, a Fig. 1i indicou que a nanopartícula PFP / PLGA possui uma casca muito mais fina e o núcleo redondo, enquanto a nanopartícula CPDP revela uma casca relativamente mais espessa e o núcleo em forma oval devido ao encapsulamento de DTX e Ce6.
Imagem de ultrassom in vitro
É destacado que o PFP possui excelente capacidade de mudança de fase. A transformação de líquido em gás não apenas ajuda as nanopartículas a se agregarem no local do tumor, mas também autoriza sua capacidade de aumentar a eficiência da imagem de ultrassom [42]. Para demonstrar isso, a irradiação LIFU foi aplicada como um gatilho para induzir a transformação de fase do PFP, ou seja, o efeito de vaporização de gotículas acústicas (ADV) [43]. Os resultados mostraram que as intensidades da escala de cinza foram mantidas em um nível relativamente baixo antes da irradiação LIFU, enquanto após a intensidade e o tempo de irradiação de LIFU aumentaram, a tendência de imagem de ultrassom aprimorada foi revelada tanto em 2D quanto em CEUS (Fig. 2a). A análise acústica do ImageJ convenceu ainda mais o resultado pelo valor elevado da escala de cinza (Fig. 2b, c), o que foi consistente com os achados de imagem. Deve-se notar que o resultado mais significativo de 2D e CEUS obtido quando a intensidade LIFU atingiu 2 W / cm 2 e durou 120 s. Os resultados acima demonstraram que o PFP foi encapsulado com sucesso em NPs de CPDP, e a capacidade de imagem de ultrassom foi significativamente promovida em intensidade mais alta, bem como em maior tempo de administração de LIFU.
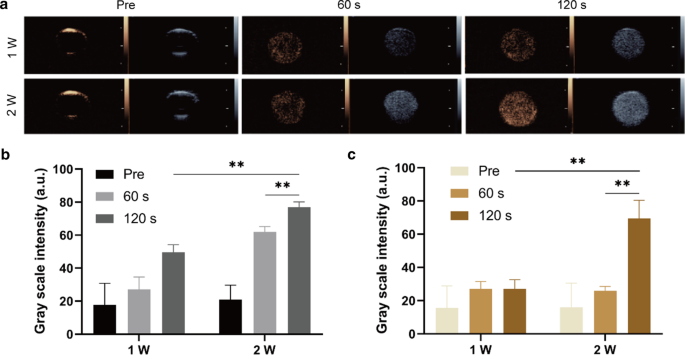
a Imagens de ultrassom de 2D e CEUS em diferentes intensidades e tempos de duração LIFU. b A intensidade da escala de cinza correspondente em diferentes intensidades e tempos de imagens 2D e c Imagem CEUS (** p <0,01, n =3)
Captação celular e geração de ROS in vitro de CPDP NPs por irradiação LIFU
Conforme o resultado do CLSM mostrado na Fig. 3, a captação celular de NPs do CPDP exibiu uma tendência aumentada em diferentes intervalos de tempo, atingindo a agregação mais significativa na coincubação de 8 horas.
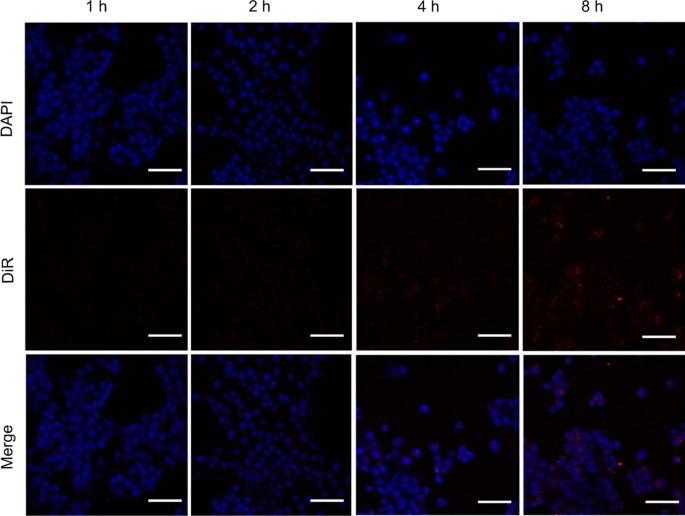
A captação celular 4T1 de CPDP NPs durante diferentes intervalos de tempo (azul:células 4T1 coradas com DAPI. Vermelho:CPDP NPs marcados com DiR, a barra de escala é de 50 μm)
A principal estratégia da terapia sonodinâmica (SDT) é a geração de ROS - uma série de produtos de redução de elétron único - para induzir a apoptose das células cancerosas e inibir a proliferação celular [44]. Ressalta-se que quando exposto ao ultrassom, o sonossensibilizador está sujeito a desencadear a produção de ROS; entretanto, uma quantidade considerável de energia será liberada durante todo o processo [45]. Dado que o ultrassom e o sonossensibilizador são elementos dispensáveis para promover o SDT, portanto, a geração de ROS intracelular foi projetada e analisada para investigar as diferenças entre os grupos divididos. De acordo com a Fig. 4a, a quantidade de ROS gerada pelo grupo de irradiação Ce6 livre mais LIFU foi insignificante, o que pode ser porque o metabolismo rápido do Ce6 livre leva a uma produção de ROS insatisfatória. Pelo contrário, a intensidade fluorescente mais forte foi revelada pelo grupo CPDP NPs + LIFU. Foi assumido que o Ce6 encapsulado estava bem protegido e, portanto, foi mantido longe de ser metabolizado. Como consequência, após a estimulação LIFU, Ce6 foi liberado para produzir ROS abundantes. Comparativamente, não houve sinais fluorescentes significativos encontrados em outros grupos (Fig. 4b).
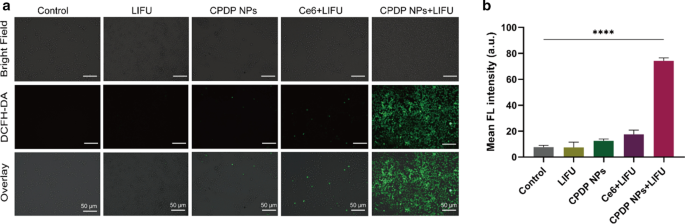
a Imagens CLSM de geração de ROS com vários tratamentos e b a análise de intensidade FL correspondente (**** p <0,0001, n =3). As barras de escala são 50 μm
Citotoxicidade in vitro e capacidade de tratamento combinada de NPs de CPDP
O ensaio Cell Counting Kit-8 (CCK-8) foi introduzido para testar a citotoxicidade in vitro de CPDP NPs. A este respeito, diferentes grupos foram concebidos com ou sem irradiação LIFU em diferentes concentrações. Os resultados indicaram que após uma co-incubação de 24 h sem exposição LIFU, não houve efeito óbvio da taxa de sobrevivência de CPDP NPs, mesmo na concentração mais alta (0,8 mg / mL), demonstrando a biossegurança desejável de CPDP NPs (Fig. 5a). Em contraste, mostrou que houve uma diminuição notável da viabilidade celular após a irradiação de LIFU, mostrando que a combinação de NPs de CPDP e LIFU desencadeou notavelmente a morte de células 4T1, o que foi consistente com a geração de ROS in vitro.
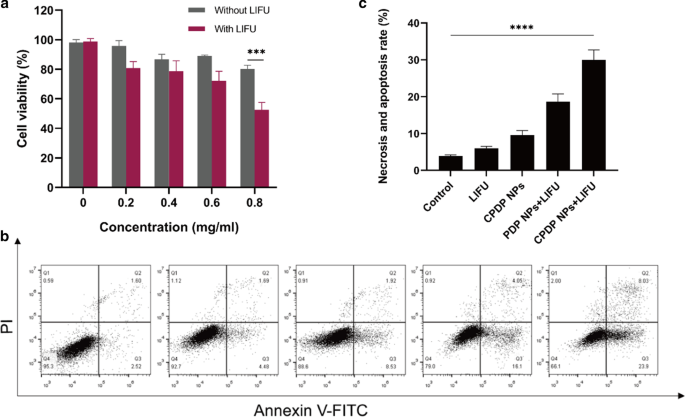
a Relative cell viability with or without LIFU irradiation under different CPDP NPs concentrations. b 4T1 tumor cell apoptosis and necrosis by flow cytometry assay and c the data of corresponding necrosis and apoptosis rate analysis (****p < 0.0001, ***p < 0.001, n =3)
To further evaluate SDT efficacy, a flow cytometry assay was introduced. As the results shown in Fig. 5b, c, the index of cell necrosis and apoptosis was highest observed in CPDP NPs + LIFU group, while other groups showed no obvious and necrosis and apoptosis. Notably, the necrosis and apoptosis rate of CPDP NPs + LIFU group was threefold higher than that of CPDP NPs only group, which ensured the significant tumor cell death efficiency of SDT from another respect. Intriguingly, compared with PDP NPs + LIFU group, cell necrosis and apoptosis rate in CPDP NPs + LIFU group was significantly increased, exhibiting the synergistic therapy efficiency of SDT and chemotherapy.
In Vitro Inhibition of Cell Metastasis
The invasive and migration capability of tumor cells are indispensable in tumor progression [46, 47]. As shown in Fig. 6a, the closure between the physical gap of CPDP NPs + LIFU group was significantly wider than other groups, indicating a relatively slower speed of migrating efficiency. According to the ImageJ software analysis (Fig. 6c), the migration rate of CPDP NPs + LIFU group was also remarkably reduced compared with other groups.
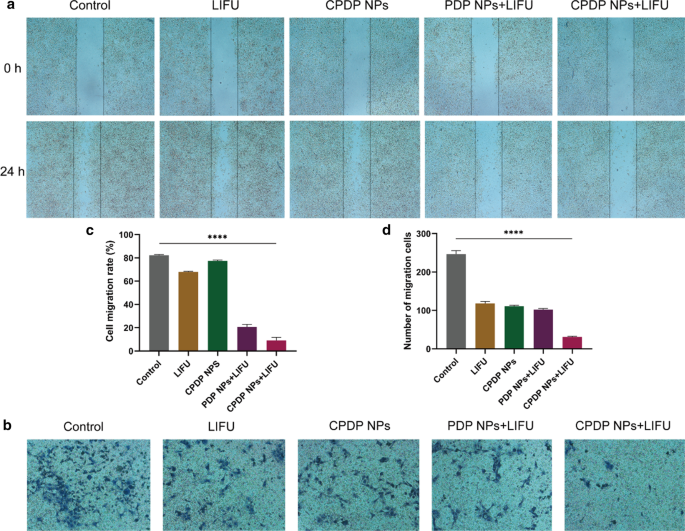
a The wound healing and b The transwell assay after various treatments. c The corresponding migration rate of wound-healing assay. d The corresponding migration number of tranwell assay (****p < 0.0001, n =3)
Similarly in the transwell assay, compared with the swift migration speed of other groups, CPDP NPs + LIFU group revealed a significant reduction of cell number (Fig. 6b), which demonstrated an excellent anti-migration capability of the synergistic therapy. Specifically, with the absence of SDT (CPDP NPs only and LIFU only group), the number of tumor cells was mildly decreased (Fig. 6d). On the whole, due to the combination of SDT as well as chemotherapy, metastasis of 4T1 cells has been remarkably inhibited in vitro.
In Vivo Ultrasound Imaging
Since PFP was encapsulated in CPDP NPs, it is also necessary to evaluate the characteristic ultrasound imaging capability in vivo. After the injection via the tail vein of CPDP NPs, LIFU was then applied to the tumor site to acquire both 2D and CEUS imaging (Fig. 7a). The clear graphic difference between the two groups indicated that after LIFU irradiation, the corresponding intensity of CPDP NPs was elevated obviously compared with the pre-irradiation group. Further data of the average echo intensity also confirmed this result, which was also consistent with the in vitro imaging result previously (Fig. 7b, c).
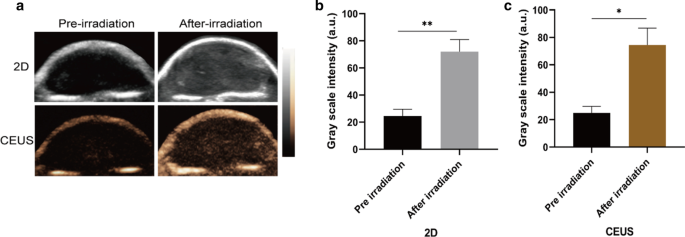
a 2D and CEUS images with and without LIFU irradiation. b , c The corresponding grayscale intensity analysis measured by ImageJ (**p < 0.01, *p < 0.05, n =3)
In Vivo Synergistic Therapeutic Efficiency of CPDP NPs
Seeing from Fig. 8a, b, the tumor volume of CPDP NPs + LIFU group was significantly smaller after 18 days of treatment than that of other groups, which may attribute to the effectiveness of ROS originated from SDT treatment as well as chemotherapy to exert a valid synergistic therapy efficiency. Similarly, photographs of mice-bearing tumors (Fig. 8a) also showed the same trend, verifying the cooperative treating efficacy of CPDP NPs triggered by LIFU exposure. Furthermore, there was no obvious weight reduction of mice between different groups (Fig. 8c). The results above all indicated a much higher inhibition rate of CPDP NPs + LIFU group, revealing that the synergistic therapy could significantly prevent tumor growth.
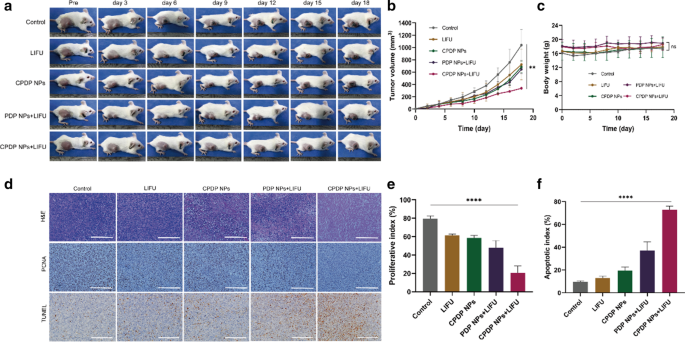
a Images of tumor-bearing mice under various treatments within the certain 18 days (n =3). b Tumor volume analysis according to various treatments (**p <0,01). c Weights of tumor-bearing mice under various treatments (ns no significance, n =3). d H&E, PCNA and TUNEL results under various treatments (scale bar:200 μm). e Analysis of PCNA proliferation index of tumors under various treatments. f Analysis of TUNEL apoptotic index of tumors under various treatments (****p <0.0001, n =3)
To further testify the therapeutic results of all groups, both H&E, PCNA, and TUNEL staining were utilized (Fig. 8d). The proliferate rate of PCNA in CPDP NPs + LIFU group was only 20.50%, which was fourfold lower than control group, threefold lower than LIFU and CPDP NPs only group and twofold lower than PDP + LIFU group, respectively, demonstrating a significant anti-tumor proliferation rate (Fig. 8e). As it is shown in Fig. 8d, f, the TUNEL results indicated CPDP NPs + LIFU group exhibited an obvious apoptosis index of 72.86%, which was much higher than control (9.66%), LIFU (12.86%), CPDP NPs (19.59%), and PDP NPs + LIFU (37.06%) group. The results above all demonstrated the effectiveness of synergistic therapy exerted in vivo, which was also proved consistent with the previous in vitro results.
Biosafety of CPDP NPs In Vivo
Despite the effective therapeutic outcome, it is of great importance to explore the biosafety of the novel established nanoparticles as well. On behalf of the safe distribution of CPDP NPs in vivo, the metabolic safety was conducted. The results showed that instead of apparent body weight loss, the mice body weight elevated gradually in all the groups of mice (Fig. 9a), which indicated a negligible negative influence of CPDP NPs. In addition, as various organs and the blood samples exhibited in Fig. 9b, no significant changes were observed in blood cell, biochemistry analysis index, and H&E staining (Fig. 9c) among different treating groups, indicating the excellent biosafety of CPDP NPs in vivo.
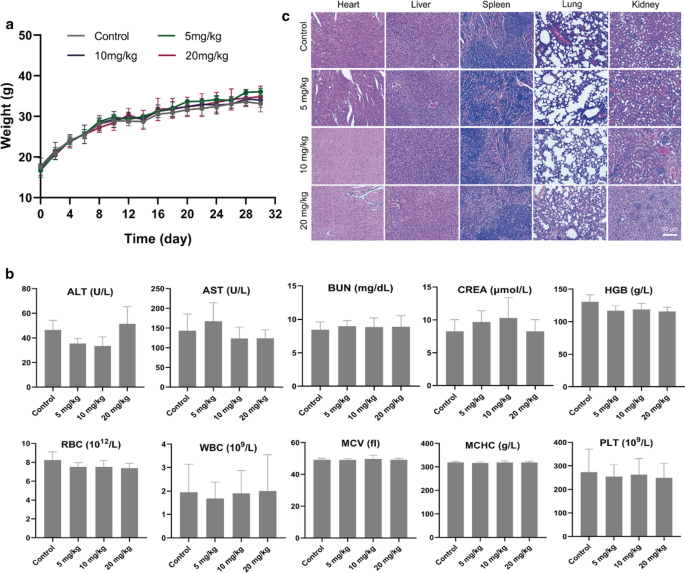
a The weights of healthy Kunming mice under various concentrations of CPDP NPs (n =3). b The blood biochemistry and blood routine examination under various concentrations of CPDP NPs within a certain period of 30 days (n =3). c H&E results of different organs (heart, liver, spleen, lung, and kidney) of mice under the same treatment (scale bar:50 μm)
In vivo Inhibition of Lung Metastasis
It is well established that the lung is the main target organ for distant metastasis of breast cancer [48]. In order to evaluate the suppressing efficiency of metastasis, lung tissues of mice were utilized for anti-metastatic investigation. As seen from Fig. 10a, b, compared with control, LIFU, CPDP NPs, and PDP + LIFU group, the CPDP NPs + LIFU group exhibited the most remarkable decrease of lung nodules, which suggested its desirable lung metastatic inhibition efficiency. A similar trend of decreasing also further indicated by H&E staining (Fig. 10c), which in all demonstrated this synergistic therapy strategy could exert effective effort in eliminating lung metastasis in mice.
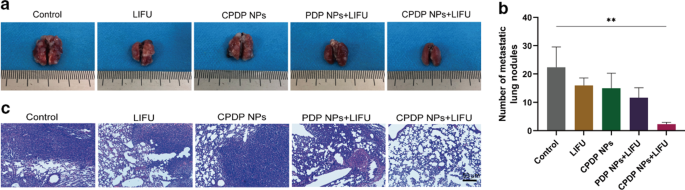
a Images of the general appearances of lung tissues. b The analysis of the metastatic lung nodules between various treatments (**p < 0.01, n =3). c Corresponding images of lung metastatic H&E staining results (scale bar:50 μm)
Discussão
It has been greatly acknowledged that the metastasis of breast cancer will extensively influence its poor prognosis [3, 49]. As a desirable therapeutic approach, SDT may serve for its high efficiency and deep penetrating capability has been extensively convinced [11, 50]. Admittedly, since certain limitations exist in the single application of sonosensitizers, using SDT alone may still be less sufficient in further cancer exploration. The development of nanotechnology combined with clinical medicine has been promoted significantly in recent years, owning to the inspiring merits such as negligible toxicity, none invasiveness, and excellent biocompatibility. Using this novel approach, researchers have made many efforts in exploring multifunctional therapeutic strategies to enhance antitumor efficiency.
The biosafety is the priority of nano-agents. As a widely accepted material approved by the Food and Drug Administration (FDA) certification, it is highlighted that PLGA could be performed as a desirable carrier in application [51, 52]. Based on its advantages, we established a nano-system to realize multifunctional therapy efficiency, exploiting PLGA as the outer structure to encapsulate sonosensitizer Ce6, phase-shift material PFP and chemotherapeutic agent DTX. The CPDP nanoparticles (CPDP NPs) were primarily observed by the core–shell structure and appropriate size so that a desirable aggregation through the EPR effect could be achieved. The cell viability of CPDP NPs has been proved to be above 80% after 24-h coincubation, indicating the well safety of this nanoplatform. Besides, the phase transformation of encapsulated PFP has also guaranteed CPDP NPs as a contrast-enhanced agent when activated by LIFU. The enhanced ultrasound imaging capability will not only ensure the ideal therapeutic window but also promote the promising future for CPDP NPs to realize an integration of accurate diagnosis and precise treatment.
The key strategy in SDT is the generation of ROS. Compared with the single employment of Ce6, the encapsulated Ce6 in PLGA exerted a desirable protection, which could be verified by the ROS result. In our study, there was only a negligible amount of ROS generated by single use of Ce6, while nanoparticle-encapsulated Ce6 produced a considerable amount of ROS, which was further proved by SDT efficiency. The result indicated that ROS generation was preserved by the encapsulated Ce6 in CPDP NPs, which could lay a firm foundation for later tumor inhibition. Besides, the drug-releasing rate showed even at pH 5.5, little Ce6 was released from nanoparticles, demonstrating a well protection of sonosensitizer by PLGA, which was further proved by the ROS production and SDT outcome with high efficiency. Interestingly, the drug-releasing efficiency of DTX and Ce6 at pH 5.5 was quite different according to the results (more than 40% and around 20%, respectively), which may possibly cause by the diverse encapsulation efficiency of the two drugs. The minor releasing rate of Ce6 demonstrated that it could be effectively protected in PLGA so that substantial ROS generation through LIFU stimulation could be reached to get a more convinced SDT efficiency. Another reason for this difference may be due to the different solvents of the two drugs during the preparation process. Specifically, DTX and PLGA were directly dissolved in dichloromethane, while Ce6 needed to be first dissolved in methanol and then added dropwise to dichloromethane, due to its poor solubility in the latter [53]. Since drug release in nanoparticles is directly related to the effectiveness of subsequent combination therapy, the assessment of drug-releasing rate as well as ROS generation result has mutually proved this point. Current researches have suggested that using chemotherapy alone may not significantly reverse tumor progression [41]. In this study, the nanoplatform we designed demonstrated strong evidence that compared with the single employment of chemotherapy, the synergistic treatment has remarkably elevated therapeutic efficiency both in vitro and in vivo. Since LIFU stimulation optimized the therapeutic strategy, an increased cell apoptosis rate was remarkably elevated. It is worth noting that due to this synergistic strategy, lung metastasis could be significantly inhibited both at tumor cell level and inoculated mice model, which is consistent with previous reports [16, 52].
Conclusion
In conclusion, the safe and stable CPDP NPs we designed and prepared plus LIFU irradiation could remarkably eliminate breast tumor progression and its lung metastasis. With an enhanced imaging capability, this nanoplatform was also considered to be a promising contrast-enhanced agent in clinical. Hence, the novel synergistic strategy combined with LIFU might be considered as an effective treating application to reverse the poor outcome of metastatic breast cancer.
Abreviações
- LIFU:
-
Low-intensity focused ultrasound
- SDT:
-
Sonodynamic therapy
- PFP:
-
Perfluoropentane
- EPR:
-
Enhanced permeability and retention effect
- DCFH-DA:
-
Dichlorodihydrofluorescein diacetate
- PI:
-
Propidium iodide
- TEM:
-
Microscopia eletrônica de transmissão
- ROS:
-
Espécies que reagem ao oxigênio
- Ce6:
-
Chlorin e6
- DTX:
-
Docetaxel
- FBS:
-
Soro fetal bovino
- CCK-8:
-
Cell Counting Kit-8
- CPDP NPs:
-
Ce6/PFP/DTX/PLGA nanoparticles
- PDP NPs:
-
PFP/DTX/PLGA nanoparticles
Nanomateriais
- Nanopartículas multifuncionais de ouro para aplicações diagnósticas e terapêuticas aprimoradas:uma revisão
- Nanopartículas para terapia do câncer:progresso e desafios atuais
- Nanopartículas de albumina carregadas de resveratrol com circulação sanguínea prolongada e biocompatibilidade aprimorada para terapia de tumor pancreático direcionada altamente eficaz
- Novel Biocompatible Au Nanostars @ PEG Nanopartículas para imagens In Vivo CT e propriedades de depuração renal
- Síntese e desempenho in vitro de nanopartículas de ferro-platina revestidas com polipirrole para terapia fototérmica e imagem fotoacústica
- Superresfriamento de água controlado por nanopartículas e ultrassom
- Nanodots MoSe2 biocompatíveis e direcionados a tumor @ Nanoesferas de albumina como agente de terapia de modalidade dupla para radioterapia fototérmica sinérgica
- Nanopartículas magnéticas funcionalizadas para aplicações biomédicas, administração de medicamentos e imagens
- Nanopartículas compostas à base de polidopamina com cascas de polímero redox-lábil para liberação controlada de drogas e terapia quimio-fototérmica aprimorada
- Nanopartículas de ouro bioconjugadas ambientalmente compatíveis como agentes de contraste eficientes para imagiologia de câncer induzida por inflamação



