Fabricação de hidrogéis compostos de poli (ácido acrílico) / nitreto de boro com excelentes propriedades mecânicas e autocura rápida por meio de interações físicas hierárquicas
Resumo
Muitos tecidos vivos possuem excelentes propriedades mecânicas e capacidade de autocura. Para imitar esses tecidos vivos, uma série de novos hidrogéis compostos, nanofolhas de nitreto de boro com superfície modificada de poli (ácido acrílico) (PAA / BNNS-NH 2 ) foram fabricados simplesmente por meio de interações físicas hierárquicas:interação de coordenação de metal em escala molecular entre –COOH de PAA e Fe 3+ e ligação H em nanoescala entre –COOH de PAA e –NH 2 de BNNS-NH 2 . Os hidrogéis compostos exibem excelentes propriedades mecânicas (incluindo aumento da tensão de fratura, alongamento, resistência, módulo de Young e energia dissipada) e capacidade de cura rápida sem qualquer estímulo externo. Especialmente, o B 0,5 P 70 (o hidrogel com concentração de BNNS de 0,5 mg mL - 1 , o teor de água de 70% em peso) exibe uma tensão de fratura de ~ 1311 kPa e tenacidade de ~ 4,7 MJ m - 3 , quase ~ 3 vezes e ~ 8 vezes para B 0 P 70 , respectivamente. As excelentes propriedades, aliadas ao método simples de preparação, conferem a esses hidrogéis compostos potenciais aplicações.
Histórico
Hidrogéis com redes tridimensionais formadas por ligações covalentes e / ou reticulação de interações físicas contendo grande quantidade de água possuem alta hidrofilicidade, capacidade de retenção de água e biocompatibilidade não excepcional [1,2,3,4], podendo ser uma das mais biomateriais populares. No entanto, a maioria dos hidrogéis tem propriedades mecânicas pobres, o que limita amplamente as aplicações. É bem conhecido que muitos tecidos vivos, como músculos, ligamentos e pele, possuem excelentes propriedades mecânicas e significativa capacidade de cicatrizar feridas de forma autônoma [5,6,7]. Inspirados por esses tecidos vivos, materiais com altas propriedades mecânicas e capacidade de autocura foram explorados para várias aplicações [8, 9], incluindo engenharia de tecidos, liberação de drogas, curativo para feridas, lentes de contato, sensores e atuadores [2, 10, 11,12]. Ihsan et al. relataram um hidrogel de polianfolito autocurável por meio da reforma das ligações irônicas na superfície da fratura [7]. Zhang et al. projetou um hidrogel autocurável de PVA com processo rápido de autocura através de ligações de hidrogênio [13]. Tao et al. preparou um hidrogel de autocura com resistência ao frio reticulado por ligação dinâmica de éster catecol-borato que permite a autocura em temperatura ambiente e em baixa temperatura [14]. No entanto, todos esses materiais autocuráveis têm uma fraqueza comum:propriedades mecânicas ruins [15,16,17,18,19] limitam amplamente as aplicações.
A fim de melhorar as propriedades mecânicas dos hidrogéis, alguns nanomateriais inorgânicos foram introduzidos nos sistemas reticulados. Han et al. relataram um hidrogel supermolecular usando nanofolhas de óxido de grafeno para reduzir a temperatura para autocura [15]. Si et al. explorou um novo hidrogéis de nanofibra com alto teor de água, superelástico e com memória de forma [20]. O flexível SiO 2 nanofibras foram introduzidas para melhorar as propriedades mecânicas e para acelerar a memória de forma e a resposta à pressão. Especialmente, Duan et al. desenvolveu hidrogéis compostos de poli (álcool vinílico) / nitreto de boro (PVA / BNNS) com propriedades mecânicas aprimoradas [21]. Gao et al. fabricou um hidrogel nanocompósito preenchido com montmorilonita esfoliada que melhorou dramaticamente o alongamento da fratura [22]. Zhong et al. projetou hidrogéis nanocompósitos de óxido de grafeno (GO) / poli (ácido acrílico) (PAA / GO) que aumentaram significativamente as propriedades mecânicas [23]. Os novos hidrogéis compostos de autocura com propriedades mecânicas aprimoradas ainda são muito procurados, embora os hidrogéis explorados tenham avançado significativamente nos últimos anos. Nanofolhas de nitreto de boro, “grafeno branco”, exibem muitas propriedades excelentes, incluindo excelentes propriedades mecânicas, extraordinária inércia química e notável não toxicidade [24,25,26]. Notavelmente, as nanofolhas BN modificadas na superfície serviram como nanopreenchimentos nos hidrogéis nanocompósitos aprimoram as propriedades mecânicas e térmicas e foram relatadas em trabalhos recentes [27, 28]. Portanto, o desenvolvimento de um novo hidrogel composto com nanofolhas BN modificadas por superfície ainda é muito procurado.
Aqui, os novos hidrogéis compostos são fabricados a partir de poli (ácido acrílico) (PAA) e nanofolhas de nitreto de boro modificadas por grupos amino (BNNS-NH 2 ) por meio de interações físicas hierárquicas:interação de coordenação de metal em escala molecular entre –COOH de PAA e íon férrico (Fe 3+ ) e ligação H em nanoescala entre –COOH e BNNS-NH 2 foi reportado. A introdução de BNNS-NH 2 melhorou a propriedade mecânica e acelerou o processo de autocura dos hidrogéis. Este trabalho fornece uma nova rota para a preparação de hidrogéis com excelentes propriedades mecânicas e rápida capacidade de autocura.
Método / Experimental
Materiais
Persulfato de potássio (KPS; 99,0%) e FeCl 3 · 6H 2 O (99,0%) foram adquiridos da J&K Chemical Technology e o ácido acrílico (AA; 98,0%) foi adquirido da Sigma-Aldrich. Todos estes produtos químicos foram usados como recebidos sem qualquer purificação. A rodamina B (95,0%) foi adquirida à Sigma-Aldrich. BNNS-NH 2 foi obtido por nosso trabalho anterior [24]. Água desionizada foi usada ao longo dos experimentos.
Preparação de BNNS-NH 2 Dispersão
BNNS-NH 2 foi preparado de acordo com nosso trabalho anterior [24]. Para fazer BNNS-NH 2 constantemente disperso na rede de polímero, é indispensável preparar o BNNS-NH 2 dispersões de água. Para obter o BNNS-NH estável 2 dispersões, agitação magnética e banho de ultrassom foram utilizados à temperatura ambiente. O BNNS-NH 2 dispersões com concentração de 1,0, 0,8, 0,5 e 0,1 mg mL - 1 foram obtidos pelo seguinte procedimento. Os 100 mg, 80 mg, 50 mg e 10 mg de BNNS-NH 2 foram adicionados em 100 mL de água desionizada, respectivamente, sob agitação magnética (1000 rpm) por 24 h em temperatura ambiente em ar ambiente para obter misturas e, em seguida, as misturas foram sonicadas (20 kHz) em temperatura ambiente por 2 h em ar ambiente para obter dispersões estáveis. Para proibir a perda da solução aquosa, as dispersões obtidas foram conservadas em recipientes lacrados com diferentes marcações para posterior preparação de hidrogéis autocurantes.
Preparação do hidrogel autocurativo
O PAA como o polímero comum com grupos -COOH abundantes permite estabelecer a quantidade de ligações de hidrogênio intracadeia e intercadeia que dota o polímero de possuir elasticidade superior e força favorável [29]. Além disso, as interações de coordenação de metal são configuradas entre –COOH de PAA e íon férrico (Fe 3+ ) Os dois tipos de ligações não covalentes reversíveis equiparam o hidrogel com a propriedade de autocura. Os hidrogéis reticulados por ligações não covalentes sempre possuem propriedades mecânicas inferiores. A fim de aumentar a força do hidrogel, BNNS-NH 2 foi introduzido na rede tridimensional de polímero, que estabeleceu ligações de hidrogênio entre –NH 2 de BNNS-NH 2 e –COOH do PAA. Aqui, o composto PAA / BNNS-NH 2 hidrogéis foram abreviados como B x P y , em que B representa BNNS-NH 2 , x é o conteúdo do BNNS-NH 2 (mg mL - 1 ), P significa PAA / BNNS-NH 2 hidrogel composto, ey refere-se ao conteúdo de água do PAA / BNNS-NH 2 hidrogel composto (fração de massa,% em peso). Os hidrogéis foram preparados de acordo com um procedimento descrito abaixo. Normalmente, 10 mL de AA, 0,25 g de FeCl 3 · 6H 2 O (1,05 mol% de AA) e 0,1 g de KPS (0,25 mol% de AA) foram dissolvidos em BNNS-NH 2 dispersões com diferentes concentrações ou água desionizada sob agitação magnética (1000 rpm) em temperatura ambiente por 10 min sob ar ambiente para formar uma mistura homogênea. Depois disso, N 2 foi borbulhado na mistura para remover o oxigênio (10 min) e, em seguida, a polimerização foi realizada a 25 ° C em banho-maria durante 6 h para formar hidrogéis. Hidrogéis preparados conforme procedimento acima mencionado e parâmetros de BNNS-NH 2 dispersões com a concentração de 1,0, 0,8, 0,5 e 0,1 mg mL - 1 foram denotados como B 1 P 90 , B 0.8 P 90 , B 0,5 P 90 , e B 0.1 P 90 , respectivamente, enquanto os hidrogéis preparados a partir de água desionizada foram nomeados como B 0 P 90 .
É bem conhecido que os hidrogéis com diferentes teores de água possuem propriedades mecânicas totalmente diferentes. Para caracterizar a influência do teor de água nas propriedades mecânicas dos hidrogéis, os hidrogéis com diferentes teores de água foram preparados da seguinte forma. Em primeiro lugar, o B x P 90 os hidrogéis foram preparados conforme o procedimento e os parâmetros mencionados acima. Então, o B x conforme preparado P 90 os hidrogéis foram expostos ao ar à temperatura ambiente por diferentes tempos, dependendo do conteúdo final de água dos hidrogéis. Nesse sentido, os hidrogéis de secagem obtidos com diferentes teores de água foram rotulados como B x P 70 , B x P 50 , e B x P 25 , respectivamente. O teor de água foi calculado pela fórmula:teor de água = W w / W t , onde o W w é o peso da água e W t é o peso total do hidrogel. Por outro lado, as densidades de reticulação de B x P 90 os hidrogéis foram calculados a partir dos resultados de medições reológicas, e é bem conhecido que a maior densidade de reticulação leva a uma propriedade mecânica mais robusta. Para verificar a teoria, é imprescindível realizar os ensaios de tração. No entanto, o B x P 90 os hidrogéis eram tão macios que a máquina de teste de material elétrico universal não conseguia reconhecer a amostra que não exibia carga, portanto, os hidrogéis compostos com menor teor de água eram altamente necessários para a fabricação. Os hidrogéis com diferentes conteúdos de água foram cortados em diferentes formas ou tamanhos para os vários testes a seguir.
Teste mecânico
A fim de caracterizar as propriedades mecânicas dos hidrogéis, os hidrogéis preparados foram cortados em forma de flocos (50 mm × 2 mm × 2 mm) e testados pela máquina de teste de material elétrico universal com uma célula de carga de 200 N sob uma velocidade de 50 mm min - 1 a 25 ° C e uma umidade de aproximadamente 45%. A tensão de tração ( σ ) representando a força foi calculada pela equação: σ = F / ( a × b ), onde F , a , e b foram força de carregamento e largura e espessura dos hidrogéis, respectivamente. A deformação ( ε ) representando a extensibilidade foi definida como a mudança do comprimento, ilustrada pela fórmula: ε =( l - l 0 ) / l 0 × 100%, onde l e l 0 representam os comprimentos após e antes do teste, respectivamente. A rigidez foi caracterizada pelo módulo de Young que foi obtido a partir da inclinação da curva tensão-deformação nas baixas deformações. A tenacidade das amostras foi ilustrada como a área sob as curvas tensão-deformação. Os ensaios de tração cíclica foram realizados na mesma condição experimental que objetivou a obtenção da energia dissipada. A energia dissipada foi caracterizada pela área entre as curvas de carga-descarga e X -eixo.
Caracterização
Os espectros de infravermelho com transformada de Fourier (FTIR) foram realizados para registrar os caracteres FTIR das amostras, os quais foram registrados em um espectrômetro Thermo Scientific Nicolet 6700 em modo de reflexão total atenuada (ATR), com resolução de 4 cm - 1 dentro do intervalo 400–4000 cm - 1 . A morfologia dos hidrogéis após o processo de secagem por congelamento foi observada em micrografias eletrônicas de varredura (SEM, Carl Zeiss AG, ZEISS EV0 MA15). Para analisar a viscoelasticidade dos hidrogéis e calcular a densidade de reticulação, as medições reológicas foram realizadas usando um reômetro (HAAKE MARS III Thermo Fisher Scientific Limited, China) para medir os módulos de armazenamento (G ') e módulos de perda (G ”). Os ensaios de tração foram realizados para analisar as propriedades mecânicas das amostras, os quais foram conduzidos em uma máquina de ensaio de materiais elétricos universal com célula de carga 200 N (Instron 2360).
Resultados e discussão
O PAA / BNNS-NH 2 hidrogéis compostos foram simplesmente formados por polimerização in situ de AA, com a presença de Fe 3+ e o BNNS-NH 2 . As cadeias macromoleculares de PAA formadas foram reticuladas por interações físicas hierarquicamente:interação de coordenação de metal entre carboxilas (–COOH) do PAA e Fe 3+ em escala molecular e interação de ligação de hidrogênio entre –COOH do PAA e –NH 2 de BNNS-NH 2 em nanoescala, resultando na formação de redes tridimensionais (Esquema 1).
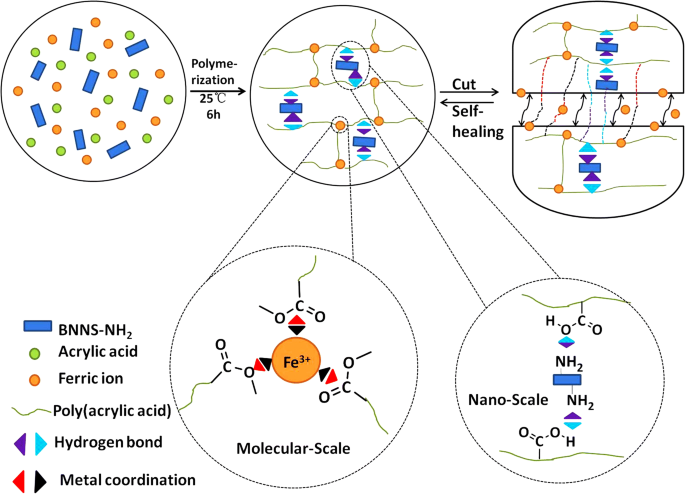
Esquema que ilustra a formação de um PAA / BNNS-NH 2 hidrogel composto com capacidade de autocura
Os dois tipos diferentes de interações físicas dentro do PAA / BNNS-NH 2 hidrogéis compostos foram revelados primeiramente por espectroscopia FTIR. A partir dos resultados da Fig. 1, o PAA mostra um alongamento característico (alongamento –C =O) a 1690 cm - 1 , que mudou para 1620 cm - 1 no PAA / BNNS-NH 2 hidrogel composto. Esta mudança indica a existência de interações de ligações de hidrogênio entre –COOH do PAA e –NH 2 de BNNS-NH 2 [30, 31]. A presença de ligação de hidrogênio pode ser verificada pelo fato de que os picos característicos em 3400 cm - 1 para –COOH tornou-se menos óbvio no hidrogel composto [32, 33]. O pico em 3230 cm - 1 pode ser atribuído à vibração de alongamento N – H no hidrogel composto. A interação da coordenação do metal foi revelada pelo pico em 620 cm - 1 em PAA hidrogel e hidrogel composto, demonstrando que a interação de coordenação de metal entre Fe 3+ e –COO - foi formado no sistema de rede [34]. O B – N no plano que se estende a 1388 cm - 1 e as vibrações de flexão B-N-B fora do plano em 1780 cm −1 pode ser visto a partir do hidrogel composto (Fig. 1a), confirmando a presença de BNNS-NH 2 .
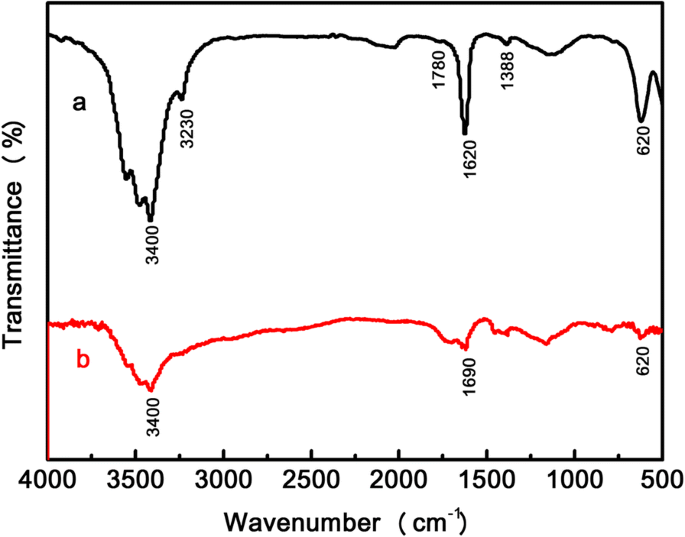
Espectros FTIR de a um hidrogel composto e b um hidrogel PAA
Após a secagem, as morfologias desses hidrogéis foram observadas por MEV. Estruturas porosas foram observadas no hidrogel PAA (Fig. 2a, b) e B x P y hidrogel composto (Fig. 2c). Os poros maiores têm um diâmetro médio de cerca de dezenas de micrômetros e os poros menores têm um diâmetro médio em nanoescala. A presença de poros pode fornecer alta elasticidade e compressibilidade aos hidrogéis [35]. Em comparação com os hidrogéis de PAA, os poros dentro do hidrogel composto são mais isolados e uniformes em tamanhos (Fig. 2c). E o BNNSs-NH 2 pode ser observado em uma imagem SEM (Fig. 2d) de hidrogel contendo BNNSs-NH 2 e foram apontados por setas, e a imagem inserida verificou ainda a presença do BNNS-NH 2 [34]. Para entender os efeitos das interações de dois tipos, testes de tração de hidrogéis compostos com diferentes BNNS-NH 2 concentrações foram conduzidas e os resultados desses hidrogéis com diferentes conteúdos de água são mostrados na Fig. 3a-c. Sem BNNS-NH 2 , a tensão de fratura de B 0 P 70 hidrogel tinha cerca de 406 kPa, e a tensão de fratura de B 0,1 P 70 aumentado para 526 kPa pela introdução de uma pequena quantidade de BNNS-NH 2 . O B 0,5 P 70 exibe uma tensão de fratura de 1311 kPa, quase três vezes para B 0 P 70 e duas vezes para B 0.1 P 70 , como mostrado na Fig. 3a. O resultado excedeu em muito os hidrogéis compostos anteriores em trabalhos publicados [34]. Isso significa que a ligação de hidrogênio formada entre –COOH do PAA e –NH 2 de BNNS-NH 2 aumentou significativamente as propriedades mecânicas [36]. No entanto, a tensão de fratura diminuiu quando o BNNS-NH 2 a concentração continuou a aumentar. A tensão de fratura se torna ainda menor do que B 0 P 70 , que indicou que um equilíbrio principal de interações de coordenação de metal e ligações de hidrogênio foi alcançado no BNNS-NH 2 concentração de 0,5 mg mL - 1 . Correspondentemente, as maiores tensões de fratura também foram realizadas no mesmo BNNS-NH 2 concentração (0,5 mg mL - 1 ) dentro de hidrogéis compostos com o teor de água de 50% em peso e 25% em peso (Fig. 3b, c) que foi um fator importante para afetar as propriedades mecânicas do hidrogel [37, 38]. As tensões de fratura dos hidrogéis compostos foram notavelmente melhoradas (Arquivo adicional 1:Figura S1-S5) quando o teor de água diminuiu para 50% em peso e 25% em peso, atribuído ao espaço estreito entre as cadeias com baixo teor de água [35]. Notavelmente, o B x P y os hidrogéis foram capazes de resistir à tração, amarração, flexão e torção mesmo sob alto grau de deformações (Fig. 3d – g, Arquivo adicional 1:Figura S6). A adição de BNNS-NH 2 pode alterar ligeiramente o pH da solução devido à presença de –NH 2 grupos, levando a uma mudança na constante de associação entre –COOH e Fe 3+ . O equilíbrio entre as interações de coordenação de metal e ligações de hidrogênio era dependente do BNNS-NH 2 concentração com o conteúdo constante de Fe 3+ . O excelente comportamento mecânico do hidrogel composto resultou do equilíbrio ideal entre a interação de coordenação de metal em escala molecular e as interações de ligação de hidrogênio em nanoescala [36].

Imagens SEM de a , b PAA hidrogel e c , d hidrogel composto. O BNNS-NH 2 foi apontado por setas em ( d ), e a imagem inserida em ( d ) é a imagem ampliada do BNNS-NH 2
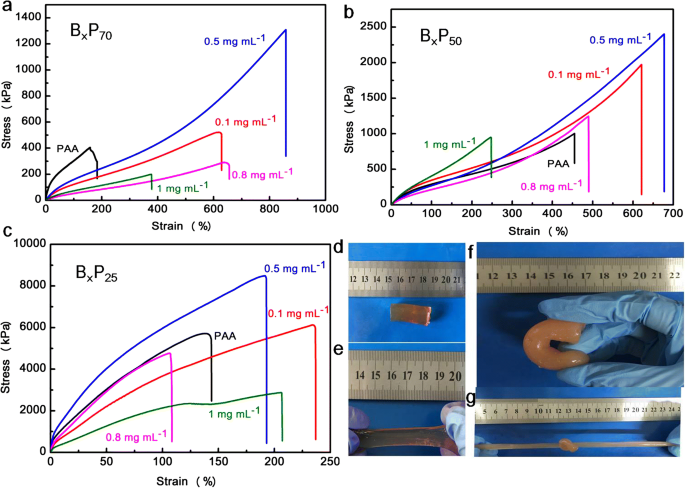
Curvas de tensão-deformação dos hidrogéis compostos: a B x P 70 , b B x P 50 , e c B x P 25 . A fotografia digital de hidrogéis compostos: d original, e esticado, f dobrado e g esticado depois de ser amarrado
Os efeitos do BNNS-NH 2 concentração nas propriedades mecânicas de B x P 90 foram estudados por medição reológica (Fig. 4a). Para todas as amostras, seus módulos de armazenamento (G ') são sempre maiores do que os módulos de perda correspondentes (G ") na faixa de frequência de 0,1 a 100 rad s - 1 , indicando a formação de redes tridimensionais [34, 36]. Com o aumento da frequência, G 'e G "aumentaram, mas o aumento em G" é mais acentuado, mostrando seus comportamentos de cisalhamento [34]. B 0,5 P 90 exibiu o G 'mais alto, o que é consistente com os resultados dos testes de tração. Do módulo de cisalhamento de equilíbrio ( G e ), densidade de reticulação ( N ) desses hidrogéis podem ser calculados usando a fórmula 1 [39,40,41].
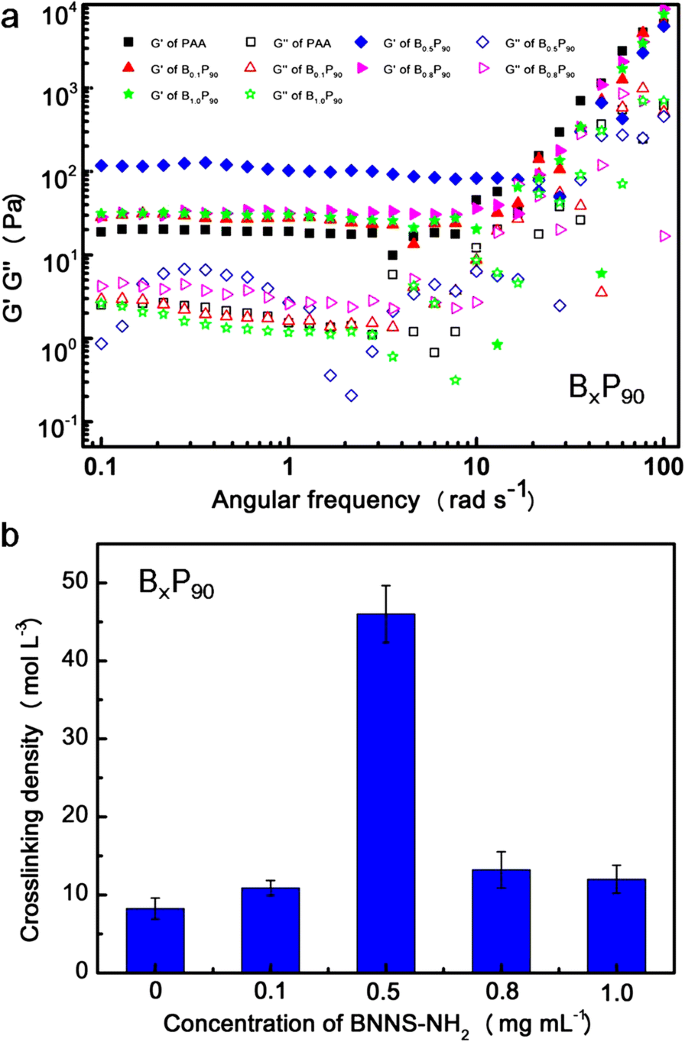
a Dependência de frequência dos módulos de armazenamento (G ’) e módulos de perda (G”) de B x P 90 a uma tensão de 0,1%. b Densidade de reticulação de B x P 90 calculado pelo módulo de cisalhamento de equilíbrio
Aqui, G e , R , e T são o valor do terraço de G ', constante do gás e temperatura absoluta, respectivamente. A densidade de reticulação é mostrada na Fig. 4b. Com aumento na concentração de BNNS-NH 2 , a densidade de reticulação aumentou, o que demonstra que BNNS-NH 2 também serviu como um reticulador nos hidrogéis compostos por meio de interações de ligações de hidrogênio entre –COOH do PAA e –NH 2 de BNNS-NH 2 . No entanto, a densidade de reticulação diminuiu quando o BNNS-NH 2 a concentração é superior a 0,5 mg mL - 1 que correspondeu com os resultados das propriedades mecânicas [40]. É ilustrado que o excesso de BNNS-NH 2 leva à reunião das nanofolhas, o que prejudica o aprimoramento dos hidrogéis compostos, como B 0.8 P y e B 1.0 P y [41, 42].
Para obter hidrogéis com excelentes propriedades mecânicas, o equilíbrio ideal de interações de ligação de hidrogênio e interações de coordenação de metal pode ser alcançado ajustando o BNNS-NH 2 concentrações enquanto o conteúdo de Fe 3+ é constante. A rigidez e o módulo de Young que representam a rigidez são mostrados na Fig. 5a e na Fig. 5b, respectivamente [24, 36, 37]. Da Fig. 5a, os hidrogéis tornaram-se rígidos com a diminuição do teor de água ou aumento do BNNS-NH 2 concentração até 0,5 mg mL - 1 consistente com os resultados do teste de tração (Arquivo adicional 1:Figura S7).
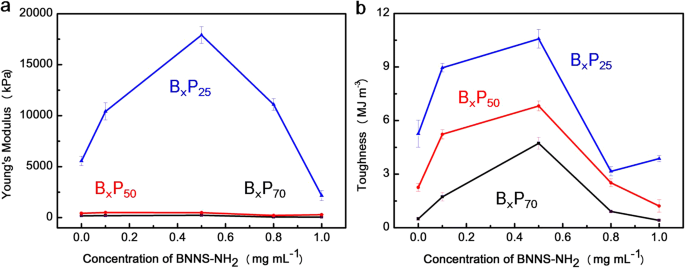
a Módulo de Young e b tenacidade de hidrogéis compostos com diferentes conteúdos de água e BNNS-NH 2 concentrações
A tenacidade é observada na Fig. 5b. É claro que a tenacidade aumenta com a diminuição do teor de água, semelhante à tendência do módulo de Young. Sem BNNS-NH 2 , a resistência de B 0 P 70 era cerca de 0,5 MJ m - 3 , e com BNNS-NH 2 , a resistência de B 0,5 P 70 aumentou para ~ 4,7 MJ m - 3 , quase oito vezes maior que B 0 P 70 . O B 0,5 P 25 exibiu o maior módulo de Young de ~ 17,9 MPa, maior resistência à tração de ~ 8491 kPa e maior resistência de ~ 10,5 MJ m - 3 , que é muito maior do que B 0 P 25 .
A rigidez da maioria dos hidrogéis de polímero diminui com o aumento da tenacidade correspondente. De acordo com o modelo de Lake-Thomas [42, 43], a tenacidade aumenta, mas a rigidez diminui com a diminuição da densidade de reticulação. Neste trabalho, um novo tipo de hidrogel com alta rigidez e alta tenacidade (B 0,5 P y ) (Fig. 5) foi fabricado, o que é diferente dos hidrogéis convencionais (alta rigidez / baixa tenacidade ou baixa rigidez / alta tenacidade). As propriedades excepcionais podem ser atribuídas à existência de interações hierárquicas:interações de coordenação de metais em escala molecular e ligações de hidrogênio em nanoescala.
Testes cíclicos de tração de B x P 70 e B x P 50 foram conduzidas na deformação de 200% (Fig. 6a, b). Loops de histerese óbvios foram observados para B x P 70 e B x P 50 , e B x P 50 mostraram loops de histerese muito maiores, indicando o conteúdo de água determinando a dissipação de energia devido a mais ligações de hidrogênio sendo estabelecidas entre as cadeias de polímero por causa das redes encolhidas [37]. A energia dissipada aumentou com o aumento do BNNS-NH 2 concentração, e o valor máximo foi obtido na concentração de 0,5 mg mL - 1 devido ao estabelecimento de numerosas ligações de hidrogênio entre BNNS-NH 2 e cadeias de PAA [34]. No entanto, a energia dissipada diminuiu quando BNNS-NH 2 a concentração aumentou para 0,8 e para 1,0 mg mL - 1 , devido à alta concentração de BNNS-NH 2 levando à agregação das nanofolhas [41, 42]. Esta explicação também é adequada para curvas de tensão-deformação específicas e resultados de reologia de B x P y hidrogéis.
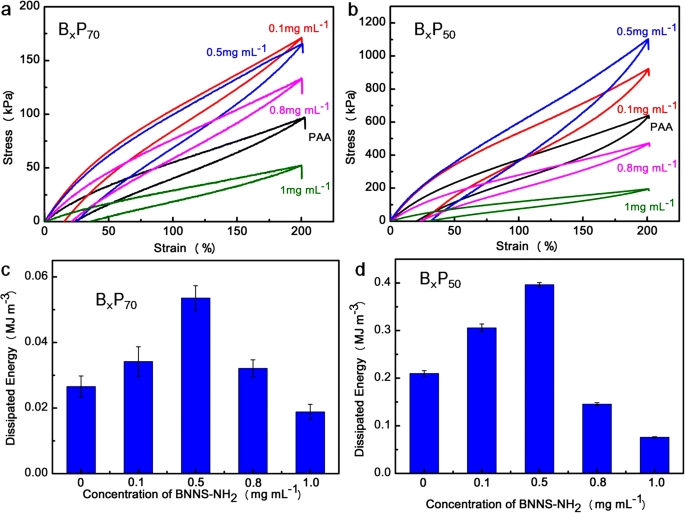
Tensão cíclica das curvas de carga-descarga de a B x P 70 e b B x P 50 ; a energia dissipada de c B x P 70 e d B x P 50
O rápido processo de autocura pode ser realizado sem qualquer estímulo externo com base nas abundantes interações físicas:interações de coordenação de metal e ligações de hidrogênio. Conforme mostrado na Fig. 7a-c, o hidrogel original foi cortado em três partes (duas partes foram tingidas de vermelho pela Rodamina B para distinguir as cicatrizes do hidrogel danificado) e então eles entraram em contato com as superfícies danificadas. Sem qualquer estímulo externo, o hidrogel cortado em contato por 10 min em temperatura ambiente, o hidrogel curado pode ser esticado para certa tensão. A eficiência de autocura pode ser calculada a partir da razão da tensão de fratura dos hidrogéis curados e dos hidrogéis originais. B original 0 P 70 exibiu tensão de fratura de ~ 410 kPa, e o hidrogel curado correspondente exibiu uma tensão de fratura de apenas ~ 37 kPa, indicando que a eficiência de autocura foi de apenas 9%. Em comparação, a tensão de fratura do B 1 original e curado P 70 eram cerca de ~ 203 kPa e ~ 166 kPa, respectivamente, e a eficiência de autocura é de cerca de 81%, o que é significativamente maior do que os hidrogéis sem o BNNS-NH 2 . Da mesma forma, como mostrado na Fig. 7e, a eficiência de autocura de B 0 P 50 hidrogel foi de 31,8%, enquanto o B 1 P 50 hidrogel foi de 94,6%. Este resultado indica que a presença de ligações de hidrogênio em nanoescala entre BNNS-NH 2 e as cadeias de polímero de PAA em nanoescala aumentaram a capacidade de autocura atribuindo que o conteúdo das ligações reversíveis é o fator de influência chave da eficiência de autocura, e é bem conhecido que a eficiência de autocura é proporcional ao conteúdo do reversível ligações [16, 21, 36, 42]. No entanto, enquanto o conteúdo de água foi reduzido para 25% em peso (Arquivo adicional 1:Figura S8), a eficiência de autocura diminuiu drasticamente, porque o movimento de Fe 3+ foi impedido com um conteúdo de água tão baixo. Esta suposição foi confirmada pelo fato de que a eficiência de cura de B x P 90 era muito melhor do que outro teor de água, com apenas 10 minutos necessários atribuídos ao motivo de que maiores teores de água tornam o Fe 3+ para migrar facilmente e restabelecer as ligações de hidrogênio prontamente [36].
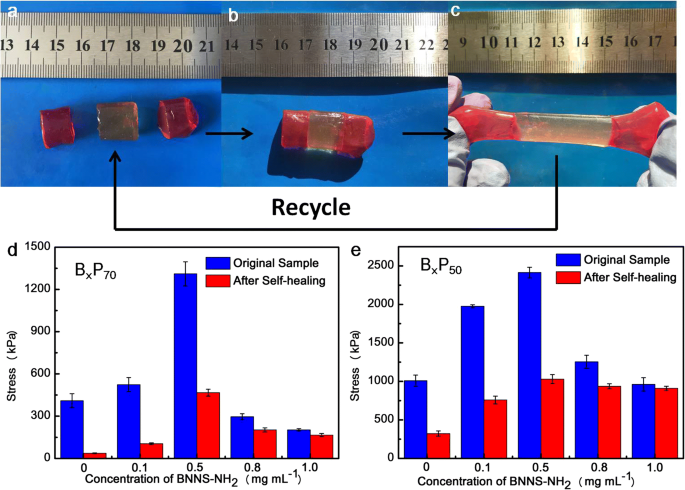
Processo de autocura de B 0,5 P 90 ( a ) o hidrogel foi cortado em três partes (as duas partes terminais foram tingidas de vermelho pela Rodamina B). b Coloque as três partes estritamente juntas, uma a uma. c Após 10 minutos de cura, o hidrogel curado pode ser alongado. d As tensões de fratura do B x original P 70 e curou B x P 70 . e As tensões de fratura do B x original P 50 e curou B x P 50. O tempo de cura foi de 1 h
Conclusões
Em resumo, os novos hidrogéis compostos foram fabricados por meio de interações físicas hierárquicas:a interação de coordenação de metal em escala molecular e ligação de hidrogênio em nanoescala. Os hidrogéis exibem maior rigidez (cerca de 17,9 MPa), resistência (cerca de 10,5 MJ m - 3 ), extensão e capacidade de autocura. A reversibilidade da interação de coordenação de metal e interação de ligação de hidrogênio é responsável pelas propriedades mecânicas aprimoradas e eficiência de autocura. Combinado com uma preparação fácil, propriedades mecânicas aprimoradas e capacidade de autocura tornam esses hidrogéis compostos adequados para muitas aplicações potenciais.
Abreviações
- B x P y :
-
Hidrogel composto com o BNNS-NH 2 concentração de x mg mL - 1 e conteúdo de água de y % em peso
- Fe 3+ :
-
Íon férrico
- FTIR:
-
Transformada de Fourier Infra-vermelho
- PAA / BNNS-NH 2 :
-
Nanofolhas de poli (ácido acrílico) / nitreto de boro com superfície modificada
- PAA / GO:
-
Óxido de grafeno / poli (ácido acrílico)
- SEM:
-
Digitalizando micrografias eletrônicas
Nanomateriais
- Propriedades e aplicações do tântalo
- Síntese e propriedades eletroquímicas de materiais catódicos de LiNi0,5Mn1,5O4 com dopagem composta Cr3 + e F− para baterias de íon-lítio
- Síntese fácil de compósito CuSCN colorido e condutor revestido com nanopartículas de CuS
- Fabricação fácil de composto de polianilina porosa multi-hierárquica como sensor de pressão e sensor de gás com sensibilidade ajustável
- Propriedades elétricas de materiais compostos com alinhamento assistido por campo elétrico de cargas de nanocarbono
- Estabilidade aprimorada de nanopartículas magnéticas de ouro com poli (ácido 4-estirenossulfônico-ácido co-maleico):propriedades ópticas sob medida para detecção de proteínas
- Síntese de aquecimento de estado sólido de composto de poli (3,4-etilenodioxitiofeno) / ouro / grafeno e sua aplicação para determinação amperométrica de nitrito e iodato
- Fabricação, Caracterização e Atividade Biológica de Sistemas de Nanotransmissão de Avermectina com Diferentes Tamanhos de Partículas
- Dependência da toxicidade das nanopartículas em suas propriedades físicas e químicas
- Propriedades dos Materiais de Engenharia:Gerais, Físicas e Mecânicas



