Fósforo emissor de luz verde ativado por Eu2 +, obtido a partir de íons de dopagem com zeólita-3A em ambientes aéreos com Eu3 + e seus diodos emissores de luz verde eficientes
Resumo
Eu 2+ - fósforos ativados são amplamente aplicados em áreas de iluminação e exibição devido ao seu bom desempenho óptico. Neste artigo, um excelente zeólito-3A com emissão de verde:1,3% em peso de fósforo Eu é preparado por um método de reação térmica elevada verde e ecologicamente correto, sem qualquer atmosfera ou agentes redutores. Enquanto isso, o mecanismo de redução de Eu 3+ íons para Eu 2+ íons é investigado. Os resultados do experimento mostram que a morfologia, a estrutura cristalina e a propriedade luminescente são afetadas pela temperatura de sinterização. A amostra resultante mostra que a banda larga de excitação está na faixa de 310–450 nm e o pico da banda larga de emissão está localizado em 523 nm. Além disso, zeólita-3A:1,3% em peso de fósforo Eu é encapsulado em um chip emissor de UV comercial para fabricar um diodo emissor de luz verde (LED) de pureza com as coordenadas de cor da Commission Internationale de L'Eclairage (CIE) em (0,295, 0,537 )
Histórico
Materiais luminescentes são amplamente utilizados em muitos campos, como iluminação e dispositivos de exibição [1,2,3,4,5]. Ao longo dos anos, materiais luminescentes ativados por európio (Eu) de terras raras (RE) têm recebido mais atenção devido às suas propriedades ópticas únicas, como alto brilho [6, 7], alta estabilidade química [8, 9] e excelente eco-amizade [8, 10]. Em particular, os íons Eu têm dois estados de oxidação de divalente (Eu 2+ ) e trivalente (Eu 3+ ), exibindo diferentes características de emissão. Geralmente, eu 3+ íons são principalmente como um ativador emissor de vermelho que se originou de 5 D 0 → 7 F J ( J =1, 2, 3, 4 e 5) transições [11,12,13]. No entanto, eu 2+ íons, seus elétrons 5d localizados nos orbitais externos, são suscetíveis aos seus arredores. Assim, suas emissões são facilmente afetadas pelo ambiente do campo cristalino, possuindo uma ampla região do ultravioleta (UV) ao vermelho. Chen et al. preparado Eu 2+ -fluorofosfatos ativados Ba 3 GdNa (PO 4 ) 3 F com fósforo com emissão de cor dupla azul e vermelho [14]. Sato et al. relatado emissor de vermelho Ca 2 SiO 4 :Eu 2+ fósforos [15]. Lin et al. Eu sintetizado 2+ , Mn 2+ -ativado Ca 9 Mg (PO 4 ) 6 F 2 fósforos com emissão de cor azul a amarela [16]. É sugerido que Eu 2+ fósforos ativados causados por transições eletrônicas 5d-4f permitidas por paridade mostram forte banda larga de emissão [7]. Portanto, o Eu 2+ fósforos ativados são o foco principal dos materiais luminescentes nos últimos anos.
Hoje em dia, eu 2+ -materiais luminescentes dopados são obtidos reduzindo Eu 3+ para eu 2+ , porque não há eu natural 2+ -materiais dopados. Normalmente, pode ser realizado em uma atmosfera redutora, incluindo H 2 , H 2 / N 2 ou CO. Por exemplo, Gao et al. recentemente obtido eu 2+ Fósforo ativado de Eu 3+ - USY trocado (Na 28 Si 168 Al 28 · 240H 2 Razão O, Si / Al =6) zeólitas por tratamento térmico em H 2 / N 2 atmosfera redutora [17]. Chen et al. relatou que eu 2+ -sensibilizado Sr 6 Ca 4 (PO 4 ) 6 F 2 :Tb 3+ fósforo pode ser obtido usando o método de estado sólido de alta temperatura em H 2 / N 2 atmosfera redutora [18]. No entanto, a reação em atmosfera redutiva é relativamente perigosa e requer um ambiente de trabalho bem equipado, o que acarreta um custo mais elevado de fósforos. Além disso, a poluição ambiental será produzida se a reação for conduzida em condições de redução de CO. Portanto, um método de preparação verde, ecológico e de baixo custo atraiu mais atenção.
Como é bem sabido, Eu 3+ entre alguns hospedeiros compostos especiais, como boratos [19], fosfatos [20] e aluminatos [21], também podem ser reduzidos a Eu 2+ no ar a uma temperatura elevada. É sugerido que todos esses compostos contêm BO tetraédrico rígido 4 , PO 4 , AlO 4 , ou octaédrico AlO 6 estrutura do grupo, envolvendo e isolando o Eu 2+ produzido íons de oxigênio [21, 22]. As zeólitas, como um tipo de aluminossilicato, não são apenas minerais naturais, mas também podem ser sintetizadas na indústria a um custo menor [23,24,25,26,27,28]. Notavelmente, sua estrutura pode satisfazer os requisitos mencionados acima, reduzindo Eu 3+ íons para Eu 2+ íons e fazendo Eu 2+ íons estáveis. Eles também são amplamente utilizados como excelentes materiais hospedeiros para aplicações de materiais luminescentes devido à alta estabilidade química [29, 30] e assim por diante. Entre vários zeólitos, zeólita-3A (\ (\ frac {2} {3} \) K 2 O · \ (\ frac {1} {3} \) Na 2 O · Al 2 O 3 · 2SiO 2 · \ (\ Frac {9} {2} \) H 2 A razão O, Si / Al ≈ 1) tem sido usada como material hospedeiro para fósforo de conversão descendente. Aqui, alcançamos Eu 2+ Fósforo de zeólita-3A ativado por método de tratamento térmico de alta sem qualquer atmosfera redutora. A UE obtida 2+ O fósforo zeólito-3A ativado tem um rendimento quântico de cerca de 36,6%. Este método de preparação é seguro, ecológico e ecologicamente correto. A ampla banda de excitação da amostra que obtivemos está na faixa de 310–450 nm, e o pico da banda de emissão está localizado em 523 nm. E as amostras são estáveis e facilmente re-preparadas. Ao encapsular zeólita-3A emissora de verde:1,3% em peso de fósforo Eu em um chip emissor de UV, adquirimos um bom LED verde com as coordenadas de cor da Commission Internationale de L'Eclairage (CIE) em (0,295, 0,537) e brilho de 231,6 cd / m 2 sob tensão de 3 V. Esses resultados não apenas mostram uma abordagem de preparação simples e ecológica, mas também fornecem um fósforo de emissão verde excelente com aplicações promissoras nas áreas de iluminação e exibição.
Métodos
O objetivo do estudo
Nosso objetivo é preparar a UE 2+ - fósforos ativados com emissão verde brilhante por meio de método de síntese seguro, verde e ecológico, sem redução da atmosfera.
Materiais
Zeólita-3A (\ (\ frac {2} {3} \) K 2 O · \ (\ frac {1} {3} \) Na 2 O · Al 2 O 3 · 2SiO 2 · \ (\ Frac {9} {2} \) H 2 Razão O, Si / Al ≈ 1) adquirido de Shanghai Tongxing Molecular Sieve Co., LTD, e óxido de európio (Eu 2 O 3 ) obtidos de Sinopharm Co., Ltd, foram usados sem qualquer purificação adicional. Resina de silicone e chip azul InGaN (5 mm × 5 mm, λ =375 nm) foram recebidos da Shenzhen Looking Long Technology Co., Ltd.
Síntese de Amostras
Eu 2+ As amostras de zeólita-3A ativadas foram preparadas usando um método típico de reação de estado sólido de alta temperatura. Em primeiro lugar, diferentes quantidades estequiométricas de zeólita-3A e Eu 2 O 3 foram bem misturados e bem moídos em almofariz de ágata por 40 min. E então, eles foram sinterizados em diferentes temperaturas sem reduzir a atmosfera. Finalmente, as amostras alvo foram obtidas após o resfriamento.
Fabricação de LEDs verdes
Eu 2+ em pó de zeólito-3A ativado e resina de silicone foram misturados de acordo com a proporção de massa de 1:5, em seguida, agitados homogeneamente. A composição foi revestida em um chip InGaN e curada sob 60 ° C por cerca de 2 h. Finalmente, a espessura do compósito foi medida em cerca de 1 mm.
Caracterização
A morfologia e a estrutura dos produtos resultantes foram caracterizadas através de microscópio eletrônico de varredura por emissão de campo (FESEM, FEI Sirion-200) e difração de raios-X (XRD, Philips X’Pert) com radiação Cu Kα ( λ =0,15405 nm). As curvas de análise termogravimétrica (TG) foram medidas por SDT Q600 V20.9 Build 20, que foram obtidas da temperatura ambiente a 800 ° C com uma taxa de aquecimento de 10 ° C / min em uma atmosfera de nitrogênio (taxa de fluxo de 10 ml / min) . Os espectros de excitação de fotoluminescência (PLE) e fotoluminescência (PL) foram obtidos à temperatura ambiente usando os espectrômetros de fluorescência de estado estacionário e de resolução de tempo FLS920 da Edinburgh Instruments equipados com uma lâmpada Xe de 450-W. O estado de oxidação do elemento európio foi investigado por espectroscopia de fotoelétrons de raios-X (XPS, ESCALAB 250). O espectro de eletroluminescência (EL) foi investigado pelo espectrômetro Ocean Optics FLAME-S-VIS-NIR com uma esfera integradora de fibra (FOIS-1) e um eletrômetro Keithley 2400.
Resultados e discussão
A Figura 1a mostra a imagem SEM do zeólito-3A puro. Pode-se observar que a morfologia da zeólita-3A original é uma estrutura cúbica irregular com o comprimento lateral de cerca de 1,5 μm. Zeólita-3A:fósforos de 1,3% em peso de Eu são obtidos através do método de reação em estado sólido de alta temperatura, sem qualquer atmosfera redutora. A morfologia e a estrutura do zeólito-3A:1,3% em peso de fósforo Eu obtido a 1400 ° C por 3 h são caracterizadas pelo microscópio eletrônico de varredura de emissão de campo e medições de difração de raios-X, como mostrado na Fig. 1b, c, respectivamente. A Figura 1b mostra que as partículas apresentam estrutura morfológica irregular e a distribuição dos tamanhos dos cristalitos não é uniforme. Comparando a Fig. 1b com a, pode-se verificar que as partículas de zeólita são agregadas umas às outras após sinterização a 1400 ° C por 3 h. Como pode ser visto na Fig. 1c, todos os picos de difração no padrão de XRD de zeólito-3A:1,3% em peso de fósforo Eu estão em bom acordo com a fase de zeólito-3A puro (JCPDS no. 00-019-1227), e não outros picos de impureza são observados. Isso significa que eu 2+ íons são introduzidos com sucesso nas redes hospedeiras do zeólito e uma certa quantidade de Eu 2+ A dopagem de íons obviamente não altera a estrutura cristalina [10]. A Figura 1d mostra curvas TG de zeólito-3A e zeólito-3A puro:1,3% em peso de fósforo Eu sinterizado a 1400 ° C. Pode-se observar que há uma perda de massa contínua durante o aquecimento até cerca de 266 ° C na curva TG para o zeólito-3A puro, onde atinge um valor de cerca de 19,45%. Isso corresponde à liberação de água fisicamente ligada, localizada nas cavidades e canais da zeólita-3A [31]. O fenômeno de perda de massa não é óbvio, pois aumenta a temperatura sequencialmente. Como visto a partir da curva TG do zeólito-3A:1,3% em peso de fósforo Eu sinterizado a 1400 ° C, quase não há perda de massa. Estes resultados indicam que o zeólito-3A:1,3% em peso de Eu sinterizado a 1400 ° C é muito estável.
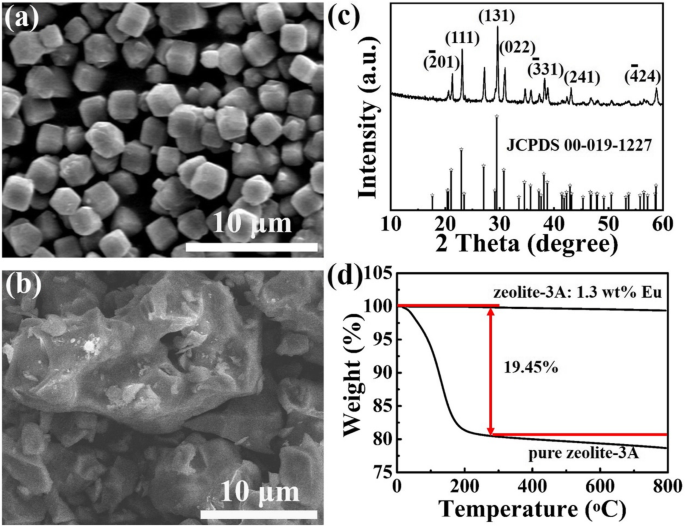
As imagens SEM de a zeólito-3A e b puro zeólita-3A:1,3% em peso de fósforo Eu sinterizado a 1400 ° C por 3 h. c Padrão de XRD de zeólita-3A:1,3% em peso de fósforo Eu sinterizado a 1400 ° C por 3 h. d Curvas TG de zeólita-3A e zeólita-3A pura:1,3% em peso de fósforo Eu sinterizado a 1400 ° C por 3 h
A Figura 2 mostra as imagens de SEM e padrões de XRD do zeólito-3A:1,3% em peso de fósforos Eu sinterizados em diferentes temperaturas. A partir das imagens de MEV (Fig. 2a-d), é claro observar que a morfologia muda significativamente com o aumento da temperatura de sinterização. Quando a temperatura de sinterização é relativamente mais baixa (600 ° C e 800 ° C), a morfologia das amostras ainda se mantém como a zeólita-3A intocada, ou seja, em formato cúbico com tamanho médio de 1,5 μm (mostrado na Fig. 1a) . Porém, pode-se observar que as partículas começam a agregar quando a temperatura de sinterização atinge 1000 ° C e 1200 ° C. Conforme a temperatura de sinterização aumenta, as partículas podem continuar a se agregar e formar uma estrutura massiva (Fig. 1b). Enquanto isso, seus padrões de XRD são mostrados na Fig. 2e. É notável que os picos de difração de amostras preparadas a 600 ° C e 800 ° C não são absolutamente indexados ao cartão padrão zeólito-3A puro (JCPDS nº 00-019-1227). Duas amostras existem picos de difração extra localizados em 12,5 ° e 16,3 °, que são atribuídos aos picos de Eu 2 O 3 (JCPDS nº 00-012-0384). Isso significa que os íons Eu não podem ser incorporados com sucesso nas redes hospedeiras da zeólita quando a temperatura de calcinação é inferior a 800 ° C [32]. No entanto, as amostras sinterizadas acima de 1000 ° C mostram picos correspondentes aos principais picos característicos do cartão padrão zeólito-3A puro.
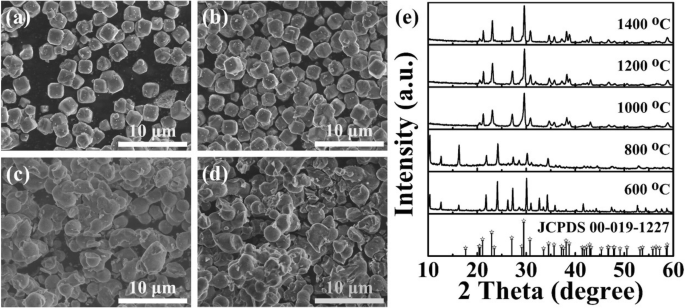
Imagens SEM do zeólito-3A:1,3% em peso de fósforos Eu sinterizados a 600 ° C ( a ), 800 ° C ( b ), 1000 ° C ( c ), e 1200 ° C ( d ), respectivamente. e Padrões de XRD de zeólita-3A:1,3% em peso de fósforos Eu sinterizados em diferentes temperaturas, respectivamente
Para investigar o efeito da temperatura de calcinação na emissão de PL, os espectros de emissão de PL das amostras em diferentes temperaturas de calcinação são testados e mostrados na Fig. 3a. Como visto na inserção, as amostras sinterizadas a 600 ° C e 800 ° C mostram apenas o pico de emissão vermelha centrado em 617 nm, que é atribuído ao 5 D 0 → 7 F 2 transição elétrica-dipolo de Eu 3+ íon [33]. À medida que a temperatura de sinterização aumenta, o pico de emissão vermelha torna-se gradualmente fraco e o pico de emissão verde (centrado em 523 nm) é obviamente observado. Especialmente, a amostra preparada a 1400 ° C mostra principalmente uma característica típica Eu 2+ emissão centrada em 523 nm, que é devido ao 4f 6 5d → 4f 7 transição [34]. Ao comparar as diferentes curvas de PL na Fig. 3a, pode-se observar que a quantidade de Eu 3+ → Eu 2+ aumenta continuamente com o aumento da temperatura de sinterização. Este resultado coincide com o dos padrões de XRD na Fig. 2e. Ou seja, Eu 3+ íon é a principal forma quando a temperatura de calcinação é inferior a 1000 ° C. Eu 3+ íons são gradualmente reduzidos para Eu 2+ íons quando a temperatura de sinterização é superior a 1000 ° C. A Figura 3b mostra os espectros de PLE e PL da amostra sinterizada a 1400 ° C. Pode-se descobrir que o espectro de PLE mostra uma banda de excitação ampla entre cerca de 310 e 450 nm [7, 35]. E a inserção é a fotografia que mostra uma emissão de luz verde brilhante com a iluminação de uma lâmpada UV de 365 nm. O espectro de PL na Fig. 3b é consistente com a cor testemunhada na fotografia.
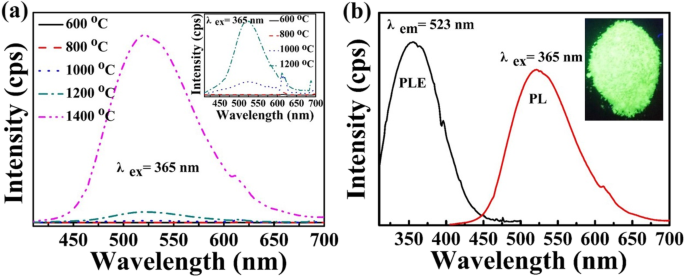
a Espectro de emissão PL para zeólita-3A:1,3% em peso de fósforos Eu sinterizados em diferentes temperaturas, respectivamente. A inserção mostra os espectros de ampliação. b espectros de excitação de fotoluminescência (PLE) e de emissão de fotoluminescência (PL) para zeólita-3A:1,3% em peso de fósforos de Eu sinterizados a 1400 ° C por 3 h. A inserção é a fotografia da amostra com a iluminação de uma lâmpada UV de 365 nm
A fim de investigar melhor o estado de oxidação do elemento Eu, o padrão XPS de Eu3d para a amostra obtida a 1400 ° C é monitorado e mostrado na Fig. 4. Os picos localizados em 1165 eV e 1135 eV correspondem a Eu 3+ estado de oxidação, mas os picos em torno de 1155 eV e 1125 eV são atribuídos a Eu 2+ estado de oxidação [11, 36]. Este resultado mostra que alguns dos Eu 3+ os íons são reduzidos a Eu 2+ íons no hospedeiro zeólita sob reação de tratamento térmico de alta, e este resultado é consistente com os espectros PL (Fig. 3). O possível mecanismo de reação pode ser mostrado nas seguintes equações:
$$ {\ mathrm {Eu}} _ 2 {\ mathrm {O}} _ 3 \ overset {{\ mathrm {K}} _ 2 \ mathrm {O}} {\ to} \ kern0.5em 2 {\ left [{\ mathrm {Eu}} ^ {3 +} \ right]} _ {\ mathrm {K}} ^ {\ ast \ ast} + \ kern0.5em 4 {V} _ {\ mathrm {K}} ^ {\ prime } +3 {\ mathrm {O}} _ {\ mathrm {O}} ^ {\ times} $$ (1) $$ {V} _ {\ mathrm {K}} ^ {\ prime} \ to {V } _ {\ mathrm {K}} ^ {\ times} \ kern0.5em + {\ mathrm {e}} ^ {\ prime} $$ (2) $$ {\ left [{\ mathrm {Eu}} ^ {3 +} \ right]} _ {\ mathrm {K}} ^ {\ ast \ ast} \ kern0.5em + {\ mathrm {e}} ^ {\ prime} \ to {\ left [{\ mathrm { Eu}} ^ {2 +} \ right]} _ {\ mathrm {K}} ^ {\ ast} $$ (3) $$ {\ left [{\ mathrm {Eu}} ^ {2 +} \ right ]} _ {\ mathrm {K}} ^ {\ ast} + {\ mathrm {e}} ^ {\ prime} \ to {\ left [{\ mathrm {Eu}} ^ {2 +} \ right]} _ {\ mathrm {K}} ^ {\ times} $$ (4)
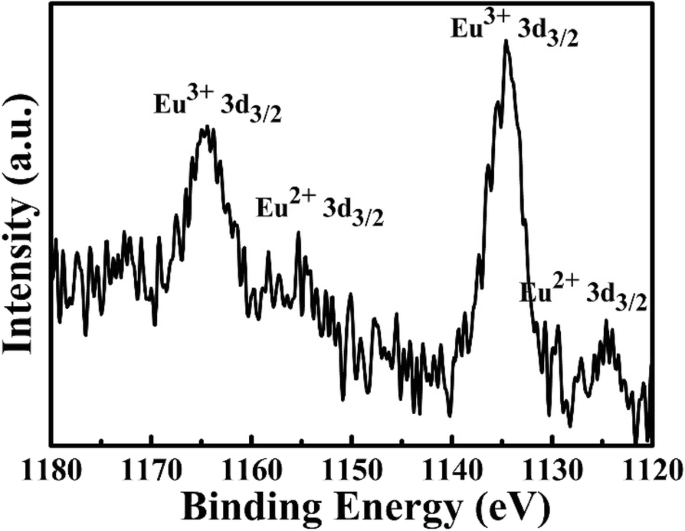
Espectro XPS para o elemento Eu do zeólito-3A:1,3% em peso de fósforos Eu sinterizados a 1400 ° C por 3 h
Aqui, [Eu 3+ ] K e [Eu 2+ ] K representam Eu 3+ e eu 2+ substituição de íons por K + posição dos íons, respectivamente; O o representa a posição de um oxigênio para o oxigênio no cristal da matriz; e V K é a vaga de K + íon. Sobrescrito “*,” “**,” “′,” e “×” indicam uma carga positiva, duas cargas positivas, uma carga negativa e eletroneutralidade, respectivamente. Durante a sinterização, Eu 3+ íon substitui K + posição no zeólito. Para manter o saldo da carga, um Eu 3+ íon irá substituir por três K + íons. Assim, dois defeitos de vacância de K + íons ( V K ′ ) e um defeito de Eu 3+ íon ([Eu 3+ ] K ** ), que carrega uma carga negativa e duas cargas positivas na aparência, respectivamente, criará no hospedeiro zeólito (visto da Eq. (1)). Em seguida, a vaga V K ′ atuará como um doador de elétrons (visto da Eq. (2)), e o [Eu 3+ ] K ** defeito é o aceitador dos elétrons. Em alta temperatura, [Eu 3+ ] K ** irá capturar um elétron da vaga de K + íons ( V K ′ ) e esse elétron será preenchido na órbita 4f do íon Eu. Portanto, eu 3+ íon é reduzido para Eu 2+ e [Eu 3+ ] K ** defeito torna-se [Eu 2+ ] K * defeito (visto da Eq. (3)). Neste momento, a posição de Eu 2+ íon está com uma carga positiva aparente. [Eu 2+ ] K * defeito atrairia o elétron negativo de outro K + vacância ao seu redor e torna-se eletroneutralidade aparente [Eu 2+ ] K × (mostrado na Eq. (4)) [11, 21, 22, 37,38,39,40,41].
É sugerido que a estrutura tetragonal tridimensional rígida de AlO 4 e SiO 4 pode envolver Eu 2+ íons e isolá-los do oxigênio e, em seguida, Eu 2+ pode existir constantemente em nossos fósforos de objetivo.
Para otimizar a propriedade da zeólita-3A:1,3% em peso de fósforo Eu e observar o efeito do elemento Eu na PL, os espectros de emissão da PL e a intensidade relativa da PL para diferentes quantidades estequiométricas de zeólita-3A e Eu 2 O 3 são mostrados na Fig. 5. Pode ser visto na Fig. 5a que a intensidade de emissão de Eu 2+ aumenta com a concentração de dopagem de Eu 2 O 3 aumentando de 0,9 para 1,3%. No entanto, diminui com o aumento contínuo da concentração de dopante. Pode-se observar claramente que o efeito PL é melhor quando a concentração de Eu-doping está em torno de 1,3%. Pode-se explicar que quanto mais eu 2+ íons, os centros mais luminescentes. Quando a concentração do elemento Eu está além de 1,3%, a diminuição da intensidade do PL pode ser atribuída à extinção da concentração, que é causada principalmente pela transferência de energia entre Eu 2+ íons. Quando a concentração de Eu 2+ íons aumentam, a distância entre eu 2+ os íons serão curtos e, então, a transferência de energia aumentará [42,43,44]. A curva de barra de erro da intensidade relativa PL versus concentração de dopagem Eu é mostrada na Fig. 5b. Isso indica que a variação da intensidade relativa de PL para cada concentração de Eu é pequena, o que significa que essas amostras são muito repetíveis.
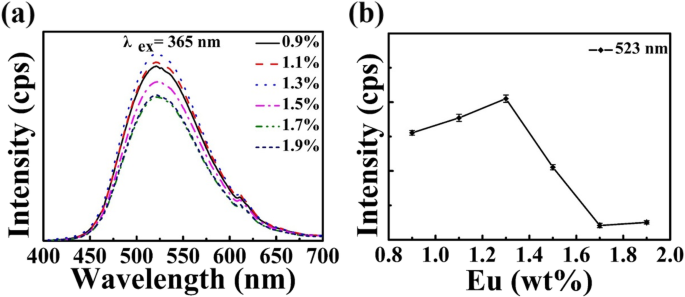
a Espectros de emissão PL e b a intensidade relativa PL varia com a concentração do elemento Eu para zeólita-3A:1,3% em peso de fósforos Eu ( x =0,9 ~ 1,9) sinterizado a 1400 ° C por 3 h
Como prova de aplicação de iluminação, o zeólito-3A emissor de verde:1,3% em peso de fósforo Eu é encapsulado em um chip emissor de UV para fabricar LED verde. O espectro de emissão EL na tensão de 3 V é mostrado na Fig. 6a. Pode-se descobrir que os picos de emissão do chip emissor de UV e do fósforo emissor de verde estão localizados a ~ 375 nm e ~ 523 nm, respectivamente. E a inserção é a fotografia de um LED verde funcionando que emite uma luz verde brilhante com uma voltagem de 3 V. As coordenadas de cor (Fig. 6b) são calculadas como (0,295, 0,537) para o LED verde resultante, indicando pureza superior da cor verde.
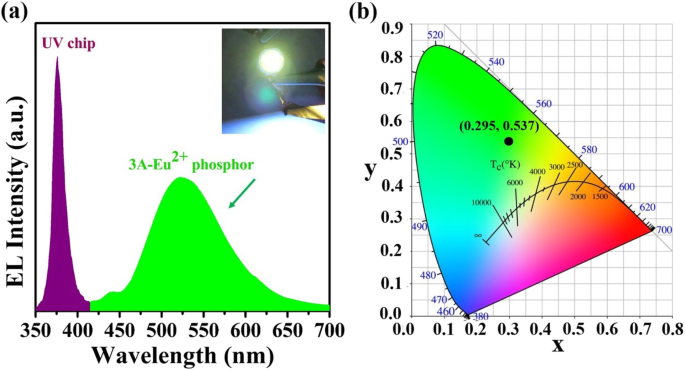
a Espectro de emissão de eletroluminescência com voltagem de 3 V para zeólita-3A:1,3% em peso de fósforo Eu sinterizado a 1400 ° C por 3 h, e a inserção é uma fotografia de LED verde funcionando com voltagem de 3 V. b Coordenada de cor no diagrama CIE1931
Conclusões
Neste trabalho, obtivemos uma emissão verde brilhante zeólita-3A:Eu 2+ fósforo com um rendimento quântico de cerca de 36,6% e o pico de emissão localizado a 523 nm por meio de um método de reação térmica de alta temperatura ecologicamente correto sem qualquer atmosfera redutora. Além disso, a amostra tem uma ampla banda de excitação na faixa de 310-450 nm, que pode corresponder à excitação do chip UV comercial (na verdade, λ =375 nm). Eu 2+ Os íons podem ser incorporados gradualmente nas redes hospedeiras da zeólita conforme a temperatura de calcinação aumenta. Nossa pesquisa mostra que a temperatura ótima de sinterização é 1400 ° C e a melhor concentração de dopagem de íons Eu é 1,3%. Fazendo uso do zeólito-3A emissor de verde:Eu 2+ fósforo encapsulado em um chip emissor de UV, um bom LED verde com as coordenadas de cor da Commission Internationale de L’Eclairage (CIE) em (0,295, 0,537) e brilho de 231,6 cd / m 2 é obtido. E a emissão verde zeólita-3A:fósforos de 1,3% em peso de Eu com propriedades luminescentes crescentes serão aplicações promissoras para iluminação e exibição.
Disponibilidade de dados e materiais
Os conjuntos de dados que suportam as conclusões deste artigo estão disponíveis no artigo.
Abreviações
- CIE:
-
Commission Internationale de L'Eclairage
- EL:
-
Eletroluminescência
- Eu:
-
Europium
- FESEM:
-
Microscópio eletrônico de varredura de emissão de campo
- LED:
-
Diodo emissor de luz
- PL:
-
Fotoluminescência
- PLE:
-
Excitação fotoluminescente
- RE:
-
Terra rara
- TG:
-
Análise termogravimétrica
- XPS:
-
espectroscopia de fotoelétrons de raios-X
- XRD:
-
Difração de raios X
Nanomateriais
- Software de manutenção móvel e sua função na criação de fluxos de trabalho eficientes
- Remoção adsortiva de íons de cobre (II) de solução aquosa usando um nanoadsorvente de magnetita de resíduos de escala de moinho:Síntese, caracterização, adsorção e modelagem cinética Estud…
- Dopagem Substitucional para Mineral Aluminossilicato e Desempenho Superior de Divisão de Água
- Síntese One-Pot Green da Microsfera SnO2 Decorada com Ag:um Catalisador Eficiente e Reutilizável para Redução de 4-Nitrofenol
- Síntese verde de pontos quânticos InP / ZnS Core / Shell para aplicação em diodos emissores de luz livres de metais pesados
- Preparação de nanoesferas poliméricas impressas com íons de paládio (II) e sua remoção de paládio (II) da solução aquosa
- Platycodon saponins from Platycodi Radix (Platycodon grandiflorum) para a síntese verde de nanopartículas de ouro e prata
- Diodos emissores de luz ultravioleta baseados em AlGaN quase isentos de eficiência com uma camada de bloqueio de elétrons tipo p de superrede especificamente projetada para alta eficiência de dopag…
- Fabricação de nanofibras helicoidais CA / TPU e sua análise de mecanismo
- Avaliação de toxicidade de nanopartículas de PEG-PCCL e investigação preliminar sobre seu efeito antitumoral de carregamento de paclitaxel



