Dopagem Substitucional para Mineral Aluminossilicato e Desempenho Superior de Divisão de Água
Resumo
O dopagem de substituição é uma estratégia na qual impurezas atômicas são opcionalmente adicionadas a um material hospedeiro para promover suas propriedades, enquanto a evolução da estrutura geométrica e eletrônica do mineral de nanoargila natural após o dopagem de metal de substituição ainda é ambígua. Este artigo primeiro projetou uma estratégia de dopagem de lantânio (La) eficiente para argila nanotubular (nanotubo de halloysite, HNT) por meio do equilíbrio dinâmico de um átomo substitucional na presença de AlCl saturado 3 solução, e a caracterização sistemática das amostras foi realizada. Outros cálculos da teoria funcional da densidade (DFT) foram realizados para revelar a evolução da estrutura geométrica e eletrônica sobre o dopagem de metais, bem como para verificar o efeito do dopagem de La em nível de átomo. O carregamento de CdS e seu desempenho de divisão de água correspondente podem demonstrar o efeito do doping de La. Nanopartículas de CdS (11% em peso) foram depositadas uniformemente na superfície do nanotubo de aloisita dopado com La (La-HNT) com o tamanho médio de 5 nm, e a notável taxa de evolução de hidrogênio fotocatalítico de CdS / La-HNT atingiu até 47,5 μmol / h. Os resultados podem fornecer uma nova estratégia para dopagem com íons metálicos e uma visão construtiva do mecanismo de dopagem substitucional.
Histórico
Minerais de aluminossilicato (por exemplo, caulinita [1,2,3], zeólita [4, 5] montmorilonita [6, 7] e aloisita [8,9,10,11,12,13]) foram extensivamente investigados como suporte do catalisador materiais porque não são tóxicos para o meio ambiente e estão disponíveis em abundância e de baixo custo em depósitos naturais. Uma série de técnicas têm sido usadas para melhorar as funcionalidades dos materiais de suporte, como revestimento de polímero [14, 15], revestimento de carbono [8] e dopagem atômica [16,17,18,19]. Os minerais aluminossilicatos dopados podem se formar na natureza, mas sua síntese em um laboratório permite várias propriedades com os dopantes especificados [20,21,22,23]. A incorporação de íons metálicos na estrutura da camada de aluminossilicato torna o nanomaterial correspondente atraente para várias aplicações, incluindo catálise [24,25,26], liberação controlada de produtos farmacêuticos [27, 28], bem como baterias de íon de lítio [29, 30]. Recentemente, com base em cálculos da teoria funcional da densidade (DFT), a estabilidade, propriedades eletrônicas e mecânicas dos aluminossilicatos nanoestruturados, como imogolita, aloisita e crisotila, foram reveladas [31]. No entanto, o mecanismo de dopagem substitucional e a evolução da estrutura eletrônica de um metal nos aluminossilicatos ainda são ambíguos [32, 33].
Com o objetivo de melhorar nossa compreensão deste mecanismo, projetamos uma estratégia de dopagem eficiente para um dos minerais de aluminossilicato representativos (nanotubo de halloysite [34,35,36], HNT) através do equilíbrio dinâmico de um átomo substitucional na presença de saturados AlCl 3 solução, que continha sal de lantânio. Em seguida, uma estratégia de dopagem atômica substitucional baseada na dopagem La na estrutura HNT e a parte substituída do átomo de Al da folha de Al – O é apresentada. Halloysite (HNTs, Al 2 Si 2 O 5 (OH) 4 ∙ nH 2 O), como um mineral de argila natural, contém gibbsita Al (OH) octaédrica 3 e tetraédrico SiO 4 folhas, e também consiste em cilindros ocos formados por múltiplas camadas laminadas. O CdS é um material semicondutor atraente que pode converter energia solar em energia química sob irradiação de luz visível. A incorporação de nanopartículas de CdS em La-HNTs e seu desempenho de separação de água correspondente pode demonstrar os efeitos do doping de La. O processo de difusão de Al 3+ solução saturada e as folhas de alumina de haloysite, a mudança de formas de cristal e estruturas de superfície, e a possibilidade de atividade catalítica aumentada foram investigados em detalhes. As microestruturas e morfologias das amostras foram caracterizadas, e a estrutura interfacial entre CdS e La-HNT foi investigada. A atividade fotocatalítica do hidrogênio foi avaliada e o papel do La-HNT para aumentar a atividade catalítica do CdS / La-HNT também foi investigado.
Métodos
Seção Experimental
Preparação de materiais
Nanotubos de Halloysite (HNT) foram obtidos em Hunan, China. Todos os produtos químicos eram de grau analítico e usados sem purificação adicional. HNT foram pré-tratados via dispersão de emulsão, filtração, lavagem com água destilada e secagem por 8 h a 313 K. La-HNT foram sintetizados por uma rota hidrotérmica modificada. Uma quantidade de 34,3 g de AlCl 3 foi dissolvido em 60 mL de água desionizada para formar AlCl 3 solução supersaturada, enquanto 3 mmol HNT e 6 mmol La (NO 3 ) 3 · 6H 2 O foram dissolvidos em água desionizada (5 mL), respectivamente. Então La (NÃO 3 ) 3 · 6H 2 Solução O e a pasta de HNT foram adicionadas a AlCl 3 solução supersaturada para formar uma suspensão. A suspensão resultante foi agitada por 10 min em um béquer de polipropileno e sonicada por 10 min para quebrar agregações de material de partida. O volume foi limitado a 70 mL (L / S =70–80). A mistura foi transferida para uma garrafa de Teflon (100 mL) e tratada sob pressão autogerada sem agitação a 373 K por 48 h. A autoclave foi resfriada naturalmente à temperatura ambiente, e os precipitados obtidos foram filtrados e lavados várias vezes com água desionizada e finalmente secos a 353 K em vácuo (denotado como La-HNT). Para comparação, HNT tratado com ácido sintetizado por 1,00 g de HNT foi dissolvido em 250 mL de solução de HCl 6 M a 373 K em banho-maria. A reação foi realizada em frasco cônico por 4 h com agitação constante. O balão cônico foi resfriado naturalmente à temperatura ambiente, e os precipitados obtidos foram filtrados e lavados várias vezes com água desionizada e finalmente secos a 353 K em vácuo (denotado como HNT tratado com ácido).
CdS / La-HNT foram sintetizados usando o método de Reação e Adsorção de Camada Iônica Sucessiva (SILAR), 3 mmol La-HNT foi dissolvido em 50 mL de Cd 0,5 M (NO 3 ) 2 solução de etanol por 5 min, enxaguada com etanol e, em seguida, dissolvida por mais 5 min em 50 mL de Na 2 0,5 M S solução de metanol e enxaguada novamente com metanol. Esse ciclo de imersão foi repetido várias vezes até que a deposição desejada de nanopartículas de CdS fosse alcançada. Em seguida, os precipitados obtidos foram filtrados e lavados várias vezes com água desionizada e, finalmente, secos a 353 K em vácuo (denominado CdS / D-Lax-HNT).
Caracterização
A análise de espectroscopia de fotoelétrons de raios-X (XPS) foi realizada usando um espectrômetro Thermo Fisher Scientific K-Alpha 1063 equipado com uma fonte de raios-X monocromática Al Ka. A pressão da câmara de teste foi mantida abaixo de 10 −9 mbar durante a aquisição espectral. A energia de ligação XPS (BE) foi internamente referenciada ao C 1 s pico (BE =284,1 eV). As fases cristalinas foram identificadas por análise de XRD usando um difratômetro de pó RIGAKU D / max-2550VB1 18-kW com radiação Cu Ka ( λ =1,5418 Å). Os dados foram coletados na faixa de varredura 2θ =10–80 °, com uma velocidade de varredura de 2 ° / min. Os espectros de FTIR foram registrados usando um espectrofotômetro Nicolet 5700. A área de superfície específica foi calculada a partir das isotermas de adsorção de nitrogênio usando a equação de Brunauer – Emmet – Teller (BET). Imagens de microscopia eletrônica de transmissão (TEM) foram obtidas usando um instrumento JEOL JEM-200CX equipado com uma espectroscopia de energia dispersiva de raios-X (EDS) a uma tensão de aceleração de 200 kV. O espectro (PL) da amostra foi detectado em um espectrômetro de fluorescência Hitachi H-4500 usando uma lâmpada Xe como fonte de luz. Os espectros de UV-vis de amostras em solução aquosa foram obtidos usando um espectrômetro UV-2400 (Shimadzu Corp., Japão). Estado sólido 29 Si e 27 Os espectros de RMN Al MAS foram registrados usando um espectrômetro Bruker AMX400 em um campo magnético estático de 9,4 T a uma frequência de ressonância de 79,49 MHz. A análise eletroquímica foi realizada em uma célula convencional de três eletrodos utilizando um fio preto de platina e um eletrodo de calomelano saturado (SCE) como contra-eletrodo e eletrodo de referência, respectivamente. O eletrodo de trabalho foi preparado em vidro condutor FTO (óxido de flúor e estanho). Em detalhe, 20 mg de amostra foram adicionados a 10 mL de etanol e formaram uma suspensão uniforme. Como em um processo padrão de spin-coating, a suspensão de etanol foi espalhada sobre o vidro FTO, cuja lateral foi previamente protegida com fita adesiva. A centrifugação foi realizada em alta velocidade de 150 rps e, em seguida, seca em estufa a 70 ° C por 1 h. As respostas de fotocorrente transitória de diferentes amostras foram medidas em 0,1 M Na 2 S + 0,02 M Na 2 SO 3 solução aquosa sob irradiação de luz visível (≥420 nm) a 0 V vs. SCE. A área iluminada do eletrodo de trabalho é de 2 cm 2 . O experimento fotoeletroquímico foi realizado usando uma estação de trabalho eletroquímica CHI-660A (ChenHua Instruments Co. Ltd., Xangai, China). A espectroscopia de impedância eletroquímica (EIS) foi medida com uma estação de trabalho eletroquímica CHI-660A (ChenHua Instruments Co. Ltd., Shanghai, China), e o eletrólito consistia em 0,01 mol / L de hexacianoferrato de potássio (III), 0,01 mol / L de hexacianoferrato de potássio (II) e 0,5 mol / L de KCl. O potencial aplicado foi o potencial de circuito aberto (OCP).
Reação fotocatalítica
As reações de separação de água foram realizadas em uma circulação fechada de gás dentro de um vácuo. Uma amostra de 100 mg de fotocatalisador em pó foi dispersa em uma solução aquosa de 300 mL de Na 2 0,1 M S e 0,1 M Na 2 SO 3 . A fonte de luz era uma lâmpada Xe de 300 W e a intensidade da luz atingindo a superfície da solução de reação era 135 mW / cm 2 . A quantidade de H 2 a evolução foi determinada usando um cromatógrafo de gás (Agilent Technologies:6890 N).
Detalhes computacionais
Todos os cálculos foram realizados com o código CASTEP, com base na teoria funcional da densidade de primeiro princípio (DFT). O potencial de aproximação da densidade local (LDA) foi usado para os cálculos. O formalismo de onda plana de pseudo-potencial ultrassoft e um corte de energia de 400 eV foram usados. A grade Monkhorst-Pack com 3 × 3 × 1 k A malha de pontos foi usada para o cálculo preciso dos resultados do DOS, enquanto o ponto Gama foi usado durante o relaxamento da geometria. A energia total autoconsistente no estado fundamental foi efetivamente obtida pelo esquema de mistura de densidade. Para otimizações de geometria, o limite de convergência para tolerância de campo autoconsistente (SCF) foi definido como 1,0 × 10 −6 eV / átomo, todas as forças sobre os átomos convergiram para menos de 0,03 eV / Å, o tensor de tensão total foi reduzido para a ordem de 0,05 GPa e o deslocamento iônico máximo estava dentro de 0,001 Å. Os parâmetros da célula e a coordenação atômica das estruturas foram otimizados usando um algoritmo de minimização Broyden – Fletcher – Goldfarb – Shanno (BFGS).
Resultados e discussão
A integridade da morfologia é importante para garantir o sucesso da dopagem porque o ácido pode danificar a estrutura da haloisita enquanto AlCl saturado 3 solução não. Imagens TEM de HNT e La-HNT são mostradas na Fig. 1. HNT mostra uma estrutura tubular de multicamadas 0,7-1,5 μm de comprimento, com um diâmetro externo de 50–75 nm e um diâmetro interno de 10–30 nm (Fig. 1a). Após a dopagem com La, a morfologia tubular típica foi mantida com o conteúdo de La de 4,2% (Fig. 1b). Para o HNT tratado com ácido, a morfologia tubular típica também foi mantida (arquivo adicional 1:Figura S1a), mas amorfa.
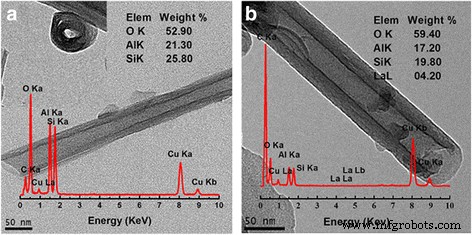
Imagens TEM de a HNT e b Amostras La-HNT
A estrutura do HNT pode ser influenciada pela dopagem devido ao maior tamanho do átomo de La usado para substituir o átomo de Al. Para La-HNT, os dados característicos da aloisita (cartão JCPDS nº 29-1487) podem ser observados na Fig. 2a e Arquivo adicional 1:Tabela S1, que indicam que a fase cristalina de La-HNT permaneceu. O ligeiro deslocamento do primeiro pico em La-HNTs é atribuído à substituição de átomos de Al por átomos de La de maior tamanho, o que confere o aumento do espaçamento (001) interlamelar. No entanto, há apenas um pico amplo centrado em 22 ° para HNT tratado com ácido (arquivo adicional 1:Figura S1b), o que indica que há sílica amorfa. Os espectros de FTIR de HNT e La-HNT são mostrados na Fig. 2b, e a atribuição relativa de cada pico vibracional está listada no arquivo adicional 1:Tabela S2. Para HNT, essas atribuições são baseadas nas literaturas anteriores [37,38,39,40]. Para La-HNT, a vibração de deformação O – H dos grupos Al – OH internos a 909 cm −1 e a vibração de deformação Al – OSi de folhas tetraédricas Al – O em 553 cm −1 mudar para 915 e 544 cm −1 , respectivamente. No entanto, a folha octaédrica de gibbsita de halloysita é completamente destruída e as bandas de alongamento Al – O desaparecem para o HNT tratado com ácido (Arquivo adicional 1:Figura S1c). Todas essas observações comprovam o sucesso do doping de La na estrutura do HNT e a mudança da estrutura do HNT influenciada pelo doping de La. O 27 Os espectros de RMN Al CP / MAS de amostras de HNT e La-HNT são apresentados na Fig. 2c. O sinal de ressonância em -3 ppm é atribuído a 6-coordenado Al. O sinal de ressonância a 64 ppm é atribuído ao Al coordenado em 4 mudando para 58 ppm após a dopagem de La, indicando que o ambiente do átomo de Al foi influenciado pela dopagem de La. No entanto, existem três picos em −111,32, −101,70 e −91,71 ppm no HNT tratado com ácido, identificado como Si (OSi) 4 , Si (OSi) 3 OH e Si (OSi) 2 (OH) 2 (Arquivo adicional 1:Figura S1d), respectivamente. As isotermas de sorção de nitrogênio de HNT e La-HNT são mostradas na Fig. 2d, e os dados relativos estão resumidos no Arquivo adicional 1:Tabela S3. A S APOSTA , o volume do poro e o diâmetro médio dos poros de La-HNT são 59 m 2 / g, 0,37 cm 3 / ge 25 nm, respectivamente. A S APOSTA e os valores de volume de poro de La-HNT são inferiores aos de HNT (82 m 2 / g, 0,41 cm 3 / g), enquanto seu diâmetro médio de poro (25 nm) é maior do que o de HNT (20 nm). No entanto, o S APOSTA valor e volume de poro para o HNT tratado com ácido são três vezes maiores do que o de HNT (arquivo adicional 1:Figura S1e). Todos esses resultados demonstram que o La doping influencia na estrutura do HNT, visto que o S BET para La-HNT é inferior ao de HNT, e há uma diminuição no volume total dos poros. A diminuição S BET e o volume do poro pode ser atribuído à parte das camadas de halloysite colapsadas, e o aumento do tamanho do poro pode ser associado com o átomo de Al sendo substituído pelo átomo de La, consistente com as análises de XRD e FTIR [18]. Portanto, especula-se que o La-HNT pode servir como um excelente suporte, alterando o desempenho químico e estrutural da aloisita e, portanto, pode contribuir para a atividade de catálise aprimorada para materiais nanocompósitos catalíticos à base de HNT.
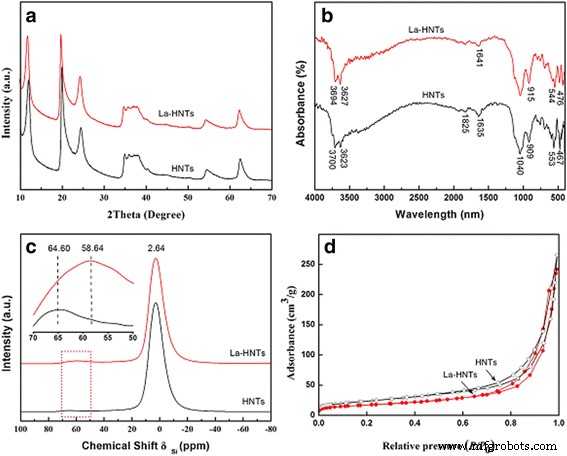
a Padrões de XRD, b Espectro FTIR, c 27 Espectro de Al NMR e d Isotermas de adsorção-dessorção de nitrogênio de amostras HNT e La-HNT
Para confirmar os efeitos da dopagem com La, nanopartículas de CdS foram depositadas na superfície de La-HNT e HNT. A Figura 3a-c, e mostra claramente que a superfície de HNT e La-HNT são bem cobertas por uma camada de nanopartículas de CdS contínua, densa e uniforme com uma espessura de cerca de 5 nm. No entanto, o elemento La não foi detectado na amostra CdS / La-HNT (inserção na Fig. 3e). O desaparecimento do elemento La nos CdS / La-HNTs pode ser atribuído ao abrigo da camada de nanopartículas de CdS, mais o elemento relevante de baixo La. A proporção de CdS em CdS / HNT para CdS / La-HNT é de 11% em peso. A Figura 3d, f mostra uma imagem HRTEM típica da camada de revestimento de nanopartículas de CdS na superfície do hospedeiro com um diâmetro de 5 nm, correspondendo ao tamanho de partícula de 5 nm calculado pela equação de Scherrer (arquivo adicional 1:Figura S2).
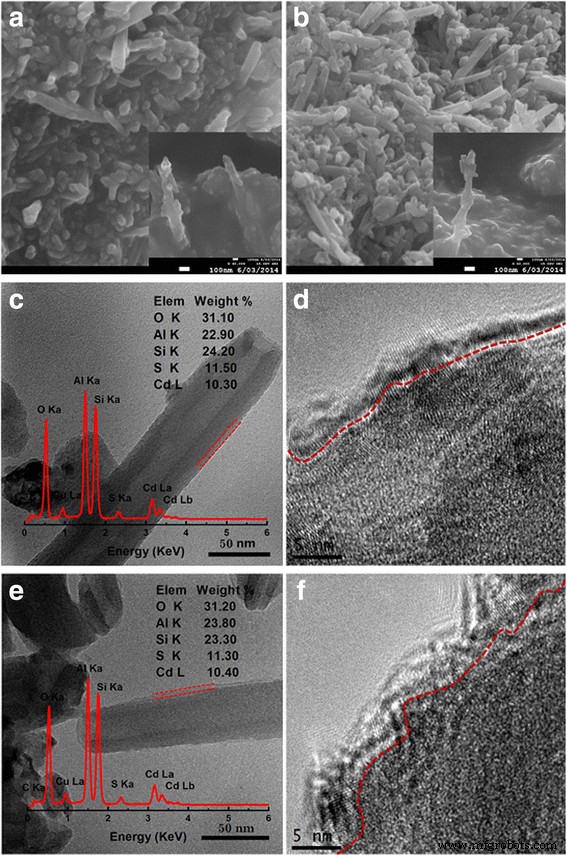
Imagens SEM e TEM de a , c , d CdS / HNT e b , e , f Amostras CdS / La-HNT
As propriedades ópticas dos compósitos HNT, La-HNT, CdS / HNT e CdS / La-HNT são caracterizadas por espectroscopia de refletância difusa de UV-vis (Fig. 4a). As bordas de absorção de CdS / HNT e CdS / La-HNT estão em 554 e 562 nm, respectivamente, e CdS / La-HNT mostra maior intensidade de absorção do que CdS / HNT na região de luz visível. Os compósitos La-HNT não apresentam absorção na região do UV, e as características de absorção são semelhantes às do HNT no aspecto de ampla absorção na região da luz visível. O obtido E g os valores são 2,31 e 2,25 eV para CdS / HNT e CdS / La-HNT, respectivamente. O desempenho catalítico de La-HNT para separação de água foi avaliado para revelar como o processo de dopagem e a alteração microestrutural correspondente afetam as propriedades macroscópicas. Fotocatalítico H 2 a evolução de CdS / HNT e CdS / La-HNT (Fig. 4b) foi conduzida em uma solução aquosa contendo SO 3 2− e S 2− íons como reagentes de sacrifício sob irradiação de luz solar simulada [41,42,43]. Os resultados mostram que o fotocatalítico H 2 taxa de CdS / La-HNT (47,5 μmol / h) é maior do que a de CdS / HNT (26,0 μmol / h) nas mesmas condições de reação (arquivo adicional 1:Tabela S4), e CdS / La-HNT e CdS / HNT mostra uma taxa de hidrogenação mais alta do que a maioria dos fotocatalisadores baseados em CdS relatados anteriormente da literatura [43-45]. Para descobrir se o H fotocatalítico superior 2 taxa deriva de La doping, as respostas de fotocorrente transitória de CdS / HNT e CdS / La-HNT foram medidas na Fig. 4c. Pode ser visto claramente que a fotocorrente aumenta para um valor alto rapidamente sob iluminação, e a fotocorrente diminui para quase zero quando a luz está desligada. Os resultados mostram que a intensidade da fotocorrente do CdS / La-HNT é maior do que a do CdS / HNT, indicando que a separação mais eficiente dos portadores de carga foi influenciada pelo dopagem com La.
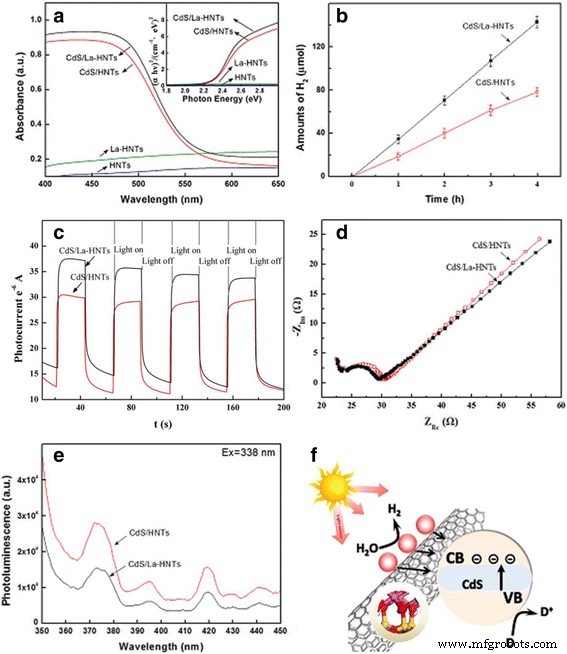
a Espectro UV-vis, b curva fotocatalítica de hidrogênio, c as respostas da fotocorrente transitória, d Gráficos de impedância de Nyquist, e Espectros PL e f esquema catalítico correspondente de amostras de CdS / HNT e CdS / La-HNT
A fim de examinar a transferência de carga e transporte de íons, a espectroscopia de impedância eletroquímica (EIS) foi empregada [2], e o comportamento da impedância de CdS / HNT e CdS / La-HNT foram medidos na Fig. 4d. Os gráficos de Nyquist mostraram um semicírculo, que ocorreu devido ao processo eletroquímico em um nível de alta frequência, seguido por uma linha que indica a resistência difusiva do eletrólito e dos materiais ativos. O semicírculo confinou a resistência de transferência de carga, que está intimamente relacionada com a reversibilidade das reações eletroquímicas. O CdS / La-HNT mostra um arco menor do que o do CdS / HNT, indicando que a dopagem com La levou a uma transferência de carga mais eficiente sobre o CdS / La-HNT.
O menor raio de semicírculo de CdS / La-HNTs em comparação com CdS / HNTs revelou que o nanocompósito de CdS / La-HNTs tem menor resistência à transferência de carga e boa resistência eletroquímica. Os efeitos da dopagem com La também são confirmados pelos espectros de emissão de fotoluminescência (PL) (Fig. 4e), quanto menor a intensidade de PL, maior a eficiência na separação elétron-buraco fotogerado.
Aqui, investigamos a estrutura da superfície de HNT para confirmar ainda mais o ambiente do átomo de Al influenciado pelo doping de La. A gama completa de espectros XPS de HNT e La-HNT são exibidos na Fig. 5a, e a concentração atômica relativa é mostrada no arquivo adicional 1:Tabela S5. Os elementos Si e Al são detectados em HNTs e La-HNTs, enquanto o elemento La é detectado apenas em La-HNT. A razão de concentração de Al / Si é de 0,62 em La-HNT, inferior à de HNT (0,88), o que pode ser devido ao átomo de Al sendo substituído pelo átomo de La. Para o HNT tratado com ácido, apenas Si 2 p e O 1 s são detectados devido à remoção da folha de alumina (arquivo adicional 1:Figura S1f). A Figura 5b mostra o La 3 d espectros, e suas posições de pico são observadas em 835,7 eV (La 3 d 5/2 ), 839,0 eV (La 3 d 5/2 ), 852,3 eV (La 3 d 3/2 ), e 855,9 eV (La 3 d 3/2 ), respectivamente. A Figura 5c, d mostra o Al 2 p e Si 2 p espectros e suas posições de pico são observados em 74,8 eV (Al – OH), 74,3 eV (Al – O), 103,3 eV (Si – OH) e 102,7 eV (Si – O), respectivamente. Notavelmente, os valores de energia de ligação (BE) do átomo de Al em Al – OH e Al – OSi mudaram para 75,1 e 74,6 eV, respectivamente, enquanto a posição do valor de BE dos átomos de Si não mudou. Assim, todos os resultados acima confirmam que o átomo de La substituiu parte do átomo de Al da folha de Al-O e o ambiente dos átomos de Al foi influenciado.
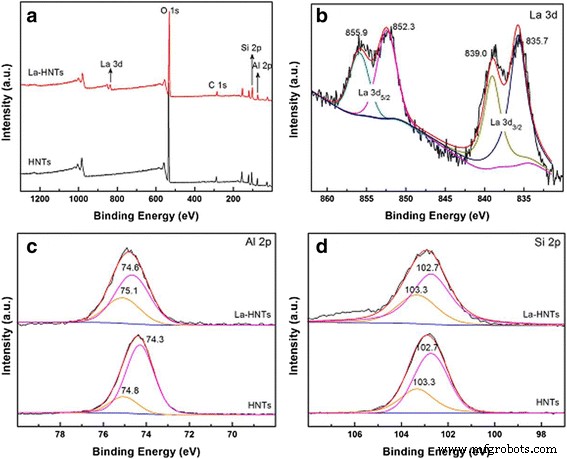
a gama completa, b La3d, c Al2p e d Espectros Si2p XPS de amostras HNT e La-HNT
Com base na caracterização da dopagem de La na estrutura HNT e a parte substituída do átomo de Al da folha de Al-O, um modelo de dopagem atômica substitucional foi proposto como segue (Fig. 6). Cada camada de HNT consiste em uma folha tetraédrica de Si e uma folha octaédrica de Al. A distância entre as células unitárias é difícil de mudar devido à forte força de acoplamento, de modo que as moléculas de água não podem entrar. Assim, a aloisita foi identificada como o mineral aluminossilicato de baixa atividade. No estágio inicial, o típico AlCl saturado 3 solução foi escolhida porque AlCl anidro 3 é um ácido de Lewis forte, capaz de formar adutos à base de ácido de Lewis com água, como AlO 2 2− , HCl e H 3 O + . A corrosão começa pelos adutos à base de ácido de Lewis interagindo com a alumina na estrutura da aloisita, e a extensão da reação aumenta com a concentração de Al 3+ aumentando. Como a concentração de Al 3+ já está supersaturada, formar-se-á uma camada de inibição, próxima à superfície da aloisita. Nessa situação, pode ocorrer substituição catiônica na camada de inibição. The La 3+ íons seguindo Al 3+ solução saturada são substituídos com os átomos de alumínio solúvel de halloysite na camada de inibição de acordo com o princípio da concentração de conservação de solução saturada de íons. Em seguida, o equilíbrio dinâmico de dopagem atômica substitucional formada e compósitos de halloysita dopados com La são alcançados. O uso de autoclave no processo foi para forçar o processo de dopagem, pois o raio de La 3+ íon é maior do que Al 3+ . As formas de cristal e estruturas de superfície podem ser obviamente alteradas por dopagem, e o desempenho químico e estrutural do suporte seria melhorado, o que traz uniformidade contínua ao carregamento de nanopartículas e melhora a atividade de catálise para materiais nanocompósitos catalíticos.
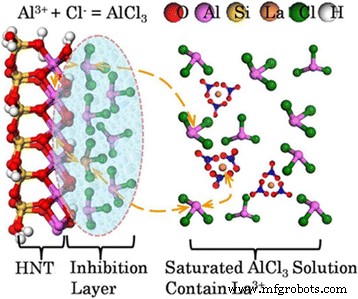
Mecanismo proposto de La doping em HNT
Os cálculos da teoria funcional da densidade de primeiro princípio (DFT) foram realizados para investigar a racionalidade do mecanismo de dopagem e o efeito do doping de La. O modelo de estrutura do HNT é simulado usando aproximações cristalinas, e o La-HNT é construído substituindo o átomo de Al da halloysita pelo átomo de La. A estrutura de HNT usando a estrutura de caulinita é simulada (Fig. 7a, b), e as estruturas de superfície são construídas pela clivagem de uma estrutura de camada 2 × 1 de duas espessuras de camada de Al – O – Si do volume da halloysite. Um espaço de vácuo de 15 Å é usado. O La-HNT é construído substituindo um Al na folha de Al do halloysite por um átomo de La ou adicionando La (OH) 3 na superfície do halloysite (Fig. 7c, d). Foi descoberto que as ligações Al – O (Al s –O) e ligações Si – O perpendiculares à camada plana (Si ps –O) na superfície HNT são ligeiramente aumentados em comparação com a da estrutura em massa de HNT (Arquivo adicional 1:Figura S3), ou seja, 0,05–0,10 e 0,02–0,03 Å, respectivamente. Ao mesmo tempo, as ligações Si – O na camada plana (Si é –O) diminuiu. Além disso, a distribuição da ligação O – H na superfície HNT é ampliada devido ao efeito de superfície. Para o caso com dopagem, uma contração do Al s –O e Si ps –O ligações, bem como uma expansão do Si é A ligação –O ocorre após o relaxamento da estrutura atômica da superfície La-HNT (Arquivo adicional 1:Figura S3). A estrutura local em torno de La mostra que as seis ligações La – O possuem um comprimento de ligação (cerca de 2,3–2,5 Å) muito mais longo do que ligações Al – O, o que aumenta o espaço ao redor do local de dopagem La (Arquivo adicional 1:Figura S4a). Notavelmente, o alongamento de três ligações OH superficiais com H indo diretamente para os átomos O de La (OH) 3 (H La ) induz três grupos OH de superfície reativa em torno do átomo de La na superfície de La-HNT.
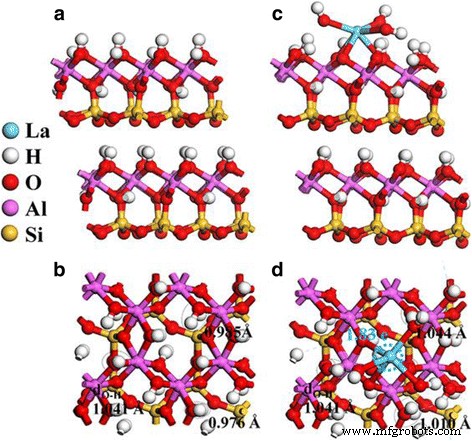
Estrutura geométrica de a vista lateral e b vista superior de HNT e c vista lateral e d vista superior de La-HNT
A carga de Mulliken calculada para o átomo de La em La-HNT é 1,83 e (Fig. 7d), que corresponde aos estados de valância +3. O resultado do PDOS mostra uma lacuna de banda de 5,2 eV para HNT primitivo, e a banda de valência perto do nível de fermi é composta principalmente por O 2 p estado enquanto a banda de condução mínima (CBM) é misturada principalmente por H 1 s , Si 3 s 3 p , e parcialmente O 2 p , Al 3 s Estados 3p (arquivo adicional 1:Figura S4b). O suporte de La na superfície HNT introduz La 5 d estados no CBM (Fig. 8a, roxo), e o reativo La dopant com 5 d z 2 orbitais é confirmado como uma impureza do tipo doador. Enquanto isso, os três grupos OH em torno de La forneceram alguns pares de elétrons solitários (Fig. 8a, amarelo e verde) na banda de valência máxima (VBM), o que aumentará a capacidade de absorção da superfície. A diferença de densidade de carga em torno da interface La-HNT mostra que há uma transferência de carga dos átomos de Al circundantes da superfície HNT para os dopantes La após a dopagem La (Fig. 8b). Supõe-se que os La dopantes podem servir como uma ponte de transferência de carga entre a superfície HNT e nanopartículas funcionais como o CdS e, portanto, a taxa de evolução de hidrogênio fotocatalítico seria aumentada. Assim, a conformidade da experimentação e simulação verificou a racionalidade do modelo de simulação e do modelo de dopagem atômica substitucional.
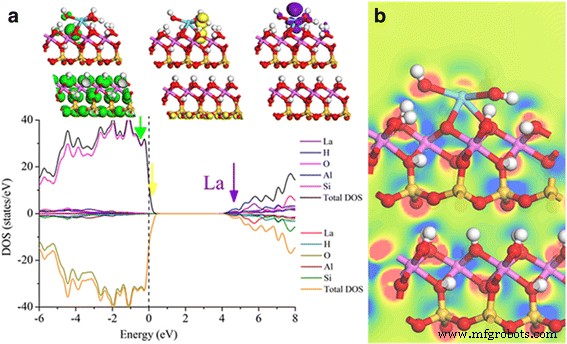
a Os resultados PDOS da superfície La-HNT. b Diferença de densidade de carga da interface La-HNT traçada ao longo do plano designado pelas linhas pontilhadas mostrado no painel inferior da Fig. 7c. Azul corresponde ao esgotamento da carga e vermelho para cobrar ganho. As isosuperfícies são mostradas no intervalo [−0,08, 0,08] (e / Å 3 ) Contornos de densidade de carga constante são separados por 0,005 eV / Å 3
Conclusões
Em resumo, os nanotubos de halloysite naturais foram dopados com sucesso pelo átomo de La. A dopagem de La na estrutura do HNT leva a formas de cristal e mudanças óbvias na estrutura da superfície, o que traz uniformidade contínua para o carregamento de CdS e altera a atividade de catálise para materiais compósitos nano-catalíticos, resultando em uma taxa de evolução de hidrogênio fotocatalítico aprimorada. O contraste da evolução fotocatalítica do hidrogênio de CdS / La-HNT e CdS / HNT confirma a alta eficiência da dopagem de La. Este resultado é muito encorajador e deve ser altamente aplicável para estender a técnica de dopagem a outros minerais de aluminossilicato e o design correspondente de materiais funcionais.
Nanomateriais
- Monitoramento de desempenho que funciona tanto para operações de TI quanto para proprietários de aplicativos
- Tornando o desempenho do aplicativo melhor para usuários e clientes da CyrusOne
- Requisitos para um bom desempenho do link de comunicação:Modulação e Demodulação IQ
- Nanofibras e filamentos para entrega aprimorada de drogas
- HDPE representa uma mudança de etapa no desempenho de garrafas e recipientes moldados por sopro
- Nanopartículas para terapia do câncer:progresso e desafios atuais
- Engenharia de processo de revestimento por imersão e otimização de desempenho para dispositivos eletrocrômicos de três estados
- Síntese e propriedades eletroquímicas de materiais catódicos de LiNi0,5Mn1,5O4 com dopagem composta Cr3 + e F− para baterias de íon-lítio
- Preparação de micrromateriais híbridos MnO2 revestidos com PPy e seu desempenho cíclico aprimorado como ânodo para baterias de íon-lítio
- O Caso para Divisão de Estoque, por Marcas Grandes e Pequenas



