Caracterização estrutural da cadeia auto-montada como a nanoestrutura do casco do Fe-FeOx Core
Resumo
Um dos grandes desafios de estudar as nanoestruturas de ferro da camada central é saber a natureza da camada de óxido, ou seja, se é γ-Fe 2 O 3 (Maghemite), Fe 3 O 4 (Magnetita), α -Fe 2 O 3 (Hematita) ou FeO (Wustita). Ao conhecer a natureza da camada de óxido de ferro com núcleo de ferro zero valente, pode-se determinar o comportamento químico ou físico das nanoestruturas núcleo-camada. Nanochains núcleo-casca de Fe (NCs) foram preparados através da redução de Fe 3+ íons por boro-hidreto de sódio em solução aquosa em atmosfera ambiente, e Fe NCs foram posteriormente envelhecidos em água por até 240 min. XRD foi usado para estudar a estrutura de Fe NCs. Uma análise mais aprofundada da natureza do núcleo-casca de Fe NCs foi feita por TEM, os resultados mostraram aumento na espessura da casca de óxido (de 2,5, 4, 6 a 10 nm) conforme o tempo de envelhecimento da água aumenta (de 0 min, 120 min, 240 min a 360 min). A espectroscopia Raman foi empregada para estudar a natureza do óxido de Fe NCs. Para confirmar ainda mais a fase de magnetita em Fe NCs, a espectroscopia Mössbauer foi realizada em Fe NCs-0 e Fe NCs-6. O resultado mostra a presença de magnetita na amostra antes do envelhecimento em água, e a amostra após envelhecimento prolongado contém a fase de hematita pura . Isso mostra que a oxidação prolongada da água transforma a estrutura da casca de Fe NCs de uma mistura de hematita e magnetita em uma casca de hematita pura. As propriedades magnéticas dos Fe NCs foram medidas por VSM a 320 K. Por causa dos altos valores de magnetização de saturação (Ms), Fe NCs podem ser usados como r 2 agentes de contraste para imagem por ressonância magnética (MRI) em um futuro próximo.
Introdução
Nanofios magnéticos (NWs) sintetizados através de métodos de template ou montagem têm grandes momentos magnéticos e anisotropia de forma, como mostrado na Fig. 1. Trabalhos anteriores afirmam que estruturas semelhantes a cadeias com altas relações de aspecto são mais eficientes em aplicações biomédicas, especialmente para separação magnética, hipertermia magnética (MH) e MRI do que nanopartículas [1, 2]. Para MH 1-D, NWs magnéticos podem fornecer áreas reativas de fricção maiores do que nanopartículas de dimensão zero (0-D). Isso permite que NWs magnéticos unidimensionais (1-D) tenham uma melhor eficiência de aquecimento, o que reduz o tempo de tratamento dos pacientes com câncer. Park et al. [3] relataram que nanoworms 1-D mostram capacidade superior de direcionamento de tumor in vivo do que nanoesferas com o diâmetro semelhante. Jeotikanta et al. preparado [4] Fe 3 O 4 nanobastões (NRs) pela hidrólise de FeCl 3 solução aquosa e funcionalizada com polietilenoimina para agente de contraste MRI. Eles descobriram que o r 2 relaxividade de NRs é maior do que nanopartículas usando igual volume de material. Os óxidos de ferro NWs superam NPs semelhantes durante o teste de R 2 relaxitivities [5]. O R calculado 2 valor para NWs é 116 mM −1 s −1 que é maior do que NPs (70 mM −1 s −1 ) O autor conclui que a natureza alongada e a maior magnetização de saturação dos NWs resultam em contraste MR melhorado [5].
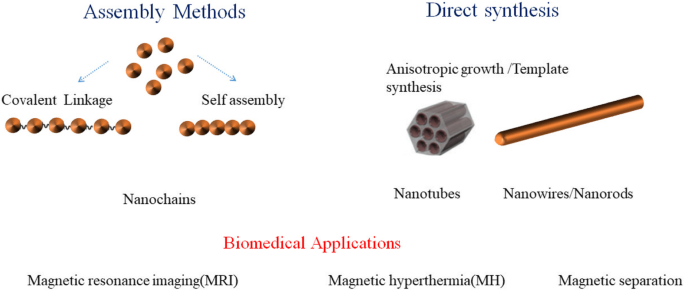
Nanofios magnéticos anisotrópicos de alta forma preparados através de síntese direta ou métodos de montagem e suas aplicações biomédicas
Apesar do fato de que as propriedades estruturais gerais das nanoestruturas de ferro núcleo-casca sejam bem estudadas, a estrutura exata e a fase das camadas de óxido são difíceis de determinar. A composição e fase da camada de óxido formada em um núcleo de ferro depende da distância do núcleo de Fe interno às camadas de óxido externas, ou seja, geralmente uma progressão de Fe zero valente → FeO → Fe 3 O 4 → Fe 2 O 3 ocorre [6]. Embora, para a oxidação à temperatura ambiente, uma camada de óxido muito fina foi formada que era difícil de diferenciar a variação espacial das conchas de óxido. Para oxidação à temperatura ambiente usando EELS em caracterizações TEM, alguns autores afirmam que a casca de óxido de ferro é feita de γ -Fe 2 O 3 ou Fe 3 O 4 [7, 8] ou que FeO foi inicialmente formado e após o aquecimento a casca de FeO foi transformada em γ -Fe 2 O 3 ou Fe 3 O 4 shell [9]. No entanto γ -Fe 2 O 3 e Fe 3 O 4 são fases metaestáveis do ferro e podem se transformar em α -Fe 2 O 3 após oxidação a alta temperatura até 500 ° C [10]. Além disso, o procedimento de oxidação do núcleo de ferro zero-valente é fortemente influenciado pela solução aquosa oxigenada e a oxidação ocorre em um H 2 Interface O e óxido [11]. À medida que ocorre a transferência de íons de ferro do núcleo de ferro zero valente para a camada de óxido, ocorre a formação de uma nova fase de óxido. Oxidação semelhante também foi encontrada em [12] com a presença de oxigênio.
O objetivo desta pesquisa foi estudar a estrutura de Fe NCs recém-preparados sintetizados pela redução da solução de cloreto de Ferro (III) pela adição de solução de borohidreto de sódio. Estudo mostra que a espessura da casca e o diâmetro do núcleo magnético dos Fe NCs são ajustáveis. XRD, FE-SEM e TEM foram usados para estudar a estrutura e a natureza do núcleo-casca de Fe-NCs. Além disso, a espectroscopia Raman com laser verde (comprimento de onda de excitação 532 nm) e laser He-Ne (comprimento de onda de excitação 633 nm) foi empregada para estudar a natureza do óxido de Fe-NCs. Os resultados foram ainda confirmados por espectroscopia Mössbauer em FeNCs-0 e FeNCs-6 a 320 K. A fim de estudar o efeito de magnetização em Fe-NCs, para futuras possíveis aplicações biomédicas , as propriedades magnéticas em Fe NCs-0, Fe NCs-2, Fe NCs-4 e Fe NCs-6 foram medidas por VSM em temperatura ambiente. Depois de examinar os valores de magnetização de saturação de Fe NCs, é possível sugerir que Fe NCs podem ser usados como r 2 agentes de contraste para imagem por ressonância magnética (MRI) em um futuro próximo.
Métodos
Químicos
Hexa-hidrato de cloreto férrico (FeCl 3 .6H 2 O) (99% puro) e boro-hidreto de sódio (NaBH 4 ) (98% puro) foram adquiridos da National Medicines Corporation Ltd. (China). Gás argônio altamente puro (99,9%) foi adquirido da empresa de gás Hubei Minghui (China).
Síntese de Core-Shell Fe NCs
Para a síntese de NCs de Fe de núcleo-casca, 3 g de hexahidrato de cloreto férrico (FeCl 3 .6H 2 O) foi dissolvido em 1000 ml de água desionizada (DI) para formar uma solução de cloreto de Ferro (III). Boro-hidreto de sódio (NaBH 4 ) solução foi formada adicionando 6 g de NaBH 4 adicionado a 400 mL de água DI [13]. A adição de NaBH 4 solução foi feita na taxa de 1,5 mL / s em solução férrica sem agitação e deixou a solução por 0 min, 120 min, 240 min e 360 min. Precipitados pretos foram formados, coletados da solução e lavados com água DI e etanol e secos sob gás argônio (Ar) para caracterizações. Os Fe NCs foram formados pela redução da solução de cloreto de Ferro (III) pela adição de solução de borohidreto de sódio, o que é feito seguindo a reação [13],
$$ 3B {H} _4 ^ {-} + 3 {H} _2O + Fe {\ left ({H} _2O \ right)} _ 6 ^ 3 =Fe + 3B {(OH)} _ 3 + 1/2 {H} _2 $$
Pela adição do NaBH 4 solução na solução férrica núcleos de ferro são formados sob H 2 proteção. Pela automontagem de núcleos de ferro devido à alta interação magnética entre eles, nanoestruturas semelhantes a cadeias foram formadas. A Figura 2 mostra a síntese e formação de Fe NCs core-shell preparados por meio de reação de redução.
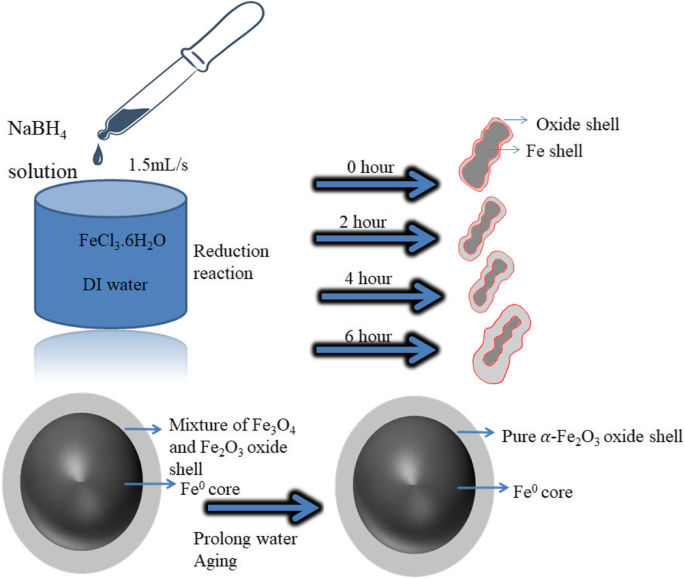
Ilustração esquemática da síntese e formação de Fe NCs de núcleo-casca
Caracterizações
Os NWs de Fe de núcleo-casca foram examinados usando microscopia eletrônica de varredura por emissão de campo (FE-SEM, NOVA 400 Nano) com espectroscopia de raios-X de dispersão de energia (EDX, Le350 PentaFETx – 3). Para observações FE-SEM, os Fe NWs foram pulverizados com uma fina camada de ouro por 100 segundos. A difração de raios-X (XRD, X’Pert PRO MRD, PANalytical, Holanda) foi feita com Cu-K α radiação, espectrômetro Raman (laboratório RAM HR JY-Evaluation) com comprimento de onda de excitação de 532 nm (com potência de 60 mW e potência do laser de 6 mW) e com laser He-Ne (com laser de 0,1, 0,6, 1 e 3 mW potência). A microscopia eletrônica de transmissão (TEM) foi realizada em um microscópio eletrônico Tecnai G2 F30 S-TWIN operando a 300 kV. Para observações de TEM, as amostras foram preparadas dispersando os pós em etanol absoluto por ultrassom. As medições magnéticas foram realizadas usando um magnetômetro de amostra vibratória (VSM, Lake Shore 7307). As curvas de magnetização M / Ms Vs H (KOe) foram medidas sob um campo magnético de até 20 KOe. A espectroscopia Mössbauer foi realizada usando fonte de raio 57Co /:Rhc (14,4 KeV) montada em uma unidade eletromagnética com sinais de velocidade triangular a 320 K. Os espectros eram mínimos quadrados ajustados para obter os parâmetros hiperfinos.
Resultados e discussão
FE-SEM
A Figura 3a-d mostra imagens FESEM de Fe NCs-0, Fe NCs-2, Fe NCs-4 e Fe NCs-6, através da reação de redução de tri-cloreto de ferro por borohidreto de sódio a 0, 120 , 240 e 360 min. Pode-se ver na Fig. 3a-d que a nanoestrutura de Fe obtida aparece como uma cadeia de nanopartículas de Fe ligadas entre si. Além disso, cada uma das nanopartículas de Fe é separada da outra por uma interface de óxido fina, que é uma característica específica do método de síntese aplicado utilizado neste estudo. A Figura 3e mostra a composição de Fe NCs-2 medida usando EDX. O pico de ferro (Fe) com pico de oxigênio (O) aparece como ombro para pico de Fe que é observado, além do pico de carbono (C) foi observado devido à fita de carbono que foi usada como substrato durante a caracterização do FESEM e picos de ouro (Au) vêm da pulverização catódica da amostra com ouro para fins de condução. A inserção da Fig. 3e mostra a porcentagem atômica de Fe e O em Fe NCs-2 (At% =O, 22,35%; Fe, 77,65%).

a - e Imagem FE-SEM de ( a ) FeNCs – 0, ( b ) FeNCs – 2, ( c ) FeNCs – 4, ( d ) FeNCs – 6, ( e ) Padrão de EDX de Fe NCs – 2, a tabela de inserção mostra a porcentagem atômica e em peso do elemento de ferro e oxigênio
XRD
A Figura 4a-d mostra os padrões de raios-X de Fe NCs-0, Fe NCs-2, Fe NCs-4 e Fe NCs-6. O pico dominante encontra-se em 2 θ =44,9 ° pode ser inequivocamente atribuído a bcc Fe de acordo com o arquivo JCDP nº 6-696 com a =0,2866A ° . XRD é a técnica mais comumente usada para a confirmação da natureza amorfa do óxido de ferro [14, 15]. Uma linha plana mostra a falta de periodicidade na rede cristalina. Portanto, a ausência de picos de difração de Braggs pode ser o marcador de identificação da natureza amorfa do Fe 2 O 3 [15] e sua distinção de polimorfos (hametita e maghemita) Fe 2 O 3 . Além disso, foi visto na figura de XRD que o pico característico de Fe BCC em 44,9 ° tem uma mudança muito leve em direção ao ângulo inferior com o aumento do conteúdo de oxigênio em Fe NCs. Este fenômeno pode ser observado devido à diferença de raios iônicos entre o elemento principal (Fe) e o íon dopante (O) [16], o que indica que átomos de O foram produzidos com sucesso na superfície dos Fe NCs. Como o pico do óxido não aparece na difração de raios-X, os resultados foram posteriormente confirmados por TEM, espectroscopia Raman e espectroscopia Mössbauer.
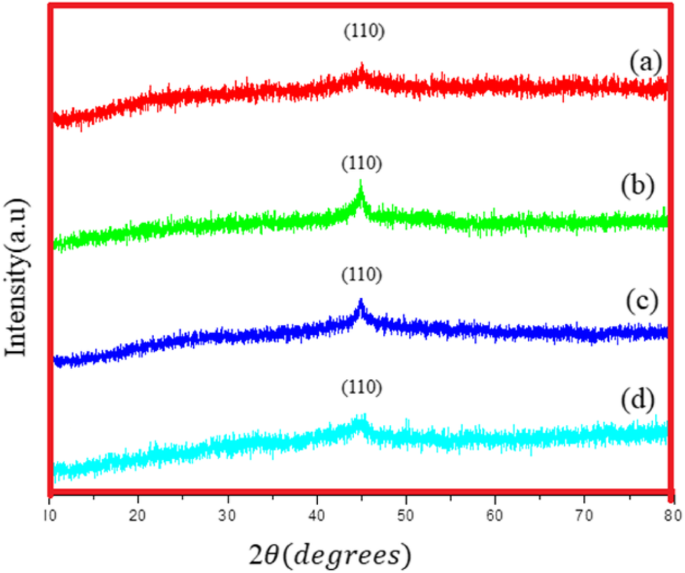
Padrão de XRD de (a) Fe NCs-0, (b) Fe NCs-2, (c) Fe NCs-4 e (d) Fe NCs-6
TEM
O resultado foi posteriormente confirmado pelo TEM. A Figura 5a-d mostra o TEM de Fe NCs-0, Fe NCs-2, Fe NCs-4, Fe NCs-6. Notavelmente, o contraste entre o centro escuro e a borda cinza foi visto claramente, sugerindo a estrutura núcleo-concha dos NCs. Como está claro na Fig. 5a, o invólucro de Fe NCs-0 era de cerca de 2,5 nm, conforme a oxidação na água aumenta de 0 a 120 min, o invólucro aumentou em espessura para 4 nm (Fig. 5b), aumentando ainda mais o tempo de reação até 240 min a espessura do óxido da casca foi aumentada para 6 nm (Fig. 5c), finalmente o envelhecimento em água por 360 min a casca do óxido foi aumentada para 10 nm (Fig. 5 d). Como fica claro a partir da observação do TEM, há um aumento gradual na espessura da casca de 2,5, 4, 6 a 10 nm. Pode-se concluir que mais tempo de envelhecimento em água resulta em uma camada de óxido mais espessa devido à reação do ferro zero valente com O 2 / H 2 O na solução. O aumento da espessura da casca também foi observado por Xue et al. pela preparação do nanocompósito core-shell, sintetizado através do método de refluxo fácil [17, 18].
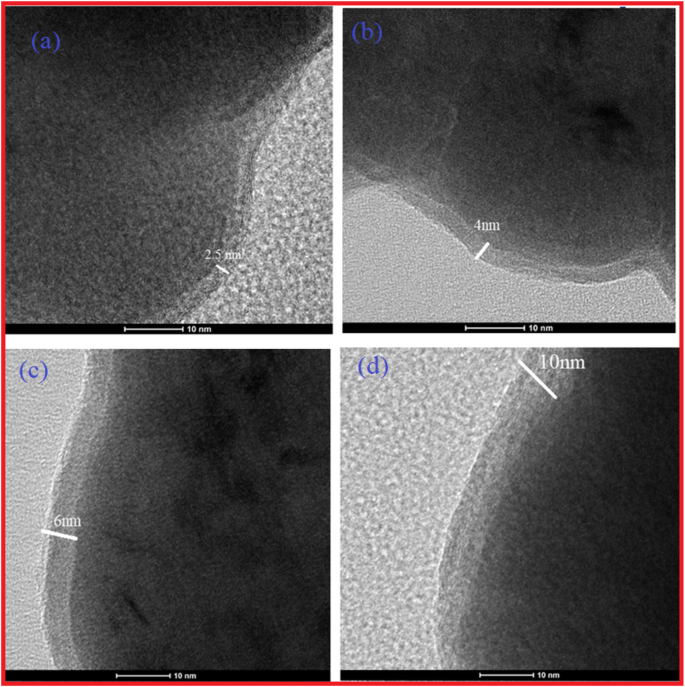
Imagem TEM de a Fe NCs-0, b Fe NCs-2, c Fe NCs-4 e d Fe NCs- (6) mostrando a natureza core-shell de Fe NCs com um aumento na espessura do óxido de 2,5 nm, 4 nm, 6 nm e 10 nm
Espectroscopia Raman
A espectroscopia Raman é uma técnica analítica que tem sido usada para estudar a estrutura dos óxidos de ferro por muitos anos [19,20,21,22,23]. Ele fornece uma avaliação clara da fase de óxido e pode medir a cristalinidade da amostra em estudo, observando os modos de fônon. A espectroscopia vibracional Raman é uma ótima ferramenta para caracterizar os pós ou filmes de óxido, visto que estudos anteriores mostram que os polimorfos de óxido de ferro (hematita, maghemita e magnetita) apresentam sinais Raman distintos [20, 24, 25]. A Figura 6 mostra espectros Raman coletados de Fe NCs na potência do laser de 60 mW, medido com laser verde (532 nm). Os picos apareceram em 217 cm −1 (A 1g ), 275 cm −1 (E g ), e 386 cm −1 (E g ), e uma grande protuberância foi observada entre 1200 e 1300 cm −1 , corresponde à fase de hematita com picos deslocados para números de onda mais baixos (conforme os dados anteriores coletados na Tabela 1). Esta mudança de pico pode corresponder à oxidação do laser; a alta temperatura induzida pela potência do laser focado pode resultar na mudança de fase do material, o que também é observado pelo grupo de estudos de Mendili et al. [29,30,31]. Para confirmar ainda mais a natureza do óxido de Fe NCs, espectros Raman foram feitos em potências de laser mais baixas (6 mW) usando laser verde (532 nm) e laser He-Ne (633 nm). A Figura 7a mostra picos (laser verde) no comprimento de onda de 214 cm −1 (A 1g ), 278 cm −1 (E g ), 394 cm −1 (E g ), 490 cm −1 (A 1g ), 597 cm −1 (E g ), e 1290 cm −1 . Como está claro a partir dos dados Raman coletados na Tabela 1, esses picos podem corresponder aos picos de hematita com o número de onda deslocado em direção aos números de onda inferiores. Então, o laser He-Ne (Fig. 7b) foi usado com potência do laser de 6 mW. Os picos no número de onda 224 cm −1 (A 1g ), 287 cm −1 (E g ) e 484 cm −1 (A 1g ), e 1306 cm −1 corresponde à fase de hematita pura [10, 24, 32]. Conhecendo a relação \ ({P} _ {\ mathrm {scattered}} \ propto \ frac {I_0} {\ lambda ^ 4} \) (onde P disperso é o tempo de espalhamento Raman e λ é o comprimento de onda do laser), o tempo de varredura para o laser He-Ne é maior do que o laser verde, o que fornece melhores resultados para os NCs de Fe núcleo-casca sintetizados por meio de reação de redução. Conforme claro na Fig. 7b, um pico fraco apareceu em 660 cm −1 para Fe NCs-0 e Fe NCs-2. Este pico foi visto por outros grupos em espectros Raman de hematita e pode ser a presença de contaminação de magnetita [24, 33]. Para confirmar ainda mais a fase de magnetita em Fe NCs, os espectros Raman foram coletados com potências de laser mais baixas (0,1 mW, 0,6 mW, 1 mW e 2 mW) usando laser He-Ne (os resultados são fornecidos no arquivo adicional 1). Nenhum sinal Raman foi visto, apenas uma linha plana foi observada em baixas potências do laser. Os espectros Raman foram coletados a 3 mW usando laser He-Ne como mostrado na Fig. 8. Um forte pico de magnetita aparece claramente em 670 cm −1 (A 1g ) para Fe NCs-0 com picos de hematita em 224 cm −1 (A 1g ), 287 cm −1 (E g ) 406 cm −1 (E g ), 500 cm −1 (A 1g ), e 1310 cm −1 (E g ) números de onda. O pico de magnetita muda para baixo número de onda com menores intensidades para Fe NCs-2 e desaparece para Fe NCs-4 e Fe NCs-6. A partir da espectroscopia Raman, pode-se supor que a camada de Fe NCs-4 e Fe NCs-6 correspondem à fase de hematita pura.
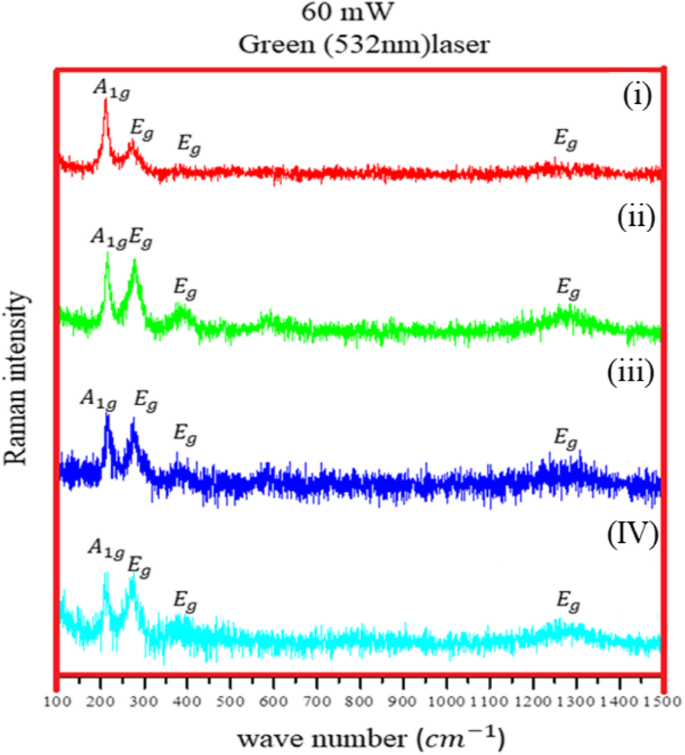
Espectros Raman de (i) FeNCs-0, (ii) FeNCs-2, (iii) FeNCs-4, (IV) FeNCs-6 com potência do laser de 60 mW com laser verde
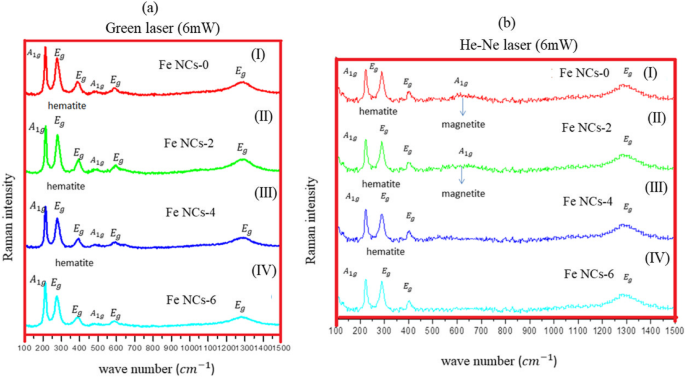
Espectros Raman de a Fe NCs-0 (I), Fe NCs-2 (II), Fe NCs-4 (III) e Fe NCs-6 (IV) coletados a 6 mW de potência do laser com laser verde e b Fe NCs-0 (I), Fe NCs-2 (II), Fe NCs-4 (III) e Fe NCs-6 (IV) coletados na potência do laser de 6 mW com laser He-Ne
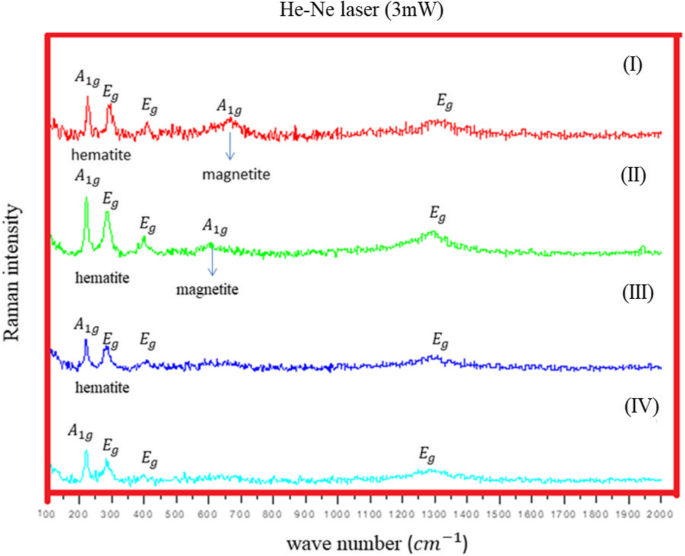
Espectros Raman de Fe NCs-0 (I), Fe NCs-2 (II), Fe NCs-4 (III), Fe NCs-6 (IV) a 3 mW de potência do laser com laser He-Ne
Espectro Mössbauer
A fim de confirmar a fase de magnetita em Fe NCs, a espectroscopia Mössbauer foi realizada em Fe NCs-0 e Fe NCs-6. Os espectros Mössbauer para Fe NCs-0 são obtidos a 320 K e são mostrados na Fig. 9. Os espectros Mössbauer para Fe NCs-6 são obtidos a 320 K e são mostrados na Fig. 10. Espectros de seis linhas bem resolvidos são observados em ambos os espectros. Os valores dos deslocamentos do isômero ( δ ), divisão de quadrupolo ( Q ), campo hiperfino ( H ), as larguras das linhas e a população do local são deduzidas dos dados de Mössbauer. Os melhores ajustes aos dados experimentais foram obtidos com um dubleto de quadrupolo e quatro sextetos de Zeeman. O deslocamento do isômero fornece informações sobre a distribuição de carga do elétron. Um dupleto com deslocamentos de isômero ( δ ) 0,24 mm / se divisão quadrupolo ( Q ) 0,94 mm / s, em Fe NCs-0, e em Fe NCs-6 com δ 0,21 mm / se Q 1,11 mm / s atribuídos a Fe super paramagnético +3 estado, também visto por outros pesquisadores enquanto estudavam Fe 2 O 3 nanopartículas [34,35,36,37]. Os sextetos especificam estados de spin magnético em Fe NCs. O δ valores de 0,7 a 1,4 mm / s são atribuídos a Fe +2 e valores de 0,1 a 0,6 mm / s indicando ferro em Fe +3 estado [38,39,40,41]. δ os valores dados na Tabela 2 para sexteto 2 são 0,10 mm / se para Q são - 0,04 mm / s, o que mostra que o estado de valência do ferro é +3. Valores semelhantes também são observados por Joos et al. [42] para Fe 3 O 4 nanopartículas; eles atribuíram esses valores ao tetraédrico Fe +3 . δ os valores para Fe NCs-6 dados na Tabela 3 para sexteto 3 e 4 são 0,15 mm / se 0,20 mm / s mostram Fe +3 em Fe 2 O 3 . Xie et al. [43] atribuiu valores semelhantes para Fe 2 maior O 3 nanopartículas. Pôde-se deduzir dos dados de Mössbauer que há uma pequena contaminação de magnetita que está presente em Fe NCs-0 e Fe NCs-6 e corresponde à camada de hematita pura. Korecki e Gradmann [44] fizeram espectroscopia Mössbauer em filmes de Fe (110), os valores de deslocamento do isômero obtidos são 0,02 mm / s, 0,04 mm / s e 0,07 mm / s. Esses valores corresponderam bem aos valores de Fe bcc dados na Tabela 2 e na Tabela 3 para Fe NCs-0 e Fe NCs-6. Espera-se que a concentração de Fe nos Fe NCs diminua à medida que a camada de óxido aumenta de 2,5 para 10 nm. A população local de Fe diminui e a população local de hematita aumenta significativamente em Fe NCs-6. A divisão quadrupolar e as larguras das linhas também mudam com o aumento da espessura da casca de Fe NCs-0 para Fe NCs-6.
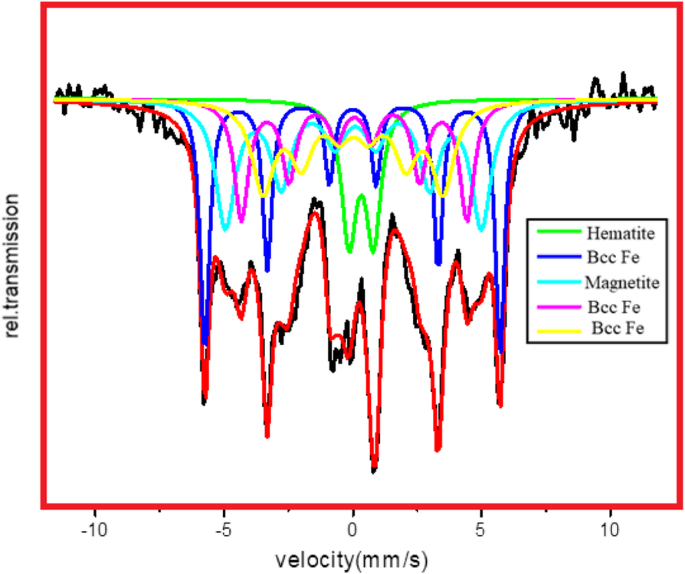
Espectros Mössbauer de Fe NCs-0 a 320 K
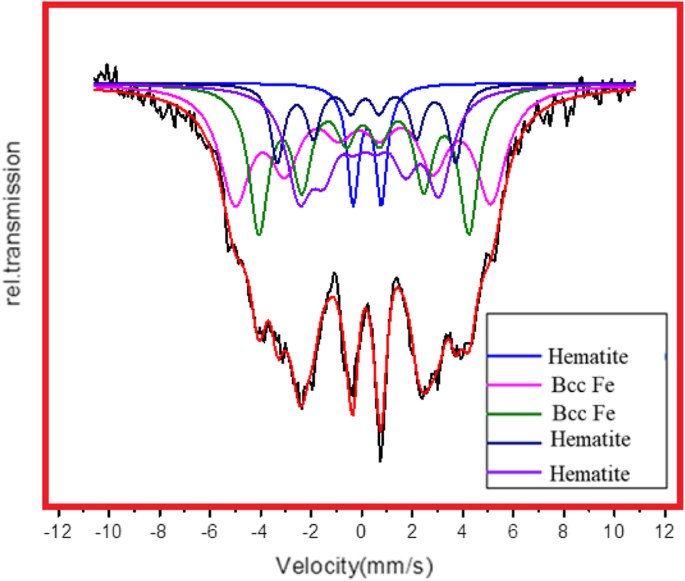
Espectros Mössbauer de Fe NCs-6 a 320 K
A ilustração esquemática (Esquema 1) descreve o mecanismo para a formação de Fe NCs core-shell explicado por O 2 rota de ativação por oxidação de Fe NCs em água. Esquema 1a mostra que quando Fe zero valente foi exposto a H 2 O e O 2 a camada de óxido de ferro foi produzida na superfície do Fe NC. Conforme o tempo de reação na água aumenta de 0 a 360 min, o crescimento da camada de óxido aumenta e o núcleo de Fe diminui. A oxidação do núcleo de Fe ocorre devido à transferência de elétrons do núcleo de Fe para a camada de óxido de ferro através da banda de condução. A transferência de elétrons ocorre devido ao efeito da função trabalho. Como a função trabalho do Fe (4,5 eV) é menor que a da magnetita (5,52 eV) e da hematita (5,6 eV), a transferência de elétrons ocorre para diminuir as energias então a posição do nível de Fermi foi ajustada [45, 46]. A oxidação de Fe zero valente a Fe +2 íons (íons ferrosos) foi seguido com a transferência de 2 elétrons do núcleo de Fe NCs para o gás oxigênio na solução para produzir peróxido de hidrogênio (Esquema 1b) [47].
$$ {Fe} ^ 0 + {O} _2 + 2 {H} ^ {+} \ para {Fe} ^ {2 +} + {H} _2 {O} _2 $$
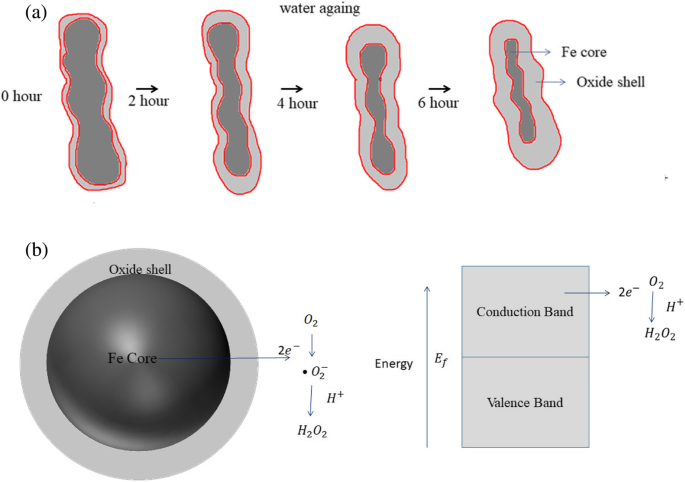
a Formação de Fe NCs preparados por 120, 240 e 360 min de envelhecimento em água, b mecanismo de O 2 rota de ativação sobre os Fe NCs do núcleo-shell
Além disso, H 2 O 2 reage com íons ferrosos para produzir radical hidroxila e íons férricos [47].
$$ {Fe} ^ {2 +} + {H} _2 {O} _2 \ a {Fe} ^ {3 +} + {OH} ^ {-} + \ bullet \ kern0.5em OH $$
A taxa de transferência de elétrons pode ser afetada pelo aumento da espessura da camada de óxido. A análise TEM mostra que conforme o tempo de reação na água aumenta, a espessura da camada de óxido aumenta, o que poderia interromper a taxa de transferência de elétrons ainda mais. Na temperatura abaixo de 150 ° C, a transferência de elétrons ocorre principalmente por resultados de tunelamento de elétrons na formação da camada de óxido de até alguns nanômetros [48]. Então, após a oxidação prolongada da água, uma camada de óxido estável foi formada na superfície do núcleo de Fe, porque durante a síntese, os precipitados obtidos de Fe NCs foram secos sob a atmosfera inerte (no nosso caso, Argônio) para reduzir o risco de oxidação posterior . Esses Fe NCs podem ser estáveis por até 6 meses sem oxidação adicional, o que os torna biocompatíveis e candidatos adequados para aplicações biomédicas.
VSM
As propriedades magnéticas do Fe NCs foram medidas a 320 K conforme mostrado na Fig. 11. É claro na Fig. 11 que o Fe NCs-0 e Fe NCs-2 possuem o valor de magnetização de saturação (Ms) de 1400 emu / ge 1420 emu / g, que é maior do que Fe NCs-4 e Fe NCs-6 com valores de Ms de 1200 emu / ge 910 emu / g. No estágio inicial de oxidação (por 0 min e 120 min), a casca de Fe NCs-0 e Fe NCs-2 foi feita de uma mistura de magnetita e hematita que causam redução na contribuição do núcleo de Fe zero valente, mas devido a presença de magnetita em ambas as amostras possuem alto momento magnético, portanto o valor de magnetização de saturação do Fe NCs-0 está mais próximo do Fe NCs-2. Mas com o aumento do envelhecimento da água (de 120, 240 a 360 min), a magnetita é gradualmente convertida em hematita , e também o núcleo de Fe diminui, de modo que a magnetização de saturação das amostras Fe NCs-2, FeNCs-4 e Fe NCs-6 também diminui (ou seja, 1420 emu /, 1200 emu / g, 910 emu / g). A Figura 12 mostra a dependência dos valores de Ms (emu / g) no aumento da espessura da casca oxidada para Fe NCs-0, Fe NCs-2, Fe NCs-4 e Fe NCs-6 com um diâmetro médio semelhante de 96 nm e diferente R core / R shell razão (Tabela 4).
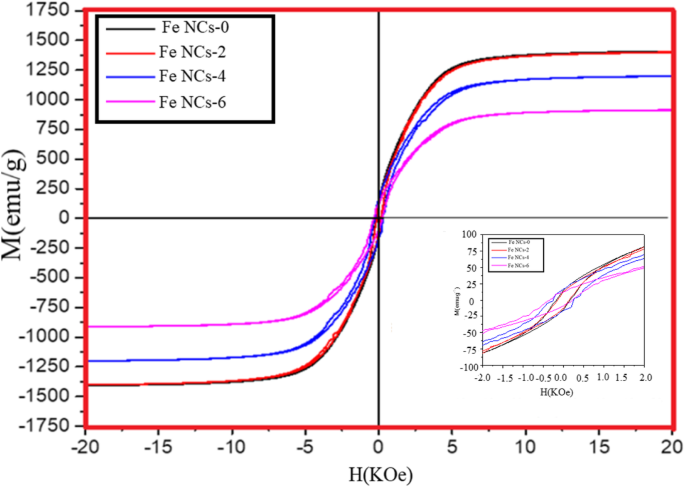
Histerese magnética medida à temperatura ambiente, a inserção mostra a curva ampliada entre - 2,0 e 2,0 kOe
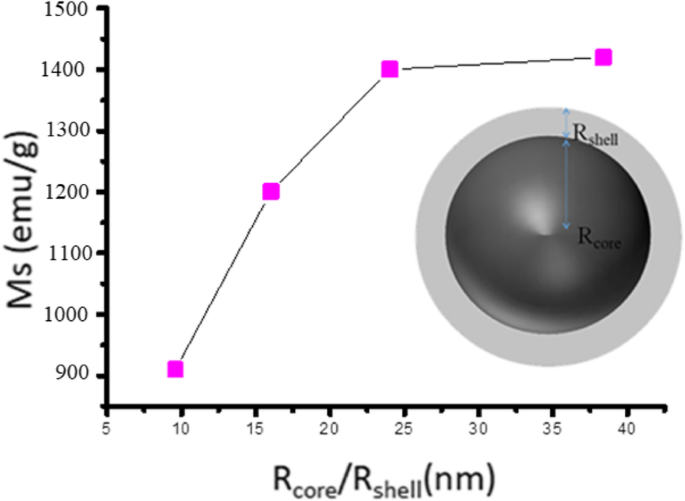
Ms Vs R core / R shell curva, tomando o diâmetro médio de Fe NCs 96 nm
Para explicar os fenômenos de reversão de magnetização em cadeia composta de partículas esféricas de domínio único, Jacobs e Beans [49] introduziram o “modelo de cadeia de esferas”. O modelo de cadeia de esferas pode ser aplicado para Fe NCs, considerando a montagem em cadeia de nanopartículas de Fe [49]. Embora o módulo seja aplicável apenas às partículas de domínio único com interações dipolares de longo alcance entre, neste caso, os valores de Hc para Fe NCs são considerados muito baixos em comparação com os valores previstos em [49]. Os dois mecanismos importantes, mecanismo de ventilação e mecanismo de ondulação, estão relacionados a dois estados próprios de magnetização. No nosso caso, ambos os mecanismos não são aplicáveis. Recentemente, Krajewski et al. [50] estudaram propriedades estruturais e magnéticas de Fe NCs e NPs e previram que Fe NCs seguem o mecanismo de ventilação. Embora (1) ao contrário dos resultados de Zhang e Manthirama [51], seu estudo não forneceu a prova de que Fe NCs se encontram na região de domínio único (ou seja, os resultados de Zhang e Manthirama mostram que os valores de Hc de Fe NCs aumentam com o aumento do diâmetro da partícula , e na faixa de diâmetro de 28–35 nm, o valor de Hc permanece quase máximo (≈ 1250 Oe), esta é a região que corresponde a um único domínio de Fe NCs). (2) Em segundo lugar, o valor de Hc em seu estudo [50] encontrado muito baixo (ou seja, 300 Oe) do que estudos teóricos anteriores que explicam o mecanismo de ventilação (ou seja, Hc ≥ 900 Oe para n =2 – ∞, onde n é o número de partículas na cadeia) [49]. (3) Finalmente, não há explicação sobre o comportamento de reversão da magnetização de Fe NCs.
Trabalhos anteriores mostram que, para aplicações de ressonância magnética, a morfologia das nanopartículas (valor Ms, tamanho e material dopante) foi fortemente considerada para melhorar o r 2 valores [52,53,54]. A teoria da esfera externa da mecânica quântica explica que o r 2 a relaxividade depende do raio efetivo e do valor Ms do núcleo superparamagnético [55, 56]. A relaxividade r 2 de NPs de Fe superparamagnéticos podem ser explicados por [57,58,59,60]
$$ {r} _2 =\ frac {\ left (256 {\ pi} ^ 2 {\ gamma} ^ 2 \ right) {kM} _s ^ 2 {r} ^ 2} {D \ left (1+ \ frac {L} {r} \ right)} $$ (1)
onde γ e Ms são magnetização de saturação, r é o raio do núcleo magnético, L é a espessura, D é a difusividade das moléculas de água, e k é o fator de conversão. Esta equação mostra que r 2 os valores dependem diretamente dos valores de Ms e do raio do material magnético. Tendo isso em mente, Fe NCs-0 pode ser um candidato potencial para r 2 agentes de contraste para ressonância magnética em um futuro próximo.
Conclusão
A análise estrutural de Fe NCs foi feita por XRD, TEM, espectroscopia Raman e espectroscopia Mössbauer. A análise de XRD mostra que o núcleo de Fe NCs foi feito por bcc Fe, mas nenhum pico de óxido de ferro foi observado. Os resultados do TEM mostram que uma fina camada de óxido foi formada em Fe NCs, confirmando a natureza do núcleo-casca dos Fe NCs. Com o aumento do tempo de reação em água de 0 para 360 min, a espessura da camada de óxido aumenta de 2,5 para 10 nm. Estudos Raman mostram que a camada de Fe NCs-0 e Fe NCs-2 era uma mistura da fase de hematita e magnetita. O pico de magnetita parece desaparecer para Fe NCs-4 e Fe NCs-6. Analisando a espectroscopia Mössbauer sobre Fe NCs-0 e Fe NCs-6, observou-se que o núcleo do Fe NCs-0 e Fe NCs-6 era de Fe bcc. A camada de Fe NCs-0 foi feita de magnetita, e a fase de hematita e a camada de Fe NCs-6 mostram a fase de hematita pura. O possível mecanismo para a formação de NCs de Fe núcleo-casca, conforme deduzido da espectroscopia Mössbauer e da espectroscopia Raman, é o tempo inicial de oxidação; o núcleo de Fe zero valente foi imediatamente coberto por uma camada de magnetita e concha de hematita, mas devido ao tempo prolongado de oxidação da água a magnetita foi gradualmente convertida em hematita. As propriedades magnéticas dos Fe NCs foram medidas por VSM à temperatura ambiente. Os valores de Ms diminuem com o aumento da camada de óxido, devido a um aumento na contribuição de menos momento magnético da fase de hematita.
Disponibilidade de dados e materiais
The datasets supporting the conclusions of this article are included within the article.
Abreviações
- 0-D:
-
Zero dimensional
- 1-D:
-
One dimensional
- DI:
-
Deionized
- EDX:
-
Energy-dispersive X-ray spectroscopy
- FE-SEM:
-
Field emission scanning electron miscroscopy
- H:
-
Hyperfine field
- Hc:
-
Coercivity
- MH:
-
Magnetic hyperthermia
- Mr:
-
Remanent magnetization
- MRI:
-
Magnetic resonance imaging
- Ms:
-
Saturation magnetization
- NCs:
-
Nanochains
- NWs:
-
Nanowires
- Q:
-
Quadrupole splitting
- TEM:
-
Microscopia eletrônica de transmissão
- VSM:
-
Vibrating sample magnetometer
- XRD:
-
Difração de raios X
- δ :
-
Isomer shifts
Nanomateriais
- Indutores
- Estilhaços
- Nanocups podem dobrar luz
- Tratamento de campo eletromagnético RF de absorvedores de luz de Kesterita tetragonal CZTSSe
- Síntese de pontos quânticos do tipo II / tipo I suprimida por reabsorção / CdS / ZnS Core / Shell Quantum Dots e sua aplicação para ensaio de imunossorvente
- Síntese verde de pontos quânticos InP / ZnS Core / Shell para aplicação em diodos emissores de luz livres de metais pesados
- Fabricação, caracterização e citotoxicidade de nanopartículas de carbonato de cálcio derivadas de casca de ouro conjugada em forma esférica para aplicações biomédicas
- Controle eletroquímico reversível sobre luminescência fotoexcitada do filme de pontos quânticos do núcleo / casca / ZnS
- Sondando as propriedades estruturais, eletrônicas e magnéticas dos aglomerados Ag n V (n =1–12)
- Profundos efeitos interfaciais em CoFe2O4 / Fe3O4 e Fe3O4 / CoFe2O4 Core / Nanopartículas de Shell



