Síntese de pontos quânticos do tipo II / tipo I suprimida por reabsorção / CdS / ZnS Core / Shell Quantum Dots e sua aplicação para ensaio de imunossorvente
Resumo
Nós relatamos um método one-pot sem fosfina para sintetizar pontos quânticos de núcleo-casca de ZnSe / CdS / ZnS (QDs) com estruturas compostas tipo II / tipo I e propriedades de supressão de reabsorção consequentes. Os QDs sintetizados possuem alta eficiência de emissão vermelha (com rendimento quântico de 82%) e alta estabilidade óptica. Em comparação com QDs tipo I, os QDs ZnSe / CdS / ZnS mostram maior deslocamento de Stokes e menor reabsorção, o que pode reduzir a perda de emissão e melhorar o nível de saída de fluorescência. Os QDs ZnSe / CdS / ZnS são usados como marcadores fluorescentes para explorar sua aplicação em ensaio imunossorvente ligado a fluorescência (FLISA) pela primeira vez na detecção de proteína C reativa (CRP) com um limite de detecção (LOD) de 0,85 ng / mL, que é mais sensível do que o FLISA baseado em QDs de CdSe / ZnS tipo I (1,00 ng / mL). Os resultados indicam que os QDs ZnSe / CdS / ZnS tipo II / tipo I podem ser bons candidatos para aplicações em detecção de informação biomédica.
Histórico
Os pontos quânticos de semicondutores (QDs) fluorescentes de núcleo / casca são caracterizados pelas excelentes propriedades ópticas, como faixa de emissão mais ampla, rendimentos quânticos de fotoluminescência (PL) mais altos (QYs) e estabilidade óptica e química mais alta do que os corantes orgânicos tradicionais. Essas vantagens abrem oportunidades para avanços revolucionários em rótulos fluorescentes para diagnósticos biomédicos, imagem molecular e campo fotoelétrico [1,2,3,4,5,6,7]. De acordo com o alinhamento da banda entre o núcleo e os materiais do invólucro, os QDs do núcleo / invólucro podem ser classificados como estruturas tipo I, tipo reverso I e tipo II. Tipo-I QDs caracterizados pela estrutura de alinhamento de banda "aninhada", que pode confinar os elétrons e buracos na região do núcleo para aumentar a recombinação radiativa e separar fisicamente a superfície do núcleo óptico ativo de seu meio circundante e, assim, melhorar a intensidade PL e estabilidade óptica [6,7,8,9]. Apesar dessas propriedades favoráveis, um pequeno deslocamento de Stokes (apenas uma dúzia de nanômetros), referido como a diferença entre os espectros de absorção e PL, gera uma reabsorção séria, levando a uma perda geral de emissão e limitando sua aplicação na determinação quantitativa [10, 11]. Em contraste, os QDs do tipo II com alinhamento de bandgap escalonado promovem a separação espacial do elétron e do buraco em diferentes regiões da estrutura do núcleo / camada. A energia de transição de recombinação e – h da borda da banda subsequente é menor do que o intervalo de banda de qualquer um dos componentes do material constituinte, levando a uma emissão significativa deslocada para o vermelho, que não está disponível com nenhum dos materiais monocomponentes. A força do oscilador do primeiro recurso de absorção de excitons dos QDs do tipo II diminui drasticamente em comparação com os QDs centrais [12, 13]. A emissão amplamente alterada para o vermelho e o primeiro pico de absorção de exciton achatado reduzem a sobreposição dos espectros de absorção e emissão, o que suprime a reabsorção, e beneficia a detecção quantitativa biológica. Os QDs ZnSe / CdS tipo II típicos têm emissão ajustável de violeta azulado a faixa vermelha e reabsorção suprimida [13]. No entanto, os elétrons deslocalizados na camada CdS são vulneráveis à captura de defeitos de superfície ou meio circundante, levando a um baixo rendimento quântico de fluorescência. Uma solução viável é revestir os QDs de ZnSe / CdS com a camada mais externa de ZnS não apenas para passivar a superfície para aumentar o rendimento quântico e estabilidade óptica, mas também para restringir o vazamento do elemento Cd tóxico, reduzindo a biotoxicidade. Até o momento, a maioria das pesquisas tem se concentrado em QDs tipo I, e apenas algumas foram realizadas em QDs ZnSe / CdS / ZnS tipo II / tipo I [12,13,14,15]. Além disso, todos os estudos sobre o processo de síntese de ZnSe / CdS / ZnS QDs usaram uma preparação de duas etapas por pré-purificação de QDs de núcleo de ZnSe bruto e fosfinas tóxicas e caras. Além disso, nenhum deles envolveu a aplicação de ZnSe / CdS / ZnS QDs na detecção biológica.
Aqui, relatamos um método one-pot sem fosfina para sintetizar QDs de emissão vermelha de alta qualidade ZnSe / CdS / ZnS tipo II / núcleo / shell tipo I com o recurso de reabsorção-supressão e o primeiro uso dos QDs para fabricar ensaio imunossorvente ligado à fluorescência (FLISA). Usamos precursor de Se altamente reativo e baixo tóxico (ODE-Se) e oleato de zinco para sintetizar QDs de núcleo de ZnSe de alta qualidade e, em seguida, alcançamos o crescimento multishell sem purificação de pontos quânticos do núcleo. Isso mostra uma grande promessa para a síntese em larga escala de pontos quânticos de núcleo / camada. O rendimento quântico de vermelho como preparado emitindo QDs de ZnSe / CdS / ZnS tipo II / tipo I pode chegar a 82% com menor teor de cádmio tóxico, o que é particularmente importante para reduzir a biotoxicidade no campo biomédico. Além disso, os QDs têm grande deslocamento de Stokes, bem como primeiro pico de absorção achatado, o que leva a uma baixa sobreposição de PL e espectros de absorção e efeito de reabsorção suprimido.
A proteína C reativa (CRP), como uma proteína de fase aguda das células do fígado, tem sido considerada um indicador precoce de infecção e distúrbios autoimunes. Essas doenças geralmente começam com níveis de CRP muito baixos. Portanto, a análise de imunoensaio quantitativo sensível dos níveis de PCR em amostras biológicas é de fundamental importância para o diagnóstico e monitoramento da evolução das doenças [16]. Comparado com o ensaio imunoenzimático tradicional (ELISA), o FLISA economiza tempo sem reação enzimática e é menos sensível às condições ambientais decorrentes da qualidade óptica dos QDs fluorescentes [17]. Portanto, FLISA tornou-se um novo ponto de acesso de pesquisa de imunoensaio quantitativo [2, 18,19,20,21]. Aqui, demonstramos em primeiro lugar o imunoensaio quantitativo FLISA usando QDs de ZnSe / CdS / ZnS tipo II / núcleo / concha solúvel em água como sonda fluorescente. O limite de detecção (LOD) para detecção quantitativa da proteína CRP atingiu 0,85 ng / mL, que foi 15% mais sensível do que o CdSe / ZnS tipo I com QDs FLISA em experimentos de controle. Os altos QYs, excelente estabilidade óptica e baixo efeito de reabsorção podem promover a aplicação de QDs de ZnSe / CdS / ZnS tipo II / tipo I em biomedicina e campo fotoelétrico.
Métodos
Químicos
Óxido de cádmio (CdO, 99,99%), óxido de zinco (ZnO, 99,9%, pó), selênio (Se, 99,9%, pó), 1-octadeceno (ODE, 90%), 1-octanotiol (OT, 98%), ido oleico (OA, 90%) Poli (anidrido maleico-alt-1-octadeceno) (PMAO) e ido 2- (N-morfolino) etanossulfico (MES) foram adquiridos da Aldrich. Óleo de parafina (grau analítico), acetona (grau analítico), hexanos (grau analítico) e metanol (grau analítico) foram obtidos de Beijing Chemical Reagent Co., Ltd, China. NaOH, HCl, Na 2 CO 3 , NaHCO 3 , KH 2 PO 4 , Na 2 HPO 4 , H 3 BO 3 , Na 2 B 4 O 7 · 10H 2 O e Tween-20 foram adquiridos de Shanghai Sangon Co., Ltd, China. Albumina de soro bovino (BSA) e soro de bezerro foram adquiridos da Sigma. 1-etil-3- (3- (dimetilamino) propil) carbodiimida (EDC), N-hidroxissulfosuccinimida (sulfo-NHS) e as microplacas foram adquiridas na Thermo Fisher Scientific (EUA). O anticorpo monoclonal anti-proteína C de camundongo e o antígeno CRP foram obtidos na Abcam (EUA). Todos os produtos químicos e solventes foram usados como recebidos sem purificação adicional.
Solução de estoque para o precursor Se (0,1 M)
Se (6 mmol) e ODE (60 mL) foram carregados em um balão de três gargalos de 100 mL e, em seguida, aquecidos a 220 ° C por 180 min sob nitrogênio para obter uma solução amarela transparente.
Solução de estoque para o precursor Zn (0,4 M) e o precursor Cd (0,2 M)
ZnO (30 mmol), ácido oleico (30 mL) e 45 mL ODE foram carregados em um frasco de três gargalos de 100 mL e aquecidos a 310 ° C sob nitrogênio para obter uma solução límpida. A solução resultante foi deixada arrefecer até 140 ° C para injeção. O processo de preparação para o precursor Cd foi igual ao precursor Zn, exceto que a concentração foi ajustada para 0,2 M e a temperatura da reação foi ajustada para 240 ° C.
Síntese típica de QDs de ZnSe / CdS / ZnS Tipo II / Tipo I
Como um procedimento sintético típico, 4 mL de precursor de Se e ODE (15 mL) foram colocados em um frasco redondo de 100 mL. A mistura foi aquecida a 310 ° C. Nesta temperatura, 2 mL do precursor de Zn foram rapidamente injetados no frasco de reação. As alíquotas foram extraídas em diferentes intervalos de tempo para monitorar a evolução da posição PL, que se coordena com o tamanho de partícula dos QDs. Quando os nanocristais do núcleo atingiram a dimensão desejada, a temperatura da reação foi reduzida para 230 ° C para o crescimento da camada de CdS. Sem quaisquer etapas de purificação, como a mistura de precursor Cd e 1-octanotiol (o rádio molar de OT e cátion é 1:1,2) começou a ser adicionado gota a gota com uma bomba de seringa a uma taxa de 3 mL / h, enquanto a temperatura era elevado a 310 ° C. O mesmo processo foi aplicado ao crescimento da casca do ZnS. Alíquotas de QDs foram retiradas durante a reação para analisar o desenvolvimento de QDs de núcleo / casca de ZnSe / CdS / ZnS. Os QDs núcleo / casca conforme preparados foram purificados pela adição de acetona e, em seguida, redispersos em clorofórmio.
Síntese típica de QDs CdSe / ZnS Tipo I
CdSe / ZnS QDs foram sintetizados conforme descrito em nossos relatórios anteriores [7]. Posteriormente, o processo de transferência de fase, sondas de detecção de QDs-anticorpo e a preparação de FLISA foram iguais aos de ZnSe / CdS / ZnS QDs, que seriam descritos a seguir.
Transferência de fase de QDs de ZnSe / CdS / ZnS para bioaplicação
Poli (anidrido maleico-alt-1-octadeceno) (PMAO) - um oligômero anfifílico cujas extremidades hidrofóbicas se intercalam com o revestimento orgânico em QDs e grupos terminais hidrofílicos estão livres para interagir com o tampão circundante - foi usado para transferir QDs hidrofóbicos em puros agua. O ZnSe / CdS / ZnS QDs e PMAO foram misturados e dissolvidos em clorofórmio com sonicação (razão molar de QD / PMAO foi de 1:7). Depois disso, o clorofórmio foi então removido por evaporação rotativa a 45 ° C. Então, um volume igual de NaHCO 0,1 M 3 solução aquosa (pH =8,5) foi adicionada para dissolver o QDs-PMAO. Os QDs de ZnSe / CdS / ZnS tipo II / tipo I encapsulados em PMAO não apresentam perda de fluorescência e apresentam alta estabilidade em solução aquosa em uma ampla faixa de ambientes de pH.
Preparação de sondas de detecção de anticorpos QDs
O procedimento foi amplamente relatado em literaturas anteriores [1,2,3]. Os QDs-PMAO foram primeiramente conjugados com o anticorpo monoclonal CRP através da ativação desses grupos -COOH por EDC e sulfo-NHS. Em seguida, uma certa quantidade de anticorpos monoclonais CRP foram adicionados aos QDs e dissolvidos em tampão BS e, em seguida, foram bloqueados por BSA. Finalmente, o produto foi lavado com tampão BS 5 mM (pH =8,0) sob centrifugação. O QDs-mAb foi armazenado em 50 μL de tampão BS (5 mM, pH =8,0).
Preparação da microplaca de fluorescência revestida com anticorpo
O anticorpo primário (a concentração de anticorpo monoclonal CRP foi de 1,8 mg / mL) foi diluído com um tampão carbonato-bicarbonato (pH 50 mM =9,6, tampão CB) em cada poço da microplaca. Posteriormente, a microplaca foi coberta com filme selante e incubada a 4 ° C por 24 h. Para remover o anticorpo de revestimento extra, a microplaca foi lavada três vezes com um tampão de lavagem (0,05% Tween-20 em PBS 10 mM, pH =7,4). Em seguida, os locais de ligação em excesso foram bloqueados com 0,5% (p / v) BSA em PBS 10 mM (pH =7,4) para incubação durante a noite a 4 ° C. Este processo garantiu que todos os lados de ligação disponíveis e restantes dos poços da microplaca fossem cobertos. A microplaca foi seca em câmara com temperatura e umidade constantes por 24 h, a seguir armazenada a 4 ° C para uso futuro.
Detecção quantitativa de CRP por imunoensaio ligado à fluorescência
Em cada poço de uma microplaca de 96 poços, o anticorpo de revestimento contido foi adicionado 100 μL do antígeno padrão e diluído em uma série de concentrações com o tampão de amostra. As placas foram incubadas a 37 ° C durante 30 min e depois lavadas cinco vezes com um tampão de lavagem. Em seguida, 100 μL das sondas QDs-mAb foram diluídas com o tampão da sonda (soro de bezerro a 10% (v / v) em PBS 0,1 M) em cada poço foram incubadas e lavadas da mesma forma que o processo acima mencionado.
Caracterização
A absorção de UV-vis em temperatura ambiente e os espectros de PL foram medidos com um espectrofotômetro Ocean Optics (modo PC2000-ISA). Os rendimentos quânticos PL (QYs) foram determinados por comparação da intensidade de fluorescência integrada das amostras QD em solução com a do padrão de QYs conhecidos (Rodamina 101 (R101) solução de etanol (0,01% HCl, QY =100%) como o padrão) . Os estudos de microscopia eletrônica de transmissão (TEM) foram realizados usando um microscópio eletrônico JEOL JEM-2010 operando a 200 kV. A determinação das fases dos produtos foi realizada em difratômetro de raios X (D8-ADVANCE) utilizando radiação Cu-Ka (comprimento de onda =1,54 Å). Os tamanhos dos QDs e da sonda de anticorpo QD foram registrados usando dispersão de luz dinâmica (Nano-ZS 90, Malvern Instruments, UK).
Resultados e discussão
Os espectros de absorção UV-vis e PL do processo de crescimento da casca são mostrados na Fig. 1. O deslocamento de Stokes do núcleo ZnSe é de apenas 8 nm com o primeiro pico de absorção em 420 nm e pico de emissão em 428 nm, e largura total de emissão na metade máximo (FWHM) de 17 nm. No entanto, quando apenas uma monocamada (ML) de camada de CdS cresceu no núcleo ZnSe, o deslocamento de Stokes aumentou significativamente para 54 nm com o primeiro pico de absorção em 497 nm e pico de emissão em 551 nm, com largura total de emissão na metade do máximo (FWHM) de 38 nm. Devido à deslocalização da função de onda do elétron, a emissão de PL de ZnSe / CdS QDs (629 nm) é desviada para o vermelho em relação aos QDs de núcleo ZnSe (428 nm) e o FWHM ampliado para 52 nm com a deposição de camada de CdS. O PL FWHM ampliado originou-se de uma interação exciton-fônon semelhante a Frölich [22, 23]. Além disso, a força do oscilador do primeiro pico de absorção enfraqueceu rapidamente devido à transição espacialmente indireta do tipo II da banda de valência do ZnSe para a banda de condução do CdS. O fenômeno é comum em QDs do tipo II [24,25,26]. Enquanto o aumento dramático na absorção na região espectral do azul (<500 nm) foi atribuído ao intervalo de banda do material CdS em massa (2,42 eV). Em consequência, a emissão vermelha, o primeiro pico de absorção de exciton achatado e a absorção robusta na região de comprimento de onda curto (<500 nm) de QDs de ZnSe / CdS tipo II resultaram em grande deslocamento de Stokes e supressão de reabsorção. Com o crescimento sequencial da camada de ZnS, o PL foi deslocado para o comprimento de onda curto e o FWHM foi reduzido de 52 nm para 43 nm. Este fenômeno foi atribuído ao fato de que os átomos de Zn se difundem nas regiões ricas em Cd para formar uma camada de gradiente em alta temperatura, aumentando assim o deslocamento de banda da camada. O QYs pode aumentar de 20 a 82% durante o processo de crescimento da casca de CdS e ZnS em núcleos de ZnSe.
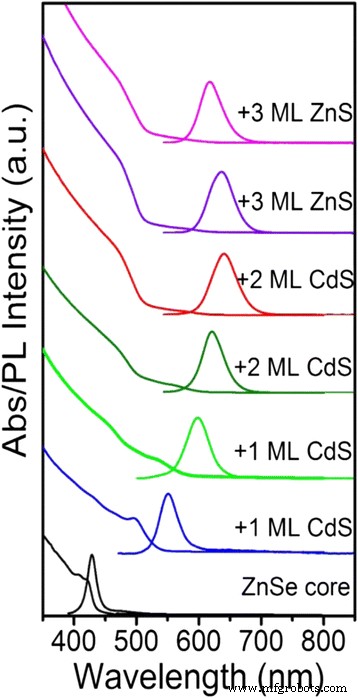
Evolução da absorção de UV-vis e espectros de PL após o crescimento consecutivo de QDs de núcleo / casca de ZnSe / CdS / ZnS
Foi digno de nota que o excesso de precursor Zn-OA em relação ao precursor de Se na solução de núcleo foi necessário para obter QDs de núcleo ZnSe monodispersos e de alta qualidade. Como resultado, o invólucro da liga ZnCdSeS seria inevitavelmente formado durante a adição do precursor do invólucro Cd-OT no estágio inicial, uma vez que a alta temperatura (> 200 ° C) promoveu a troca catiônica e difusão entre Zn 2 + e Cd 2+ , e o octanotiol rico no precursor Cd-OT também poderia reagir com o excesso de Zn-OA [7, 12, 27, 28]. O invólucro da liga pode não apenas reduzir a tensão interfacial e o defeito para aumentar os QYs, mas também gerar barreira de energia para os orifícios. A borda da banda de condução do material do invólucro da liga ZnCdSeS estava localizada entre a do ZnSe e do CdS, enquanto a borda da banda de valência era mais profunda do que o CdS. Isso formou um vale potencial maior na borda da banda de valência como uma camada de bloqueio adicional para os orifícios (Esquema 1) [12]. Esta estrutura de banda de energia pode reduzir ainda mais a sobreposição de elétrons e lacunas para diminuir a força do primeiro pico de absorção de excitons e suprimir a reabsorção.
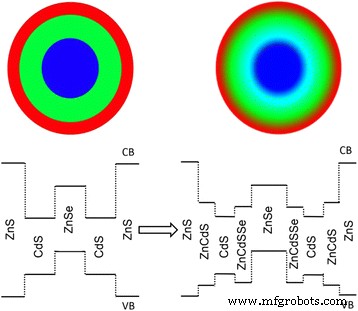
A estrutura esquemática ( up ) e o alinhamento da banda ( inferior ) para QDs ZnSe / CdS / ZnS tipo II / tipo I com base nas interfaces abrupta e ligada correspondentes, respectivamente
As informações sobre a estrutura de banda de núcleo / casca e a evolução de PL e absorvância durante o crescimento de casca podem ser ainda verificadas pela comparação de XRD, TEM e HRTEM de nanocristais de núcleo e núcleo / casca. Os padrões de pó XRD do núcleo ZnSe, ZnSe / CdS e núcleo / concha ZnSe / CdS / ZnS (a imagem à esquerda da Fig. 2) mostram que os picos de difração tornam-se nítidos e mudam para posições correspondentes a Wurtzita em massa (WZ) CdS ou estruturas de cristal ZnS. Este resultado é consistente com os valores previstos para o maior volume de CdS ou shell ZnS em comparação com o núcleo ZnSe nos QDs núcleo / shell finais e testemunha o crescimento de multishells. Além disso, uma transformação de núcleos de zinco blende (ZB) tipo ZnSe em núcleo / casca do tipo WZ ocorreu com o revestimento de CdS e ZnS. Este fenômeno foi relatado em sistemas CdSe / CdS core / shell QD [29, 30]. As imagens TEM dos QDs do núcleo e vários QDs do núcleo / casca são mostrados nas Fig. 2a - 2 F. Todas as imagens TEM mostram QDs esféricos quase monodispersos com diâmetros médios gradualmente increscentes do núcleo ZnSe original (3,90 nm) para o tipo ZnSe / 6CdS II QDs (7,98 nm) e ZnSe / 6CdS / 6ZnS tipo II / tipo I QDs (11,92 nm). Conforme mostrado na imagem HRTEM de QDs do núcleo ZnSe (inserção da Fig. 2a), o espaçamento da rede dos planos (111) é de 0,32 nm, e os QDs possuem boa cristalinidade e monodispersidade. Com o crescimento das cascas, o parâmetro de rede apresentou alteração correspondente (0,35 nm para CdS e 0,31 nm para ZnS) de acordo com os dados de XRD. Os resultados sugeriram claramente o crescimento controlável de CdS e subsequentes materiais de casca de ZnS.
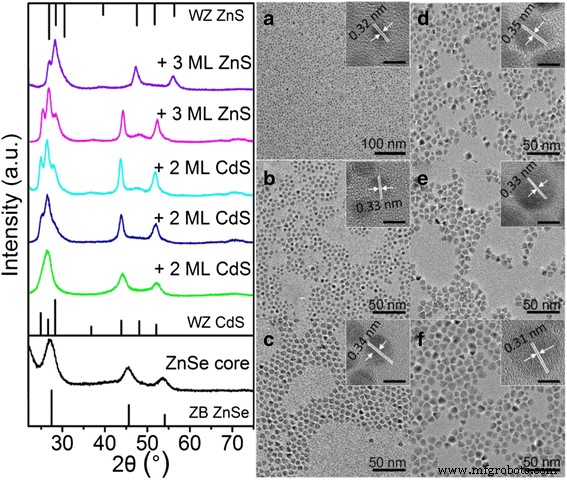
Esquerda :Padrões de XRD de QDs ZnSe / CdS / ZnS tipo II / tipo I com diferentes estágios de crescimento de casca. As linhas de difração para zinco blende (ZB) ZnSe (inferior), WZ CdS ( meio ) e WZ ZnS ( topo ) são indexados. Certo :o TEM e HRTEM correspondentes ( inserção , barra de 5 nm) imagens do núcleo ZnSe ( a ), QDs ZnSe / CdS tipo II com 2 ML ( b ), 4 ML ( c ) e 6 ML ( d ) Shell CdS, respectivamente, e QDs ZnSe / CdS / ZnS tipo II / tipo I com 3 ML (E) e 6 ML (F), respectivamente
Enquanto isso, para confirmar a evolução da composição durante o crescimento de multishell, a análise de espectroscopia de energia dispersiva de raios-X (EDS) foi realizada para diferentes estágios do crescimento do núcleo / casca, conforme mostrado no arquivo adicional 1:Tabela S1. Os dados de EDS mostram que as alterações correspondentes de conteúdo de Cd, Se, Zn e S estão de acordo com o estágio de crescimento da casca. Mas é importante notar que a razão molar Cd / (Zn + Cd) nos QDs ZnSe / CdS resultantes é maior do que a razão de alimentação Cd / (Zn + Cd) devido à troca catiônica entre Zn 2 + e Cd 2+ durante o processo de revestimento da casca de CdS no núcleo de ZnSe acima de 200 ° C. Em comparação com a literatura publicada sobre QDs de CdSe / CdS / ZnS tipo I típicos (razão molar de Cd ~ 40%) [31], os QDs de tipo II / tipo I ZnSe / CdS / ZnS continham muito menos elemento Cd (~ 13%).
Uma comparação visual de QDs hidrofóbicos em clorofórmio e QDs capeados com PMAO em água sob a luz do sol e luz ultravioleta é mostrada no arquivo adicional 1:Figura S1 (A). Parece que ambas as soluções QD não são perturbadas e não há agregação de nanopartículas. Ambos os QDs emitiram a mesma luz vermelha quando iluminados com uma lâmpada ultravioleta portátil (365 nm). Arquivo adicional 1:A Figura S1 (B) mostra a absorção UV-visível e espectros PL de QDs antes e depois da transferência de fase. Comparado com os QDs hidrofóbicos em clorofórmio, o espectro de PL de QDs capeados com PMAO tem mudança desprezível, indicando nenhuma mudança óbvia no tamanho de partícula e nas propriedades de PL. Arquivo adicional 1:As Figuras S1 (C) e (D) apresentam as imagens TEM dos QDs antes e depois da transferência de fase, que determina ainda mais a morfologia e o estado dos QDs protegidos por PMAO. Parece que os QDs capeados com PMAO são bem isolados e raramente observados como agregados.
A fim de confirmar a formação de QDs encapsulados em PMAO durante o processo de transferência de fase, a espectroscopia FTIR foi usada para caracterizar os grupos funcionais na superfície de QDs (mostrado no arquivo adicional 1:Figura S2). A diminuição do pico em 1777 cm −1 (comparou PMAO com QDs-PMAO) e o aumento do pico em 1715 cm −1 (comparou as três amostras) foram atribuídos à decomposição do anidrido e à formação de -COOH. Os resultados do FTIR indicaram que o polímero anfifílico PMAO foi revestido com sucesso na superfície dos QDs de ZnSe / CdS / ZnS.
A estabilidade dos QDs preparados é muito importante para o tratamento subsequente. A Figura 3a mostra a evolução da estabilidade PL relativa de QDs de ZnSe / CdS / ZnS hidrofóbicos após as etapas de purificação. A intensidade PL de QDs de núcleo / casca de ZnSe / CdS / ZnS poderia manter 85% após muitos ciclos de purificação em hexanos. Como mostrado na Fig. 3b, a estabilidade coloidal do QDs-PMAO em tampão BS (pH =7,2) foi estimada em função do tempo a 25 ° C. A intensidade de PL quase se manteve constante e a solução era límpida mesmo após 400 h. Isso indica que o QDs-PMAO é estável na solução BS sem qualquer dano. A Figura 3c mostra a variação na intensidade de PL de QDs-PMAO que foram imersos em solução de pH ácido a básico (pH =1-14, ajustado por HCl ou NaOH) por 30 min. A intensidade PL de QDs hidrofílicos poderia reter mais de 85%, exceto quando o PH =14. A Figura 3d mostra o efeito do parâmetro de temperatura na intensidade de fluorescência relativa de QDs-PMAO. A intensidade da fluorescência diminuiu gradualmente com o aumento da temperatura, mas ainda manteve 76% a 90 ° C, enquanto os picos de PL mudaram gradualmente para um comprimento de onda mais longo devido à expansão térmica e ao efeito de acoplamento elétron-fônon. Todas as avaliações de estabilidade indicam que o ZnSe / CdS / ZnS tipo-II / tipo-I QDs e QDs-PMAO eram muito estáveis e, portanto, adequados para aplicações biológicas.
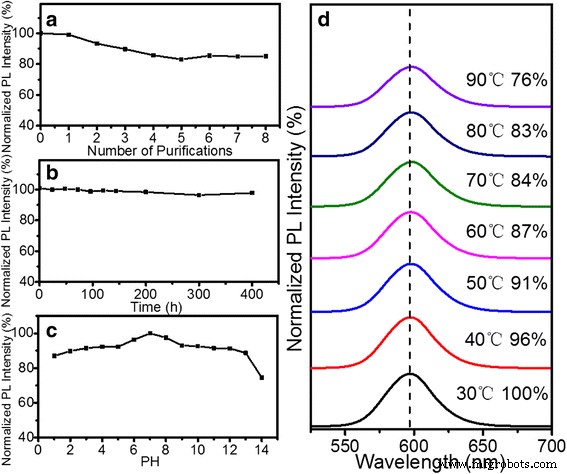
Teste de estabilidade de QDs hidrofóbicos após ( a ) etapas repetidas do processo de purificação; teste de estabilidade de QDs-PMAO após ( b ) Buffer BS, ( c ) PH e ( d ) temperatura
A PCR é uma proteína de fase aguda das células hepáticas, e seu nível é considerado um indicador precoce de infecção e distúrbios autoimunes. Aqui, os QDs de ZnSe / CdS / ZnS capeados com PMAO como sintetizados são acoplados com CRP para demonstrar a possibilidade de aplicação em imunoensaio quantitativo. O diagrama de comparação dos espectros de fluorescência de QDs de ZnSe / CdS / ZnS aquoso e o QDs-mAb são mostrados na Fig. 4a. Claramente, a forma do pico PL de ambas as amostras são aproximadamente idênticas, exceto que a intensidade da fluorescência diminui para 60% após a reação de acoplamento devido à perda inevitável da amostra durante o processo de separação por centrifugação. Isso prova a excelente estabilidade óptica de QDs de ZnSe / CdS / ZnS tipo II / tipo I mesmo após o processo de acoplamento da proteína do anticorpo.
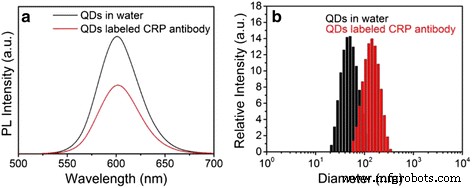
Espectro de fluorescência ( a ) e espalhamento de luz dinâmico ( b ) do QDs-PMAO e QDs-mAb no buffer
Para investigar melhor o efeito da conjugação no tamanho dos QDs, os QDs e QDs-mAb aquosos são caracterizados por espalhamento de luz dinâmico (DLS). Os resultados DLS (Fig. 4b) mostram claramente que ambas as amostras têm distribuição de tamanho estreita com boa monodispersidade e mantêm uma forma discreta sem agregação, enquanto o tamanho hidrodinâmico aumenta de 46 para 120 nm após o processo de acoplamento. Isso demonstra o sucesso na conjugação com anticorpos CRP.
Além disso, usamos os pontos quânticos compostos ZnSe / CdS / ZnS tipo II / tipo I em vez de QDs CdSe / ZnS tipo I como sonda fluorescente para estabelecer um FLISA para detecção quantitativa de CRP. O processo de montagem é mostrado no arquivo Adicional 1:Esquema S1. A Figura 5a mostra a intensidade de fluorescência relativa do marcador de fluorescência de QDs para imunoensaio na detecção de várias concentrações de antígenos de CRP (o antígeno de CRP padrão é diluído para 0, 1, 5, 10, 50, 100, 200, 400 ng / mL). Obviamente, a intensidade do PL aumenta gradativamente com o aumento da concentração de PCR. A Figura 5b mostra que a correlação entre a intensidade de fluorescência e as concentrações alvo de CRP obedecem a uma equação da curva de regressão quadrática de y =44230 + 8121,1x-10,3x 2 com um coeficiente de correlação de 0,9991, que quanto mais próximo de 1, melhor. As concentrações de trabalho variam de 0 a 400 ng / mL. O LOD é um dos principais parâmetros do imunoensaio para FLISA. Ao usar o composto ZnSe / CdS / ZnS tipo II / QDs tipo I como sonda fluorescente, a sensibilidade da detecção quantitativa de CRP é de 0,85 ng / mL, que é 15% mais sensível do que a de FLISA com base no tipo CdSe / ZnS -I QDs (1,00 ng / ml) (no arquivo adicional 1:Figura S3).
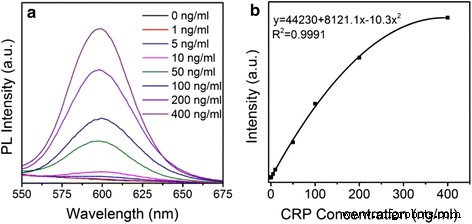
Espectro de fotoluminescência de FLISA para determinação de diferentes concentrações de antígeno CRP ( a ) e as curvas padrão ( b )
Além disso, experimentos de recuperação foram usados para avaliar o efeito da matriz do FLISA com uma série de antígenos CRP padrão conhecidos para análise, e as concentrações finais cobriram os níveis de risco baixo, médio e alto. Conforme mostrado na Tabela 1, todas as taxas de recuperação estão na faixa de 83,61-105,9%. Esses resultados indicam que o FLISA baseado em QDs ZnSe / CdS / ZnS tipo II / tipo I com propriedade de supressão de reabsorção tem alta precisão e é de grandes vantagens na detecção de imunoensaios quantitativos.
Conclusões
Relatamos um método one-pot sem fosfina para sintetizar QDs de núcleo / concha de ZnSe / CdS / ZnS suprimido por reabsorção com grande deslocamento de Stokes e primeiro pico de absorção plano. Essas características reduzem a reabsorção e melhoram o nível de saída de fluorescência. Os QDs sintetizados têm alto QY (82%) e alta estabilidade contra várias condições de teste. Então, primeiro usamos ZnSe / CdS / ZnS QDs como sonda de fluorescência em FLISA para a detecção quantitativa da proteína CRP com alta sensibilidade (LOD de 0,85 ng / mL). Isso indica que os QDs de ZnSe / CdS / ZnS tipo II / núcleo / concha suprimidos por reabsorção têm potencial promissor para aplicação em campos biomedicina e fotoelétricos.
Abreviações
- BSA:
-
Albumina sérica bovina
- CRP:
-
proteína C-reativa
- DLS:
-
Espalhamento de luz dinâmico
- EDC:
-
1-etil-3- (3- (dimetilamino) propil) carbodiimida
- EDS:
-
Espectroscopia de energia dispersiva de raios-x
- ELISA:
-
Ensaio de imunoabsorção enzimática
- FLISA:
-
Ensaio imunossorvente ligado à fluorescência
- FWHM:
-
Largura total pela metade no máximo
- LOD:
-
Limite de detecção
- MES:
-
Ácido 2- (N-morfolino) etanossulfônico
- OT:
-
1-octanotiol
- PMAO:
-
Poli (anidrido maleico-alt-1-octadeceno)
- QDs:
-
Pontos quânticos
- QYs:
-
Rendimentos quânticos
- sulfo-NHS:
-
N-Hidroxissulfosuccinimida
Nanomateriais
- Avanços e desafios dos nanomateriais fluorescentes para aplicações biomédicas e de síntese
- Síntese de pontos quânticos de carbono co-dopados com N, S ricos em piridínicos como imitações de enzimas eficazes
- Síntese verde de pontos quânticos InP / ZnS Core / Shell para aplicação em diodos emissores de luz livres de metais pesados
- Síntese de nanocristais de ZnO e aplicação em células solares de polímero invertido
- Síntese de aquecimento de estado sólido de composto de poli (3,4-etilenodioxitiofeno) / ouro / grafeno e sua aplicação para determinação amperométrica de nitrito e iodato
- Síntese de pontos quânticos de sulfeto de antimônio solúvel em água e suas propriedades fotoelétricas
- Controle eletroquímico reversível sobre luminescência fotoexcitada do filme de pontos quânticos do núcleo / casca / ZnS
- Síntese fácil e ecológica de nanofios de Co3O4 e sua aplicação promissora com grafeno em baterias de íon-lítio
- Síntese sonoquímica fácil de uma etapa e propriedades fotocatalíticas de compostos de pontos quânticos de grafeno / Ag3PO4
- Síntese e caracterização de BiOCl modificado e sua aplicação na adsorção de corantes de baixa concentração de solução aquosa



