Sistema de monitoramento da decomposição térmica in situ da fase gasosa Ciclopentadienil Tris (dimetilamino) Zircônio (CpZr (NMe2) 3) Com base em FT-IR e QMS para Deposição de Camada Atômica
Resumo
Desenvolvemos um sistema recentemente projetado com base no monitoramento in situ com espectroscopia de infravermelho por transformada de Fourier (FT-IR) e espectrometria de massa quadrupolo (QMS) para a compreensão do mecanismo de decomposição e subprodutos do Ciclopentadienil Tris (dimetilamino) Zircônio (CpZr (NMe) vaporizado> 2 ) 3 ) durante a movimentação para a câmara de processo em várias temperaturas porque os produtos de decomposição térmica de precursores indesejados podem afetar a confiabilidade do processo. Os dados FT-IR mostram que o –CH 3 a intensidade do pico diminui enquanto o –CH 2 - e as intensidades de pico C =N aumentam à medida que a temperatura aumenta de 100 para 250 ° C. Este resultado é atribuído à decomposição dos ligantes dimetilamido. Com base nos dados FT-IR, também pode ser assumido que um novo produto de decomposição está se formando a 250 ° C. Enquanto a análise de QMS in situ demonstra que CpZr vaporizado (NMe 2 ) 3 decompõe-se em N-etilmetanimina em vez de metilmetilenoimina. O monitoramento in situ com espectroscopia FT-IR e QMS fornece informações úteis para a compreensão do comportamento e decomposição de CpZr (NMe 2 ) 3 na fase gasosa, o que não foi comprovado antes. O estudo para entender a decomposição do precursor vaporizado é a primeira tentativa e pode ser fornecido como informação útil para melhorar a confiabilidade de um processo de deposição de filme ultrafino avançado usando deposição de camada atômica no futuro.
Introdução
O contínuo esforço para miniaturizar dispositivos eletrônicos tem levado a problemas relacionados à confiabilidade devido ao aumento do vazamento de corrente por tunelamento direto [1]. Para resolver este problema, materiais high-k com grandes lacunas de banda e constantes dielétricas altas, como Al 2 O 3 , Y 2 O 3 , HfO 2 , e ZrO 2 , são usados [2]. ZrO 2 é especialmente útil como uma camada isolante e dielétrica devido ao seu largo intervalo de banda (3,4 eV à temperatura ambiente), alto índice de refração, deslocamento de banda adequado em Si, corrente de fuga aceitavelmente baixa e boa estabilidade térmica [3, 4]. Por essas razões, este material é amplamente utilizado em sensores de gás e dispositivos optoeletrônicos [5].
ZrO ultrafino 2 os filmes são normalmente depositados por deposição de vapor químico (CVD) [3, 6] ou deposição de camada atômica (ALD) [7, 8]. Dos dois, o ALD (que é baseado em reações autolimitadas e tecnologias de controle de superfície alternadas) tem muitas vantagens, incluindo controle sobre a espessura da camada no nível subnm por meio do crescimento camada por camada, deposição de filme fino altamente uniforme, a formação de estruturas sem defeitos e boa reprodutibilidade [9]. Como tal, ALD é a principal técnica usada na fabricação de dispositivos em nanoescala [6].
Como o crescimento de filme fino com base em ALD prossegue por meio de reações químicas de precursores vaporizados e co-reagentes, é importante selecionar o precursor apropriado para um processo bem-sucedido [10, 11]. Em geral, um precursor de metal ALD deve ter uma alta pressão de vapor, um alto grau de pureza e baixa viscosidade e estabilidade química e térmica superior. A estabilidade térmica do precursor é particularmente importante, porque o precursor é mantido em alta temperatura no recipiente de borbulhamento enquanto é vaporizado e também exposto a temperaturas elevadas na linha de gás que alimenta o precursor vaporizado na câmara [12].
A estabilidade térmica do precursor do processo ALD deve ser considerada em dois pontos. Os precursores são expostos a um estresse térmico consistente porque os precursores são aquecidos para serem vaporizados durante o processo ALD. Além disso, a linha de gás para alimentar os precursores vaporizados na câmara é aquecida acima da temperatura do vaporizador para evitar a condensação ou coagulação dos precursores vaporizados e facilitar a difusão. Neste momento, a linha de gás é aquecida a uma temperatura mais alta, pois está mais próxima da câmara do evaporador. Geralmente é aquecido a uma temperatura entre 100 e 200 ° C. Portanto, a alta estabilidade térmica deve ser garantida para que a decomposição térmica não ocorra nesta faixa de temperatura. Porém, o precursor que tem estabilidade térmica muito alta não decompõe o ligante na temperatura do processo e leva à degradação da confiabilidade do filme [13]. Portanto, a decomposição térmica do ligante deve ocorrer na temperatura do processo. A fim de dois requisitos conflitantes sobre a estabilidade térmica do precursor, muitos pesquisadores estão projetando uma nova estrutura precursora [14,15,16].
A estabilidade térmica e o mecanismo de decomposição do precursor foram estudados por analisador termogravimétrico (TGA), calorímetro diferencial de varredura (DSC), infravermelho por transformada de Fourier (FT-IR) e espectroscopia, e espectroscopia de massa quadrupolar (QMS) [17,18,19 , 20,21,22]. TGA e DSC são usados principalmente para identificar rapidamente a janela de processo de um precursor, pois fornece informações sobre as propriedades térmicas dos materiais. FT-IR e QMS são usados para entender a reação dos precursores. Principalmente os estudos sobre os mecanismos de decomposição do precursor usando FT-IR e QMS têm sido usados para entender os mecanismos de reação nos substratos de deposição [23, 24]. O FT-IR fornece rapidamente informações sobre os dados precisos do precursor ou sua reação química [12], e o QMS torna conhecido as espécies gasosas que se relacionam com a reação de superfície [25, 26]. No entanto, os espectros FT-IR têm possibilidade de sobreposição múltipla porque muitas espécies IR-ativas são geradas durante o processo ALD [27], e uma variedade de moléculas com o mesmo valor de medição QMS presente porque QMS é detectado pelo impacto de elétrons de um filamento [26, 28]. A combinação de FT-IR e QMS é muito útil para complementar suas respectivas fraquezas e ajudar a entender a estabilidade térmica e o mecanismo de decomposição do precursor.
A decomposição térmica em precursores vaporizados em movimento devido à exposição ao estresse térmico não tem recebido atenção. Porém, a compreensão desse mecanismo pode fornecer informações muito úteis para a otimização do processo e o projeto de um novo precursor, pois a decomposição térmica de precursores indesejados pode afetar a confiabilidade do processo.
Neste estudo, tentamos entender sobre o mecanismo de decomposição térmica do precursor típico Ciclopentadienil Tris (dimetilamino) Zircônio (CpZr (NMe 2 ) 3 ; Cp:ciclopentadienil (C 5 H 5 ), Me:metil (-CH 3 ) na fase gasosa usando um sistema recém-projetado com base no monitoramento in situ usando espectroscopia de infravermelho com transformada de Fourier (FT-IR) e espectrometria de massa quadrupolar (QMS).
Métodos Experimentais
Os sistemas de monitoramento in situ recém-projetados
A Figura 1 mostra um esquema do sistema de monitoramento in situ projetado para examinar a decomposição térmica de precursores vaporizados. Neste estudo, os sistemas de monitoramento in situ são recentemente projetados para observar o comportamento do precursor exposto ao estresse térmico no vapor.
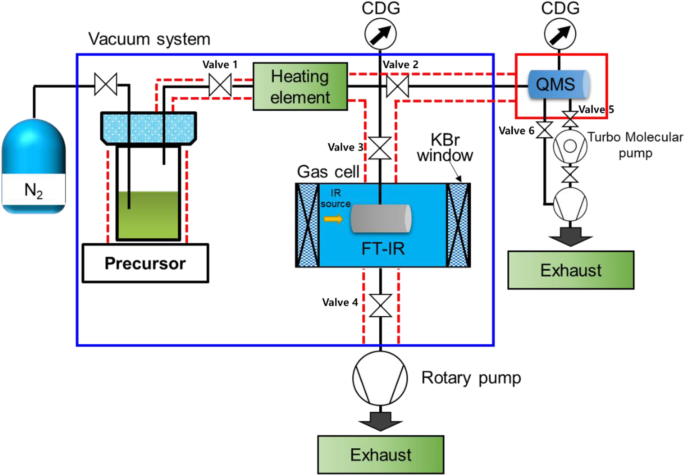
Esquema dos sistemas de monitoramento in-situ recém-projetados
Este aparelho compreende um sistema de vácuo conectado a um borbulhador, uma linha de alimentação com uma válvula, um elemento de aquecimento e uma célula de gás conectada a um espectrômetro FT-IR (Nicolet, Avatar 360). O sistema de vácuo feito em laboratório foi mantido a uma pressão de 10 −3 Torr usando uma bomba rotativa e o nível de pressão foi medido com um medidor de diafragma de capacitância (CDG) com um intervalo de 10 Torr. Em cada ensaio, o precursor era colocado dentro do borbulhador (que era mantido a 80 ° C), após o que o material vaporizado era fornecido para a linha de alimentação, que era construída em aço inoxidável (SUS) e possuía gaxetas de aço inoxidável em cada conexão além de válvulas manuais que permitiam a aplicação de vácuo. Tanto a linha de alimentação quanto a célula de gás FT-IR foram mantidas a 100 ° C para evitar a condensação do precursor. A célula de gás foi construída com janelas de KBr, tinha um volume de 45,5 mL e também foi mantida a um vácuo de 10 −3 Torr. O FT-IR empregou um detector de Hg-Cd-Te e resfriado com nitrogênio líquido. O espaçamento entre a fonte IR e a janela KBr é de 5 cm. Um elemento de aquecimento especialmente projetado permitiu que a temperatura do precursor vaporizado fosse controlada até 500 ° C.
Um instrumento QMS (Inficon, Transpector CPM) também foi conectado ao sistema de vácuo para permitir a análise adicional do precursor vaporizado e foi mantido a 150 ° C com uma camisa de aquecimento. A pressão interna no instrumento QMS foi mantida em 10 −8 Torr usando uma combinação de uma bomba turbomolecular e uma bomba rotativa, e essa pressão foi monitorada com um CDG.
Métodos de caracterização
O CpZr (NMe 2 ) 3 (Soulbrain, 99,8%) foi vaporizado por aquecimento do borbulhador de aço inoxidável. Durante os 10 min iniciais, todas as válvulas dos sistemas de monitoramento in situ foram abertas e o CpZr vaporizado (NMe 2 ) 3 foi passado para obter o precursor vaporizado idêntico. As válvulas 2 e 3 foram fechadas e os vapores resultantes foram transferidos para a zona de alta temperatura. As válvulas 1, 2 e 3 foram fechadas para isolar o CpZr vaporizado (NMe 2 ) 3 por 5 min no elemento de aquecimento para fornecer estresse térmico suficiente. Nessa altura, o elemento de aquecimento foi aquecido a temperaturas de 100 a 250 ° C em incrementos de 25 ° C. As válvulas 2 e 3 foram abertas e 4, 5 e 6 foram fechadas para mover os produtos de decomposição para FT-IR e QMS. As válvulas 2 e 3 foram fechadas e os produtos de decomposição resultantes foram avaliados usando a instrumentação FT-IR e QMS. O FT-IR adquiriu espectros na faixa de 500 a 3500 cm −1 com uma resolução espectral de 8 cm −1 , somando 32 varreduras para obter cada espectro. O QMS analisou íons na faixa de 1 a 300 unidades de massa atômica (amu), operando no modo de ionização por impacto de elétrons com uma energia de ionização de 30 eV. Depois de medido, as válvulas 4, 5 e 6 foram abertas para remover o CpZr aquecido (NMe 2 ) 3 por 10 min.
Resultados e discussão
O precursor incluindo frações ciclopentadienil tende a exibir alta estabilidade térmica devido à forte ligação entre esses grupos e átomos de metal, e CpZr (NMe 2 ) 3 é normalmente processado em temperaturas de 300 a 380 ° C [29,30,31].
Portanto, a decomposição térmica do CpZr vaporizado (NMe 2 ) 3 esperava-se que procurasse principalmente nos ligantes de trimetilamina em vez de nas ligações ciclopentadienil-Zr. Com base nesta suposição, os principais produtos de decomposição esperados estão resumidos na Tabela 1 [32,33,34]. E, os mecanismos dos principais produtos de decomposição esperados são os seguintes:
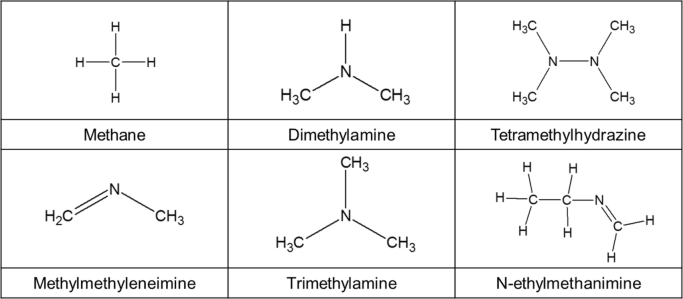
Reação de hidrogenação do ligante dimetilamino
H 2 + • NMe 2 → H • + HNMe 2
Reação de eliminação de hidrogênio do ligante dimetilamino
• NMe 2 + • NMe 2 → HNMe 2 + CH 2 =N-CH 3
Ligação covalente de ligante dimetilamino
• NMe 2 + • NMe 2 → (CH 3 ) 2 N-N (CH 3 ) 2
Reação de 1,2-eliminação da tetrametilhidrazina
(CH 3 ) 2 N-M (NCH 2 ) 3 → N (CH 3 ) 3 + H 3 C-N =M (NMe 2 ) 2
A Figura 2a mostra o resultado de TGA com a estrutura molecular de CpZr (NMe 2 ) 3 , enquanto a Fig. 2 b – d apresenta os espectros FT-IR adquiridos em várias temperaturas de decomposição.
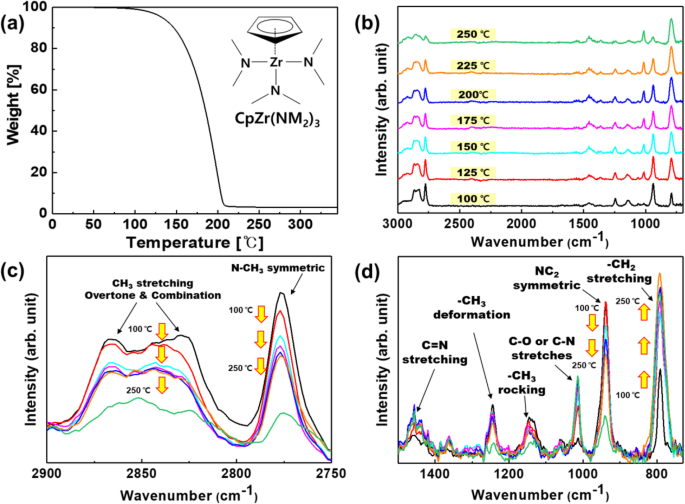
Resultado de TGA com estrutura química e espectro de FT-IR de 100 a 250 ° C de CpZr (NMe 2 ) 3 . a Estrutura química, espectro FT-IR, b faixa completa de 3000 ~ 700 cm −1 , c intervalo de 3000 ~ 2750 cm −1 , e d intervalo de 1300 ~ 700 cm −1
O resultado da análise TGA mostra a temperatura de decomposição térmica aproximada de CpZr (NMe 2 ) 3 . As temperaturas ocorridas em que a perda de massa são 0,5% e 5% são 87,6 ° C e 132,6 ° C, respectivamente. Também confirmamos que o peso não se tornou zero em alta temperatura. Isso significa que o Cp Zr (NMe 2 ) 3 não é completamente decomposto e materiais não voláteis são gerados e permanecem.
Os picos de absorção primários gerados pela fase gasosa CpZr (NMe 2 ) 3 foram associados ao alongamento de alcano C – H (cerca de 3000–2840 cm −1 ), N – CH 3 alongamento simétrico (2776 cm −1 ), Alongamento C =N (cerca de 1500–1400 cm −1 ), –CH 3 deformação (1241 cm −1 ), –CH 3 balanço (1142 cm −1 ), NC 2 alongamento simétrico (939 cm −1 ), e –CH 2 - alongamento (794 cm −1 ) Conforme a temperatura do vapor foi aumentada de 100 para 250 ° C, as intensidades desses picos de absorção principais diminuíram, exceto para o pico relacionado a –CH 2 - alongamento (Fig. 3). Como observado acima, no caso de CpZr (NMe 2 ) 3 , o ligante de trimetilamina é mais prontamente decomposto termicamente do que o ligante de ciclopentadienil, devido à diferença nas energias de dissociação das ligações Zr – N e C – N. Portanto, era esperado que a dimetilamina seria produzida pela reação de hidrogenação do ligante de dimetilamido como resultado da clivagem das ligações Zr-N no composto. Também é provável que as ligações C =N foram formadas pela reação de eliminação de hidrogênio dos ligantes de dimetilamido, porque a intensidade do pico FT-IR associada com o alongamento da ligação C =N em 1450 cm −1 aumentou com o aumento da temperatura (Fig. 3 e), de acordo com o produto previsto na Tabela 1.
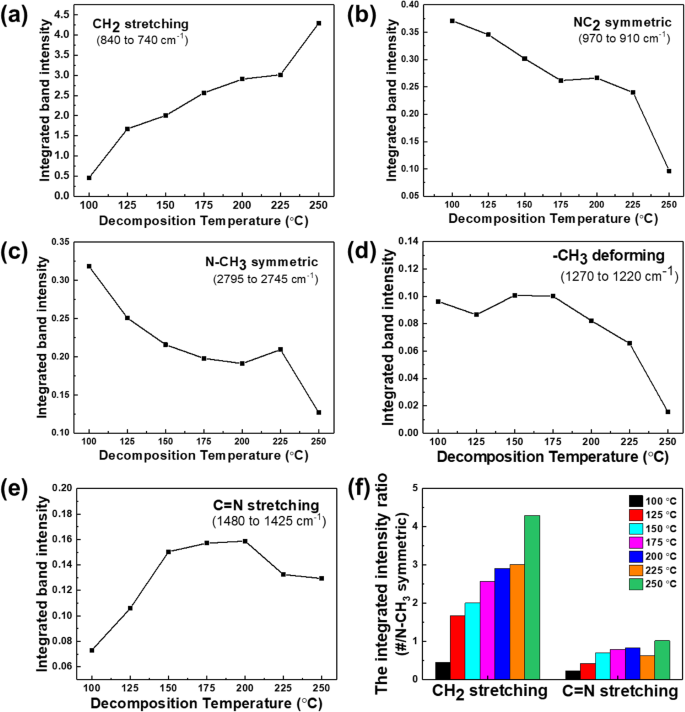
Intensidade de banda integrada e normalizada de CpZr (NMe 2 ) 3 foco do pico principal do espectro na região do espectro a –CH 2 - alongamento (840 a 740 cm −1 ), b NC 2 simétrico (970 a 910 cm −1 ), c N – CH 3 simétrico (2795 a 2745 cm −1 ), d –CH 3 deformando (1270 a 1220 cm −1 ) e e Alongamento C =N (1480 a 1425 cm −1 ) bandas, f a relação de intensidade integrada de pico principal / N – CH 3 áreas de pico
A intensidade do pico resultante de –CH 3 a deformação diminuiu drasticamente a 250 ° C e as intensidades dos outros picos associados com –CH 3 os grupos também mudaram abruptamente (Fig. 3 c, d). Além disso, quando o –CH 2 - as intensidades de pico de alongamento e C =N são normalizadas para N – CH 3 intensidade de pico, o –CH 2 - o pico aumenta abruptamente de intensidade a 250 ° C. Esses dados demonstram que a decomposição de –CH 3 grupos procede rapidamente a 250 ° C e que a reação que produz –CH 2 - os grupos procedem mais prontamente do que em outras temperaturas. Em contraste, a intensidade do pico de alongamento C =N não é significativamente aumentada em comparação com o aumento no –CH 2 - pico (Fig. 3 f). Portanto, parece que as reações de decomposição de CpZr (NMe 2 ) 3 a 250 ° C diferem do mecanismo proposto anteriormente, no qual predominam as reações de decomposição dos ligantes dimetilamido, como hidrogenação e eliminação de hidrogênio (Fig. 3 f).
A Figura 4 fornece os dados de análise do SGQ. O QMS usado neste estudo foi capaz de monitorar íons até 300 amu e CpZr (NMe 2 ) 3 e seus fragmentos têm massas de 228 e 144 amu, respectivamente. No entanto, o CpZr (NMe 2 ) 3 o íon parental a 144 amu só foi detectado a uma temperatura de aquecimento de 100 ° C. Acima desta temperatura, fragmentos com massas inferiores a 80 amu foram observados como resultado da rápida decomposição do CpZr vaporizado (NMe 2 ) 3 (Fig. 4 a).
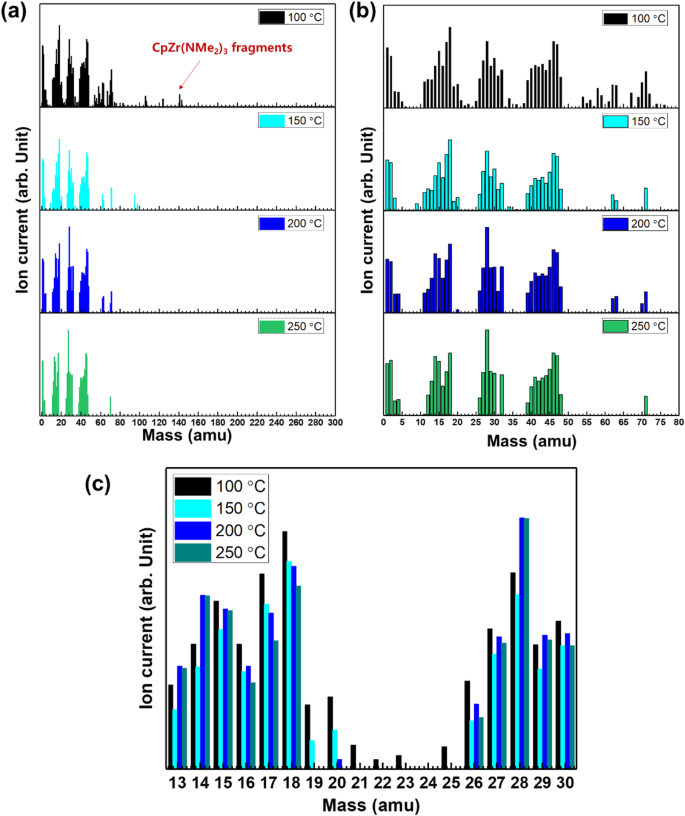
Dados de análise de QMS de CpZr (NMe 2 ) 3 a 0 a 300 amu, b 0 a 80 amu e c 13 a 30 amu
A Tabela 2 resume os produtos de decomposição térmica obtidos do CpZr (NMe 2 ) 3 . Os íons que aparecem em 5 amu e abaixo são atribuídos à ionização de hidrogênio e hidrogênio, de 10-20 amu a metano e ionização de metano, de 25-32 amu a N-etilmetanimina, fragmentos de trimetilamina e ionização, de 40-50 amu a dimetilamina e Ionização de N-etilmetanimina e de 60-75 amu para ciclopentadienil e ionização de ciclopentadienil (Fig. 4 b).
Os espectros FT-IR sugerem que –CH 3 os grupos se decompõem em –CH 2 - e que ligações C =N são formadas, enquanto outras reações de decomposição também ocorrem a ou acima de 250 ° C. A Figura 4 c mostra que as massas atribuídas a –CH 2 - (13, 14 e 15 amu) aumentam com o aumento da temperatura de aquecimento, enquanto as massas associadas com metano e ionização de metila (16, 17 e 18 amu) diminuem com o aumento da temperatura de aquecimento. Portanto, esses resultados confirmam que ambas as análises FT-IR e QMS fornecem resultados semelhantes em relação às reações de decomposição de CpZr vaporizado (NMe 2 ) 3 .
Os produtos de decomposição esperados que têm ligações C =N são metilmetilenoimina e N-etilmetanimina, que apareceriam em valores de massa de 22 e 28 amu, respectivamente. Os resultados da análise de QMS mostram que os picos de 21, 22 e 23 amu foram fracos ou ausentes, enquanto os picos de 27, 28 e 29 amu foram fortes e aumentaram em intensidade com o aumento da temperatura (Fig. 4 c). Esses resultados confirmam o mecanismo de decomposição sugerido pela análise FT-IR, na qual o ligante dimetilamido é decomposto para gerar diferentes produtos de decomposição dependendo da temperatura de aquecimento. Com base nos dados de análise, prevemos o mecanismo de decomposição principal de CpZr (NMe 2 ) 3 na fase gasosa (Fig. 5).
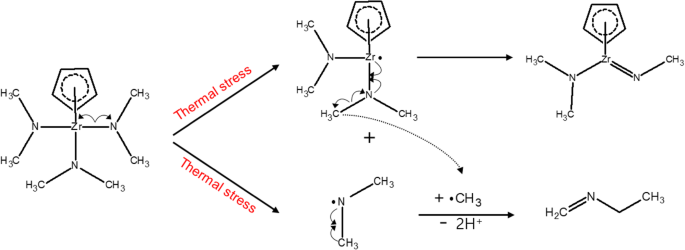
Os principais mecanismos de decomposição esperados de CpZr (NMe 2 ) 3 nas fases de gás
Quando CpZr (NMe 2 ) 3 é exposto a temperaturas de aquecimento abaixo de 250 ° C, tem dois mecanismos de decomposição diferentes. Metilmetilenoimina que pode deixar de reagir devido à energia térmica insuficiente e N-etilmetanimina são misturados a temperaturas de 100 ° C e abaixo, e N-etilmetanimina está presente apenas em temperaturas acima de 100 ° C. Quando CpZr (NMe 2 ) 3 é exposto a temperaturas de aquecimento de 250 ° C e acima, N-etilmetanimina e produtos de decomposição desconhecidos contendo CH 2 ligações são produzidas como produtos de decomposição.
Pode confirmar a partir da análise que quando CpZr (NMe 2 ) 3 é exposta ao estresse térmico, a metilmetilenoimina é gerada preferencialmente, a N-etilmetanimina é gerada por meio de reações adicionais e produtos de decomposição desconhecidos contendo CH 2 ligações são geradas quando expostas a energia térmica mais alta acima de 250 ° C. Portanto, podemos prever facilmente a metilmetilenoimina em temperaturas inferiores a 100 ° C e produtos de decomposição desconhecidos contendo CH 2 a ligação a temperaturas acima de 250 ° C existe como uma decomposição principal.
O mecanismo de decomposição térmica do CpZr vaporizado (NMe 2 ) 3 , que foi confirmado pelo uso de nossos sistemas de monitoramento in situ recentemente desenvolvidos, deve fornecer informações muito úteis para a otimização do processo ALD e o projeto de novos precursores. Além disso, tentamos sugerir esses mecanismos esperados, e mostrou que os sistemas de monitoramento in situ são úteis para entender o mecanismo de reação incluindo decomposição térmica na fase gasosa de vários materiais.
Conclusão
Este trabalho desenvolveu um sistema de monitoramento in situ usando FT-IR e QMS e aplicou esta nova técnica para avaliar a decomposição de CpZr vaporizado (NMe 2 ) 3 . A análise de FT-IR determinou que os ligantes de trimetilamina foram decompostos e que a dimetilamina foi formada por meio de uma reação de hidrogenação. Os dados também demonstram que –CH 2 - e os grupos C =N foram gerados por reações de eliminação conforme a temperatura aumentava. No entanto, a análise FT-IR in situ não foi capaz de confirmar qual produto possuindo ligações C =N foi obtido a partir da decomposição de ligantes de dimetilamido. Os dados de QMS demonstraram que a N-etilmetanimina foi produzida em uma extensão muito maior do que a metilmetilenoimina por meio da decomposição dos ligantes de dimetilamido conforme a temperatura aumentava.
Como resultado, estimamos o mecanismo de reação analisando os produtos de decomposição do CpZr vaporizado (NMe 2 ) 3 por estresse térmico usando FT-IR e confirmou que o produto de decomposição com grupos C =N é N-etilmetanimina usando análise de QMS. O mecanismo de decomposição térmica do CpZr vaporizado (NMe 2 ) 3 fornece informações muito úteis para a otimização do processo ALD e novo design de precursor.
Disponibilidade de dados e materiais
Todos os dados que sustentam as conclusões deste artigo estão incluídos no artigo.
Abreviações
- CpZr (NMe 2 ) 3 :
-
Ciclopentadienil Tris (dimetilamino) Zircônio
- FT-IR:
-
Espectroscopia de infravermelho com transformada de Fourier
- QMS:
-
Espectrometria de massa quadrupolo
- CVD:
-
Deposição de vapor químico
- ALD:
-
Deposição de camada atômica
- TGA:
-
Analisador termogravimétrico
- DSC:
-
Calorímetro diferencial de varredura
Nanomateriais
- Instrumentação de monitoramento de benzeno para as indústrias química, farmacêutica e petroquímica
- Tecnologias de Deposição de Camada Atômica Avançada para Micro-LEDs e VCSELs
- O rearranjo atômico de poços quânticos múltiplos baseados em GaN em gás misto H2 / NH3 para melhorar propriedades estruturais e ópticas
- Revelando a estrutura atômica e eletrônica das nanofibras de carbono de copo empilhado
- O Projeto da Camada de Emissão para Multiplicadores de Elétrons
- Características de chaveamento resistivo bipolar de dispositivos RRAM de estrutura tricamada de HfO2 / TiO2 / HfO2 em substratos revestidos com Pt e TiN fabricados por deposição de camada atômica
- Atendendo às necessidades industriais com a solução de monitoramento de gás alimentada por IoT
- Sensor de gás vestível para monitoramento de saúde e meio ambiente
- Freios, embreagens e materiais de fricção para a indústria de petróleo e gás
- Os desafios e oportunidades do “All Digital” para o Sistema de Gestão da Qualidade (SGQ)



