Otimização de nanoencapsulação em aglomerados de células semelhantes a ilhotas porcinas neonatais usando polimerssomas
Resumo
Pesquisas comprovando métodos para nanoencapsulação de grupos de células semelhantes a ilhotas porcinas neonatais (NPCCs) usando polimerssomas (PSomes) formados com polímeros de polietilenoglicol-bloco-poli lactídeo. Aqui, nossos estudos apresentam procedimento de nanoencapsulação eficiente com dano mínimo e perda de NPCCs. Usamos N-hidroxisuccinimida (NHS) no terminal N de PSomes para induzir a ligação de grupos amina na matriz extracelular em torno de NPCCs. O meio de cultura F-10 com albumina de soro bovino foi usado no procedimento de nanoencapsulação para minimizar danos e perda de NPCCs. Finalmente, induzimos a reticulação entre PSomes bifuncionais (NHS- / NH 2 -PSomes). O meio de cultura F-10 contendo 0,25% de BSA com pH de 7,3 minimizou o dano e a perda de NPCCs após a nanoencapsulação em comparação com o uso de tampão HBSS básico (pH 8,0). Além disso, induzimos a nanoencapsulação eficiente através da conjugação de PSomes usando PSomes bifuncionais (NHS- / NH 2 -PSomes).
Introdução
O uso do transplante de ilhotas alo no tratamento do diabetes tipo 1 é limitado devido à falta de doadores adequados. Em vez disso, há um aumento gradual no uso de ilhotas animais no transplante de xeno-ilhotas, com os porcos emergindo como espécies doadoras ideais [1]. Quando os porcos são usados como doadores durante o transplante, podem ser usadas ilhotas separadas, com base na idade dos porcos. Freqüentemente, aglomerados de células semelhantes a ilhotas porcinas neonatais (NPCCs) são preferidos em relação às ilhotas porcinas adultas (APIs) devido à sua acessibilidade e facilidade de isolamento. Além disso, os NPCCs podem proliferar gradualmente após o transplante, prolongando sua função in vivo [1, 2]. No entanto, quando NPCCs são transplantados em veias portais de primatas humanos ou não humanos (NHP), variações entre espécies podem causar reações imunológicas, como reação inflamatória instantânea mediada por sangue (IBMIR) ou rejeição hiperaguda, levando à perda precoce do enxerto [3]. Para resolver esse problema, o encapsulamento de NPCCs que podem inibir várias respostas imunes é necessário. Existem três tipos de encapsulamento:macro, micro e nano encapsulamento. A macroencapsulação usa um dispositivo contendo ilhotas, que é então implantado ao redor dos vasos sanguíneos para liberar insulina através de uma membrana semipermeável em resposta aos níveis de glicose no sangue. Micro-encapsulamento embala um pequeno número de ilhotas em uma cápsula porosa. Embora essas encapsulações possam proteger as ilhotas da rejeição imunológica, efeitos colaterais, como colapso da membrana ou geração de trombo, foram relatados em estudos in vivo. As ilhotas também perturbam o fluxo de hormônios, nutrientes ou oxigênio devido ao aumento da distância de difusão. A nanoencapsulação é a estratégia de modificação da superfície celular induzindo ligação entre as células e proteínas exógenas, principalmente o polietilenoglicol (PEG), na transfusão de sangue [4].
A nanoencapsulação usando PEG tem sido amplamente utilizada como um método de modificação para melhorar a eficácia e as propriedades físico-químicas de proteínas ou peptídeos alvo [5]. Em particular, a nanoencapsulação de ilhotas pode ter efeitos inibidores em resposta ao ataque de células imunes e reconhecimento de anticorpos. O PEG é amplamente utilizado para o revestimento de células por causa de suas propriedades biocompatíveis, como não imunogenicidade, mascaramento de antígeno e efeito não incrustante [6]. Entre as nanopartículas utilizadas para a nanoencapsulação de NPCCs, "polimersomos" (PSomes) baseados em PEG-bloco-poli lactídeo (PEG-b-PLA) são os mais adequados porque são estáveis e simples de modificar; eles também podem incorporar reagentes hidrofílicos e hidrofóbicos em sua montagem [7, 8]. A modificação da superfície das ilhotas usando polímeros (contendo PEG) é realizada através da ligação covalente ou não covalente entre a matriz extracelular (ECM) da ilhota e o polímero conjugado do grupo funcional [9].
Em estudos anteriores, uma solução salina balanceada de Hank básica (HBSS, pH 8,0) foi usada como tampão de reação de nanoencapsulação de ilhotas devido à sua capacidade de facilitar N-hidroxissuccinimida (NHS) -NH 2 ligação [10,11,12]. No entanto, para minimizar o dano celular aos NPCCs durante a nanoencapsulação, usamos o meio F-10 (meio de cultura NPCCs) com pH fisiológico (pH 7,3). Além disso, como preservar a quantidade de NPCCs após a nanoencapsulação é importante para o transplante da quantidade correta de células, adicionamos albumina de soro bovino (BSA), que reveste o fundo da placa de cultura de células com um polímero de cadeia longa, para aumentar a recuperação taxa [13]. Em nosso estudo anterior, a nanoencapsulação de NPCCs com PSomes foi realizada por meio de grupos funcionais únicos, como NHS ou NH 2 , que são usados para induzir ligação covalente ou interação eletrostática com ECM de NPCCs, respectivamente. No entanto, como a afinidade de ligação diminui ao longo do tempo, estratégias são necessárias para aumentar a eficiência de ligação [14]. PSome com grupos bifuncionais pode ser usado como candidato para aumentar a eficiência do revestimento devido à sua capacidade de agregar. Portanto, induzimos uma reticulação entre PSomes contendo grupos bifuncionais (NHS- / NH 2 -PSome) que pode se ligar não apenas ao ECM de NPCCs, mas também a cada PSome por meio de interação covalente ou interação eletrostática, aumentando assim a eficiência do nanoencapsulamento.
Neste estudo, investigamos a possível aplicação da nanoencapsulação em NPCCs por meio de método otimizado na área de xenotransplante de ilhotas suínas.
Materiais e métodos
Animais
Todos os experimentos com animais foram aprovados pelo Comitê Institucional de Uso e Cuidado de Animais do Instituto de MGENPLUS co. ltd. (# 2019-1), e todos os procedimentos foram realizados de acordo com as diretrizes estabelecidas pelo comitê. A cirurgia foi realizada sob anestesia geral e foram feitos esforços para garantir que os animais experimentassem o mínimo de dor. Os porcos foram mortos antes da pancreatectomia.
Isolamento de aglomerados de células semelhantes a ilhotas suínas neonatais (NPCCs)
NPCCs foram isolados de leitões de 3 a 5 dias de idade. Resumidamente, os leitões foram anestesiados com cetamina (10 mg / kg, Yuhan, Seul, Coréia) e cloridrato de xilazina (1 mg / kg, Rompun; Bayer Coréia, Seul, Coréia) injeção no músculo femoral e depois mortos por injeção de cloreto de potássio ( Sigma-Aldrich, MO, EUA) no coração. O pâncreas foi exposto por meio de uma incisão abdominal, colhido e imerso em solução salina balanceada de Hank (HBSS, Biosesang, Gyeonggi-do, Coreia) com bicarbonato de sódio 8,3 mM, N- (2-hidroxietil) piperazina-N ′ - 10 mM ( Ácido 2-etanossulfônico) (HEPES) (Sigma-Aldrich, MO, EUA) e 0,5% antibiótico-antimicótico (Biowest, MO, EUA). O pâncreas foi dividido em 1–2 mm 3 fragmentos e digerido em colagenase tipo V (1 mg / ml, Sigma-Aldrich, MO, EUA) em HBSS por 10 min. HBSS frio contendo 10% de soro fetal bovino (FBS) (Biowest, MO, EUA) foi adicionado ao tecido do pâncreas digerido para interromper a atividade da enzima. Os tecidos do pâncreas digeridos foram lavados em HBSS e, após ressuspensão, os tecidos foram filtrados em um pluriStrainer 500 μm (pluriSelect, Leipzig, Alemanha) e lavados em HBSS. Finalmente, NPCCs foram semeados e cultivados em 5% de CO 2 a 37 ° C em meio F-10 (Gibco, CA, EUA) suplementado com 0,25% de albumina de soro bovino (BSA) (genDepot, TX, EUA), nicotinamida 10 mM, D-glicose 10 mM, L-glutamina 2 mM, 2 mM de cloreto de cálcio di-hidratado, 50 μM de isobutilmetilxantina (IBMX), 20 μg / ml de ciprofloxacina (Sigma-Aldrich, MO, EUA) e 1% de antibiótico-antimicótico. NPCCs foram cultivados por 5 dias [15], com 10 nM de exendina-4 (Prospec, Ness-Ziona, Israel) sendo adicionado ao meio de cultura todos os dias.
Avaliação in vitro de NPCCs e NPCCs nanoencapsulados
Após a cultura, o número de NPCCs foi contado como equivalente de ilhotas (IEQ) usando o retículo da ocular na ocular. A viabilidade foi avaliada usando coloração com laranja de acridina (AO, 0,67 μM, Sigma-Aldrich, MO, EUA) e iodeto de propídio (PI, 75 μM, Sigma-Aldrich, MO, EUA). Para realizar o ensaio de secreção de insulina estimulada por glicose (GSIS), 20-30 NPCCs foram colhidos e pré-incubados com uma concentração baixa de D-glicose (2,8 mM) em tampão de bicarbonato de Krebs-Ringer (KRBB) por 1 h. NPCCs foram então incubados com baixo D-glicose (2,8 mM) em tampão KRBB por 1 h seguido por solução de alto D-glicose (28,0 mM) em KRBB por 1 h. Os sobrenadantes foram coletados para medir a secreção de insulina em baixas e altas concentrações de glicose [11]. A quantidade de insulina secretada de cada amostra foi medida usando um kit de ELISA para Human / Canine / Porcine Insulin Quantikine (R&D systems, MN, EUA). O índice de estimulação (SI) foi calculado dividindo as quantidades de insulina em altas concentrações de glicose (28,0 mM) por aquelas em baixas concentrações de glicose (2,8 mM).
Preparação de Polymersome (PSome)
Para preparar PSomes, copolímeros de N-hidroxissuccinimida-poli (etilenoglicol) -bloco-poli (lactida) (10 mg / ml, NHS-PEG-b-PLA) ou amina-poli (etilenoglicol) -bloco-poli (lactídeo ) copolímeros (10 mg / ml, NH 2 -PEG-b-PLA; Polímeros Nanosoft, NC, EUA) foram dissolvidos em 1 ml de dimetilsulfóxido (DMSO, Sigma-Aldrich, MO, EUA). Além de preparar PSome bifuncional, cada copolímero (NHS ou NH 2 -PEG-b-PLA) dissolvido em DMSO foi misturado em proporções. Água destilada (DH2O) foi adicionada à solução de polímero para perfazer uma concentração final de 1 mg / ml. A solução de polímero foi sonicada em um ultrasonicator (Sea han ultrasonic, Seul, Coréia) por 5 min. 1,1′-Dioctadecil-3,3,3 ′, 3′-tetrametilindodicarbocianina, sal 4-clorobenzenossulfonato (DiD; Biotium, CA, EUA) foi adicionado à solução de polímero durante a sonicação para permitir a visualização. Finalmente, a mistura foi dialisada em DH2O por 3 dias.
Nano-encapsulamento
O PSome foi diluído em tampão de reação de nanoencapsulação (ou HBSS (pH 7,3 ou pH 8,0) ou meio F-10 simples sem suplementos (pH 7,3 ou pH 8,0), com ou sem BSA 0,25%). A nanoencapsulação foi realizada adicionando o PSome a NPCCs em meios de cultura. Para fazer isso, 10.000 IEQs de NPCCs foram semeados em um prato de cultura de células de 6 poços (SPL, Gyeonggi-do, Coreia) e PSome diluído adicionado aos NPCCs e incubados em 5% de CO 2 a 37 ° C durante 1 h. Um grupo de controle negativo (NC) (NPCCs não revestidos sem PSomes) foi incubado nas mesmas condições do grupo experimental. Após a incubação, os NPCCs nanoencapsulados foram colhidos e cultivados em meio de cultura F-10.
Eficiência de NPCCs nanoencapsulados
Os NPCCs nanoencapsulados com PSome conjugados com DiD foram visualizados usando microscopia de fluorescência (Leica, Wetzlar, Alemanha) ou microscopia confocal de varredura a laser (CLSM; Carl Zeiss, Oberkochen, Alemanha). A intensidade de NPCCs ligados a PSome conjugados com DiD foi quantificada pelo cálculo da intensidade média de fluorescência (MFI) usando o software ImageJ (NIH, Bethesda, EUA). Os núcleos nas células foram contrastados com 4 ', 6-diamidino-2-fenilindol (DAPI).
Ensaio de Permeabilidade Polymersome
Os NPCCs NHS-PSome nanoencapsulados em F-10 ou F-10 (0,25% BSA) foram incubados com isotiocianato de fluoresceína (FITC) -conjugado dextrano de pesos moleculares variáveis (10, 20, 70 e 250 kDa) por 2 h . A penetração de dextrano conjugado com FITC em NPCCs NHS-PSome nanoencapsulados foi confirmada para cada peso molecular por meio de um microscópio de varredura a laser confocal.
Ensaio de viabilidade de células poliméricas
O NHS-PSome nanoencapsulado THP-1 (linha de células monocíticas humanas) em RPMI 1640 (Biowest, MO, EUA) foi incubado por 1 h. A viabilidade de NHS-PSome nanoencapsulado THP-1 foi medida de acordo com o protocolo apresentado no kit de ensaio de proliferação de células MTT (iNtRon Biotechnology, Seongnam- si, Korea).
Análise estatística
O teste t não pareado foi realizado no GraphPad Prism 6.0. A significância estatística foi expressa como *, ** *** e **** indicando o P valor de ≤ 0,05, ≤ 0,01, ≤ 0,001 e ≤ 0,0001.
Resultados
Avaliação cultural e funcional de NPCCs
NPCCs foram cultivados por 5 dias, e controles de qualidade, incluindo viabilidade e GSIS, foram realizados. O número total de NPCCs foi 21.014,0 IEQ / g / pâncreas. A viabilidade, pela coloração AO / PI, foi de 89,9%. GSIS, que foi realizado para confirmar a responsividade dos NPCCs à concentração de glicose, deu um índice de estimulação médio (SI) de 2,3 (Tabela 1, Arquivo adicional 1:Fig. S1).
Concentração PSome necessária para nanoencapsulamento eficiente de NPCCs
Para determinar a concentração de PSome necessária para nanoencapsulação eficiente, adicionamos concentrações variáveis de NHS-PSome aos NPCCs. NHS-PSome foi estocado a uma concentração de 1 mg / ml em DH 2 O e diluída a 1:5, 1:10, 1:20 e 1:40 para dar concentrações finais variando de 0,2 a 0,025 mg / ml. A eficiência da nanoencapsulação foi medida por MFI de NPCCs nanoencapsulados PSome carregados com DiD. A concentração final de 0,1 mg / ml (diluição 1:10) mostrou a maior intensidade de fluorescência 2 dias após a nanoencapsulação (Fig. 1a e b) e a subsequente nanoencapsulação de NPCCs foi conduzida nesta concentração.
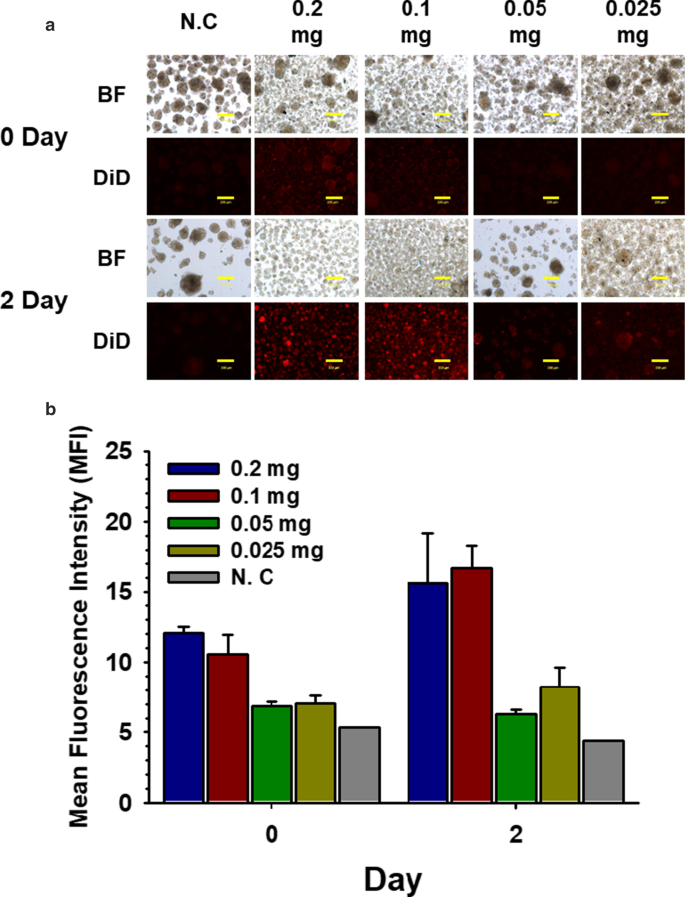
Otimização da concentração de PSome para nanoencapsulação efetiva em 0 e 2 dias. Otimização da concentração de PSome para nanoencapsulação eficaz. a NHS-PSome carregado com DiD foi tratado em NPCCs em várias concentrações (BF; campo claro). As barras de escala representam 200 μm. b MFI de NPCCs nanoencapsulados com PSome carregados com DiD ( n =3) e controle NC ( n =1)
Eficiência aprimorada de nanoencapsulação em mídia F-10 com pH fisiológico
A nanoencapsulação de ilhotas pancreáticas (contendo NPCCs) é frequentemente realizada em tampão HBSS básico (pH 8,0 ou superior) para aumentar a afinidade de ligação entre NH2 em ECM de ilhotas e NHS conjugado em polímero. No entanto, a nanoencapsulação em buffer HBSS básico pode potencialmente danificar NPCCs. Assim, para minimizar o dano de NPCCs e determinar o efeito do pH no NHS-NH 2 ligação, NPCCs foram nanoencapsulados através de NHS-PSome em tampões HBSS ou meio de cultura F-10 simples (usado neste estudo para cultivar NPCCs) com pH 7,3 (fisiológico) ou pH 8,0 (básico), respectivamente. Quando os NPCCs foram nanoencapsulados em F-10, a morfologia normal dos NPCCs foi mantida (Fig. 2a), e a eficiência do nanoencapsulamento com base em MFI foi significativamente aumentada em comparação com o grupo HBSS, independentemente do pH nos dias 0 e 6 (Fig. 2b). Embora os grupos HBSS tenham mostrado diferença significativa entre pH 7,3 e 8,0 no dia 6, a intensidade da nanoencapsulação foi significativamente reduzida em comparação com o grupo F-10. Assim, usamos meio de cultura F-10 fisiológico (pH 7,3) como o tampão de reação de nanoencapsulação em experimentos subsequentes para minimizar o dano potencial de NPCCs.
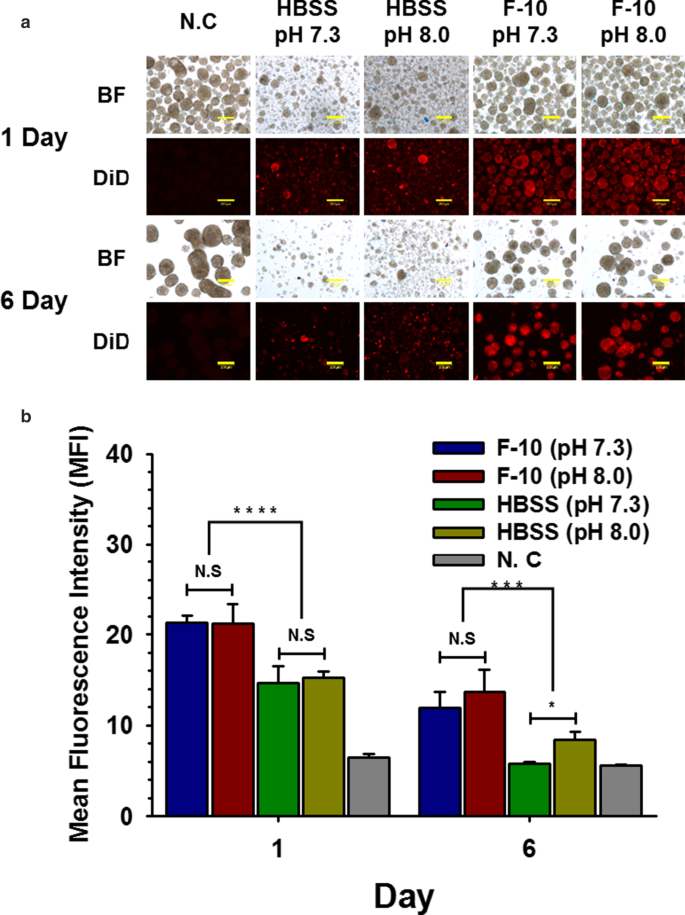
Comparações de eficiência de revestimento de nanoencapsulação em vários buffers de reação em 1 e 6 dias. Comparações de eficiência de revestimento de nanoencapsulação em vários buffers de reação. a NPCCs nanoencapsulados em HBSS (pH 7,3 e pH 8,0) ou F-10 (pH 7,3 e pH 8,0) usando NHS-PSome conjugado com DiD (BF; campo claro). As barras de escala representam 200 um; b MFI de NPCCs nanoencapsulados em HBSS (pH 7,3 e pH 8,0) ou F-10 (pH 7,3 e pH 8,0) usando NHS-PSome conjugado com DiD (todos os grupos; n =3). Os dados representam a média ± D.P. * p <0,05, *** p <0,001 e **** p <0,0001 versus outros grupos
Taxa de recuperação aumentada de NPCCs após nanoencapsulamento
Embora o dano celular de NPCCs tenha sido minimizado em F-10, a quantidade de NPCCs coletada após a nanoencapsulação foi significativamente reduzida. Para resolver este problema, adicionamos 0,25% de BSA ao meio F-10 durante a cultura e a nanoencapsulação de NPCCs usando NHS-PSome. Confirmamos inicialmente se a adição de 0,25% de BSA ao meio F-10 afeta a eficiência do revestimento e a permeabilidade seletiva, permitindo a passagem de pequenas moléculas (10 e 20 kDa de dextrano conjugado com FITC) enquanto bloqueia moléculas maiores (70 e 250 kDa conjugado com FITC dextran), como uma função essencial de PSome. Como resultado, o revestimento conformado foi mostrado em imagens de CLSM (Fig. 3a, Mid) e a permeabilidade seletiva foi mantida normalmente (Fig. 3b, dextrano conjugado com FITC) em NHS-PSome NPCCs nanoencapsulados com F-10 contendo 0,25 % BSA em comparação com F-10, embora a MFI tenha sido ligeiramente reduzida (Fig. 3b). As quantidades de NPCCs coletadas após nanoencapsulamento mostraram taxa de recuperação significativamente maior (71,9%) em F-10 com BSA de 0,25% do que em F-10 sem BSA (42,3%) (Fig. 3c). A viabilidade (NC:89,5%, NHS-PSome:90,3%) e secreção de insulina estimulada por glicose (NC:2,1, NHS-PSome:1,6) de NPCCs em F-10 com 0,25% BSA também foram mantidas após nanoencapsulação (Fig. . 4a, b, Arquivo adicional 1:Fig. S2). Nossos resultados indicam que a adição de 0,25% de BSA pode aumentar significativamente a taxa de recuperação de NPCCs após nanoencapsulação e não afetou a eficiência de revestimento ou função de PSome.
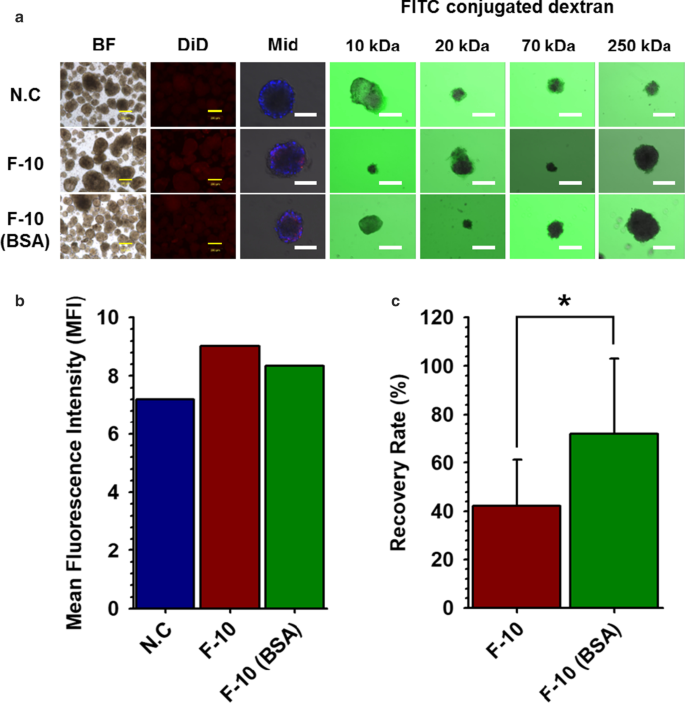
Comparações de eficiência de revestimento após adição de 0,25% de BSA em buffers de reação de nanoencapsulação para aumentar a taxa de recuperação. Comparações de eficiência de revestimento após adição de 0,25% de BSA em buffers de reação de nanoencapsulação para aumentar a taxa de recuperação. a Eficiência de revestimento e permeabilidade seletiva de NPCCs nanoencapsulados com NHS-PSome em F-10 ou F-10 com BSA de 0,25% (BF; campo claro, Mid; imagem do meio usando CLSM de NPCCs NHS-PSome nanoencapsulados conjugados com DiD, Dextrano conjugado com FITC; imagem do meio usando CLSM de dextrano conjugado com FITC em NPCCs NHS-PSome nanoencapsulados). Blue in Mid representam a célula por meio de coloração DAPI. As barras de escala são 200 (BF e DiD) e 100 (dextrano conjugado com Mid e FITC) μm; b MFI de NPCCs nanoencapsulados usando NHS-PSome conjugado com DiD; c Taxa de recuperação de NPCCs após nanoencapsulamento em F-10 ( n =12) ou F-10 com 0,25% BSA ( n =12). Os dados representam a média ± D.P. * p <0,05 versus F-10
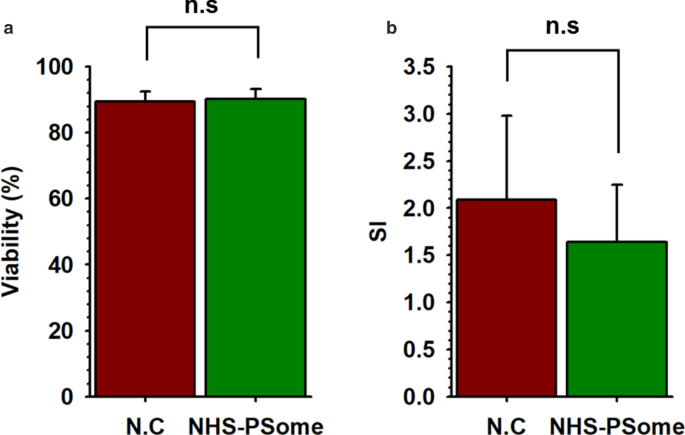
Viabilidade e funcionalidade de NPCCs NHS-PSome nanoencapsulados usando F-10 com 0,25% de BSA. Viabilidade e funcionalidade de NPCCs NHS-PSome nanoencapsulados usando F-10 com 0,25% de BSA. a Viabilidade de NPCCs NHS-PSome nanoencapsulados ( n =6) e controle NC ( n =6); b SI de NHS-PSome NPCCs nanoencapsulados ( n =5) e controle NC ( n =5). Os dados representam a média ± D.P.
Estabilidade aprimorada de nanoencapsulamento por meio de PSomes de cross-linking
Para induzir uma nanoencapsulação mais estável de NPCCs, tentamos conjugar PSomes com dois grupos funcionais diferentes. Primeiro, conduzimos o nanoencapsulamento dos NPCCs adicionando simultaneamente diferentes proporções de PSomes contendo NHS e NH 2 grupos bifuncionais (NHS- / NH 2 -PSome) em um PSome (Esquema 1). A eficiência da nanoencapsulação foi confirmada pelo MFI de DiD conjugado em PSome nanoencapsulado NPCCs. As imagens resultantes da microscopia de fluorescência não mostraram diferenças significativas entre os grupos 9:1, 5:5 e 1:9 de NHS- / NH2-PSome nanoencapsulados NPCCs (9:1, 5:5, 1:9) no dia 0 e dia (Fig. 5a). No entanto, nos resultados CLSM, o grupo 5:5 parecia estar revestido e 1:9 apresentava revestimento insuficiente, enquanto o grupo 9:1 formava um revestimento conformado, no dia 1 (Fig. 5b). Portanto, determinamos a proporção ideal de NHS- / NH2 em PSome como sendo 9:1. Quando os ensaios funcionais foram realizados para o grupo 9:1, nossos resultados mostraram que a viabilidade do grupo 9:1 foi significativamente diminuída quando comparada com a do controle NC (92,1%), mas a viabilidade foi mantida em níveis normais (87,8 %). A função SI do grupo 9:1 era normal (3,0) quando comparada com a do controle NC (3,7) (fig. 5c, d).
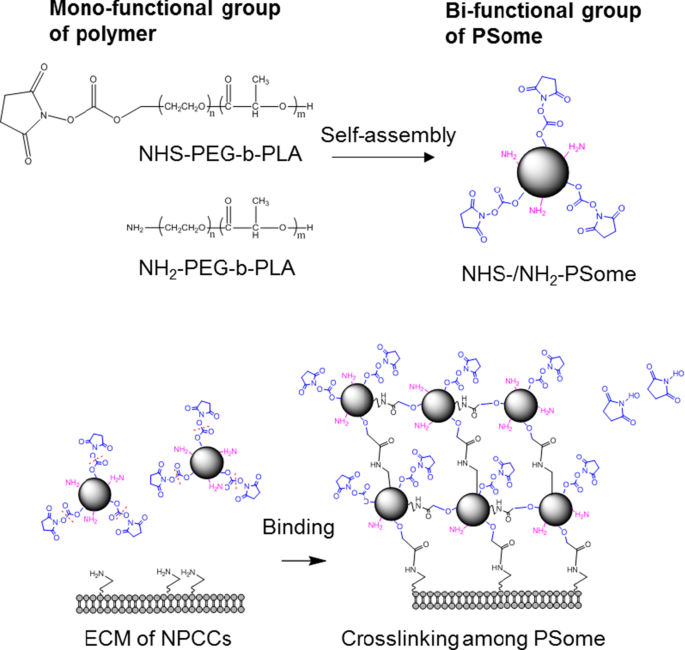
A ilustração de estabilidade melhorada de nanoencapsulação por reticulação de PSomes
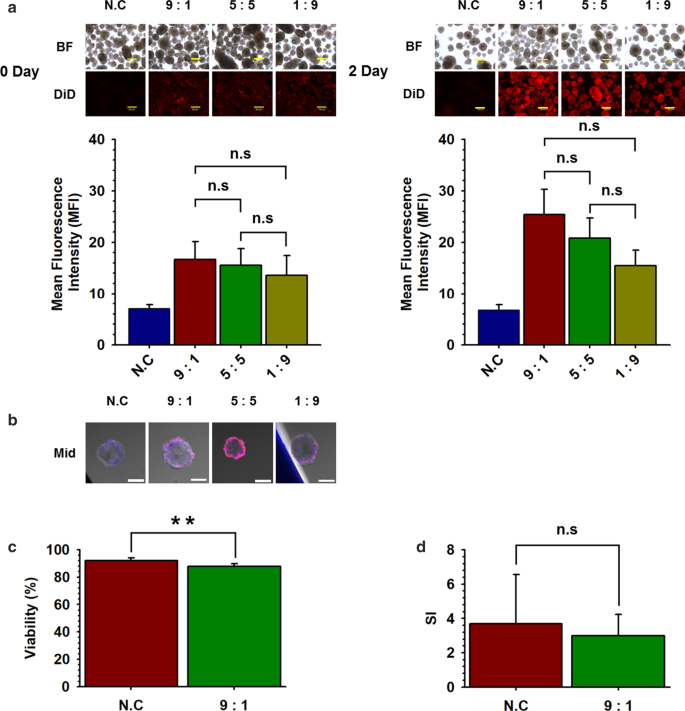
Eficiência de revestimento e funcionalidade do NHS- / NH 2 - Alguns NPCCs nanoencapsulados. Eficiência de revestimento e funcionalidade do NHS- / NH 2 - Alguns NPCCs nanoencapsulados. a DiD conjugado 9:1, 5:5, 1:9 de NHS- / NH 2 -PSome NPCCs nanoencapsulados (9:1, 5:5, 1:9) (NC; NPCCs não revestidos). MFI mostra a intensidade de NPCCs nanoencapsulados com PSome conjugados com DiD ( n =3) e controle NC ( n =3). As barras de escala representam 200 um; b CLSM de NHS- / NH conjugado com DiD 2 -PSome NPCCs nanoencapsulados (imagem intermediária usando CLSM de NHS- / NH conjugado com DiD 2 -PSome nano-NPCCs encapsulados). Blue in Mid representam a célula através da coloração DAPI. As barras de escala representam 100 um; C. Viabilidade de 9:1 ( n =9) e controle NC ( n =3). Os dados representam a média ± D.P. ** p <0,01 versus NC; D. SI de 9:1 ( n =9) e controle NC ( n =3). Os dados representam a média ± D.P.
Discussão
O diabetes mellitus, comumente conhecido como diabetes, é uma doença metabólica caracterizada por níveis elevados de glicose no sangue. O diabetes tipo 1 resulta da falha das células beta do pâncreas em produzir insulina suficiente [16]. O transplante de ilhotas pancreáticas contendo células β produtoras de insulina foi recentemente usado para curar o diabetes tipo 1. No entanto, o transplante de ilhotas é limitado devido à escassez de doadores; em vez disso, o xenotransplante usando ilhotas de animais não humanos surgiu como uma fonte alternativa de tecido de doador. Devido às suas semelhanças fisiológicas com os humanos, facilidade de criação em massa e disponibilidade de criação em instalações livres de patógenos, os porcos são considerados um modelo animal ideal para o transplante de xeno-ilhotas [1]. Especialmente, os NPCCs foram usados de maneira tão valiosa quanto os APIs. Embora a maturidade dos NPCCs seja inferior à dos APIs, os NPCCs têm algumas vantagens sobre os APIs, incluindo, um procedimento de isolamento de ilhotas relativamente simples e barato, capacidade de desenvolver resistência a ambientes hipóxicos e proliferação in vivo após o transplante [1,2,3] . Por essas razões, usamos porcos neonatais de 3 a 5 dias de idade como a fonte de ilhotas neste estudo.
Infelizmente, uma vez que ilhotas de porco são implantadas em vasos sanguíneos de primatas humanos ou não humanos, muitas vezes ocorrem reações imunológicas graves, como IBMIR ou rejeição hiperaguda. IBMIR geralmente ocorre devido a vários fatores de tecido (FT) expressos em ilhotas de porco que medeiam a coagulação em vasos sanguíneos humanos por meio da ativação de uma via extrínseca. Antígenos alfa-galactose ou não-gal expressos na superfície de células de porco também podem ser alvos de anticorpos humanos naturais, seguidos por uma ativação em cascata complementar chamada rejeição hiperaguda. Como resultado, os enxertos são perdidos após a hipóxia pela formação de coágulos a partir da via de coagulação e morte celular pela ativação do complemento no hospedeiro [3]. Para resolver esses problemas, o encapsulamento, um método de revestimento de ilhotas pancreáticas com materiais biocompatíveis para protegê-los contra o ataque de anticorpos ou reações do complemento, foi tentado. Primeiro, o macro-encapsulamento usa um dispositivo com uma membrana semipermeável contendo a ilhota e é implantado próximo aos vasos sanguíneos onde libera insulina na corrente sanguínea em resposta aos níveis de glicose no sangue [4]. Em segundo lugar, a microencapsulação, principalmente usando alginato, tem permeabilidade seletiva e pode permitir que oxigênio e nutrientes passem por sua superfície porosa, enquanto bloqueia múltiplas citocinas e a infiltração de células imunes. No entanto, porque eles usam o mesmo tamanho de cápsulas, independentemente do tamanho das ilhotas, é difícil revestir as ilhotas de forma conformada. Além disso, pode ocorrer fibrose, envolvendo o enxerto após o transplante [17]. Por último, a modificação da superfície das ilhotas (nanoencapsulação) usa principalmente polietilenoglicol (PEG) que tem propriedade de "efeito furtivo" que bloqueia a interação de materiais revestidos com polímero "furtivo" (PEG) e componentes no sangue (células imunes) em vivo [11, 18]. Nossa estratégia de nanoencapsulação NPCCs usa os copolímeros PEG modificados (PEG-b-PLA, Polymersome, PSome). Além disso, o Psome tem propriedades hidrofílicas e hidrofóbicas e pode incorporar imunossupressores ou fatores envolvidos na diferenciação ou crescimento celular [8].
A nanoencapsulação de ilhotas usando PEG foi realizada em tampão HBSS básico (pH 8,0 ou superior) para aumentar a afinidade de ligação entre NHS em PEG e NH 2 na ECM da ilhota [10,11,12]. No entanto, uma vez que essas condições não podem fornecer um ambiente de cultura de células adequado, tentamos a nanoencapsulação em um ambiente que imita a condição de cultura de NPCC. Para resolver os problemas acima, testamos mídia F-10 simples, meio de cultura base de NPCCs, com pH fisiológico (sem quaisquer suplementos) usado como o tampão de reação de nanoencapsulação. A nanoencapsulação em F-10 com pH fisiológico mostrou uma eficiência de revestimento semelhante e manteve a morfologia normal de NPCCs quando comparada com a condição de cultura usando tampão HBSS básico (Fig. 3). Portanto, podemos propor uma plataforma que minimiza os danos de NPCC durante a nanoencapsulação em um ambiente de simulação de cultura de NPCC.
Embora o método de nanoencapsulamento para minimizar os danos de NPCC tenha sido estabelecido, a quantidade residual de NPCCs coletados após o nanoencapsulamento diminuiu quando o nanoencapsulamento foi realizado em placas de Petri. Isso significa que você precisa de mais NPCCs para nanoencapsulamento para transplante. De acordo com relatórios anteriores, o rendimento das ilhotas foi melhorado em algumas linhagens de camundongos usando BSA durante o isolamento [19]. Além disso, o BSA foi usado como uma cultura em suspensão por pré-revestimento da superfície das placas de cultura de células em culturas de células de hepatoma de rato [13]. Portanto, para aumentar a quantidade de NPCCs após a nanoencapsulação, 0,25% de BSA foi adicionado ao tampão de reação de nanoencapsulação F-10, igual à concentração de BSA usada para a cultura de NPCCs. Como resultado, a taxa de recuperação de NPCC aumentou significativamente após nanoencapsulamento (Fig. 4). Isso significa que o número correto de ilhotas (contendo NPCCs) após a nanoencapsulação pode ser previsto e transplantado, minimizando a perda de ilhotas (contendo NPCCs). Em resumo, este estudo usando F-10 com 0,25% de BSA para nanoencapsulação mostrou que (i) a morfologia normal de NPCCs foi mantida, (ii) a ligação entre PSome conjugado com NHS e NH2 em ECM de NPCCs não foi interferida e (iii) a taxa de recuperação de NPCCs após nano-encapsulamento aumentou.
Finalmente, tentamos aumentar a estabilidade da nanoencapsulação através de (i) conjugação entre PSomes e (ii) ligação entre PSomes e ECM de NPCCs. Primeiro, os polímeros NHS- e NH2-PEG-b-PLA foram misturados proporcionalmente para formar o PSome bifuncional (NHS- / NH2-PSome) que pode se ligar a PSome e ECM de NPCCs. Postulamos que a conjugação poderia ser eficientemente alcançada por grupos bifuncionais dentro de um PSome em vez de conjugar dois PSomes com grupos monofuncionais devido à interrupção potencial causada pela ligação entre PSomes com o mesmo grupo funcional (NHS-NHS e NH2-NH2). Como visto a partir dos resultados, o revestimento conformal de NPCCs foi alcançado em uma proporção de 9:1 de NHS- / NH2-PSome nanoencapsulado NPCCs, e a viabilidade e funcionalidade foram mantidas (Fig. 5). No entanto, mais estudos são necessários para quantificar a força da ligação PSome, para provar que a nanoencapsulação com PSome bifuncional resultou em um encapsulamento mais estável do que com o PSome mono-funcional. Portanto, sugerimos que nossas condições de nanoencapsulação eficazes que imitam o ambiente de cultura NPCC podem ser usadas na estratégia de nanoencapsulação usando ilhotas contendo NPCCs (arquivo adicional 1).
Conclusão
Este estudo foi conduzido para determinar um método ideal de nanoencapsulação de ilhotas pancreáticas (NPCCs) usando polimerssomas baseados em PEG (PSomes). Em primeiro lugar, o uso de meio de cultura F-10 com pH de 7,3 pode manter a morfologia normal de NPCCs após a nanoencapsulação em comparação com o uso de tampão HBSS básico (pH 8,0), minimizando assim os danos aos NPCCs durante o encapsulamento. Em segundo lugar, a adição de 0,25% de BSA ao meio F-10 melhorou o rendimento de NPCCs em aproximadamente 1,7 vezes após a nanoencapsulação. Finalmente, induzimos uma nanoencapsulação mais estável através da conjugação de PSomes bifuncionais (NHS- / NH2-PSomes). Os métodos de nanoencapsulação apresentados neste artigo podem ser aplicáveis na nanoencapsulação de ilhotas pancreáticas usando nanopartículas à base de PEG.
Disponibilidade de dados e materiais
Não aplicável.
Abreviações
- DiD:
-
1,1′-Dioctadecyl-3,3,3′,3′-tetramethylindodicarbocyanine, 4-chlorobenzenesulfonate salt
- AO:
-
Acridine orange
- APIs:
-
Adult porcine islets
- BSA:
-
Albumina sérica bovina
- BF:
-
Campo brilhante
- CLSM:
-
Confocal laser scanning microscopy
- DAPI:
-
4′,6-Diamidino-2- phenylindole
- DMSO:
-
Dimetilsulfóxido
- DH2O:
-
Água destilada
- ELISA:
-
Ensaio de imunoabsorção enzimática
- FBS:
-
Soro fetal bovino
- FITC:
-
Fluorescein isothiocyanate
- GSIS:
-
Glucose-stimulated insulin secretion
- HBSS:
-
Hank’s balanced salt solution
- IBMIR:
-
Instant blood-mediated inflammatory reaction
- IEQ:
-
Islet equivalent
- IBMX:
-
Isobutylmethylxanthine
- KRBB:
-
Krebs–Ringer bicarbonate buffer
- MFI:
-
Mean fluorescence intensity
- HEPES:
-
N-(2-Hydroxyethyl)piperazine-N′-(2-ethanesulfonic acid)
- NC:
-
Negative control
- NPCCs:
-
Neonatal porcine islet like cell clusters
- NHS:
-
N-hydroxysuccinimide
- NHP:
-
Non-human primate
- PLA:
-
Poly lactide
- PEG:
-
Polietileno glicol
- PSomes:
-
Polymersomes
- PI:
-
Propidium iodide
- SI:
-
Stimulation index
- TF:
-
Tissue factor
Nanomateriais
- C# usando
- Avançando para 7nm
- Usando ângulos para melhorar o futuro da eletrônica
- Concreto inteligente usando nanopartículas
- Otimização de Filme Fino Altamente Refletivo para Micro-LEDs de Ângulo Total
- Fabricação de alto rendimento de nanofibras de qualidade usando eletrofiação de superfície livre modificada
- A otimização da programação de DRAM 1T sem capacitor baseada no TFET de porta dupla
- Efeito catalítico de aglomerados de Pd na combustão de poli (N-vinil-2-pirrolidona)
- Sondando as propriedades estruturais, eletrônicas e magnéticas dos aglomerados Ag n V (n =1–12)
- Otimização de células solares GaAs Nanowire Pin Junction Array usando Heterojunções AlGaAs / GaAs



