Nanoestruturas de MgO dopadas com óxido de grafeno para degradação de corante altamente eficiente e ação bactericida
Resumo
Várias concentrações (0,01, 0,03 e 0,05 em peso) de nanofolhas de óxido de grafeno (GO) foram dopadas em nanoestruturas de óxido de magnésio (MgO) usando a técnica de precipitação química. O objetivo foi estudar o efeito das concentrações do dopante GO sobre o comportamento catalítico e antibacteriano de quantidade fixa de MgO. A técnica de XRD revelou fase cúbica de MgO, enquanto sua natureza cristalina foi confirmada por meio de perfis SAED. Presença de grupos funcionais e Mg-O (443 cm −1 ) na região da impressão digital foi evidente com espectroscopia FTIR. As propriedades ópticas foram registradas via espectroscopia UV-visível com redshift apontando para uma diminuição na energia do gap de 5,0 para 4,8 eV após dopagem. O comportamento da recombinação elétron-buraco foi examinado por espectroscopia de fotoluminescência (PL). Os espectros Raman exibiram banda D (1338 cm −1 ) e banda G (1598 cm −1 ) evidente para o doping GO. A formação da nanoestrutura com morfologia cúbica e hexagonal foi confirmada com TEM, enquanto o espaçamento d médio entre camadas de 0,23 nm foi avaliado usando HR-TEM. A existência de dopantes e a avaliação da constituição elementar Mg, O foram corroboradas pela técnica de EDS. A atividade catalítica contra o azul de metila ciprofloxacina (MBCF) foi significativamente reduzida (45%) para maior concentração de dopante GO (0,05), enquanto a atividade bactericida do MgO contra E. coli foi melhorado significativamente (zona de inibição de 4,85 mm) após dopagem com maior concentração (0,05) de GO, devido à formação de nanobastões.
Introdução
A água é o componente mais essencial para a sobrevivência das criaturas vivas. A industrialização em grande escala e o aumento do aquecimento global com o passar do tempo estão diminuindo o nível de água potável rapidamente. A superfície da Terra é coberta por 71% da água, onde rios, lagos e água doce subterrânea representam apenas 0,03% da água total, que é considerada útil para beber [1, 2]. 2,5% da água é digna de consumo, enquanto o restante dos 97,5% é água salgada; portanto, o abastecimento de água doce é escasso em relação às altas demandas. Aproximadamente, 750 milhões de habitantes da Terra estão enfrentando escassez de água limpa e um número crescente de micropoluentes na água se tornou perigoso para o ecossistema. O mundo está enfrentando consequências catastróficas causadas pela poluição ambiental e da água. As indústrias são a principal fonte de poluição da água devido à descarga de águas residuais injetadas com compostos nocivos e potencialmente tóxicos. Diferentes indústrias, como têxtil, impressão em papel e indústria alimentícia, usam compostos aromáticos que podem se dissolver facilmente na água, causando poluição da água e riscos à saúde [3]. A rápida industrialização e urbanização causaram poluição ambiental significativa por meio de metais pesados que são persistentes no meio ambiente. A exposição adversa a metais pesados no meio ambiente é um sério risco para os seres vivos [4]. De acordo com a OMS, os limites máximos admissíveis de metais na água são, por exemplo, ferro (0,1 mg / L), cálcio (75 mg / L), magnésio (50 mg / L), cobre (1 mg / L) e chumbo ( 0,05 mg / L). O perfil de toxicidade de metais pesados relatado pela USEPA inclui chumbo (dano / fatal ao cérebro), cádmio (dano renal) e cromo (problemas do trato respiratório) [5]. Os corantes tóxicos estão colocando em risco vidas aquáticas, bloqueando a luz solar, que é necessária para o crescimento dos organismos vivos. As espécies aquáticas consomem esses corantes venenosos, enquanto essas espécies, por sua vez, são consumidas por pessoas, prejudicando sua saúde [6].
Várias abordagens tradicionais para a extração de corantes de águas residuais foram sugeridas, incluindo evaporação [7], extração de solvente [8], coagulação [9], troca iônica [10], separação por membrana [11], técnicas físicas, químicas e biológicas [12] ] O grande problema é que essas técnicas convencionais de tratamento são caras quando atingem o nível de larga escala. Diante disso, os pesquisadores desenvolveram vários adsorventes como zeólita, carvão ativado, nanotubos de carbono, polímeros e materiais de grafeno. O método de adsorção é amplamente utilizado no tratamento de águas residuais para degradar os corantes reativos [13,14,15,16,17]. Um tratamento adequado dos corantes, como adsorção e degradação catalítica são propostos para a remoção dos corantes para melhorar a qualidade de vida. A adsorção é econômica, mas a recuperação do catalisador ainda é um problema que pode produzir materiais perigosos. A degradação catalítica é ligeiramente cara; no entanto, é relativamente simples e tem a vantagem de ser reciclável [18]. Numerosos semicondutores de óxido (TiO 2 , ZnO, MgO, Fe 2 O 3 e WO 3 ) foram amplamente relatados como catalisadores para a degradação de corantes orgânicos devido à sua alta estabilidade química, natureza livre de tóxicos, alta atividade e custo-benefício.
Entre estes, o MgO atóxico e de baixo custo tem se mostrado eficaz nas áreas de adsorção, catálise para água poluída, produtos supercondutores e materiais antibacterianos [19,20,21]. Nos últimos anos, várias nanoestruturas de MgO, contendo nanopartículas, nanoflores e nanofolhas foram fabricadas com sucesso [22]. Recentemente, o MgO com um grande gap de banda de 7,8 eV revelou muito interesse por causa de propriedades únicas:ópticas, eletrônicas e magnéticas [23]. É amplamente reconhecido que defeitos pontuais em cristais, como lacunas de oxigênio [ V o (ou seja, F + -tipo centro, F + centro, ou F c )] pode alterar a eficiência do material em sólidos de MgO desencapados [24]. Além disso, o MgO tem densidade inferior em comparação com outros óxidos de metal, incluindo óxido cúprico, óxido de zinco e óxido de ferro [25]. MgO é um óxido de metal alcalino-terroso com um alto pH de carga zero [26], área de superfície ∼250-300 m 2 / g [27] e potencial zeta de cerca de -29,89 mV [28]. A pesquisa descobriu que o tamanho da partícula e a área de superfície específica são fatores cruciais que afetam o desempenho de adsorção. Conseqüentemente, as propriedades de superfície dos produtos resultantes são significativamente afetadas pela temperatura de calcinação durante a síntese [29,30,31,32,33]. O MgO não tóxico possui aplicações orgânicas aprimoradas como um agente antibacteriano para o alívio da azia e regeneração óssea em comparação com outros compostos de Mg, conforme confirmado pela U.S. Food and Drug Administration (21CFR184.1431) [34,35,36].
Na última década, folhas espessas de óxido de grafeno (GO) material à base de carbono foram extensivamente estudadas para diferentes aplicações [37]. Nanomateriais bidimensionais GO demonstram grande mobilidade de elétrons, forte estabilidade química, ampla área de superfície e alta condutividade térmica [38, 39]. O derivado químico do grafeno é GO possuindo área de superfície de cerca de 736,6 m 2 / g (teórico) [40] e valor potencial zeta de - 113,77 mV [41] contendo grupos epóxido, carboxílico e hidroxila. Esses grupos funcionais resultam em uma carga negativa e hidrofilicidade e produzem prontamente a dispersão de GO em solução aquosa para construir uma suspensão estável [42, 43].
Além disso, vários estudos investigaram a degradação do corante têxtil para MgO, onde o MgO foi preparado por decomposição térmica e usado para a degradação do azul de metileno. 90% deste corante degradou após 180 min [44]. Além disso, o MgO foi preparado por meio de um método sol-gel com tamanho de partícula de 15-25 nm, para eliminação de 98,3% do corante em águas residuais após 300 min [45]. O objetivo deste estudo é verificar a influência do dopante GO no MgO, para o qual vários pesos as proporções (0, 0,01, 0,03 e 0,05) de GO foram dopadas em MgO usando o método de precipitação química. Foram estudados os efeitos do dopante GO em diferentes características do MgO, tais como composição estrutural, morfológica e química na catálise e ação antibacteriana. Por outro lado, a motivação por trás do uso desses nanocompósitos é explorar o uso significativo de nanomateriais plasmônicos para aumentar a atividade antimicrobiana e também catalítica de óxidos metálicos.
Seção Experimental
Materiais
Cloreto de magnésio (MgCl 2 · 6H 2 O, 99%), nitrato de sódio (NaNO 3 , 98%) e hidróxido de sódio (NaOH, 98%) foram adquiridos da Sigma Aldrich. Pó de grafite (99,5%), ácido sulfúrico (H 2 SO 4 ) e permanganato de potássio (KMnO 4 , 99,5%) foram adquiridos da Analar.
Síntese de óxido de magnésio e óxido de grafeno
Seguindo a estratégia de co-precipitação química úmida, MgO dopado com GO foi preparado. O método Hummer modificado [46] foi usado na preparação do GO. Para preparar MgO, quantidade desejada de MgCl 2 · 6H 2 O (0,5 M) foram agitados em 50 mL de água desionizada (água DI) na placa quente. O pH da solução agitada foi mantido a 12 usando NaOH (0,1 M), que foi agitado durante 4 h a 80 ° C. A solução agitada foi centrifugada a 3500 rpm por 15 min subsequentemente; o sobrenadante foi recolhido e seco a 120 ° C durante 24 h na estufa. O pó coletado foi moído usando almofariz e pilão para obter pós finos de MgO não dopado e GO (0,01, 0,03 e 0,05) dopado. O diagrama esquemático da preparação de MgO dopado com GO é mostrado na Fig. 1.
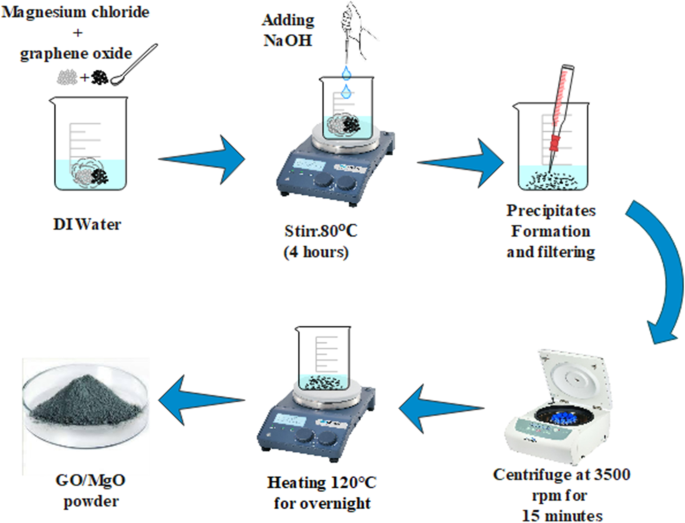
Diagrama esquemático do esquema de síntese de nanoestruturas de MgO dopadas com GO
Catálise
A atividade catalítica de nanoestruturas de MgO dopadas com GO foi testada contra 3 mL de MBCF (azul de metila ciprofloxacina) misturado em 400 μL de NaBH recém-preparado 4 (agente redutor). NaOH e H 2 SO 4 (400 μL) foram adicionados para obter a natureza básica e ácida da solução, respectivamente. Em seguida, 400 μL de MgO dopado foram adicionados à solução à base de agente redutor. Mais tarde, a cor azul do corante preparado (MBCF) começou a desmaiar, indicando a degradação do corante do MBCF em Leuco-MBCF (incolor). As amostras recebidas da solução desmaiada em vários intervalos foram capturadas com espectrofotômetro UV-Vis na faixa de 200-800 nm, conforme mostrado na Fig. 2.
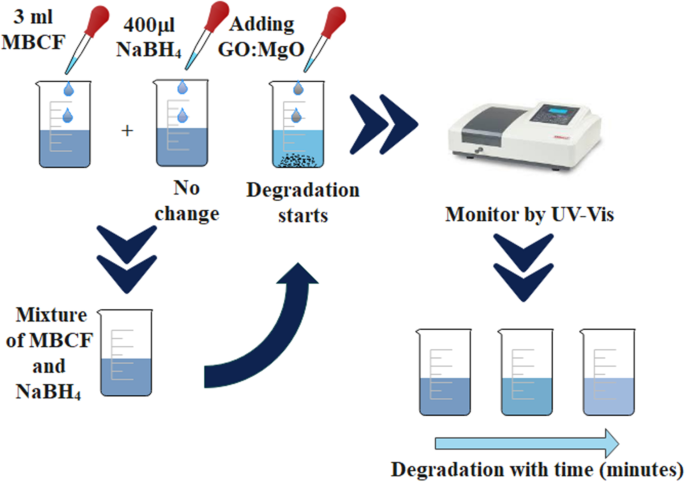
Representação esquemática da atividade catalítica durante a degradação do corante
Isolamento e identificação de S. aureus e E. coli
Amostras de leite de ovelha com mastite positiva foram obtidas de muitas clínicas veterinárias e fazendas em Punjab e cultivadas em ágar sangue de ovelha (SBA) 5%. Durante a noite a 37 ° C, as amostras culturais foram incubadas. Isolados bacterianos segregados foram purificados por estrias em MacConkey e ágar de sal de manitol (MA e MSA) em tripletos mantendo ~ pH 7, respectivamente. A validação das colônias padrão prosseguiu com coloração de Gram e análise bioquímica (ou seja, testes de catalase e coagulase).
Atividade antibacteriana
O comportamento antibacteriano do material sintetizado foi avaliado por meio de ensaio de difusão de poços com swab de 0,5 McFarland de E. isolado coli e S. aureus cepas bacterianas em MA e MSA, respectivamente. Uma broca de cortiça estéril foi usada para formar poços com um diâmetro de 6 mm nas placas MA e MSA e concentrações distintas de MgO puro e dopado (0,5 e 1,0 mg / 0,5 mL) foram carregadas em cada poço como dose mínima e máxima em comparação com ciprofloxacina (0,005 mg / 0,5 mL) e água DI (0,55 mL) como controles positivo e negativo, respectivamente, em condições assépticas. Após uma incubação durante a noite a 37 ° C, a eficácia antimicrobiana foi alcançada pelo cálculo das áreas de inibição em milímetros (mm) usando o compasso Vernier.
Análise estatística
Uma análise de variação unilateral (ANOVA) com SPSS 20 foi usada para estimar a eficácia antimicrobiana em termos de pontuação da zona de inibição (mm).
Caracterização de materiais
Para identificar a estrutura cristalina e as fases dos produtos preparados, as amostras foram avaliadas por meio de difratômetro de raios-X (modelo:PAN Analytical Xpert – PRO) utilizando radiação Cu-Kα ( λ =1,540 Å) e 2 θ valores de 10 ° a 85 °. O estudo dos grupos funcionais anexados foi adquirido através de FTIR (espectrômetro Perkin Elmer) usado em 4000–400 cm −1 alcance. Os espectros de absorção foram registrados com espectrofotômetro UV-Vis (Genesys 10S) na faixa de 200-700 nm, enquanto usando um espectrofluorômetro (JASCO, FP-8300), espectroscopia de fotoluminescência (PL) foi realizada. Os espectros Raman são medidos com microscópio DXR Raman (Thermo Scientific) usando laser baseado em λ =532 nm (6 mV). A composição elementar foi obtida via SEM – EDS usando o software INCA EDS, enquanto o espaçamento d foi visualizado com o auxílio de microscópio eletrônico de transmissão de alta resolução (HR-TEM modelo JEOL JEM 2100F).
Resultados e discussão
O DRX de MgO e MgO dopado com GO foi conduzido para identificar a estrutura cristalina, o tamanho e a composição da fase na Fig. 3a. Picos observados em 2 θ ° =37 °, 43,10 °, 62,5 °, 74,7 ° e 78,8 ° estavam de acordo com (111), (200), (220), (311) e (222) planos confirmando que MgO tinha estrutura cúbica coincidente com (JCPDS 75-1525) [47]. Após a dopagem, os picos de difração foram idênticos apontando para o pequeno conteúdo de dopante GO usado, que não foi detectável. O tamanho médio do cristalito foi calculado a partir dos picos de difração usando a equação de Debye-Scherrer, que foi encontrada em 13,28 nm. O espaçamento d calculado (0,21 nm) foi atribuído ao plano de rede (200) do MgO cúbico. Os padrões de difração de elétrons de área selecionada (SAED) das amostras indicaram a natureza cristalina do MgO (Fig. 3b-d). O ponto brilhante dos anéis concêntricos se relacionou bem com os planos de XRD de MgO [48].
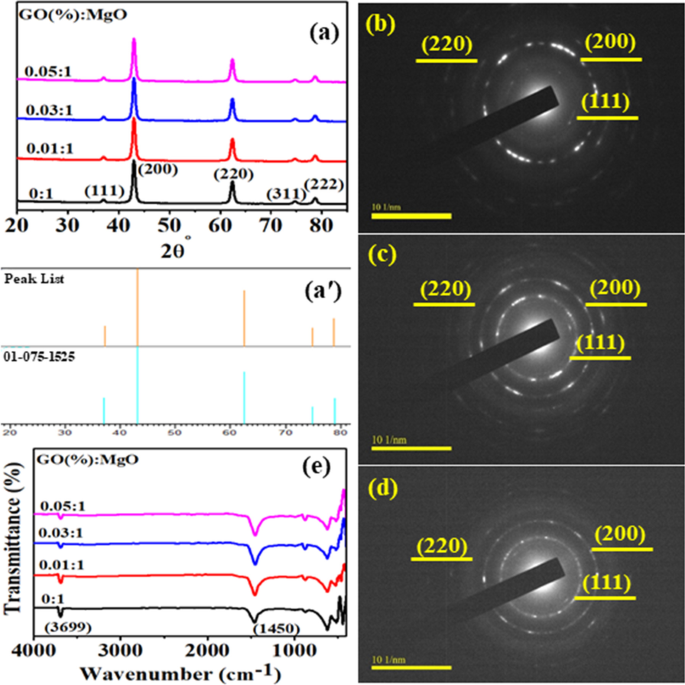
a Padrão de XRD de MgO dopado com GO, a ′ Código de referência de MgO, b Padrão SAED de (0:1), c GO (0,01:1, d (0,05:1), e Espectros FTIR
A fim de examinar os grupos funcionais anexados de MgO dopado, o FTIR foi operado no número de onda de 4000 a 400 cm -1 intervalo conforme ilustrado na Fig. 3e. Pico de transmitância em torno de 3699 cm −1 em MgO dopado foi atribuída a vibração de alongamento característica de grupos hidroxila (álcool) obtidos devido à reação entre a superfície de MgO e vapores de água no ar [3]. Observou-se a redução da intensidade do pico com a introdução do GO, que é atribuída às lâminas dopantes enroladas ao MgO. A banda encontrada em 1450 cm −1 foi relacionado a vibrações de alongamento assimétrico de íons carbonato (C – O), enquanto os picos de vibração de flexão correspondentes foram observados em ~ 865 e ~ 867 cm −1 [48]. No entanto, a diminuição da intensidade das bandas mencionadas anteriormente foi observada para a amostra de MgO dopada com GO [20]. Faixa encontrada por volta de 443 cm −1 mostrando a presença de vibração de alongamento caracterizada por Mg-O [49].
Os espectros de absorção de MgO livre de dopante e dopado foram coletados na faixa de 220 a 700 nm (Fig. 4a). A absorção de banda para MgO encontrada em ~ 250 e ~ 320 nm pode ser endossada para vacâncias de oxigênio (F e F 2 2+ ) centros, respectivamente. Em uma excitação λ =250 nm, o processo de fotoionização do centro F está envolvido, liderado pela equação F + hυ ↔ F + + e [23]. O pico de absorção de GO foi encontrado em torno de 230 nm, que pode ser atribuído a π - π * transições de C =C no sistema de carbono amorfo [50], após aumento da absorção de dopagem acompanhado de redshift. O gap diminuiu ligeiramente (5,0–4,8 eV) com o aumento da quantidade de GO em uma quantidade fixa de MgO, conforme ilustrado na Fig. 4b. Este redshift sugere efeitos morfológicos em cristais com vários sítios ativos ou pode ser efeito de confinamento quântico [51].
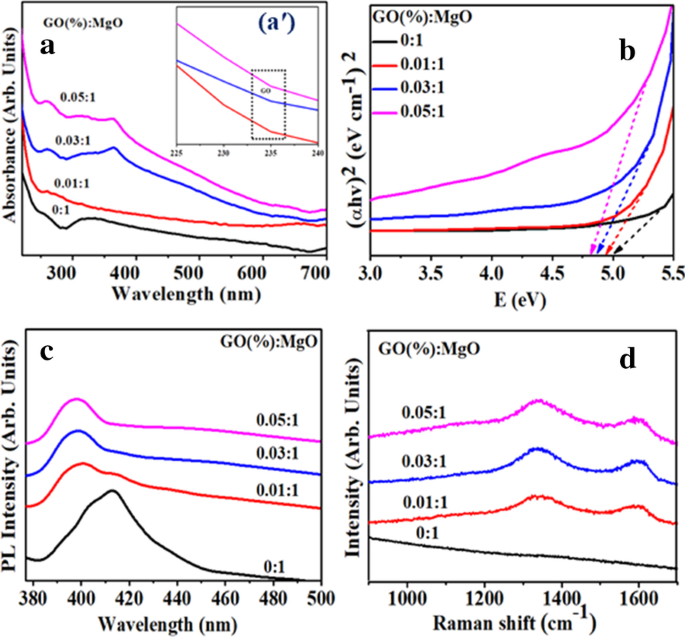
a Espectros de absorção de diferentes amostras de MgO dopado com GO, aʹ Espectro de absorção ampliado de GO-MgO, b Gráfico Tauc, c Espectros PL e d Espectros Raman de nanoestruturas GO-MgO
A Figura 4c revela espectros de emissão PL de MgO dopado medido variando de 377 a 500 nm com um excitante λ de 350 nm. Para determinar a eficiência de recombinação de portadores de carga (migração) e eficácia de aprisionamento, PL foi utilizado. O pico de emissão de PL em 414 nm resulta da transição da banda de defeito devido aos níveis de energia produzidos com várias vacâncias de ânions do tipo F (vacância de íons de oxigênio) [52]. A emissão PL de GO é geralmente atribuída à recombinação elétron-buraco de estados eletrônicos confinados adjacentes à banda de valência de amplo alcance (VB) e parte inferior da banda de condução (CB). Na estrutura atômica, a emissão é gerada principalmente a partir de transições eletrônicas entre a região do carbono não oxidado (–C =C–) e a borda da região do átomo de carbono oxidado (C – O, C =O e O =C – OH) [53]. Os picos de GO-MgO revelaram blueshift e exibiram baixa intensidade, o que indica uma taxa reduzida de recombinação que pode ser devido à transferência de elétrons de um nível de energia mais alto para novos estados gerados.
A estrutura da superfície e a desordem das amostras fabricadas foram analisadas por meio de espectroscopia Raman, conforme apresentado na Fig. 4d. O espectro da amostra de controle de Raman não mostrou nenhum pico característico em 100-1600 cm −1 região, o que sugere baixa intensidade de espalhamento de fônons de MgO [54, 55]. No caso de amostras dopadas, bandas localizadas em torno de 1338 cm −1 (Banda D) e 1598 cm −1 (Banda G) confirmou a presença de GO na amostra [56]. Banda D é atribuída ao defeito em sp 3 átomos de carbono (C) e banda G é proveniente de E 2g espalhamento de fônon (espalhamento de 1ª ordem) de sp 2 Átomos C. O aumento da intensidade dos picos D e G é obtido com o aumento da concentração de dopagem. Além disso, a relação de intensidade ( I D / eu G ) das bandas D e G indicaram grau de desordem de sp 2 Domínios C [46].
Para confirmar a estrutura cristalina e morfologia do MgO dopado, HR-TEM foi empregado (Fig. 5). A imagem HRTEM (5a) da amostra livre de dopante tem nanoestrutura em forma de hexágono aglomerado. Com a incorporação do GO, a morfologia do hexágono da nanoestrutura foi mesclada com as nanofolhas do GO e a formação da estrutura do tipo bastonete na presença de hexágonos foi observada. A agregação aumentou com o aumento da quantidade de dopante em MgO onde foram encontrados bastonetes e morfologia hexagonal das nanoestruturas. Vale ressaltar que o diâmetro da nanoestrutura do hexágono diminuiu com a maior concentração de GO, confirmando a interação entre MgO e GO.
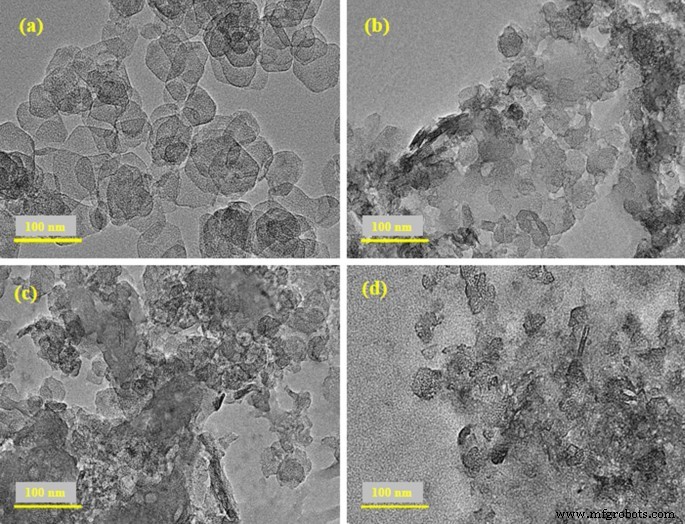
a - d Imagens HR-TEM de várias concentrações de MgO dopado com GO (0, 0,01, 0,03 e 0,05), respectivamente
O espaçamento d entre camadas foi medido com imagens HR-TEM usando o software Gatan, conforme ilustrado na Fig. 6a-d. Os valores de espaçamento d para várias concentrações (0:1, 0,01:1, 0,03:1 e 0,05:1) de MgO dopado com GO foram calculados como 0,250, 0,240, 0,20 e 0,24 nm, respectivamente, atribuídos ao plano (200) de MgO (Fig. 6a-d) conforme sincronizado com os resultados de XRD. Além disso, a mudança nos valores de espaçamento d foi atribuída à dopagem de GO em redes de MgO.
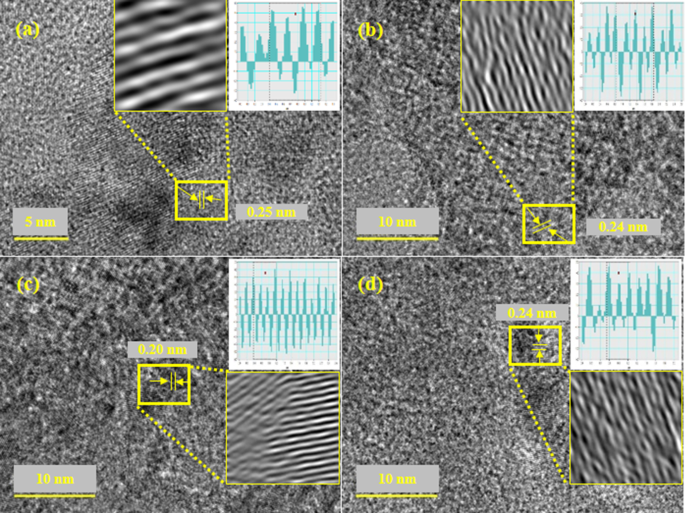
espaçamento d calculado usando imagens HR-TEM de GO-MgO ( a - d ) com conteúdo GO (0, 0,01, 0,03, 0,05)
A análise SEM – EDS revelou as informações detalhadas na superfície da amostra em relação à sua composição elementar. Os espectros de EDS de MgO e várias razões (0,01:1, 0,03:1 e 0,05:1) de GO em MgO são expressos na Fig. 7a-d, respectivamente. A presença de magnésio (Mg) e oxigênio (O) detectados na Fig. 7a são a confirmação da formação de MgO. O pico de carbono (C) foi atribuído às nanofolhas de GO, enquanto o pico elementar de Na nas amostras foi observado devido ao uso de NaOH durante o processo de síntese para manter o pH.
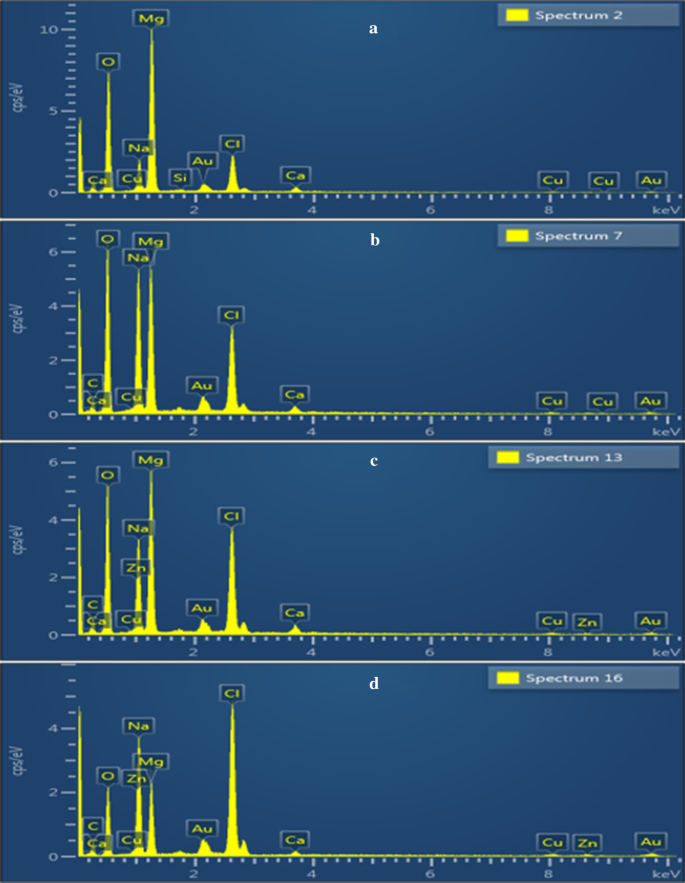
Análise SEM – EDS de MgO dopado com GO ( a - d ) com conteúdo GO (0, 0,01, 0,03 e 0,05), respectivamente
Para testar a atividade catalítica de MgO dopado com GO, os espectros de absorção de UV-Vis obtidos na degradação da amostra de referência (MBCF) foram usados. Reduzindo a capacidade de NaBH 4 com MBCF não foi significativamente afetado após 200 min, conforme demonstrado na Fig. 8a-d. Em condição neutra, solução MBCF (3 mL) adicionada em 400 μL de NaBH 4 e amostras de 3 mL dentro de 180-160 min mostraram redução limitada (4,8% de degradação) para amostras não dopadas e dopadas. Além disso, na atividade básica para as amostras (0:1, 0,01:1, 0,03:1, 0,05:1) resultou 11, 3,5, 12, 26% de degradação em 3 min, respectivamente (Fig. 8a-d). A função catalítica mais elevada foi obtida em solução ácida com maior concentração (0,05) de GO em nanoestruturas de MgO mostrando 45% de degradação em 1 min, conforme ilustrado na Fig. 8d.
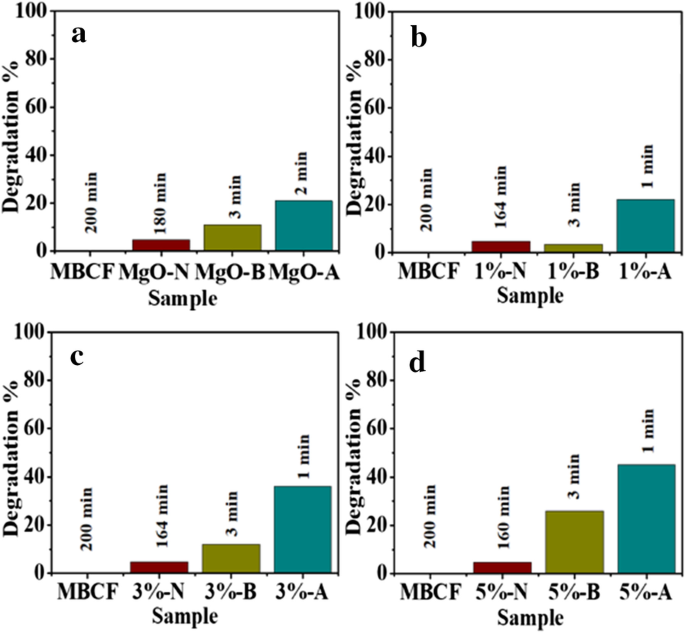
a - d Catálise de MBCF em branco e MgO dopado com GO em meio corante diferente [neutro (N), básico (B) e ácido (A)], respectivamente
Durante a catálise, redução em MBCF na presença de NaBH 4 , os materiais sintetizados atuam como retransmissores de elétrons, de modo que a transferência de elétrons do BH 4 - íons (doador) para MBCF (aceitador) resulta na redução do corante [57]. Abundantes sítios ativos de adsorção aprimorada de nanoestruturas para BH 4 - íons e moléculas de corante para reagir entre si. O pH da solução também afeta o desempenho de degradação. Para meio ácido (H 2 SO 4 ), atividade catalítica aprimorada, que é atribuída ao aumento da geração de H + íons oferecidos para serem adsorvidos na superfície da nanoestrutura. Após a adição de NaOH para meio básico, o número de grupos hidroxila aumenta levando à oxidação de produtos reduzidos e diminuição da atividade catalítica. Os resultados mostraram que a degradação do corante por nanoestruturas em meio ácido foi muito maior em comparação com a condição básica.
A eficácia antibacteriana in vitro de MgO puro e dopado com GO foi realizada contra G −ve e + ve isolados por ensaio de difusão em poço (Tabela 1). Os resultados mostraram uma ação microbicida melhorada e sinergismo de GO-MgO para E. coli em comparação com S. aureus , consulte a Tabela 1. Significativo ( p <0,05) as áreas de inibição foram registradas como (1,55–4,75 mm) e (2,10–4,85 mm) para E. coli na dose mínima e máxima, respectivamente, e (1,30–4,00 mm) para S. aureus em alta dose. Todas as concentrações mostraram eficácia antibacteriana zero para S. aureus em dose baixa. A comparação dos resultados procedeu com −ve controle água DI (0 mm) e + ve controle ciprofloxacina (7,15 mm) e (11,25 mm) áreas de inibição para E. coli e S. aureus , respectivamente.
No geral, as nanoestruturas dopadas revelaram atividade bactericida zero em relação a G + ve em dose baixa, enquanto a eficácia em relação a G-ve foi substancial ( p <0,05) em relação a G + ve em conteúdo dopado.
Os estresses oxidativos de nanoestruturas projetadas dependem de diversos fatores, como forma, tamanho e concentração de nanopartículas, que desempenham um papel importante na ação antibacteriana [58]. Materiais de tamanho nanométrico pequenos produzem eficientemente espécies reativas de oxigênio (ROS), causando danos à membrana celular da bactéria e extrusão do citoplasma, resultando em explosão de bactérias, ver Fig. 9 [59]. Em segundo lugar, a interferência catiônica nanomaterial significativa com fragmentos de membrana celular bacteriana negativa resulta em colapso. Atividade antibacteriana da nanopartícula de MgO aumentada contra E. coli, que foi devido à geração de uma grande quantidade de O 2 - e pode ser peroxidação lipídica e ROS [60]. Na amostra de dopante, a atividade antibacteriana aumentou devido ao aumento da concentração de GO.
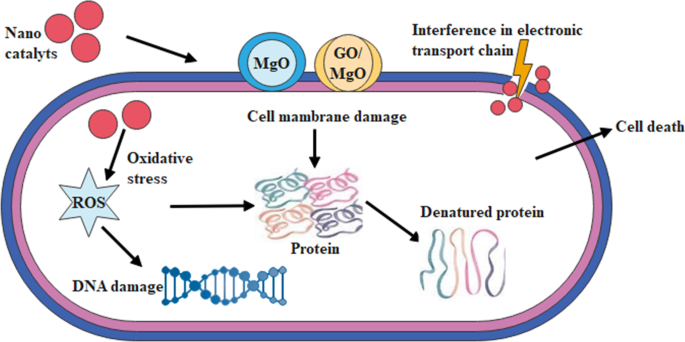
Mecanismo proposto de nanoestruturas de GO-MgO de atividade bactericida
| Amostras | Controlar a lacuna da banda de amostra (eV) | Diminuição do gap (eV) | Referências |
|---|---|---|---|
| ZnO dopado com GO | 3,6 | 2.9 | [61] |
| GO dopado com Ag | 4.10 | 3,50 | [2] |
| ZnO dopado com GO | 3,10 | 2,98 | [62] |
| MgO dopado com GO | 5.0 | 4.8 | Estudo atual |
Conclusão
No presente trabalho, nanoestruturas de MgO dopadas com GO foram sintetizadas com sucesso através da rota de precipitação química. A estrutura cúbica do MgO foi observada pela técnica de XRD e confirmada com HRTEM. Ligação molecular de Mg-O com vários grupos funcionais e picos de transmitância característicos de MgO em torno de 443 cm -1 na região da impressão digital foram registrados usando FTIR. A absorção aumentou com a dopagem, que introduziu o desvio para o vermelho em concentrações mais altas de GO. O intervalo de banda calculado usando o gráfico de Tauc do espectro de absorção de MgO dopado encontrado ser 4,8 eV (alta concentração) em comparação com o MgO (5,0 eV) foi atribuído ao redshift na absorção após dopagem. A morfologia cúbica e hexagonal das nanoestruturas foi observada em MgO e o crescimento de estruturas semelhantes a bastonetes foi observado após dopagem com uma diminuição no diâmetro dos hexágonos em HR-TEM. Além disso, o espaçamento d médio (0,23 nm) do HRTEM com o software Gatan é compatível com o XRD. A análise de EDS revelou composição elementar que mostrou confirmação de Mg, O com dopagem GO. Com a incorporação de GO, a intensidade de PL diminuiu de 414 nm acompanhada de um blueshift indicando baixa taxa de recombinação de excitons. A presença da banda D e G (em 1338, 1598 cm −1 , respectivamente) associado a sp 3 e sp 2 Átomo C foram verificados com Raman. A atividade catalítica foi avaliada e a maior degradação do corante de cerca de 45% foi alcançada em condição ácida por 0,05 GO-MgO. Além disso, os resultados experimentais mostraram maior eficácia bactericida do GO-MgO contra G –ve ( E. coli ) em relação ao G + ve ( S. aureus ) Além disso, o sinergismo de GO-MgO mostrou maior eficácia bactericida contra G-ve ( E. coli ) em comparação com G + ve ( S. aureus ) Este estudo explorou as propriedades dopante-dependentes de nanocompósitos de MgO que podem ser empregados na limpeza de águas industriais poluídas e em aplicações antimicrobianas para remediação ambiental.
Disponibilidade de dados e materiais
Todos os dados estão totalmente disponíveis sem restrição.
Abreviações
- EDS:
-
Espectroscopia de raios-X de dispersão de energia
- FTIR:
-
Espectroscopia de infravermelho com transformada de Fourier
- FESEM:
-
Microscopia eletrônica de varredura por emissão de campo
- G + ve:
-
Gram-positivo
- G –ve:
-
Gram negativo
- GO:
-
Grafeno
- HR-TEM:
-
Microscopia eletrônica de transmissão de alta resolução
- JCPDS:
-
Comitê conjunto sobre padrões de difração de pó
- MgO:
-
Óxido de magnésio
- UV – Vis:
-
Espectroscopia ultravioleta-visível
- XRD:
-
Difração de raios X
Nanomateriais
- Grafeno em alto-falantes e fones de ouvido
- S, N Co-dopado de grafeno Quantum Dot / TiO2 Compósitos para geração eficiente de hidrogênio fotocatalítico
- Compostos de grafeno e polímero para aplicações de supercapacitor:uma revisão
- Dopagem Substitucional para Mineral Aluminossilicato e Desempenho Superior de Divisão de Água
- Hierarquia hierárquica de esferas ocas de ZnO @ TiO2 para evolução de hidrogênio fotocatalítico altamente eficiente
- CdS Nanoparticle-Modified α-Fe2O3 / TiO2 Nanorod Array Photoanode para eficiente fotoeletroquímica oxidação de água
- Um Projeto Eficiente e Eficaz de Nanofios InP para Captação Máxima de Energia Solar
- Avaliação de estruturas de grafeno / WO3 e grafeno / CeO x como eletrodos para aplicações de supercapacitor
- Aerogel de Grafeno / Polianilina com Superelasticidade e Alta Capacitância como Eletrodo de Supercapacitor Altamente Tolerante à Compressão
- Nanocristal Sb2O3 dopado com S:um catalisador de luz visível eficiente para degradação orgânica



