Síntese de material anódico esférico Li4Ti5O12 revestido de prata por um método hidrotérmico assistido por Sol-Gel
Resumo
ᅟ
Li esférico revestido com Ag 4 Ti 5 O 12 O compósito foi sintetizado com sucesso através de um método hidrotérmico assistido por sol-gel usando uma mistura de etilenoglicol e nitrato de prata como o precursor, e a influência do conteúdo do revestimento de Ag nas propriedades eletroquímicas do seu foi extensivamente investigada. A análise de difração de raios-X (XRD) indicou que o revestimento de Ag não altera a estrutura espinélica de Li 4 Ti 5 O 12 . As análises de espectroscopia de impedância eletroquímica (EIS) demonstraram que a excelente condutividade elétrica do Li 4 Ti 5 O 12 / Ag resultou da presença da camada de revestimento de prata altamente condutora. Além disso, a camada de prata nano-espessa, que foi uniformemente revestida nas partículas, melhorou significativamente a capacidade de taxa deste material. Como consequência, o Li esférico de tamanho micron revestido de prata 4 Ti 5 O 12 exibiu excelente desempenho eletroquímico. Assim, com um teor de prata apropriado de 5% em peso, o Li 4 Ti 5 O 12 / Ag entregou a maior capacidade de 186,34 mAh g −1 a 0,5C, que é maior do que a de outras amostras, e manteve 92,69% de sua capacidade inicial a 5C após 100 ciclos. Mesmo a 10 ° C após 100 ciclos, ele ainda tinha uma retenção de capacidade de 89,17%, demonstrando notável estabilidade de ciclo.
Registro do teste
ISRCTN NARL-D-17-00568
Destaques
- 1.
Li esférico 4 Ti 5 O 12 / Compostos de Ag foram sintetizados através de um método hidrotérmico assistido por sol-gel usando etilenoglicol e uma mistura de nitrato de prata como o precursor para a camada de revestimento, o que melhorou significativamente a condutividade eletrônica e o desempenho eletroquímico de Li 4 Ti 5 O 12 .
- 2.
A morfologia esférica pode induzir uma grande densidade compactada e, conseqüentemente, aumentar a densidade volumétrica de energia.
Histórico
Na última década, as baterias recarregáveis de íons de lítio (LIBs) demonstraram muitas vantagens. Eles são leves; têm um tamanho pequeno, alta tensão e alta densidade de energia; e têm despertado grande interesse como dispositivo de armazenamento eletroquímico de energia para redução de emissões de escapamento e economia de combustível [1, 2]. No entanto, o preço dos precursores de lítio, questões de segurança e vida e baixa densidade de energia são obstáculos para a aplicação de LIBs para armazenamento de energia em grande escala no futuro [3]. Portanto, para desenvolver materiais substitutos que atendam às demandas de segurança do armazenamento em larga escala, grandes esforços têm sido feitos [4].
Titanato de lítio de espinélio de cubo (Li 4 Ti 5 O 12 ) materiais, os materiais anódicos de baterias de íon-lítio, tornaram-se um material promissor por causa de sua característica estrutural de deformação zero durante o processo de intercalação e desintercalação de Li 4 Ti 5 O 12 [5,6,7,8,9]. Este material tem uma voltagem de inserção e extração de plataforma de lítio de ~ 1,55 V (vs. Li / Li + ), evitando a formação de filmes de interface de eletrólito sólido (SEI) que consomem lítio, o que deve ser benéfico para aumentar a segurança e o bom ciclo dos LIBs. Portanto, Li 4 Ti 5 O 12 tornou-se um dos materiais potenciais em aplicações comerciais e pesquisa científica. Li 4 Ti 5 O 12 foi preparado por meio de vários métodos, por exemplo, estado sólido, deposição sem eletrodos, microondas e método sol-gel. Em relação ao método do estado sólido, alguns estudos têm mostrado que ele possui uma rota de síntese simples e baixo custo de síntese devido à menor distância para Li + difusão e transferência de elétrons, Li 4 Ti 5 O 12 exibe uma excelente capacidade de taxa, mas a reação de estado sólido não pode fornecer uma morfologia uniforme com um tamanho estreito. No entanto, o processo de deposição sem eletrodos tem uma rota de síntese complexa. Para a síntese sol-gel de Li 4 Ti 5 O 12 , vários pesquisadores relataram que pode produzir produtos com uma distribuição uniformemente homogênea e partículas estreitas com bom controle estequiométrico.
Apesar dessas muitas vantagens, as principais desvantagens do Li 4 Ti 5 O 12 são sua baixa condutividade eletrônica e iônica e seu lento coeficiente de difusão de íons de lítio, o que resulta em uma capacidade de taxa pobre. Inúmeras estratégias, incluindo redução do tamanho do cristalito [10], dopagem com íons metálicos de alta valência [11,12,13] e revestimento com fases condutoras [14,15,16,17], têm sido adotadas para melhorar o transporte de descarga / carga propriedades dos eletrodos. Além disso, outra maneira de aumentar a condutividade eletrônica é sintetizar Li nanoestruturado 4 Ti 5 O 12 . As nanoestruturas fornecem uma área de contato eletrodo / eletrólito maior para aumentar a cinética de intercalação e reduzir os caminhos de difusão para acelerar Li + e transporte de elétrons [18]. Entre essas abordagens, a maneira mais eficaz de melhorar as propriedades eletroquímicas do Li 4 Ti 5 O 12 é a modificação de superfície condutiva. Aslihan et al. [2] Li sintetizado 4 Ti 5 O 12 através do método sol-gel, e então o Li 4 como sintetizado Ti 5 O 12 foi revestido superficialmente com prata por deposição não eletrolítica. Os resultados mostraram que o revestimento de prata (revestimento de Ag) fornece uma matriz altamente condutora para Li + inserção, melhorando a condutividade eletrônica. Zhu et al. [19] preparado nano-tamanho revestido com carbono Li 4 Ti 5 O 12 microesferas nanoporosas com uma capacidade de taxa notável por meio de um processo de pré-revestimento de carbono em combinação com um método de secagem por pulverização e indicaram que as partículas esféricas de tamanho mícron induzem uma grande densidade compactada, resultando no aumento da densidade de energia volumétrica. No entanto, como sintetizar Li de tamanho micron revestido com Ag 4 Ti 5 O 12 partículas esféricas por meio de um método hidrotérmico assistido por sol-gel não foram relatadas.
Aqui, relatamos um método hidrotérmico assistido por sol-gel para sintetizar o Li esférico de tamanho mícron 4 Ti 5 O 12 / Composto de Ag usando etilenoglicol e uma mistura de nitrato de prata como um precursor, e o conteúdo do revestimento de Ag foi ajustado controlando a quantidade de elemento de prata no precursor. As propriedades eletroquímicas do Li 4 Ti 5 O 12 / Ag com morfologia esférica foram investigados em detalhes.
Experimental
Síntese de Li Prístino 4 Ti 5 O 12 e modificação de sua superfície com Ag
Síntese do precursor esférico por meio do método Sol-Gel
O precursor esférico glicolato de titânio (TG) foi sintetizado pelo método sol-gel. Primeiro, 2 mL de titanato de tetrabutila foram adicionados lentamente à solução, que continha AgNO 3 (em uma quantidade apropriada para ser solúvel em 50 mL de glicol), sob agitação vigorosa para formar a solução precursora. Em segundo lugar, a solução precursora foi adicionada a uma mistura de 150 mL de acetona que continha 0,1 mL de Tween 80 e a agitação foi continuada por 1 h à temperatura ambiente para formar precipitados. Em seguida, os precipitados foram envelhecidos por 8 h, separados por filtração e lavados duas vezes com álcool anidro. Por fim, os pós precursores foram obtidos por tratamento térmico a 80 ° C por 6 h em estufa seguido de trituração.
Síntese de Li esférico 4 Ti 5 O 12 / Ag
O esférico Li 4 Ti 5 O 12 / Ag foi preparado através do método hidrotérmico. Primeiro, LiOH · H 2 O e o precursor em uma razão molar de 3,9:1 foram homogeneamente misturados por agitação com 40 mL de álcool como meio por 1 h para formar uma mistura, que foi então aquecida a 180 ° C por 12 h em utensílios de Teflon selados até precipitar foram obtidos. Em segundo lugar, os precipitados foram recolhidos por centrifugação (5000 rpm, 5 min) e posteriormente lavados com etanol anidro várias vezes. Em seguida, foram secos em estufa a 80 ° C por 2 h. Finalmente, os precipitados foram aquecidos em uma mufla a 700 ° C por 2 h (taxa de aquecimento de 5 ° C · min −1 ) no ar depois de serem triturados e, em seguida, resfriados naturalmente à temperatura ambiente para obter Li esférico 4 Ti 5 O 12 / Ag em pó.
Caracterização do material
A estrutura do Li 4 Ti 5 O 12 as amostras foram identificadas por difração de raios-X (XRD, Rigaku D / max-PC2200) usando uma fonte de radiação Cu Kα (λ =0,15405 nm) com uma taxa de varredura de 4 ° min −1 de 10 ° a 80 ° e operado a 40 KV e 20 mA. A morfologia e o tamanho das partículas dos materiais foram explorados via MEV (microscopia eletrônica de varredura, Supra 55 Zeiss) e TEM (microscopia eletrônica de transmissão, JEOL-2100).
Medições eletroquímicas
Os desempenhos eletroquímicos dos produtos foram testados usando uma célula tipo moeda CR2025. Os eletrodos de trabalho foram preparados pela mistura de 80% em peso de Li 4 Ti 5 O 12 / Ag materiais ativos, 10% em peso de Super-P condutor e 10% em peso de aglutinante de fluoreto de polivinilideno (PVDF) em solvente N-metil-2-pirrolidona (NMP) para formar uma pasta uniforme. Em seguida, a pasta foi vazada sobre uma folha de alumínio e seca sob vácuo a 80 ° C durante 12 h para remover o solvente residual. Em seguida, a folha foi prensada e cortada em discos. Uma membrana microporosa de polipropileno Celgard 2400 e uma folha de lítio foram usadas como separador e eletrodo negativo, respectivamente. A solução de eletrólito era 1 M LiPF 6 em carbonato de etileno (EC), carbonato de dimetila (DMC) e carbonato de metil etileno (EMC) em uma razão volumétrica de 1:1:1. As células foram montadas em um porta-luvas cheio de argônio, onde os níveis de umidade e oxigênio foram mantidos abaixo de 1 ppm. Os testes eletroquímicos dos produtos foram avaliados usando um sistema de teste LAND CT2001A (Wuhan, China). Os testes de voltametria cíclica (CV) foram registrados em uma estação de trabalho eletroquímica CHI600A a 0,1 mV s −1 taxa de varredura de 1,0 a 2,5 V (vs. Li / Li + ) As medições EIS foram realizadas na faixa de frequência de 100 KHz a 10 mHz com uma perturbação de 5 mV.
Resultados e discussão
Propriedades estruturais e morfológicas
O efeito da quantidade de aditivo Ag no Li 4 Ti 5 O 12 / Pós de Ag foram investigados. Os padrões de XRD do Li esférico revestido com Ag 4 Ti 5 O 12 os compósitos são dados na Fig. 1. Pode ser facilmente visto que os principais picos de difração de todos os espécimes aparecem em 18,4 °, 35,54 °, 43,2 °, 57,2 °, 62,8 ° e 66,1 ° e são indexados como (111), (311), (400), (333), (440) e (531), respectivamente. Esses picos estão de acordo com o Li 4 Ti 5 O 12 padrão de difração padrão [20], exceto para padrões característicos do metal Ag (2θ =38,1 °, 44,3 °, 64,4 °). Nenhum pico de difração de impureza foi detectado em qualquer uma das amostras. Além disso, o pico de intensidade da prata aumentou correspondentemente com o aumento da quantidade de Ag.
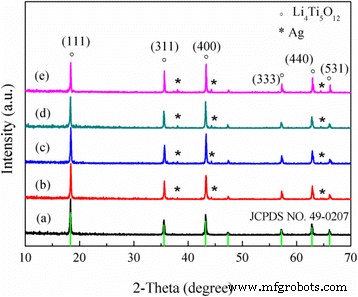
Padrões de XRD do Li 4 Ti 5 O 12 / Ag. ( a ) 0% em peso, ( b ) 1% em peso, ( c ) 3% em peso, ( d ) 5% em peso e ( e ) 7% em peso
Parâmetros de rede do Li 4 Ti 5 O 12 / Amostras de Ag com diferentes revestimentos de Ag são fornecidas na Tabela 1. Não foram observadas alterações significativas com o aumento do conteúdo de Ag. Assim, foi sugerido que a prata é principalmente revestida na forma de Ag elementar na superfície de Li 4 Ti 5 O 12 partículas, mas não penetrando na rede do espinélio Li 4 Ti 5 O 12 . Porque o raio iônico de Ag + (0,126 nm) é substancialmente maior do que o Ti 4+ (0,068 nm), o Li 4 sintetizado Ti 5 O 12 / Amostra Ag era apenas um composto de metal Ag e Li 4 Ti 5 O 12 Estágio.
A Figura 2 mostra as imagens SEM do precursor conforme preparado (a 1 -e 1 ) e Li 4 Ti 5 O 12 / Ag (a 2 -e 2 ) Conforme mostrado na Fig. 2, todas as amostras exibem uma estrutura uniformemente esférica com uma distribuição de tamanho estreita de 5–10 μm, o que é benéfico para um contato entre os materiais ativos e o eletrodo. A partir das imagens SEM, o precursor esférico, partículas de glicolato de titânio (TG), mostra uma linha suave, enquanto o Li 4 Ti 5 O 12 / Partículas de Ag apresentam uma linha rugosa. Além disso, uma boa dispersão poderia ampliar a área de contato eletrodo-eletrólito e acelerar significativamente o transporte de Li + e elétron. No entanto, a superfície do Li 4 Ti 5 O 12 / As amostras de Ag não são obviamente mais suaves do que as do precursor preparado e do glicolato de titânio e existem até certo ponto como uma aglomeração. Além disso, os tamanhos de partícula de diferentes Li 4 Ti 5 O 12 / Compostos de Ag são muito maiores do que os de Li sem Ag 4 Ti 5 O 12 ; entretanto, o fenômeno de aglomeração se torna mais óbvio com o aumento do teor de prata.

Imagens SEM do precursor e do Li 4 Ti 5 O 12 / Ag. ( a ) 0% em peso, ( b ) 1% em peso, ( c ) 3% em peso, ( d ) 5% em peso, ( e ) 7% em peso
A distribuição de prata no interior das partículas de tamanho mícron foi investigada adicionalmente, e análises de TEM e HRTEM foram fornecidas na Fig. 3. As imagens de TEM (Fig. 3a) mostram que o tamanho de micron revestido com Ag 5% em peso -esférico Li 4 Ti 5 O 12 as partículas são uniformemente revestidas por uma camada de prata com espessura de 3 ~ 4 nm, indicando que a camada de prata forma uma rede condutiva na superfície de todo o material, o que facilita o transporte de íons de lítio e elétrons. Como mostrado na Fig. 3b, a superfície do Li 4 de tamanho mícron Ti 5 O 12 / Partículas de Ag não são lisas, e o d - espaçamento de 5% em peso de Li revestido com Ag 4 Ti 5 O 12 partículas é 0,484 nm, o que combina bem com o plano LTO (111). Isso sugere que nenhuma nova fase foi gerada na superfície das partículas LTO, mas havia uma fina camada de revestimento nas partículas.

( a ) TEM e ( b ) Imagens HRTEM de Li 5% em peso revestido com prata 4 Ti 5 O 12 , em que a "linha" indica a camada de prata revestida
Propriedades eletroquímicas
A Figura 4 mostra as primeiras curvas de carga-descarga do Li esférico de tamanho mícron 4 Ti 5 O 12 / Eletrodos de Ag revestidos com diferentes conteúdos de Ag em diferentes taxas. Como pode ser visto na Fig. 4, todos os perfis exibem um platô de tensão extremamente plana de 1,55 V (vs. Li / Li + ), indicando uma transição de duas fases entre Li 4 Ti 5 O 12 e Li 7 Ti 5 O 12 para inserção de lítio [21]. A plataforma de tensão de Li 4 Ti 5 O 12 / Compostos de Ag são mais longos que os de Li sem Ag 4 Ti 5 O 12 . Com um conteúdo crescente de Ag, para uma plataforma de descarga mais longa do Li 4 Ti 5 O 12 / Compostos Ag, a capacidade de manter a plataforma é mais forte, sugerindo que uma boa condutividade eletrônica pode efetivamente reduzir a polarização do material durante o processo de reação do eletrodo e melhorar a utilização do material.
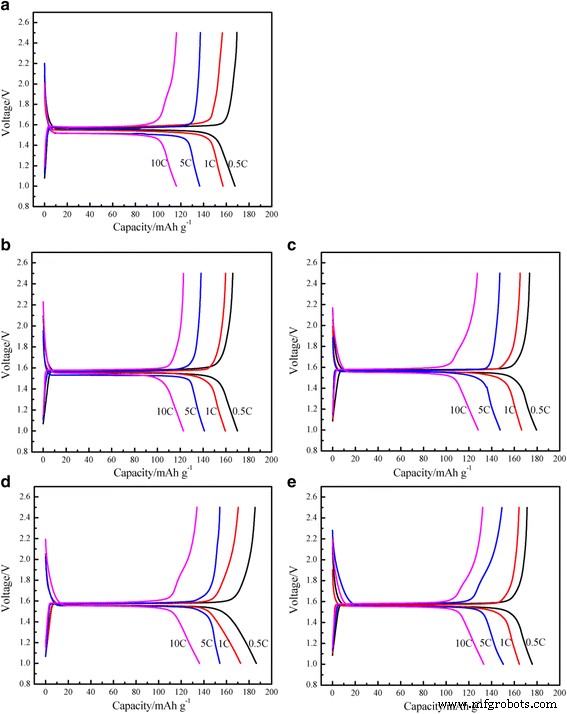
As curvas de carga-descarga inicial com várias densidades de corrente do Li 4 Ti 5 O 12 / Ag. ( a ) 0% em peso, ( b ) 1% em peso, ( c ) 3% em peso, ( d ) 5% em peso, ( e ) 7% em peso
Conforme mostrado na Fig. 4, Li livre de Ag 4 Ti 5 O 12 entregou uma capacidade específica de descarga inicial de 167,62 mAh g −1 a uma taxa de 0,5C, enquanto a capacidade entregue do Li esférico de tamanho micron revestido com Ag 4 Ti 5 O 12 os compostos aumentaram com o aumento da quantidade de prata:170,10, 179,54 e 186,34 mAh g −1 para 1, 3 e 5% em peso, respectivamente. Mas 7% em peso de Li revestido com Ag 4 Ti 5 O 12 exibiu um comportamento um pouco diferente. A capacidade específica de descarga fornecida diminuiu com o aumento da quantidade de prata:175,86 mAh g −1 para 7% em peso. O 5% em peso de Li revestido com Ag 4 Ti 5 O 12 ganhou a maior capacidade de descarga inicial e as capacidades específicas de descarga inicial alcançaram 186,34, 172,47, 154,12 e 136,06 mAh g −1 nas correntes específicas de 0,5, 1, 5 e 10C, respectivamente. Devido à baixa condutividade eletrônica e lento Li + difusão, o material exibe uma grande polarização em altas taxas de carga / descarga. O aditivo Ag altamente condutivo pode aumentar significativamente a reação de intercalação da superfície e reduzir a polarização [20, 22]. Mesmo o maior teor de Ag (7% em peso) pode fornecer o mais longo platô de voltagem, e o metal prata em si não pode ser totalmente intercalado no lítio. Em vez disso, o alto teor de Ag levará a uma diminuição na capacidade específica de Li 4 Ti 5 O 12 / Ag. Portanto, um conteúdo apropriado de prata pode não apenas melhorar efetivamente a condutividade do Li 4 Ti 5 O 12 e reduzir a polarização do Li 4 Ti 5 O 12 no processo de reação, mas também pode reduzir a perda da capacidade reversível devido ao revestimento de Ag.
As capacidades de taxa do Ag-free Li 4 Ti 5 O 12 e 5% em peso de Li revestido com Ag 4 Ti 5 O 12 compósito foram analisados em densidades de corrente de 0,5, 1, 5 e 10C, e os resultados são mostrados na Fig. 5. Como mostrado, a capacidade inicial de 5% em peso de Li revestido com Ag 4 Ti 5 O 12 composto a 5C era 154,12 mAh g −1 . Após 30 ciclos, a capacidade ainda era mantida em 150.50 mAh g −1 , retendo mais de 97,65% da capacidade inicial. Quando foi aumentado para 10C, a capacidade de descarga aparentemente caiu de 136,06 mAh g −1 a 130,81 mAh g −1 após 30 ciclos. Já a eficiência de retenção da capacidade ainda pôde ser mantida em 96,14%. Além disso, o desempenho de ciclismo do Li 4 Ti 5 O 12 / O composto Ag foi significativamente melhor do que o Ag-free Li 4 Ti 5 O 12 em várias taxas de carga-descarga. Como mostrado na Fig. 6a, com um conteúdo de prata apropriado de 5% em peso, o Li revestido de prata 4 Ti 5 O 12 entregou a maior capacidade de 186,34 mAh g −1 a 0,5C, que é maior do que a de outras amostras, e manteve 92,69% de sua capacidade inicial a 5C após 100 ciclos. Mesmo a 10 ° C após 100 ciclos (Fig. 6b), ele ainda tinha uma capacidade de retenção de 89,17%, demonstrando notável estabilidade de ciclo. Os resultados sugeriram que sob condições experimentais favoráveis, o Li 4 Ti 5 O 12 o revestimento de superfície de Ag não só aumentou a condutividade eletrônica e iônica, mas também aumentou obviamente o transporte de elétrons durante a reação de inserção / extração de lítio e melhorou significativamente a estabilidade do ciclo do Li 4 Ti 5 O 12 .
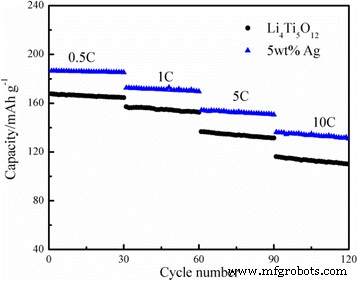
Capacidade de taxa de Li sem Ag e 5% em peso de Li revestido com Ag 4 Ti 5 O 12 sob diferentes taxas atuais
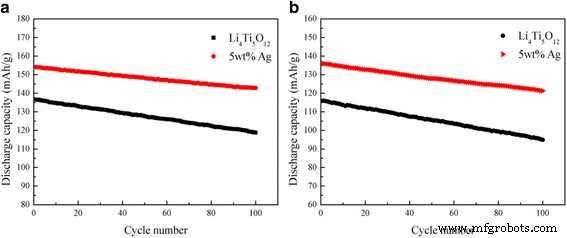
O desempenho de ciclagem do Li livre de Ag e 5% em peso revestido com Ag 4 Ti 5 O 12 a 5 ° C ( a ) e 10 ° C ( b )
A Figura 7 apresenta os voltamogramas cíclicos (CVs) do Li livre de Ag 4 Ti 5 O 12 e 5% em peso de Li revestido com Ag 4 Ti 5 O 12 composto obtido a uma taxa lenta de 0,1 mV s −1 . Obviamente, picos redox reversíveis entre 1,0 e 2,5 V foram obtidos, os quais são atribuídos à inserção e extração de íons de lítio, sugerindo que não há formação de fase intermediária durante a inserção e desinserção do lítio. Enquanto isso, a área do pico redox dessas duas curvas é quase igual, indicando uma alta eficiência coulômbica [23]. As diferenças de potencial entre os picos de oxidação e redução de 5% em peso de Li revestido com Ag 4 Ti 5 O 12 é 0,244 V, que é ligeiramente inferior ao do Li 4 livre de Ag Ti 5 O 12 (0,24 V). Isto sugere que o revestimento de superfície apropriado do aditivo Ag altamente condutor reduziu significativamente a polarização do Li 4 Ti 5 O 12 amostra e efetivamente melhorou seu desempenho eletroquímico. Além disso, os picos redox de 5% em peso de Li revestido com Ag 4 Ti 5 O 12 são mais nítidos e maiores do que os de Li sem Ag 4 Ti 5 O 12 , o que indica que um revestimento Ag apropriado pode melhorar o desempenho dinâmico do eletrodo.
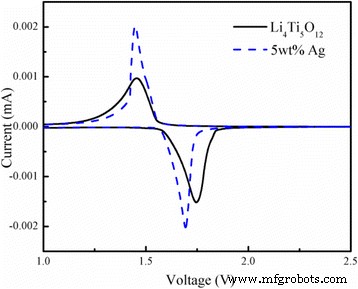
Curvas CV de Li livre de Ag e 5% em peso de Li revestido com Ag 4 Ti 5 O 12 composto
Medições de espectroscopia de impedância eletroquímica (EIS) de Li livre de Ag 4 Ti 5 O 12 e 5% em peso de Li revestido com Ag 4 Ti 5 O 12 foram conduzidas na faixa de frequência de 10 5 a 0,01 Hz antes dos ciclos galvanostáticos. Além disso, o circuito equivalente (inserido) e os dados de impedância correspondentes são mostrados na Fig. 8. No circuito equivalente, Rs representa a resistência da solução de eletrólito, que reflete a condutividade elétrica do eletrólito, separador e eletrodos. (intersecção com o Z ′ eixo em alta frequência), R ct mostra a resistência de transferência de carga em materiais, CPE é a capacitância do filme de dupla camada e passivação, e W é a impedância de Warburg, que está relacionada à difusão do íon de lítio na região de baixa frequência. Os parâmetros obtidos pelo ajuste estão listados na Tabela 2. Conforme mostrado na Fig. 8, ambas as curvas EIS eram compostas por um semicírculo deprimido na região de alta frequência e uma linha reta oblíqua na região de baixa frequência. O diâmetro do semicírculo representa a resistência de transferência de carga, e a reta oblíqua está relacionada à impedância de Warburg [24]. A impedância dos semicírculos na região de alta frequência corresponde ao processo de transferência de carga da interface do eletrodo e eletrólito líquido, e a linha reta na região de baixa frequência pode ser expressa como o comportamento de difusão dos íons de lítio na estrutura do óxido [25,26, 27,28]. Como mostrado na Fig. 8, o diâmetro do semicírculo do 5% em peso de Li revestido com Ag 4 Ti 5 O 12 é mais curto do que o Li 4 vazio Ti 5 O 12 , indicando que uma quantidade adequada de revestimento de Ag pode aumentar a condutividade eletrônica de Li 4 Ti 5 O 12 , e isso tem a ver com o processo de transferência de carga, onde Li + e os elétrons alcançam a superfície do eletrodo simultaneamente para completar a reação. Isso depende principalmente da reação redox na superfície dos materiais ativos. A menor resistência à transferência de carga do Li 5% em peso revestido com Ag 4 Ti 5 O 12 refletiu reações de transferência de carga mais rápidas em suas interfaces eletrodo / eletrólito.
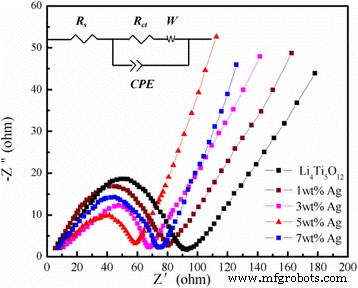
Padrões EIS do puro Li 4 Ti 5 O 12 e o Li 4 Ti 5 O 12 revestido com diferentes conteúdos de Ag
O coeficiente de difusão química do íon de lítio pode ser calculado a partir do gráfico na região de baixa frequência usando a seguinte Eq. (1) [29,30,31,32,33].
$$ {D} _ {{\ mathrm {Li}} ^ {+}} =\ frac {R ^ 2 {T} ^ 2} {2 {A} ^ 2 {n} ^ 4 {F} ^ 4 { C} _ {Li} ^ 2 {\ sigma_w} ^ 2} $$ (1)
Aqui, \ ({D} _ {{\ mathrm {Li}} ^ {+}} \) é o coeficiente de difusão de íons de lítio, R é a constante do gás (8.314 JK mol −1 ), T é a temperatura absoluta (298 K), A é a área de superfície do eletrodo, n é o número de elétrons por molécula que participa da reação de transferência eletrônica, F é a constante de Faraday (96.500 C mol −1 ), C Li é a concentração de íons de lítio no Li 4 Ti 5 O 12 eletrodo, e σ w é o fator Warburg, que tem a seguinte relação com Ζ re :
$$ {Z} _ {\ mathrm {re}} ={R} _S + {R} _ {\ mathrm {ct}} + {\ sigma} _w \ cdot {\ omega} ^ {- 0,5} $$ (2 )
Além disso, a relação entre Z re e a raiz quadrada recíproca da frequência na frequência baixa é mostrada na Fig. 9. Todos os parâmetros obtidos e calculados a partir do EIS estão resumidos na Tabela 2. Conforme mostrado na Tabela 2, \ ({D} _ {\ mathrm { L} {\ mathrm {i}} ^ {+}} \) do 5% em peso de Li revestido com Ag 4 Ti 5 O 12 é 6,73 × 10 −11 , que é uma ordem de magnitude maior do que Li 4 Ti 5 O 12 (8,69 × 10 −12 ) O 5% em peso de Li revestido com Ag 4 Ti 5 O 12 tem o maior coeficiente de difusão de lítio em comparação com o de Li livre de Ag 4 Ti 5 O 12 e 1, 3 e 7% em peso de Li revestido com Ag 4 Ti 5 O 12 compósitos, indicando que o revestimento com Ag é uma forma eficaz de melhorar a condutividade eletrônica. Consequentemente, a capacidade de taxa de 5% em peso de Li revestido com Ag 4 Ti 5 O 12 pode ser substancialmente melhorado.
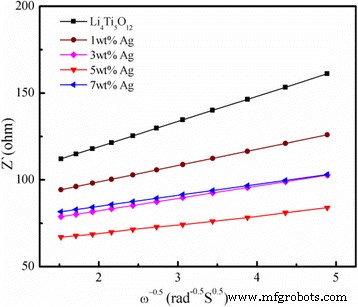
Gráfico de Z re conspirou contra ω −0,5 na região de baixa frequência para o Li 4 Ti 5 O 12 e Li 4 Ti 5 O 12 revestido com diferentes conteúdos de Ag
Conclusões
Materiais anódicos esféricos Li 4 Ti 5 O 12 / Compósitos de Ag com alta densidade compactada foram preparados por um método hidrotérmico assistido por sol-gel. Os testes eletroquímicos mostram que a quantidade apropriada de revestimento de Ag pode melhorar significativamente a condutividade eletrônica de Li 4 Ti 5 O 12 e aumentar a estabilidade do ciclo. O teor ideal de prata é de 5% em peso, o que pode resultar em excelente desempenho eletroquímico. No entanto, o conteúdo excessivo de prata fará com que as propriedades eletroquímicas do material piorem. Portanto, Li esférico revestido com Ag apropriado 4 Ti 5 O 12 O composto é um material de armazenamento de lítio superior com alta capacidade e excelente segurança, e tem potencial real como um material promissor em baterias de íon de lítio potentes.
Nanomateriais
- Método de preparação do material de contato de cobre e tungstênio
- Método C#
- Estratégia de sinterização hidrotérmica para material de ânodo LiNb3O8 estruturado poroso e oco
- Síntese fácil de nanopartículas de SiO2 @ C ancoradas em MWNT como materiais de ânodo de alto desempenho para baterias de íon-lítio
- Síntese hidrotérmica de nanopartículas de In2O3 híbridos gêmeos heteroestruturas de ZnO de disco hexagonal para atividades fotocatalíticas aprimoradas e estabilidade
- Composto de MoS2 / Acetileno com poucas camadas como um ânodo eficiente para baterias de íon-lítio
- Método de pós-tratamento para a síntese de nanopartículas FePt-Fe3O4 binárias monodispersas
- Efeito do método de síntese de La1 - xSr x MnO3 nanopartículas de manganita em suas propriedades
- Composto de Si / Grafeno incorporado fabricado por redução térmica de magnésio como material de ânodo para baterias de íon-lítio
- Novo método cria memória de computador com óxido de titânio



