Na4Mn9O18 / Composto de Nanotubo de Carbono como um Material de Alto Desempenho Eletroquímico para Baterias Aquosas de Íons de Sódio
Resumo
A bateria aquosa de íon de sódio (ASIB) é um dos novos e promissores sistemas de armazenamento de energia devido aos recursos abundantes de sódio, bem como à eficiência e segurança do eletrólito. Aqui, relatamos um sistema ASIB com Na 4 Mn 9 O 18 / nanotubo de carbono (NMO / CNT) como cátodo, metal Zn como ânodo e um novo Na + / Zn 2+ íon misturado como eletrólito. O NMO / CNT com estrutura microesférica é preparado por um método simples de secagem por pulverização. A bateria preparada oferece uma alta capacidade específica reversível e ciclabilidade estável. Além disso, a bateria exibe uma capacidade de descarga reversível estável de 53,2 mAh g −1 mesmo a uma alta taxa de corrente de 4 C após 150 ciclos. Nossos resultados confirmam que o composto NMO / CNT é um material eletrodo cátodo promissor para ASIBs.
Histórico
As baterias de íon-lítio (LIBs) são consideradas fontes de energia promissoras para suas aplicações em dispositivos eletrônicos portáteis [1, 2]. Especificamente, vários sistemas LIB aquosos têm atraído atenção crescente devido ao seu baixo custo, segurança e capacidade de alta taxa [3]. Em 1994, o grupo Dahn pela primeira vez propôs um sistema LIB aquoso [4]. Desde então, muitos materiais de eletrodo, como LiFePO 4 [5], LiMn 2 O 4 [6] e LiCoO 2 [7] foram desenvolvidos. No entanto, os relatórios anteriores enfocam os materiais de lítio como ânodo. No entanto, o lítio tem baixa abundância na crosta terrestre, o que poderia aumentar os custos e reduzir a implementação em grande escala [8].
As baterias aquosas de íon de sódio (ASIBs) ganharam muita atenção como substitutas para as baterias LIBs aquosas devido às boas propriedades químicas e aos baixos preços do sódio. Atualmente, vários materiais à base de sódio, como Na 3 V 2 (PO 4 ) 3 [9], Na 2 FeP 2 O 7 [10], Na 2 CuFe (CN) 6 [11], e Na 4 Mn 9 O 18 foram desenvolvidos como materiais ativos para ASIBs [12]. Entre eles, Na 4 Mn 9 O 18 (NMO) com estrutura ortogonal tem dois tipos de túneis (tipo S e tipo O) formados pelo MnO 6 octahedra e MnO 5 pirâmides quadradas. Dois sítios de sódio ocupam os grandes túneis do tipo S, assim como um sítio de sódio ocupa túneis menores do tipo O [13]. Esses túneis em NMO são propícios à transmissão de íons de sódio. No entanto, baixa condutividade e enorme expansão de volume do NMO durante a inserção / extração de Na + grande resultando na pulverização do material ativo dificultam sua aplicação como cátodo em ASIBs. [14,15,16]. Portanto, várias abordagens têm sido desenvolvidas para resolver os problemas acima mencionados. Um dos métodos eficazes é compor com materiais de carbono com grande estabilidade condutiva e química que pode amortecer a mudança de volume, melhorando simultaneamente a condutividade elétrica do eletrodo [17, 18]. Hoje em dia, materiais de carbono nanoestruturados como carbono poroso [19], carbono esférico [20], grafeno [21] e nanotubo de carbono [3, 22] são amplamente utilizados como suportes de materiais ativos. Entre os vários substratos, o nanotubo de carbono poderia formar um esqueleto condutor, que pode aumentar o caminho de transmissão de elétrons e melhorar as propriedades mecânicas do material [23]. Além disso, a estrutura do material catódico, como tamanho de partícula, morfologia microscópica e área de superfície específica afetam seriamente o desempenho eletroquímico da bateria [24]. Comparados aos pós irregulares, os pós microesféricos com distribuições estreitas de tamanho exibem grandes propriedades eletroquímicas devido à sua alta densidade compactada. A secagem por pulverização é uma rota eficaz para sintetizar pós multicomponentes e esféricos homogêneos [25]. As amostras compostas com estrutura microesférica, como LiFePO 4 / C e Li 4 Ti 5 O 12 / C [24, 26] foram sintetizados por secagem por spray e são usados em baterias de íon-lítio, mas técnicas de secagem por spray raramente são usadas em baterias de íon sódio.
Neste trabalho, relatamos pela primeira vez a preparação do Na 4 Mn 9 O 18 / nanotubo de carbono (NMO / CNT) composto com estrutura microesférica via método de secagem por spray (Fig. 1). Os ASIBs foram então construídos com NMO / CNT como um cátodo, o romance Na + / Zn 2+ íons mistos como eletrólitos e zinco metálico como ânodo. Neste novo sistema de bateria, as propriedades eletroquímicas do composto NMO / CNT resultante como cátodo foram investigadas.
O diagrama esquemático de NMO / CNT
Métodos
Preparação do material
O precursor do composto NMO / CNT foi inicialmente preparado como se segue:4,0 mg de dispersão aquosa de CNT (9% em peso, Timesnano, Chengdu) foi adicionado a 30 mL de 0,1 M KMnO 4 e solução aquosa de NaOH 3,0 M sob agitação. Em seguida, 30 mL de 0,28 M MnSO 4 solução foi gotejada na solução misturada acima, e a precipitação marrom foi produzida repentinamente. A precipitação resultante foi obtida por método centrífugo e deixada em repouso por 24 horas para formar a amostra envelhecida por via úmida. Em seguida, 4 g de amostra envelhecida por úmido foram adicionados a 100 mL de solução de NaOH 15 M e agitados por 25 min para formar a suspensão marrom escura. Finalmente, a suspensão foi aquecida a 180 ° C por 24 h usando uma autoclave de aço inoxidável de 150 mL com um forro de Teflon. O precursor composto NMO / CNT foi lavado repetidamente com água desionizada e seco a 80 ° C ao ar.
Para preparar o composto NMO / CNT, 0,6 g de precursor NMO / CNT foi adicionado em 150 mL de água desionizada com ultra-sonicação por 15 min para formar uma suspensão marrom. A suspensão foi adicionada à máquina de secagem por pulverização (HOLVES, Pequim) por bomba peristáltica a 6 mL min -1 . Em seguida, foi atomizado a 205 ° C aplicando um bico de dois fluidos com pressão de atomização de 0,8 MPa e temperatura de saída de 110 ° C. O pó obtido é o composto NMO / CNT desejado com estrutura microesférica. A partícula NMO de referência sem CNT foi preparada seguindo as mesmas condições.
Caracterização do material
A data de difração de pó de raios-X (XRD) das amostras preparadas foi medida por uma difração de raios-X (XRD, D8 Discover, Bruker) empregando radiação Cu Kα. A análise termogravimétrica (TG, SDT Q-600, TA Instruments-Waters LLC) foi realizada de 25 a 1000 ° C com uma taxa de aquecimento de 10 ° C min −1 sob o ar. A espectroscopia Raman foi realizada usando um sistema Jobin-Yvon T6400 Micro-Raman com um laser de íon de argônio 532 nm. A análise de microscopia eletrônica de varredura (SEM) foi coletada em um microscópio eletrônico de varredura Hitachi Limited S-4800. A estrutura interna e a difração de elétrons de área selecionada (SAED) das amostras foram estudadas usando um microscópio eletrônico de transmissão de alta resolução JEOL JEM-2800 (HR-TEM) a 160 kV. O conteúdo de Mn no eletrólito foi medido por espectroscopia de emissão óptica com plasma indutivo acoplado (ICP-OES, PRODIGY XP, LEEMON).
Medições eletroquímicas
Para preparar o eletrodo composto NMO / CNT, a pasta foi primeiro preparada por mistura com 80% em peso da amostra preparada, 10% em peso de negro de acetileno e 10% em peso de fluoreto de polivinilideno (PVDF) em N -metil-2-pirrolidona (NMP). A pasta acima foi espalhada uniformemente em um coletor de corrente de folha de carbono e seca a 75 ° C por 12 h. A folha de carbono acima e a folha de metal de Zn foram cortadas em discos circulares com 15 mm de diâmetro como cátodo e ânodo, respectivamente. A solução contendo 1 M Na 2 SO 4 e 0,5 M ZnSO 4 com o pH =4 foi usado como eletrólito, e tapete de vidro absorvido (NSG Corporation) foi aplicado como separador [27, 28]. 2025 baterias do tipo moeda foram montadas em atmosfera de ar antes dos testes eletroquímicos. O desempenho do ciclo de carga / descarga foi investigado em um sistema de teste de bateria (Neware, Shenzhen) na faixa potencial de 1–1,85 V (vs. Zn 2+ / Zn). Voltametrias cíclicas (CVs) foram realizadas pela estação de trabalho eletroquímica (Princeton, VersaSTAT 4) na faixa de potencial de 1–2 V (vs. Zn 2+ / Zn). A espectroscopia de impedância eletroquímica (EIS) foi realizada usando a estação de trabalho eletroquímica (Princeton, VersaSTAT 4) na faixa de frequência de 0,01–100 kHz.
Resultados e discussão
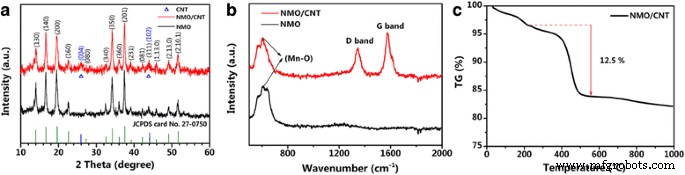
Os padrões de XRD do NMO / CNT e NMO são mostrados na Fig. 2a. Ambos os padrões de XRD concordam bem com a fase de NMO (JCPDS # 27-0750) [29], revelando que o método hidrotérmico e de secagem por pulverização é uma via válida para a síntese do Na 4 Mn 9 O 18 à base de materiais. O padrão de XRD de NMO / CNT exibe dois picos ampliados em ca. 26 ° e 44 ° no compósito NMO / CNT, que estão associados aos planos grafíticos (004) e (102) do CNT, respectivamente [30, 31], sugerindo que o compósito NMO / CNT foi preparado com sucesso.

a Padrões de XRD de NMO / CNT e NMO. b Espectro Raman de NMO / CNT e NMO. c Curvas TG do composto NMO / CNT a uma taxa de aquecimento de 10 ° C / min sob ar
A Figura 2b mostra os espectros Raman do composto NMO / CNT e da amostra NMO pura. Os picos amplos em cerca de 600-650 cm −1 pode estar relacionado às vibrações de alongamento da banda Mn – O [23]. O espectro do NMO / CNT mostra dois picos amplos e fortes localizados a cerca de 1347 cm −1 (Banda D) e 1575 cm −1 (G-band), correspondendo ao carbono grafítico no CNT [32, 33]. Os resultados Raman confirmam que o NMO / CNT conforme preparado consiste em CNT puro e nanopartículas de NMO cristalinas. O conteúdo real de CNT no composto NMO / CNT foi medido por análise de TG em fluxo de ar. Conforme mostrado na Fig. 2c, a primeira perda de peso do NMO / CNT abaixo de 220 ° C é causada pela evaporação de moléculas de água adsorvidas. A seguinte grande perda de peso, ocorrendo de 350 a 500 ° C, está relacionada à combustão do CNT. Com base na curva TG do composto NMO / CNT, o conteúdo real de NMO no composto é calculado em 87% em peso.
SEM e TEM foram usados para determinar as morfologias das amostras. A Figura 3a mostra a imagem SEM do composto NMO / CNT, onde microesferas uniformes com diâmetro de cerca de 5–7 μm podem ser observadas. Uma das esferas é ampliada na inserção da Fig. 3a, e o CNT entrelaçado pode ser observado. As redes CNT são muito importantes porque podem capturar NMO da estrutura da haste. A Figura 3b exibe uma imagem TEM do composto NMO / CNT; mais claramente, o estado de reticulação de NMO / CNT pode ser observado. Os NMOs em forma de bastão com diâmetro de cerca de 30–50 nm são enrolados juntos por CNT que pode aumentar a condutividade elétrica do material catódico composto. A Figura 3c mostra as franjas da rede com uma distância entre as franjas de 0,45 e 0,33 nm, correspondendo a (200) de NMO e (004) de CNT, respectivamente. O padrão SAED (Fig. 3d) exibe a natureza de cristal único de NMO, indicando uma alta cristalinidade de NMO. E os anéis de difração homogêneos do CNT também podem ser observados a partir do padrão SAED, o que confirma que o NMO é composto com sucesso com CNT por um método simples de secagem por pulverização.

A morfologia e estrutura do NMO / CNT. a Imagem SEM; b Imagem TEM; c Imagem HRTEM; d Padrão SAED
A Figura 4a mostra as curvas CV da célula com o composto NMO / CNT como cátodo a uma taxa de san de 0,1 mV s −1 . As curvas CV mostram dois picos de redução em torno de 1,20 e 1,37 V (vs. Zn 2+ / Zn), bem como um pico de oxidação em cerca de 1,53 V (vs. Zn 2+ / Zn) durante o ciclo inicial. O pico de oxidação no ciclo inicial mostra uma corrente de pico mais alta em comparação com o resto das varreduras / ciclos, o que pode ser devido às transições de fase multi-atômicas iniciais para adaptar a cepa quando o íon Na foi extraído dos materiais NMO / CNT, indicando algum grau de irreversibilidade no primeiro ciclo [34]. Para os ciclos seguintes, os dados exibem dois pares redox principais em cerca de 1,50 / 1,20 V e 1,62 / 1,37 V (vs. Zn 2+ / Zn), respectivamente. Eles estão associados com a desinserção e inserção de íons Na de / para a estrutura cristalina ortorrômbica de NMO no eletrólito aquoso. Durante o processo de carga, os íons Na são extraídos do cátodo NMO / CNT para o eletrólito, o que é acompanhado pela liberação dos elétrons enquanto os íons Zn são depositados na superfície do ânodo de zinco. Quando a bateria é descarregada, o zinco do ânodo perde os elétrons e se dissolve no eletrólito, enquanto no cátodo a reação é revertida e os íons Na são inseridos no cátodo para formar NMO / CNT [35]. Essas reações podem ser representadas da seguinte forma:
$$ {\ displaystyle \ begin {array} {l} \ mathrm {ânodo} \ \ mathrm {reação}:{\ mathrm {Zn}} ^ {2 +} + 2 {\ mathrm {e}} ^ {-} \ iff \ mathrm {Zn} \\ {} \ mathrm {cátodo} \ \ mathrm {reação}:{\ mathrm {Na}} _ 4 {\ mathrm {Mn}} _ 9 {\ mathrm {O}} _ {18} \ iff {\ mathrm {Na}} _ {4-x} {\ mathrm {Mn}} _ 9 {\ mathrm {O}} _ {18} + x {\ mathrm {Na}} ^ {+} + x { \ mathrm {e}} ^ {-} \\ {} \ mathrm {total} \ \ mathrm {reação}:2 {\ mathrm {Na}} _ 4 {\ mathrm {Mn}} _ 9 {\ mathrm {O}} _ {18} + x {\ mathrm {Zn}} ^ {2 +} \ iff 2 {\ mathrm {Na}} _ {4-x} {\ mathrm {Mn}} _ 9 {\ mathrm {O}} _ {18} + 2x {\ mathrm {Na}} ^ {+} + x \ mathrm {Zn} \ end {array}} $$
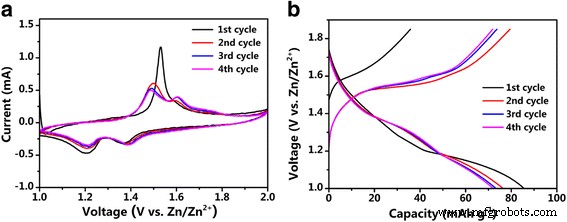
Desempenho eletroquímico do eletrodo NMO / CNT. (a) Comportamento CV do eletrodo NMO / CNT a uma taxa de varredura de 0,1 mV s −1 . (b) Perfis de tensão de descarga / carga do eletrodo NMO / CNT para o 1º, 2º, 3º e 4º ciclos a 4 C
O pico de oxidação fraco em cerca de 2 V (vs. Zn 2+ / Zn) está relacionado à decomposição da água no eletrólito [27]. Com o aumento dos ciclos, os potenciais do pico redox tendem a ser estáveis. Os picos simétricos demonstram que o processo de desinserção / inserção do íon Na pode ser considerado altamente reversível. Foi relatado que, para os materiais NMO, a diminuição da capacidade surgirá da dissolução contínua de Mn 2+ após uma reação de desproporção de Mn 3+ em Mn 2+ e Mn 4+ [29]. Para avaliar o efeito desse fenômeno em nossa bateria, o conteúdo de íons Mn no eletrólito foi medido por ICP-OES. A concentração de íons Mn em 25 mL de eletrólito em contato com 0,12 g de material ativo foi medida em diferentes ambientes ácidos, conforme mostrado na Tabela 1.
Os resultados desse experimento mostraram que o teor de íons Mn diminuiu com o aumento do pH. Portanto, o pH do eletrólito foi ajustado para 4 [36], o que inibe a reação de desproporção mencionada acima e reduz a dissolução de Mn.
A descarga / carga galvanostática foi conduzida para medir a capacidade de armazenamento de Na. A partir da curva CV, aprendemos que a voltagem deve ser inferior a 2 V para evitar a reação de decomposição da água. A Figura 4b ilustra as curvas de descarga / carga do eletrodo NMO / CNT durante os quatro ciclos iniciais a 4 C na faixa de potencial de 1–1,85 V (vs. Zn 2+ / Zn). No primeiro ciclo, a capacidade de carga é de apenas 35,8 mAh g −1 e a capacidade de descarga correspondente considerável é 85,6 mAh g −1 . Assim, a eficiência coulômbica no ciclo inicial é de 239,4%, muito maior que 100%, o que se deve à decomposição da água intersticial e ao baixo teor de íon Na [37]. Após o primeiro ciclo, os planaltos potenciais foram bem mantidos após ciclos adicionais. Existem dois platôs potenciais conspícuos em cerca de 1,37 e 1,2 V (vs. Zn 2+ / Zn) nas curvas de descarga, bem como dois platôs em cerca de 1,50 e 1,62 V (vs. Zn 2+ / Zn), que corresponde ao 2º, 3º e 4º ciclos CV.
A Figura 5a apresenta o desempenho do ciclo dos eletrodos NMO e NMO / CNT a uma taxa de 4 ° C. Pode ser visto que as capacidades de descarga inicial de NMO e NMO / CNT são tão altas quanto 62,7 e 85,6 mAh g −1 , respectivamente. As capacidades dos dois eletrodos diferentes caíram rapidamente nos primeiros ciclos, que estão relacionadas à reação irreversível no ciclo inicial. Em seguida, as capacidades dos eletrodos são estabilizadas para os ciclos contínuos. A eficiência coulômbica do eletrodo NMO / CNT se aproxima gradualmente de 100% e se mantém estável durante os ciclos seguintes. Para o eletrodo NMO / CNT, ele oferece uma capacidade reversível de 53,2 mAh g −1 após 150 ciclos, melhor do que o eletrodo NMO (40 mAh g −1 ) A elevada capacidade específica de descarga pode advir da introdução da rede de transmissão eletrónica do CNT, que promove a transferência de carga e a evolução de fase. Além disso, o CNT pode tamponar o estresse e a tensão sobre o Na + desinserção / inserção de íons por serem flexíveis [23]. Além disso, a estrutura esférica do NMO / CNT pode fornecer a difusão rápida do íon Na e do eletrólito. O aprimoramento do desempenho eletroquímico de NMO / CNT também pode ser atribuído ao uso de um eletrólito adequado. Para fins de comparação, uma célula foi montada com 1 M Na 2 SO 4 solução aquosa como eletrólito. Esta célula entregou uma capacidade de descarga reversível de apenas cerca de 24 mAh g −1 após 150 ciclos (Fig. 5b), ou seja, a capacidade reversível do sistema foi significativamente reduzida quando não há ZnSO 4 no eletrólito.
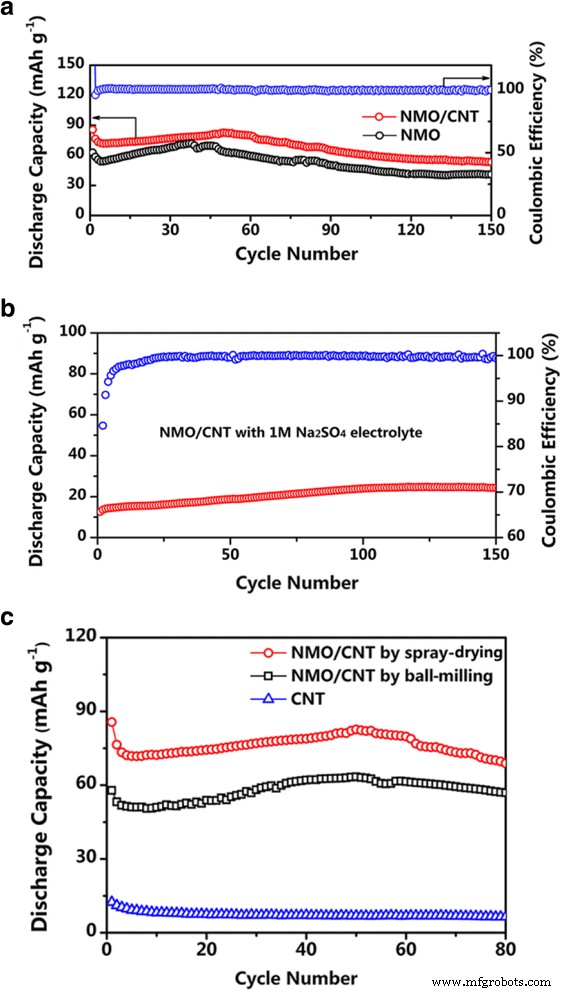
Desempenhos de ciclismo a 4 C. a Comparação do desempenho de ciclagem dos eletrodos NMO e NMO / CNT e eficiência coulômbica do eletrodo NMO / CNT. b Desempenho de ciclagem e eficiência coulômbica do eletrodo NMO / CNT com 1 M Na 2 SO 4 eletrólito. c Comparação de desempenho de ciclagem de eletrodos NMO / CNT por meio do método de secagem por pulverização e método de moagem de bolas, respectivamente
A fim de ilustrar um efeito positivo da morfologia do compósito NMO / CNT em seus desempenhos eletroquímicos, o compósito NMO / CNT não esférico foi sintetizado por meio de um método simples de moagem de bolas. NMO e CNT com uma razão de peso de 87:13 foram misturados por moagem de bolas a 400 rpm por 6 h para obter este material compósito de referência. O desempenho eletroquímico deste compósito é mostrado na Fig. 5c junto com o do compósito esférico NMO / CNT por secagem por pulverização. Pode ser visto que NMO / CNT não esférico exibe capacidades de descarga notavelmente mais baixas em comparação com a contraparte esférica, composto NMO / CNT por secagem por pulverização. Na Fig. 5c, os dados eletroquímicos para CNT puro foram incluídos para avaliar sua contribuição para a capacidade da célula. CNT oferece uma pequena capacidade reversível de 6,5 mAh g −1 a 4 C e não contribui notavelmente para a capacidade total, e seu papel principal é aumentar a condutividade do composto e apoiar suas propriedades mecânicas.
Para demonstrar o desempenho da taxa do composto NMO / CNT, as capacidades de taxa foram testadas em várias densidades de corrente de 1 a 4 C. A Figura 6 mostra que o composto NMO / CNT oferece uma capacidade de descarga reversível de 96, 77, 66 e 58 mAh g −1 na corrente de 1, 2, 3 e 4 C, respectivamente. É importante ressaltar que, após as medições de alta densidade de corrente, uma vez que a densidade de corrente voltou a 1 C, a capacidade específica foi quase revertida ao mesmo nível. Como pode ser visto, as capacidades de descarga reversível do NMO em cada taxa de corrente foram menores do que a do NMO / CNT, mas o eletrodo também recuperou quase cheio de sua capacidade reversível 50 mAh g −1 quando a taxa foi modulada de volta para 1 C. Esses resultados não apenas ilustram que o CNT do composto NMO / CNT aumentou a capacidade reversível, mas também indicam que o material NMO tem a alta tolerância a abusos que pode exibir excelente desempenho de taxa. O excelente desempenho da taxa de NMO e do composto NMO / CNT pode ser devido à estrutura microesférica que pode aumentar o transporte de massa do íon Na e do eletrólito.
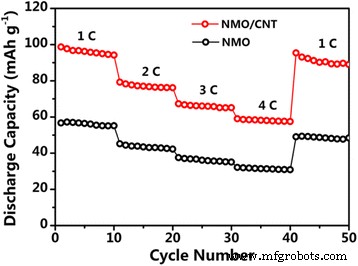
Classifique o desempenho dos eletrodos NMO e NMO / CNT de 1 a 4 C
Espectroscopia de impedância eletroquímica (EIS) dos eletrodos NMO e NMO / CNT medida com a faixa de frequência de 10 5 –0,01 Hz são exibidos na Fig. 7. A inserção da Fig. 7a é um modelo de circuito equivalente simples aplicado para ajustar o EIS. O R S é a resistência eletrolítica dos componentes da célula, R CT está relacionado ao procedimento de transferência de carga na interface eletrodo-eletrólito, Z W é a impedância de Warburg associada à difusão do íon sódio no eletrodo, e o CPE está associado à capacitância de camada dupla [38]. Conforme mostrado na Fig. 7a, a resistência de transferência de carga ( R CT ) do eletrodo NMO / CNT é 133 Ω, e o valor é significativamente menor do que o do NMO (207 Ω), demonstrando que os CNT são benéficos para o aprimoramento do desempenho eletroquímico do eletrodo NMO / CNT. Além disso, a resistência do NMO / CNT aumenta gradativamente com o andamento do ciclo conforme mostrado na Fig. 7b, que está relacionada à ativação interna do eletrodo, correspondendo à imagem do desempenho do ciclismo (Fig. 5a). Os espectros EIS do 50º e 100º ciclos são quase idênticos, o que sugere que as resistências são relativamente estáveis à medida que o ciclo avança.
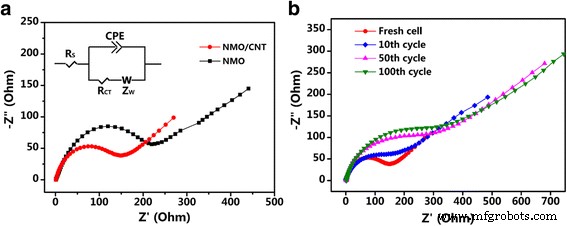
(a) Espectros EIS de eletrodos NMO e NMO / CNT no novo ciclo e o modelo de circuito equivalente de ajuste de plotagem ( inserção ) (b) Espectros EIS do eletrodo NMO / CNT na célula nova, 10º, 50º e 100º ciclos
A Tabela 2 compara os dados de desempenho relatados para o Na x MnO 2 à base de cátodos para baterias de íon de sódio aquosas. Pode-se observar que o eletrodo NMO / CNT preparado neste trabalho apresenta desempenho eletroquímico superior aos relatados. A uma alta taxa de 4 C, o eletrodo fornece uma capacidade de descarga aprimorada de 53,2 mAh g −1 com a menor faixa de potencial aplicada (1–1,85 V). Esses resultados indicam que o composto NMO / CNT é um cátodo promissor para baterias aquosas de íon sódio.
Conclusões
Em resumo, as partículas de NMO / CNT foram sintetizadas com sucesso pelo método de secagem por spray. Além disso, foi desenvolvida uma bateria aquosa de íon de sódio usando Zn metálico e NMO / CNT como eletrodos negativo e positivo, respectivamente. O eletrodo NMO / CNT mostra uma capacidade de descarga maior de 96 mAh g −1 com taxa de 1 C e 53,2 mAh g −1 a uma taxa de 4 C mesmo após 150 ciclos completos em comparação com o eletrodo NMO. O desempenho eletroquímico superior do composto NMO / CNT pode surgir de sua estrutura esférica que pode fornecer transporte rápido e a adição de CNT que pode aumentar a condutividade do composto. No geral, o NMO / CNT é um material catódico promissor para ASIBs seguros e eficientes.
Abreviações
- ASIBs:
-
Baterias de íon de sódio aquosas
- CV:
-
Voltametria cíclica
- EIS:
-
Espectroscopia de impedância eletroquímica
- HR-TEM:
-
Microscópio eletrônico de transmissão de alta resolução
- LIBs:
-
Baterias de íon-lítio
- NMO:
-
Na 4 Mn 9 O 18
- NMO / CNT:
-
Na 4 Mn 9 O 18 / nanotubo de carbono
- NMP:
-
N -metil-2-pirrolidona
- PVDF:
-
Fluoreto de polivinilideno
- SAED:
-
Difração de elétrons de área selecionada
- SEM:
-
Microscopia eletrônica de varredura
- TG:
-
Termogravimétrico
- XRD:
-
Difração de pó de raios-x
Nanomateriais
- Impressão 3D com material de alta resistência - Composto de Fibra de Carbono-Náilon
- NiCo2S4 @ NiMoO4 Core-Shell Heterostructure Nanotube Arrays cultivados em Ni Foam como um eletrodo livre de aglutinante exibiu alto desempenho eletroquímico com alta capacidade
- Composto mecânico de LiNi0.8Co0.15Al0.05O2 / nanotubos de carbono com desempenho eletroquímico aprimorado para baterias de íon-lítio
- Alto desempenho fotocatalítico de dois tipos de fotocatalisadores compostos de TiO2 modificados com grafeno
- Síntese e propriedades eletroquímicas de materiais catódicos de LiNi0,5Mn1,5O4 com dopagem composta Cr3 + e F− para baterias de íon-lítio
- Composto de MoS2 / Acetileno com poucas camadas como um ânodo eficiente para baterias de íon-lítio
- Nanoesferas de carbono monodispersas com estrutura porosa hierárquica como material de eletrodo para supercapacitor
- Composto de carbono cerâmico CARBOPRINT® Si1
- Composto de carbono cerâmico CARBOPRINT® Si2
- Composto de carbono cerâmico CARBOPRINT® Si3



