Novo suporte de catalisador anódico para célula de combustível de metanol direto:caracterizações e desempenho de célula única
Resumo
Este estudo apresenta uma nova nanofibra de dióxido de titânio e carbono (TiO 2 -CNF) suporte para catalisador anódico em célula de combustível de metanol direto. O processo de síntese catalítica envolve vários métodos, nomeadamente os métodos de sol-gel, electrospinning e deposição. O eletrocatalisador sintetizado é comparado com outros três eletrocatalisadores com diferentes tipos de suporte. Todos esses eletrocatalisadores diferem com base em uma série de características físicas e eletroquímicas. Resultados experimentais mostram que o TiO 2 O suporte -CNF deu a maior densidade de corrente em 345,64 mA mg catalisador −1 , o que é equivalente a 5,54 vezes maior do que o suporte de carbono, enquanto a densidade de energia é quase o dobro do eletrocatalisador comercial.
Histórico
Uma célula de combustível de metanol direto (DMFC) é um dos candidatos mais promissores para uma fonte de energia renovável. É um sistema gerador de energia que produz energia elétrica ao converter a energia de um combustível líquido químico (metanol) diretamente, sem dispositivos auxiliares. DMFCs são movidos por suas possibilidades emocionantes em transporte e aplicação estacionária. Além disso, os pesquisadores também acreditam que este sistema é uma das fontes de energia mais promissoras para muitas aplicações móveis e portáteis, bem como uma nova alternativa à tecnologia de bateria recarregável. Os DMFCs oferecem muitas vantagens, incluindo um sistema de tamanho e peso menores. Eles também são portadores de energia limpa e reduzem a poluição. Porém, apesar dessas vantagens, também enfrentam problemas que dificultam sua comercialização. Os problemas mais desafiadores são a fraca cinética de eletro-oxidação do metanol e o baixo desempenho do sistema. O custo geral precisa ser reduzido e problemas como cruzamento de metanol, durabilidade, estabilidade, calor e gerenciamento de água precisam ser melhorados para que o DMFC seja bem-sucedido [1,2,3].
O desenvolvimento do DMFC começou há uma década com a criação de muitas soluções que utilizavam catalisadores. Um dos estudos sobre a melhoria do desempenho do DMFC analisou diferentes estruturas de suporte do catalisador, incluindo nanofibra de carbono (CNF), nanotubo de carbono (CNT), nanofio de carbono (CNW) e outras camadas de estrutura. A adição de novo material ao catalisador, incluindo a criação de um novo catalisador híbrido, também se tornou uma tendência na evolução do DMFC [4,5,6]. Apesar desta pesquisa, ainda existem problemas, especialmente aqueles relacionados à baixa atividade catalítica, estabilidade e condutividade para operação eletrônica e protônica.
Platina (Pt) é o melhor catalisador para a reação de oxidação do hidrogênio (HOR) e a reação de redução do oxigênio (ORR). Apesar de ser eficaz em aplicações de eletrocatalisadores [7,8,9,10], Pt é caro, o que requer mais pesquisas para encontrar um novo catalisador. Atualmente, o bimetálico platina-rutênio (PtRu) é o melhor catalisador para DMFC. O uso deste catalisador reduziu o carregamento de Pt, o que reduziu o custo do eletrocatalisador de DMFC com uma proporção padrão de 1:1. O papel do Ru neste catalisador bimetálico é remover o monóxido de carbono (CO) dos sítios ativos para o HOR o que leva a superar o envenenamento por CO do catalisador [11, 12]. De acordo com um estudo de Bock et al., PtRu apresentou atividade catalítica superior no DMFC, e ficou claro que o desempenho catalítico dependia fortemente da distribuição dos sítios Pt e Ru em nível atômico [13]. No entanto, o problema de oxidação de baixo metanol não pode ser resolvido usando o catalisador PtRu, portanto, alterações adicionais do catalisador devem ser realizadas para auxiliar a indústria de células de combustível.
Os óxidos de metal são os materiais mais importantes usados para melhorar a eletrocatálise de DMFC. Dióxido de titânio (TiO 2 ), também conhecido como titânia, é uma substância inorgânica naturalmente estável, não inflamável e altamente resistente à corrosão. Titânia também não é classificada como uma substância perigosa pelo Sistema Globalmente Harmonizado (GHS) de Classificação e Rotulagem de Produtos Químicos das Nações Unidas (ONU). Além disso, as estruturas cristalinas do TiO 2 são termodinamicamente estáveis e ajudam a criar um material composto com boa estabilidade eletroquímica e térmica [14]. Os portadores de carga da forma anatase tornam-se excitados mais profundamente no material a granel, criam mais reações de superfície e aumentam gradativamente a atividade catalítica [15]. O comportamento eletrônico do material é aprimorado quando a interação entre o TiO 2 óxido de metal e o outro material ocorre. Este aumento também pode melhorar a atividade de oxidação, reduzindo os potenciais de oxidação do CO [6]. O uso de TiO 2 como um suporte para o metal catalisador afeta a cinética da reação e o mecanismo de reação [16]. TiO 2 tem todos os benefícios listados anteriormente para muitas aplicações em vários setores. Apesar desses benefícios, o principal problema que impede seu uso generalizado para aplicações em células de combustível é sua baixa condutividade. No entanto, para superar este problema, altas cargas de um catalisador de Pt sobre TiO 2 composto com um material condutor elétrico, como carbono dopado com N, e o emprego de TiO subestequiométrico 2 são necessários [5].
Este estudo relatou a síntese e caracterização de nanofibra de dióxido de titânio-carbono (TiO 2 -CNF) depositado em um catalisador de platina-rutênio (PtRu) para a aplicação de DMFC. O objetivo do estudo foi sintetizar o eletrocatalisador composto com TiO 2 em uma estrutura de nanofibra que pode reduzir o efeito de envenenamento do catalisador enquanto aumenta a atividade catalítica para melhorar o desempenho do DMFC mais do que o eletrocatalisador PtRu / C comercial. TiO 2 -CNF foi preparado por eletrofiação, seguido de carbonização; finalmente, PtRu foi depositado com uma anotação de PtRu / TiO 2 -CNF. Para caracterizar o PtRu / TiO preparado 2 Foram utilizados eletrocatalisadores compostos CNF com diferentes suportes, difração de raios X (XRD), Brunauer-Emmett-Teller (BET), microscópio eletrônico de varredura (MEV) e microscópio eletrônico de transmissão (TEM). O desempenho do eletrocatalisador foi avaliado por voltametria cíclica (CV), área de superfície eletroquímica (ECSA), análise de Tafel, cronoamperometria (CA) e célula única DMFC. Todas as informações de desempenho foram comparadas com vários outros suportes, incluindo C, CNF e TiO 2 . Com base nos resultados experimentais, foi discutido o efeito da utilização do óxido metálico como suporte para melhorar a atividade catalítica na DMFC.
Métodos
Materiais
Isopropóxido de titânio (TiPP, 97%) foi obtido da Sigma-Aldrich Co., Ltd. Poli (acetato de vinil) (PVAc (Mw 500.000)), dimetilformamida (DMF (99,8%)) e ácido acético (99,7%) foram recebidos da Sigma-Aldrich Co., Ltd. Etanol (99,8%) foi adquirido da R&M Chemical Reagents. Esses reagentes químicos foram usados para a preparação de nanofibras. A deposição incluiu um precursor Pt, H 2 PtCl 6 (40% de conteúdo), da Merck, Alemanha, e um precursor de Ru, RuCl 3 (Conteúdo de 45-55%) e agente redutor, boro-hidreto de sódio (NaBH 4 , 96%), da Sigma-Aldrich Co., Ltd. O suporte de catalisador comercial para C, CNF e TiO 2 nanopó foram obtidos de Cabot Corporation, Cheap Tubes Inc. e Sigma-Aldrich Co., Ltd., respectivamente. As propriedades detalhadas para o suporte do catalisador estão tabuladas na Tabela 1. Todos os reagentes químicos foram usados sem purificação adicional.
Preparação do TiO 2 -CNF
TiO 2 -CNF foi sintetizado usando o método sol-gel e a técnica de eletrofiação. A solução de PVAc (11,5% em peso) foi preparada dissolvendo o polímero com DMF durante 1 h a uma temperatura de 60 ° C e foi continuamente agitada durante a noite. 50% em peso de TiPP e algumas gotas de etanol e ácido acético foram misturados na solução de PVAc e agitados com um homogeneizador até a mistura ficar homogênea. A solução misturada foi alimentada a partir de uma seringa com uma agulha de aço inoxidável para a técnica de eletrofiação a uma taxa constante de 0,1 mL h −1 , uma tensão aplicada de 16 kV, e uma distância de 18 cm entre a ponta e o coletor. A nanofibra eletrofiada foi seca por 5 h em temperatura ambiente e continuou a se estabilizar a 130 ° C por 8 h. A fibra foi carbonizada em forno tubular a 600 ° C por 2 h em atmosfera de nitrogênio. A fibra calcinada então passou por um processo de controle de tamanho usando um almofariz e pilão antes de ser usada neste estudo.
Preparação do eletrocatalisador composto
Todos os eletrocatalisadores foram sintetizados usando o método de deposição por redução química de NaBH 4 . Os 20% em peso de PtRu com a razão atômica de 1:1 são carregados em diferentes suportes de catalisador, que são suporte sintetizado, TiO 2 -CNF, e outros três suportes comerciais, C, CNF e TiO 2 . Uma mistura de água desionizada (água DI) e álcool isopropílico (IPA) foi adicionada ao material de suporte e sonicada por 30 min. Os precursores foram misturados na mistura de suporte e foram continuamente agitados por mais 30 minutos até que a solução estivesse bem misturada. O valor de pH da solução foi ajustado para 8 usando uma solução de NaOH 1 M. Em seguida, a temperatura da solução foi aumentada para 80 ° C. Um volume de 25 mL de uma solução 0,2 M de NaBH 4 foi adicionado gota a gota à solução e agitado durante mais uma hora. A mistura foi resfriada, filtrada e lavada repetidamente com água DI. O pó do eletrocatalisador foi seco por 3 h a 120 ° C sob vácuo e triturado com um pilão e almofariz para obter um pó fino.
Caracterização do eletrocatalisador
O padrão de difração de raios X (XRD) e a estrutura cristalina para todos os eletrocatalisadores foram investigados com um difratômetro de raios X (D8 Advance / Bruker AXS Germany) usando amostras em pó e operado a 40 kV e 20 mA. A área de superfície e a análise de tamanho de poro usando BET foi tratada pela Micromeritics ASAP 2020 na condição de isoterma de adsorção / dessorção de nitrogênio a 77 K. Um estudo da morfologia da superfície para as nanofibras suportadas por eletrocatalisador e o eletrocatalisador preparado foi conduzido usando elétron de varredura de emissão de campo microscopia (FESEM (SUPRA 55 VP)). A análise de mapeamento foi feita para observar a distribuição dos elementos em uma área selecionada no eletrocatalisador composto. A estrutura detalhada do eletrocatalisador de suporte e compósito foi analisada com imagens de alta resolução obtidas por microscopia eletrônica de transmissão (TEM (Tecnai G2 F20 X-Twin)).
Avaliação da medição eletroquímica
As medições eletroquímicas foram avaliadas pela estação de trabalho eletroquímica Autolab. A atividade da reação de oxidação do metanol (MOR) para o eletrocatalisador foi medida usando a voltametria cíclica (CV) de um sistema de células de três eletrodos. Este sistema utilizou um eletrodo de carbono vítreo (GCE, 3 mm de diâmetro) como eletrodo de trabalho e eletrodos de Pt e cloreto de prata / prata (Ag / AgCl) como eletrodos contador e de referência, respectivamente, operados em temperatura ambiente. O eletrodo de trabalho deve ser limpo com papel de polir e alumina antes de ser usado. A preparação da tinta do eletrocatalisador para o eletrodo de trabalho foi dispersa ultrassonicamente com 15 mg do eletrocatalisador em uma mistura de 400 μL de água DI, 400 μL de IPA e 125 μL de solução de Nafion (5% em peso) por 30 min. Uma micropipeta foi usada para transferir 2,5 μL de tinta do eletrocatalisador para um GCE. O eletrodo de trabalho foi seco ao ar por 1 h em temperatura ambiente e, em seguida, aquecido em um forno por 30 min a 80 ° C. O eletrodo de trabalho estava então pronto para a medição CV. Uma solução de 0,5 M H 2 SO 4 em metanol 2 M foi preparado como um eletrólito. Esta solução de eletrólito foi borbulhada com gás nitrogênio (N 2 ) por 20 min para atingir o conteúdo livre de oxigênio. A medição de CV foi realizada a uma taxa de varredura de 20 mV s −1 , e a faixa de potenciais foi de 0 a 1,1 V vs. Ag / AgCl. O desempenho de longo prazo de todos os eletrocatalisadores foi avaliado por meio da cronoamperometria (CA) na solução eletrolítica a um potencial de 0,5 V por 3600 s.
Fabricação de MEA
O conjunto de eletrodo de membrana (MEA) consiste em três partes principais:membrana, ânodo e cátodo. Nafion 117 é selecionado como uma membrana, e a membrana é tratada para remover as impurezas usando peróxido de hidrogênio (H 2 O 2 ) e água DI conforme aplicada no estudo de Hasran et al. [17]. A membrana tratada é armazenada no copo cheio de água DI até que esteja pronta para ser usada. O pano de carbono é usado como camada de suporte do ânodo e do cátodo. Este pano de carbono é tratado com 5% em peso de politetrafluoroetileno (PTFE) para torná-lo impermeável. O pano de carbono é imerso na solução de PTFE e seco no forno por 30 min a 380 ° C. A camada de suporte é revestida com uma camada de difusão de gás de carbono, onde a carga é de 2 mg cm −2 . O carbono é misturado com a dispersão IPA e Nafion D520 (Dupont). A pasta de carbono é fundida no pano de carbono e seca no forno a 100 ° C durante 1 h. Então, a camada do eletrocatalisador está pronta para ser revestida e sintetizada por PtRu / TiO 2 -CNF e eletrocatalisador comercial PtRu / C, usado para a parte do ânodo, e Pt / C para a parte do cátodo. 2 mg cm −2 carregamento do eletrocatalisador é adicionado com IPA (1100 μL), água DI (300 μL) e dispersão de Nafion (24 mg). A solução é dispersa no homogeneizador por 1 min e lançada no tecido de carbono. O ânodo e o cátodo são secos no forno por 1 hora a 100 ° C. O ânodo e o cátodo são fixados juntamente com a membrana no meio usando uma prensa a quente na condição de 135 ° C e 50 kPa por 3 min. O MEA está pronto para ser usado em testes de desempenho de célula única.
Teste de desempenho de célula única
O teste de desempenho de célula única DMFC foi conduzido em condição passiva e à temperatura ambiente. O MEA com um 2 de 4 cm a área ativa é indicada na célula única, onde a parte do ânodo é fixada no tanque de metanol. Dez mililitros de metanol 3 M são colocados no tanque e testados usando potenciostato / galvanostato (WonATech, Coréia). A curva de polarização celular é obtida para diferentes eletrocatalisadores.
Resultados e discussão
Caracterização estrutural
O padrão e a estrutura cristalina do suporte de catalisador fabricado, TiO 2 -CNF, eletrocatalisador sintetizado, PtRu / TiO 2 -CNF e outros eletrocatalisadores (PtRu / C, PtRu / CNF e PtRu / TiO 2 ) foram investigados por análise de XRD. Esta análise foi concluída usando um difratômetro de raios-X na faixa de 5 ° -90 ° com 2 θ , conforme mostrado na Fig. 1. O resultado para TiO sintetizado 2 -CNF mostra a existência de todos os materiais, TiO 2 , e C. O pico de difração de 25 ° (1 0 1) representa o TiO 2 estrutura anatase, enquanto o pico em 27 ° (1 1 0) é o TiO 2 estrutura do rutilo. Essas estruturas existentes se formam em estrutura tetragonal (estrutura cristalográfica para anatásio e rutilo) [18]. No entanto, esta amostra tinha a estrutura anatase porque o TiO 2 a estrutura mudou de anatásio para rutilo enquanto a amostra foi exposta a temperaturas superiores a 700 ° C [19], enquanto a temperatura utilizada nesta pesquisa foi de apenas 600 ° C.
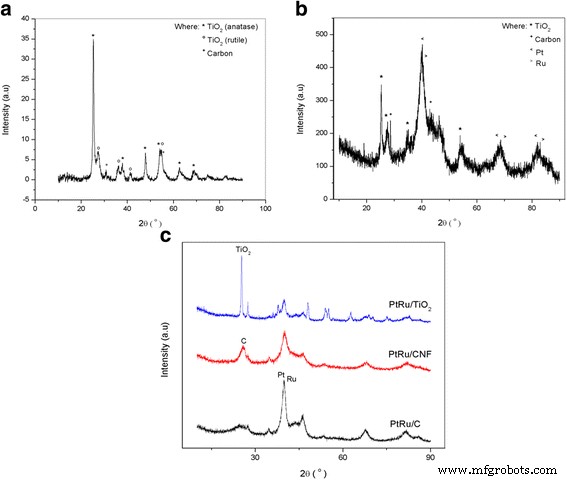
Padrões de difração de raios-X. a TiO 2 -CNF, b PtRu / TiO 2 -CNF e c eletrocatalisadores comparados
O TiO 2 -CNF mostra mais picos de difração para TiO 2 anatase a 38 ° (1 1 2), 48 ° (2 0 0), 55 ° (2 1 1), 63 ° (2 0 4), 69 ° (1 1 6) e 75 ° (2 1 5) , enquanto aqueles do TiO 2 rutilo são 36 ° (1 0 1), 41 ° (1 1 1) e 54 ° (2 1 1). O carbono aparece nos picos de difração de 31 ° (1 1 0) e 55 ° (2 1 1) na estrutura cúbica. O padrão XRD para PtRu / TiO 2 O eletrocatalisador -CNF mostra o pico de difração para todos os eletrocatalisadores envolvidos, Pt, Ru, TiO 2 e C. O pico para TiO 2 e C é quase o mesmo com o TiO 2 Amostra -CNF, e Pt e Ru se destacam com outros quatro picos para cada material, que é Pt em 39,7 ° (1 1 1), 46,2 ° (2 0 0), 67,5 ° (2 2 0) e 81,3 ° (3 1 1). Os picos de difração para Ru são 40,7 ° (1 1 1), 47 ° (2 0 0), 69 ° (2 2 0) e 83,7 ° (3 1 1). Ambos os metais vêm na estrutura cúbica. O eletrocatalisador sintetizado é comparado com alguns eletrocatalisadores suportados com diferentes suportes de catalisador, nomeadamente negro de fumo (PtRu / C), nanofibra de carbono (PtRu / CNF) e nanopartículas de dióxido de titânio (PtRu / TiO 2 ), e o padrão de difração é descoberto na Fig. 1c.
Os ângulos de Bragg altos eram claramente visíveis, especialmente na faixa de 25 ° –60 ° para toda a amostra do eletrocatalisador. Isso mostrou que houve uma interação bimetálica ou liga que ocorreu no catalisador [20]. Uma intensidade fraca e ampla foi observada para todas as amostras do eletrocatalisador, o que ilustra altas dispersões na amostra preparada. O tamanho do cristalito foi medido usando a equação de Debye-Scherrer [8]; tamanho do cristalito =0,98 α / β cos θ . Onde α é o comprimento de onda do raio-X, θ é o ângulo no pico, e β é a largura do pico na metade da altura. O valor do tamanho do cristalito estava disponível através do software Eva para análise dos resultados de XRD, e foi calculado usando a equação de Debye-Scherrer. O tamanho do cristalito para todas as amostras está tabulado na Tabela 2. O tamanho do cristalito para PtRu foi calculado como 4,64 a 9,84 nm, TiO 2 variou de 19 a 38,4 nm, e C estava entre 10,7 e 19,2 nm.
A área de superfície e a análise da porosidade de todas as amostras do eletrocatalisador foram analisadas usando a análise BET. A isoterma de absorção / dessorção de nitrogênio é realizada a 77 K. A área de superfície, o volume total dos poros e o diâmetro médio dos poros de PtRu / TiO 2 -CNF, PtRu / C, PtRu / CNF e PtRu / TiO 2 os eletrocatalisadores estão listados na Tabela 3. A área de superfície BET para a estrutura de nanofibras do composto de óxido de metal, PtRu / TiO 2 Eletrocatalisador -CNF, mostra o valor mais baixo com 50,59 m 2 / g, seguido por PtRu / CNF, PtRu / TiO 2 e eletrocatalisadores PtRu / C em ordem crescente. Os resultados obtidos neste estudo são próximos aos resultados da área de superfície BET conduzida por outro estudo [6], onde o eletrocatalisador PtRu / C mostra uma área de superfície muito maior em comparação com o eletrocatalisador composto de óxido metálico.
O volume total do poro, V Poro total , mostra os resultados em ordem crescente iniciada por PtRu / TiO 2 -CNF
Os gráficos de isoterma de adsorção / dessorção de nitrogênio a 77 K para todos os eletrocatalisadores são resumidos na Fig. 2. Os resultados mostram que os poros para todas as amostras de eletrocatalisadores destacam propriedades mesoporosas, que têm um diâmetro médio dentro da faixa de 2-50 nm, que pode em grande parte pode ser atribuído à grande lacuna encontrada na rede do eletrocatalisador. Este tipo de eletrocatalisador tem a capacidade de aumentar o nível de distribuição e homogeneidade do catalisador imobilizado, resultando em melhora da estabilidade e da atividade catalítica [22].
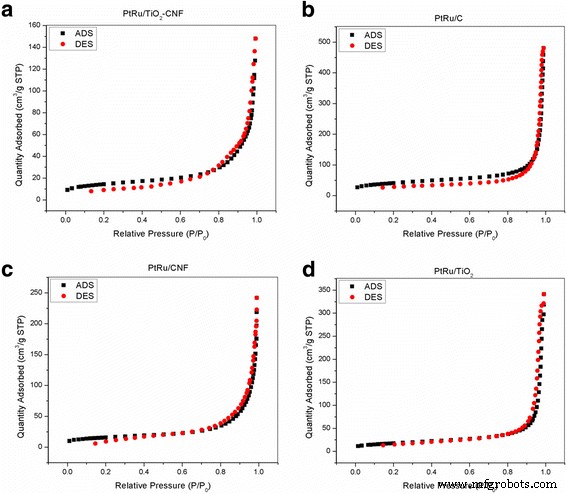
Isoterma de adsorção de nitrogênio (ADS) e dessorção (DES) a 77 K. a PtRu / TiO 2 -CNF, b PtRu / C, c PtRu / CNF e d PtRu / TiO 2
O diâmetro médio dos poros das quatro amostras de eletrocatalisadores testadas estava entre 22 e 33 nm, e o diâmetro dos poros do PtRu / TiO 2 -CNF apresentou o menor diâmetro em comparação com outros eletrocatalisadores. O tamanho de diâmetro pequeno ilustra o tamanho da partícula como um todo. O pequeno tamanho de partícula tem uma alta relação superfície-volume e potencialmente resulta em aumento da reatividade e solubilidade da superfície e é capaz de alterar o perfil de toxicidade da substância. Além disso, a observação no gráfico de isoterma de adsorção / dessorção de nitrogênio parece plana a uma pressão relativamente baixa ( P / P o ≤ 0,6), o que pode ser devido à absorção de micropore na amostra. Em uma área de pressão relativamente alta (0,6 < P / P o <1,0), há um incremento na capacidade de adsorção da amostra devido à adsorção de moléculas de nitrogênio em monocamada e / ou multicamadas na meso-estrutura.
A Figura 9 mostra as imagens SEM para o suporte de nanofibras, TiO 2 -CNF. A imagem ilustra que a nanofibra é produzida suavemente sem quaisquer aglomerados, grânulos ou nanofibras conectadas, o que acontece devido aos parâmetros de eletrofiação equivalentes [23]. A distribuição do tamanho do diâmetro do TiO 2 -CNF é investigado através da coleta de 100 medições de diâmetro para este suporte de catalisador e analisado pelo “Software Origin”, e o tamanho do diâmetro de distribuição é 136,73 ± 39,56 nm no intervalo de 90-170 nm.
O eletrocatalisador preparado, PtRu / TiO 2 -CNF, também foi submetido à análise SEM, e a imagem é mostrada na Fig. 10. A Figura 10a é o catalisador depositado no suporte, PtRu / TiO 2 -CNF, após o processo de moagem. A imagem SEM identificou que a fibra longa é coberta com nanopartículas de Pt e Ru. No entanto, a imagem mostra alguma aglomeração de nanopartículas de Pt e Ru. Para ver a distribuição de Pt e Ru, o mapeamento é mostrado na Fig. 10b para Pt e na Fig. 10c para Ru. Os resultados do mapeamento ilustraram que os dois metais estavam uniformemente dispersos na nanofibra; no entanto, ocorreu alguma aglomeração para Pt devido a um erro durante o processo de deposição. A aglomeração de nanopartículas foi um resultado da reação devido ao uso excessivo da solução de NaOH durante o ajuste do pH para o processo de deposição [24].
As imagens TEM para o suporte de catalisador preparado, TiO 2 -CNF e eletrocatalisador, PtRu / TiO 2 -CNF, são mostrados na Fig. 11. As imagens TEM do suporte do catalisador Fig. 11a mostram que o TiO 2 foi homogeneamente disperso em um diâmetro de 136 nm de nanofibra de carbono, devido à dispersão homogênea da solução de polímero e TiO 2 precursor durante o método sol-gel. A Figura 11b mostra a imagem do catalisador depositado no TiO 2 -CNF, onde partículas de PtRu com um diâmetro de aproximadamente 7 nm foram depositadas no TiO 2 -CNF e exposto ao TiO 2 superfície. Esta conexão e a exposição ao TiO 2 pode produzir um ponto de reação mais ativo durante a performance. No entanto, as partículas de PtRu aglomeraram-se e não foram distribuídas homogeneamente na superfície da nanofibra.
Caracterização eletroquímica
A caracterização eletroquímica é aplicada a todos os catalisadores, para verificar seu potencial e desempenho como catalisador anódico em DMFC. Existem duas medições principais nesta seção, que é a voltametria cíclica (CV), para medir o desempenho eletrocatalítico, e a cronoamperometria (CA), para testar a estabilidade e durabilidade das amostras a longo prazo. A Figura 3 mostra os perfis de CV de todos os catalisadores em 0,5 M H 2 SO 4 solução na faixa de potencial entre - 0,2 e 1,2 V. A região de adsorção / dessorção de hidrogênio, na faixa de - 0,2 a 0,1 V, também é indicada quando a área de superfície ativa eletroquímica (ECSA) é calculada. O ECSA é a estimativa da área de superfície das nanopartículas de PtRu no eletrocatalisador [25]. O procedimento envolveu um ciclo de corrente do eletrodo na faixa de voltagem, onde as reações de transferência de carga são limitadas por adsorção nos locais de ativação. A carga total necessária para a adsorção / dessorção em monocamada é usada como sítios de superfície reativos para ECSA [26]. O resultado de ECSA avaliado é relatado na Tabela 4. ECSA para a medição de CV foi determinado usando a equação abaixo:
$$ \ mathrm {ECSA} \ \ left ({\ mathrm {m}} ^ 2 {\ mathrm {g}} _ {\ mathrm {Pt}} ^ {- 1} \ right) =\ frac {Q} { \ varGamma. {W} _ {Pt}} $$
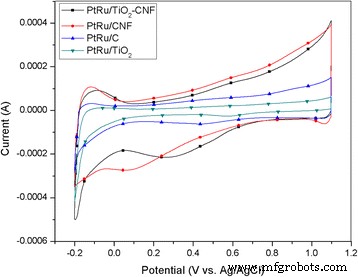
Perfis de voltametria cíclica dos diferentes suportes de catalisador, PtRu / TiO 2 -CNF, PtRu / CNF, PtRu / C e PtRu / TiO 2 em 0,5 M H 2 SO 4 solução na taxa de varredura de 20 mV s −1
onde Q é a densidade de carga ou área sob o gráfico ((C) do experimento CV), Γ (2,1 Cm Pt −2 ) é a constante para a carga necessária para reduzir a monocamada de prótons na Pt, e W Pt é o carregamento Pt (g Pt ) no eletrodo. Os resultados do cálculo ECSA mostram que o eletrocatalisador sintetizado, PtRu / TiO 2 -CNF, tem o maior valor de 10,4 m 2 g PtRu −1 , seguido de PtRu / CNF (8,4 m 2 / g PtRu ), PtRu / C (0,94 m 2 g PtRu −1 ), e PtRu / TiO 2 (0,76 m 2 g PtRu −1 ) Isso aconteceu devido a vários fatores-chave. Um deles é o tamanho do cristalito de PtRu, conforme mencionado na Tabela 2 da análise de XRD; o tamanho do cristalito PtRu para PtRu / TiO 2 -CNF é o menor e mostra um alto valor de ECSA. O menor tamanho de cristalito pode provocar um aumento no catalisador e na área de superfície de reação. A tendência do tamanho do cristalito é seguida pela tendência do valor ECSA para PtRu / CNF e PtRu / C. No entanto, PtRu / TiO 2 amostra supostamente pode produzir valor de ECSA maior do que PtRu / C, uma vez que o tamanho do cristalito é menor, mas o ECSA obtido é menor. Isso pode ocorrer devido à aglomeração da partícula de PtRu na amostra. Esta aglomeração pode reduzir a área de superfície potencial para reagir e diminuir o ECSA.
O desempenho eletrocatalítico do eletrocatalisador sintetizado e de outro eletrocatalisador foi analisado com CV, conforme ilustrado na Fig. 4. A curva CV para os eletrocatalisadores, incluindo PtRu / TiO 2 -CNF, PtRu / C, PtRu / CNF e PtRu / TiO 2 , é medido em metanol 2 M com H 0,5 M 2 SO 4 com saturado N 2 gás à temperatura ambiente. As curvas múltiplas são medidas dentro da faixa de potencial de - 0,1 a 1,1 V vs. Ag / AgCl. A Figura 4 mostra que a densidade de corrente de pico em ordem decrescente foi PtRu / TiO 2 -CNF> PtRu / CNF> PtRu / C> PtRu / TiO 2 . A densidade de corrente de pico de PtRu / TiO 2 -CNF para o MOR parecia ser de aproximadamente 0,639 V vs. Ag / AgCl. A densidade de corrente de pico e outros valores de CV para todas as amostras são relatados na Tabela 4. O valor de densidade de corrente para o PtRu / TiO 2 O catalisador -CNF é 345,64 mA (mg PtRu ) −1 , que são 1,85 e 5,54 vezes maiores do que PtRu / CNF e eletrocatalisador comercial, PtRu / C. Isso mostra que o TiO 2 O suporte do catalisador -CNF foi um substituto melhor para o suporte do catalisador de negro de fumo. Isso porque a mistura de nanofibras, por meio do processo de carbonização, pode aumentar a condutividade elétrica e térmica do catalisador [27].
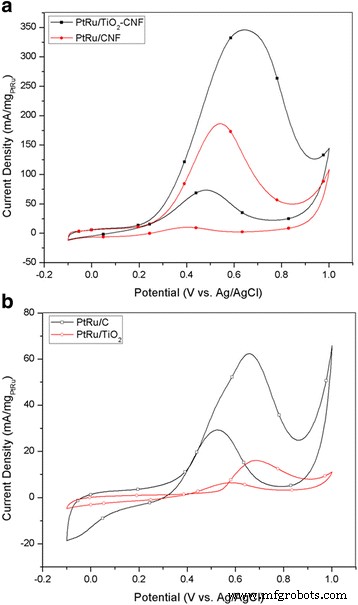
CV em metanol 2 M e H 0,5 M 2 SO 4 na taxa de varredura de 20 mV s −1 . a PtRu / TiO 2 -CNF e PtRu / CNF. b PtRu / C e PtRu / TiO 2
A estrutura de nanofibra no eletrocatalisador composto pode aumentar a área de superfície geral e o local de reação ativo na área de superfície do eletrocatalisador. Outra vantagem era a presença de TiO de alta anatase 2 composição resultante da análise de XRD. Maior atividade eletrocatalítica é adquirida por anatase do que rutilo TiO 2 . A interação metal-suporte também mostra efeito positivo com maior densidade de corrente de pico, onde a combinação de material entre PtRu e TiO 2 -CNF exibe uma combinação bem-sucedida para eletrocatalisador em DMFC. O segundo maior pico de densidade de corrente com o valor de 186,29 mA / mg PtRu pertence a PtRu / CNF que é 2,99 vezes maior do que o eletrocatalisador comercial, PtRu / C. Esse resultado é compatível com o estudo de Zainoodin et al. [28] e Ito et al. [29]. A semelhança de PtRu / TiO 2 -CNF e PtRu / CNF é a estrutura de suporte do catalisador de nanofibras. A alta densidade de corrente de pico para ambas as amostras demonstra que a nanofibra pode dar um excelente desempenho de oxidação do metanol devido à capacidade da nanofibra de aumentar a área de superfície do eletrocatalisador e melhorar a atividade catalítica. O desempenho para PtRu / C é muito inferior ao que resultou da aglomeração de PtRu, onde o valor de ECSA e tamanho de cristalito de XRD são apresentados. Esta situação reduz o potencial da superfície do eletrocatalisador para ser um local ativo e diminui o desempenho do eletrocatalisador. A atividade muito baixa de PtRu / TiO 2 foi devido à natureza do TiO 2 suporte de catalisador com baixa condutividade elétrica [4]. Esses resultados mostram claramente que o meio eletrocondutor foi essencial para os sistemas catalisadores para uma reação eletroquímica [30].
As múltiplas curvas CV na Fig. 4a, b mostram a varredura invertida, e o pequeno pico de oxidação aparece entre 0,4 e 0,57 V vs. Ag / AgCl. A formação de espécies carbonáceas oxidadas incompletas durante o primeiro pico de oxidação resultou na pequena oxidação na varredura reversa, também conhecida como pico de oxidação reversa [31]. Este pico de oxidação mostra a tolerância do eletrocatalisador em relação às espécies carbonáceas, calculando a razão de avanço ( I f ) and reversed (I b ) oxidation peak. The oxidation peak ratio called as CO tolerance is tabulated in Table 4. The result shows that both samples using nanofiber support, PtRu/TiO2 -CNF, and PtRu/CNF have the highest electrocatalyst tolerance against carbonaceous species, which means these can lower the catalyst poisoning potential, with the ratio exceeding 4.7 respectively. This result shows that nanofiber structure and the combination of metal oxide in electrocatalyst can reduce the main problem faced by DMFC technology and have high potential to replace the commercial support used in this technology.
The synthesis electrocatalyst, PtRu/TiO2 -CNF, is compared with other PtRu-based electrocatalyst, nanostructured catalyst support, and combination of metal oxide in electrocatalyst for DMFC technology and shown in Table 5. The result shows that the peak current density for PtRu/TiO2 -CNF is the highest among other electrocatalysts. However, the high value of current density is obtained by using the nanostructure catalyst support and TiO2 as one of the side material in the composite electrocatalyst. Even though there are several different types of metal oxide used in the other study, the performance shows a gap with the TiO2 -utilized electrocatalyst.
Other than CV, linear sweep voltammetry (LSV) is one of the important electrochemical studies of electroactive substance. LSV is quite similar to CV, which measures the current response as a voltage function. Figure 5 shows the LSV plot for all the electrocatalysts that were measured in 2 M methanol and 0.5 M H2 SO 4 at the scan rate of 20 mVs −1 in the N2 gas environment. The result shows that the synthesized electrocatalyst, PtRu/TiO2 -CNF, shows the highest current density that was calculated over the electrode surface area. The trend of the current density for LSV and CV is equalized. The LSV point shows the rising region between 0.5 and 0.7 V vs Ag/AgCl, and this region is known as a Tafel region that appeared when the electron transfer kinetics occur in the electrocatalyst surface [32]. The LSV data is extracted to present Tafel plot, where it relates the electrochemical reaction rate to the overpotential.
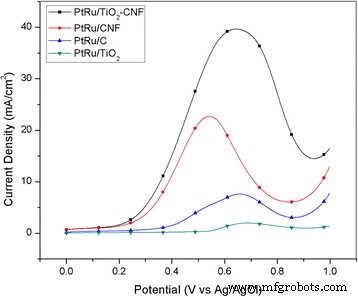
LSV in 2 M methanol and 0.5 M H2 SO 4 at the scan rate of 20 mV s −1 for all samples
The Tafel plot of overpotential, E , against log I is presented in Fig. 6, and data extraction of the plot is tabulated in Table 6. This plot can provide and calculate the slope of anodic Tafel plot (b a ) and ionic exchanging current density (j ) from the slope and interception of the Tafel plot. Anodic Tafel slope, b a , for all the electrocatalyst has not much difference in value, while the ionic exchange current density gives a big gap between each electrocatalyst. The ionic exchange current density is also known as a catalytic activity explainer [33]. The j for all electrocatalysts shows the difference, where the highest value belongs to PtRu/TiO2 -CNF with the value of 0.5012 mA cm −2 . This result demonstrates that the synthesized electrocatalyst can produce the highest catalytic activity of bimetallic PtRu compared with other electrocatalyst. Even though the bimetallic composition for all the electrocatalysts is same, the synthesized electrocatalyst gets a greater help from the metal oxide in producing the highest active area for catalytic activity. PtRu/CNF and PtRu/C electrocatalysts have the same value, while PtRu/TiO2 has the lowest of ionic exchange current density with 0.112 and 0.046 mA cm −2 , respectivamente.
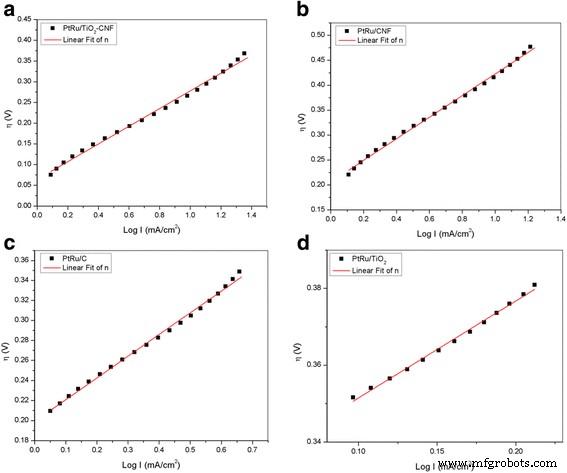
Tafel plot of the electrocatalyst a PtRu/TiO2 -CNF, b PtRu/CNF, c PtRu/C, and d PtRu/TiO2
The CA experiments were conducted to determine the stability and durability of the electrocatalyst for the long-term performance of MOR in a 2-M solution of methanol containing 0.5 M H2 SO 4 for 3600 s. Figure 7 shows the CA curve for the PtRu/TiO2 -CNF, PtRu/C, PtRu/CNF, and PtRu/TiO2 electrocatalysts at a constant potential, 0.5 V. The current density of PtRu/TiO2 electrocatalysts shows the effect of a sharp drop at the start of the experiment, possibly due to the effect of poisoning by methanol oxidation mediation. The PtRu/TiO2 -CNF, PtRu/CNF, and PtRu/C electrocatalysts showed a slight decline of approximately 5 and 3% in current density, respectively. After 3600 s, all of the electrocatalysts were stable, and the reducing current density ratios in increasing order are as follows:PtRu/CNF (6.16) < PtRu/TiO2 -CNF (6.54) < PtRu/C (11.66) < PtRu/TiO2 (14.82). The PtRu/TiO2 -CNF electrocatalyst showed the reducing current density ratio is slightly higher than PtRu/CNF, but this electrocatalyst reached the highest current density of all the electrocatalysts. This was due to good dispersion of the catalyst support and also to increased use of catalysis [6].
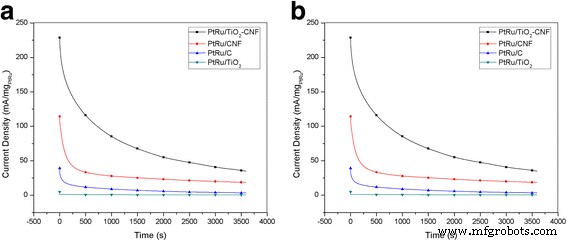
CA curve at potential of 0.5 V vs Ag/AgCl for PtRu/TiO2 -CNF, PtRu/C, PtRu/CNF, and PtRu/TiO2 catalisadores
DMFC Single-Cell Performance
The synthesized electrocatalyst, PtRu/TiO2 -CNF, with the highest electrochemical/half-cell performance was tested with single-cell performance. The performance is compared with commercial electrocatalyst, PtRu/C, using same composition, 20 wt% of PtRu. The 4-cm 2 anode electrocatalyst layer clamped with cathode and membrane to be MEA, ready for single-cell performance using 3 M methanol of passive system. Figure 8 shows the current–voltage curve for PtRu/TiO2 -CNF and PtRu/C. The PtRu/TiO2 -CNF showed the highest performance compared to the commercial electrocatalyst, which is 1.66 times higher. The maximum power density for synthesized electrocatalyst was 3.8 mW cm −2 , while PtRu/C was 2.2 mW cm −2 .
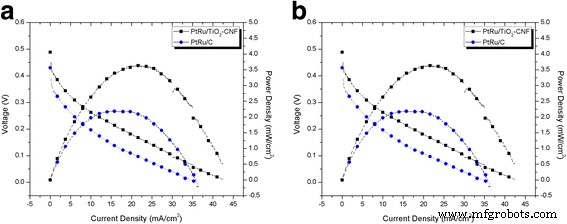
Current–voltage curve for PtRu/TiO2 -CNF and PtRu/C in 3 M methanol with 2 mg cm −2 catalyst loading at room temperature
The best PtRu/TiO2 -CNF performance is confirmed by comparing this result with the previous study of commercial PtRu/C electrocatalyst, using the same catalyst loading in passive mode system that is tabulated in Table 7. The overall electrochemical and single-cell performance conclude that the combination of bimetallic catalyst, PtRu, and introduction of metal oxide nanofiber with carbon nanofiber have high potential to be replaced with PtRu/C in DMFC technology (Figs. 9, 10, and 11). By using the low composition of bimetallic catalyst and electrocatalyst loading, the synthesized electrocatalyst reveals the superior DMFC performance.
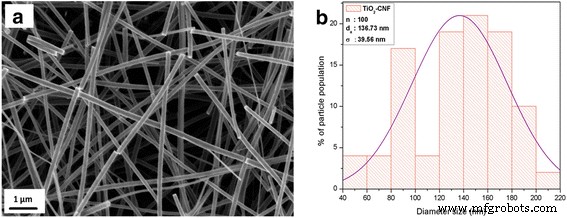
Imagens SEM. a TiO 2 -CNF image (magnification × 10,000). b Distribution of diameter size for TiO2 -CNF

PtRu/TiO2 -CNF catalyst after deposition and milling. a SEM images (magnification × 30,000), b mapping of Pt nanoparticles, and c mapping of Ru nanoparticles

TEM images for prepared a TiO 2 -CNF catalyst support and b PtRu/TiO2 -CNF electrocatalyst
Conclusões
O TiO 2 -CNF was synthesized using an electrospinning method and applied in the DMFC as a catalyst support for an anodic catalyst. The catalytic activity for the electrocatalyst was prepared for different catalyst supports including PtRu/TiO2 -CNF, PtRu/C, PtRu/CNF, and PtRu/TiO2 , which were compared with one another. The results showed that the prepared electrocatalyst, PtRu/TiO2 -CNF, had the highest current density, which was 5.54 times higher than that of the commercial electrocatalyst, PtRu/C. The DMFC single-cell performance of PtRu/TiO2 -CNF reveals the superior performance almost twice higher than that of PtRu/C. The highest catalytic activity was due to the nanofiber catalyst structure and the introduction of TiO2 as the catalyst support. The reaction with the metal support interface between the PtRu and TiO2 -CNF catalysts helped to improve the properties of the catalyst layer. PtRu/TiO2 -CNF is a promising candidate for support of the anode catalyst in DMFCs.
Abreviações
- BET:
-
Brunauer-Emmett-Teller
- CA:
-
Chronoamperometry
- CNF:
-
Carbon nanofiber
- CNT:
-
Nanotubo de carbono
- CNW:
-
Carbon nanowire
- CV:
-
Voltametria cíclica
- DI:
-
Deionizada
- DMF:
-
Dimetilformamida
- DMFC:
-
Direct methanol fuel cell
- ECSA:
-
Electrochemical surface area
- GCE:
-
Eletrodo de carbono vítreo
- GHS:
-
Globally Harmonized System
- HOR:
-
Hydrogen oxidation reaction
- IPA:
-
Isopropyl alcohol
- LSV:
-
Voltametria de varredura linear
- MEA:
-
Membrane electrode assembly
- MOR:
-
Methanol oxidation reaction
- ORR:
-
Oxygen reduction reaction
- PTFE:
-
Politetrafluoroetileno
- SEM:
-
Microscópio eletrônico de varredura
- TEM:
-
Microscopia eletrônica de transmissão
- UN:
-
Nações Unidas
- XRD:
-
Difração de raios X
Nanomateriais
- Garras de injeção de combustível personalizadas para impressão em 3D para um robô de seleção e colocação
- Nanofibras e filamentos para entrega aprimorada de drogas
- Técnicas para Fabricação de Aditivos e Prototipagem
- Novo Náilon 6 Estabilizado por Calor para Trem de Força Híbrido e Elétrico
- Síntese One-Pot Green da Microsfera SnO2 Decorada com Ag:um Catalisador Eficiente e Reutilizável para Redução de 4-Nitrofenol
- Novel Biocompatible Au Nanostars @ PEG Nanopartículas para imagens In Vivo CT e propriedades de depuração renal
- Fabricação e caracterização de novo composto de suporte de catalisador anódico de nanofibra de carbono Tio2 para célula de combustível de metanol direto via método de eletrofiação
- Desempenho aprimorado de um novo catalisador PdAu / VGCNF anódico para eletro-oxidação em uma célula de combustível de glicerol
- Como maximizar a eficiência de combustível para construção pesada e equipamentos agrícolas
- A fabricação e ferramentaria de peças metálicas para sistemas de injeção de combustível



