Propriedades de preparação e antibiofilme de filmes compostos de óxido de zinco / alumina anódica porosa
Resumo
Os filmes de PAA (alumina anódica porosa) foram preparados por oxidação anódica em duas etapas após tempos diferentes e, em seguida, os filmes compósitos de ZnO / PAA foram preparados pelo método sol-gel em sua superfície. Enquanto isso, os filmes compostos de ZnO / PAA foram caracterizados por difração de raios X (XRD), analisador termogravimétrico / térmico diferencial (TG / DTA), espectrômetro infravermelho por transformada de Fourier (FT-IR), microscopia eletrônica de varredura (SEM), microscopia eletrônica de transmissão (TEM), difração de elétrons de área selecionada (SAED) e ângulo de contato de água (CA). As propriedades antibiofilme dos filmes compostos de ZnO / PAA em Shewanella putrefaciens foram medidos simultaneamente. Os resultados mostram que as micromorfologias dos filmes compostos de PAA e ZnO / PAA são afetadas pelo segundo tempo de anodização. O ZnO é uma estrutura wurtzita hexagonal, e as partículas de ZnO com um diâmetro de 10-30 nm se fixam nas superfícies interna ou externa do PAA. Após serem modificados por Si69, os filmes de ZnO são traduzidos da hidrofilia para a hidrofobicidade. O filme de ZnO / PAA com as propriedades antibiofilme ideais é preparado na superfície do PAA por anodização em duas etapas por 40 min. A adesão de Shewanella putrefaciens é restringido por sua super-hidrofobicidade, e o crescimento de bactérias do biofilme é inibido por suas abundantes partículas de ZnO.
Histórico
Como sabemos, a bactéria pode aderir a superfícies sólidas e formar um biofilme escorregadio em ambientes apropriados [1]. Normalmente, os biofilmes de bactérias aderem firmemente às superfícies de materiais, como aço inoxidável [2], borracha [3], vidro [4] e poliestireno [5]. O biofilme resultaria em corrosão de equipamentos [6] e contaminação de alimentos [7], levando a enormes perdas econômicas. Muitos estudos indicaram que a adesão do biofilme é afetada pelas propriedades da superfície do material, como rugosidade [8,9,10,11], microestrutura [12, 13], hidrofilia [14,15,16,17] e constituintes do antibiótico [18,19,20]. Bohinc et al. [10] apontaram que a aderência bacteriana aumentaria com a rugosidade da superfície do vidro. Singh et al. [12] demonstraram que a alta rugosidade superficial pode melhorar a adsorção de proteínas e acelerar a adesão bacteriana e a formação de biofilme. Bonsaglia et al. descobriram que Listeria monocytogenes aderiu a superfícies hidrofílicas (por exemplo, aço inoxidável e vidro) melhor do que as hidrofóbicas (por exemplo, poliestireno) [14]. Outros estudos também provaram que a superfície hidrofóbica não era boa para a adesão do biofilme [16, 17]. Alguns estudos demonstraram que os constituintes do antibiótico podem inibir a formação de biofilme [18,19,20]. Trezentas e quatro superfícies de aço inoxidável contendo Cu têm grandes propriedades antibacterianas e antibiofilme, aproveitando a atividade antimicrobiana do elemento Cu [18]. Em suma, as propriedades da superfície são cruciais para as propriedades antibiofilme dos materiais.
Os materiais de alumínio têm sido amplamente utilizados, e a alumina anódica porosa (PAA) tem atraído mais atenção nos campos da função elétrica da luz, função catalítica e função de detecção nos últimos anos [21,22,23,24], e sua atividade antimicrobiana foi relatado. Ferraz et al. [24] relataram que o PAA pode induzir a ativação aderente de monócitos / macrófagos devido à sua fase de matriz e nanoporosidade.
Além disso, filmes finos de óxido de zinco (ZnO) têm sido estudados como um excelente material para agentes antibacterianos e antifúngicos. A aderência de Pseudomonas aeruginosa para filmes de ZnO com estruturas de superfície de nanorod era mais fraco do que o de vidro e ZnO pulverizado, e mais P. aeruginosa são mortos nos filmes ZnO [25]. Enquanto isso, uma pesquisa apontou que as superfícies revestidas com ZnO restringiram drasticamente a formação de biofilme, e a geração de radicais hidroxila desempenhou um papel fundamental na atividade do antibiofilme, mas não na existência de íons de zinco [26]. Além disso, os filmes compostos de ZnO podem ser usados em muitos campos para restringir a formação de biofilme e terão boas perspectivas de aplicação na preservação de produtos aquáticos [27]. O ZnO é hidrofílico, enquanto os filmes hidrofóbicos são bons para restringir a adesão do biofilme. Assim, é necessário melhorar as propriedades hidrofóbicas do filme de ZnO.
Os produtos aquáticos são muito perecíveis devido à sua deterioração microbiana [28]. Em condições de armazenamento aeróbio, Pseudomonas spp. e Shewanella putrefaciens são conhecidos como organismos de deterioração dominantes [29]. Shewanella putrefaciens tem natureza psicrotrófica e pode reduzir trimetilamina- N -óxido para trimetilamina [30]. Então, Shewanella putrefaciens será usado como a bactéria indicadora neste artigo.
As microestruturas dos filmes de ZnO seriam diferentes devido à sua base de PAA, e então as propriedades do antibiofilme seriam afetadas. Neste trabalho, filmes de ZnO foram preparados sobre PAA com diferentes morfologias e modificados para melhorar a hidrofobicidade. As propriedades antibiofilme de Shewanella putrefaciens dos filmes compostos de ZnO / PAA foram estudados. Os resultados fornecem valor potencial para as aplicações em embalagens de alimentos, equipamentos de processamento de alimentos e outros campos de materiais funcionais antibacterianos.
Materiais e métodos
Materiais
Todos os reagentes usados neste estudo eram analiticamente puros. A água desionizada e estéril foi utilizada para preparar soluções com condutividade inferior a 0,5 mS / cm. Shewanella putrefaciens ATCC8071 foi adquirido na American Type Culture Collection. Folhas de alumínio de 0,3 mm de espessura com pureza de alumínio acima de 99,99% foram adquiridas de Shengshida Metal materials Co., Ltd. (China).
Preparação de filmes compostos ZnO / PAA
Preparação de filmes de alumina anódica porosa (PAA)
Uma folha de alumínio de alta pureza foi cortada em pequenas dimensões de 10 × 30 mm 2 e foi polido com pasta de polimento de sílica de 50 nm por um polidor (WV80, Positec Machinery Co., Ltd., China) e foi desengraxado por ultrassom em acetona a 53 kHz, 280 W por 15 min (SK8210HP, Kudos Ultrasonic Instruments Co. Ltd ., Xangai). Em seguida, as lâminas foram lavadas duas vezes com etanol e água, respectivamente. As folhas de alumínio pré-tratadas foram usadas como ânodo, a folha de grafite de área igual como cátodo e a solução de ácido oxálico 0,3 mol / L como eletrólito. A primeira anodização foi nas condições de 30 ° C e 40 V por 90 min. Depois disso, as folhas de alumínio foram imersas na solução mista de 6,0% em peso H 3 PO 4 e 1,8% em peso H 2 CrO 4 a 60 ° C por 4 h para remover as camadas de alumina. A segunda anodização foi então realizada nas mesmas condições, mas por 0, 40, 60 e 80 min, respectivamente. Os filmes de alumina anódica porosa (PAA) com um modelo de porta diferente foram obtidos.
Preparação de filmes compostos ZnO / PAA
Em primeiro lugar, o volume igual de solução de etanol de acetato de zinco 0,02 mol / L e solução de etanol de NaOH 0,04 mol / L foram misturados sob agitação rápida a 70 ° C por 5 min e, em seguida, os filmes de PAA (folhas de alumínio) foram imersos na solução misturada sob um grau de vácuo de - 0,085 MPa. Em seguida, a solução foi aquecida à ebulição. Depois que se tornou um sol azul fino, as folhas de alumínio foram retiradas e enxaguadas com água desionizada. Em seguida, as amostras foram secas a vácuo a -0,085 MPa, 80 ° C por 6 h, e os filmes compósitos de ZnO / PAA foram preparados após calcinados a 480 ° C por 2 h em atmosfera de ar. Os pós de óxido de zinco foram preparados simultaneamente. Finalmente, os filmes compostos de ZnO / PAA e os pós foram modificados por 1,0% em peso de solução de etanol de Si69 a 65 ° C por 2 h e, em seguida, secos a vácuo a -0,085 MPa, 40 ° C por 12 h.
Caracterização de filmes compostos ZnO / PAA
A difração de raios-X dos pós de óxido de zinco foi realizada usando difratômetro de pó de raios-X (Rigaku Ultima IV, Rigaku, Japão) em uma etapa de 0,02 ° e 2 θ faixa de 10 ° -80 ° com radiação CuKa de 40 kV, 50 mA. As alterações térmicas e perda de peso das amostras foram analisadas por analisador termogravimétrico / térmico diferencial (TG / DTA, Perkin Elmer Diamond). Os espectros de infravermelho com transformada de Fourier (FT-IR) foram registrados com um espectrômetro Scimitar 2000 Near FT-IR (Agilent, americano) na faixa de 4000–400 cm −1 . As micrografias de superfície dos filmes PAA e dos filmes compostos ZnO / PAA foram obtidas por microscopia eletrônica de varredura de emissão de campo (FESEM, S-4800, Hitachi, Japão). As morfologias das nanopartículas removidas dos filmes compostos de ZnO / PAA são medidas por microscopia eletrônica de transmissão de emissão de campo (FETEM, Jem-2100F, JEOL, Japão) e a difração de elétrons da área selecionada (SAED, Jem-2100F, EOL, Japão) do amostras foram examinadas. Os ângulos de contato com a água (CA) dos filmes compostos (antes / depois da modificação) foram medidos pelo método da gota séssil em várias posições diferentes em cada superfície de amostra usando gotículas de 3,0 μL de água deionizada (SL200B, EUA).
As propriedades do antibiofilme dos filmes compostos ZnO / PAA
Cultivo de Shewanella putrefaciens Biofilme
A suspensão de bactérias de ativação secundária de Shewanella putrefaciens (OD 595 ≈ 0,5) e água peptonada alcalina (APW) de 3% (m / v) NaCl foram misturados uniformemente na proporção de 1:200 ( v / v ) Filmes compostos de ZnO / PAA (0,5 × 0,5 cm) foram imersos em inóculos diluídos de 3 mL e incubados a 28 ° C por um determinado tempo. Sob esta condição, Shewanella putrefaciens cresceu bem e mostrou forte capacidade proliferativa.
Ensaio de adesão de Shewanella putrefaciens Biofilmes em filmes compostos ZnO / PAA
Após cultivo em suspensão bacteriana de Shewanella putrefaciens por um certo tempo, os filmes compósitos de ZnO / PAA com biofilme foram transferidos para outros tubos de centrífuga estéreis e lavados três vezes com 1 mL de solução de NaCl 0,85% (m / v) estéril para remoção das bactérias livres. O biofilme foi corado com 1 mL de 0,2% w / w violeta de cristal durante 15 min à temperatura ambiente e foi lavado três vezes com 1 mL de solução de NaCl 0,85% (m / v) estéril para remover o violeta de cristal redundante. Em seguida, os biofilmes corados foram removidos por ultrassom em 33% ( v / v ) ácido acético de 200 μL a 53 kHz, 280 W por 10 min. O OD 595 (densidade óptica a 595 nm) da solução acima foi registrada por um leitor de microplaca VICTOR ™ X3 (Perkin Elmer, América) nas placas de microtitulação de 96 poços. Os resultados foram apresentados como “médias ± desvios padrão” da experiência três vezes paralela.
Ensaio de contagem bacteriana total de Shewanella putrefaciens Biofilme em filmes compostos ZnO / PAA
Os filmes compostos de ZnO / PAA com biofilme foram lavados três vezes com solução salina tamponada com fosfato estéril (PBS, pH 7,4; 137 mmol / L NaCl, 2,7 mmol / L KCl, 10 mmol / L Na 2 HPO 4 e 1,8 mmol / L KH 2 PO 4 ) para desalojar bactérias flutuantes, e os biofilmes corados foram removidos por ultrassom em 10 mL de PBS estéril a 53 KHz, 280 W por 10 min. Posteriormente, a contagem bacteriana total nos biofilmes foi medida pelo método de contagem em placa. Com o experimento três vezes paralelo, os resultados foram mostrados como "médias ± desvios padrão" e a curva de crescimento da colônia das bactérias do biofilme foi desenhada.
A medição das micrografias de Shewanella putrefaciens Biofilmes
Após a remoção das bactérias flutuantes, os filmes compostos de ZnO / PAA com biofilme foram imersos em 2,5% ( w / v ) glutaraldeído a 4 ° C durante 4 h. Posteriormente, as amostras foram desidratadas a cada 30 min com 50, 70, 80 e 90% ( v / v ) etanol, respectivamente. Após imersão em álcool etílico absoluto por 1 hora, as amostras foram secas ao ar natural em bancada limpa. As micrografias de superfície das amostras foram fotografadas por FESEM (S-4800, Hitachi, Japão) após pulverização catódica revestida a 3 kV por 40 s.
A medição CLSM de Shewanella putrefaciens Biofilmes
Os filmes compostos de ZnO / PAA com biofilme foram lavados com solução salina tamponada com fosfato (PBS, pH =7,4) por três vezes para remover as bactérias flutuantes, e as amostras foram coradas no escuro por 15 min na solução mista de 0,01% em peso laranja de acridina (AO, Sigma, América) e iodeto de propídio 0,1% em peso (PI, Sigma, América). Em seguida, as amostras foram lavadas três vezes com PBS para desalojar a solução de tingimento redundante, e o excesso de umidade foi desalojado. Dez microlitros de agentes de selagem anti-fluorescência (Biosharp BL701A, China) foram jogados nos biofilmes, e as amostras foram armazenadas a 4 ° C sem luz. As proporções de células vivas e mortas dos biofilmes foram observadas usando microscópio confocal de varredura a laser (CLSM, TCS-SP5 II, Germany Leica Instrument Co., Ltd.) [31, 32].
Resultados e discussão
Caracterização de filmes ZnO
Caracterização de XRD dos pós de ZnO preparados pelo processo Sol-gel
As propriedades antibacterianas e antibiofilme do óxido de zinco são afetadas por sua estrutura cristalina [33, 34]. A Figura 1 mostra que a estrutura cristalina das amostras é transformada após calcinada. Antes das calcinações, as amostras são contidas na estrutura wurtzita hexagonal do ZnO. Os picos de difração a 31,70 °, 34,52 °, 36,31 °, 47,68 °, 56,82 °, 62,92 ° e 67,92 ° de 2 θ correspondem a (100), (002), (101), (102), (110), (103) e (112) planos de cristal de óxido de zinco (PDF # 36-1451, a = b =3.250 e c =5,207), respectivamente. Os amplos picos de difração indicam baixa cristalinidade e pequenas partículas de ZnO. Enquanto isso, picos menos impuros revelam o intermediário na amostra. Depois de calcinados a 230 ° C, os picos impuros desaparecem e o ruído medido diminui, mas a largura dos picos de difração é invariável. Isso significa que o intermediário desaparece e o grau do cristal aumenta. Com o aumento da temperatura de calcinação, os picos de difração do ZnO tornam-se mais nítidos, indicando que a cristalinidade aumenta e as partículas de cristal crescem.
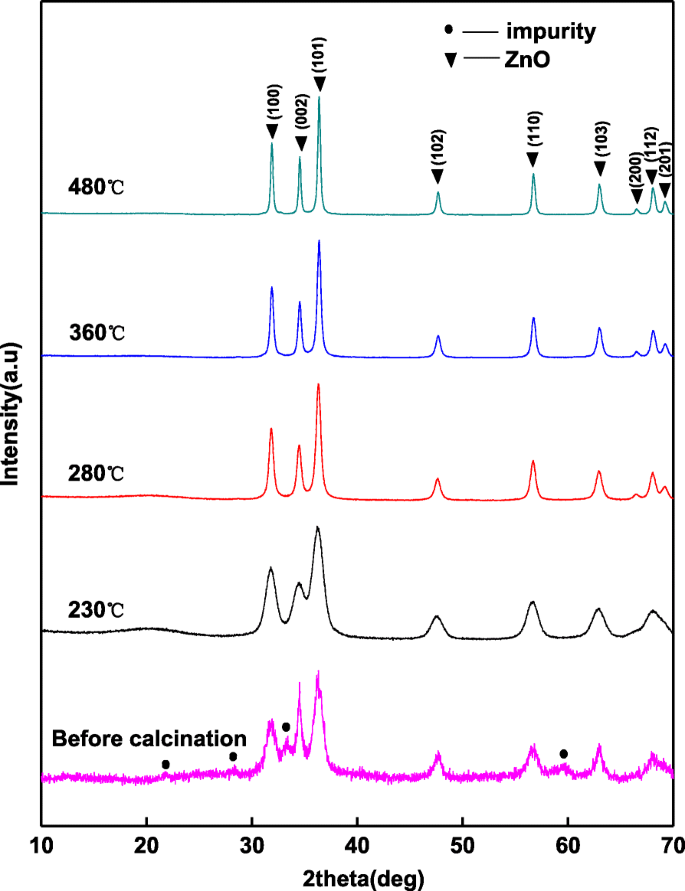
Padrões de XRD dos pós de óxido de zinco calcinados em diferentes temperaturas
Apenas água ligada do Zn (CH 3 COO) 2 · 2H 2 O é produzido na solução de etanol de Zn (CH 3 COO) 2 , e a hidrólise de CH 3 COO - é inibido. Em primeiro lugar, o Zn (CH 3 COO) 2 é hidrolisado e produzido o produto intermediário.
4Zn (CH 3 COO) 2 · 2H 2 O → Zn 4 O (CH 3 COO) 6 + 2CH 3 COOH + 3H 2 O (1)
No processo de aquecimento, o colossol é facilitado pela solução de etanol de NaOH e o efeito estérico espacial de CH 3 COO - é de grande importância para a estabilidade do colossol ZnO. Enquanto isso, a reação neutra de CH 3 COOH com NaOH acontece.
5Zn 4 O (CH 3 COO) 6 + 22 NaOH + 13H 2 O → 4Zn 5 (OH) 8 (CH 3 COO) 2 · 2H 2 O + 22CH 3 COONa (2)
CH 3 COOH + NaOH → CH 3 COONa + H 2 O (3)
Spanhel e Anderson [35] indicaram que os alcogéis de óxido de zinco são formados a partir de grãos de ZnO por agregação e crescimento de Ostwald (envelhecimento). Então, o intermediário de Zn 5 (OH) 8 (CH 3 COO) 2 · 2H 2 O é aquecido e decomposto na fase de ZnO [36, 37]. Assim, a estrutura wurtzita hexagonal do ZnO é a base da gelatina seca antes da calcinação.
Zn 5 (OH) 8 (CH 3 COO) 2 · 2H 2 O → 5ZnO + 2CH 3 COOH + 5H 2 O (4)
Hosono et al. [37] confirmaram este mecanismo de reação. A solução de etanol de Zn (CH 3 COO) 2 · 2H 2 O transformou-se em produtos coloidais durante o aquecimento a 60 ° C, e os resultados de XRD mostram que o produto seco da gelatina é uma mistura de ZnO e Zn5 (OH) cristalino 8 (CH 3 COO) 2 · 2H 2 O. Após refluxo por 48 h, as partículas são transformadas na wurtzite ZnO.
Análise TG / DTA
O resultado TG / DTA da gelatina de óxido de zinco é mostrado na Fig. 2, e a curva TG pode ser dividida em três estágios. No primeiro estágio, a perda de massa é de 68,6% da temperatura ambiente até 100 ° C, e existe um pico endotérmico a 62 ° C. Corresponde ao solvente etanol e água perdidos na gelatina de óxido de zinco. No segundo estágio, a perda de massa é de apenas 3,8% de 100 a 400 ° C. Os resultados de XRD mostram que a impureza desapareceu, o aumento da cristalinidade e o crescimento das partículas de cristal após calcinadas a 230, 280 e 360 ° C, respectivamente. Uma pequena quantidade de perda de massa pode ser a perda de água dos poros e a transição da impureza. De 400 a 850 ° C, não há perda de massa e pico endotérmico, indicando que não há transformação do cristal nesta etapa. Enquanto isso, o resultado de XRD mostra que o cristal cresce após calcinação a 480 ° C. Os resultados de TG / DTA são consistentes com os resultados de XRD.
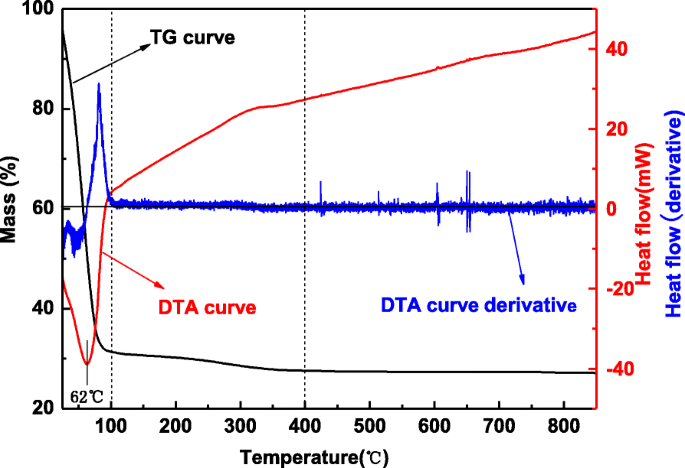
Gráficos TG / DTA para gelatina de óxido de zinco
Caracterização FT-IR de películas de óxido de zinco não modificadas / modificadas
A Figura 3 mostra os espectros FT-IR dos filmes de ZnO modificados não modificados e hidrofóbicos. Os picos amplos em 3600-3300 cm −1 são atribuídos à vibração de alongamento de −OH e ao pico em 1651 cm −1 é atribuído à vibração de flexão de –OH, respectivamente, indicando a água absorvida e a água capilar nas amostras [38]. Os picos em 2360 e 2328 cm −1 são atribuídos ao dióxido de carbono no ar. Os picos em 2943 e 2864 cm −1 são devido a vibrações de alongamento assimétricas e simétricas de −CH 2 , respectivamente. O pico mais forte em 1475 cm −1 é atribuída à vibração de flexão no plano ou vibração de tesoura de −CH 2 grupos [39], e o pico em 895 cm −1 é atribuída às vibrações de alongamento dos grupos Si-O [40]. Os picos são cerca de 440 e 414 cm −1 são atribuídos à vibração da estrutura de grupos Zn-O do ZnO não modificado / modificado [41]. Os resultados indicam que a modificação faz ligações –S – S– de Si69 se romperem e trietoxissililpropil é enxertado nas amostras, de modo que as propriedades hidrofóbicas dos filmes de ZnO aumentam. Wang [42] relatou que a dispersão de nano-ZnO poderia ser melhorada pela modificação in situ de Si69 e Si69 enxertados na superfície de partículas de nano-ZnO através da reação química. Isso é consistente com os resultados de nossa análise.
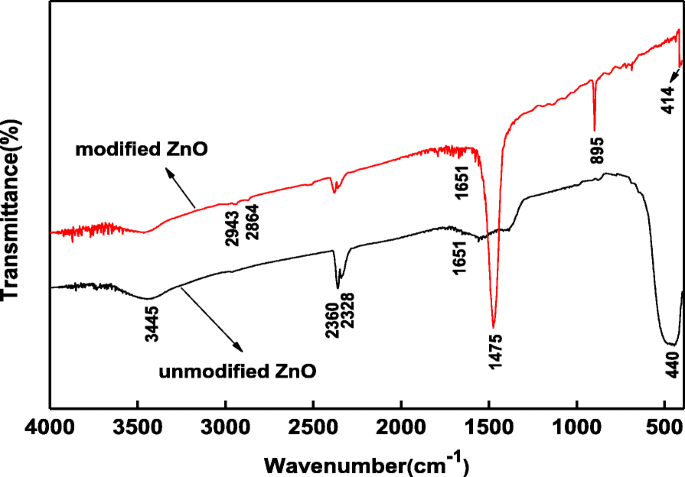
Espectros FT-IR dos filmes de óxido de zinco não modificados / modificados
Análise de Micromorfologias de Filmes PAA
As morfologias dos filmes de PAA são afetadas pelo segundo tempo de oxidação anodizado. Conforme mostrado na Fig. 4, após a remoção das camadas de alumina da primeira anodização, o filme de PAA é uma estrutura em favo de mel hexagonal serrada com nanoporos de 5–10 nm (Fig. 4a). Após a anodização em duas etapas por 40 min, os nanoporos são transformados em quadros de camadas multicamadas (Fig. 4b). Após anodização em duas etapas por 60 min, os quadros de casca de multicamadas desbotam e o diâmetro dos nanoporos é ampliado para 20-40 nm, entretanto, existem as cristas na superfície (Fig. 4c). Estendendo o tempo de anodização de duas etapas para 80 min, os nanoporos são aumentados para 60-70 nm e as cristas desaparecem (Fig. 4d).

Imagens SEM da alumina anódica porosa (PAA) com diferentes tempos de duração da segunda anodização a 0 min, b 40 min, c 60 min e d 80 min
De acordo com a teoria da dissolução assistida por campo ácida (AFAD) [43], no processo de anodização, os filmes de óxido da camada barreira tornam-se não uniformes, e as cristas são formadas. Nestes pontos, a formação e o desenvolvimento do microporoso são promovidos pelo agravamento da AFAD. Com o segundo tempo de anodização prolongado, os orifícios ordenados e passantes são formados gradualmente na superfície e, em seguida, as estruturas e cristas de camadas múltiplas desapareceram (Fig. 4b-d). O resultado é semelhante ao Reddy’s, que preparou PAA por meio do processo de anodização de duas etapas em ácido oxálico 0,3 mol / L [44].
Análise de Micromorfologias de Filmes ZnO
As propriedades antobiofilme das superfícies dos materiais são afetadas por sua morfologia e substâncias [12]. Como mostrado na Fig. 5, as morfologias dos filmes de ZnO são significativamente diferentes, as quais são preparadas nos filmes de PAA com diferentes tempos de duração da segunda anodização. Nas superfícies do filme de PAA com nanoporos de 5–10 nm, as grandes partículas aglomeradas de 20–30 nm são densamente ligadas e formaram filmes de ZnO espessos (Fig. 5a). Na superfície do filme de PAA que é preparado por anodização de duas etapas com duração de 40 min, os quadros de revestimento multicamadas são mantidos no filme de ZnO (Fig. 5b). Conforme mostrado na Fig. 5c, as partículas de ZnO foram fixadas ao esqueleto do filme de PAA e formaram orifícios maiores. Na amostra com nanoporos de 60–70 nm, as partículas de ZnO de 10–20 nm são fixadas na borda dos orifícios de PAA e uma parte das partículas entrou nos nanoporos (Fig. 5d). Este pode ser o colossol entrando nos orifícios maiores sob condição de vácuo e então formar as partículas de ZnO. Os resultados acima indicam que quanto menor for o diâmetro dos nanoporos do PAA, maior será a taxa de aderência do ZnO. Wu et al. [45] consideram que as partículas de colossol se formam facilmente na parede dos orifícios devido ao negativo das partículas do sol e ao positivo das paredes dos poros do PAA. O achado também é consistente com o estudo de Bousslama et al. [46]. O colossol apenas se fixa na parede dos orifícios quando o filme de PAA é imerso em sol de zinco por 24 h, e então os orifícios ficam cheios por 48 h, indicando que as partículas de colossol aderiram preferencialmente na parede dos orifícios.

Imagens SEM dos filmes ZnO preparados no PAA com diferentes tempos de duração de anodização em duas etapas a 0 min, b 40 min, c 60 min e d 80 min
Os resultados acima mostram que as partículas de colossol facilmente entram em grandes orifícios e se fixam na superfície interna sob condição de vácuo; no entanto, as partículas de colossol apenas se fixam nos esqueletos das superfícies externas do PAA com os pequenos orifícios.
As imagens TEM do filme de ZnO raspado do filme composto de ZnO / PAA são mostradas na Fig. 6. Na superfície de PAA preparada apenas por anodização de uma etapa, as partículas delaminadas de ZnO têm cerca de 10 nm, mas as partículas de 20-30 nm são mostrados na imagem SEM (Fig. 5a), indicando que as partículas de ZnO estão aglomeradas. Na superfície do PAA preparada por anodização em duas etapas, as partículas delaminadas de ZnO têm aproximadamente 20 nm e uma parte das partículas está aglomerada nos locais individuais. É manifestado que as partículas de ZnO são fixadas na borda dos orifícios de PAA primeiro (Fig. 6c, e, f).

Imagens TEM ( a , c , e , f ) e padrões SAED ( b , d ) dos filmes ZnO preparados no PAA com tempo diferente de duração de anodização em duas etapas a , b 0 min c , d 40 min; e 60 min; e f 80 min
Os planos de rede (100), (101), (102), (110) e (103) da estrutura wurtzita hexagonal ZnO são mostrados em padrões SAED (Fig. 6b, d), indicando que ZnO é uma wurtzita hexagonal. Os resultados são coincidentes com a análise de XRD.
Caracterização de hidrofobicidade-hidrofilicidade da superfície do filme de ZnO
Para diminuir a adesão bacteriana dos materiais, os filmes de ZnO preparados com diferentes micromorfologias são tratados para melhorar a hidrofobicidade e o ângulo de contato com a água da superfície do filme fino antes e depois da modificação é mostrado na Tabela 1.
Antes da modificação, os filmes de ZnO são hidrofílicos devido aos grupos hidroxila de superfície nas partículas de ZnO. A hidrofilicidade é melhor devido à sua estrutura porosa que se preparou na superfície do PAA com anodização em duas etapas com duração de 40 min. Para as outras amostras com duração de anodização de duas etapas de 60 e 80 min, a hidrofilia diminui gradualmente devido à baixa quantidade de adesivo de ZnO. Para a amostra com duração de anodização de uma etapa, a baixa hidrofilia se deve à sua estrutura não porosa.
Após a modificação, os filmes de ZnO são traduzidos em hidrofóbicos. De acordo com a análise FT-IR, o trietoxissililpropil é enxertado nas amostras após a ruptura das ligações –S – S– do Si69. Enquanto isso, pode ser resultado de sua estrutura porosa e mais partículas de ZnO; o filme tem a maior hidrofobicidade com duração de anodização de duas etapas de 40 min.
Caracterização de Shewanella putrefaciens Biofilmes
Chi et al. [47] relataram que o alumínio anodizado não tem atividade antibacteriana para bactérias Gram-negativas ( Escherichia coli e P. aeruginosa ) e bactérias Gram-positivas ( Streptococcus faecalis e Staphylococcus aureus ) No entanto, o ZnO tem uma excelente atividade antibacteriana e antibiofilme [25,26,27], e há uma correlação positiva entre a atividade antibacteriana e antibiofilme [48, 49]. Além disso, as propriedades antibacterianas do ZnO são afetadas por sua microestrutura [50, 51]. Para obter uma excelente superfície com atividade antibiofilme, os filmes de ZnO com diferentes microestruturas foram preparados sobre filmes de PAA com diferentes tempos de duração da segunda anodização, e as propriedades do antibiofilme foram medidas.
A adesão dos biofilmes e curvas de crescimento das bactérias do biofilme
A formação e o desenvolvimento do biofilme bacteriano podem ser concluídos em cinco etapas:a adesão reversível da bactéria à superfície inicialmente; a conversão da adesão reversível para a adesão irreversível; a formação inicial do biofilme; o desenvolvimento do biofilme amadurecido; e a degeneração do biofilme e o retorno da bactéria ao estado planctônico [52].
Conforme mostrado na Fig. 7 (1), em 2 horas, a aderência de Shewanella putrefaciens o biofilme nos filmes de ZnO aumenta rapidamente, ilustrando a conversão da adesão reversível de bactérias em adesão irreversível. De 2 a 12 h, a aderência do biofilme aumenta gradativamente, que é a fase de crescimento do biofilme. De 12 a 24 h, a aderência do biofilme aumenta ou diminui ligeiramente, manifestando o estágio maduro do biofilme. Após 24 h, a aderência do biofilme diminui, e os biofilmes entram no estágio de degeneração. A Figura 7 (2) mostra que a tendência de variação das bactérias do biofilme está de acordo com a aderência do biofilme, indicando que o desenvolvimento do biofilme depende da bactéria do biofilme.
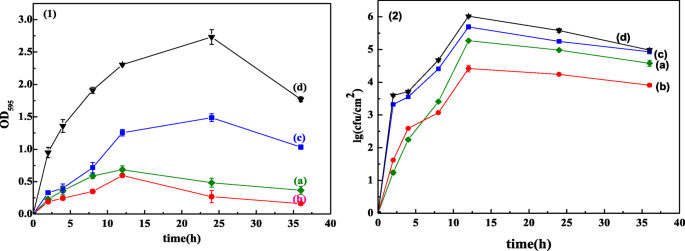
A adesão de Shewanella putrefaciens biofilme ( 1 ) e curva de crescimento da colônia das bactérias do biofilme ( 2 ) nos filmes de ZnO preparados em PAA com tempo diferente de duração de anodização de duas etapas (a) 0 min, (b) 40 min, (c) 60 min e (d) 80 min
Além disso, para o filme de ZnO preparado na superfície de PAA com duração de anodização em duas etapas por 80 min, a aderência do biofilme e a quantidade total de bactérias do biofilme são ambas as mais altas entre as quatro amostras. No entanto, para o filme de ZnO preparado na superfície do PAA com duração de anodização em duas etapas por 40 min, a propriedade do antibiofilme é ótima. Isso pode ser devido à aderência do biofilme que é inibida pela maior hidrofobicidade, e então menos exopolissacarídeos (EPS) e o outro nutriente contra o crescimento do biofilme bacteriano. Para o filme de ZnO preparado na superfície do PAA com anodização em duas etapas com duração de 80 min, sua hidrofilia é boa para a aderência inicial do biofilme, e menos partículas de ZnO não inibem o crescimento da bactéria do biofilme. Enquanto isso, mais materiais adesivos de biofilme nutrem as bactérias do biofilme, e as bactérias do biofilme se multiplicam rapidamente. Consistente com nossa pesquisa, a aderência do biofilme é inibida pela maior hidrofobicidade do filme de ZnO no estágio inicial de formação do biofilme [49]. A aderência dos biofilmes é afetada pelas propriedades hidrofóbicas e hidrofílicas dos materiais [14, 53, 54]. Bonsaglia et al. [14] relatou que L. monocitogenes aderir à superfície hidrofílica mais facilmente do que à superfície hidrofóbica. Muitos estudos descobriram que a adesão bacteriana é reduzida ou inibida pela superfície hidrofóbica [47, 54]. Shaer et al. [54] indicated that the biofilm colonization on the functionalizing orthopedic hardware could be prevented by hydrophobic polycations. Chen et al. [55] also suggested that the biofilm could be inhibited by low surface free energy. The results matched those from us.
The Morphological Characteristics of Shewanella putrefaciens Biofilm
The microtopographies of Shewanella putrefaciens biofilm at various stages are shown in Fig. 8.

SEM images of the biofilms on the zinc oxide films prepared on PAA with different time of two-step anodization duration a 0 min, b 40 min, c 60 min, and d 80 min
After cultivated for 2 h, there are less adhesive materials on the ZnO film prepared on PAA without two-step anodization (a) and with two-step anodization duration for 40 min (b), but more adhesive materials and a few bacteria on the other two (c, d). It is indicated that the anti-adhesive properties of the former two are better than the latter two, it is consistent with Fig. 7. After cultivated for 12 h, more and more EPS and bacteria are attached to ZnO films, signifying the rapid growth of the biofilm. At 24 h, the EPS films are thickened gradually and biofilm bacteria grew well, indicating mature biofilms. At 36 h, the deciduous EPS films and dead bacteria illustrate the biofilm degenerating stage.
According to the antibacterial mechanisms of dissolved metallic ions, the dissolved zinc ions are combined with active proteinase of bacteria, make proteinase lose its bioactivity, and damage its bacterial cells to death [34, 56]. Thus, the antibacterial properties of the former two (a, b) are superior to the latter two (c, d) due to their plentiful ZnO particles on the films. Xie [57] and Jones [58] also thought that the antibacterial abilities strengthened with the dosage increasing of ZnO particles. Meanwhile, the adhesive materials and bacteria on the sample (d) are all more than the others, according to the analysis of adhesion of Shewanella putrefaciens biofilm and colony growth curve of the biofilm bacteria (Fig. 7). Feng et al. [59] found that the hypha of Escherichia coli easily reached into the PAA pores with diameters of 50 and 100 nm, and the biofilm accumulated and adhered to the surface of PAA. However, there is no hypha of Shewanella putrefaciens could be observed in our study. It can be inferred that the optimal antibiofilm properties are ascribed to the lower hydrophobicity of ZnO film in the initial stage of the biofilm formation.
The CLSM Characteristics of the ZnO/PAA Composite Biofilms
As shown in CLSM images, the live Shewanella putrefaciens bacteria are green, and the dead ones are red (Fig. 9). The black images indicate that the counts of live bacteria on the surfaces are few after biofilm cultivation for 2 h. Biofilm bacteria multiply rapidly, and the counts of live bacteria are significantly increased with the cultivation time. More dead bacteria are observed in the former two (a, b) at 24 h and in all samples at 36 h. The counts of dead bacteria of the latter two (c, d) are less than that of the former two (a, b). The results indicate that the antibacterial properties of the former two (a, b) are superior to that of the latter two (c, d), which is according to the previous analysis.
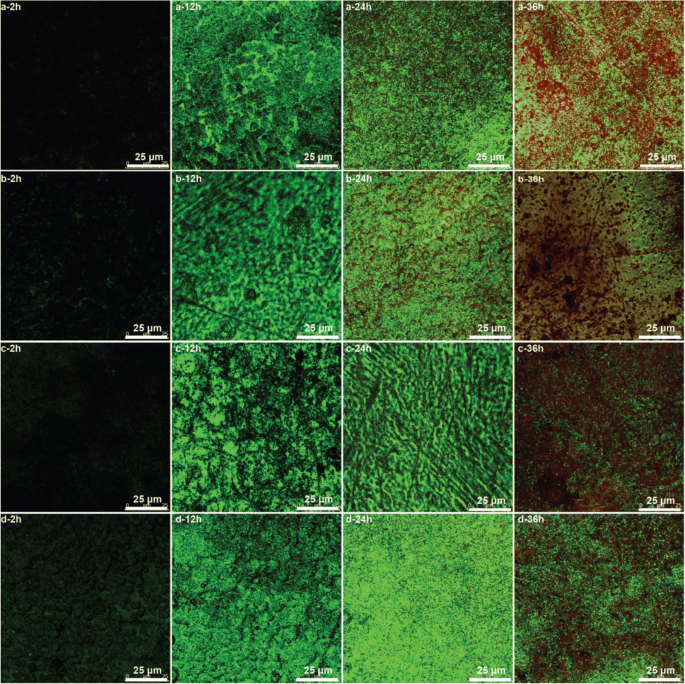
CLSM images biofilms formed on the zinc oxide films prepared on PAA with different time of two-step anodization duration a 0 min, b 40 min, c 60 min, and d 80 min
Conclusions
In this work, the PAA films with different microstructures were prepared by two-step anodic oxidation first, and then the ZnO/PAA composite films are prepared by sol-gel. The ZnO films are hydrophilic due to the surface hydroxyl group on the ZnO particles. After being modified by Si69, the ZnO films translate to hydrophobicity because of its hydrophobic group. The antibiofilm properties of the ZnO films are affected by the hydrophobicity and amount of ZnO particles. The hydrophobicity inhibits the initial adherence of the biofilm and less EPS and the other nutrient against the growth of biofilm bacteria. So, the antibiofilm properties of the ZnO/PAA film are optimal which are prepared on the PAA surface with two-step anodization duration for 40 min because of its super-hydrophobicity and plenty of ZnO particles.
Abreviações
- AO:
-
Acridine orange
- CA:
-
Water contact angle
- EPS:
-
Exopolysaccharides
- FT-IR:
-
Fourier transform infrared spectrometer
- PAA:
-
Porous anodic alumina
- PBS:
-
Phosphate-buffered saline
- PI:
-
Propidium iodide
- SAED:
-
Selected area electron diffraction
- SEM:
-
Microscopia eletrônica de varredura
- TEM:
-
Microscopia eletrônica de transmissão
- TG/DTA:
-
Thermogravimetric/differential thermal analyze
- XRD:
-
X-ray diffusion
Nanomateriais
- Preparação e propriedades magnéticas de nanopartículas de espinélio FeMn2O4 dopadas com cobalto
- Em direção aos nanofluidos de TiO2 - Parte 1:Preparação e propriedades
- Composto Híbrido de Sílica Nanoestruturada / Ouro-Celulose Ligado Amino-POSS via Processo Sol-Gel e Suas Propriedades
- Nanotubos de titanato Nanocompósitos de óxido de grafeno decorado:Preparação, Retardância de Chama e Fotodegradação
- Fabricação fácil de composto de polianilina porosa multi-hierárquica como sensor de pressão e sensor de gás com sensibilidade ajustável
- Efeitos da Espessura de Bicamada nas Propriedades Morfológicas, Óticas e Elétricas de Nanolaminados de Al2O3 / ZnO
- Ajustando as morfologias de superfície e propriedades dos filmes ZnO pelo projeto da camada interfacial
- Ajuste de nível de Fermi de filmes ZnO por meio de deposição de camada atômica superciclada
- Preparação e propriedades ópticas de filmes GeBi usando o método de epitaxia de feixe molecular
- Morfologia, estrutura e propriedades ópticas de filmes semicondutores com Nanislands GeSiSn e camadas deformadas



