Nanopartículas de ouro bioconjugadas ambientalmente compatíveis como agentes de contraste eficientes para imagiologia de câncer induzida por inflamação
Resumo
Para muitos cânceres, a detecção precoce é a chave para melhorar a sobrevida e reduzir a morbidade, que está associada a ressecções radicais devido ao diagnóstico tardio. Aqui, nós descrevemos a eficiência de nanopartículas de ouro conjugadas com anticorpo primário (AuNPs) para atingir especificamente processos inflamatórios crônicos, especialmente macrófagos M2, em seções de tecido de colite ulcerativa (UC) e esteatohepatite em ratos que podem levar a câncer colorretal e carcinoma de fígado, respectivamente. Neste estudo, demonstramos que AuNPs sintetizados por um método simples, barato e ambientalmente compatível podem ser facilmente conjugados com os anticorpos anti-COX-2, anti-MIF e Alexa Fluor® 488 (ALEXA) para realizar a coloração de imunofluorescência em pacientes inflamados tecidos. Além disso, mostramos que nanopartículas de ouro conjugadas com anticorpo primário (AuNPs) podem ser usadas para direcionar macrófagos M2 por citometria de fluxo. Nós projetamos três protocolos de coloração de imunofluorescência de seção de tecido com AuNPs por 30 min e incubação durante a noite, bem como um protocolo de citometria de fluxo de marcação de macrófagos M2 com AuNPs por 30 min. Os resultados de imunofluorescência e citometria de fluxo sugerem que a conjugação foi alcançada por adsorção direta de anticorpos na superfície AuNPs. Quando comparado com o protocolo ALEXA padrão em imunofluorescência (IF) e citometria de fluxo (FC), nosso protocolo de incubação de 30 min usando AuNPs em vez de ALEXA diminuiu de aproximadamente 23 h para 5 h para IF e de 4 h para 1 h para FC, provando ser menos trabalhoso, o que torna o método elegível para o diagnóstico de câncer induzido por inflamação.
Introdução
Na pesquisa médica e biológica, o interesse por nanopartículas de ouro (AuNPs) para estudos de microscopia óptica e procedimentos diagnósticos, especialmente microscopia confocal a laser, está aumentando. O uso de conjugados de anticorpo / AuNP permite a detecção em tempo real da absorção de ouro em células vivas (por exemplo, células cancerosas) no nível de partículas individuais, permitindo a estimativa de quantidades intracelulares de NPs [1,2,3].
As propriedades físico-químicas dos AuNPs permitem que eles sejam usados em muitos estudos médicos, como genômica, biossensibilidade, imunoensaio, química clínica, detecção e fototermólise de microrganismos e células cancerosas [1]. Faulk e Taylor [4] descreveram o primeiro método de conjugação de anticorpos com ouro coloidal para visualização microscópica eletrônica direta dos antígenos de superfície de salmonelas. Desde então, muitos estudos foram desenvolvidos visando a aplicação de nanopartículas conjugadas com biomacromoléculas, como anticorpos, lectinas e enzimas, em diferentes áreas, por exemplo, bioquímica, microbiologia, imunologia e morfologia [1, 4]. Em estudos de câncer, agentes de contraste baseados em AuNP altamente específicos e sensíveis são usados tanto para raios-X quanto para modalidades de imagem óptica, uma vez que AuNPs são capazes de aumentar a intensidade de fluorescência de moléculas conjugadas [5, 6].
Em 2014, demonstramos que AuNPs podem ser aplicados ao método de coloração por imunofluorescência indireta (IF) em culturas de células [6]. No presente estudo, descrevemos três novos métodos de coloração por imunofluorescência (IF) usando AuNPs. Aqui, usamos seções de tecido e comparamos a intensidade de fluorescência de cada um desses métodos com o protocolo de coloração padrão com o anticorpo Alexa Fluor® 488 (ALEXA) (A1) com o objetivo de otimizar uma técnica fluorescente para aplicação clínica [7,8,9 ]
A imagem de fluorescência (FI) para o direcionamento de células cancerosas utiliza uma variedade de tecnologias de imagem óptica a fim de melhorar a detecção de neoplasia precoce com base em assinaturas moleculares específicas para câncer [10]. Desde 2013, houve um rápido aumento no número de ensaios clínicos usando FI. O rastreamento é geralmente considerado para pacientes de alto risco, que é baseado em uma combinação de fatores de estilo de vida, genética ou história pessoal de doença, enquanto a vigilância é reservada para pacientes com diagnóstico de displasia / inflamação crônica ou aqueles com suspeita de malignidade. FI pode ajudar na identificação de lesões malignas com especificidade e sensibilidade melhoradas em comparação com as técnicas disponíveis atualmente. Além disso, a triagem baseada em FI pode fornecer uma maneira menos invasiva e mais econômica de detectar lesões cancerígenas ou pré-cancerosas. Especificamente, a capacidade do FI de detectar lesões mais cedo do que os métodos de triagem convencionais não só resultará em melhores resultados de tratamento, mas também em custos de tratamento reduzidos, pois evitará a necessidade de cuidados multimodais, que são necessários para aqueles diagnosticados em diagnósticos posteriores [11] . Neste estudo, demonstramos que os conjugados de anticorpo / AuNPs podem ser aplicados com sucesso para imagens de inflamação crônica por meio de microscopia de fluorescência.
Métodos / Experimental
Objetivo do estudo
O objetivo deste estudo é demonstrar como as propriedades de fluorescência de nanopartículas de ouro podem ser utilizadas em técnicas de IF e citometria de fluxo. Além disso, comparamos os protocolos testados com AuNPs ao protocolo padrão usando ALEXA e comprovamos que é possível usar os AuNPs em um protocolo, que é mais rápido, mas tão confiável quanto o protocolo padrão.
Produtos Químicos e Reagentes
Tricloreto de ouro (30% em peso em HCl), polivinilpirrolidona (PVP, MW =10.000), hidróxido de sódio, membrana de celulose para tubos de diálise e glicerol foram produtos da Sigma-Aldrich Chemical Co (Saint Louis, EUA). O ácido sulfúrico e o peróxido de hidrogênio foram adquiridos da Vetec (Rio de Janeiro, Brasil). A solução salina tamponada com fosfato (PBS) e albumina de soro bovino (BSA, 5%) foram adquiridos da Life Technologies Corporation © (Califórnia, EUA). Anti-COX-2 (ciclooxigenase-2 ) e anticorpos primários anti-MIF (fator de inibição da migração de macrófagos) foram adquiridos da Santa Cruz Biotechnology (São Paulo, Brasil), enquanto o anticorpo secundário Goat Anti-Rat IgG H&L Alexa Fluor® 488 foi adquirido da ABCAM® (Cambridge, Reino Unido). Fluoroshield Mounting Medium com DAPI (20 ml) da ABCAM® (Cambridge, UK) foi usado para contracoloração de DNA.
Produção e caracterização de AuNPs e espectroscopia de fluorescência
AuNPs esféricos (7,1 nm) foram produzidos e caracterizados de acordo com um estudo de Gasparotto et al. [12]. Resumidamente, todos os utensílios de vidro foram mantidos em KMnO 4 + Solução de NaOH durante a noite, enxaguada com água desionizada, mantida em H 2 O 2 + H 2 SO 4 solução (1:1 v / v ) por 10 min, novamente enxaguado com água desionizada e seco antes de usar. PVP (0,20 g) e cloreto de ouro (6,80 mg) foram dissolvidos em 10 ml de água. Num copo separado, o glicerol (0,18 g) e NaOH (0,080 g) foram dissolvidos em 10 ml de água. A solução de glicerol-NaOH foi então adicionada ao AuCl 3 -PVP solução para produzir as seguintes concentrações finais:1,0 mmol / L −1 Au 3+ , NaOH 0,10 M, glicerol 0,10 M e 10 g / L −1 PVP. A mistura final apresentou uma cor vermelha profunda devido à formação de AuNPs. Os espectros de absorção coloidal ultravioleta-visível dos AuNPs foram adquiridos com um espectrofotômetro Evolution 60S UV-visível (Thermo Scientific, MA, EUA). A espectroscopia de fluorescência foi realizada com um espectrofluorofotômetro RF-5301 PC (Shimadzu, Kyoto, Japão).
Design experimental
Todos os três protocolos foram testados em grupos de controle de dois modelos inflamatórios crônicos, colite ulcerativa induzida por ácido acético (UC) [7] e esteatohepatite induzida por álcool [8, 9] em ratos.
A UC induzida por ácido acético foi realizada em ratas Wistar (220 ± 20 g de PV), obtidas no Centro de Biotecnologia da Universidade Federal da Paraíba. Os animais foram divididos em dois grupos ( n =5 por grupo):controle de ácido acético e ratos não colíticos. Os animais jejuaram durante a noite e anestesiados com cetamina (70 mg / kg, 10%) e xilazina (10 mg / kg, 2%). A UC foi induzida de acordo com métodos originalmente descritos por MacPherson e Pfeiffer [13] e modificados por Millar et al. [14]. Um cateter foi cuidadosamente inserido no cólon. Em seguida, ácido acético a 10% (0,5 ml) em solução salina a 0,9% foi instilado no lúmen do cólon. O grupo não colítico recebeu 0,5 ml de solução salina 0,9% por via intracolônica. Os ratos foram mantidos em posição supina de Trendelenburg por 30 s para evitar vazamento da instilação intracolônica.
Os animais jejuaram durante a noite e foram sacrificados com overdose de tiopental, 48 horas após a indução. Em seguida, o cólon foi removido assepticamente, enxaguado com PBS e colocado em uma placa gelada. O cólon foi limpo de gordura e mesentério. Em seguida, cada corpo de prova foi pesado e seu comprimento medido sob carga constante (2 g). Em seguida, o cólon foi aberto longitudinalmente e classificado para dano macroscopicamente visível em uma escala de 0 a 10 de acordo com os critérios descritos por Bell et al. [15].
A esteatohepatite alcoólica foi induzida em ratos Wistar machos (290 ± 10 g de PV) obtidos no Departamento de Biofísica e Farmacologia da Universidade Federal do Rio Grande do Norte (UFRN). Os animais foram divididos em dois grupos ( n =5 por grupo):ratos alcoólicos e não alcoólicos. Solução de etanol (7 g / kg de peso corporal de 30% v / v ) foi usado como uma dose crônica para o grupo de alcoólatras. Os animais do grupo não alcoólico por via oral receberam um volume equivalente de solução salina (NaCl 0,9%) por gavagem. Os procedimentos de gavage foram realizados uma vez ao dia em ambos os grupos durante 28 dias.
No dia 29, a eutanásia foi realizada por injeção intraperitoneal de 7,5 ml / kg de cetamina (50 mg / ml) e 2,5 ml / kg de xilazina (20 mg / ml). Antes da eutanásia, todos os grupos de animais foram mantidos em jejum por 12 horas. Uma vez inconscientes, os animais foram submetidos a punção cardíaca seguida de remoção do fígado. Fragmentos de fígado foram imersos em formaldeído tamponado a 10% para análise histopatológica.
Os animais de UC induzida por ácido acético e esteatohepatite induzida por álcool foram alojados em condições padrão (ciclo claro / escuro de 12 h, 22 ± 0,1 ° C e 50-55% de umidade) com ad libitum acesso a alimentos e água. Os animais foram tratados de acordo com os princípios éticos para experimentação animal.
Histologia
Cinco blocos de parafina dos controles positivos (controle do ácido acético e controle do álcool) de cada modelo de inflamação foram usados para coloração IF indireta. Os anticorpos primários anti-COX-2 e anti-MIF foram considerados bons marcadores de inflamação em UC induzida por ácido acético e esteatohepatite induzida por álcool, respectivamente, fornecendo uma coloração confiável em termos de intensidade de fluorescência que pode ser usada para comparar diferentes protocolos.
Os tecidos foram fixados em formaldeído tamponado a 10%, desidratado com álcool etílico (70%, 80%, 90%, 95% e P.A.), clarificado em xilol e impregnado em parafina seguindo o protocolo padrão [8]. Antes do preparo dos cortes para a coloração indireta de IF, as lâminas foram mantidas em estufa a 60 ° C por 24 h.
Projetos de imunofluorescência e protocolos
Três seções de tecido (4 μm) de cada animal foram desparafinizadas em xileno e lavadas em uma série de concentrações decrescentes de etanol, de etanol 99% a etanol 50%. Finalmente, as seções de tecido foram lavadas duas vezes em dH 2 O e uma lavagem com PBS. A recuperação do antígeno foi realizada colocando as seções em um citrato de sódio 10 mM com 0,05% de Tween 20 a 95 ° C por 30 min e, subsequentemente, à temperatura ambiente (TA) por 20 min. O ruído / sinal de fundo foi reduzido incubando as seções em 0,1% de negro de Sudão em álcool 70% à temperatura ambiente por 20 min, seguido por três lavagens em 0,02% de PBS-Tween 20. As amostras foram permeabilizadas em 0,2% de Triton-X-100 em PBS (três lavagens, 5 min cada), lavado em PBS e, em seguida, bloqueado com PBS, 5% BSA, dH 2 O e Triton-X-100. As lâminas foram incubadas com solução de bloco em câmara úmida por 2 h. Conforme mostrado na Tabela 1 e Fig. 1, a incubação dos anticorpos primários anti-COX-2 e anti-MIF foi realizada seguindo três protocolos diferentes (NP1, NP2 e NP3). Esses protocolos foram comparados a dois protocolos baseados em ALEXA que diferem no tempo de incubação do anticorpo primário - o protocolo padrão ALEXA (incubação noturna) adotado por nosso grupo de pesquisa como protocolo padrão para a maioria dos procedimentos (A1) e protocolo modificado ALEXA (A2; Incubação de 30 min). NP1 é um método de coloração por imunofluorescência dependente de nanopartículas com 30 minutos para incubação primária. Os anticorpos primários foram diluídos em 1% BSA nas proporções de 1:500 (anti-COX-2) e 1:400 (anti-MIF), e cada amostra foi incubada em uma câmara de umidade à temperatura ambiente (20 ° C) por 30 min . Em seguida, 100-150 μl de AuNPs foram adicionados às amostras, que foram incubadas em temperatura ambiente (20 ° C) por mais 30 min. No segundo protocolo dependente de nanopartículas (NP2), os anticorpos primários foram diluídos em BSA a 1% e aplicados diretamente nas lâminas, que permaneceram na geladeira durante a noite. Portanto, A2 e NP1 são protocolos de incubação de 30 minutos, mas A2 é realizado com um anticorpo fluorescente secundário (ALEXA), enquanto NP1 tem AuNPs como fluoróforos. Isso também se aplica aos protocolos de incubação noturna A1 e NP2. Após os respectivos tempos de incubação, as lâminas de cada protocolo foram lavadas três vezes com PBS para remoção do excesso de anticorpo primário. Em seguida, 100-150 μl de nanopartículas foram adicionados a cada lâmina em NP2, enquanto ALEXA (1:400) foi adicionado em A1. Após 1 h de incubação com AuNPs (NP2) e ALEXA (A1), todas as lâminas foram lavadas três vezes com PBS.
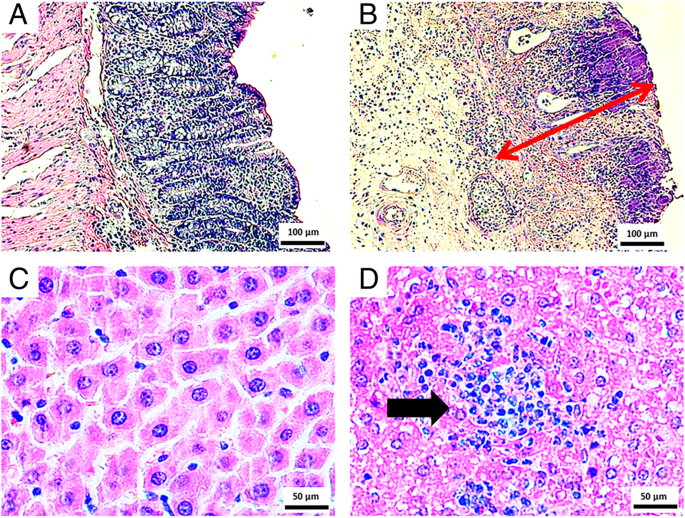
Imagens de coloração com hematoxilina e eosina de UC induzida por ácido acético e grupos de controle de esteatohepatite induzida por álcool. a Controle negativo do modelo UC (× 100; barra de escala =100 μm). b UC induzida por ácido acético. A seta vermelha indica infiltração de leucócitos na área da mucosa (× 100; barra de escala =100 µm). c Controle negativo de esteatohepatite (× 200; barra de escala =50 μm). d Esteatohepatite induzida por álcool. A seta preta indica infiltração de leucócitos (× 200; barra de escala =50 μm)
O terceiro protocolo (NP3) foi projetado para explorar as propriedades de amplificação de AuNPs em sistemas fluorescentes. No NP3, AuNPs foram aplicados durante a diluição de ALEXA em BSA a 1%. Três diluições de anticorpo secundário (1:200, 1:400 e 1:800) em BSA com AuNPs foram testadas a fim de comparar as intensidades de fluorescência de cada diluição para A1. As diluições foram preparadas de forma que o volume de AuNPs fosse proporcional ao volume de BSA, por exemplo, para uma diluição de 1:200, 2 μl de ALEXA foram diluídos em 199 μl de AuNPs + 199 μl de BSA. O tempo de incubação para os anticorpos primários em A1 e NP3 foi de aproximadamente 18 h (durante a noite), enquanto o tempo de incubação para a suspensão de ALEXA + AuNPs foi de 1 h.
Finalmente, as amostras foram montadas usando Fluoroshield Mounting Medium com DAPI. As lâminas foram armazenadas em caixa protegida contra luz e mantidas a 4 ° C até a análise microscópica. Imagens fluorescentes foram obtidas com um microscópio vertical Zeiss Observer z.1 para imagens de fluorescência e campo claro (objetivas × 20 e × 10, Carl Zeiss, Jena, Alemanha) com AxioCam MRc. O parâmetro da média aritmética do software Zeiss ZEN lite blue edition (Carl Zeiss) foi utilizado para avaliar quantitativamente a intensidade da fluorescência pixel a pixel para cada imagem do canal ALEXA. Foram analisadas pelo menos três amostras de cada animal (cinco animais por grupo) e tiradas cinco fotos de cada fragmento com a objetiva × 10.
Indução de TAMs polarizados M2 in vitro
Para avaliação de nanopartículas de ouro conjugadas com anticorpo primário (AuNPs) em macrófagos M2, células RAW 264.7 (5 × 10 5 células / poço em uma placa de 12 poços) foram cultivadas em meio completo com 10% de soro fetal bovino suplementado com 20 ng / ml de IL-4 por 24 h. Após tratamento com IL-4, as células foram lavadas três vezes com DMEM isento de soro, seguido de cultura no mesmo meio por 48 h. As células foram analisadas usando um microscópio óptico Telaval 31 (ZEISS, Oberkochen, Alemanha).
Citometria de fluxo
Após incubação com IL-4 por 48 h, células RAW 264.7 e macrófagos M2 (1,5 × 10 4 células / poço em uma placa de 12 poços) foram coletados com um raspador e bloqueados com 0,5 g de BSA em 100 ml de PBS (PBA) por 45 min, seguido de incubação com CD163 anti-camundongo conjugado com PerCP (1:1000) e FITC -CD86 anti-camundongo conjugado (1:1000) a 4 ° C por 60 min. Além disso, macrófagos M2 foram marcados com COX-2 e anticorpos primários MIF e então conjugados a AuNPs. TAMs polarizados M2 foram coletados e fixados com 2% de paraformaldeído em PBS por 10 min, seguido de incubação com o anti-COX-2 e anti-MIF primário (1:100) por 60 min a 4 ° C e; em seguida, as células foram marcadas com anticorpo secundário conjugado com Alexa® Fluor 488 de anti-coelho de cabra (Thermo Fisher Scientific) em solução de incubação (1:100) em temperatura ambiente por 60 min, conforme descrito no protocolo padrão Alexa [16]. Seguindo o protocolo (N1) em que AuNPs substituem o anticorpo secundário conjugado com Alexa® Fluor 488 anti-coelho de cabra, os macrófagos M2 foram colhidos, lavados com PBS e incubados com o anti-COX-2 e anti-MIF primário (1:100 ) em solução de incubação à temperatura ambiente durante 30 min. Em seguida, as células foram incubadas com AuNPs (1:5) a 4 ° C por 30 min (excitação de AuNPs a 520 nm). Após a etapa de lavagem final, as células marcadas foram analisadas em um software BD FACSCanto II (BD Biosciences, Holanda) e FlowJo (versão 10.1; Tree Star Inc., Reino Unido). Todas as análises de citometria de fluxo foram realizadas com amostras em triplicata e repetidas três vezes. A comparação entre os protocolos ALEXA e AuNPs padrão é mostrada na Tabela 2.
Análise estatística
Análise de variância (ANOVA) e post hoc de Bonferroni teste foram realizados para análise de imunofluorescência. Para análise de citometria de fluxo, as diferenças significativas entre os grupos foram calculadas usando ANOVA e teste de Dunn, conforme indicado. A p <0,05 foi considerado estatisticamente significativo para todas as análises realizadas.
Resultados
Análise microscópica
O corte na Fig. 1a mostra um corte de tecido corado com hematoxilina e eosina (controle negativo). O processo inflamatório crônico induzido pelo ácido acético é ilustrado na Fig. 1b, que revela perda da arquitetura do tecido com conseqüente destruição do epitélio, redução das células caliciformes, presença de hemorragias e leucócitos próximos aos locais lesados. Na figura, o acúmulo de gotículas de gordura e o infiltrado inflamatório (neutrófilos e linfócitos) foram observados em fígados de ratos submetidos à exposição crônica ao álcool.
Em termos de intensidade de fluorescência, AuNPs parecia semelhante a ALEXA, que é um fluoróforo convencional para coloração IF. Em ambas as amostras de fígado e cólon, as diferenças na intensidade de fluorescência de NP1 e NP2 foram mínimas ou inexistentes quando comparadas com A1. Na Fig. 2, são mostradas múltiplas comparações entre os protocolos IF testados usando anticorpos primários anti-COX-2 e anti-MIF. As Figuras 2a e d demonstram que as intensidades de fluorescência de A2, NP1 e NP2 não são significativamente diferentes em comparação com o protocolo A1 ( # p > 0,05), sugerindo que os protocolos de incubação de 30 minutos (usando ALEXA ou AuNPs) podem ser aplicáveis em um contexto de diagnóstico.
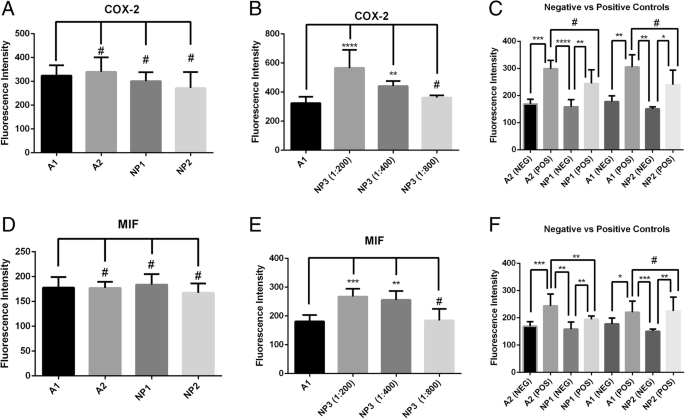
Comparação da intensidade de fluorescência entre os grupos. a Intensidade de fluorescência de AuNPs em A2, NP1 e NP2 em comparação com UC induzida por ácido acético apenas A1 (anticorpo anti-COX-2). b Todas as diluições de NP3 (1:200, 1:400 e 1:800) em comparação com a intensidade de fluorescência de A1 (1:400) apenas UC induzida por ácido acético (anticorpo anti-COX-2). c Comparação da intensidade de fluorescência entre animais induzidos por ácido acético e controles negativos após curto período de tempo (A2 e NP1) e incubação noturna (A1 e NP2). d Intensidade de fluorescência de AuNPs em A2, NP1 e NP2 em comparação com esteatohepatite induzida por álcool apenas A1 (anticorpo anti-MIF). e Todas as diluições de NP3 (1:200, 1:400 e 1:800) em comparação com a intensidade de fluorescência de A1 (1:400) apenas induzida por álcool de esteatohepatite (anticorpo anti-MIF). f Comparação da intensidade de fluorescência entre animais com esteatohepatite induzida por álcool e controles negativos após 30 minutos de incubação (A2 e NP1) e incubação noturna (A1 e NP2). Estatísticas:ANOVA e teste post hoc de Bonferroni, # p ≥ 0,05, ** p <0,01, *** p <0,001 e **** p <0,0001
Além disso, o protocolo NP3 (Fig. 2b, e) demonstrou que é possível combinar os AuNPs para ALEXA de modo que a intensidade de fluorescência detectada fosse aumentada (*** p <0,001), permitindo até o dobro da diluição de ALEXA sem a diminuição da fluorescência em relação à diluição de 1:400 originalmente testada em A1 ( # p > 0,05).
Finalmente, comparamos os grupos doentes aos grupos saudáveis (Fig. 2f) para demonstrar que todos os protocolos testados, seja com ALEXA ou com AuNPs, são eficazes na detecção do início de processos inflamatórios caracterizados pelos antígenos COX-2 e MIF. As Figuras 3 e 4 suportam os dados mostrados graficamente na Fig. 2. Ambos ALEXA e AuNPs são representados em coloração verde, cuja distribuição corresponde a locais de infiltração leucocitária aumentada e lesão de tecido.
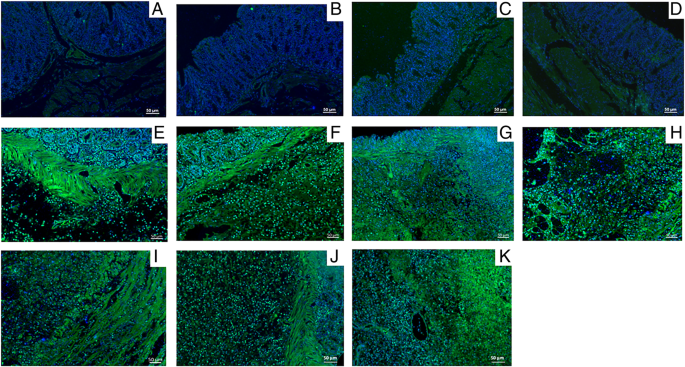
Imagens de IF anti-COX-2 de amostras de cólon de soro fisiológico (controle negativo) e os grupos UC induzidos por ácido acético corados com compostos fluorescentes verdes (ALEXA, AuNPs ou ambos) e DAPI (azul) para núcleos. a Controle negativo corado com protocolo padrão ALEXA (A1) com anti-COX-2 e ALEXA (verde). b Controle negativo corado com protocolo ALEXA modificado (A2) com anti-COX-2 e ALEXA. c Controle negativo corado com protocolo de nanopartículas 1 (NP1) com anti-COX-2 e AuNPs (verde) em vez de ALEXA. d Controle negativo corado com protocolo de nanopartículas 2 (NP2) com anti-COX-2 e AuNPs em vez de ALEXA. e Controle positivo corado com A1. f Controle positivo corado com A2. g Controle positivo corado com NP1. h Controle positivo corado com NP2. eu Controle positivo corado com protocolo de nanopartículas (NP3) com anti-COX-2 + AuNPs com 1:200 ALEXA. j Controle positivo corado com NP3 (com diluição 1:400 de ALEXA). k Controle positivo de UC corado com NP3 (com diluição 1:800 de ALEXA). Ampliações, × 200. Barra de escala =50 μm
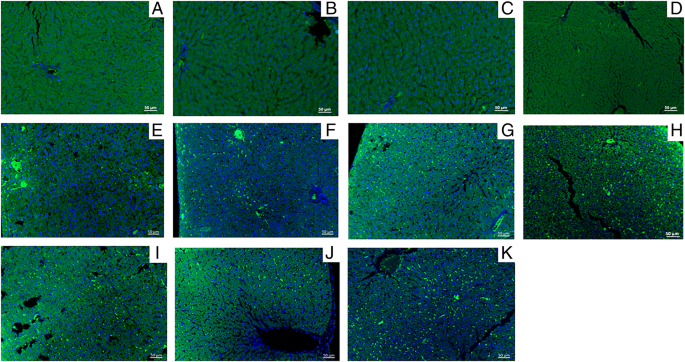
Imagens anti-MIF IF de amostras de fígado dos grupos de solução salina (controle negativo) e esteatohepatite induzida por álcool coradas com compostos fluorescentes verdes (ALEXA, AuNPs ou ambos) e DAPI (azul) para núcleos. a Controle negativo corado com protocolo padrão ALEXA (A1) com anti-MIF e ALEXA (verde). b Controle negativo corado com protocolo modificado de ALEXA (A2) com anti-MIF e ALEXA. c Controle negativo corado com protocolo de nanopartículas 1 (NP1) com anti-MIF e AuNPs (verde) no lugar de ALEXA. d Controle negativo corado com protocolo de nanopartículas 2 (NP2) com anti-MIF e AuNPs no lugar de ALEXA. e Controle positivo corado com A1. f Controle positivo corado com A2. g Controle positivo corado com NP1. h Controle positivo corado com NP2. eu Controle positivo corado com protocolo de nanopartículas 3 (NP3) com anti-MIF + AuNPs com 1:200 ALEXA. j Controle positivo corado com NP3 com diluição 1:400 de ALEXA. k Controle positivo corado com NP3 com diluição 1:800 de ALEXA. Ampliações, × 200. Barra de escala =50 μm
Em termos de aplicação clínica, o protocolo NP1 mostrou-se o mais promissor, pois, quando comparado ao protocolo A1 padrão, permite uma economia de 18 h.
Citometria de fluxo:macrófagos M2 marcados com nanopartícula de ouro conjugada com anticorpo primário (AuNP)
Para caracterizar ainda mais os macrófagos M2, a expressão de marcadores relacionados com M1 (CD86) e M2 (CD163) em células RAW 264.7 estimuladas com IL-4 foram analisadas por citometria de fluxo. Os resultados da citometria de fluxo mostraram que os marcadores relacionados a M2, como o receptor CD163, foram significativamente maiores do que a célula nativa (Fig. 5a, c, p <0,001) enquanto a expressão do receptor CD86 não mostrou qualquer diferença entre macrófagos M2 e células ingênuas (Fig. 5b, c, p > 0,05). Os resultados sugeriram que IL-4 (20 ng / ml) induziu com sucesso a alteração de macrófagos clássicos para macrófagos M2. Após esta etapa, os macrófagos M2 foram incubados com COX-2 e anticorpos primários MIF e, em seguida, rotulados com AuNPs para comparar a eficiência de nanopartículas de ouro conjugadas com anticorpo primário (AuNPs) com o protocolo padrão (ALEXA). Os resultados mostraram que nanopartículas de ouro conjugadas com anticorpos COX-2 e MIF (Fig. 5d, f, p <0,001) ou ALEXA (Fig. 5e, f, p <0,001) mostrou maior intensidade de fluorescência em macrófagos M2 quando comparados com amostras não coradas.
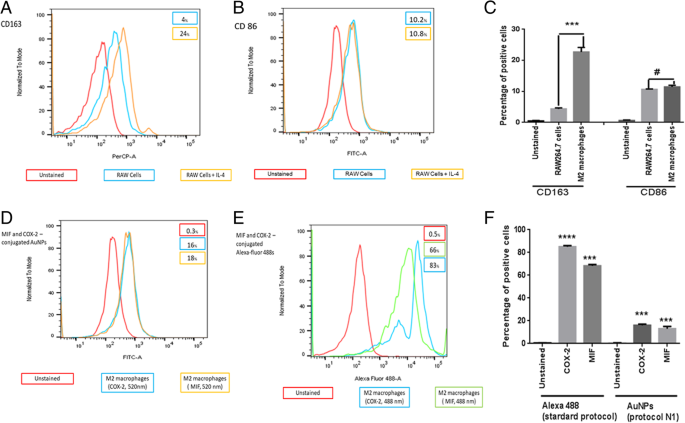
As nanopartículas de ouro conjugadas com anticorpos COX-2 e MIF (AuNPs) têm alta afinidade na superfície dos macrófagos M2. a - c Células RAW 264.7 foram estimuladas com IL-4 (20 ng / ml) por 24 h, seguido por análise de citometria de fluxo para quantificar a quantidade de CD163, um marcador de macrófago M2, e CD86, um marcador M1. d , f Nanopartículas de ouro conjugadas com anticorpos COX-2 e MIF ou e , f ALEXA 488 apresentou maior intensidade de fluorescência em macrófagos M2 quando comparados às amostras não coradas. Os dados são expressos como média ± SD, # p > 0,05, *** p <0,001, p <0,0001. Os dados de fluxo representativos mostrados são de experimentos realizados independentemente pelo menos três vezes
Espectroscopia de fluorescência
A fim de medir os espectros de emissão de fluorescência para AuNPs purificados na ausência e presença de anti-COX-2 (Fig. 6a), anti-MIF (Fig. 6b) e ALEXA (Fig. 6c), o comprimento de onda de excitação foi fixado a 320 nm e a emissão foi registrada na faixa de 650 a 900 nm. Um aumento do comprimento de onda de excitação não alterou a faixa de emissão das partículas, excluindo assim a possibilidade de um processo de espalhamento. As emissões de fluorescência aumentaram ligeiramente com a absorção de anti-COX-2 (aumento de 11,93 unidades de absorbância (au) para a concentração de anticorpo mais alta), anti-MIF (aumento de 12,15 au para a concentração de anticorpo mais alta) e ALEXA (aumento de 3,18 au para a maior concentração de anticorpos) em combinação com AuNPs.
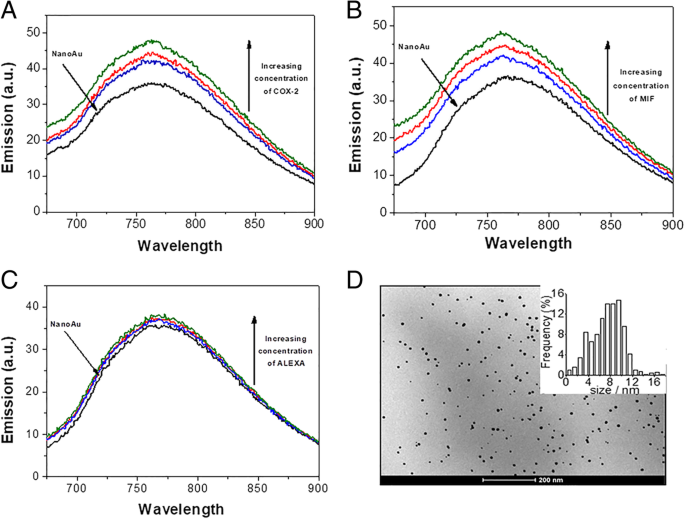
Espectros de emissão de fluorescência de AuNPs excitados em 320 nm na presença de anti-COX-2 ( a ), anti-MIF ( b ) e ALEXA ( c ) A imagem TEM das nanopartículas esféricas usadas neste estudo, mostrando seu tamanho e distribuição ( d ) Excitação e fendas de emissão foram de 10 nm. A concentração de AuNPs foi mantida constante em 29,6 ng / ml −1 . As concentrações de anticorpo são 100 ng / ml −1 (curva azul), 150 ng / ml −1 (curva vermelha) e 200 ng / ml −1 (curva verde)
Discussão
Foi demonstrado que AuNPs possuem propriedades de fluorescência, devido à sua estrutura química e tamanho, e podem atuar como moléculas amplificadoras de sinais fluorescentes. Mais específico, a própria fluorescência AuNP origina-se de interações aurófilas na superfície dos átomos de ouro [17, 18]. Os dados da Fig. 6 são semelhantes aos achados de estudos sobre nanopartículas de prata, que devem o aumento da emissão de fluorescência à competição entre as espécies adsorventes e o oxigênio molecular dissolvido em solução. Portanto, o aumento da emissão de fluorescência de nanopartículas de ouro pode ser atribuído ao fato de que o BSA é adsorvido em sua superfície [19].
O sinal de fluorescência é uma função do fenômeno de ressonância de plasmão de superfície (SPR). Assim, o aumento da quantidade de elétrons livres leva a um sinal SPR mais intenso, uma vez que SPR é a oscilação coletiva de elétrons livres. O BSA adsorvido impede que os elétrons livres da superfície se liguem às moléculas de oxigênio, levando a um aumento do sinal de fluorescência [20, 21]. Anti-COX-2, anti-MIF e ALEXA podem ter sido adsorvidos nos AuNPs, evitando assim O 2 de atingir a superfície das nanopartículas. Isto é suportado pela Fig. 6, onde o aumento do sinal de fluorescência ocorreu em concentrações muito baixas dos diferentes anticorpos. É importante notar, no entanto, que ALEXA exigiu uma concentração mais alta para causar O 2 isolamento da superfície AuNPs.
O processo inflamatório crônico é caracterizado pela infiltração de células imunes, principalmente macrófagos, nos locais de lesão por ácido acético ou etanol no respectivo modelo. A inflamação também é caracterizada pela liberação dependente de leucócitos de várias citocinas e mediadores em resposta a um patógeno ou uma condição estressante. Dentre essas citocinas, a COX-2 e o MIF são conhecidos por serem marcadores de diversos processos inflamatórios, por serem citocinas pró-inflamatórias. A coloração verde observada na Fig. 3 e Fig. 4 é devido à liberação de citocinas COX-2 e MIF, respectivamente.
In chronic UC and liver steatohepatitis, macrophages are the main cells found which can be classified into two major types:M1 macrophages and M2 macrophages. The classically activated macrophages (M1 macrophages) are proinflammatory and play a pivotal role in host defense against infection which is associated with iNOS and IL-23 production and their cell surface-expressed CD86 or HLA-DR that attract killer cells like neutrophils and/or direct Th1 (cytotoxic) responses and stimulate further M1-type responses [22]. Meanwhile, the alternatively activated macrophages (M2 macrophages) are associated with the responses to anti-inflammatory reactions as well as tissue remodeling [23]. In the tumor context, it has been documented that M2-polarized macrophages promote pro-tumor functions by production of a large array of growth factors such as COX-2 and MIF for tumor cells, which are essential for tumor proliferation [24].
It is well established that UC is an important risk factor for colonic epithelial dysplasia and adenocarcinoma [25, 26]. According to Agoff et al. [25], increased malondialdehyde (MDA) levels and upregulation of Bcl-2 during UC are potential mechanisms to explain the relationship between COX-2 overexpression and neoplastic progression. In UC, the inflammation boosts COX-2 activity, leading to genetic damage through increased production of MDA. MDA is a by-product of COX-mediated prostaglandin synthesis and lipid peroxidation, and it is also constitutively produced by COX-1. Since COX-2 upregulates Bcl-2 expression, it leads to resistance to apoptosis in UC-associated neoplasia [27].
MIF is a multipotent cytokine in the innate immune responses that contributes to hepatic injury driven by alcohol-induced steatohepatitis [28]. When steatohepatitis has developed, the liver morphology rarely goes back to normal, even after cessation. In addition, there is a higher risk of the development of cirrhosis, which is the last stage of alcoholic liver disease (ALD) before hepatocellular carcinoma (HCC) [29].
Studies show MIF presence in the sera after hepatic resection or expression in the course of liver cancer progression [30]. MIF is involved in COX-2 and PGE2 upregulation and directly promotes tumorigenesis by inhibition of p53 accumulation, which is a classic tumor suppressor gene that can promote cell cycle arrest and apoptosis in response to DNA damage [31].
In a previous study [6], we have demonstrated that AuNPs can be easily conjugated with the antibodies anti-β-catenin and anti-E-cadherin to specifically target colorectal carcinoma cells, whose clinical value can be found in an early diagnosis of cancer through non-invasive methods in body fluids such as saliva and urine. In addition, we developed a new protocol to decrease the 27 h that are usually needed for the standard protocol to about 1 h needed for our improved protocol, which makes this method eligible for a clinical colorectal cancer diagnostic.
In this study, we took advantage of the properties of AuNPs conjugated with primary antibodies and applied them for the indirect IF staining method of tissue sections. At this point, we cannot affirm whether the interaction of the antibody with the nanoparticle is purely physical or if there is a chemical bond, since the amount of antibodies used in this method are far too small to produce discernible signals in Fourier-transform infrared spectroscopy. Thus, we rely only on fluorescence data that suggest that conjugation was achieved by direct adsorption of antibodies on the AuNPs surface. Such enhancement has been rationalized in terms of competition between adsorbing species and molecular oxygen dissolved in solution, as explained before by Lima et al. [6]. We found that the replacement of ALEXA by the AuNPs in NP1 saves about 18 h (similar to A2), when compared to standard protocol and NP2 that require about 24 h, each, from the antigenic retrieval to the assembling of the slides for microscopic analysis (Fig. 7 and Table 1). The time for incubation with the primary antibody was 30 min for A2 and NP1, but overnight (18 h) for A1, NP2, and NP3 (Fig. 7a and Table 1).
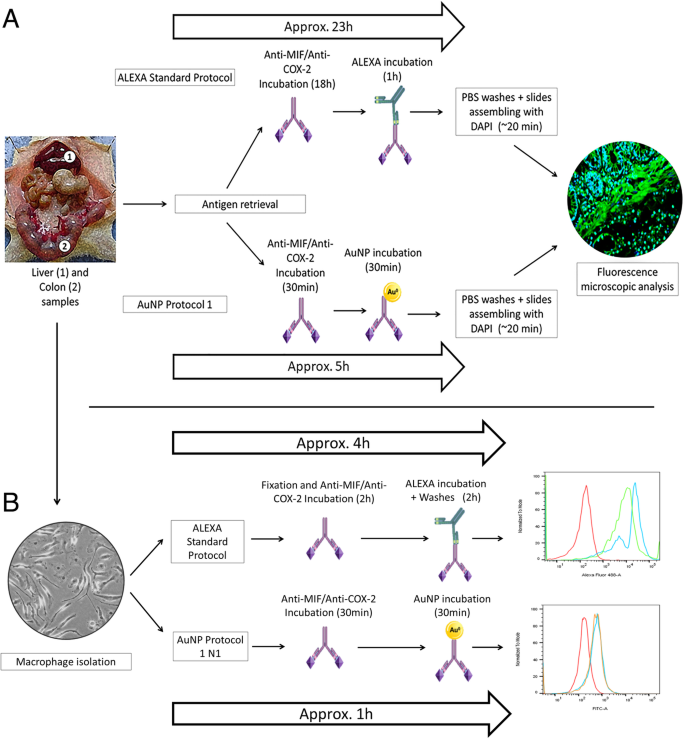
Comparative schemes illustrating the immunofluorescence (a ) and flow cytometry protocols used in this study (b ) In immunofluorescence, AuNPs may be applied in 30-min incubation protocols as fluorescence-enhancing agents, providing faster results with comparable fluorescence levels to the traditional ALEXA protocol, which makes NP1 a suitable protocol for cancer diagnose. Time was counted from the antigen retrieval to the end of the second incubation. In flow cytometry, although the ALEXA marking was higher than that of the AuNPs, the N1 protocol with AuNPs allowed a greater saving of reagents as well as reduced the time required for the technique from 4 to 1 h
Moreover, we demonstrated MIF and COX-2 primary antibody-conjugated gold nanoparticles can be arranged on the surface of M2 macrophage as a fast alternative to analyze the immune profile of inflammation-induced cancer tissues by flow cytometry. Although the standard protocol is laborious, the intensity of marking to both the primary antibodies was higher than primary antibody-conjugated gold nanoparticles. However, the primary antibody-conjugated gold nanoparticles needed less reagents and the time saving was higher as seen in the standard protocol (4 h) and in primary antibody-conjugated gold nanoparticles N1 protocol (1 h) (Fig. 7b). These results suggest that M2 macrophages can be targeted with primary antibody-conjugated gold nanoparticles either to diagnosis or therapy.
The time saving, the specificity, and the low cost provided by NP1 are especially important in cancer diagnosis, when fast and accurate results are highly required. It is important to highlight that, although the models adopted for this work were based on inflammation diseases, the inflammation markers used in this study are highly cancer-correlated and AuNPs provide multiple possibilities for application in clinical research and diagnosis.
Conclusions
All nanoparticle protocols tested showed similar fluorescent intensities to those observed in standard IF, extending the application of AuNPs, not only in research, but also in clinical diagnostics. When diluted with ALEXA, AuNPs allow greater dilutions with acceptable fluorescence intensity. More importantly, AuNPs can be used in faster protocols (e.g., 30-min incubation protocols), completely substituting ALEXA and providing a way to develop further technologies that will improve cancer diagnose and other diseases. We believe that these findings will contribute to advance research and diagnostic procedures that utilize IF methods as well as widen the applications of AuNPs in biotechnology.
Abreviações
- A1:
-
ALEXA standard protocol
- A2:
-
ALEXA modified protocol
- ALD:
-
Alcoholic liver disease
- ALEXA:
-
Alexa Fluor® 488®
- AuNP:
-
Nanopartículas de ouro
- BSA:
-
Albumina sérica bovina
- COX-2:
-
Cyclooxygenase-2
- FC:
-
Citometria de fluxo
- FI:
-
Fluorescence imaging
- IF:
-
Immunofluorescence
- MDA:
-
Malondialdehyde
- MIF:
-
Macrophage migration inhibitory factor
- NP1:
-
Nanoparticles protocol 1
NP2
Nanoparticles protocol 2
- NP3:
-
Nanoparticles protocol 3
- SPR:
-
Surface plasmon resonance
- UC:
-
Colite ulcerativa
Nanomateriais
- Nanopartículas plasmônicas
- Nanopartículas de ouro para sensores quimio
- Nanopartículas multifuncionais de ouro para aplicações diagnósticas e terapêuticas aprimoradas:uma revisão
- Nanopartículas para terapia do câncer:progresso e desafios atuais
- Bioflavonóide direcionado ao receptor de folato Nanopartículas de quitosana carregadas com genisteína para efeito anticâncer avançado em cânceres cervicais
- Novel Biocompatible Au Nanostars @ PEG Nanopartículas para imagens In Vivo CT e propriedades de depuração renal
- Poliglicerol hiper-ramificado modificado como dispersante para controle de tamanho e estabilização de nanopartículas de ouro em hidrocarbonetos
- Emissão de infravermelho próximo Cr3 + / Eu3 + Co-dopado com galogermanato de zinco Nanopartículas luminescentes de persistência para imagem celular
- Avaliação das propriedades antimicrobianas, apoptóticas e de entrega de genes de células cancerosas de nanopartículas de ouro protegidas por proteína sintetizadas a partir do fungo micorrízico …
- Síntese mediada por sementes de nanobastões de ouro de razão de aspecto ajustável para imagens fotoacústicas no infravermelho próximo



