Terapia quimio-fototérmica em câncer de mama usando ácido fólico conjugado com metotrexato a nanopartículas de SiO2
Resumo
A terapia a laser de baixo nível (LLLT) é conhecida como um tipo seguro de fototerapia para o tecido / células tumorais alvo. Além disso, o uso de nanopartículas direcionadas aumenta o sucesso da terapia contra o câncer. Este estudo foi desenvolvido para investigar o efeito combinado de ouro revestido com sílica carregada com folato (FA) / Metotrexato (MTX) (Au @ SiO 2 ) nanopartículas (NPs) e LLLT na luta contra o câncer de mama.
NPs foram sintetizados e caracterizados usando FTIR, TEM e DLS-Zeta. Os NPs tinham morfologia esférica com diâmetro médio de cerca de 25 nm e carga positiva (+13,3 mV), enquanto após a conjugação com FA e MTX sua carga líquida foi reduzida para cerca de -19,7 mV.
Nossas descobertas em estudos de captação celular mostraram claramente a captação celular aumentada de NPs após NPs carregados com FA e MTX em ambas as linhas de células de câncer de mama, especialmente em MDA-MB-231 devido à alta expressão de receptores de folato. Os resultados indicaram que LLLT teve um efeito proliferativo em ambas as linhas de células de câncer de mama, mas na presença de nanopartículas direcionadas ao câncer de mama projetado, a eficácia da terapia quimio-fototérmica combinada foi significativamente aumentada usando ensaio de MTT (p <0,05), coloração DAPI e descobertas do ciclo celular. O maior efeito apoptótico em linhas de células de câncer de mama foi observado nas células expostas a uma combinação de Au @ SiO 2 carregado com MTX-FA NP e LLLT comprovados por coloração DAPI e ciclo celular (aumentando a parada celular em subG0 / G1). Tomados em conjunto, uma combinação de quimioterapia e LLLT melhora o potencial da terapia do câncer de mama com efeitos colaterais mínimos.
Introdução
O câncer de mama (CM), por ser a mulher mais frequente, afetando o câncer recentemente foi relatado com 1,7 milhão de novos casos em todo o mundo [1]. Por causa de sua etiologia complicada e resposta pobre ao tratamento, muitas vezes conhecida como a causa central de mortes associadas ao câncer de mulheres universalmente [2,3,4,5]. Era previsível que cerca de 40.000 mulheres nos EUA morressem de BC em 2014 [2, 6, 7] “(www.cancer.org)”. Com as 522.000 mortes no total, é a quinta causa de morte por câncer com cerca de 800.000 casos em regiões menos desenvolvidas e quase a mesma frequência nas regiões desenvolvidas [1]. Nos países asiáticos a maior idade de início é entre adultos de 40 ou 50 anos em comparação com os países ocidentais que é frequente entre 60-70 anos [8]. Os principais fatores de risco do CM são sexo feminino, história familiar, idade e tendências generativas variáveis, como primeiro parto com mais de 30 anos, menarca precoce e posterior e nuliparidade [9].
O principal objetivo no combate ao câncer é desenvolver planos terapêuticos eficazes, com baixa toxicidade e alta especificidade, para eliminar tumores, principalmente suas metástases, e promover a prevenção de recorrências. Mas as abordagens de tratamento do câncer atualmente utilizadas, como cirurgia, quimioterapia e radioterapia, mostraram vários efeitos colaterais [10,11,12] e todas falham em atingir esse objetivo [13, 14]
As últimas décadas observaram grandes lutas no tratamento do câncer [15, 16]. Entre as abordagens terapêuticas populares atuais, a terapia térmica cresceu como um método de tratamento prospectivo [17]. Recentemente, a terapia fototérmica (PTT), como uma terapia contra o câncer potencialmente eficaz e não invasiva, tem atraído atenção significativa [18, 19]. O PTT baseado em nanoestruturas fotoabsorventes tornou-se uma forma diferente dos métodos gerais [20, 21]. Em um PTT típico, que usa agentes PTT para destruir o tumor, obtendo hipertermia suficiente (42 ° C) sob irradiação de laser (luz infravermelha próxima (NIR) na faixa de 700-1100 nm), foi estudado como um método altamente preciso e método negligentemente invasivo de tratamento do câncer [22,23,24,25,26,27,28].
Uma série de nanopartículas têm sido amplamente estudadas como agentes de contraste de imagem, transportadores de drogas e transformadores de modalidades de energia, como laser, ondas de rádio e ultrassom, em fenômenos térmicos responsáveis por efeitos terapêuticos [29,30,31,32,33 , 34,35,36,37,38,39].
Nanopartículas de ouro têm atraído grande atenção durante a última década devido à sua alta ressonância plasmônica de superfície localizada (LSPR) e fácil conjugação de superfície com biomoléculas [40]. Eles revelaram capacidade de conversão fototérmica de alto desempenho na área NIR [41,42,43] sem efeitos colaterais prejudiciais em sistemas biológicos [44].
Embora as nanopartículas de ouro tenham sido reconhecidas como um foto-sintetizador promissor, mas devido à sua fraca estabilidade fototérmica após irradiação NIR repetitiva, as nanopartículas de ouro perdem gradualmente sua capacidade de conversão fototérmica, o que limita seu uso na prática clínica. Além disso, as nanopartículas de ouro não são bons transportadores de drogas por causa de sua capacidade de carga de droga pobre e perfil de liberação controlada de droga [45, 46]. Alternativamente, a nanopartícula de sílica mesoporosa (MSN) era conhecida por ser um portador de proteína, DNA e fármaco apropriado devido à sua maior capacidade de carregamento de fármaco e à falta de conteúdo tóxico que é produzido a partir de sua degradação. Eles também têm uma grande área de superfície, tamanho controlável, volume de poro altamente disponível e as características de superfície desejadas se aplicam para uma modificação [47].
As nanopartículas após a conjugação com um agente quimioterapêutico e ligante direcionado ao câncer podem inibir as desvantagens da quimioterapia de rotina, como distribuição inespecífica, baixa solubilidade em água e baixos índices terapêuticos [48, 49].
Os agentes que apresentam propriedades quimioterapêuticas, como doxorrubicina, ciclofosfamida, metotrexato, fluorouracil e docetaxel, são usados isoladamente ou em combinação como os principais tratamentos, ou auxiliados por outros tratamentos como PTT. A maioria dos pacientes com câncer experimentando efeitos adversos das drogas quimioterápicas devido à sua distribuição não precisa no corpo do paciente, que afeta todos os órgãos. Essas drogas prejudicam algumas das células normais de crescimento rápido, por exemplo, células do sangue, células da membrana mucosa que cobrem os órgãos internos e folículos capilares [50,51,52,53].
O metotrexato (MTX) tem sido os medicamentos mais usados para a artrite reumatóide e vários tipos de tumores, como pele, pulmão, cabeça e pescoço e mama [54, 55]. Inibe a dihidrofolato redutase (DHFR), a enzima que contribui para a produção de tetrahidrofolato e seus subprodutos, que são necessários para a síntese de timidilato e purina e ambos são vitais para o crescimento e proliferação celular. Portanto, o bloqueio do metotrexato DHFR impede a síntese de 4 macromoléculas básicas de DNA, RNA, timidilatos e proteínas [56].
Infelizmente, assim como a maioria dos agentes PTT convencionais, o principal desafio é atingir o acúmulo seletivo de GNPs no tecido-alvo após a injeção sistêmica [57,58,59]. A terapia direcionada ao câncer permite a entrega de drogas quimioterápicas a células cancerosas específicas, ao mesmo tempo que diminui a exposição de células saudáveis normais. Isso nos levou a fornecer maior dosagem do medicamento às células cancerosas com menor toxicidade sistêmica. Nanopartículas direcionadas a ligantes são marcadores de células cancerosas precisamente identificados, que são altamente expressos na superfície das células cancerígenas [40].
O ácido fólico (folato ou vitamina B9) é um material chave para o crescimento e metabolismo celular. Devido à grande afinidade do folato para as proteínas receptoras de folato, ele é utilizado como um elemento para o direcionamento do câncer. O receptor de folato, como um biomarcador tumoral, é superexpresso em células malignas definidas, como câncer de mama, ovário, pulmão, rim, cérebro e cólon [60]. Os sistemas de liberação de fármacos conjugados com folato aumentam a captação celular do fármaco via endocitose [61].
Materiais e Método
Reagentes e materiais
Usamos água bidestilada (Ghazi Company, Tabriz, Irã) e reagentes químicos de grau analítico para nossos experimentos. Vários reagentes foram adquiridos da Sigma-Aldrich Company, incluindo:ortossilicato de tetraetila (TEOS, 98%), (3-Mercaptopropil) trimetoxissilano (MPTES, pureza de 95%), ácido fólico e rodamina B. Um grupo de materiais foi adquirido da Merck Co:ácido clorídrico (HCl, 37%), solução de amônia (25%), tolueno, hidróxido de sódio (NaOH, 98%) e outros solventes. O MTX foi comprado da Zahravi Farma Company, Tabriz, Iran.
Instrumentação
Neste estudo, para análise do tamanho e morfologia das partículas, foi utilizada a microscopia eletrônica de transmissão (TEM) (LEO 906, Alemanha). Preparamos cerca de 100μL de nossas nanopartículas suspensas em solução aquosa em temperatura ambiente. A solução foi transferida para um filme de carbono revestido em uma grade de cobre de TEM com secagem por congelamento subsequente e observada a 80KV. A determinação do tamanho de partícula foi realizada por medição DLS (espalhamento dinâmico de luz) a 25 ° C usando um Zetasizer Nano ZS90, Malvern Instruments, Malvern, UK. As medições do potencial Zeta para os NPs preparados foram realizadas por espectroscopia de correlação de fótons (Zetasizer-ZS, Malvern Instrument, UK). Um espectrofotômetro de duplo feixe de UV-Vis (UV-1601 PC modelo SHIMADZU, Kyoto, Japão) foi empregado para a medição de absorbância em cubetas de quartzo de 700μL com comprimento de caminho de 10 mm. A espectroscopia de infravermelho com transformadas de Fourier (FTIR) do espectrômetro Bruker Tensor 27, Alemanha, foi utilizada para a realização do método de pelete de KBr. As medidas de pH foram realizadas com pHmetro Metrohm 713 (Herisau, Suíça). O agitador mecânico Heidolph RZR 2102 Control Overhead Stirrer (Schwabach, Alemanha) foi usado para as agitações. A eficiência de encapsulamento de FA e MTX foi calculada usando o sistema de HPLC consistindo de um módulo de separação Waters 2690 equipado com um detector UV-vis Waters 2500 Pump 1000 (Waters, Milford, MA). A separação cromatográfica foi implementada à temperatura ambiente usando colunas de cromatografia C18 m Bondapak (250 mm 4,6 mm, 10 mm, 125 A Waters, Irlanda).
Preparação de Au @ SiO 2 Nanopartículas
O SiO 2 NPs foram sintetizados com base no método sol-gel relatado anteriormente [62, 63]. Na próxima etapa, nanopartículas revestidas com sílica funcionalizadas com tiol (TFSNPs) foram preparadas de acordo com o método mencionado em nosso estudo anterior [64]. As nanopartículas de Au foram produzidas por um método de redução de citrato (método de Turkevich) [65]. Finalmente, a superfície dos TFSNPs foi coberta por AuNPs. No início, os TFSNPs foram dispersos em água com o auxílio do sonicador de banho por pelo menos uma hora e adicionados à solução de AuNPs e sonicados por 30 min adicionais. A reação foi realizada no escuro por dois dias em agitação dinâmica a 25 ° C. The Au @ SiO 2 nanopartículas com aspecto de cor púrpura foram coletadas por centrifugação (10.000 rpm, 10 min) e secas em estufa a vácuo.
Carregamento de MTX e FA
MTX e FA foram carregados no Au @ SiO 2 nanocarreador como segue:MTX (10 mg) foi adicionado a uma suspensão bem dispersa de 10 mL de nanocarrier em PBS (5 mg / mL, pH 7,4) e agitado moderadamente em temperatura ambiente por um dia em condições de escuridão. O MTX carregou Au @ SiO 2 nanocarrier foi coletado por centrifugação. O sobrenadante foi coletado para a medição do MTX descarregado. Então MTX carregou Au @ SiO 2 o nanocarreador foi disperso em PBS (5 mg / mL, pH 7,4) e FA (10 mg) foram adicionados à solução e agitados moderadamente em temperatura ambiente por outro dia no escuro. O FA-MTX carregou Au @ SiO 2 O nanocarreador foi coletado por centrifugação e o sobrenadante foi separado para o cálculo do AF não ligado na etapa final. O FA-MTX carregou Au @ SiO 2 nanocarrier foi liofilizado e armazenado para os próximos experimentos. As quantidades de MTX e FA não ligados foram calculadas usando o método HPLC pelo protocolo relatado anteriormente [66]. O ácido fólico foi dissolvido em hidróxido de amônio (10% em peso) e diluído com a fase móvel. O tempo de retenção para MTX e ácido fólico foi de 10,5 e 5,95 min, respectivamente. Amostras triplicadas foram aplicadas. A eficiência de carregamento de drogas (DLE) foi calculada pelas seguintes fórmulas:
$$ ee \ left (\% \ right) =\ frac {\ left (inicial \ total \ drogas- Não absorvido \ drogas \ direita)} {Inicial \ total \ drogas} \ vezes 100 $$ (1)
Seleção e cultura de linhas celulares
Duas linhas de células de câncer de mama de interesse com níveis de expressão de superfície relatados receptor de folato (FR) [67], incluindo MCF-7 e MDA-MB-231, foram selecionadas e adquiridas do Pasteur Cell Bank (Teerã, Irã) para as investigações de citotoxicidade. As linhas celulares selecionadas foram cultivadas em meio completo contendo RPMI1640 (termocientífico), 10% de soro fetal bovino (FBS) e 1% de Penstrep (termocientífico) em condições térmicas e atmosféricas de 37 ° C, 5% de CO 2 e 95% de umidade.
Ensaio de citotoxicidade celular
Os ensaios de viabilidade celular foram realizados para medir a proliferação celular após diferentes tratamentos NPs sem irradiação a laser. Resumidamente:as células MCF-7 ou MDA-MB-231 foram semeadas em 96 microplacas com densidade celular de 1,5 × 10 4 por 24 h, então as células foram tratadas com MTX, Au @ SiO 2 e FA-MTX carregado Au @ SiO 2 NPs. As células sem tratamento foram consideradas controle. Na próxima etapa, o corante de tetrazólio MTT (Sigma) em concentrações finais de 5 μg / ml foi adicionado às células e incubado a 37 ° C por 4 h. Em seguida, a solução de MTT foi removida e os cristais de Furmazan sedimentados foram dissolvidos em Dimetil Sulfóxido (DMSO) (BioIdea, Irã) sob agitação suave por 10 min. Finalmente, a absorbância foi medida em 570 nm por um leitor de ELISA. A viabilidade das células foi normalizada para células de controle e o fundo foi removido por subtração das medições em branco.
Terapia a laser in vitro
Para terapia a laser de baixo nível (LLLT), o laser NIR de comprimento de onda de 810 nm (diodo laser Mustang 2000, Rússia) com dose de potência de saída de 185 mW foi usado para destruição de células cancerosas. No início, células MCF-7 e MDA-MB 231 com densidade celular de 1,5 × 10 4 tratado com o Au @ SiO 2 e FA-MTX carregado Au @ SiO 2 NPs foram então expostos à irradiação de laser com diferentes doses de laser (30, 60, 75, 90 e 105 J / cm 2 ) e tempo de exposição fixo (139 seg). As células expostas apenas à irradiação laser (sem NPs) e as células sem quaisquer NPs e tratamentos a laser consideradas como controle positivo e negativo, respectivamente. Após 24 horas de irradiação do laser, a viabilidade celular foi medida pelo método de ensaio MTT [64].
Ensaio de absorção celular de nanopartículas
Uma verificação detalhada da internalização de células NPs é essencial para confirmar o efeito específico do nanocarreador modificado de superfície para cada linha celular. No presente trabalho, empregamos tanto a citometria de fluxo quanto a microscopia quantitativa e de fluorescência para verificar qualitativamente a captação de NPs pelas linhagens celulares MCF-7 e MDA-MB-231.
Para suspensão de NPs, a solução de rodamina B (RhoD) em PBS foi adicionada junto com agitação por 24 h em temperatura ambiente e sala escura (evitando o branqueamento). Em seguida, NPs carregados com RhoD foram separados por Filtro Amicon com limite de peso molecular nominal (NMWL) de 30 kDa e centrifugados por 15 min a 5000 rpm e lavados com tampão PBS para eliminar o RhoD não ligado. As células foram semeadas em placas na densidade de 5 × 10 5 por poço e deixe chegar à confluência. As células foram tratadas com NPs carregadas com Rodamina B por 30, 90 e 180 minutos, células não tratadas usadas como controle. Em seguida, as células foram tripsinizadas e lavadas com PBS e, em seguida, a fluorescência foi quantificada com análise de citometria de fluxo (citômetro de fluxo BD Biosciences FCASCalibur; BD Biosciences, San Jose, CA, EUA). A captação intracelular de NP ou NPD marcado com rodamina B foi posteriormente confirmada por microscopia de fluorescência. As células MCF-7 e MDA-MB-231 foram cultivadas em lamelas e após 24 h as células foram tratadas com Au @ SiO 2 livre NPs e MTX-FA carregados com Au @ SiO 2 NPs. Após incubação por 30, 90 e 180 minutos, as células foram lavadas com PBS e a captação de nanocarreadores marcados com rodamina B foi observada usando um microscópio de fluorescência (microscópio Olympus Bh2-FCA, Japão).
Estudo de apoptose por microscopia de fluorescência
Um método para o estudo qualitativo nuclear da apoptose é um corante fluorescente DAPI que se liga ao DNA e é detectável por microscopia apropriada. Usamos um protocolo como relatado anteriormente para a coloração DAPI [68], resumidamente:as células MCF-7 ou MDA-MB-231 foram semeadas em vasos de formato de 6 poços a uma densidade de 5 × 10 5 e deixe-os anexar e crescer por 24 horas. Após o tratamento com MTX, Au @ SiO 2 NPs e MTX-FA carregados com Au @ SiO 2 NPs com e sem tratamento a laser as células foram lavadas com PBS (Sigma) e então submetidas à fixação em formaldeído 10% (Merck), a seguir:as células foram permeabilizadas com Triton X-100 (Sigma) por 15 minutos. Após lavagens adequadas, as células foram coradas com DAPI (sigma) durante 5 min. Por fim, os núcleos apoptóticos (fragmentados ou enrugados) foram visualizados em microscópio de fluorescência (Olympus). As células sem nenhum tratamento foram consideradas como controle negativo e as células receberam apenas irradiação laser como controle positivo.
Investigações de distúrbios do ciclo celular
As distribuições do ciclo celular MCF-7 e MDA-MB-231 foram determinadas por análise de citometria de fluxo. Desta forma, as células foram semeadas com populações iniciais de 5 × 10 5 e permitiu atingir 80% de confluência. Posteriormente, as células tratadas com MTX, Au @ SiO 2 NPs e MTX-FA carregados com Au @ SiO 2 NPs com e sem irradiação laser foram realizados. As células sem nenhum tratamento foram consideradas como controle negativo e as células receberam apenas irradiação laser como controle positivo. Em seguida, as células foram colhidas por tripsinização seguindo com lavagens de PBS adequadas. Em seguida, as células foram fixadas em Etanol (Merck) por 48 horas. Na etapa seguinte, as células fixadas foram lavadas, em seguida tratadas com Ribonuclease A (Cinaclone), com posterior adição de iodeto de propídio (PI) (Sigma) no escuro. Os sinais de fluorescência foram detectados pelo conjunto FACS da Beckton Dicinson Company.
Estatísticas do estudo
Os experimentos para cada etapa foram realizados em três repetições e os resultados foram relatados como média ± DP. A ANOVA foi usada para comparação de significância entre os grupos. As diferenças foram significâncias refletidas onde o valor da probabilidade foi calculado <0,05 pelo software SPSS.
Resultados e discussão
Caracterização de NPs sintetizados
The Au @ SiO 2 NPs foram produzidos em quatro etapas:1-síntese de SiO 2 nanopartículas, 2-adição de ligante contendo tiol a SiO2 NPs, 3-síntese de nanopartículas de ouro e 4-anexar as nanopartículas de ouro à superfície de complexos SiO2-ligante (Fig. 1). A síntese bem-sucedida de Au @ SiO 2 foi confirmado por FTIR (Fig. 2a). O pico Si – O – Si apareceu por volta de 1088 cm -1 . Um pico amplo em 3000–3700 e 803 cm –1 é creditado ao alongamento e flexão fora do plano dos grupos O – H de silanol livre, respectivamente. A vibração de alongamento alifático C – H foi mostrada como um pico forte em 2950 cm –1 . O C – O de três grupos de metoxissilano foi mostrado pelo pico em 1191 cm –1 .
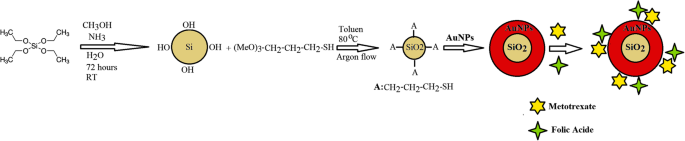
O esquema sintético em etapas para a preparação de Au biocompatível carregado com folato e metotrexato @ SiO 2 Nanopartículas NPs
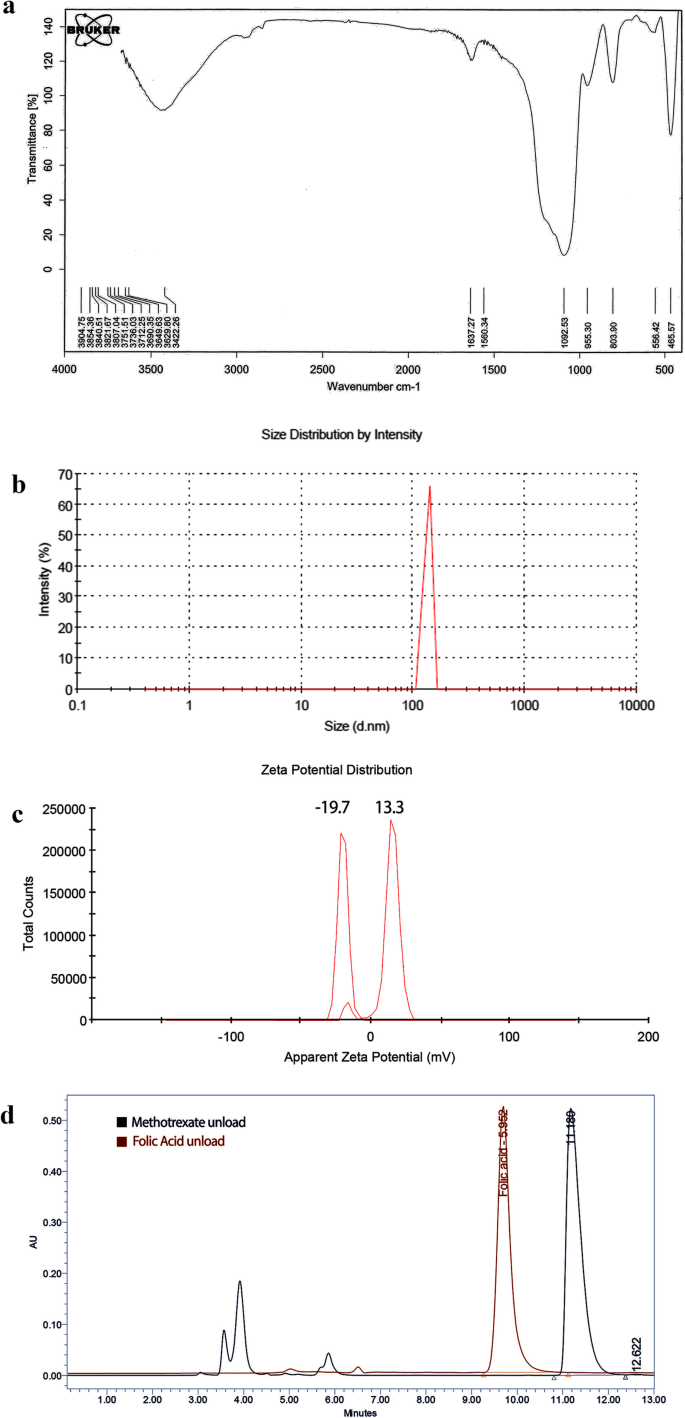
a ) Espectros FTIR de Au @ SiO 2 nanopartículas, b ) distribuição de tamanho de Au @ SiO conjugado com FA-MTX 2 NPs medidos por espalhamento dinâmico de luz (DLS) c ) O potencial zeta de Au @ SiO 2 e Au conjugado com FA-MTX @ SiO 2 NPs medidos por espalhamento de luz dinâmico (DLS) a pH =7,4 e T =25 ° C, d ) Cromatograma de MTX descarregado e FA separado de Au conjugado com FA-MTX @ SiO 2 NP medido simultaneamente pelo método HPLC
Medições de espalhamento dinâmico de luz (DLS) indicaram que FA-MTX conjugou Au @ SiO 2 O tamanho das NPs estava na faixa nanométrica (105 ± 2,3 nm) com distribuição de tamanho estreita (Fig. 2b).
O potencial Zeta é um parâmetro físico-químico importante que influencia a estabilidade das nanossuspensões. Valores de potencial zeta extremamente positivos ou negativos causam forças repulsivas maiores. Por outro lado, a alta carga das partículas, sejam elas positivas ou negativas, faz com que os NPs sejam absorvidos pelos fagócitos do fígado e eliminados do corpo. No caso de uma estabilização eletrostática e estérica combinada, um potencial zeta mínimo de ± 20 mV é desejável [69,70,71]. Os dados do potencial zeta de NPs foram comparados antes e após o carregamento com o MTX-FA em pH =7,4 e T =25 ° C (Fig. 2c). Os potenciais zeta obtidos de Au @ SiO 2 NPs eram +13,3 mV que após carga dupla de droga diminuíram para -19,7 mV que estavam na faixa desejável. O MTX e o FA tiveram uma carga líquida negativa em pH (7,4) acima de seu pka (3,8 e 4,8, 3,5 e 4,3), devido à desprotonação de dois grupos de ácido carboxílico em sua estrutura ([72], https:// pubchem.ncbi.nlm.nih.gov.). Portanto, após o carregamento simultâneo de MTX e FA em Au @ SiO 2 NPs, a carga líquida tornou-se negativa.
A análise TEM fornece o tamanho de partícula individual definido. Nanopartículas de Au foram vistas como esferas escuras dispersas nas NPs de SiO2 como uma camada de leito cinza. As imagens TEM confirmaram que os NPs de Au @ SiO2 foram sintetizados com forma esférica homogênea em que o tamanho médio das partículas era de cerca de 25 nm (Fig. 3).

Imagem TEM de Au @ SiO 2 nanopartículas
Carregamento de drogas
Aqui, o folato está mediando a captação aumentada de GNPs em certos tipos de células cancerosas que superexpressam o receptor de folato por meio de endocitose mediada por receptor para superar a baixa eficácia da internalização de GNPs, portanto, o receptor de folato conhecido como um marcador de tumor e o uso de folato cada vez mais para tumor segmentação [67, 73].
Após a conjugação das moléculas de MTX e FA em Au @ SiO 2 NPs, o potencial zeta mudou de +13,3 a -19,7 mV. Os valores estimados de pKa das duas frações de ácido carboxílico de MTX são 3,8, 4,8 e FA são 3,5 e 4,3 [72], https://pubchem.ncbi.nlm.nih.gov. Portanto, devido à desprotonação de dois grupos de ácido carboxílico de MTX e FA em pH 7,4 que está acima de seu pka, a carga líquida tornou-se negativa e indicando a conjugação bem-sucedida de MTX e FA em Au @ SiO 2 NPs. De Ying Tian et al mostra que o carregamento de MTX em nanopartículas de Au por 18 e 30 mm de diâmetro é de 15 ± 0,4% e 10 ± 1,0%, respectivamente [74]. Neste estudo, FA e MTX foram carregados em NPs de Au @ SiO2 com eficiência de encapsulação de 22,6 e 77,5%, respectivamente. O cromatograma do pico de avaliação simultâneo de MTX e FA é mostrado na Fig. 2d.
Captação celular
Como os agentes fototérmicos intracelulares podem melhorar a eficiência da terapia fototérmica do câncer [75], acredita-se que a internalização celular de materiais fototérmicos é necessária. In vitro o teste de captação celular foi realizado usando células MDA-MB-231 de câncer de mama humano, conhecidas por superexpressar o receptor de folato [40]. Para estudar o papel do FA como um agente de direcionamento e a eficiência do revestimento de superfície na absorção do Au @ SiO 2 NPs por células alvo, células MCF-7 e MDA-MB-231 foram tratadas com NPs de Au @ SiO2 e NPs de Au @ SiO2 carregados com MTX-FA. Os resultados de intensidade fluorescente média de captação de células foram mostrados na Fig. 4. Os resultados mostraram que a captação de Au @ SiO2 NPs em MCF-7 e MDA-MB-231 foi aumentada ao longo do tempo de cultura de células para todas as amostras (Figs. 4 e 5 ) Além disso, após a decoração da superfície de NPs de Au @ SiO2 com MTX e FA, a captação de células aumentou significativamente em MCF-7 e MDA-MB-231 como células que expressam o receptor de folato. A captação de NPs de Au @ SiO2 carregados com MTX-FA em células MDA-MB-231 foi maior do que MCF-7. Como as células MDA-MB-231 expressam níveis mais elevados de receptores de folato de superfície, uma porção elevada de NPs direcionados ao receptor de folato foi inserida via mecanismo de endocitose mediada por receptor, resultando em maior absorção celular. Em outro estudo, o aumento da internalização celular dos NPs conjugados com folato está ocorrendo apenas nas células cancerosas que superexpressam o aHFR e não nas células saudáveis que têm menos expressão de aHFRs na superfície celular [40]. A conjugação de NPs de Au @ SiO2 com FA pode facilitar a absorção celular de NPs e metotrexato, levando ao aumento da toxicidade para as células MDA-MB-231 [76].
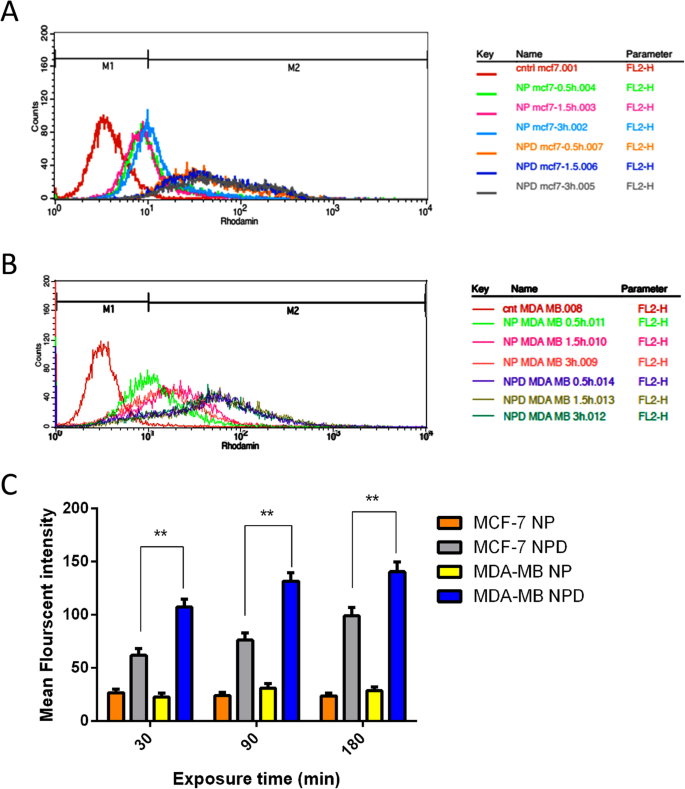
Ensaio quantitativo de captação celular de Au @ SiO marcado com rodamina B 2 nanopartículas (NP) ou rodamina B marcada com MTX-FA carregado com Au @ SiO 2 nanopartículas (NPD) em MCF-7 ( a ) e MDA-MB-231 ( b ) linhas celulares para durações de exposição de 0,5 h, 1,5 he 3h obtidas por citometria de fluxo. Células não tratadas de ambas as linhas celulares foram utilizadas como controle negativo. c Comparação da intensidade média de fluorescência de Au @ SiO marcado com rodamina B 2 nanopartículas (NP) ou rodamina B marcada com MTX-FA carregado com Au @ SiO 2 nanopartículas (NPD) para durações de exposição de 0,5 h, 1,5 he 3h obtidas por citometria de fluxo
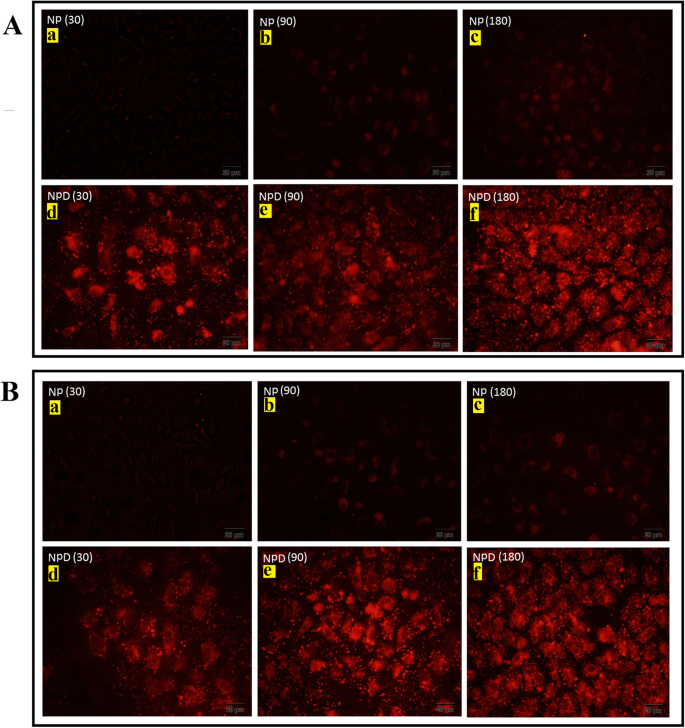
A Ensaio qualitativo de captação celular usando Au @ SiO marcado com Rodamina B 2 nanopartículas (NP) em MCF7 com durações de exposição de 30 ( a ), 90 ( b ) e 180 ( c ) min ou rodamina B marcado com MTX-FA carregado com Au @ SiO 2 nanopartículas (NPD) com durações de exposição de 30 ( d ), 90 ( e ) e 180 ( f ) min e ( B ) Ensaio qualitativo de captação celular usando Au @ SiO marcado com Rodamina B 2 nanopartículas (NP) em MDA-MB-231 com durações de exposição de 30 ( a ), 90 ( b ) e 180 ( c ) min ou rodamina B marcado com MTX-FA carregado com Au @ SiO 2 nanopartículas (NPD) com durações de exposição de 30 ( d ), 90 ( e ) e 180 ( f ) min capturado por microscopia fluorescente
Ensaio de citotoxicidade
Estudos de citotoxicidade celular in vitro do MTX livre, branco Au @ SiO 2 NPs e Au @ SiO conjugado com MTX-FA 2 NPs, foram avaliados pelo ensaio MTT por 24, 48 e 72 h (Fig. 6). Os resultados do ensaio MTT mostraram que Au @ SiO 2 NPs não tiveram efeito citotóxico nas linhas celulares MCF-7 e MDA-MB-231. Além disso, para comparar os efeitos de citotoxicidade tanto do MTX livre quanto do Au @ SiO conjugado com MTX-FA 2 NPs, a mesma concentração de MTX (25, 50, 100 e 200μg / mL) foi usada para todos os tempos de tratamento. Os resultados de citotoxicidade celular indicam que o Au @ SiO 2 conjugado com MTX livre ou MTX-FA NPs mostraram taxa de mortalidade em torno de 10-25% em ambas as linhagens celulares após 24h de tratamento. Estudos anteriores relataram o efeito proliferativo de nanopartículas de ouro em diferentes linhas celulares, como células de osteoblastos murinos MC3T3-E1 e células-tronco do ligamento periodontal humano em condições in vitro. Nossos resultados estão em linha com esses estudos e as Figuras 6a e b mostram o efeito proliferativo de NPs Au @ SiO2 livres. Portanto, o efeito citotóxico igual de nanopartículas de Au @ SiO2 carregadas com MTX e FA-MTX (NPD) pode ser devido a esse fenômeno [77, 78].
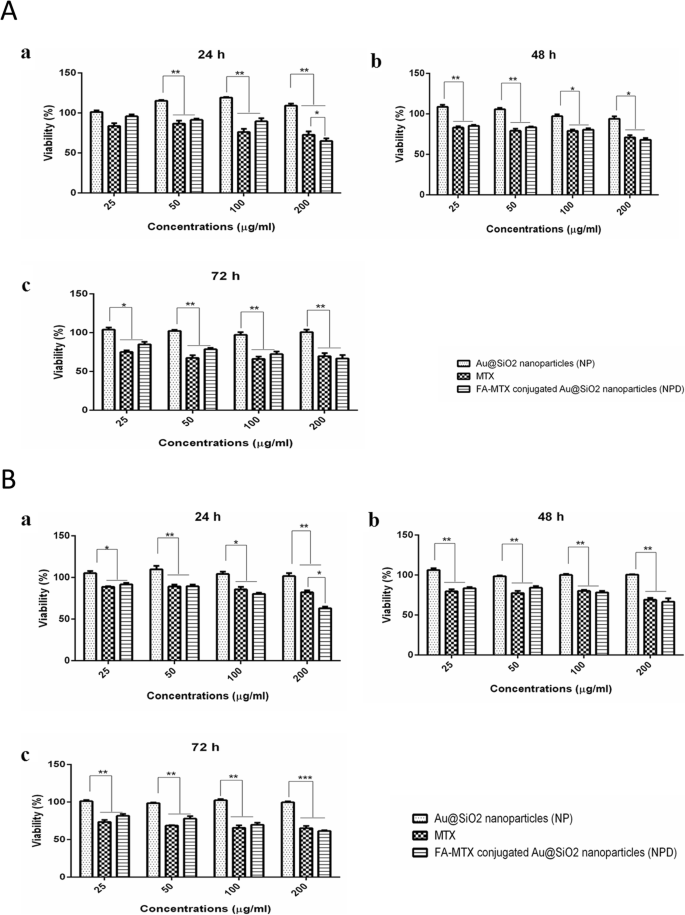
a MCF-7 e ( b ) Taxas de inibição de crescimento de células MDA-MB-231 após tratamento com diferentes concentrações de NP, MTX e FA-MTX Au @ SiO 2 nanopartículas (NPD) após o tempo de exposição de 24, 48 e 72h
Irradiação a laser
Neste estudo, a viabilidade celular de células MCF-7 e MDA-MB 231 tratadas com Au @ SiO 2 NPs e MTX-FA carregados com Au @ SiO 2 NPs após irradiação de laser com dose na faixa de 30-105 J / cm 2 foi investigado pelo ensaio MTT. A taxa de mortalidade de células MCF-7 e MDA-MB-231 tratadas com Au @ SiO carregado com MTX-FA 2 NPs (a concentração de MTX era de 100 μg / mL) após LLLT a uma dose de 75 J / cm 2 eram cerca de 39 e 45,5%, respectivamente. Enquanto na mesma condição, as células tratadas com Au @ SiO 2 NPs após irradiação de laser ou laser sozinho não mostraram morte celular óbvia. Também aumentando a dose do laser para 105 J / cm 2 a taxa de mortalidade de ambas as linhas celulares aumentou para 60-75%, enquanto ambas as células foram tratadas com Au @ SiO 2 NPs + laser ou laser sozinho na mesma dose de irradiação não mostraram efeito citotóxico. O valor de IC50 para células MCF-7 e MDA-MB-231 após terapia de combinação com Au @ SiO carregado com MTX-FA 2 NPs (dose de MTX de 100 μg / mL) e LLLT foram obtidos a uma dose de 90 e 75 J / cm 2 , respectivamente. Por outro lado, a taxa de mortalidade de Au @ SiO 2 carregado com MTX e MTX-FA NPs sem irradiação a laser na dose de MTX de 100 μg / mL (dose selecionada para estudo de terapia a laser) estava entre 15-25% em ambas as linhas celulares. Estes resultados indicaram que a combinação de MTX-FA carregado com Au @ SiO 2 NPs e terapia a laser mostraram um efeito sinérgico em ambas as linhas celulares e diminuíram significativamente a viabilidade celular ( p <0,001) em comparação com as células que receberam apenas irradiação a laser. Esses resultados indicaram que o tratamento com NPs, especialmente com estratégia de direcionamento, pode melhorar a eficácia da terapia a laser na destruição das células do câncer de mama (Fig. 7).
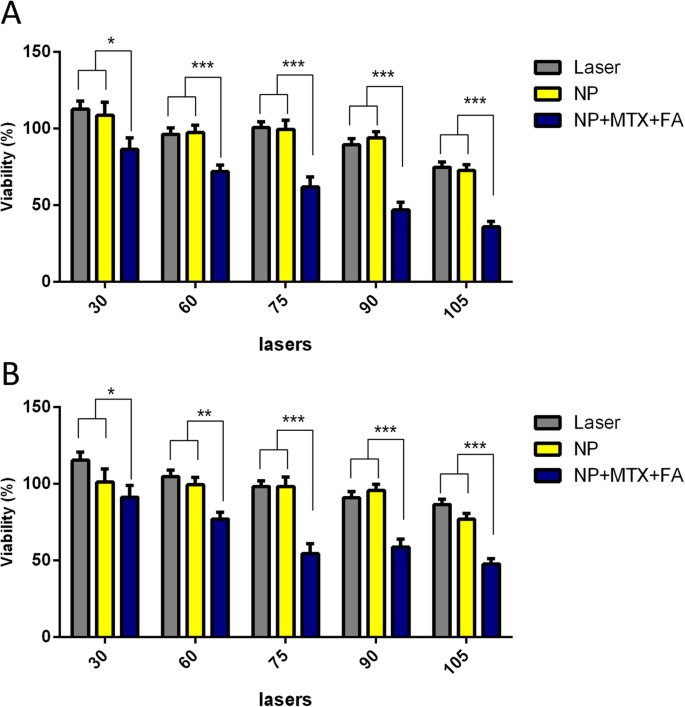
A comparison of cell growth inhibition rates exposed to different laser powers (30, 60, 75, 90 and 105 J/cm 2 ) for treatment groups of laser alone, laser + Au@SiO2 nanoparticles and laser + MTX-FA loaded Au@SiO2 nanoparticles directed for two cell line MCF-7 (a ) and MDA-MB-231(b ) with subsequent checking after 24h
Apoptosis study by DAPI
The apoptosis were studied in MCF-7 and MDA-MB-231 cells after treatment with Au@ SiO2 NPs; MTX-FA loaded Au@ SiO2 NPs with or without laser to know if laser treatment could enhance the efficacy of chemotherapy. Our results summarized in Fig. 8 indicated that normal MCF-7 and MDA-MB-231 cells without any treatment set as control as well as cells treated with laser alone or free Au@SiO2 NPs without laser irradiation had typical nuclei, lacking any apoptosis. However, MCF-7 and MDA-MB-231 cells treated with free MTX, Au@ SiO2 NPs with laser irradiation and MTX and FA loaded Au@SiO2 NPs without laser irradiation showed partial apoptotic nuclei (Fig. 8). The cells treated with MTX and FA loaded Au@SiO2 NPs in combination with laser irradiation (810 nm, 75 J/cm 2 , 139 sec) showed a major drop in MCF-7 and MDA-MB-231 cell population. Therefore, laser irradiation efficacy was enhanced after MTX/FA loaded Au@SiO2 NPs uptake on MCF-7 and MDA-MB-231 cells. Hence, the novel developed MTX and FA loaded Au@SiO2 NPs has the capability of augmenting the photothermal effects by highly fragmented cell nuclei, a radical rise in cell loss and complete damage of cells.

Apoptosis assay using DAPI staining for MCF-7 or MDA-MB-231 cells, images captured using an inverted microscope. The untreated cells as the negative control (a ), cells treated with laser (75 J/cm 2 ) as positive control (b ) cells treated with Au@SiO2 nanoparticles (NP (c ), cells treated with laser (75 J/cm 2 ) and Au@SiO2 nanoparticles (NP) (d ), cells treated with MTX without laser irradiation (e ), cells treated with MTX and laser irradiation (f ), cells treated with MTX-FA-loaded Au@SiO2 nanoparticles (NPD) without laser exposure (g ), and cells treated with MTX-FA-loaded Au@SiO2 nanoparticles (NPD) with Laser exposure (h )
Cell cycle
Cell cycle distributions after treatment with MTX, Au@SiO2 NPs and MTX and FA loaded Au@SiO2 NPs either in combination with LLLT (75 J/cm 2 ) or without laser irradiation was studied in both MCF-7 and MDA-MB-231 cells using flowcytometry and PI staining of DNA. Our study indicated that in MDA-MB-231 or MCF-7 cells, the percentage of non-treated cells (control group) were actively in phase S (Fig. 9a, b). Using 75 J/cm 2 laser treatments reduced the percentage of cells in S-phase in a non-significant manner. On the other hand the cells irradiated with LLLT without NP and drug treatment showed the significant increase in Go/G1 cell population indicated the safety of LLLT alone. Also NPs treatment did not disturb the cell cycle in both cell lines. Treatment of cells with free MTX in the absence or presence of laser irradiation showed some disturbances in cell cycles, including reduction of cells in S-phase. Using NPD alone reduced the cells in S-phase. And interestingly using MTX and FA loaded Au@SiO2 NPs (NPD) enhanced the cell percentage in sub Go/G1 as a sign of apoptosis [72]. Also the percentage of the MDA-MB-231 cells present in sub Go/G1 (around 18%) were significantly higher than MCF-7 cells (12%) in MTX and FA loaded Au@SiO2 NPs (NPD) treatment group due to the higher uptake of NPs in MDA-MB-231 cells.
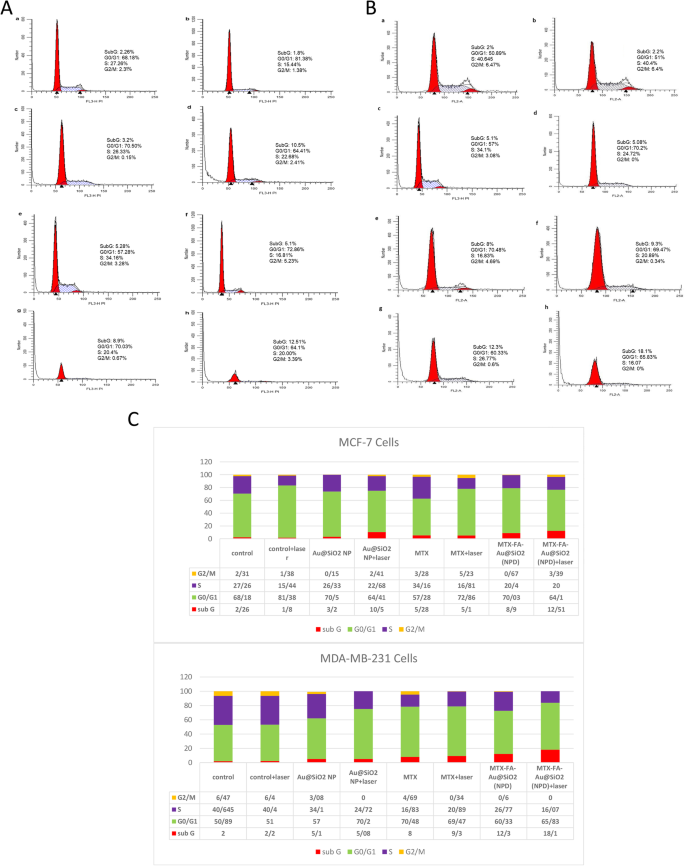
Cell cycle distributions investigated for MCF-7 (A ) or MDA-MB-231 (B ) células. The untreated cells as negative control (a ), cells treated with laser (75 J/cm 2 ) as positive control (b ) cells treated with Au@SiO2 nanoparticles (NP) (c ), cells treated with laser (75 J/cm 2 ) and Au@SiO2 nanoparticles (NP) (d ), cells treated with MTX without laser irradiation (e ), cells treated with MTX and laser irradiation (f ), cells treated with MTX-FA-loaded Au@SiO2 nanoparticles (NPD) without laser exposure (g ), and cells treated with MTX-FA-loaded Au@SiO2 nanoparticles (NPD) with Laser exposure (h ), C ) Quantitative results of cell cycle arrest and its distribution
Ramos et al , showed that in tumor cells, LLLT increases the percentage of cells in S and G2 /M phases, also they detected a reduction in proliferation and enhancing in senescence [79]. The cell cycle study after LLLT (15 J/cm2) showed a G1 arrest, which is in line with growth stopover in irradiated TK6 cells [80]. Another group reported that PTT is primarily disturbing cells in the S phase and increasing the cell population and arrest in the G2/M phase [81]. As a result, PTT can induce radio-sensitization of the cells via disturbing cell cycle [82]. Their results are in accordance with our study, which showed cell cycle disturbance and reduction of cells in S-phase. Our study also showed the increase in population of apoptotic cells (sub Go/G1) after combination chemo-photothermal therapy. Therefore, applying a combination of LLLT and MTX and FA loaded Au@SiO2 NPs (NPD) as breast cancer targeted nanoparticles could enhance the breast cancer therapy efficacy.
Conclusões
In this study MTX and FA loaded Au@SiO2 NPs was designed for target breast cancer therapy in combination with LLLT as noninvasive, FDA approved laser therapy. MTX and FA loaded Au@SiO2 NPs with spherical morphology and mean diameter of 25nm and surface charge of -19.7 was obtained. This size and surface charge is in a suitable range to increase the bio-distribution of NPs. The successful targeted strategy of this novel developed NPs was approved with a higher cellular uptake percentage of MDA-MB-231 compared to MCF-7 as two breast cancer cell lines with different folate receptor expression. The MTT assay, DAPI staining and cell cycle study's results indicated that the combination of chemo-photothermal therapy showed synergistic effect and the cytotoxicity and apoptosis effect on both breast cancer cell lines especially on MDA-MB-231 cells was increased significantly(p <0.001). Since the Au@SiO2 nanoparticles or LLLT showed no cytotoxic effects, it can be concluded that our therapeutic design has synergistic effects on targeted site. The findings of this study could be useful for designing future cancer therapy programs using bio-chemotherapy combined with low level lasers.
Disponibilidade de dados e materiais
Não aplicável
Abreviações
- Au@SiO2 :
-
Silica coated gold
- BC:
-
Câncer de mama
- DHFR:
-
Dihydrofolate reductase
- DMSO:
-
Dimethyl Sulfoxide
- FA:
-
Folato
- LLLT:
-
Low level laser therapy
- LSPR:
-
Ressonância de plasmon de superfície localizada
- MSN:
-
Nanopartícula de sílica mesoporosa
- MTX:
-
Metotrexato
- NIR:
-
Próximo ao infravermelho
- NPs:
-
Nanopartículas
- PTT:
-
Terapia fototérmica
- RhoD:
-
rhodamine B
- TFSNPs:
-
Thiol-functionalized silica-coated nanoparticles
Nanomateriais
- Nanopartículas para terapia do câncer:progresso e desafios atuais
- A detecção fotoeletroquímica aprimorada de ácido úrico em nanopartículas de Au Eletrodo de carbono vítreo modificado
- Nanopartículas de sílica para entrega de proteína intracelular:uma nova abordagem de síntese usando proteína fluorescente verde
- Efeito do método de síntese de La1 - xSr x MnO3 nanopartículas de manganita em suas propriedades
- Comparação entre o ácido fólico e a funcionalização baseada no peptídeo gH625 de nanopartículas magnéticas Fe3O4 para internalização celular aprimorada
- Propriedades das nanopartículas de óxido de zinco e sua atividade contra micróbios
- Síntese fácil de nanopartículas de irídio livres de ligante e sua biocompatibilidade in vitro
- Síntese one-pot de nanopartículas de núcleo-shell monodispersas CoFe2O4 @ Ag e sua caracterização
- O efeito da apoptose nas células cancerosas do fígado de nanopartículas de ouro modificadas com ácido litocólico
- Nova entrega de mitoxantrona com nanopartículas de pululano modificadas hidrofobicamente para inibir as células cancerosas da bexiga e o efeito do tamanho do nanofármaco na eficiência da inibiçã…



