Síntese fácil de nanopartículas de irídio livres de ligante e sua biocompatibilidade in vitro
Resumo
Nanopartículas inorgânicas de alta densidade têm se mostrado promissoras em aplicações médicas que utilizam radiação, incluindo imagens de raios-X e como intensificadores de dose de radiação para radioterapia. Nós desenvolvemos um método sintético aquoso para produzir pequenas (~ 2 nm) nanopartículas de irídio (IrNPs) por redução do cloreto de irídio (III) usando um agente redutor de boro-hidreto. Ao contrário de outros métodos de síntese baseados em solução, IrNPs uniformes e monodispersos são produzidos sem o uso de surfactantes ou outros ligantes de solubilização. Essas nanopartículas são altamente cristalinas, conforme observado por difração de raios-X e microscopia eletrônica de transmissão de alta resolução (TEM). Ensaios de toxicidade metabólica in vitro usando células de hepatócitos e macrófagos demonstram que ambos os IrNPs e o cloreto de irídio (III) são bem tolerados em concentrações de até 10 μM de irídio. Além disso, os IrNPs foram avaliados em um ensaio hemolítico e não tiveram impacto significativo sobre os glóbulos vermelhos quando expostos a concentrações de até 100 μM. No geral, esses resultados suportam o potencial para a aplicação in vivo deste nanomaterial.
Histórico
Nanopartículas de metais nobres são um dos pilares das nanotecnologias emergentes devido às suas interessantes propriedades ópticas, eletrônicas e catalíticas de superfície. Na nanomedicina, esses biomateriais exclusivos têm chamado a atenção significativa devido à capacidade de adequar suas interações biológicas por meio de modificações de superfície para uma ampla gama de aplicações [1]. Nanopartículas de ouro (AuNPs) foram investigadas extensivamente para aplicações de detecção e terapêuticas [2, 3], enquanto outros metais nobres, incluindo prata, encontraram usos de nicho, como antimicrobianos [4]. No entanto, nanopartículas compostas de elementos platinóides, comumente empregados por suas propriedades catalíticas de superfície [5], ainda não foram exaustivamente examinadas para aplicações biomédicas. A estabilidade de superfície excepcional e compatibilidade biológica conhecida desses elementos, bem como suas novas propriedades físicas potenciais em nanoescala, os tornam alternativas únicas para AuNPs.
A radiação de alta energia é amplamente utilizada na medicina, incluindo em imagens de diagnóstico e radioterapia. Portanto, materiais funcionais que interagem com a radiação, como alto número atômico e nanopartículas de alta densidade, podem melhorar o desempenho dessas modalidades. A maioria dos estudos químicos e de engenharia até agora se concentraram em AuNPs para aumentar as interações de radiação, embora o bismuto e o háfnio tenham sido examinados para aplicações diagnósticas e terapêuticas, respectivamente [6, 7].
Aqui, apresentamos um método sintético para a produção de nanopartículas de irídio (IrNPs), que devem ter forte atenuação de radiação devido à sua alta densidade. O irídio é um dos metais menos reativos, considerado geralmente biologicamente compatível e tem uma densidade elementar de 22,56 g / cm 3 (perdendo apenas para o ósmio, que é conhecido por ser altamente tóxico). Um isótopo de irídio, 192 Ir, é um emissor gama de braquiterapia comumente usado, e parte do sucesso desse material se deve à alta densidade, ou seja, ao grande número de átomos em um pequeno volume do material. No presente estudo, apresentamos a síntese de IrNPs e sua biocompatibilidade in vitro, bem como a de íons irídio, que não foi avaliada anteriormente nas linhagens celulares selecionadas. Esses novos IrNPs não foram explorados prontamente para fins médicos, apesar da inércia química e densidade superior do material. Embora o irídio seja um material relativamente caro como outros metais nobres, seu valor atual como mercadoria é de aproximadamente três quartos do preço do ouro e metade do preço do ródio, o que o torna uma alternativa econômica interessante.
Métodos
Síntese de IrNPs
Todas as reações de síntese foram realizadas à temperatura ambiente sob condições aeróbias em água 18 M + purificada. Um estoque de cloreto de irídio (III) 20 mM (Acros Organics) foi preparado por sonicação de banho e agitado por pelo menos 20 min para gerar uma solução opticamente límpida. Uma solução de morfolina de borano 1,0 M (Alfa Aesar) também foi preparada por sonicação de banho. Para sínteses em maior escala de 500 mL de volume total, 25 mL de solução de cloreto de irídio (III) foram usados (diluídos para 1,0 mM) e 5,0 mL de morfolina de borano foram adicionados (concentração final de 10 mM) com agitação rápida. A solução mudou gradualmente de castanho escuro para preto ao longo de 30 min. As nanopartículas estabilizaram por pelo menos 60 min. Esta solução coloidal foi adicionada diretamente a filtros de rotação centrífuga (Amicon Ultra-4, celulose regenerada de 10k MWCO), e as nanopartículas foram coletadas a 4000 × g e lavado em água purificada. As nanopartículas foram então suspensas em água, passadas por um filtro de seringa (Millex-MP 0,22 μm EO) e armazenadas para quantificação.
Caracterização de nanopartículas
Para a análise de espectroscopia de fotoelétrons de raios-X (XPS), as nanopartículas foram suspensas em um volume igual de ácido nítrico, coletadas por centrifugação em um tubo de microcentrífuga (5 min, 17 rcf) e suspensas em água antes da análise. A microscopia eletrônica de transmissão (TEM) foi realizada em um FEI Tecnai F-20 TEM operando a 200 kV. IrNPs purificados foram fundidos em soltar em grades TEM suportadas por Cu carbono holey (Ted Pella) e secos à temperatura ambiente durante a noite. A análise de difração de linha foi realizada usando a análise de software ImageJ. Para análise de difração de raios-X (XRD), IrNPs concentrados foram moldados em uma lâmina de vidro e secos em temperatura ambiente. Os dados de XRD foram coletados em geometria de feixe focalizado (Bragg-Brentano) em um sistema de difração de raios-X Rigaku Ultima IV usando radiação monocromatizada de grafite Cu Kα. As varreduras foram realizadas na faixa angular de 20–80 ° 2θ a uma taxa de varredura de 0,1 ° / min em temperatura ambiente. O espalhamento de luz dinâmico (DLS) foi realizado em um Malvern Nano ZSP em cubetas de poliestireno descartáveis. As nanopartículas foram suspensas na água e os dados são relatados como distribuídos por número. Os espectros de absorbância de UV-Vis foram coletados em um Tecan M200 Pro em uma placa preta de 96 poços e um volume total de solução de 100 μL. As concentrações de irídio foram ajustadas para ilustrar os picos de absorvância relativa. A análise de XPS foi realizada em um PHI Versaprobe II equipado com um analisador de elétrons hemisférico e fonte de raios-X de alumínio Kɑ (1486,7 eV). A análise de espectro foi realizada usando o pacote de software Multipak. A calibração da energia de ligação foi realizada usando o pico C1s em 284,6 eV, e o ajuste do pico foi baseado em picos assimétricos e um fundo de Shirley iterado, resultando em um valor qui-quadrado de 1,13. A espectrometria de massa com plasma indutivamente acoplado (ICP-MS) de IrNPs e solução de cloreto de irídio (III) foi avaliada antes dos ensaios de toxicidade biológica. Cinqüenta microlitros de cada solução de IrNP foram digeridos em 50 μL de água régia (3:1 M de ácido nítrico concentrado em ácido clorídrico) durante a noite a 70 ° C em um tubo de digestão. As amostras foram então diluídas em 5,0 mL de ácido nítrico a 1% para análise. O ICP-MS foi realizado em um Agilent 7900 usando hélio como gás de colisão. As curvas de calibração foram preparadas usando soluções estoque de irídio de 100–0,1 μg / mL (em HCl a 1%) e todas as amostras foram diluídas de forma que as concentrações foram medidas na faixa de dezenas de ppb.
Análise de Citotoxicidade
As linhas celulares HepG2 e J774A.1 foram semeadas em 2 × 10 5 células por poço (100 μL) em uma placa de 96 poços (DMEM com 10% de FBS) e deixou-se sedimentar por 24 h. Nanopartículas de irídio, sal de irídio, água ou DMSO foram adicionados em um volume de 10% (volume adicional de 10 μL). As células foram então incubadas por 24 ou 48 h. Para análise de viabilidade, o meio foi removido e as células foram lavadas uma vez em PBS. Cem microlitros de meio de cultura com 10% de Alamar Blue (Thermo Scientific) foram incubados com células por 2 h . O meio foi então plaqueado novamente em uma placa preta de 96 poços e a fluorescência foi lida (ex530 / em590) em um Tecan M200 Pro. Todos os dados foram realizados em quadruplicado e as experiências foram repetidas em dias independentes para confirmar as tendências gerais. Um ensaio hemolítico foi realizado conforme relatado anteriormente [8].
Resultados
Síntese e caracterização de nanopartículas de irídio
Nesta síntese, formamos IrNPs elementares a partir do sal de cloreto de irídio (III) por redução com um excesso molar de 10 vezes de borano morfolina em água. A reação é facilmente escalonável para vários litros e as partículas são formadas à temperatura ambiente em condições aeróbias. Este método sintético produz pequenos (2–3 nm) IrNPs uniformes (Fig. 1a) com um alto grau de cristalinidade, conforme observado por imagens TEM de alta resolução. Os padrões de difração obtidos a partir de TEM confirmam ainda mais a identidade dos nanocristais, com um espaçamento de linha de 0,22 nm que é indicativo da rede de difração de irídio (Fig. 1b). O padrão de difração de raios-X é muito parecido com o do irídio elementar (PDF Card No .:9008470, Fig. 1c). Conforme sintetizado, os IrNPs são coloidalmente estáveis em água e permanecem suspensos em solução por vários meses à temperatura ambiente (Fig. 1d).
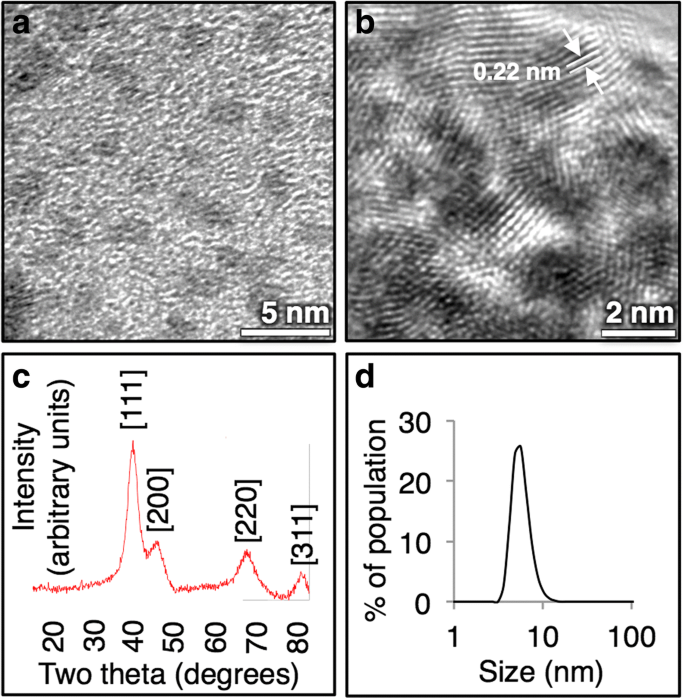
a Nanopartículas de irídio são 2-3 nm por imagem TEM, com b com um parâmetro de rede altamente cristalino. c O espectro de XRD corresponde ao irídio elementar e d partículas têm um tamanho hidrodinâmico de 5 nm em água por DLS
Os nanocristais se formam ao longo de 30 minutos, conforme observado por uma mudança de cor do precursor de irídio (III) amarelo claro para uma solução de nanopartícula preta escura (Fig. 2). Quando expostos a um ambiente básico, esses IrNPs formam um óxido de irídio previsto, que aparece em azul. As condições ácidas, como a incubação em ácido nítrico puro, não parecem afetar a cristalinidade das partículas ou a integridade do material; no entanto, induz floculação e precipitação. Além disso, a agregação também foi observada em soluções biologicamente relevantes (solução salina tamponada com fosfato e meio de cultura de tecidos) ao longo das horas, sugerindo que modificações adicionais da superfície serão necessárias para futuras aplicações biomédicas. A análise de espectroscopia de fotoelétrons de raios-X dos IrNPs lavados em ácido nítrico e suspensos em água revelam uma superfície de irídio (0) predominante, embora a análise de ajuste de pico de dados indique 20% de oxidação da superfície (Fig. 3). Nenhuma orientação de cristalito preferida de partículas é observada, seja por XRD ou por XPS. Alternativamente, a introdução de um tensoativo tiol na solução de reação durante o processo de síntese (antes da nucleação) resultou na inibição da formação de partículas.
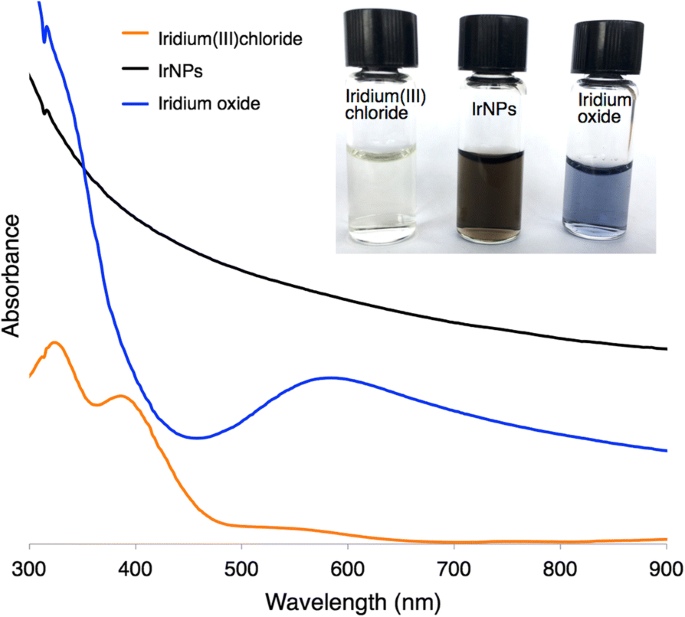
O cloreto de irídio (III) parece amarelo pálido com picos de absorvância a 324 e 386 nm. IrNPs são absorvedores de amplo espectro e aparecem em preto. O óxido de irídio (previsto), produzido a partir de IrNPs oxidados tratados em uma solução básica, aparece roxo-azulado com um pico de absorbância em 584 nm
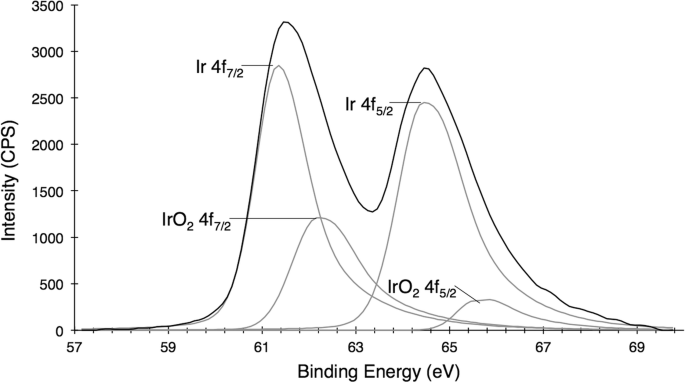
Espectroscopia de fotoelétrons de raios-X (XPS) de IrNPs um estado de superfície de irídio predominantemente elementar, com aproximadamente 20% de contaminação da superfície de óxido
Citotoxicidade de irídio
Avaliamos a compatibilidade biológica in vitro dos IrNPs não protegidos e comparamos com o sal de cloreto de irídio (III) em dois tipos de células de mamíferos. HepG2, uma linha de células de carcinoma de hepatócitos, foi usada para avaliar a toxicidade potencial para o fígado. Células de macrófagos J774A.1 foram usadas para avaliar a toxicidade para o sistema fagocítico mononuclear. As células foram incubadas com IrNPs ou cloreto de irídio (III) (normalizado para concentração total de irídio) por 24 ou 48 horas e lavadas para remover irídio extracelular, e a atividade metabólica foi avaliada usando o ensaio Alamar Blue (Fig. 4). As células HepG2 mostram aumento da atividade metabólica na presença de irídio (III) em 24 h (até 115% de viabilidade), mas a resposta é mitigada em 48 h, com 500 μM de irídio (III) reduzindo a viabilidade para 90%. As células HepG2 tiveram uma viabilidade celular reduzida, de 94 a 78% na presença de IrNPs 50 μM em 24 e 48 h. Curiosamente, as células J774A.1 mostram um aumento na atividade metabólica em resposta a IrNPs a uma concentração de 50 μM com uma viabilidade de 122% em 24 h; entretanto, após 48 h, a função celular normal foi retomada (98% de viabilidade), sugerindo uma estimulação metabólica transitória em resposta aos nanomateriais. As células J774A.1 incubadas com 500 μM de IrNPs por 24 h mostram uma resposta metabólica aparentemente neutra, mas a diminuição na viabilidade nesta concentração após 48 h sugere que isso é um resultado de toxicidade e estimulação metabólica que aparece como uma resposta de viabilidade neutra. Além disso, avaliamos a biocompatibilidade in vitro de IrNPs com sangue por meio de um ensaio hemolítico e descobrimos que os IrNPs não induziram nenhuma hemólise significativa quando incubados com eritrócitos em PBS a 37 ° C por 1 h (Arquivo adicional 1:Figura S1).
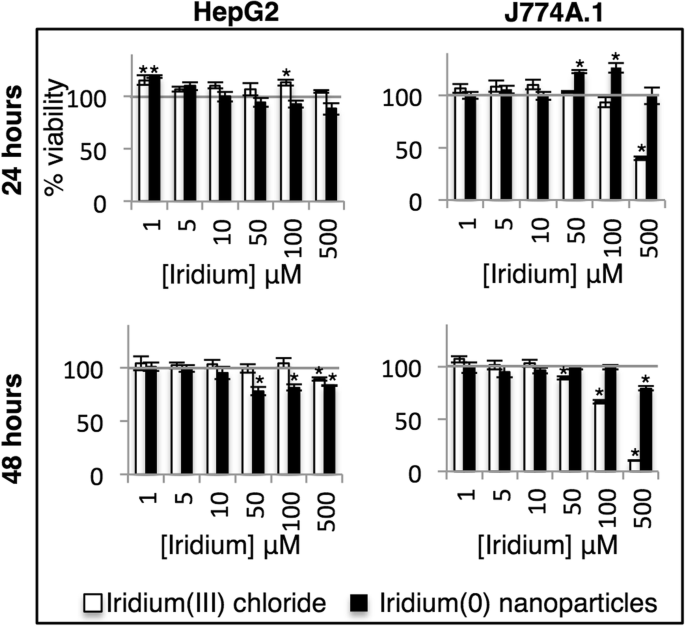
Viabilidade celular de células HepG2 e J774A.1 incubadas com nanopartículas de Ir (0) ou sal de Ir (III) por 24 ou 48 h. * Valores estatisticamente significativos ( p <0,05) em relação às células não tratadas
Discussão
Vários processos sintéticos foram examinados para produzir irídio em nanoescala para aplicações catalíticas, incluindo a redução de sais de irídio por hidretos e gás hidrogênio [9,10,11,12,13], radiação UV e gama [14,15,16,17], e redução de poliol ou álcool [18,19,20]. No entanto, muitos desses métodos sintéticos são projetados para integração de irídio em um substrato ou suporte para reações químicas e não são compatíveis com aplicações biológicas [21]. Recentemente, aerossolizado 192 Ir foi empregado como modelo de materiais em nanoescala para toxicidade pulmonar e foi escolhido por sua excepcional inércia [22, 23]. O objetivo principal desses estudos foi examinar a eliminação e a translocação de partículas finas inaladas dos pulmões; no entanto, também destaca a biocompatibilidade deste elemento.
Avaliamos a compatibilidade biológica in vitro dos IrNPs não protegidos e comparamos com o sal de cloreto de irídio (III) em dois tipos de células de mamíferos que devem acumular as maiores concentrações de nanopartículas injetadas. A toxicidade de irídio (III) em células J774A.1 segue uma curva de dose-resposta de toxicidade normal; 100 μM de irídio (III) reduz a viabilidade celular para 93 e 66%, e 500 μM resulta em 40 e 10% de viabilidade celular em 24 e 48 h, respectivamente. Esses dados refletem uma resposta específica de célula interessante ao irídio (0) e irídio (III), e prevemos explorar mais esses efeitos in vivo. Espera-se que IrNPs menores e outros nanomateriais inorgânicos fracamente solúveis sejam translocados para o rim e o fígado, com uma residência temporal curta nos rins e uma residência mais longa no fígado, o que pode impactar ainda mais os perfis de toxicidade específicos da célula. A excreção é esperada através das fezes para partículas maiores de irídio, embora esperemos que o tamanho extremamente pequeno desses IrNPs possa ser facilmente filtrado através do sistema renal se a estabilidade coloidal in vivo puder ser mantida [23].
Em preparação para aplicações in vivo, a compatibilidade sanguínea dos IrNPs foi avaliada por um ensaio hemolítico. Utilizando sangue total de camundongo, avaliamos o efeito desses IrNPs na ruptura dos eritrócitos e na liberação potencial de hemoglobina. Embora estudos aprofundados da superfície final modificada IrNP precisem ser avaliados, os blocos de construção IrNP atuais não eliciam uma resposta hemolítica detectável até concentrações extremamente altas (500 μM).
Conclusões
Concluímos a partir desses estudos que os nanocristais de irídio (0) podem ser prontamente sintetizados por uma redução de boro-hidreto aquoso simples de cloreto de irídio (III), que resulta em nanopartículas altamente cristalinas de 2-3 nm que são coloidalmente estáveis em água com uma hidrodinâmica de aproximadamente 5 nm Tamanho. Durante a exposição aguda, essas partículas não são tóxicas em concentrações de até 50 μM de irídio (em comparação com 10 μM para cloreto de irídio) em hepatócitos, estimulam a atividade metabólica em células de macrófagos e não provocam uma resposta hemolítica em concentrações práticas. Essas nanopartículas livres de ligante podem servir como blocos de construção ou núcleos para IrNPs modificados de superfície subsequentes para uso em aplicações biológicas e médicas. Uma investigação mais aprofundada das propriedades funcionais desses nanomateriais de alta densidade na presença de raios-X ou outra radiação apresenta a oportunidade para novos agentes terapêuticos e de diagnóstico.
Abreviações
- AuNP:
-
Nanopartícula de ouro
- DLS:
-
Espalhamento de luz dinâmico
- ICP-MS:
-
Espectrometria de massa com Plasma indutivamente acoplado
- IrNP:
-
Nanopartícula de irídio
- PDF:
-
Arquivo de difração de pó
- UV:
-
Ultravioleta
- XPS:
-
espectroscopia de fotoelétrons de raios-X
- XRD:
-
Difração de raios X
Nanomateriais
- Nanopartículas multifuncionais de ouro para aplicações diagnósticas e terapêuticas aprimoradas:uma revisão
- Síntese fácil e propriedades ópticas de pequenos nanocristais de selênio e nanorods
- Síntese fácil de compósito CuSCN colorido e condutor revestido com nanopartículas de CuS
- Estudo in vitro da influência das nanopartículas de Au nas linhas celulares HT29 e SPEV
- Propriedades de síntese e luminescência de nanopartículas α-NaGdF4 / β-NaYF4:Yb, Er Core – Shell solúveis em água
- Síntese e desempenho in vitro de nanopartículas de ferro-platina revestidas com polipirrole para terapia fototérmica e imagem fotoacústica
- Síntese de pontos quânticos de sulfeto de antimônio solúvel em água e suas propriedades fotoelétricas
- Efeito do método de síntese de La1 - xSr x MnO3 nanopartículas de manganita em suas propriedades
- Síntese de um vaso de nanoplacas Cu2ZnSnSe4 e sua atividade fotocatalítica orientada por luz visível
- Síntese fácil e ecológica de nanofios de Co3O4 e sua aplicação promissora com grafeno em baterias de íon-lítio



