Co-entrega de dacarbazina e ácido retinóico trans (ATRA) usando nanoformulações lipídicas para eficácia antitumoral sinérgica contra melanoma maligno
Resumo
O melanoma maligno é um câncer de pele altamente agressivo, responsável por 80% da mortalidade, e a sobrevida média geral em pacientes com melanoma metastático é de apenas 6–9 meses. O tratamento combinado por meio da administração simultânea de drogas duplas em um único nanocarreador demonstrou ser elegante e eficaz no combate ao câncer. Aqui, empregamos uma terapia de combinação à base de dacarbazina (DBZ), medicamento aprovado pela FDA para melanoma e ácido trans retinóico (ATRA), agentes anticâncer promissores carregados em nanoformulações lipídicas (RD-LNF) como uma nova estratégia de tratamento para melanoma maligno. Encapsulamos com sucesso ambas as drogas em nanoformulações lipídicas e mostramos uma liberação controlada de carga útil ao longo do tempo. Demonstramos que a entrega simultânea de DBZ e ATRA pode reduzir efetivamente a proliferação celular de maneira dependente da concentração. As nanopartículas combinatórias reduziram significativamente a capacidade de formação de colônias das células de melanoma B16F10. A análise por citômetro de fluxo mostrou que RD-LNF induziu uma maior proporção de células em apoptose com inibição significativa da progressão do ciclo celular e migração celular. Esses resultados sugerem o potencial promissor do RD-LNF no tratamento do melanoma maligno com alta eficácia.
Introdução
O melanoma maligno é uma das doenças malignas agressivas que ocorre predominantemente na pele humana [1]. O melanoma é responsável por 4% de todos os cânceres dermatológicos, porém é responsável por 80% da mortalidade por câncer de pele e se tornando uma preocupação crescente em países subdesenvolvidos e em desenvolvimento [2, 3]. O melanoma tem alta tendência a metastatizar para várias partes do corpo, incluindo cérebro, coração e pulmões, tornando-se uma das formas agressivas de doenças malignas [4]. Se diagnosticada em estágios iniciais, a excisão cirúrgica está entre as opções terapêuticas potenciais. No entanto, a intervenção cirúrgica não garante a recuperação completa do melanoma [5]. Além disso, a fase de crescimento radial desta malignidade torna-se resistente à maioria das outras opções de tratamento, incluindo quimioterapia e radioterapia [6]. Para ser específico, os receptores de peptídeos são superexpressos na superfície do câncer de melanoma, tornando-o uma perspectiva atraente. O receptor de somatostatina subtipo 2 (SSTR2) demonstrou ser altamente expresso nas células de melanoma [7].
Dacarbazina (DBZ) ou dimetil-triazeno-imidazol carboxamida (DTIC), um agente alquilante de DNA, é a única e primeira escolha de medicamento quimioterápico aprovado pela Food and Drug Administration (FDA) [8]. DBZ é um forte agente alquilante que mata as células cancerosas adicionando os grupos alquil ao DNA ou materiais nucleares das células cancerosas [9]. Apesar de sua ação potente, DBZ sofre de baixa solubilidade aquosa e meia-vida curta (41 min) na circulação sanguínea diminuindo seu efeito terapêutico no tratamento de doenças malignas do melanoma [10]. Além disso, uma taxa de resposta decepcionante entre 10 e 25% foi observada com menos de 5% de recuperação completa do câncer, indicando a limitação de uma terapia com um único agente [11, 12]. Portanto, há uma necessidade urgente de desenvolver uma estratégia alternativa para melhorar a eficácia do tratamento com DBZ.
A coadministração de vários agentes terapêuticos em administração única provou ser mais eficaz em comparação com a do agente terapêutico individual [13]. A co-entrega de agentes terapêuticos em um único sistema transportador irá conferir a atividade sinérgica, propriedades farmacocinéticas semelhantes e maior eficácia anticâncer [14]. O ácido trans-retinóico (ATRA) é um agente anticâncer promissor usado no tratamento de vários tipos de câncer [15]. O ATRA exibiu sua eficácia terapêutica ao se ligar aos receptores do ácido retinóico no núcleo das células cancerosas, resultando na inibição do crescimento, proliferação, diferenciação e eventual morte celular [16]. Ao contrário de outros agentes quimioterápicos, o ATRA não resultou em nenhum efeito adverso, como cardiotoxicidade ou hipoplasia da medula óssea. Foi relatado que o ATRA aumenta a eficácia anticâncer quando usado em combinação com um agente quimioterápico apropriado. Novamente, o ATRA lipofílico sofre de baixa solubilidade aquosa e rápida depuração sistêmica, necessitando de um sistema de entrega estável [17].
Os sistemas de entrega nanoparticulados mostraram melhorar a eficácia terapêutica da terapêutica encapsulada, liberando-a nos tecidos tumorais alvo e evitando o efeito fora do alvo na circulação sistêmica, empregando efeito de permeação e retenção (EPR) aprimorada [18, 19]. As nanopartículas lipídicas sólidas (SLN) são consideradas alternativas a muitos transportadores existentes, incluindo lipossomas ou micelas, devido às características salientes, como estabilidade aprimorada, liberação controlada de fármaco, alta eficiência de carregamento e facilidade de preparação / aumento de escala [20] . Um dos aspectos importantes do SLN como um transportador de entrega de drogas é o perfil de segurança de lipídios que são de status GRAS, bem tolerados e lipídios fisiológicos [21]. A incorporação estável de drogas no núcleo lipídico melhora a solubilidade aquosa e melhora o perfil farmacocinético e estende a estabilidade fisiológica na circulação sistêmica [22].
Neste estudo, abordamos uma estratégia promissora de co-entrega de DBZ e ATRA usando nanoformulações lipídicas para o tratamento de combinação em neoplasias de melanoma. O DBZ deve ser carregado no núcleo lipídico, enquanto o ATRA deve fazer parte da estrutura das nanopartículas. Nós estudamos as propriedades físico-químicas, absorção celular e citotoxicidade in vitro de nanopartículas combinadas. Além disso, o efeito anticâncer foi avaliado por ensaio de apoptose, análise do ciclo celular, formação de colônia e análise de migração celular.
Conclusão
Em conclusão, formulamos com sucesso nanoformulações lipídicas carregadas com dacarbazina e ácido trans retinóico. Nossos resultados demonstram claramente que o RD-LNF inibe a proliferação de células de melanoma, induz notável apoptose e inibe a progressão do ciclo celular e as migrações celulares. O trabalho futurista se concentrará no estudo da eficácia anticâncer em modelos animais clinicamente relevantes e no desenvolvimento de uma terapia direcionada à malignidade do melanoma. Este é um estudo preliminar realizado nas células de melanoma e estudos de ampla gama em diferentes modelos animais clinicamente relevantes são a próxima parte de nosso trabalho de pesquisa.
Materiais e métodos
Preparação de nanoformulações lipídicas carregadas com DBZ / ATRA
As nanopartículas lipídicas carregadas com a droga foram preparadas pelo método de sonicação. Resumidamente, 10 mg de DBZ e 10 mg de ATRA foram dissolvidos em 2 ml de uma solução de clorofórmio contendo 50 mg de Egg 1-α-fosfatidilcolina (PC) e 2 mg de DSPE-metil (polietilenoglicol) -2000 (mPEG 2000 ) O solvente orgânico foi seco usando exposição a gás árgon durante 20 min. A mistura seca de fármaco + lípido foi adicionada com 80 mg de trimiristina (Tm) e incubada a 65 ° C durante 1 h. A esta mistura de óleo, 5 ml de solução de poloxâmero a 4% foram adicionados e imediatamente sonicados a 80 W por 6 min. A emulsão resultante foi arrefecida em gelo durante 30 min. As nanopartículas foram submetidas à unidade de filtro centrífugo Amicon Ultra 0,5 (corte de 3 kDa; Merck, Alemanha) a 12000 × g por 20 min. A quantidade de DBZ e ATRA livres no filtrado foi avaliada pelo método HPLC e a eficiência de carregamento e a capacidade de carregamento foram calculadas. O sistema Waters HPLC consistindo em uma bomba binária Waters 1525, detector Waters 2487 UV, detector de fluorescência Waters 2475, aquecedor de coluna 1500 e uma coluna Symmetry C18 foi usado para a análise do fármaco. Para ATRA, a fase móvel consistia em acetonitrila e ácido trifluoroacético na proporção 90/10 v / v a uma taxa de fluxo de 1 ml / min e detectada a 348 nm. Para DBZ, foram usados acetonitrila e hidrogenofosfato dissódico 0,05 M na proporção 30/70 v / v contendo 0,5% de TEA. O pH da fase móvel foi mantido a pH 3,7 e foi utilizado um caudal de 1 ml / min.
Análise de tamanho de partícula e morfologia
A distribuição do tamanho de partícula das nanopartículas combinadas foi avaliada por Malvern Zetasizer Nano ZS90 com um laser He-Ne (633 nm). Todas as amostras foram diluídas com água destilada e os experimentos foram realizados a 24 ° C em triplicata. A morfologia da nanopartícula foi avaliada por microscópio eletrônico de transmissão (TEM; JEOL JEM200CX a 120 kV). As partículas diluídas foram coradas com ácido fosfotúngstico 2%, secas e observadas em TEM.
Liberação de droga in vitro de nanoformulações carregadas de droga
A liberação dos fármacos encapsulados foi avaliada pelo método de diálise. Dois mililitros de nanopartículas carregadas com fármaco contendo um equivalente a 1 mg de ATRA e 1 mg de DBZ foram selados em uma membrana de diálise (Spectra / Por, MWCO 3,5 kDa). O tubo de diálise foi colocado em 25 ml de tampão de liberação e mantido em rotação de 100 rpm a 37 ° C. No intervalo de tempo predeterminado até 72 h, 1 ml das amostras foram retirados e substituídos por tampão fresco de igual quantidade. A quantidade de DBZ e ATRA foi avaliada pelo método HPLC conforme descrito acima.
Cultura de células e análise de captação celular
As células de melanoma de pele de murino (B16F10) foram adquiridas na China Infrastructure of Cell Line Resources (Pequim, China). As células foram cultivadas em meio RPMI-1640 suplementado com 10% de FBS e 1% da mistura de antibióticos. Os meios foram trocados regularmente a cada 2 dias e cultivados após confluência de 90%. Para a análise de absorção celular, as células B16F10 foram semeadas em uma placa de 6 poços para 24 h de incubação. As nanopartículas foram carregadas com Coumarin-6 como um rastreador fluorescente. O meio antigo foi removido e substituído por um meio fresco contendo nanopartículas de cumarina-6-lipídios e incubado por 1–3 h em ordem reversa. As células foram lavadas e descartadas com raspador de células. As células foram centrifugadas a 1200 rpm durante 5 min e o sedimento celular foi ressuspenso em 1 ml de PBS frio. As amostras foram avaliadas por citômetro de fluxo AccuriTM C6 (BD Co., EUA).
Ensaio de citotoxicidade in vitro
O efeito citotóxico de ATRA, DBZ, D-LNF e RD-LNF livres em células B16F10 foi avaliado por ensaio de MTT. As células (1 × 10 4 ) foram semeados em cada poço da placa de 96 poços e incubados por 24 h. As células foram primeiro tratadas com diferentes concentrações de ATRA e DBZ livres e testado seu efeito anticâncer nas células de melanoma. Seguido por, as células foram tratadas com uma concentração fixa de ATRA livre, DBZ, D-LNF e RD-LNF a 25 μg / ml e 50 μg / ml, respectivamente. As células foram incubadas por 24 horas e, em seguida, o meio foi cuidadosamente removido e lavado duas vezes com PBS. Ao final, as células foram tratadas com 100 μl de solução de MTT 5 mg / ml e incubadas por 4 h. O meio de cultura foi cuidadosamente removido e 100 μl de isopropanol foram adicionados e incubados por 15 min sob condições de agitação. Os cristais de formazan dissolvidos foram estudados a 570 nm usando um leitor de microplacas. As células não tratadas foram utilizadas como controle e os cálculos foram feitos com base na viabilidade celular dos controles.
Ensaio de apoptose - Citômetro de fluxo
O efeito de apoptose de ATRA, DBZ, D-LNF e RD-LNF livre em células B16F10 foi avaliado após a coloração com PE anexina V e kit de apoptose baseado em 7AAD. As células foram semeadas em uma placa de 12 poços a uma densidade celular de 2 × 10 5 células / poço e incubadas por 24 h. As células foram tratadas com 25 μg / ml equivalentes de formulações ATRA, DBZ, D-LNF e RD-LNF livres e as células não tratadas foram consideradas como um controle. Após 24 horas de exposição ao tratamento, as células foram coradas de acordo com o protocolo do fabricante. O citômetro de fluxo AccuriTM C6 foi usado para expressão de PE e 7AAD e um mínimo de 10.000 eventos foram adquiridos no citômetro de fluxo. As células PE-positivas e 7AAD-negativas foram apoptóticas precoces; As células PE-positivas e 7AAD-positivas eram apoptóticas tardias.
Análise do ciclo celular - Citômetro de fluxo
As células foram semeadas em uma placa de 12 poços a uma densidade celular de 2 × 10 5 células / poço e incubadas por 24 h. As células foram tratadas com 25 μg / ml equivalentes de formulações ATRA, DBZ, D-LNF e RD-LNF livres e as células não tratadas foram consideradas como um controle. Após 24 h, as células tratadas foram lavadas e coletadas por tripsinização e fixadas com etanol 70% por 2 h a 4 ° C. As células foram então tratadas com ribonuclease para se livrar de qualquer contaminação de RNA. Agora, as células foram coradas com iodeto de propídio (PI) por 30 min a 37 ° C na incubadora. A fluorescência das células coradas com PI foi determinada pelo citômetro de fluxo AccuriTM C6. A fase do ciclo celular foi dividida nas fases subG1, G1, S e G2 / M.
Ensaio de formação de colônia
As células foram semeadas em placas de 12 poços a uma densidade celular de 2 × 10 5 células / poço e incubadas por 24 h. As células foram tratadas com 25 μg / ml equivalentes de formulações ATRA, DBZ, D-LNF e RD-LNF livres. As células tratadas foram tripsinizadas, lavadas e contadas usando um contador de células. As células foram então semeadas em uma placa de 6 poços a uma densidade de 1500 células / poço. As células foram então incubadas em condições ambientais de 37 ° C durante 12 dias até que as colônias fossem visíveis. As células foram lavadas com PBS e fixadas com metanol em ácido acético em água (1:1:8) por 10 min, seguido por coloração com 0,1% de coloração violeta de cristal por 45 min. As células coradas foram então observadas ao microscópio óptico.
Ensaio de migração celular
Câmara transwell de doze poços com tamanho de poro de 8 μm foi usada para este ensaio. Para iniciar o estudo, 5 × 10 4 células / poço foi semeado na câmara superior. O meio superior é desprovido de FBS, enquanto o meio da câmara inferior consiste em 10% de FBS. Após 24 h, a quantidade de células migradas para a superfície da membrana inferior foi fixada e tingida com 0,5% de corante violeta de cristal. O número de células foi contado em cinco campos que foram selecionados aleatoriamente em um microscópio de luz; o número médio de células foi registrado e analisado.
Análise estatística
Os dados são apresentados como média ± DP e realizados em triplicado, a menos que seja mencionado de outra forma separadamente. Dois grupos foram comparados usando t não pareados testes, enquanto a comparação de mais de dois grupos foi feita usando ANOVA de uma via com o teste de comparação múltipla de Turquia. As estatísticas foram realizadas usando o software GraphPad Prism e uma diferença de p <0,05 foi considerado significativo.
Resultados e discussão
Preparação e caracterização de nanoformulações lipídicas carregadas com DBZ / ATRA
O tratamento do melanoma continua sendo um grande desafio e as opções de tratamento padrão, incluindo quimioterapia ou radioterapia ou ressecção cirúrgica, serão eficazes apenas nos tumores sólidos acompanhados de mau prognóstico. O FDA aprovou medicamentos como o paclitaxel ou sua combinação, mas não conseguiu melhorar o impacto geral na sobrevida do paciente e na cura do câncer. A dacarbazina (DBZ) é a droga quimioterápica de primeira linha aprovada pelo FDA; no entanto, DBZ sofre de propriedades físico-químicas fracas e resultou em uma taxa de resposta decepcionante entre 10 e 25%. Para lidar com esses desafios, desenvolvemos uma nova estratégia terapêutica de combinação com ATRA e DBZ em nanoformulações lipídicas (Fig. 1). Nossa hipótese é que a combinação de dois componentes terapêuticos aumentará a eficácia antitumoral em doenças malignas do melanoma. Vale ressaltar que o ATRA embora exiba propriedades anticâncer, não resultou em nenhum efeito adverso no ambiente sistêmico [23]. Como o DBZ é hidrofóbico por natureza, projetamos nanoformulações lipídicas que podem incorporar de forma estável as drogas hidrofóbicas no núcleo lipídico e o ATRA será carregado como um componente estrutural das nanopartículas. As nanopartículas lipídicas que transportam os componentes terapêuticos ajudarão a entregar no tumor muito profundo no corpo. A eficiência de carregamento de DBZ e ATRA foi de 91,2 ± 1,25% e 95,8 ± 1,14%, respectivamente. A capacidade de carga de DBZ e ATRA em RD-LNF foi de 7,07 ± 0,65% p / pe 7,48 ± 1,05% p / p, respectivamente. O tamanho de partícula de D-LNF foi observado como sendo 121,5 ± 1,65 nm com um índice de polidispersidade (PDI) de 0,134 e potencial zeta de -23,5 ± 0,85 mV. O tamanho de partícula de RD-LNF foi de 138,2 ± 1,28 nm com um PDI de 0,159 e potencial zeta de - 25,4 ± 0,58 mV. O aumento no tamanho geral das partículas foi atribuído principalmente à carga estrutural do ATRA; no entanto, o tamanho final do RD-LNF foi inferior a 150 nm permitindo o acúmulo preferencial de tumores de melanoma maligno devido ao efeito EPR. Além disso, a presença de PEG hidrofílico irá prevenir a agregação de partículas e reduzir sua captação pelo sistema reticuloendotelial (RES) e, assim, melhorar seu desempenho sistêmico no corpo. A carga superficial em torno de - 25 mV confere excelente estabilidade de armazenamento. A morfologia das partículas foi investigada por microscópio eletrônico de transmissão (TEM) (Fig. 2). Como visto, tanto D-LNF quanto RD-LNF são perfeitamente esféricos em tamanho e distribuídos uniformemente na grade de cobre. A diferença de tamanho entre D-LNF e RD-LNF foi consistente com a observação DLS. A falta de resíduos de partículas, pequenas partículas e agregação indica o sucesso do processo de formulação.
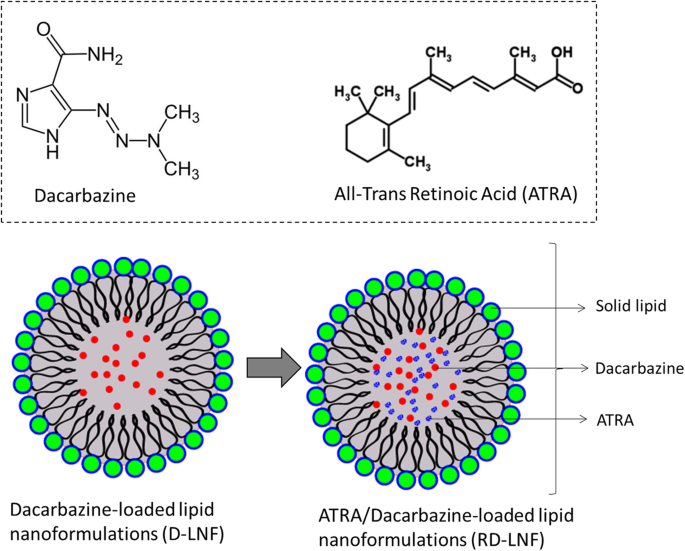
Estrutura da dacarbazina (DBZ) e do ácido all-trans retinóico (ATRA). É apresentada uma ilustração esquemática de nanoformulações lipídicas carregadas com DBZ / ATRA. A nanoformulação lipídica foi preparada pelo método de ultrassonicação. Tanto o DBZ quanto o ATRA são moléculas hidrofóbicas com peso molecular inferior a 300 g / mol. Espera-se que as moléculas hidrofóbicas se concentrem no núcleo das nanopartículas estabilizadas por um surfactante

Análise morfológica de D-LNF e RD-LNF usando microscopia eletrônica de transmissão. É apresentada uma imagem representativa que descreve a morfologia precisa
Análise de estabilidade e liberação de droga in vitro de D-LNF e RD-LNF
O RD-LNF exibiu uma excelente estabilidade em condições de pH 7,4 (PBS) e soro (10% FBS) (Fig. 3a). O tamanho das partículas não apresentou aumento significativo em ambas as condições ao longo do período de estudo, indicando a estabilidade das nanopartículas. A capacidade de liberação do fármaco em tempo hábil decide a eficácia dos sistemas de nanopartículas carregados com o fármaco. Realizamos a cinética de liberação de DBZ e ATRA de D-LNF e RD-LNF em solução salina tamponada com fosfato (PBS, pH 7,4). Como mostrado na Fig. 3b, nenhuma liberação rápida ou liberação em fases de fármaco foi observada a partir de qualquer um dos sistemas de duas nanopartículas, indicando o carregamento estável no núcleo das nanopartículas e não na superfície das nanopartículas. Nenhuma diferença significativa na liberação de DBZ foi observada de D-LNF e RD-LNF, indicando que a presença de ATRA não retardou ou alterou o padrão de liberação do fármaco. Um ligeiro atraso na liberação da droga de DBZ de RD-LNF pode ser atribuído ao aumento do comprimento do caminho atribuído ao ATRA na estrutura lipídica. É interessante notar que a liberação do ATRA foi significativamente mais lenta em comparação com a do DBZ no sistema portador RD-LNF. Diferenças significativas começaram a aparecer após 24 h até 72 h, principalmente atribuídas à natureza hidrofóbica extrema do ATRA e por ser parte do componente estrutural. No geral, a falta de liberação rápida e liberação controlada de componentes terapêuticos irá beneficiar o tratamento do câncer de melanoma.
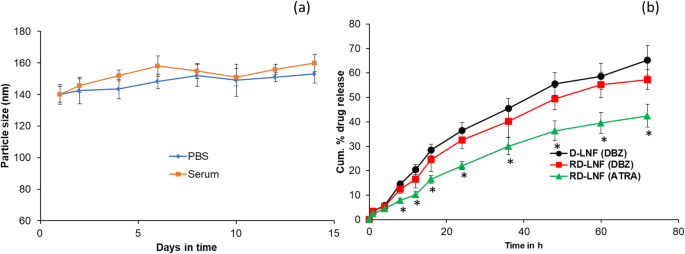
a Análise de estabilidade de RD-LNF em condições de pH 7,4 e soro (10% FBS). b Liberação de droga in vitro de DBZ de D-LNF; e liberação de drogas in vitro de DBZ e ATRA de RD-LNF. O estudo de liberação foi realizado em solução salina tamponada com fosfato (pH 7,4) por um período de estudo de 72 horas. Os resultados são apresentados como média ± desvio padrão ( n =4)
Captação celular in vitro
A absorção celular maior ou aumentada da nanopartícula determina a eficácia terapêutica nas células cancerosas. Realizamos a captação celular de RD-LNF em células cancerosas B16F10 e a Coumarin-6 foi usada como rastreador fluorescente. Como mostrado na Fig. 4, a internalização notável de nanopartículas foi observada após 1 h de incubação das nanopartículas e a captação aumentou consistentemente até 3 h. A notável captação de nanoformulações lipídicas é consistente com a maior captação celular do sistema transportador à base de lipídios. Especulou-se que a difusão passiva e o mecanismo baseado na endocitose poderiam ser responsáveis pela maior captação celular. As nanopartículas após a endocitose chegarão ao lisossoma onde os fármacos encapsulados são liberados e exibem suas respectivas ações farmacológicas.
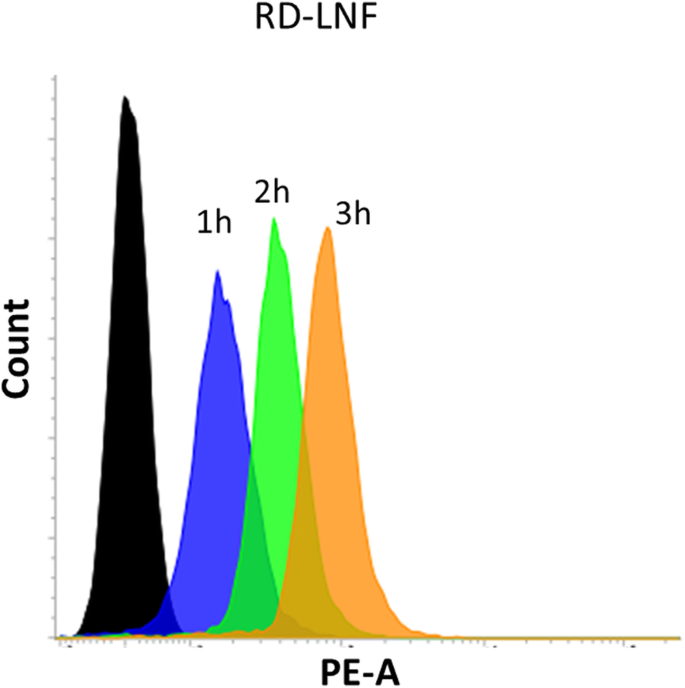
Análise de captação celular in vitro de células de melanoma B16F10. As células cancerosas foram tratadas com RD-LNF e os tempos de incubação variaram de 1h a 3h e a captação celular foi analisada por citômetro de fluxo. O Coumarin-6 foi usado como um rastreador fluorescente
Ensaio de citotoxicidade in vitro
O ensaio de MTT foi realizado em células B16F10 após tratamento com as respectivas formulações para avaliar o efeito anticâncer de agentes terapêuticos individuais (Fig. 5a). No início, a citotoxicidade de DBZ livre individual e ATRA foi avaliada. DBZ exibiu um efeito citotóxico dependente da concentração nas células cancerosas de melanoma, enquanto ATRA exibiu um efeito citotóxico significativamente maior nas células B16F10. A 100 μg / ml, DBZ exibiu uma viabilidade celular de ~ 45% em comparação com a viabilidade celular de ~ 22% para o ATRA, indicando a excelente eficácia terapêutica do ATRA. A fim de provar que a co-entrega de DBZ e ATRA poderia inibir potencialmente a progressão do câncer, nanoformulações lipídicas carregadas com DBZ + ATRA (RD-LNF) foram tratadas com células de melanoma. Nanoformulações lipídicas carregadas com DBZ (D-LNF) contendo o fármaco de entidade única foram utilizadas como grupo de referência para destacar a eficácia sinérgica do ATRA (Fig. 5b). Como esperado, a 25 μg / ml de concentração fixa, o ATRA mostrou viabilidade celular ligeiramente inferior em comparação ao DBZ, enquanto o D-LNF baseado em nanopartículas não melhorou o efeito anticâncer do DBZ e permaneceu longe de ser eficaz. Como esperado, RD-LNF mostrou viabilidade celular significativamente menor e maior efeito anticâncer em comparação com o de D-LNF, indicando um efeito terapêutico sinérgico aparente de componentes duplos para a morte de células cancerígenas de melanoma. RD-LNF mostrou um efeito anticâncer significativamente maior em comparação com qualquer outro grupo de tratamento. Pode-se esperar que a liberação lenta e sustentada de DBZ junto com a liberação lenta de ATRA do sistema nanocarreador possa contribuir para o efeito terapêutico sinérgico. Neste estudo, a dacarbazina (DBZ) foi o principal medicamento quimioterápico e o ATRA foi empregado como um componente estrutural das nanopartículas lipídicas, portanto, não criou um grupo separado para R-LNF. Estudamos o efeito anticâncer do ATRA e DBZ nus nas células cancerosas. Além disso, muitos relatórios publicados são prova do efeito anticâncer do ATRA; portanto, usamos o ATRA como um componente estrutural que também pode melhorar a eficácia anticâncer da terapêutica encapsulada de maneira sinérgica.
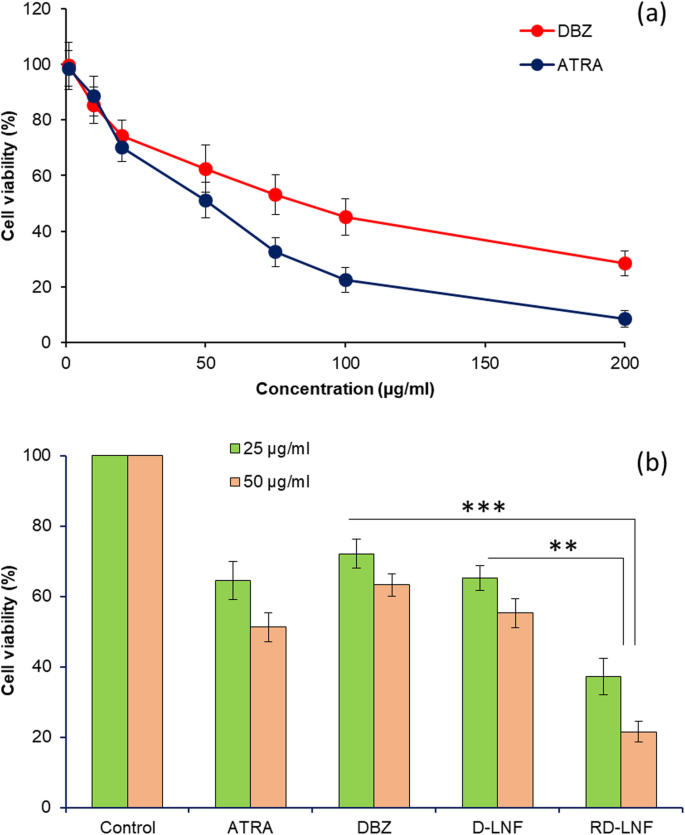
a Ensaio de citotoxicidade in vitro de DBZ livre e ATRA de maneira dependente da concentração. b Citotoxicidade in vitro de ATRA, DBZ, D-LNF e RD-LNF livres a uma concentração fixa de 25 μg / ml e 50 μg / ml
Ensaio de formação de colônia
O ensaio de formação de colônias foi realizado com o objetivo de avaliar o potencial de tumorigênese de células de melanoma. Como mostrado, o DBZ livre e o ATRA têm um papel limitado na inibição da formação de colônias e, da mesma forma, o D-LNF foi ineficaz no controle da formação de colônias (Fig. 6). Como esperado, a combinação de DBZ + ATRA resultou em uma potenciação significativa da inibição da formação de colônias em comparação com os medicamentos livres individuais ou nanopartículas carregadas com um único medicamento. O ensaio de formulação de colônia reitera ainda mais a eficácia anticâncer superior de RD-LNF sobre drogas livres.
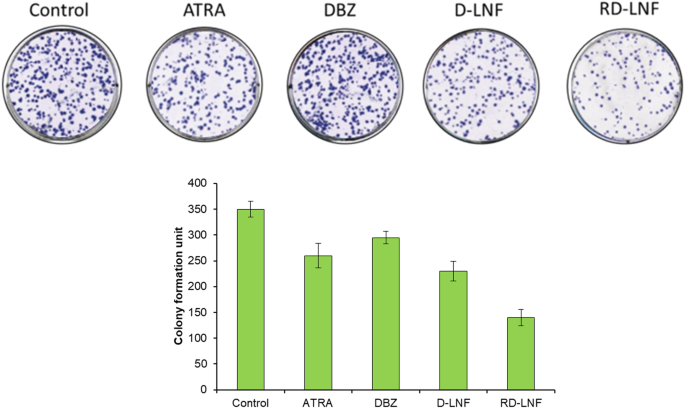
Efeito de ATRA, DBZ, D-LNF e RD-LNF livres na formação de colônias. As células B16F10 foram tratadas com as respectivas formulações e a formação de colônias foi fotografada após a coloração com violeta de cristal
Ensaio de apoptose in vitro e análise do ciclo celular
A indução de apoptose de células B16F10 após tratamento com D-LNF e RD-LNF foi estudada usando um citômetro de fluxo após a coloração das células com a mistura de anexina V-FITC / PI (Fig. 7a). Como mostrado, ATRA e DBZ causaram apenas 10-12% da apoptose das células cancerosas e muitas das células permanecem intactas. Um ligeiro aumento nas células apoptóticas iniciais foi observado após o tratamento com D-LNF pode sugerir o efeito do transportador de entrega. É importante ressaltar que RD-LNF induziu uma proporção maior de células em apoptose com uma proporção maior de células em apoptose tardia e apoptose precoce, indicando a eficácia anticâncer superior de nanopartículas combinacionais. RD-LNF mostrou que as células de apoptose tardia aumentaram 21,5%, enquanto as células de apoptose precoce aumentaram até 18,3% e a proporção de células viáveis diminuiu de 95 para 52%, respectivamente, sugerindo que a combinação de DBZ + ATRA contribuiu para a apoptose de células cancerosas e poderia inibir a inibição proliferativa de células de melanoma B16F10. O efeito de apoptose das formulações foi ainda confirmado por análise do ciclo celular. Como mostrado, DBZ e ATRA exibiram um ligeiro aumento na população sub-G0, enquanto D-LNF mostrou uma população sub-G0 relativamente mais alta em comparação com os medicamentos livres individuais (Fig. 7b). Notavelmente, um aumento notável na população sub-G0 foi observado para células de melanoma tratadas com RD-LNF, indicando a apoptose marcada das células cancerosas. É bem conhecido que DBZ pode aumentar os níveis de expressão de p21, caspase-3 e PARP clivada e, assim, promover a apoptose celular através da estabilização de p53. A indução de p53 irá inibir a progressão do ciclo celular [24, 25]. Espera-se que a combinação de DBZ + ATRA potencialize o mecanismo de apoptose e interrompa a progressão do ciclo celular das células cancerosas e exiba a eficácia anticâncer.
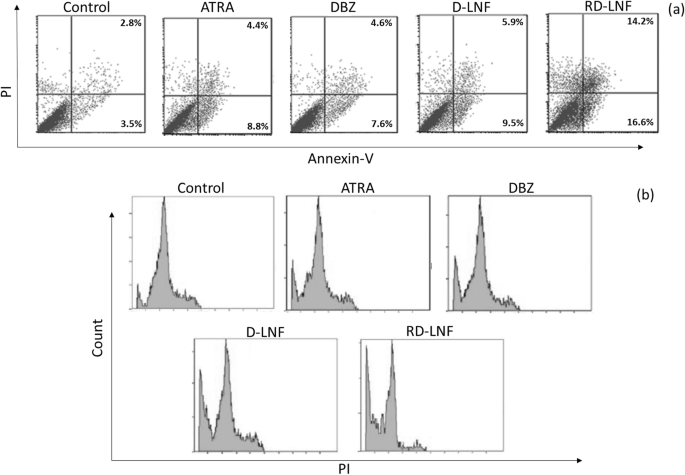
a Ilustração de apoptose de células B16F10 após tratamento com ATRA, DBZ, D-LNF e RD-LNF livres. As células não tratadas foram consideradas como um controle adequado. A apoptose foi analisada por citômetro de fluxo. b Ilustrações da análise do ciclo celular realizada em células B16F10 após o tratamento com as respectivas formulações
Efeito das nanopartículas combinacionais na migração celular
A migração celular foi analisada através da membrana transwell e observada a migração das células por coloração com violeta de cristal (Fig. 8). Após 24h, as células de controle quase alcançaram a migração completa das células cancerosas. O ATRA parece inibir a migração celular relativamente melhor do que as células tratadas com DBZ. D-LNF também mostrou um efeito inibitório notável na migração celular; no entanto, o efeito de migração celular mais notável foi observado em células de melanoma B10F16 tratadas com RD-LNF. Como visto, a variedade diminuída na migração celular foi observada em comparação com as células de controle não tratadas. Estes resultados demonstram claramente que RD-LNF diminui potencialmente a proliferação de células malignas aberrantes e suprime a migração celular de forma eficiente.
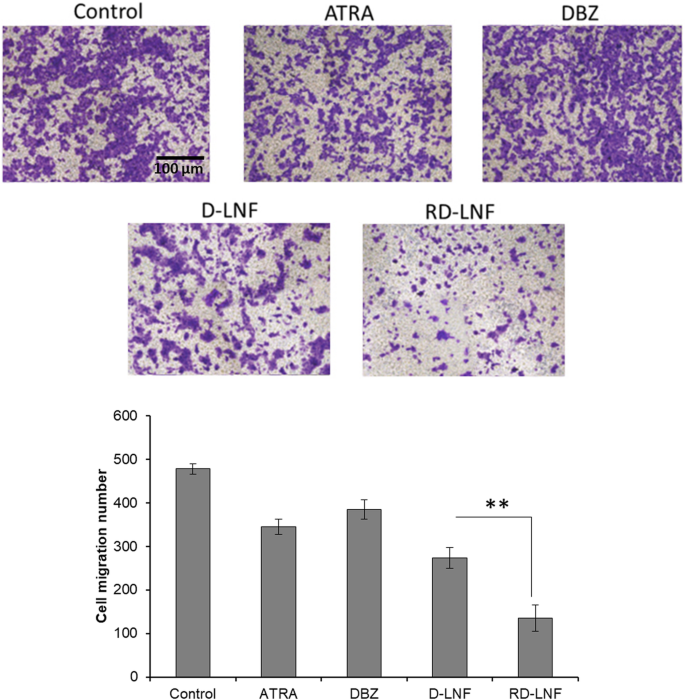
Microfotografias representativas do ensaio de migração celular de células B16F10 após tratamento com ATRA, DBZ, D-LNF e RD-LNF livres e sua quantificação
Disponibilidade de dados e materiais
Não aplicável
Abreviações
- DBZ:
-
Dacarbazina
- ATRA:
-
Ácido trans retinóico
- D-LNF:
-
Nanoformulações lipídicas carregadas com DBZ
- RD-LNF:
-
Nanoformulações lipídicas carregadas com ATRA / DBZ
- SLN:
-
Nanopartículas de lipídios sólidos
Nanomateriais
- 7 dicas e truques do CMMS para usar o Fiix CMMS
- Demonstração de um biossensor flexível à base de grafeno para detecção sensível e rápida de células cancerosas do ovário
- Nanopartículas para terapia do câncer:progresso e desafios atuais
- Eficácia antitumoral aprimorada e farmacocinética de Bufalin via lipossomas PEGuilados
- Biocompatível de ácido 5-aminolevulínico / vesículas etossômicas carregadas com nanopartículas de Au para terapia fotodinâmica / fototérmica sinérgica transdérmica in vitro de cicatrizes hip…
- Comparação entre o ácido fólico e a funcionalização baseada no peptídeo gH625 de nanopartículas magnéticas Fe3O4 para internalização celular aprimorada
- Inibidor de autofagia (LY294002) e 5-fluorouracil (5-FU) Nanolipossoma baseado em combinação para eficácia aprimorada contra carcinoma de células escamosas de esôfago
- Preparação de lipossomas de ácido glicirretínico usando método de solução monofásica de liofilização:pré-formulação, otimização e avaliação in vitro
- 5 dicas para usar escadas e plataformas industriais
- Guia de uso de equipamentos pesados para demolição e desconstrução



