Um eletrocatalisador bifuncional eficiente de MOFs co-dopados com carbono fósforo
Resumo
Ela está ansiosa para desenvolver catalisadores eletroquímicos bifuncionais de alto desempenho e baratos para a reação de redução de oxigênio (ORR) ou reação de evolução de oxigênio (OER) para a crise de energia e problemas ambientais. Aqui, relatamos uma série de materiais poliédricos co-dopados com Co-P-C derivados de ZIF com uma morfologia bem definida. O catalisador otimizado Co / P / MOFs-CNTs-700 exibiu atividades eletroquímicas favoráveis com o mais baixo sobrepotencial de 420 mV para atingir a densidade de corrente de 10 mA cm −2 para OER e a metade do potencial de 0,8 V para ORR em NaOH 0,1 M. O desempenho pode ser bem melhorado com a dopagem do recurso de fósforo que mudou muito sua morfologia. Enquanto isso, os recursos de carbono dopados também melhoram a condutividade, o que o torna um catalisador eletroquímico bifuncional promissor e pode ser comparável aos eletrocatalisadores comerciais.
Introdução
Nos últimos anos, a demanda crescente por desenvolvimento sustentável de energia atraiu grande interesse entre os pesquisadores no campo da conversão de energia eletroquímica e tecnologias de armazenamento de energia [1,2,3]. A fim de atender à demanda por conversão e distribuição de energia, a investigação de um material alternativo de eletrodo de metal não precioso com estrutura bem projetada, químico controlado e excelente desempenho eletroquímico será uma busca constante [4,5,6,7]. A reação de evolução de oxigênio (OER) e a reação de redução de oxigênio (ORR) são as reações importantes que atuam como papéis significativos na aplicação em células solares, células de eletrólise, células recarregáveis de metal-ar, células de combustível e assim por diante [8,9 , 10,11]. No entanto, a cinética maçante de OER e ORR limitou severamente a utilização em larga escala da eficiência de conversão de energia [8, 12,13,14,15].
Portanto, grandes esforços têm sido colocados para explorar um catalisador eletroquímico eficiente e estável para melhorar a reação severa de oxigênio nas últimas décadas. Sabe-se que os catalisadores de metais nobres são a referência da reação do oxigênio. No entanto, esses materiais potenciais sofriam de escassez, alto custo e baixa estabilidade. Por exemplo, o dióxido de irídio e o dióxido de rutênio, os catalisadores OER mais promissores, exibem excelentes atividades eletrocatalíticas OER tanto em condições ácidas quanto alcalinas em baixo potencial excessivo, mas ainda sem estabilidade de longo prazo. O catalisador de carbono de platina comercial como uma espécie de eletrocatalisador de cátodo com a brilhante atividade eletroquímica da ORR ainda é cruzado pelo eletrólito, é fácil de ser envenenado e carece de certa durabilidade. Consequentemente, devido às deficiências dos preciosos catalisadores acima, mais e mais pesquisadores têm se dedicado ao projeto de catalisadores eletroquímicos baseados nos elementos abundantes na terra para o desenvolvimento sustentável. Curiosamente, os materiais de estrutura orgânica metálica (MOFs) têm atraído enormes interesses devido ao seu baixo custo, fontes abundantes e capacidade de servir como modelos para a síntese de materiais nanoporosos à base de carbono. Os MOFs de materiais porosos cristalinos são geralmente fáceis de projetar formando por automontagem de íons metálicos e grupos orgânicos [16, 17]. Os complexos carbono-metal derivados deles podem possuir morfologias diferentes, exibindo áreas superficiais extremamente altas e estruturas de poros hierárquicas que contribuem fortemente para as atividades eletroquímicas de ORR e REA [18, 19]. No entanto, o grau de grafitização desses materiais é relativamente baixo, reduzindo assim a condutividade dos materiais.
Enquanto isso, os nanomateriais de carbono, devido à sua alta condutividade e morfologia controlável, são extremamente atraentes e têm sido aplicados em muitos dispositivos eletroquímicos, como a célula a combustível de polímero [2, 20]. Além disso, foi comprovado que nanomateriais de carbono dopados com elementos heterogêneos podem aumentar muito a atividade catalítica e a área química de superfície [4, 13, 20,21,22,23,24,25,26]. Os materiais de carbono heterodopados também têm efeito sinérgico na catálise direta de ORR [27, 28]. Portanto, a fim de aumentar a condutividade e a atividade catalítica dos materiais, é razoável sintetizar materiais dopados com átomos heterogêneos eficientes a partir de MOFs de materiais ricos em fontes de baixo custo, que podem ser bem aplicados em células de combustível, baterias de metal-ar e assim sobre.
Portanto, relatamos um catalisador eletroquímico bifuncional eficiente da estrutura orgânica de metal com fósforo e carbono co-dopados por um método de dopagem in situ. Descobrimos que o átomo heterogêneo de dopagem pode alterar sua morfologia e melhorar a condutividade comprovada por SEM e XPS, o que o fez processar um overpotential favoravelmente baixo de 420 mV para atingir a densidade de corrente de 10 mA cm −2 para OER e a metade do potencial de 0,8 V para ORR em NaOH 0,1 M. Este promissor catalisador eletroquímico bifuncional pode ser comparável aos eletrocatalisadores comerciais.
Métodos
Síntese de Nanomateriais de Carbono Co-MOF
A fim de sintetizar os nanomateriais de carbono Co-MOF, um método típico e simples foi realizado como segue. Em primeiro lugar, 1,28 g de 2-metilimidazol foi ultrassonicamente disperso em 20 mL de metanol para formar a solução A. 1,0 g de acetilacetonato de cobalto (II) foi ultrassonicamente disperso em 60 mL de metanol para formar a solução B. A solução A foi lentamente adicionada à solução B com ultrassom contínuo por 5 min, seguido por agitação vigorosa por mais 10 min em temperatura ambiente. Em seguida, a mistura foi selada no reator de politrafluoroetileno, que foi transferido para a estufa de secagem ao ar e aquecida da temperatura ambiente até 160 ° C e mantida a 160 ° C por 24 h, seguido por resfriamento natural até a temperatura ambiente. O pó sólido púrpura obtido foi centrifugado e lavado com metanol várias vezes e seco a 70 ° C durante a noite. Os nanocristais preparados foram pirolisados sob uma atmosfera de argônio em um tubo de quartzo de fluxo colocado no centro de um forno tubular como segue. Em primeiro lugar, a produção foi aquecida desde a temperatura ambiente até 350 ° C a uma taxa de 5 ° C / min e mantida a 350 ° C durante 1 h. Em seguida, aumentamos até a temperatura desejada (500, 600, 700, 800 e 900 ° C) por 2 h com a mesma taxa de aquecimento para obter Co-MOFs-x, onde “x” representa a temperatura de carbonização.
Síntese de nanomateriais de carbono Co / P-MOF
Para avaliar o impacto da dopagem P nas atividades eletroquímicas, diferentes fontes de fosfina foram adotadas durante a síntese. 1,28 g de 2-metilimidazol foi disperso ultrassonicamente em 20 mL de metanol para formar a solução A. 1,0 g de cobalto (II) acetilacetonato e 0,25 g de fonte de fósforo foram dispersos ultrassonicamente em 60 mL de metanol para formar a solução B. As fontes de fósforo foram hipofosfito de sódio, trifenilfosfina, e O -trimetilfenilfosfina. As etapas a seguir foram iguais às anteriores; mudamos apenas a temperatura de carbonização mais adequada para 700 ° C. Por fim, obtivemos as produções denominadas Co / P0-MOFs, CoP1-MOFs e Co / P2-MOFs, onde P0, P1 e P2 representam hipofosfito de sódio, trifenilfosfina e O -trimetilfenilfosfina, respectivamente.
Escolhemos a trifenilfosfina como fonte de fósforo e alteramos a massa da fonte de fósforo na etapa 1 para 0,5, 0,75 e 1,0 g, respectivamente. E as outras etapas experimentais permaneceram inalteradas. O produto final foi denominado Co / P / MOFs-700-0.25, Co / P / MOFs-700-0.5, Co / P / MOFs-700-0,75 e Co / P / MOFs-700-1.0, respectivamente.
Síntese de nanomateriais de carbono Co-MOFs-C
A fim de melhorar a condutividade do material, fontes adicionais de carbono foram adicionadas. 1,28 g de 2-metilimidazol foi ultrassonicamente disperso em 20 mL de metanol para formar a solução A. 1,0 g de cobalto (II) acetilacetonato e 0,125 g de fontes de carbono foram ultrassonicamente dispersos em 60 mL de metanol para formar a solução B. As fontes de carbono foram nanotubos de carbono (CNTs) , negro de acetileno (CB) e A-OMCS que foram preparados em nosso artigo formal [25] que foram tratados com ácido. As etapas a seguir foram iguais às da etapa 2.2 (1). Por fim, obtivemos as produções denominadas Co / MOFs-CNTs-700, Co / MOFs-CB-700 e Co / MOFs-A-OMCS-700, respectivamente.
Síntese de nanomateriais de carbono Co / P-MOFs-CNTs-700
A fim de melhorar a condutividade e o desempenho eletrocatalítico, fontes de carbono e materiais de carbono foram usados simultaneamente. 1,28 g de 2-metilimidazol foi ultrassonicamente disperso em 20 mL de metanol para formar a solução A. 1,0 g de cobalto (II) acetilacetonato, 0,25 g de trifenilfosfina e 0,125 g de CNTs com ácido tratado foram ultrassonicamente dispersos em 60 mL de metanol para formar a solução B. as etapas foram iguais às anteriores. Por fim, obtivemos as produções denominadas Co / P / MOFs-CNTs-700.
Caracterização dos nanomateriais de carbono sintetizado
A difração de raios X (XRD) foi realizada no difratômetro TD-3500 (Tongda, China). A espectroscopia de fotoelétrons de raios X (XPS) foi realizada usando um espectrômetro de fotoelétrons K-Alpha + (Thermo Fisher Scientific). Imagens de microscopia eletrônica de varredura (SEM) foram obtidas com um microscópio eletrônico de varredura SU8220 (Hitachi, Japão). Imagens de campo escuro anular de alto ângulo (HAADF) e análise de mapeamento elementar de espectrômetro de dispersão de energia (EDS) foram realizadas no modo de microscopia eletrônica de transmissão de varredura (STEM) em uma transmissão de emissão de campo FEI Tecnai f20 com correção de aberração; o microscópio eletrônico operou a 200 kV.
Testes eletroquímicos
Todos os dados de atividade eletroquímica foram coletados em uma estação de trabalho eletroquímica (Ivium, Holanda) em temperatura ambiente, acoplada a um sistema de eletrodo de disco rotativo (RDE) (Pine, EUA) em um sistema padrão de três eletrodos. O sistema de três eletrodos consistia em um contra-eletrodo de fio de Pt, um eletrodo de referência de Hg / HgO (solução de NaOH 0,1 M) para o meio alcalino e um eletrodo de trabalho à base de carbono vítreo (GC, 0,196 cm 2 ) Os eletrodos carregados com catalisador foram obtidos como segue. Em primeiro lugar, uma tinta de catalisador foi preparada por ultra-som de uma mistura de 1 mL de solução de etanol Nafion 0,25% em peso e 5 mg do catalisador correspondente por 30 min. Em seguida, 20 μL de tinta de catalisador foram espalhados em um eletrodo de trabalho à base de carbono vítreo nos testes RDE. Finalmente, o eletrodo de trabalho foi seco sob uma lâmpada infravermelha por 1–2 min. A carga do catalisador foi de aproximadamente 0,5 mg cm −2 . Uma solução de NaOH 0,1 M foi empregada como eletrólito e foi purgada com N 2 de alta pureza ou O 2 gás por cerca de 30 min antes do teste. Os testes de voltametria de varredura linear (LSV) foram realizados a uma taxa de rotação de 1600 rpm e uma taxa de varredura potencial de 10 mV s −1 . O teste de estabilidade foi realizado na estação de trabalho Autolab Electrochemical Instrumentation (Metrohm) em um sistema padrão de três eletrodos, no qual o OER foi por teste de cronopotenciometria conduzido sob densidade de corrente constante de 10 mA cm −2 em NaOH 0,1 M com uma carga de 0,2 mg cm −2 e a ORR foi pelo teste de resposta cronoamperométrica realizado sob potencial constante de 0,8 V na mesma condição. Todos os potenciais são calibrados com relação ao eletrodo de hidrogênio reversível (RHE).
Resultados e discussão
Conforme mostrado na Fig. 1a, a difração de raios-X (XRD) revelou que sintetizamos com sucesso poliedros de materiais de estrutura orgânica de metal de transição. Ao aumentar as temperaturas de carbonização, os picos de difração em 44,216 °, 51,522 ° e 75,853 ° tornam-se mais distintos, o que combina bem com os planos (111), (200) e (220) do cobalto cúbico (PDF # 15- 0806). Como é do conhecimento de todos, a temperatura de recozimento tem um efeito significativo no desempenho físico-químico e eletroquímico das amostras [29, 30]. Assim, nas amostras obtidas com uma série de gradiente de temperatura foram realizadas medições eletroquímicas para examinar a temperatura otimizada. A Figura 1b mostra as atividades eletroquímicas dos materiais tratados em diferentes temperaturas. É óbvio descobrir que o catalisador como preparado carbonizado a 700 ° C (Co / MOFs-700) exibe o melhor desempenho OER. O superpotencial é de cerca de 480 mV para atingir a densidade de corrente de 10 mA cm −2 em NaOH 0,1 M.
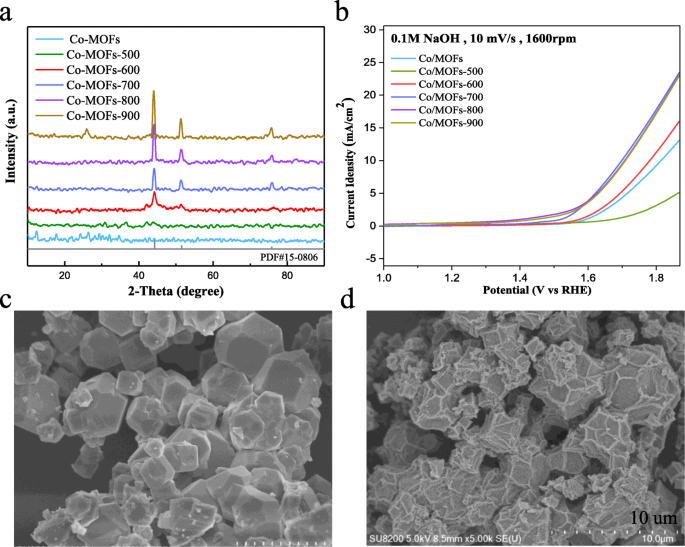
a Padrões de XRD de amostras Co / MOF antes de carbonizados e carbonizados em diferentes temperaturas. b Curvas LSV para o OER de Co / MOFs, Co / MOFs-500, Co / MOFs-600, Co / MOFs-700, Co / MOFs-800 e Co / MOFs-900. c , d Imagens SEM da amostra Co / MOFs-700 antes e depois da carbonização
Em seguida, os Co / MOFs antes da carbonização e os Co / MOFs-700 de melhor desempenho foram escolhidos para realizar as medições de MEV. Como mostrado na Fig. 1c, d, a morfologia do Co / MOFs-700 obtido mudou muito após carbonização a 700 ° C. Muitas linhas dobradas aparecem em sua superfície e não são mais suaves do que os materiais originais, sem serem carbonizadas. Mas ainda processa a morfologia do poliedro, com dispersão de partículas regular e nenhum sinal de colapso.
Como artigos anteriores relatados, a dopagem do fósforo em poliedro de estrutura orgânica de metal de transição pode aumentar a estabilidade da amostra em solução ácida ou alcalina e também pode melhorar efetivamente a atividade catalítica eletroquímica quebrando a eletroneutralidade e facilitando o O 2 adsorção [31,32,33]. Portanto, amostras dopadas com fósforo são sintetizadas com o método de dopagem in situ e investigadas o desempenho eletroquímico. Os produtos obtidos foram nomeados como Co / P0 / MOFs-700, Co / P1 / MOFs-700 e Co / P2 / MOFs-700, enquanto P0, P1 e P2 representam as fontes de fósforo do hipofosfito de sódio, trifenilfosfina e O -trimetilfenilfosfina, respectivamente.
De acordo com a Fig. 2a, os picos de difração das amostras dopadas com fósforo ainda possuem o padrão de cobalto cúbico (PDF # 15-0806), indicando que a dopagem de pequena quantidade de fósforo não alteraria a estrutura dos MOFs. Em seguida, as medidas eletroquímicas foram conduzidas para explorar a influência de diferentes fontes de fósforo nas atividades catalíticas eletroquímicas. Conforme mostrado na Fig. 2c, o potencial aberto (0,87 V) e o potencial de meia onda (0,78 V) mostram que o Co / P1 / MOFs-700 possui a melhor atividade de ORR. No entanto, é ligeiramente mais fraco do que o produto original Co / MOFs-700 carbonizado sob a mesma temperatura. A Figura 2d representa o desempenho OER de diferentes produtos dopados com fósforo. Quando a densidade de corrente limitada é 10 mA cm −2 , apenas Co / P1 / MOFs-700 possui o menor sobrepotencial de 430 mV, demonstrando que a incorporação de fósforo nas amostras pode aumentar a atividade de REA, o que é coincidência com o artigo relatado de que a incorporação de fósforo ajustaria a condutividade elétrica e, entretanto, facilitaria a rápida transferência de elétrons [34]. Além disso, a Fig. 2b mostra uma comparação entre a amostra com trifenilfosfina como fonte de fósforo e a amostra original (Fig. 1c) sem incorporação de elementos. Pode ser revelado que a incorporação de fósforo afetou fortemente a morfologia do material em comparação com Co / MOFs-700. Portanto, o dopagem de fósforo pode não apenas aumentar a atividade eletroquímica, mas também alterar a morfologia da amostra.
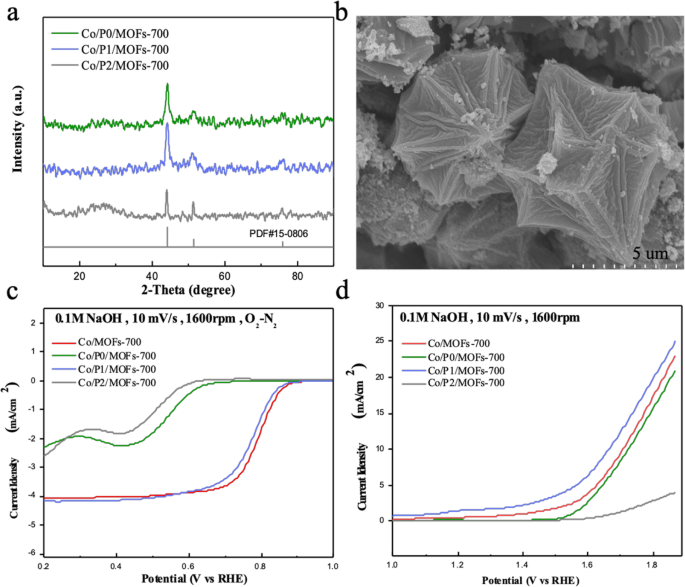
a Padrão de XRD de Co / P0 / MOFs-700, Co / P1 / MOFs-700 e Co / P2 / MOFs-700. b Imagens SEM de Co / P1 / MOFs-700. c Curvas de polarização ORR das amostras dopadas com fósforo. d Curvas de polarização OER de amostras dopadas com fósforo
Posteriormente, a fim de descobrir a razão pela qual o dopagem de fósforo pode aumentar a atividade eletroquímica, a análise XPS foi realizada para sondar a composição e o estado químico das amostras Co / MOFs-700 e Co / P1 / MOFs-700. De acordo com a Fig. 3a, a pesquisa de espectros de XPS de Co / MOFs-700 e Co / P1 / MOFs-700 mostra a presença de Co 2p, O 1s, N 1s e C 1s. É de notar que o pico de P 2p aparece na pesquisa de espectros XPS em Co / P1 / MOFs-700, mas mostra um sinal bastante fraco em comparação com picos fortes de C 1s. Além disso, a Fig. 3b mostra os espectros de Co 2p de Co / MOFs-700 e Co / P1 / MOFs-700. Verificou-se que o Co 2p 3/2 pode ser encaixado em dois picos. Os picos localizados em 778,2 ° e 780,7 ° podem ser atribuídos ao Co (0) e Co (2 + ), enquanto Co 2p 1/2 também pode ser exibido em dois picos posicionados em 793,3 ° e 796,7 °, que podem ser atribuídos ao Co (0) e Co (2 + ) Os picos do satélite foram posicionados em 786,2 ° e 802,7 ° [35,36,37]. Quando comparado com a amostra dopada com fósforo Co / P1 / MOFs-700, podemos descobrir que o Co (0) aumentou muito enquanto o Co (2 + ) diminuiu, indicando que a dopagem da fonte de fósforo durante o processo de síntese pode aumentar o teor de Co (0) nas amostras obtidas. Como é do conhecimento de todos nós, o Co (0) pode aumentar muito a condutividade, melhorando assim o desempenho eletroquímico, o que também está de acordo com o relatório anterior [38].
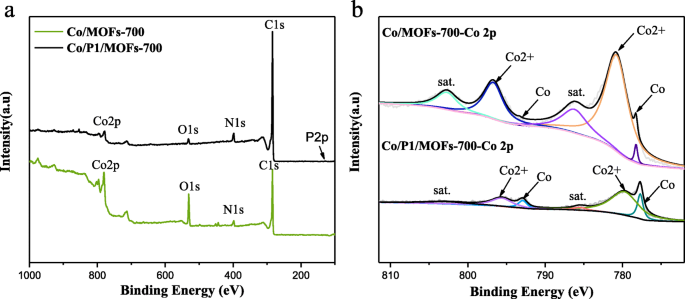
a Levantamento de espectros XPS de Co / MOFs-700 e Co / P1 / MOFs-700. b Espectros Co 2p de Co / MOFs-700 e Co / P1 / MOFs-700
Posteriormente, continuamos investigando a influência na qualidade da fonte de fósforo dopada. Os produtos obtidos com uma razão molar diferente de P foram nomeados como Co / P / MOFs-700-x ( x =0,25, 0,5, 0,75, 1,0), enquanto P representa trifenilfosfina ex representa a qualidade da fonte de fósforo. A Figura 4a mostra que ao aumentar o conteúdo de fontes de fósforo, o padrão de XRD mostra que os principais picos de difração nessas amostras ainda são cobalto (PDF # 15-0806). Como mostra a Fig. 4b, Co / P / MOFs-700-0.5 possui a melhor atividade ORR cujo potencial de meia onda foi em torno de 0,8 V entre esses produtos dopados com fósforo, mas a atividade ORR de Co / P / MOFs-700-0.5 é não aumentou significativamente em comparação com a amostra original Co / MOFs-700. Pode ser visto na Fig. 4c que a atividade OER das amostras aumentou significativamente com a adição de compostos de trifenilfosfina e diminuiu com o aumento da massa da fonte de fósforo. Quando a densidade de corrente limitada é 10 mA cm −2 , Co / P / MOFs-700-0.25 e Co / P / MOFs-700-0.5 possuem o sobrepotencial mínimo de 450 mV, indicando que apenas uma quantidade adequada de fontes de fósforo pode melhorar a atividade de OER, enquanto a quantidade de 0,25 e 0,5 apresenta a melhor . No entanto, quando comparado com o carbono de platina comercial (potencial de meia onda 0,81 V, densidade de corrente limitada 5,43 mA cm −2 ) e excelente óxido de irídio eletrocatalisador OER (1,61 V @ 10 mA cm −2 ), Co / P / MOFs-700-0.5 ainda permanece uma diferença significativa entre a densidade de corrente limitada no desempenho de ORR. Conforme relatado no artigo, quando a condutividade do material é pequena, o mesmo ocorre com a densidade de corrente limitada [39].
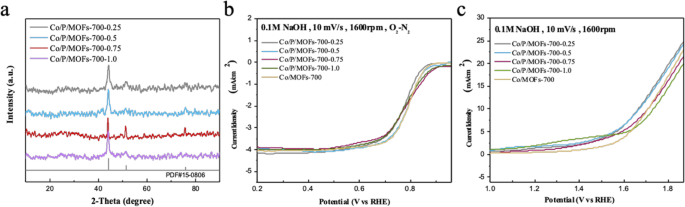
a Padrões de XRD de dopagem de diferentes conteúdos de fontes de fósforo em Co-MOFs. b , c Curvas de polarização ORR e OER de Co / MOFs-700, Co / P / MOFs-700-0.25, Co / P / MOFs-700-0.5, Co / P / MOFs-700-0,75 e Co / P / MOFs-700 -1,0, respectivamente
A fim de aumentar a condutividade, primeiro medimos o conteúdo de carbono atual do Co / P / MOFs-700-0.5 sintetizado e analisado por imagens EDS. De acordo com a Fig. 5, é óbvio que a qualidade do cobalto é responsável pela maior parte, o que leva quase 52,38%, enquanto a qualidade do carbono é relativamente inferior a 29,13%.
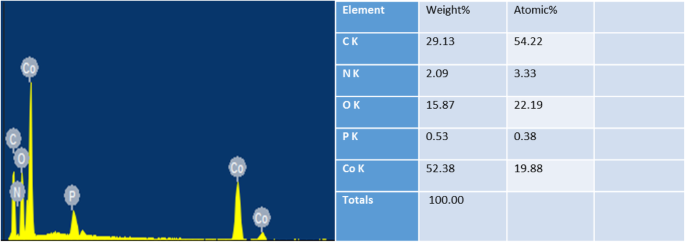
EDS de Co / P / MOFs-700-0.5
Portanto, a fim de melhorar a condutividade do material, dopamos ainda mais as amostras com carbono sem qualquer fonte de fósforo. Os produtos obtidos foram denominados Co / MOFs-CNTs-700, Co / MOFs-CB-700 e Co / MOFs-A-OMCS-700, respectivamente. A Figura 6a mostra que o carbono dopado não afetará a estrutura das amostras, que ainda mantém os mesmos picos de difração do cobalto (PDF # 15-0806). Como mostrado na Fig. 6b, pode ser visto que a densidade de corrente limitada dos produtos é muito aumentada com a incorporação da fonte de carbono na ORR, enquanto a Fig. 6c indica que a incorporação da fonte de carbono não faz sentido para melhorar as propriedades de REA dos catalisadores.
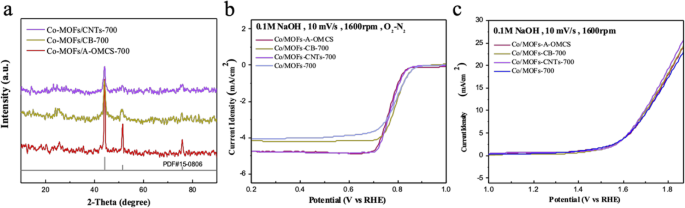
a Padrões de XRD de dopagem de diferentes conteúdos de fonte de carbono em Co-MOFs. b , c Curvas de polarização ORR e OER de Co / MOFs-700, Co / MOFs-CNTs-700, Co / MOFs-A-OMCS-700 e Co / MOFs-CB-700, respectivamente
Combinado com os dados e conclusões experimentais anteriores, dopamos a amostra original com fósforo e elementos de carbono, adicionando 0,5 g de trifenilfosfina e uma quantidade adequada de diferentes fontes de carbono (CNTs, CB e A-OMCS) ao material para comparação. As amostras obtidas foram denominadas Co / P / MOFs-CNTs-700, Co / P / MOFs-CB-700 e Co / P / MOFs-A-OMCS-700, respectivamente. De acordo com a Fig. 7a, não há mudança no padrão de XRD, com todas as amostras combinando bem com cobalto cúbico (PDF # 15-0806). Conforme mostrado na Fig. 7b, a co-dopagem com fósforo e carbono aumentou muito a densidade de corrente limitada e o desempenho de ORR dos produtos. A amostra de Co / P / MOFs-CNTs-700 exibe a melhor atividade ORR, em que o potencial de meia onda e a densidade de corrente limite são 0,8 V e 4,81 mA cm −2 e são 10 mV mais baixos do que o carbono de platina comercial. Além disso, como pode ser visto claramente na Fig. 7c, o desempenho OER dos produtos também foi muito melhorado. A amostra de Co / P / MOFs-CNTs-700 exibe a tensão de sobrepotencial mais baixa de 420 mV (Tabela 1). Comparado com a voltagem correspondente ao dióxido de irídio, Co / P / MOFs-CNTs-700 é apenas cerca de 40 mV maior do que o dióxido de irídio. Portanto, Co / P / MOFs-CNTs-700 mostra ser um eletrocatalisador bifuncional favorável.
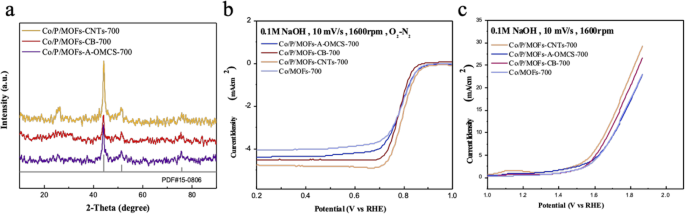
a Padrões de XRD de Co / P / MOFs-CNTs-700, Co / P / MOFs-A-OMCS-700 e Co / P / MOFs-CB-700. b , c Curvas ORR e OER LSV para as amostras acima, respectivamente
Nesse ínterim, para avaliar a estabilidade do Co / P / MOFs-CNTs-700 melhor realizado, foram realizados testes de cronopotenciometria e de resposta cronoamperométrica. Como pode ser visto na Fig. 8a, b, o overpotential apenas aumentou 1,5 mV e o desempenho ORR é reduzido em 79,5% após 18 h de testes contínuos, provando que as atividades OER e ORR de Co / P / MOFs-CNTs-700 são bastante estável em NaOH 0,1 M.
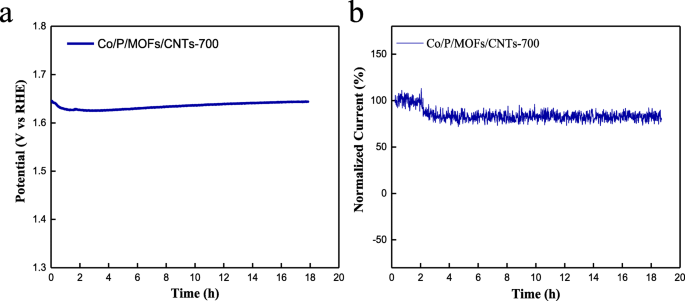
a Medição de cronopotenciometria para Co / P / MOFs-CNTs-700. b Resposta cronoamperométrica de Co / P / MOFs-CNTs-700
Microscopia eletrônica de varredura, EDS e mapeamento na amostra de Co / P / MOFs-CNTs-700 também foram realizados. Como pode ser visto na Fig. 9a-c, Co / P / MOFs-CNTs-700 reteve a morfologia do poliedro com muitas linhas semelhantes a dobras na superfície. Além disso, a incorporação de nanotubos de carbono está embutida no esqueleto do produto, o que pode aumentar a área superficial específica do produto e fornecer mais sítios de adsorção para a reação eletroquímica. A Figura 9 d – g são as análises de mapeamento da amostra. Pode-se observar que as fontes de carbono e fósforo estão uniformemente dispersas no esqueleto da amostra e tornam-se íntegras.

Imagens SEM de Co / P / MOFs-CNTs-700 ( a - c ) e o mapeamento elementar correspondente de Co ( d ), P ( e ), C ( f ) e N ( g ), respectivamente
Como mostra o EDS, o conteúdo de fósforo e carbono do material é aumentado em comparação com a amostra original de Co / MOFs-700 por dopagem in situ, levando assim ao aumento da ORR e da atividade OER (Fig. 10). É demonstrado lateralmente que a incorporação de dois tipos de elementos de fósforo e carbono pode ser benéfica para aumentar a atividade eletroquímica de materiais de estrutura orgânica de metal contendo cobalto [40], porque a eletronegatividade de P (2.19) é diferente daquela dos átomos de carbono ( C, 2,55). O co-doping quebraria a eletroneutralidade, o que pode facilitar o O 2 adsorção e melhorar a atividade ORR [41]. Enquanto isso, mais sítios ativos podem surgir devido à co-dopagem de fósforo e carbono, alterando a densidade de spin assimétrica dos heteroátomos e enfraquecendo efetivamente a ligação O-O, levando assim ao aumento da atividade ORR [42].
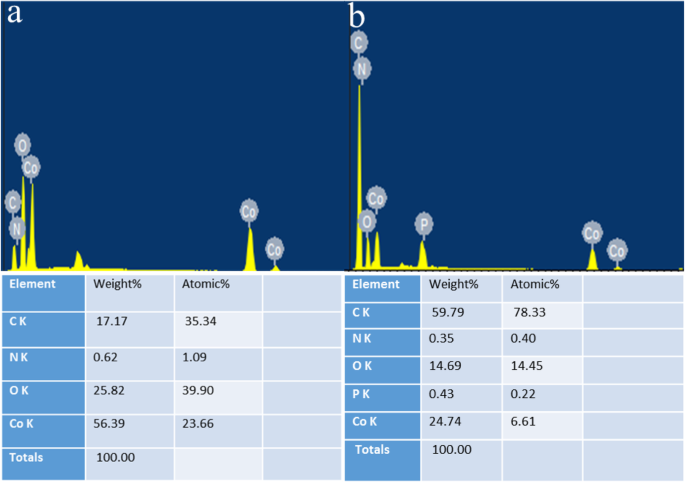
a , b Análise de EDS de Co / MOFs-700 e Co / P / MOFs-CNTs-700, respectivamente
As atividades eletroquímicas pendentes podem ser atribuídas aos seguintes motivos. Em primeiro lugar, heteroátomos de dopagem levariam à redistribuição da densidade de carga na superfície do catalisador, o que é benéfico para adsorver oxigênio e promover as atividades de ORR [43]. Em segundo lugar, a co-dopagem de átomos diferentes nos MOFs resultaria no efeito sinérgico que também contribui para o desempenho eletroquímico aprimorado [44]. Em terceiro lugar, foi provado que o mecanismo OER do catalisador à base de Co é um processo de auto-reconstrução de superfície dinâmica. Os átomos de Co na superfície podem formar uma camada ativa de oxi (hidróxido) de metal auto-montada de CoOOH, que funciona como um sítio ativo real [45]. Além da composição, a estrutura híbrida única combinada com sua alta condutividade pode fornecer uma grande área de superfície para a transferência rápida de carga.
Conclusão
Em conclusão, um nanomaterial de carbono de estrutura orgânica de metal de transição poliedro eficiente e econômico (Co / P / MOFs-CNTs-700) co-dopado com fontes de fósforo e carbono foi sintetizado com sucesso, o que pode servir como um eletroquímico bifuncional eficiente e barato catalisador. O menor superpotencial de Co / P / MOFs-CNTs-700 é 420 mV para atingir a densidade de corrente de 10 mA cm −2 para OER, e a metade do potencial é 0,8 V para ORR em NaOH 0,1 M, que é muito próximo ao dos catalisadores eletroquímicos comerciais. Ele poderia ser utilizado como um eletrocatalisador bifuncional eletroquímico promissor no campo de armazenamento de energia e também fornecer uma visão promissora para projetar um eletrocatalisador bifuncional eletroquímico.
Disponibilidade de dados e materiais
Os dados usados para apoiar as conclusões deste estudo estão incluídos no artigo.
Abreviações
- ORR:
-
Reação de redução de oxigênio
- REA:
-
Reação de evolução de oxigênio
- SEM:
-
Microscopia eletrônica de varredura
- HAADF:
-
Campo escuro anular de alto ângulo
- EDS:
-
Espectrômetro de dispersão de energia
- STEM:
-
Microscopia eletrônica de transmissão de varredura
- XPS:
-
espectroscopia de fotoelétrons de raios-X
- XRD:
-
Difração de raios X
- RDE:
-
Eletrodo de disco rotativo
- Co-MOFs-x:
-
Estruturas orgânicas de cobalto-metal-x representa a temperatura
- Co / P-MOFs:
-
Estruturas orgânicas de cobalto / fósforo-metal
- Co / P / MOFs-700-0.25:
-
Cobalto / fósforo-estruturas orgânicas de metal-700 ° C-a massa da fonte de fósforo é 0,25
- Co-MOFs-C:
-
Estruturas orgânicas de metal cobalto-carbono
- Co / P-MOFs-CNTs-700:
-
Cobalto / fósforo-estruturas orgânicas de metal-nanotubos de carbono-700 ° C
- GC:
-
Carbono vítreo
- LSV:
-
Voltametria de varredura linear
- RHE:
-
Eletrodo de hidrogênio reversível
- Pt / C:
-
Catalisador de platina / carbono
Nanomateriais
- O papel da fibra de carbono nos materiais aeroespaciais
- Fabricação de materiais compostos:Por que a fibra de carbono é a melhor
- Materiais:Vidro e PP reforçado com fibra de carbono para automotivo
- Revelando a estrutura atômica e eletrônica das nanofibras de carbono de copo empilhado
- S, N Co-dopado de grafeno Quantum Dot / TiO2 Compósitos para geração eficiente de hidrogênio fotocatalítico
- Síntese de pontos quânticos de carbono co-dopados com N, S ricos em piridínicos como imitações de enzimas eficazes
- Exploração de Zr – Metal – Estrutura Orgânica como Fotocatalisador Eficiente para Produção de Hidrogênio
- Projetando Materiais Nanotubos de Carbono Simples e Compostos por Caracterização Porosimétrica
- Na4Mn9O18 / Composto de Nanotubo de Carbono como um Material de Alto Desempenho Eletroquímico para Baterias Aquosas de Íons de Sódio
- Estudo comparativo das propriedades eletroquímicas, biomédicas e térmicas de nanomateriais naturais e sintéticos



