Influência da Água na Estrutura e Propriedades Dielétricas da Microcristalina e Nano-Celulose
Resumo
A influência da água nos diferentes estados sobre a estrutura e as propriedades dielétricas da celulose microcristalina foram estudadas por meio de raios-X, termogravimetria e espectroscopia dielétrica. Em pesquisas de celulose microcristalina (MCC) com diferentes teores de água, foi mostrado que as moléculas de água estão localizadas nos macroporos do MCC e em camadas multimoleculares hidratadas. Mostra-se que com o aumento da concentração de água em uma casca hidratada ocorre a reorganização das moléculas de celulose na superfície dos cristalitos, e como resultado, seu tamanho transversal e cristalinidade aumentam. Mostra-se que durante a concentração de água surge mais de 13% em uma concha hidratada contínua de cristalitos. Dependências de temperatura de partes reais e imaginárias de permissividade dielétrica complexa foram estudadas no intervalo de temperaturas [-180 ÷ 120] ° C em frequências de f =5, 10, 20 e 50 kHz. Um processo de relaxamento de baixa temperatura e transição de alta temperatura foram observados. Processo de relaxamento de baixa temperatura que está relacionado à transição de grupos metilol de superfície de moléculas de conformação de celulose de tg para tt é desviada para baixas temperaturas com o aumento da concentração de água na celulose microcristalina.
Histórico
A celulose usual de várias fontes vegetativas, que é um recurso ecologicamente limpo renovável praticamente inesgotável, é matéria-prima para a produção de celulose microcristalina (MCC). Determina o crescente interesse pela investigação de suas propriedades físicas e físico-químicas. Outro fator importante, que chama a atenção dos pesquisadores, é a disponibilidade das partículas cristalinas na estrutura do MCC, cujo estudo de propriedades é promissor para várias direções de desenvolvimento de tecnologias modernas. Os mais desenvolvidos a partir de tais direções são a indústria farmacêutica e cosmética [1]; entretanto, atualmente, o MCC começa a ser usado como enchimento em materiais compostos [2], eletrônica moderna [3] e óptica de laser [4, 5]. Nesse sentido, é importante a capacidade do MCC de absorver umidade, que pode afetar substancialmente suas propriedades, em particular estruturais [6], elétricas [7,8] e termofísicas [9,10].
Métodos
As Amostras
As amostras de grau MCC (Cellets-100), produzidas pela Shin-Etsu Company (Japão), foram utilizadas para investigação. O MCC inicial foi disperso em um almofariz de ágata. Para a obtenção das amostras isentas de água, as amostras foram mantidas na caixa de secagem durante 3 dias à temperatura de 115 ° C e, a seguir, foram encapsuladas no molde de prensa a vácuo. As amostras com diferentes níveis de umidade foram obtidas por sua retenção em diferentes tempos sob vapor de água saturado.
Equipamento
A análise da estrutura da amostra foi realizada usando difratômetro de raios-X DRON-3M com o tubo BSV-28 ( λ =1,54178 Å).
A análise térmica diferencial (DTA) e as investigações termogravimétricas foram realizadas usando o derivatógrafo Q-1500D. As investigações foram realizadas dentro da faixa de temperatura T =20 ÷ 250 ° com a taxa de 5 ° C / min.
As amostras para investigações dielétricas foram produzidas pela compactação do pó de MCC entre revestimentos de um aço inoxidável na pressão de 120 kg / cm 2 . Em seguida, a amostra com os revestimentos laminados foi colocada na célula termoestabilizada de quatro eletrodos, o que permitiu controlar a espessura da amostra durante as medições usando um capacitor dielétrico a ar adicional. Medições da capacidade e fator de perda desta célula em quatro frequências diferentes f =5, 10, 20, 50 kHz dentro da faixa de temperatura (-180 ÷ 120) ° C foram realizadas usando instalação automatizada baseada na ponte de corrente alternada P5083 [11].
Resultados e discussão
Investigações termogravimétricas
As investigações da quantidade de água no MCC foram realizadas usando o derivatógrafo Q-1500D. Na amostra investigada, a temperatura ( T ), mudança de massa ( m ), e taxa de mudança de massa ( dm / dT ) foram medidos simultaneamente e análises diferenciais e térmicas (DTA) foram realizadas.
Dependências da temperatura da mudança de massa relativa Δm / m 0 = ( m − m 0 ) / m 0 , m 0 –– massa da amostra inicial (ver Fig. 1) e derivada da mudança de massa dm / dT (ver Fig. 2) foram obtidos.
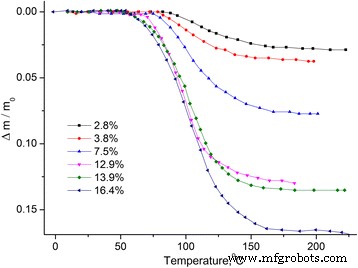
Dependência da temperatura da mudança de massa relativa do MCC. Dependência da temperatura da mudança de massa relativa Δ m / m 0 de amostras MCC com diferentes teores de água
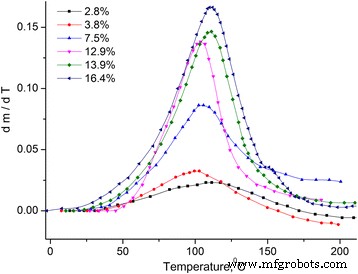
Dependência da derivada da mudança de massa do MCC com a temperatura. Dependência da derivada da mudança de massa com a temperatura dm / dT de amostras MCC com diferentes teores de água
Pode-se considerar que a perda de massa pela amostra é ocasionada pela evaporação da água, que se localiza na amostra em diferentes estados [12, 13]. Portanto, o dm / dT foi dividido em picos usando a distribuição de Gauss (ver Fig. 3).
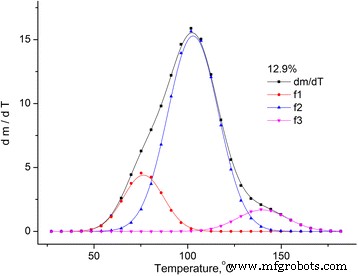
Aproximação do dm / dT dependência para amostra MCC com a umidade de 12,9%. Aproximação do dm / dT dependência para a amostra MCC com a umidade de 12,9% usando a distribuição de Gauss com três picos
A dependência de dm / dT para cada uma das amostras investigadas pode ser descrita pela superposição de três picos. O primeiro pico ( f 1 ) está relacionado com a evaporação da água de ligação físico-mecânica com MCC, que está localizada nos microporos da amostra, o segundo ( f 2 ) é causado pela água de camadas de hidrato polimolecular e monomolecular, e o terceiro pico é causado pela degradação oxidativa térmica da amostra.
Na Tabela 1, porcentagem S 1 na praça do pico geral dm / dT e porcentagem de massa w i = CS i / 100% na massa geral de diferentes tipos de água e destruição para as amostras de MCC com diferentes teores de água é mostrado .
É visto que a quantidade de água fisicamente ligada mecanicamente S 1 aumenta com o crescimento do conteúdo de água em geral e a quantidade de água nas conchas de hidrato S 2 também aumenta e atinge sua saturação na concentração da água geral de 12,9%.
Consideremos com mais detalhes o segundo pico ( f 2 ), que é causada pela desidratação dos cristais de celulose.
O método de cálculo dos parâmetros cinéticos do processo de desidratação, como a energia de ativação E e fator pré-exponencial ( k 0 ) são descritos em [12]. A equação cinética do processo de dessorção pode ser apresentada como:
$$ \ frac {dQ} {dt} =- k {Q} ^ n, k =\ frac {-dQ / dt} {Q ^ n}. $$ (1)
Um grau de cobertura dos cristalitos de celulose pelas moléculas de água ( Q ) muda de 1 (para o material inicial) para 0 (a água inteira é desidratada). Uma ordem de reação ( n ) é um número inteiro de 1 a 3; presume-se que seja conhecido a partir do experimento. A constante da taxa de reação ( k ) pode ser escrito como:
$$ k ={k} _0 \ exp \ left (- \ frac {E} {RT} \ right), $$ (2)
onde R é uma constante de gás universal. O valor de E é tomado nesta aproximação como uma constante, o que significa uma equivalência de todos os centros de hidratação da superfície dos cristais do MCC. O fator pré-exponencial pode ser escrito como k 0 =ZP , onde Z é o número teórico de descontinuidades de ligações de hidrogênio entre as moléculas de água e celulose (MCC) em uma camada de hidrato por unidade de tempo, e P é um fator de probabilidade que leva em consideração todos os efeitos causados por um desvio da idealidade. A probabilidade de quebrar a ligação de hidrogênio entre a molécula de água e a celulose é muito maior em uma concentração mais alta de moléculas de água na casca hidratada, então a molécula de água após a quebra da ligação não forma uma nova ligação com o nó livre vizinho, mas traduz a partir da camada de hidrato. Portanto, o fator pré-exponencial da taxa de reação é pequeno nas baixas concentrações de água e aumenta com o aumento da concentração de água na camada hidratada. Quando a saturação da camada hidratada é alcançada (todos os nós estão ocupados), então k 0 não depende da concentração da umidade. Isso é observado para o sistema de água MCC em uma concentração de mais de 12,9%.
Após a substituição da Eq. 1 na Eq. 2 e logaritmo, obtemos:
$$ \ ln k =\ ln \ left [\ frac {-dQ / dt} {Q ^ n} \ right] =\ ln {k} _0- \ frac {E} {RT}. $$ (3)
Sob condições iniciais Q t = 0 = 1, Q t =∞ = 0 e taxa de aquecimento constante ( β ), isto é, na dependência linear da temperatura no tempo
$$ T (t) ={T} _0 + \ beta t, $$ (4)
os seguintes relacionamentos são cumpridos
$$ Q (t) =\ frac {S_T} {S_0}; - \ frac {dQ} {dt} =\ beta \ frac {f_3} {S_0}, $$ (5)
onde S 0 e S T são as áreas do terreno f 2 sob todo o pico e parte do pico de T para ∞
$$ {S} _T ={\ displaystyle \ underset {T} {\ overset {\ infty} {\ int}} {f} _2dT, {S} _0 =} {\ displaystyle \ underset {0} {\ overset { \ infty} {\ int}} {f} _2dT}. $$ (6)
Se todas as suposições colocadas neste método estiverem corretas e a ordem de reação n é escolhido corretamente, então a dependência \ (\ ln \ left [\ frac {-dQ / dt} {Q ^ n} \ right] \) na temperatura inversa (Eq. 3) é linear em toda a faixa de temperatura. Tendo valores experimentais de f 3 e β , usando expressões Eqs. 5 e 6, pode-se obter Q e dQ / dt , e parâmetros de cinética não isotérmica k 0 e E são calculados a partir da Eq. 3
Uma vantagem deste método é o uso de todo o conjunto de dados experimentais, incluindo a parte de alta temperatura do termograma, que é especialmente importante na determinação da ordem n , determinação do mecanismo de reação e justiça do modelo.
As dependências de \ (\ ln \ left [\ frac {-dQ / dt} {Q ^ n} \ right] \) de uma temperatura reversa para os padrões investigados (Fig. 4) foram construídas. Essas dependências são aproximadas por linhas retas por meio do método dos mínimos quadrados. Verifica-se que o maior coeficiente de Pearson é observado em n =2.
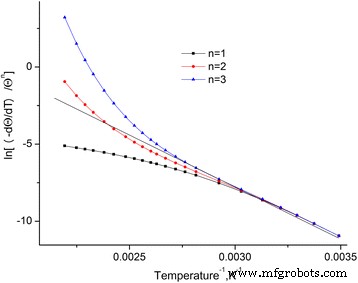
Dependência de \ (\ ln \ left [\ frac {-dQ / dt} {Q ^ n} \ right] \) na temperatura reversa para diferentes ordens de reação. Dependência de \ (\ ln \ left [\ frac {-dQ / dt} {Q ^ n} \ right] \) da temperatura reversa para diferentes ordens de reação
Energia de ativação calculada ( E ) e fator pré-exponencial ( k 0 ) das amostras de MCC investigadas são apresentadas na Tabela 2 (ver Fig. 5). Assumindo que a energia de ativação está conectada com o arrebatamento das ligações de hidrogênio, que compreendem 25 k J / mol [10], é possível calcular o seu número N 1 (ver Tabela 2).
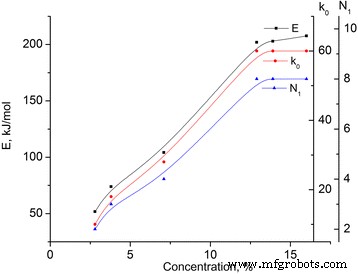
Dependências de energia de ativação ( E ), fator pré-exponencial ( k 0 ), e número de ligações de hidrogênio N 1 para as amostras de MCC. Dependências de energia de ativação ( E ), fator pré-exponencial ( k 0 ), e número de ligações de hidrogênio N 1 para as amostras de MCC com diferentes teores de água
É visto que com o aumento da concentração de água fisicamente e quimicamente ligada, o aumento da energia de ativação ( E ) é observada e, na concentração de 12,9%, atinge a sua saturação. O valor da energia de ativação para o estado saturado corresponde a oito ligações de hidrogênio.
Portanto, podemos assumir que na concentração de água de 12,9%, a camada contínua de hidrato dos cristais de MCC é formada na amostra.
Análise de difração de raios-X
As dependências da intensidade da radiação de raios X difratados para a celulose microcristalina com diferentes concentrações de água no ângulo de difração I (2 θ ) dentro da faixa de ângulos [5 ÷ 45] ° (ver Fig. 6) com o passo de mudança de ângulo de 0,1 ° foram obtidos.
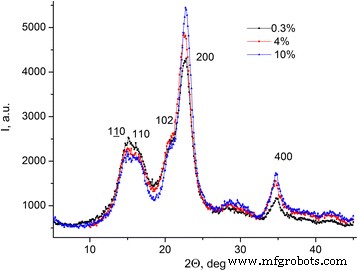
Dependências da intensidade da radiação de raios X difratados para MCC. Dependências da intensidade da radiação de raios X difratados para MCC com diferentes concentrações de água no ângulo de difração I (2 θ )
Máximos, que correspondem a diferentes planícies cristalográficas, são observados no difractograma de raios-X do MCC (ver Fig. 6).
O grau de cristalinidade ( C k ) de MCC foi calculado pela intensidade integral de espalhamento de raios-X como uma razão entre os reflexos estruturais e a intensidade total do padrão de difração, excluindo o fundo no intervalo 2 θ [5 ÷ 45] ° (ver Fig. 6). Dados de C k para as amostras de MCC são apresentadas na Tabela 3 [14].
As dimensões transversais dos cristalitos de celulose na direção normal ao sistema foram calculadas pela fórmula de Debye-Sherrer [15].
$$ {B} _ {\ mathrm {hkl}} =\ frac {k \ lambda} {h \ cdot \ cos {\ theta} _ {\ mathrm {hkl}}}, $$ (7)
onde k =0,94 --- fator de forma adimensional, λ --- comprimento de onda da radiação CuKα (1,54178 Å); h --- meia largura do reflexo (hlk), θ hlk --- ângulo de difração do sistema de planícies (hlk). Urotropina foi usada como um etalon para maior confiança. O erro instrumental foi estimado usando o etalon, e as correções para a meia-largura do reflexo foram calculadas.
Dados das dimensões B hlk para amostras de MCC com diferentes conteúdos de água e cristalinidade são apresentadas na Tabela 3.
Conclui-se dos resultados obtidos (Tabela 3 e Fig. 7) que a dimensão transversal dos cristalitos e a cristalinidade crescem com a concentração de água. O crescimento das dimensões ocorre em diferentes direções em aproximadamente 0,4 nm. O diâmetro médio da molécula de celulose é da ordem de d =0,8 nm. Portanto, com o aumento da concentração de água, pode ocorrer um ordenamento das moléculas de celulose na camada limite e, como conseqüência, aumento da dimensão transversal dos cristalitos de celulose e da cristalinidade.
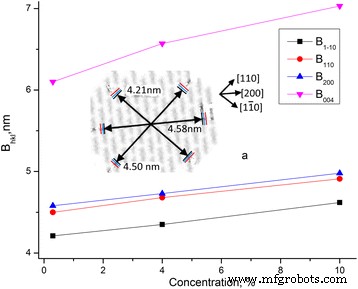
Dependências das dimensões do cristalito do MCC B hlk no conteúdo de água. Dependências das dimensões do cristalito do MCC B hlk no conteúdo de água, a --- dimensões transversais do cristalito MCC ( preto ) e crescimento de sua dimensão com o aumento da umidade ( azul --- MCC + 4% e vermelho --- MCC + 10%)
Propriedades dielétricas da MCC
Dependências da temperatura das partes reais e imaginárias da permissividade dielétrica complexa dentro da faixa de temperatura [-180 ÷ 120] ° C nas frequências f =5, 10, 20 e 50 kHz para as amostras MCC + 0,3% H 2 O (ver Figs. 8 e 9) foram investigados.
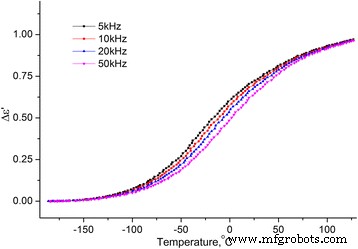
Dependência da temperatura da mudança de incremento da parte real da permissividade dielétrica complexa. Dependência da temperatura da mudança de incremento da parte real (Δ ε ′ = ε ′ ( T ) - ε ∞ , \ ({\ varepsilon} _ {\ infty} ={\ left. {\ varepsilon} ^ {\ prime} \ right |} _ {T =-180 {} ^ o \ mathrm {C}} \)) de a permissividade dielétrica complexa MCC + 0,3% H 2 O nas frequências 5, 10, 20 e 50 kHz
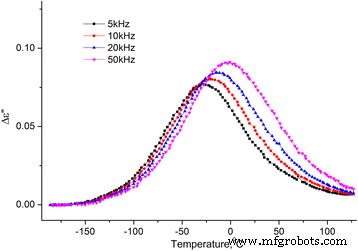
Dependência da temperatura da parte imaginária da permissividade dielétrica do MCC + 0,3% H 2 O. Dependência da temperatura da parte imaginária da permissividade dielétrica de MCC + 0,3% H 2 O nas frequências 5, 10, 20 e 50 kHz
Dos dois processos observados nas dependências da temperatura de ∆ ε ′ ( T ) e ε ′ ′ ( T ), a baixa temperatura é um relaxamento desde o máximo em ∆ ε ′ ( T ) e a inflexão em ε ′ ′ ( T ) é deslocado com o aumento da frequência. Normalmente, esse processo é chamado de processo β, seu mecanismo molecular ainda não está estabelecido. Assumimos que ela está relacionada à reorientação dos grupos metilol na superfície dos cristalitos do MCC, e essa reorientação ocorre com uma mudança na conformação dos grupos metilol tg para tt , a quebra da ligação H intramolecular e a formação da ligação H com a molécula de água adsorvida [16].
O processo de alta temperatura nas dependências ∆ ε ′ ( T ) e ε ′ ′ ( T ) não muda com a variação de frequência, sua intensidade aumenta com a concentração de água no MCC (ver Figs. 10 e 11). Assumimos que a razão para isso é a dessorção da água com o aumento da temperatura com sua posterior condensação nos poros, o que leva a um aumento acentuado da temperatura ε ′ E ε ′ Da amostra. Com o aumento da temperatura, ocorre a evaporação da água, e ∆ ε ′ ( T ) e ε ′ ′ ( T ) diminuir.
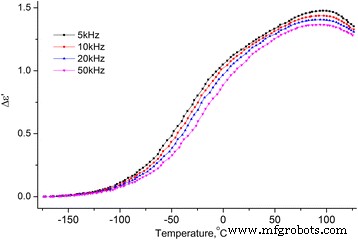
Dependência da temperatura do incremento da parte real da permissividade dielétrica MCC + 2,8% H 2 O. Dependência do incremento da parte real com a temperatura (Δ ε ′ = ε ′ ( T ) - ε ∞ , onde \ ({\ varepsilon} _ {\ infty} ={\ left. {\ varepsilon} ^ {\ prime} \ right |} _ {T =-180 {} ^ oC} \)) da permissividade dielétrica MCC + 2,8% H 2 O nas frequências 5, 10, 20 e 50 kHz
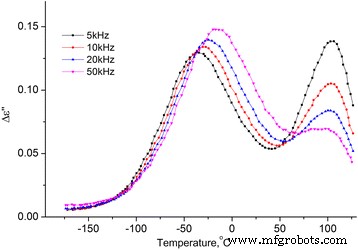
Dependência da temperatura da parte imaginária da permissividade dielétrica do MCC + 2,8% H 2 O. Dependência da temperatura da parte imaginária da permissividade dielétrica do MCC + 2,8% H 2 O nas frequências 5, 10, 20 e 50 kHz
Na Fig. 12, dependências do incremento da parte real ( Δε ′ = ε ′ ( T ) - ε ∞ , onde \ ({\ varepsilon} _ {\ infty} ={\ left. {\ varepsilon} ^ {\ prime} \ right |} _ {T =-180 {} ^ oC} \)) da permissividade dielétrica em temperatura na frequência de 10 kHz são apresentados para amostras investigadas de MCC com diferentes teores de água.
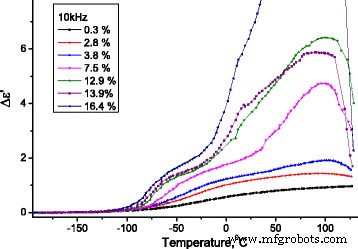
Dependência da temperatura da mudança de incremento da parte real da permissividade dielétrica do MCC. Dependência da temperatura da mudança de incremento da parte real (Δ ε ′ = ε ′ ( T ) - ε ∞ , onde \ ({\ varepsilon} _ {\ infty} ={\ left. {\ varepsilon} ^ {\ prime} \ right |} _ {T =-180 {} ^ oC} \)) da permissividade dielétrica de Amostras MCC com diferentes teores de água
Foi mostrado em [16] que o processo de relaxamento de baixa temperatura, que está conectado com a transição do grupo metilol de tg para tt conformação, pode ser descrita pelo modelo com um tempo de relaxação [17]
$$ \ tau =\ frac {2 \ pi} {\ omega_0} \ frac {\ exp \ left (\ raisebox {1ex} {$ U $} \! \ left / \! \ raisebox {-1ex} {$ kT $} \ right. \ right)} {1+ \ exp \ left (\ raisebox {1ex} {$ - V $} \! \ left / \! \ raisebox {-1ex} {$ kT $} \ right. \ direita)} $$ (8)
e para o incremento da permissividade dielétrica a seguinte fórmula é válida:
$$ \ varDelta \ varepsilon ={\ varejpsilon} ^ {\ prime} (T) - {\ varejpsilon} _ {\ infty} =\ frac {N {\ mu} ^ 2} {3k {\ varepsilon} _0T} \ cdot \ frac {\ exp \ left (\ raisebox {1ex} {$ - V $} \! \ left / \! \ raisebox {-1ex} {$ kT $} \ right. \ right)} {{\ left [ 1+ \ exp \ left (\ raisebox {1ex} {$ - V $} \! \ Left / \! \ Raisebox {-1ex} {$ kT $} \ right. \ Right) \ right]} ^ 2}, $$ (9)
onde ε ′ (T) –– é a permissividade dielétrica da amostra na temperatura T , N é a concentração de osciladores de relaxamento, μ 2 é o quadrado médio da diferença dos momentos dipolares dos osciladores de relaxamento em duas posições de equilíbrio, e V é a diferença de energias dos osciladores de relaxamento nessas posições de equilíbrio.
Durante a aproximação da dependência do incremento da parte real da permissividade dielétrica complexa para amostras MCC com umidade diferente pela dependência (Eq. 9), valores de N e V foram obtidos (ver Tabela 4) em relação à diferença de momentos dipolares de osciladores de relaxamento em duas posições de equilíbrio, que foi calculada em relação à estrutura espacial do grupo metilol μ =5,57 D =18,381 ⋅ 10 - 30 C ⋅ m .
É visto na Tabela 4 que com o aumento do teor de água, a diferença de energia V não muda, mas a concentração de grupos metilol, que contribui no relaxamento dielétrico, aumenta.
Na Fig. 13, as dependências da parte imaginária da permissividade dielétrica da temperatura na frequência f =10 kHz para amostras estudadas de MCC com diferentes teores de água são apresentados.
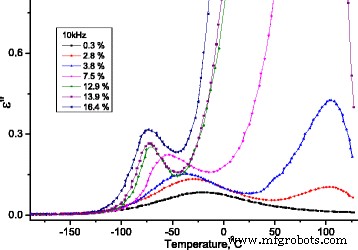
Dependência da temperatura da parte imaginária da permissividade dielétrica para amostras de MCC com diferentes teores de água. Dependência da temperatura da parte imaginária da permissividade dielétrica para amostras de MCC com diferentes teores de água
Para o processo de relaxamento sob aproximação de um tempo de relaxamento ( τ = τ 0 exp (( U - TΔS ) / kT ) e sob condição de máximo de dependência da parte imaginária de permissividade dielétrica complexa ( ε ′ ′ ( T , f )) ωτ =1 , mudanças de entropia ΔS / k (ver Fig. 14) e energia de ativação U (ver Fig. 14) com concentração de água.
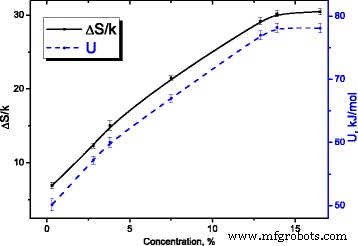
Dependências da entropia e da energia de ativação do processo de relaxamento na concentração de água no MCC. Dependências da entropia e da energia de ativação do processo de relaxamento na concentração de água no MCC
Assumimos que a entropia de ativação do processo de relaxamento está conectada com a probabilidade de formação de ligações de hidrogênio do grupo metilol com moléculas de água circundantes [18].
Seu crescimento atesta o aumento do número médio de moléculas de água, que circundam esses grupos na superfície dos cristalitos do MCC.
A saturação da dependência ∆ S / k (ver Fig. 14) no crescimento da concentração de água é uma consequência da formação de concha de hidrato sólido no sistema de cristalitos MCC como resultado da incorporação de aglomerados de superfície separados de moléculas de água após atingir sua concentração limite, que é determinada por superfície específica da água disponível do sistema de cristalitos MCC durante o seu intumescimento.
O crescimento da energia de ativação U ( C ) do processo de relaxamento (ver Fig. 14) e a saturação de sua dependência da concentração de água tem a mesma natureza que a ativação de entropia é indicativa da estruturação da superfície dos cristalitos de MCC durante a formação de sua casca de hidrato sólido.
Conclusões
Estudos de propriedades dielétricas, termofísicas e estruturais de amostras de MCC com diferentes graus de umidade foram realizados. A existência de processos de relaxação, que estão ligados à reorientação dos grupos metilol de superfície da molécula de celulose pela mudança de suas conformações de tg para tt é mostrado.
Durante a retenção da amostra de MCC no vapor de água saturado, a camada de hidrato começa a se formar gradualmente na superfície dos cristalitos de celulose. Ele estrutura a camada limite dos cristalitos do MCC. Na concentração de água, é observada formação superior a 13% de camada de hidrato sólido em cristalitos MCC.
A formação da camada de hidrato resulta no deslocamento do processo de relaxamento para o lado de baixas temperaturas devido à sua influência na barreira potencial e na alteração das vibrações nas posições de equilíbrio dos grupos metilol de superfície da molécula de celulose em sua transição da conformação tg para tt .
Nanomateriais
- O que é liga de cobalto e quais são as propriedades da liga de cobalto?
- O lado desconfortável, imprevisível e aleatório da manutenção
- Quais são as aplicações e propriedades do aço manganês?
- IoT e gerenciamento de água em casa
- Revelando a estrutura atômica e eletrônica das nanofibras de carbono de copo empilhado
- Estrutura e propriedades eletrônicas da nanoargila caulinita dopada com metal de transição
- O efeito do plasma sem equilíbrio de contato nas propriedades estruturais e magnéticas de Mn Х Fe3 - X О4 Spinels
- Explorando a relação entre EDM e a indústria aeroespacial
- Película de capacitor:as propriedades, construção e aplicação
- Compressores de ar e secadores:o par perfeito



