Fabricação e caracterização de óxido de grafeno funcionalizado de taurina com 5-fluorouracil como sistemas de administração de medicamentos anticâncer
Resumo
Recentemente, os sistemas nanocarrier para medicamentos contra o câncer, especialmente os sistemas de entrega de medicamentos baseados em GO, tornaram-se uma bênção para pacientes com câncer. Neste estudo, escolhemos Tau para funcionalizar a superfície GO para melhorar sua biocompatibilidade. Em primeiro lugar, o GO em nanoescala foi sintetizado pelo método Hummer modificado e pelo método de remoção ultrassônica. O carreador de óxido de grafeno modificado com taurina (Tau-GO) foi sintetizado por método químico para obtenção de Tau-GO que apresenta boa dispersibilidade e estabilidade em água, potencial zeta de -38,8 mV e tamanho de partícula de 242 nm. Com base nos critérios de avaliação da eficiência de encapsulação, a formulação ideal foi determinada para combinar Tau-GO e 5-FU por ligação não covalente. O 5-FU-Tau-GO foi mais estável em ambiente neutro do que em ambiente ácido, e com uma certa resposta de pH e efeito de liberação sustentada. In vivo, comparamos as administrações orais e intravenosas de 5-FU e 5-FU-Tau-GO, respectivamente, usando testes farmacocinéticos e parâmetros relacionados e demonstramos que a administração oral ou intravenosa de 5-FU-Tau-GO prolonga o tempo de ação de 5 -FU no corpo e melhora sua biodisponibilidade. Além disso, a inibição de células HepG2 que foi medida pelo ensaio MTT, mostrou que o IC 50 valor de 5-FU foi de 196 ± 8,73 μg / mL, e o IC 50 o valor de 5-FU-Tau-GO foi de 65,2 ± 0,7 μg / mL, indicando que 5- FU-Tau-GO é mais potente contra as células HepG2 e tem um efeito inibitório mais forte nas células cancerosas. O efeito na morfologia celular que foi medido usando a coloração AO / EB também mostrou que 5-FU-Tau-GO não apenas interrompeu as células, mas também induziu apoptose significativamente em comparação com 5-FU. Também verificamos por projeto auxiliado por computador que o Tau-GO pode se ligar melhor a 5-FU do que ao GO não modificado, e que o sistema 5-FU-Tau-GO formado é mais estável e propício à transferência e liberação de 5- FU in vivo.
Introdução
A quimioterapia ainda é um método comum usado no tratamento de vários tipos de câncer [1]. Um obstáculo significativo da maioria dos agentes quimioterápicos é sua incapacidade de penetrar nos tecidos tumorais, em concentrações eficazes, ou seus indesejáveis efeitos colaterais nos tecidos normais [2]. Portanto, os cientistas concentraram seus esforços no desenvolvimento de um sistema potente de liberação de drogas que pode atingir a taxa controlada de liberação de drogas em tecidos tumorais para garantir a administração e terapia eficazes da droga.
Muitos materiais nanométricos incluindo lipossomas [3], polímeros [4], nanopartículas [5], dendrímeros [6], micelas [7] e óxido de grafeno [8, 9] foram desenvolvidos para a entrega de vários medicamentos. Entre esses nanomateriais, o óxido de grafeno (GO) é um novo nanomaterial de carbono que é quimicamente esfoliado de grafite oxidada e exibe várias propriedades físicas e químicas fascinantes, como grupos funcionais abundantes, grande área de superfície específica, alta quantidade de carga de droga e excelente dispersão capacidade na água [10,11,12]. Além disso, a maioria dos resultados experimentais in vitro mostrou que uma baixa concentração de GO poderia ser usada como substrato para o crescimento celular e para ativar células do sistema imunológico. Portanto, GO tem sido amplamente utilizado no diagnóstico de doenças [13], imagem e rastreamento de células cancerígenas [14], terapia fototérmica do câncer [15], engenharia de tecidos [16], administração de drogas direcionadas [17] e, especialmente, como um anti- carreadores de drogas tumorais [18, 19]. No entanto, vários grupos de pesquisa relataram que uma alta concentração de GO tem efeitos citotóxicos óbvios em estudos pré-clínicos e clínicos. O mecanismo pelo qual o GO produz efeitos tóxicos in vivo é por meio do estresse oxidativo e da superprodução de espécies reativas de oxigênio intracelular, induzindo apoptose celular e causando inflamação severa, edema pulmonar e formação de granuloma [20]. Portanto, é de importância crítica resolver a questão da toxicidade do GO.
Alegadamente, a funcionalização de ligações covalentes ou não covalentes pode reduzir a forte interação hidrofóbica entre GO e células. Isso foi demonstrado por vários estudos que mostraram que a funcionalização do GO melhora sua biocompatibilidade e quase elimina sua toxicidade in vivo e in vitro. Yang et al. estudaram, pela primeira vez, a biodistribuição de longo prazo da conjugação covalente de PEG-GO em camundongos usando um método de radiomarcação, e os resultados mostraram que o PEG-GO poderia ser excretado gradualmente de camundongos, provavelmente na urina e nas fezes [21]. Zhang et al. comparou o GO funcionalizado com DEX com o GO e descobriu que o GO-DEX pode reduzir notavelmente a toxicidade celular e ser eliminado principalmente dos camundongos em uma semana [22]. Além disso, a ligação não covalente do GO ao pluronic F127 resulta em solubilidade e estabilidade benigna em condições fisiológicas e uma baixa toxicidade [23]. Embora vários polímeros ou moléculas tenham sido usados para funcionalizar o GO, resultados significativos foram alcançados neste campo. No entanto, ainda são necessários esforços para desenvolver métodos simples para construir um bom carreador de medicamentos à base de GO biocompatíveis.
Taurina (Tau) é um aminoácido semi-essencial com boa estabilidade e solubilidade em água. Tau pode prevenir doenças cardiovasculares e cerebrovasculares, manter a função visual, proteger as células e regular a imunidade. Numerosos estudos propuseram que Tau tem propriedades antitumorais através de sua regulação positiva ou regulação negativa dos fatores de expressão que desempenham papéis importantes em vários tipos de câncer, incluindo câncer de pulmão, estômago, colorretal e mama [24]. Assim, o GO funcionalizado com Tau pode exercer um papel superior como um carreador de drogas antitumorais. Neste artigo, usamos, pela primeira vez, o GO covalente Tau funcionalizado como um nanocarreador e avaliamos sua citotoxicidade in vitro. Além disso, o 5-fluorouracil (5-FU) foi usado como uma droga anticâncer que foi carregada de forma não covalente na superfície do Tau-GO para construir um sistema de distribuição de droga. O 5-FU-Tau-GO pode não apenas reduzir os efeitos colaterais nos tecidos normais, mas também melhorar a biodisponibilidade do medicamento. Consequentemente, o Tau-GO foi desenvolvido com sucesso como um novo nanomaterial baseado em GO que pode ter aplicações biomédicas significativas no futuro.
Experimentos e métodos
Materiais
O pó de grafite, solução salina tamponada com fosfato (PBS) e dimetilsulfóxido (DMSO) foram adquiridos de Tianjin Laibo Chemical Co., Ltd .; Carbodiimida (EDC), N-hidroxissuccinimida (NHS), ácido clorídrico (HCl) e peróxido de hidrogênio (H 2 O 2 30%) foram adquiridos da Shandong Yuwang Industrial Co., Ltd .; Taurina (Tau), 5-fluorouracil (5-FU), células de hepatoma humano (HepG2), solução de penicilina-estreptomicina e soro fetal bovino (FBS) foram adquiridos de Dalian Meilun Biotechnology Co., Ltd .; ácido sulfúrico (H 2 SO 4 98%) e permanganato de potássio (KMnO 4 ) foram adquiridos a Nanjing Chemical Reagent Co., Ltd .; nitrato de sódio (NaNO 3 ) e dodecilsulfato de sódio (SDS-Na) foram adquiridos a Shanghai Jinjinle Industrial Co., Ltd .; O MTT foi adquirido da Sigma-Aldrich, Inc; DMEM foi adquirido de HyClone, Inc; Os ratos foram adquiridos no Benxi Changsheng Experimental Animal Center. Todos os outros reagentes e produtos químicos eram analiticamente puros e estavam disponíveis comercialmente.
Síntese GO
O GO foi preparado a partir de pó de grafite de acordo com um método modificado de Hummer. Em primeiro lugar, 168 mL de ácido sulfúrico a 98% foram adicionados ao longo da parede do frasco de um frasco de três gargalos que foi colocado em um banho de gelo com termômetro, e 5 g de grafite e 4 g de nitrato de sódio foram adicionados quando a temperatura atingiu 5 ° C. Em seguida, 22,5 g de permanganato de potássio foram adicionados lentamente em lotes por 1 h e a temperatura foi mantida abaixo de 5 ° C. Depois disso, o balão de três gargalos foi transferido para um banho de óleo e a mistura obtida foi reagida a 35 ° C por 30 min, então a temperatura foi aumentada para 65 ° C e a reação foi agitada por 30 min. Seguindo esta etapa, a temperatura foi aumentada para 85 ° C e a mistura foi posteriormente reagida por 1 h para obter uma pasta marrom-púrpura. Esta mistura foi deixada em repouso por 1 semana, transferida para um béquer com 700 mL de água quente, e o peróxido de hidrogênio a 30% foi adicionado gota a gota até se tornar marrom amarelado. A mistura foi centrifugada a 10.000 rpm, lavada com água quente e este processo foi repetido várias vezes até o pH do sobrenadante ser 7,0. Finalmente, o produto foi seco em um liofilizador a vácuo e o nano GO foi obtido.
Síntese Tau-GO
Um GO de 50 mg pesado com precisão foi dissolvido em 50 mL de água destilada, e 150 mg de EDC e 100 mg de NHS foram adicionados para ativar o GO por ultrassonicação em um banho de água gelada por 20 min. Em seguida, 10 mL de solução aquosa de Tau (0,1 g / mL) foram adicionados lentamente (gota a gota) à solução aquosa GO preparada e o pH foi ajustado para 6-7 por HCl e continuamente agitado por 24 h em um quarto no escuro. O produto foi recolhido por centrifugação a 5000 rpm durante 10 min e lavado 3 vezes com água destilada. O Tau-GO foi coletado após liofilização.
Carregamento de 5-FU
Uma quantidade de 20 ml de solução Tau-GO foi submetida a ultrassom por 2 h. Uma quantidade pesada com precisão de 5-FU foi dissolvida em uma quantidade apropriada de água destilada e lentamente adicionada gota a gota à solução de Tau-GO preparada sob agitação à temperatura ambiente, em seguida, sonicada a 30 ° C no escuro por 1,5 h. Os produtos foram centrifugados a 5000 rpm durante 10 min a 4 ° C. O sedimento inferior foi lavado com 20 mL de água destilada e centrifugado (5000 rpm por 10 min a 4 ° C), e o processo foi repetido 3 vezes. A camada inferior foi liofilizada, o sobrenadante foi colocado em um béquer, pesado o volume, a concentração de 5-FU foi determinada em 1200 HPLC (Agilent, EUA). As condições de detecção foram as seguintes:coluna cromatográfica:C18 (4,6 × 250 nm, 5 μm); temperatura da coluna:25 ° C; fase móvel:0,1% KH 2 PO 4 solução com pH 5,5; taxa de fluxo:1,0 mL / min; volume de injeção:20μL; e comprimento de onda de medição:265 nm. A taxa de encapsulação (EE) e a eficiência de carregamento de droga (LE) foram obtidas pela seguinte fórmula:
$$ \ begin {align} {\ text {EE}} \ left (\% \ right) &=\ frac {{M_ {1} - C_ {1} \ times L_ {1}}} {{M_ {1 }}} \ times 100 \% \\ {\ text {LE}} \ left (\% \ right) &=\ frac {{M_ {1} - C_ {1} \ times L_ {1}}} {{ 20C_ {0} + M_ {1} - C_ {1} \ vezes L_ {1}}} \ vezes 100 \% \\ \ end {alinhado} $$
A dose total de 5-FU foi registrada como M 1 , a concentração e o volume de 5-FU livre foram registrados como C 1 e L 1 , e a concentração do transportador foi registrada como C 0 .
Caracterização
Para caracterizar o nanocompósito preparado, espectros de infravermelho de transformada de Fourier (FT-IR) foram varridos de 4000 a 400 cm −1 no espectrômetro IRAffinity-1 (Shimadzu, Japão) para confirmar as interações. Os espectros de absorção de UV-vis foram registrados em um espectrofotômetro de varredura UV-3600 (Shimadzu, Japão). As amostras foram dissolvidas em água destilada e os tamanhos de partícula, potenciais zeta e valores de PDI foram obtidos em um instrumento Nano-ZS 90 Nano (Malvern, Reino Unido). As morfologias das amostras foram analisadas em microscopia eletrônica de transmissão (TEM) JEM-2100 (JEOL, Japão). As análises termogravimétricas (TGA) foram realizadas usando um analisador termogravimétrico (NETZSCH, Alemanha) a uma taxa de aquecimento de 10 ° C / min de 0 a 800 ° C sob uma atmosfera de nitrogênio. A medição de XRD das amostras foi realizada por difratômetro de raios-X (Bruker, Alemanha) com uma radiação de cobre CuKα ( λ =1,5406 Å) em um ângulo amplo com ângulo 2θ. As medições de XPS foram realizadas usando uma sonda Omicron ESCA com um Al Karadiation monocromado (Thermo, América).
Liberação de droga in vitro
A liberação do fármaco in vitro foi realizada em pH 1,2 (ambiente gástrico simulado), pH 6,5 (ambiente simulado de células cancerígenas do fígado) e pH 7,4 (ambiente fisiológico simulado) a 37 ° C (temperatura corporal simulada), respectivamente. Resumidamente, 15 mg de 5-FU-Tau-GO foram colocados em uma membrana de diálise, imersos em 50 mL de soluções tampão contendo 0,1% de SDS-Na com pH de 1,2, 6,5 e 7,4. Todas as amostras foram colocadas em banho-maria com agitação contínua a uma velocidade de 100 rpm e a uma temperatura de 37 ° C. Em pontos de tempo predeterminados (0 min, 5 min, 10 min, 20 min, 30 min, 1 h, 1,5 h, 2 h, 2,5 h, 3 h, 4 h, 8 h, 12 h, 24 h, 48 h e 72 h), 1 mL de cada amostra foi retirado e substituído por 1 mL de solução tampão fresca contendo 0,1% de SDS-Na para manter o mesmo volume de meio de liberação. O meio liberado foi centrifugado e analisado usando 1200 HPLC.
Estudos de citotoxicidade in vitro
Ensaio MTT
O ensaio MTT foi usado para avaliar a citotoxicidade de 5-FU, Tau-GO e 5-FU-Tau-GO. Resumidamente, as células de hepatoma HepG2 humano foram cultivadas em meio DEME, suplementado com 10% de FBS e 1% de antibióticos (solução de penicilina-estreptomicina) a 37 ° C em uma atmosfera umidificada de 5% de CO 2 . As células foram semeadas em uma placa de 96 poços a uma densidade de 5 × 10 3 células por poço contendo 100 μL de meio DEME, suplementado com FBS e antibióticos. A placa foi colocada por 24 h em uma câmara umidificada a 37 ° C contendo 5% de CO 2 . Depois disso, o meio de crescimento foi removido e recarregado com 100 μL de meio fresco que continha várias concentrações (5, 10, 20, 40, 60, 80 e 100 μg / ml) de 5-FU, Tau-GO, 5-FU- Tau-GO, respectivamente. Após uma incubação de 24 horas, as células foram tratadas com 20 μL de solução de MTT e posteriormente incubadas por 4 horas. Em seguida, o meio foi aspirado e os cristais de formazan foram dissolvidos em 150 μL de DMSO. Finalmente, as placas de poços foram agitadas a 37 ° C por 15 min em um oscilador de temperatura constante. A densidade óptica (DO) de cada amostra foi medida a 570 nm usando um leitor de microplaca. Os experimentos foram realizados em triplicata. A taxa de inibição celular foi calculada a partir dos resultados usando a seguinte fórmula:
$$ {\ text {Cell}} \; {\ text {inibição}} \; {\ text {taxa}} =\ frac {{{\ text {OD}} _ {{{\ text {control}}} } - {\ text {OD}} _ {{{\ text {tratado}}}}}} {{{\ text {OD}} _ {{{\ text {control}}}}}} \ vezes 100 \ % $$
onde OD control é a absorbância obtida por células de controle não tratadas, OD tratadas é a absorbância obtida pelas células tratadas.
Ensaio de coloração AO / EB
A coloração dupla AO / EB foi usada para avaliar as alterações morfológicas das células que foram tratadas com 5-FU, Tau-GO e 5-FU-Tau-GO. Resumidamente, as células HepG2 em uma fase de crescimento logarítmico foram semeadas em uma placa de 6 poços a uma densidade de 10.000 células por poço e cultivadas em uma incubadora a 37 ° C e sob 5% de CO 2 atmosfera. Após 24 h, as células foram tratadas com uma concentração fixa de 5-FU, Tau-GO ou 5-FU-Tau-GO e posteriormente incubadas por 24 h. O meio em cada poço foi removido e as células foram lavadas duas vezes com PBS. Em seguida, 1 mL de PBS suplementado com 40 μL de corantes fluorescentes (1 mg / mL AO e 1 mg / mL EB foram misturados na proporção de 1:1) foram adicionados a cada poço e incubados por 10 min sem luz. As células coradas foram observadas em microscópio de fluorescência e as imagens foram tiradas aleatoriamente.
Estudo Farmacocinético
Todos os experimentos com animais foram conduzidos de acordo com as políticas e princípios formulados pelo Comitê de Ética e Proteção Animal. Um total de 24 ratos SD machos, com pesos corporais de 230-270 g, jejuaram por 12 horas e foram divididos aleatoriamente em 4 grupos antes da administração do medicamento. Os grupos A e B foram injetados por via intravenosa com soluções de 5-FU e 5-FU-Tau-GO, e os grupos C e D receberam soluções orais de 5-FU e 5-FU-Tau-GO, respectivamente. Todos os grupos receberam uma dose de 20 mg / kg. Após a administração do medicamento, as amostras de sangue (cerca de 0,5 mL) foram coletadas em tubos de anticoagulação em determinados pontos de tempo (15 min, 1 h, 2 h, 4 h, 6 h, 8 h, 12 h, 16 h, 24 h e 48 h). As amostras de plasma foram separadas por centrifugação a 7500 rpm e a 4 ° C por 10 min. Então, 200 μL de plasma e 50 mg (NH 4 ) 2 SO 4 foram combinados em um tubo (10 μL de solução de padrão interno 5-BrU 40 μg / mL, secos com nitrogênio em banho-maria a 40 ° C, agitados em vórtex por 5 min e centrifugados a 10800 rpm por 3 min. Em seguida, o tubo foi adicionado com 900 μL de solução de acetato de etila / isopropanol (85:15, v / v), agitado em vórtice por 3 min e centrifugado a 10800 rpm por 15 min. O sobrenadante foi removido e seco com nitrogênio, 100 μL de fase móvel foram adicionados e o tubo foi agitado com vórtice por 1 min. Finalmente, a solução resultante coletada do sobrenadante foi medida por 1200 HPLC.
Simulação de Dinâmica Molecular
A simulação da dinâmica molecular é usada principalmente para analisar a força de interação entre o fármaco e o portador e o comportamento de difusão do fármaco. A estrutura química do 5-FU foi construída usando Chemdraw of chem office 2014, e as estruturas do Tau-GO e GO foram conduzidas no módulo Polymer and Molecule Builders usando o software de simulação molecular Materials Studio (versão 7.0, Accelrys Inc. , EUA). Todos os compostos construídos foram geometricamente otimizados sob o campo de força COMPASS II, e a conformação com a menor energia foi selecionada como a conformação estável. Um equilíbrio de 10 ps, NVT foi conduzido para cada sistema. A simulação foi realizada com 100 ps MD para obter uma estrutura balanceada a 298 K e 101,325 kPa com um tamanho de etapa de 1 fs. Finalmente, o deslocamento quadrático médio (MSD) e a densidade de energia coesiva (CED) foram obtidos para cada sistema, e o coeficiente de difusão (D) foi dado pela seguinte fórmula:
$$ D =\ frac {1} {2d} \ mathop {\ lim} \ limits _ {\ tau \ to \ infty} \ frac {{\ text {d}}} {{{\ text {d}} \ tau }} \ left [{\ left. {r \ overrightarrow {\ left (t \ right)} - r \ overrightarrow {\ left (0 \ right)}} \ right]} \ right. ^ {2} $$
onde o d é a dimensão do sistema, \ (r \ overrightarrow {\ left (t \ right)} \) e \ (r \ overrightarrow {\ left (0 \ right)} \) são o vetor de posição da molécula do fármaco no tempo t e 0, respectivamente, \ (\ left [{\ left. {r \ overrightarrow {\ left (t \ right)} - r \ overrightarrow {\ left (0 \ right)}} \ right]} \ right. ^ { 2} \) significa MSD.
Resultados e discussão
Caracterização
O conjugado Tau-GO foi fabricado por uma ligação amida de GO e Tau. A síntese bem-sucedida do nanocompósito foi validada por espectros FT-IR (Fig. 1). A presença das funcionalidades de oxigênio no GO foi confirmada pelos picos de absorbância em –OH (~ 3405 cm −1 ), C =O (1723 cm −1 ), C =C (1628 cm −1 ) e C – OH (1391 cm −1 ) Esses resultados comprovaram o sucesso da preparação do GO (Fig. 1a) [25]. Além de alguns picos característicos de GO, os novos picos em 1638 cm −1 e 3427 cm −1 correspondia ao grupo amida, e 1164 cm −1 e 1085 cm −1 correspondeu a –SO. O espectro Tau-GO indicou claramente que Tau foi funcionalizado na superfície GO (Fig. 1b). Na Fig. 2b, o pico característico de –SO 3 a 1164 cm −1 foi inundado pela ação de ligações de hidrogênio e não era visível nos espectros de FT-IR. Portanto, o 5-FU foi carregado com sucesso no Tau-GO.
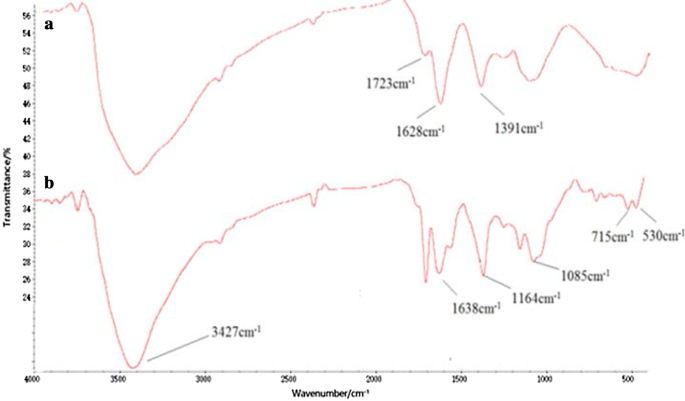
Espectro FT-IR de GO ( a ) e Tau-GO ( b )
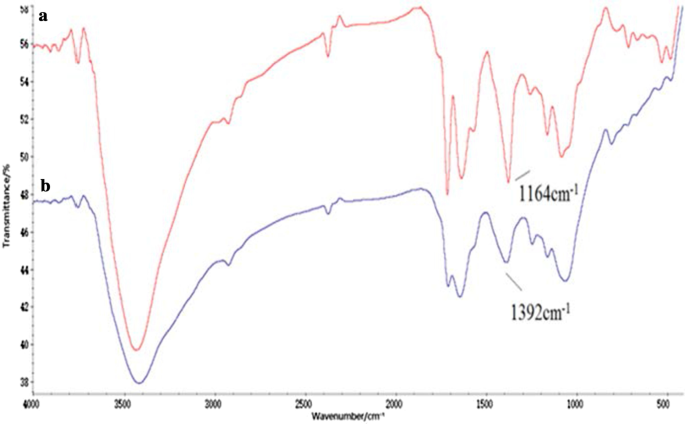
Espectro FT-IR de Tau-GO ( a ) e 5-FU-Tau-GO ( b )
Os espectros de absorção GO UV-Vis são mostrados na Fig. 3. O pico de absorção óbvio em 234 nm foi atribuído à transição π – π * das ligações C =C do grafeno. Além disso, o pico de ombro de 300 nm foi atribuído à transição n – π * das ligações de óxido de grafeno C =O no grupo carboxila ou carbonila. Os dois picos de absorção característicos provaram ser preparações bem-sucedidas de GO.
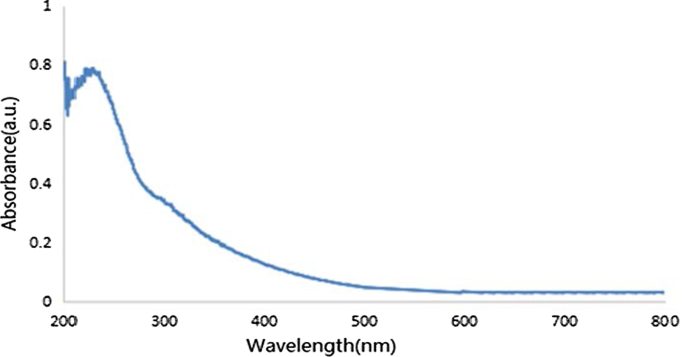
Espectro UV de GO
O tamanho de GO, Tau-GO e 5-FU-Tau-GO são mostrados na Fig. 4. O potencial zeta de GO, Tau-GO e 5-FU-Tau-GO são mostrados na Fig. 5. O tamanho de as folhas GO eram de aproximadamente 221 nm e o valor de PDI era de aproximadamente 0,188, indicando que o GO preparado tem uma distribuição uniforme e boa estabilidade. O potencial zeta era de aproximadamente - 33,3 mV, indicando que a carga negativa se deve principalmente à presença de muitos grupos contendo oxigênio na superfície. Quando o GO foi modificado com Tau via ligação amida, os grupos amino substituíram alguns dos grupos carboxila e o –SO 3 tinha uma capacidade de ionização mais forte em solução, o potencial zeta diminuiu e tornou-se - 38,8 mV. O tamanho e os valores de PDI de Tau-GO foram de aproximadamente 242 nm e 0,190. Em seguida, 5-FU foi carregado no Tau-GO por uma ligação não covalente. O potencial zeta era de aproximadamente - 26,7 mV e o valor absoluto era superior a 20 mV. Além disso, o tamanho e os valores de PDI de 5-FU-Tau-GO foram de aproximadamente 264 nm e 0,182, isso indica que a repulsão eletrostática entre as partículas é grande, o que não é fácil de causar agregação ou precipitação, e que Tau tem boa solubilidade em água , GO também tem boa solubilidade em água porque sua superfície é modificada por grupos funcionais contendo oxigênio. O uso do transportador Tau-GO para carregar 5-FU melhora significativamente a solubilidade de 5-FU em água, de modo que 5-FU-Tau-GO pode ser disperso de forma estável em solução aquosa.
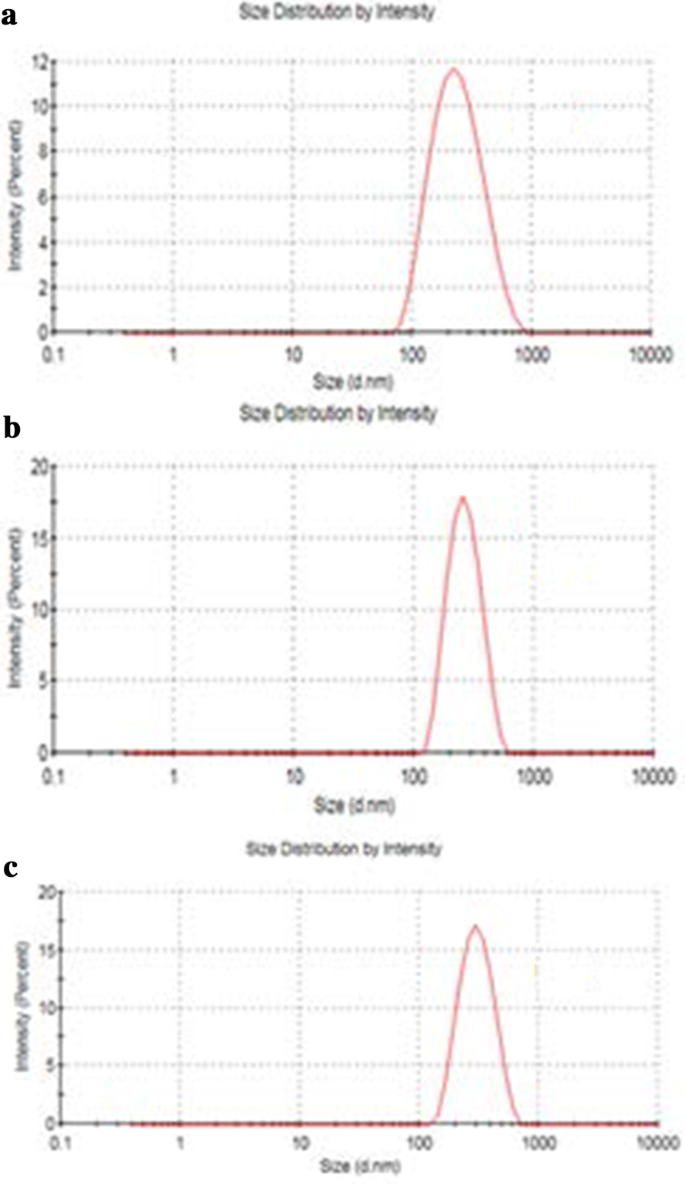
Tamanho de partícula de GO ( a ), Tau-GO ( b ), e 5-FU-Tau-GO ( c )
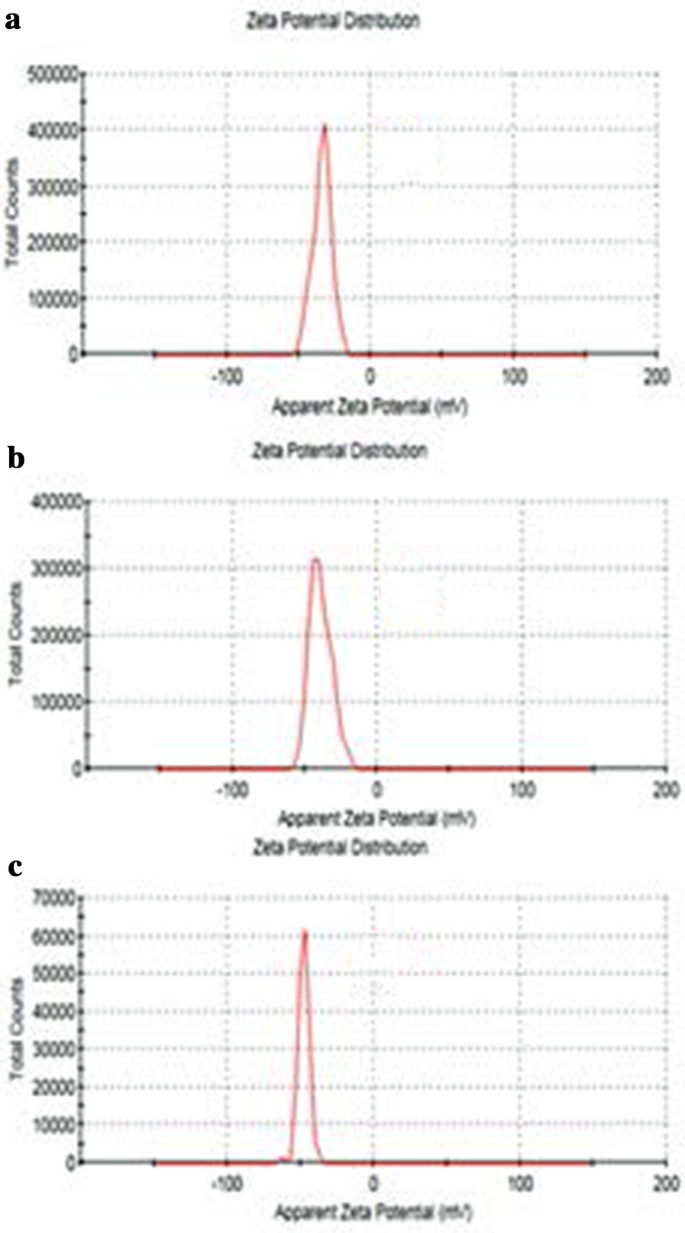
Potenciais Zeta de GO ( a ), Tau-GO ( b ), e 5-FU-Tau-GO ( c )
As morfologias de GO, Tau-GO e 5-FU-Tau-GO foram caracterizadas por TEM (Fig. 6). O GO é uma estrutura plana com rugas na superfície, ilustrando que se trata de uma estrutura bidimensional plana (Fig. 6a). Comparado com GO, o tamanho do Tau-GO foi ligeiramente aumentado, mas ainda mostrou uma estrutura lamelar (Fig. 6b). A imagem 5-FU-Tau-GO mostrou que os materiais não se agregaram ou mudaram com a estrutura lamelar inicial do GO permanecendo intacta (Fig. 6c). Conseqüentemente, Tau-GO e 5-FU-Tau-GO tiveram uma boa estabilidade.

TEM de GO ( a ), Tau-GO ( b ) e 5-FU-Tau-GO ( c )
A análise termogravimétrica foi utilizada para quantificar as composições dos compósitos. As curvas TGA de GO e Tau-GO são mostradas na Fig. 7. GO e Tau-GO têm massas remanescentes de 39,73% e 34,22% em uma atmosfera de nitrogênio de 800 ° C. Portanto, ao comparar os valores de mudança de peso, o conteúdo de Tau no Tau-GO foi determinado em aproximadamente 13%.
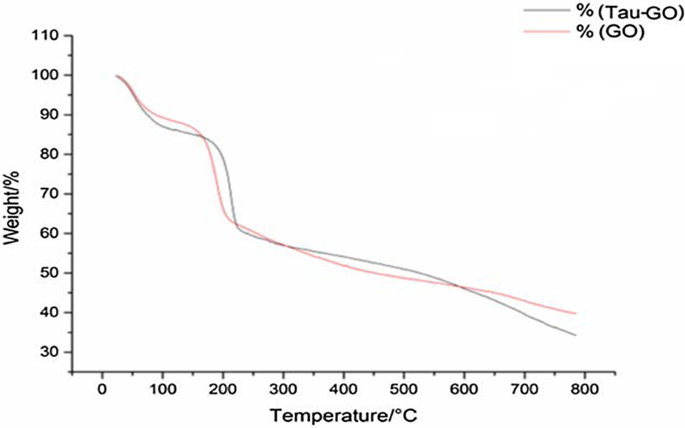
TAG de GO e Tau-GO
Os padrões de XRD de Tau, GO e Tau-GO são mostrados na Fig. 8. O pico característico de GO pode ser observado a 10,7 ° do valor 2θ, o que confirma a formação de GO com oxidação completa para forte oxidação química e processo de esfoliação . Após funcionalizado com Tau na superfície GO, o padrão de difração do pico diminuiu ligeiramente no valor 2θ de 8,2. Isso significa que o GO foi funcionalizado com sucesso por Tau.
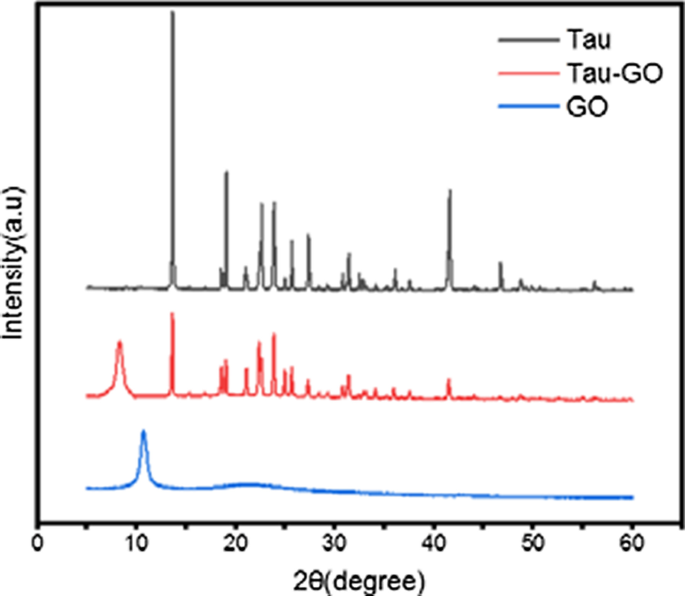
Padrões de XRD de Tau, Tau-GO e GO
Os espectros C1s XPS do GO e Tau-GO são apresentados na Fig. 9. Os espectros C1s XPS do GO indicam que existe um considerável grau de oxidação, com a presença de quatro átomos de carbono correspondentes a diferentes grupos funcionais. Os espectros C1s XPS de Tau-GO também exibem esses mesmos átomos de carbono. Além disso, o aparecimento de picos de componentes relacionados à ligação C – N foram atribuídos aos grupos amino, grupos amida. Esses resultados também indicam que o GO é funcionalizado com sucesso por Tau.
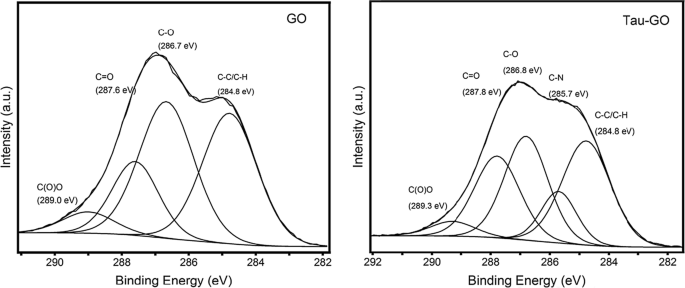
Padrões C1s XPS de GO e Tau-GO
Carregamento de drogas e comportamentos de liberação
O 5-FU foi adsorvido no nanocarreador Tau-GO por meio de interações não covalentes. A curva de calibração de 5-FU era y =62,135 x + 21.873 ( r =0,9999), e a faixa foi de 6,5 ~ 250 µg / mL. A taxa de encapsulação (EE) e a eficiência de carregamento de droga (LE) foram determinadas por concentrações de droga não ligadas para avaliar o desempenho de carga de droga. Os resultados mostraram que o EE aumentou com o aumento da concentração do fármaco e que o maior valor de EE foi de 83,2%. De acordo com a fórmula, o LE foi de 33,7%, ou seja, 508,52 μg de 5-FU podem ser adsorvidos em 1 mg de Tau-GO. Portanto, Tau-GO é um portador de drogas promissor que pode atingir uma grande carga de drogas. Os possíveis mecanismos da alta capacidade de carga de 5-FU no Tau-GO podem ser resumidos pelas seguintes explicações:em primeiro lugar, Tau é usado para funcionalizar GO e introduzir grupos funcionais ativos (–SO 3 ) –SO 3 possui forte capacidade de ionização na solução, o que reduz a aglomeração entre GO e facilita o carregamento de 5-FU no Tau-GO. Em segundo lugar, o potencial Zeta de 5-FU-Tau-GO é 12,1 mV diferente daquele do Tau-GO, o que indica que 5-FU é carregado na superfície do Tau-GO, e a interação eletrostática desempenha um papel importante no carregamento de 5-FU. Por último, existem muitas formas de ligações de hidrogênio entre 5-FU e o portador Tau-GO, incluindo –COOH em Tau-GO e –NH– em 5-FU, –COOH em Tau-GO e-em 5-FU C =O , –OH em Tau-GO e –NH– em 5-FU, –OH em Tau-GO e –C =O em 5-FU, –COOH e 5-FU em Tau-GO –F em Tau-GO, - COOH em Tau-GO e –F em 5-FU, essas ligações de hidrogênio tornam o 5-FU-Tau-GO estável em solução.
A liberação cumulativa in vitro de 5-FU do 5-FU-Tau-GO, na temperatura de 37 ° C em solução de pH 1,2, 6,5 e 7,4 PBS (simular ambiente gástrico, ambiente de células de câncer de fígado e ambiente fisiológico, respectivamente) é mostrado na Fig. 10. Verificou-se que o comportamento do 5-FU liberado foi afetado pelo valor de pH do ambiente. Em um tampão de pH 7,4, a liberação do fármaco foi lenta e contínua, e a quantidade total liberada do fármaco foi de aproximadamente 70,84% após 72 h. Em contraste, a quantidade liberada de fármaco em pH 7,4 foi significativamente menor do que em pH 1,2 e pH 6,5 no mesmo ponto de tempo. A carga total de droga que foi liberada do 5-FU-Tau-GO pode ser alcançada em aproximadamente 90,29% e 85,75% e em pH 1,2 e pH 6,5, respectivamente. Pode ser atribuído às interações π-π e ligações de hidrogênio entre 5-FU e Tau-GO. Quanto mais baixo for o valor do pH, maior será o grau de protonação da ligação de hidrogênio. Portanto, a força da ligação de hidrogênio foi controlada pelo valor do pH, o que levou à liberação de 5-FU. Este sistema de entrega de drogas sensível ao pH desempenha um papel importante em drogas antitumorais e pode alcançar a liberação das drogas na célula tumoral.
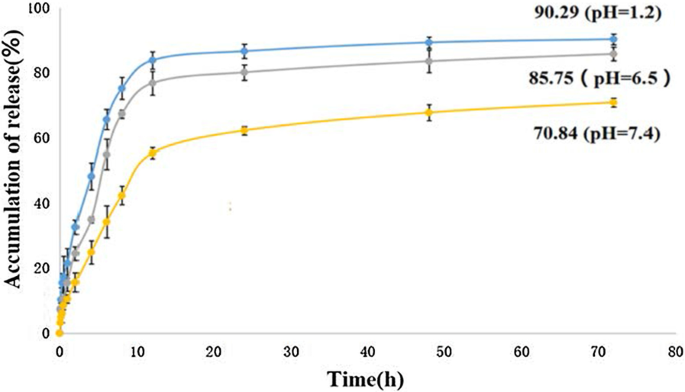
Curvas de liberação in vitro de 5-FU-Tau-GO em solução salina de fosfato a 37 ° C
Estudos de citotoxicidade in vitro
Para avaliar a toxicidade potencial e a eficácia da terapia tumoral do nanocarreador, a viabilidade celular in vitro foi realizada em células HepG2 usando ensaios de MTT (Fig. 11). O Tau-GO não apresentou citotoxicidade significativa em diferentes concentrações. Após o carregamento de 5-FU, o 5-FU-Tau-GO mostrou um efeito de inibição óbvio e, de maneira dependente da dose, portanto, o nanocarreador tinha a capacidade de entregar drogas antitumorais. O IC 50 o valor de 5-FU-Tau-GO foi 65,2 ± 0,7 μg / mL, que foi mais tóxico do que o 5-FU livre (196 ± 8,73 μg / mL). Isso pode ser devido à capacidade da taurina de induzir apoptose em células tumorais, aumentando indiretamente o efeito inibitório de 5-FU nas células. Além disso, pode ser observado a partir do experimento de liberação in vitro que o 5-FU carregado no Tau-GO pode ser liberado gradualmente nas células. Portanto, o tempo efetivo de 5-FU-Tau-GO nas células foi maior do que o de 5-FU livre e, portanto, produziu uma melhor inibição.
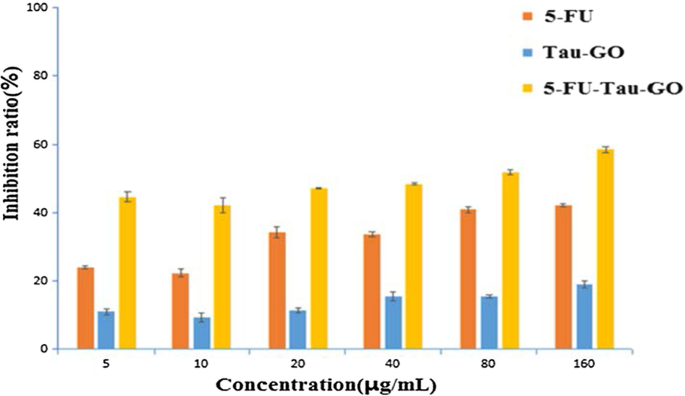
The viability of different concentrations of 5-FU, Tau-GO, and 5-FU-Tau-GO
AO fluorescent agent could emit green fluorescence when it passed through intact cell membranes and stained nuclei, while EB only marked the nucleus of damaged cells that emitted a red/orange fluorescence. The cells with early and late apoptosis presented greenish yellow or orange nuclei with the AO/EB stain, respectively. Therefore, AO/EB staining was performed to investigate whether the cells death was associated with apoptosis using characteristics of cell morphological changes. The results obtained from the AO/EB staining are presented in Fig. 12. Control cells were in spindle shape and with green nuclei. In the cell group that was cultured with Tau-GO alone, small parts of the nuclei were invaginated and with dark green or orange-red staining. Significant orange or red apoptotic cells with chromatin fragments and apoptotic bodies were observed in the 5-FU alone group. Compared with 5-FU, 5-FU-Tau-GO caused more damage to HepG2 cell morphology, which not only broke the cells, but also caused a large amount of apoptosis in cancer cells. As can be seen from the pictures, almost all the cells that were treated with 5-FU-Tau-GO, had morphological changes, a large number of cell debris and apoptotic bodies, indicating that the 5-FU-Tau-GO nano drug delivery system had a good killing effect on HepG2 cells.
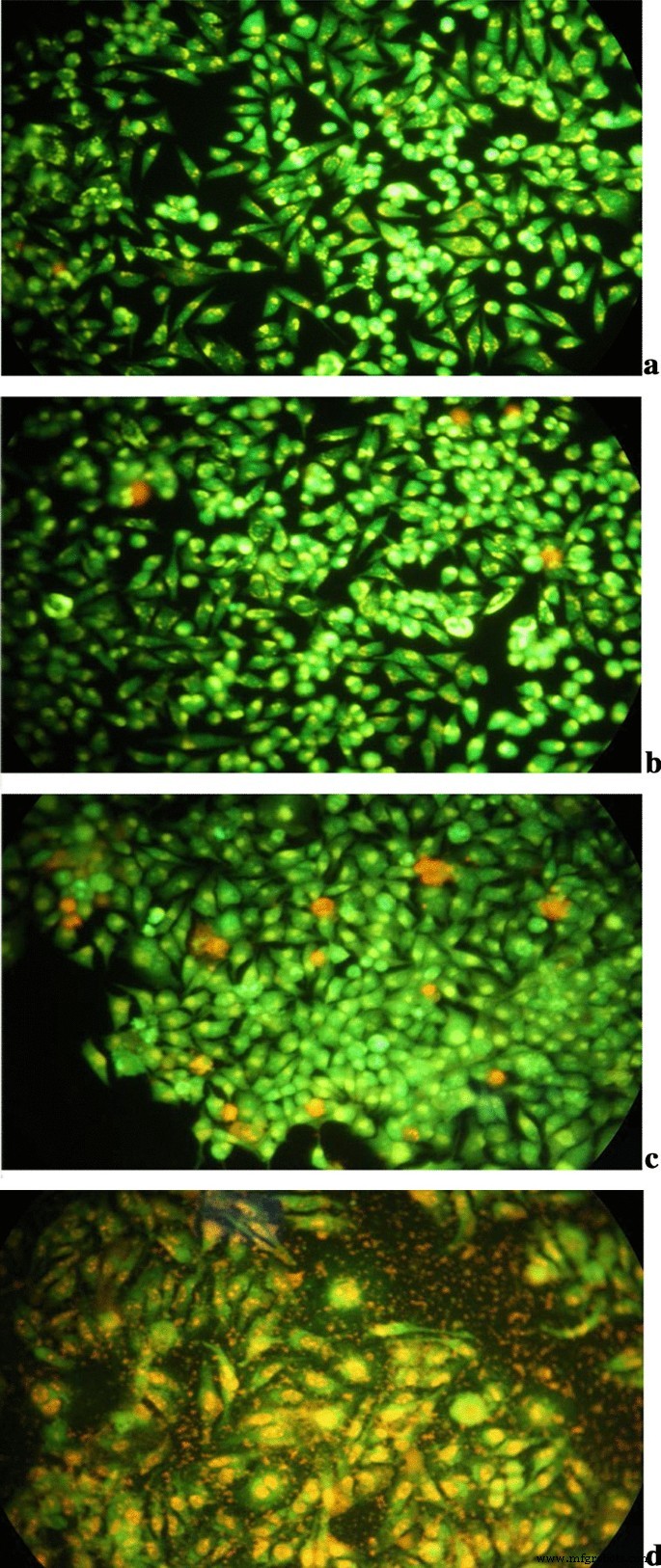
The AO/EB of control (a ), Tau-GO (b ), 5-FU (c ), and 5-FU-Tau-GO (d )
Pharmacokinetic Studies
The pharmacokinetic studies of 5-FU and 5-FU-Tau-GO were performed in SD rats. The profiles of 5-FU concentration in plasma vs. time, following oral administration, are presented in Fig. 13a. We found that the tendency of the two curves was similar, but the 5-FU plasma concentration from the 5-FU-Tau-GO nanocarrier was higher than that from the 5-FU alone and this was observed at each measured time point. Figure 13b shows the 5-FU in vivo release profiles via tail vein. The 5-FU-Tau-GO could achieve sustained drug release over 24 h, and the drug concentration gradually decreased in the first few hours, indicating that 5-FU was slowly released.
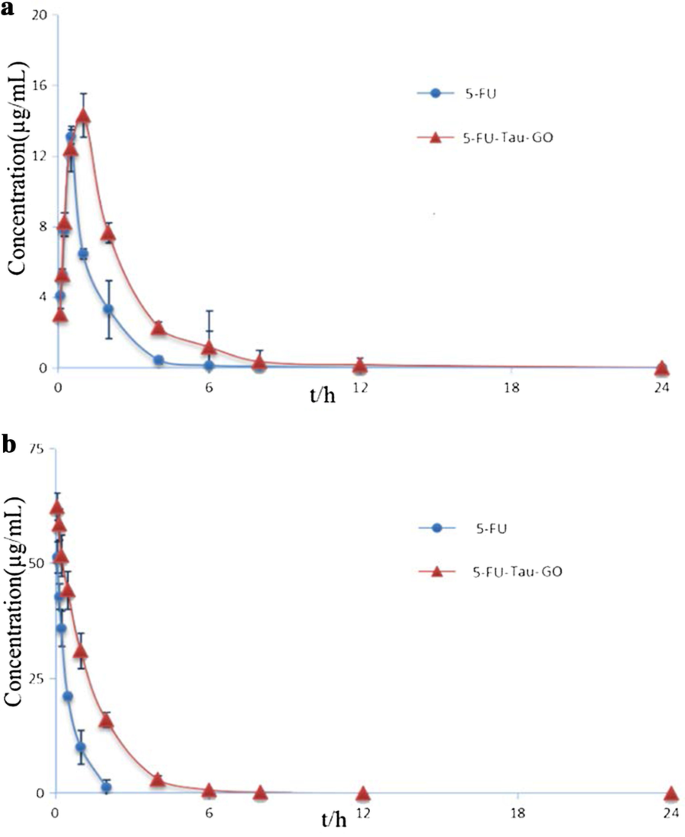
In vivo pharmacokinetic standard curves of 5-FU and 5-FU-Tau-GO through oral administration (a ) In vivo pharmacokinetic standard curve of 5-FU and 5-FU-Tau-GO through intravenous injection (b )
The two-compartment model was used to analyze the pharmacokinetic parameters of oral or intravenous administration in rats. The pharmacokinetic parameters are presented in Table 1. Compared with the 5-FU, the 5-FU-Tau-GO showed higher T1/2β that were 2.3 times by oral administration, and 3.0 times by intravenous injection, respectively. Moreover, the area under the concentration time curve (AUC0−t ) of 5-FU-Tau-GO nanocomplexes was roughy 2.1-fold higher through the oral administration, and 2.8-fold higher through intravenous injection when compared to that of the 5-FU solution, respectively. Therefore, we concluded that 5-FU-Tau-GO could significantly extend 5-FU retention time in vivo and improve bioavailability. In addition, the T1/2β of the 5-FU-Tau-GO nanocomplexes that were orally administered (1.67 ± 1.15 h), was longer than that of the intravenous injection (1.33 ± 0.64 h); however, the AUC0−t of oral administration (36.02 ± 1.83 mg/L*h) was lower than that of intravenous injection (96.50 ± 8.70 mg/L*h). These results might be due to two aspects:on the one hand, when administered by intravenous injection, the drug directly enters the blood system for circulation and without passing through the gastrointestinal barrier for redistribution; on the other hand, because 5-FU easily causes a certain damage to the gastrointestinal system, it may also affect the effective use of drugs in the body.
MD Simulations
The docking and molecular dynamics of unmodified GO, Tau-GO and 5-FU were simulated by molecular docking and molecular dynamics simulation. The molecular docking results of GO, Tau-GO and 5-FU are shown in Fig. 14, where it can be seen that the bond lengths of 5-FU and GO and Tau-GO are 3.66 Å and 2. 602 Å, respectively. Moreover, from the calculation results, the binding energies of 5-FU to GO and Tau-GO were 47.69 kcal/mol and 25.04 kcal/mol, respectively. These indicated that the binding force of Tau-GO and 5-FU was stronger than that of GO and 5-FU. This is due to Tau polar atoms, such as S and N, forming a stronger non-covalent bond with 5-FU, that makes the force between Tau-GO and 5-FU stronger.
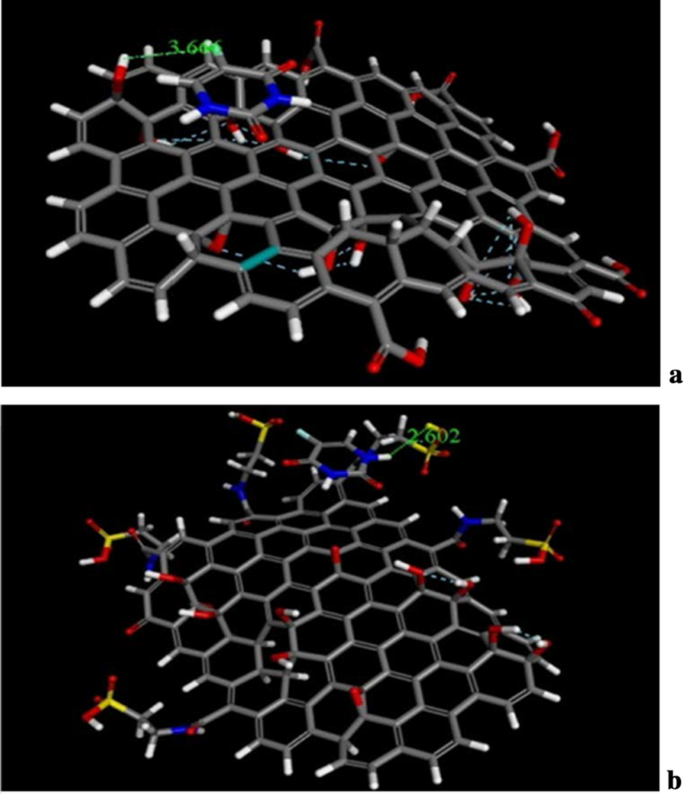
The Molecular docking of GO sheets with 5-FU (a ) The molecular docking of Tau-GO with 5-FU (b )
The diagrams of the molecular dynamics simulation of GO, Tau-GO and 5-FU were shown in Fig. 15. According to the calculation results, the CED of 5-FU-GO and 5-FU-Tau-GO were 2.67*10 8 and 2.83*10 8 , respectivamente. These results showed a stronger interaction between the drug and the Tau-GO. The graphs between MSD and time were plotted (Fig. 16) to obtain the diffusion coefficient via MSD. The drug diffusion coefficients were obtained by the slope divided by 6 as follows:0.094m 2 /s and 0.058 m 2 /s. These show that the force between Tau-GO and 5-FU is stronger, which is consistent with the results of the molecular docking. Therefore, the functionalized GO makes the entire carrier more abundant in atoms and groups; Therefore, making the non-covalent bond with 5-FU stronger, and the entire system more stable.
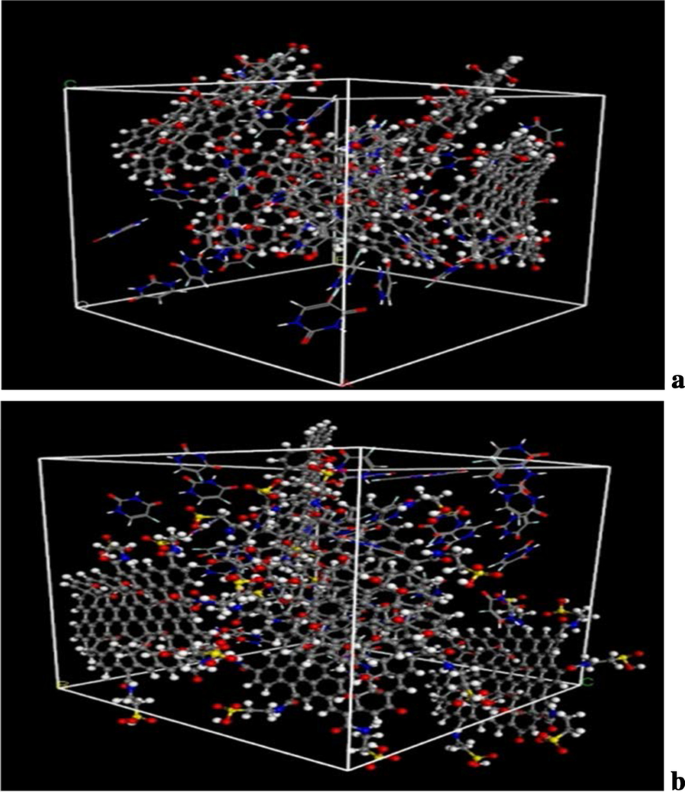
Snapshots of the GO and 5-FU at the end of the MD (a ) Snapshots of the Tau-GO and 5-FU at the end of the MD (b )
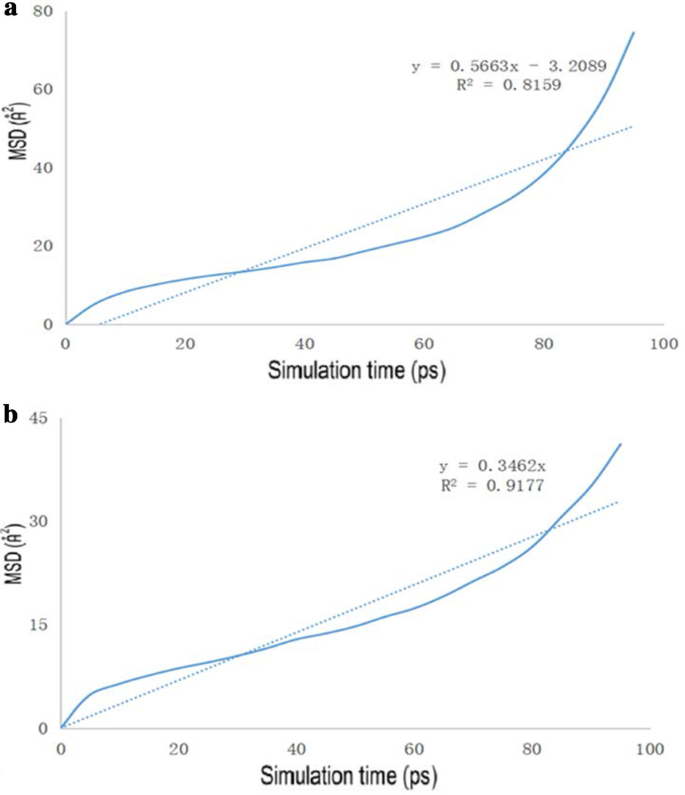
The drug MSD profiles of the GO and 5-FU (a ), Tau-GO and 5-FU (b )
Conclusões
In summary, we successfully prepared a Tau-GO nanocomposite through a simple chemical method. GO functionalization with Tau has a good stability and improves its biocompatibility. The unique structure and brilliant properties of Tau-GO nanocarriers offer great opportunities for the loading and delivery of 5-FU. The 5-FU-Tau-GO has a potential anti-tumor ability and an excellent circulation time of drugs. Therefore, we believe that the modification of GO by the carrier Tau for 5-FU loading, is an effective and applicable tool for constructing a 5-FU-Tau-GO nano drug delivery system for the delivery of anticancer drugs and anti-tumor therapy.
Disponibilidade de dados e materiais
Os conjuntos de dados usados e / ou analisados durante o estudo atual estão disponíveis junto ao autor correspondente, mediante solicitação razoável.
Abreviações
- GO:
-
Óxido de grafeno
- Tau:
-
Taurina
- 5-FU:
-
5-fluorouracil
- 5-FU-Tau-GO:
-
Taurine functionalized graphene oxide loading 5-fluorouracil
- EE:
-
Encapsulation ratio
- LE:
-
Drug-loading efficiency
- FT-IR:
-
Transformada de Fourier Infra-vermelho
- TEM:
-
Microscopia eletrônica de transmissão
- TGA:
-
Thermogravimetric analyses
- MSD:
-
Mean square displacement
- CED:
-
Cohesive energy density
Nanomateriais
- Nanofibras e filamentos para entrega aprimorada de drogas
- Nanopartículas de FePO4 biocompatíveis:entrega de drogas, estabilização de RNA e atividade funcional
- Nanotubos de titanato Nanocompósitos de óxido de grafeno decorado:Preparação, Retardância de Chama e Fotodegradação
- Biossegurança e capacidade antibacteriana do grafeno e do óxido de grafeno in vitro e in vivo
- RGO e redes de grafeno tridimensionais TIMs co-modificados com alto desempenho
- Mecanismo de condução e resistência aprimorada em RRAM baseado em HfO2 com tratamento de nitridação
- Fabricação, Caracterização e Atividade Biológica de Sistemas de Nanotransmissão de Avermectina com Diferentes Tamanhos de Partículas
- Avaliação de estruturas de grafeno / WO3 e grafeno / CeO x como eletrodos para aplicações de supercapacitor
- Aerogel de Grafeno / Polianilina com Superelasticidade e Alta Capacitância como Eletrodo de Supercapacitor Altamente Tolerante à Compressão
- Fabricação e caracterização de Nano-Clips de ZnO pelo processo mediado por poliol



