Influência do parâmetro de ajuste de pH para modificação de sol-gel na estrutura, microestrutura e propriedades magnéticas da ferrita de estrôncio nanocristalina
Resumo
Síntese de ferrita de estrôncio nanocristalina (SrFe 12 O 19 ) via sol-gel é sensível aos seus parâmetros de modificação. Portanto, neste estudo, uma tentativa de regular o pH como um parâmetro de modificação sol-gel durante a preparação de SrFe 12 O 19 nanopartículas sinterizadas a uma temperatura de sinterização baixa de 900 ° C. A relação de variação de pH (pH 0 a 8) em comportamentos estruturais, microestruturais e magnéticos de SrFe 12 O 19 nanopartículas foram caracterizadas por difração de raios-X (XRD), microscópio de varredura por emissão de campo (FESEM) e magnetômetro de amostra vibrante (VSM). A variação do pH do precursor exibiu um forte efeito na densidade sinterizada, estrutura cristalina e propriedades magnéticas do SrFe 12 O 19 nanopartículas. Como o pH é 0, o SrFe 12 O 19 produziu densidade relativamente maior, magnetização de saturação, M s , e coercividade, H c , a uma temperatura de sinterização baixa de 900 ° C. O tamanho do grão de SrFe 12 O 19 é obtido no intervalo de 73,6 a 133,3 nm. A porosidade da amostra afetou a densidade e as propriedades magnéticas do SrFe 12 O 19 ferrite. É sugerido que o SrFe 12 sinterizado a baixa temperatura O 19 em pH 0 exibido M s de 44,19 emu / ge H c de 6403,6 Oe, possuindo um potencial significativo para aplicação em ímã permanente de cerâmica co-queimada em baixa temperatura.
Destaque
-
Síntese de ferrita de estrôncio (SrFe 12 O 19 ) nanopartículas usando a técnica de autocombustão sol-gel.
-
O SrFe 12 O 19 A fase nanoferrita foi obtida em baixa temperatura de sinterização, 900 ° C.
-
Parâmetro magnético de magnetização de saturação M s , remanescente M r , e coercividade H c diminuir à medida que o pH aumenta.
Histórico
Ferrita de estrôncio (SrFe 12 O 19 ) foi extensivamente estudado quanto às suas aplicações potenciais em dispositivos de microondas, gravação magnética de alta densidade, dispositivos eletrônicos e ímã permanente. Ferritas de ímã permanente são amplamente utilizadas na indústria de manufatura elétrica devido às suas várias vantagens [1] e propriedades impressionantes, como alta resistividade elétrica [2], grande perda de histerese e alta coercividade intrínseca [3]. É mais conhecido como uma boa resistência ao calor e resistência à corrosão e útil para muitas aplicações. A ferrita de estrôncio tem atraído mais estudos científicos nos últimos anos devido à sua alta anisotropia magnética, que é responsável pela alta coercividade da estrutura cristalina [4, 5] e, portanto, pode garantir uma alta coercividade mesmo quando o tamanho das partículas é reduzido a nanoescala com estrutura de domínio único. O ferromagnetismo exibido por SrFe 12 O 19 é atribuído ao Fe 3+ sub-redes de íons presentes na estrutura. Eles são distribuídos em três octaédricos (12 k, 2a, 4f 2 ), um tetraédrico (4f 1 ), e um local bipiramidal (2b). Destes locais, 12 k, 2a e 2b são representados como os estados de rotação alta e 4f 1 e 4f 2 são considerados como os estados de spin baixo [6, 7]. Os momentos magnéticos do Fe 3+ íons são acoplados uns aos outros por interações de supertroca mediadas por O 2− íons. O Sr. 2+ íon é responsável pela grande anisotropia magnética uniaxial, pois causa uma perturbação da rede cristalina [8]. Hexaferrita de estrôncio (SrFe 12 O 19 ) as nanopartículas têm um tamanho médio de partícula inferior a 0,1 μm e são feitas de distribuição de tamanho de partícula homogênea [9]. O tamanho de partícula menor produz uma grande área de superfície, aumentando significativamente o SrFe 12 O 19 Propriedades das nanopartículas, como suas propriedades químicas, físicas, mecânicas e magnéticas, resultando em propriedades interessantes para aplicações de nanoferrita.
O método convencional de cerâmica de estado sólido é difícil na obtenção de nanopartículas e partículas de tamanho único [4, 5]. Ele tem limitações, como longa programação de aquecimento em alta temperatura de sinterização de cerca de 1300 ° C, maior tamanho de grão / partícula obtido e maior consumo de tempo. As condições experimentais envolvidas na fabricação das nanopartículas de ferrita desempenham um papel fundamental nas propriedades resultantes, bem como no tamanho das partículas das nanopartículas de ferrita. A fim de alcançar SrFe altamente homogêneo 12 O 19 nanopartículas consistindo de uma estrutura de domínio único em baixa temperatura de sinterização ou calcinação, vários métodos foram introduzidos para que uma ampla distribuição de tamanho de grão com crescimento anomólico de grão promovido durante a sinterização pudesse ser evitado. Os métodos incluem co-precipitação [9, 10], método de fusão de sal [11], hidrotermal [12, 13], microemulsão [14] e processo sol-gel [1, 4, 15]. Dentre esses métodos, a rota sol-gel é um método de baixo custo, simples e confiável para controlar a estequiometria e produzir ferrita nanocristalina. O processo sol-gel produz um óxido misto homogêneo que pode diminuir a temperatura de calcinação e produzir um tamanho de cristalito menor [3]. Otimizar a razão molar de Fe para Sr (Fe / Sr) é muito importante para produzir uma amostra monofásica, partícula ultrafina e menores temperaturas de calcinação [1]. Esta proporção varia com a mudança nas matérias-primas e com a mudança no método de produção [1]. Em alta temperatura de calcinação, tanto o tamanho do grão quanto o acoplamento de troca aumentam. Estes serão desfavoráveis para a obtenção de um ímã permanente de boa qualidade [16]. Em geral, os alcóxidos metálicos são freqüentemente usados como matérias-primas no processo sol-gel, mas muitos dos alcóxidos são muito difíceis de serem obtidos e tratados devido à alta sensibilidade à umidade atmosférica. Além disso, não é fácil controlar a taxa de hidrólise do alcóxido quando cerâmicas multicomponentes devem ser preparadas. Sais metálicos são empregados neste estudo por serem muito úteis, baratos e fáceis de manusear. Além disso, os sais metálicos podem ser dissolvidos em muitos tipos de solventes orgânicos, formando complexos metálicos pela quelação dos íons metálicos com ligantes orgânicos [17]. Vários processos de modificação de sol-gel foram relatados, como ajuste de pH [1, 18], agente básico [3], surfactante [1], ácido carboxílico [2] e sais de metal de partida [3], para reduzir o temperatura final de calcinação, tamanho do cristalito [2] e alta anisotropia de SrFe 12 O 19 nanopartículas [12]. Nos métodos sol-gel, a capacidade de formar hidróxidos e / ou óxidos depende fortemente do pH da solução e da razão carga / raio do cátion metálico [17]. Além disso, o pH do sol controla a quantidade de H + ou OH - íons no sol que efetivamente determinam a polimerização das ligações metal-oxigênio. Além disso, sabe-se que durante o processo sol-gel, o processo de complexação com ácido cítrico é sensível aos valores de pH [19, 20]. Portanto, a homogeneidade do sol que é essencial para a formação da fase seria determinada pelo pH da solução. É bem conhecido que as propriedades magnéticas de SrFe 12 O 19 são fortemente dependentes de sua morfologia, tamanho de partícula / grão, forma, orientação e configurações de domínio, modificando os parâmetros de síntese. Portanto, neste trabalho, pretendemos regular o pH da solução como um parâmetro de modificação sol-gel para produzir ferrita nanocristalina com valores consideráveis de propriedades magnéticas em uma temperatura de calcinação mais baixa.
Métodos
As sequências experimentais deste estudo consistiram em duas etapas principais que foram a síntese de nanopartículas de ferrita de estrôncio através do método sol-gel (a seção "Síntese de Nanopartículas de Ferrita de Estrôncio") e foram seguidas pelas caracterizações de propriedades estruturais, microestruturais e magnéticas de ferrita de estrôncio preparada (seção “Caracterizações da ferrita de estrôncio”).
Síntese de nanopartículas de ferrita de estrôncio
Nanopartículas de ferrita de estrôncio foram sintetizadas por meio do método sol-gel. Neste método, nitrato de estrôncio anidro Sr granular (NO 3 ) 2 (98%, Alfa Aeser), nitrato de ferro (III) Fe (NO 3 ) 3 (99%, HmbG), ácido cítrico C 3 H 4 (OH) (COOH) 3 (99%, Alfa Aeser), amônia NH 4 OH (25%, SYSTERM) e água desionizada foram usados como materiais de partida para a preparação da amostra. Quantidades apropriadas de Sr (NO 3 ) 2 e Fe (NÃO 3 ) 3 são dissolvidos em 100 ml de água desionizada durante alguns minutos a 60 ° C com uma rotação do agitador constante de 250 rpm para preparar uma solução aquosa. O ácido cítrico foi adicionado como um agente quelante com razão molar de citrato para nitrato (C / N =0,75), e a temperatura foi elevada para 80 ° C. As misturas foram continuamente agitadas e NH 4 OH foi adicionado a fim de variar o pH de pH 0 a pH 8. O pH foi medido por medidor de pH / ORP HI2211 (instrumentos HANNA). As soluções foram continuamente agitadas e aquecidas durante várias horas a 90 ° C, e a solução transformou-se lentamente em um gel pegajoso verde. Após a formação de um gel denso e pegajoso, a temperatura da placa quente é então aumentada até 200 ° C e os géis são queimados por uma hora para o processo de desidratação. Os pós obtidos foram calcinados a 900 ° C por 6 h com taxa de aquecimento de 5 ° C / min. Uma descrição passo a passo do procedimento de síntese de SrFe 12 O 19 nanopartículas é mostrado na Fig. 1.
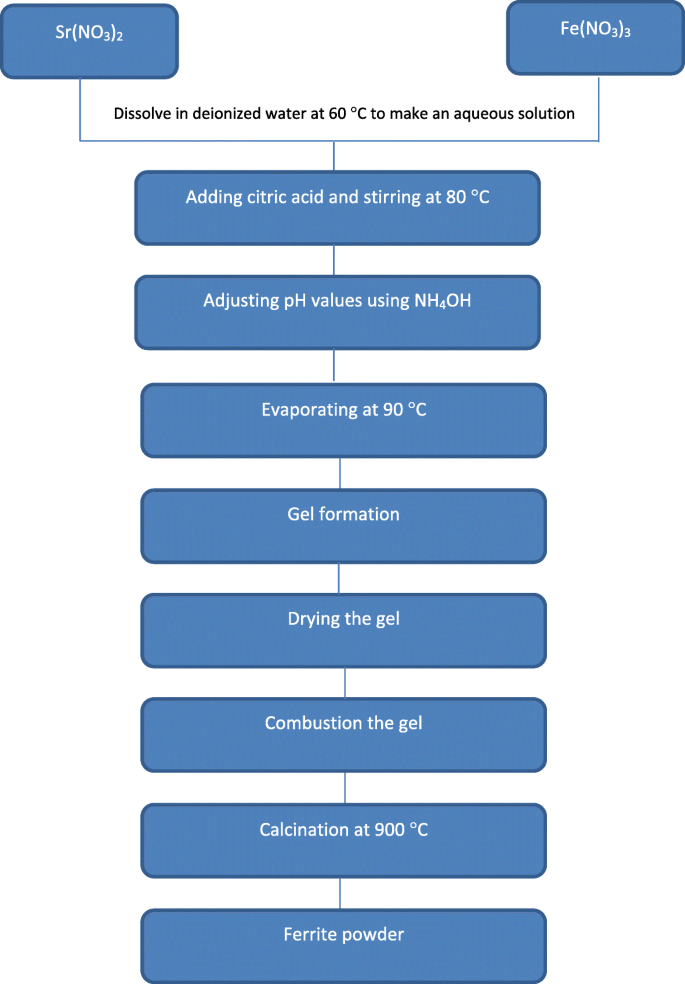
Fluxograma para preparar SrFe 12 O 19 nanopartículas em pó pelo método sol-gel
Caracterizações de ferrita de estrôncio
A medição da caracterização da ferrita de estrôncio foi realizada em termos de suas propriedades estruturais, microestruturais e magnéticas. A explicação detalhada é mostrada nas subseções a seguir.
Propriedades Estruturais
A caracterização estrutural das amostras foi caracterizada pela técnica de difração de raios X (XRD) usando um difratômetro de raios X Philips X’pert modelo 7602 EA Almelo com radiação Cu Kα a 1,5418 Å. A faixa de ângulo de difração usada é de 20 ° a 80 ° em temperatura ambiente. A corrente de aceleração e a tensão de trabalho foram 35 mA e 4,0 kV, respectivamente. Os dados foram analisados usando um software X’Pert High Score Plus.
A caracterização do infravermelho por transformada de Fourier (FTIR) foi realizada por um espectrômetro de infravermelho por transformada de Fourier Perkin Elmer modelo 1650 para determinar o espectro infravermelho das bandas de absorção e emissão da amostra. Foi realizado entre espectros infravermelhos de 280-4000 cm −1 .
Propriedades da microestrutura
A observação microestrutural foi realizada em microscópio eletrônico de varredura por emissão de campo (FESEM) em máquina FEI Nova NanoSEM 230. A distribuição da imagem de tamanho de grão foi fixada em uma ampliação de 100kx com voltagem de aceleração de 5,0 kV. As distribuições de tamanhos de grãos foram obtidas tomando 200 imagens de grãos diferentes para a amostra e estimando os diâmetros médios de grãos individuais usando o software imageJ. A distribuição do tamanho do grão foi medida por um método de interceptação linear média.
Densidade
A densidade foi medida usando um Densitômetro Hildebrand Modelo H-300 S. A densidade do pellet sinterizado foi obtida usando o princípio de Arquimedes com água como meio fluido pela Eq. 1,
$$ {\ rho} _ {\ mathrm {exp}} =\ left (\ frac {W _ {\ mathrm {air}} - {W} _ {\ mathrm {água}}} {W _ {\ mathrm {água} }} \ right) \ times {\ rho} _w $$ (1)
ρ exp é a densidade da amostra medida, ρ w é a densidade da água, W ar é o peso da amostra no ar, e W água é o peso da amostra em água.
Propriedades magnéticas
As propriedades magnéticas das amostras foram medidas por um magnetômetro de amostra vibratória (VSM), modelo 7404 LakeShore. A medição foi realizada à temperatura ambiente. O campo externo de 12 kOe foi aplicado paralelamente à amostra.
Resultados e discussão
Análise Estrutural
A Figura 2 mostra os espectros de difração de raios-X (XRD) de SrFe 12 O 19 nanocristalino variando o pH. A estrutura dos picos de XRD foi referida ao padrão SrFe 12 O 19 com código de referência JCPDS de 98-004-3603. Os picos característicos e índices de miller de SrFe 12 O 19 também são mostrados na figura. A maior intensidade pode ser observada em 2θ (34,218 °) com índices de Miller de [1 1 4]. A formação de SrFe monofásico 12 O 19 foi obtido a uma temperatura de calcinação relativamente baixa de 900 ° C. Não foram observados picos correspondentes a alguns dos precursores do reagente ou outras fases secundárias e produtos intermediários, exceto para a amostra preparada em pH 8 onde uma pequena quantidade de hematita Fe 2 O 3 fase foi detectada e todas as amostras têm uma boa cristalinidade como mostrado na figura. A formação de Fe secundário 2 O 3 fase observada para a amostra preparada em pH 8 reduziu a pureza de SrFe 12 O 19 para 87,8%. The Fe 2 O 3 os padrões foram indexados ao código de referência ICSD 98-004-1067. A presença de Fe 2 O 3 fase é devido à temperatura de calcinação insuficiente para a amostra preparada em pH 8 [21]. Verificou-se que a alta acidez em solução média de pH 0 a 3 favoreceu a formação de SrFe de alta cristalinidade 12 O 19 Estágio. O aumento do pH do sol ajudou na formação de géis de ferro carregados negativamente e na adsorção de íons Sr carregados positivamente em géis de ferro. Consequentemente, uma solução mais homogênea foi obtida, o que resulta na fácil formação de SrFe 12 O 19 fase [3] . Mesmo com a formação de SrFe 12 O 19 é mais fácil com o aumento do pH, agregados cerâmicos heterogêneos podem ser formados devido a mudanças localizadas na vizinhança imediata do complexo em polimerização [22]. Portanto, o crescimento cristalino pode ser inibido, reduzindo a cristalinidade a partir de pH 4. Isso foi mostrado pelo aumento da intensidade do pico de XRD pela melhoria da cristalinidade de SrFe 12 O 19 preparado usando pH 1 a pH 3, no entanto diminuiu lentamente com valores de pH aumentados de 4 para 8. A formação de SrFe cristalino 12 O 19 após ser calcinado a 900 ° C é atribuído ao maior grau de homogeneidade composicional, bem como ao maior calor gerado pela reação exotérmica de nitratos e ácido cítrico [21].
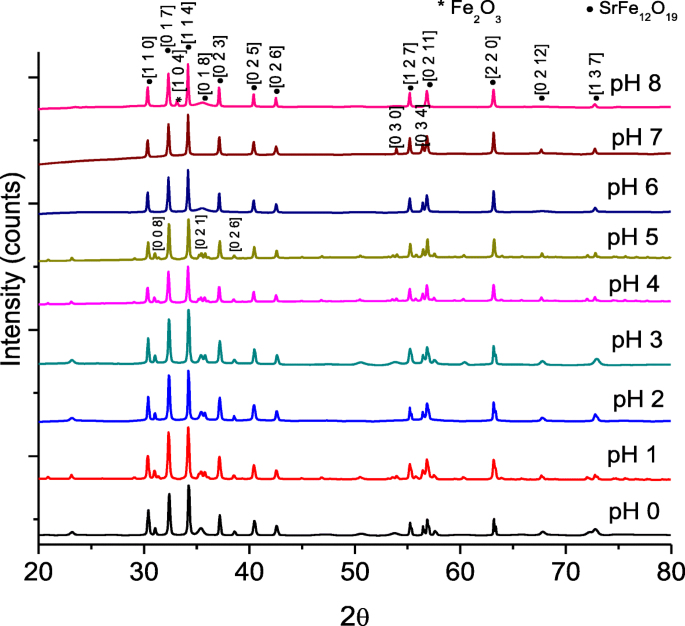
O espectro de difração de raios-X de SrFe 12 O 19 para pH 0 a pH 8, sinterizado a 900 ° C
O parâmetro de rede a e c valor observado não era muito diferente em comparação com o SrFe teórico 12 O 19 constante de rede onde a =5,8820 Å e c =23,0230 Å [23] (Fig. 3). O a e c os parâmetros observados são semelhantes aos de Masoudpanah et al. [3] e Dang et al. [12]. A célula de volume V célula e densidade de XRD ρ xrd usados neste estudo dependem do parâmetro cristalográfico que tem um sistema de cristal hexagonal com grupo espacial de P63 / mmc . O V célula foram calculados usando a Eq. (2);
$$ {V} _ {\ mathrm {cell}} =\ frac {\ sqrt {3}} {2} {a} ^ 2c $$ (2)
onde a e c são a constante de rede. A densidade teórica ρ teoria da amostra foi calculada usando a Eq. (3),
$$ {\ rho} _ {\ mathrm {teoria}} =\ frac {2M} {N_AV} $$ (3)
onde M é o peso molecular de SrFe 12 O 19 que é igual a 1061,765 g. O peso de duas moléculas em uma célula unitária é 2 × 1061,765 =2123,53 g; N A é o número do Avogadro (6.022 × 10 23 mol −1 )
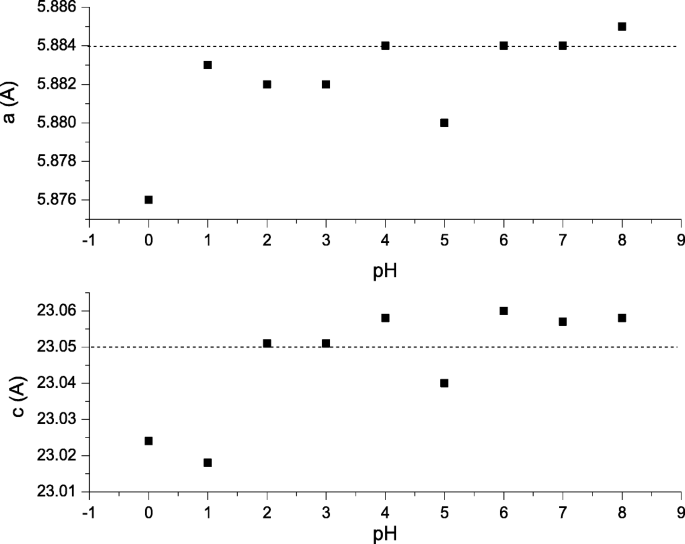
Os parâmetros de rede a e c de SrFe 12 O 19 nanopartículas para pH 0 a pH 8, sinterizadas a 900 ° C. As linhas tracejadas são os valores de referência dos parâmetros de rede a e c
A porosidade P das amostras pode ser calculado usando a Eq. (4);
$$ P =\ left (\ frac {1 - {\ rho} _ {\ mathrm {exp}}} {\ rho _ {\ mathrm {teoria}}} \ right) \ times 100 \% $$ (4)
Conforme o valor do pH aumentou, a densidade experimental das amostras ρ exp foi diminuída, exceto por algumas flutuações observadas para amostras preparadas em pH 4, 6 e 7 com valor ótimo de densidade experimental e menos porosidade obtida para amostra preparada em pH 4. A densidade e porosidade ótimas foram registradas como 4,693 g / cm 3 e 8,15% respectivamente (Fig. 4, Tabela 1). A densidade de raios X mostrada na Tabela 1 é maior do que a densidade experimental, o que pode ser devido à presença de poros criados durante o processo de sinterização. A característica porosa dos aglomerados também é atribuída à liberação de uma grande quantidade de gás, como NH 3 durante o processo de combustão [24].
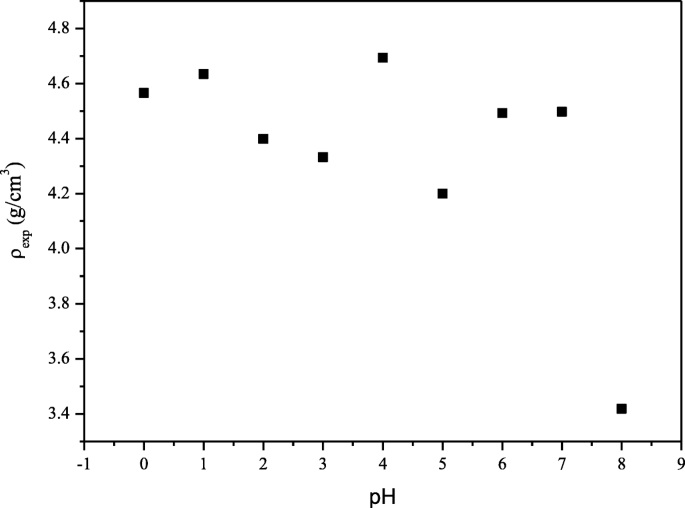
Densidade experimental de SrFe 12 O 19 nanopartículas para pH 0 a pH 8, sinterizadas a 900 ° C
Os espectros de FTIR de SrFe sinterizado 12 O 19 em pH variando de 0 a pH 8 são mostrados na Fig. 5. Os espectros de FTIR de um precursor apareceram visivelmente na faixa de 430, 583, 904 e 1446 cm -1 de bandas características de IR. A banda de absorção em 436 cm −1 foi indicado como uma banda de alongamento de CH 2 , comprovando a presença de composto saturado de CH [25]. Bandas a 583 cm ‑1 mostram a vibração característica do metal de oxigênio Sr – O Fe – O [20]. As bandas de absorção variam de 443–600 cm −1 foram atribuídos à formação de ferrita de estrôncio como vibração de alongamento da ligação metal-oxigênio [26,27,28,29]. Isso confirma que, o SrFe 12 O 19 foi formado a uma temperatura de sinterização de 900 ° C. As bandas relativamente fortes e largas nos picos 904 cm −1 revelou que havia um grupo funcional amina para vibração N – H devido à decomposição de NH 3 . Enquanto isso, Pereira et al. [29] também afirmaram que uma ampla vibração de alongamento de Sr-O indica a formação de nanoferrita de estrôncio. A banda de absorção em 1446 cm −1 indica a vibração das bandas de Fe – O – Fe devido à decomposição do metal com a banda de óxidos [25].
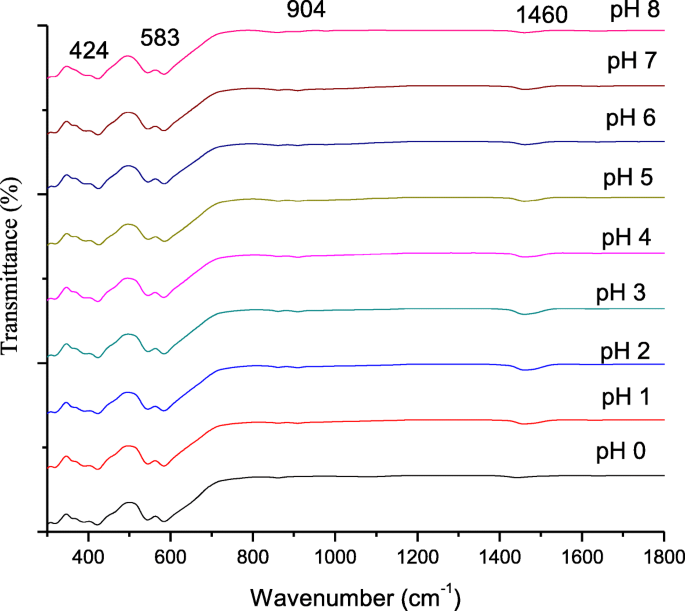
Os espectros de FTIR de SrFe 12 O 19 para pH 0 a pH 8, sinterizado a 900 ° C
Análise microestrutural
As imagens da microestrutura do SrFe em massa 12 O 19 e os espectros de EDX são mostrados na Fig. 6, enquanto as distribuições de tamanho de grão das amostras são mostradas na Fig. 7. Os tamanhos médios de grão foram encontrados na faixa de 73,6 a 133,3 nm. O tamanho médio dos grãos das amostras não apresenta grande variação, exceto para as amostras com pH 4 e pH 8. Os tamanhos dos grãos foram aglomerados com o aumento do valor de pH. Um tamanho de grão relativamente pequeno e empacotado com uma média de 73,6 nm e distribuição de tamanho de grão mais estreita entre todos foi observado para pH 0. O tamanho de grão aumentou com o aumento dos valores de pH de pH 0 para pH 3, diminuiu em pH 4 e aumentou ainda mais até pH 8. Os resultados estão de acordo com os espectros de XRD como mostrado na Fig. 2 que o grau de cristalinidade reduzido para a amostra em pH 4. A partir da Fig. 6e, para a amostra preparada em pH 4, mostra que os grãos não são homogeneamente distribuídos e não uniformemente formados.

As micrografias FESEM de amostras sinterizadas a 900 ° C por variação de pH: a pH 0, b pH 1, c pH 2, d pH 3, e pH 4, f pH 5, g pH 6, h pH 7 e i pH 8
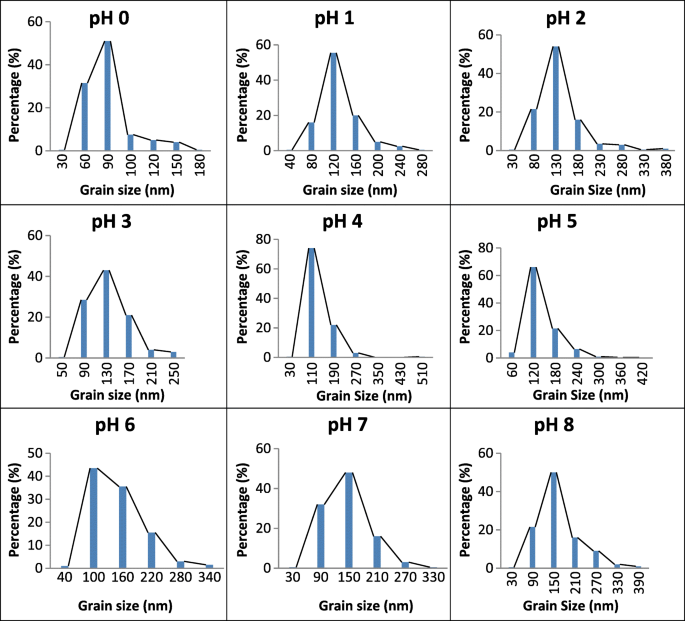
Distribuição de tamanho de grão para SrFe 12 O 19 calcinado a 900 ° C por variação de pH: a pH 0, b pH 1, c pH 2, d pH 3, e pH 4, f pH 5, g pH 6, h pH 7 e i pH 8
O melhor tamanho de grão exibiu maior M s , M r , e H c . Os grãos para amostras com pH 0 eram de forma esférica e em contato com outro grão para formar uma estrutura de estrangulamento. O contato foi evidente com o aumento dos valores de pH, mostrando uma estrutura de grãos mais alongada. As distribuições de tamanho / forma de grão tornaram-se maiores e não uniformes à medida que os valores de pH aumentaram. O histograma da distribuição do tamanho do grão mudou de tamanhos de grão pequenos para exibir tamanhos de grão maiores. O aumento da taxa de combustão e o calor liberado da reação também podem aumentar o tamanho do cristalito [30]. As linhas vermelhas pontilhadas no histograma (Fig. 7) marcaram o tamanho médio do grão da amostra. A microestrutura mostrou que algumas das amostras exibiram grande porosidade devido à presença de álcool polivinílico durante a preparação de SrFe a granel 12 O 19 nanoferrita em pellet, bem como liberação de gás durante o preparo da amostra.
Comportamentos magnéticos
O desenvolvimento de M - H O ciclo de histerese em vários pH é ilustrado na Fig. 8. Uma confirmação adicional desta evolução pode ser vista a partir da variação da magnetização de saturação, M s , remanência, M r , razão de esquadria, M r / M s , e coercividade, H c , em função do pH tabulado na Tabela 1. A magnetização por unidade de massa não está diretamente relacionada à microestrutura da amostra; portanto, a magnetização por unidade de volume foi calculada multiplicando a magnetização por unidade de massa pela densidade experimental, ρ exp . O M s , M r , e H c geralmente diminuem com o aumento do pH pela adição de amônia em um precursor de sol-gel. A diminuição dos parâmetros magnéticos conforme o pH aumenta pode ser devido à existência de grande quantidade de fases diamagnéticas de amônia NH 3 . Parece que o principal efeito do NH diamagnético 3 são para isolar nanopartículas de ferrita Sr umas das outras, reduzindo assim a interação de troca entre elas e são conhecidos por ter um efeito prejudicial sobre M s e M r . Como visto anteriormente na seção “Análise microestrutural”, a microestrutura de SrFe 12 O 19 foi afetado pelo aumento do valor do pH. Isso está de acordo com os achados relatados por Yang et al. [31], onde as partículas se tornaram maiores [32] com o aumento do pH de 5 para 11. As partículas maiores foram altamente afetadas pela forte interação magnética entre átomos magnéticos de Fe nos grãos [33].
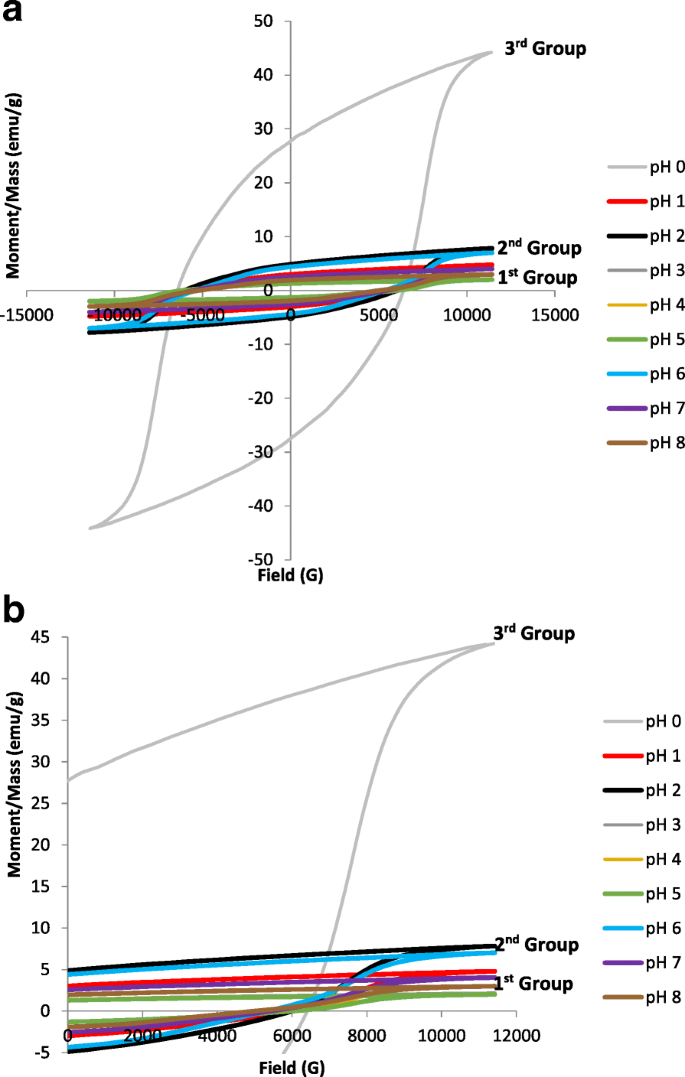
O M - H loops de histerese de SrFe 12 O 19 para a pH 0 a pH 8 e b gráfico de close-up, variando o pH sinterizado a 900 ° C
O M - H Os loops de histerese na Fig. 8 foram examinados, e três grupos significativos de loops de histerese caracterizados pelas formas e valores de grupo diferenciado puderam ser observados. O primeiro grupo consistiu na maioria das amostras preparadas que são amostras preparadas usando pH 1, 3, 4, 5, 7 e 8. Este grupo correspondeu às propriedades ferromagnéticas fracas com baixos valores de M s e M r . Sabe-se que M s é particularmente dependente da cristalinidade da amostra. Isso pode ser visto nas amostras preparadas usando pH 4, 5, 7 e 8, onde a cristalinidade foi reduzida para as amostras, apresentando assim valores mais baixos de M s . Além disso, a presença de 28,2% α-Fe 2 O 3 impureza como fase secundária foi detectada na amostra preparada usando pH 8, reduzindo a cristalinidade da amostra e, consequentemente, reduzindo o M s valor. Mesmo que os espectros de XRD observados na Fig. 2 exibam alto grau de cristalinidade para amostras preparadas usando pH 3, os valores de propriedades magnéticas baixas resultantes podem estar sujeitos a diminuição na densidade (ver Tabela 1) devido à presença de poros, afetando assim o coercividade na amostra. Desde M s está relacionado com H c conforme mostrado na Eq. (5) [34], o M s diminuiu quando o H c aumentou.
$$ {H} _c =\ frac {2 {K} _1} {M_s} $$ (5)
Sabe-se também que a porosidade afeta o processo de magnetização, pois os poros funcionam como um gerador de campo desmagnetizador [35].
É perceptível que pH 2 e pH 6 caíram no segundo grupo em que as amostras apresentam parâmetros de histerese moderados (Fig. 8). As amostras neste grupo exibiram forma semelhante de ciclo de histerese com o primeiro grupo, mas com valores ligeiramente mais elevados de M s e M r . O H c os valores registrados para as amostras preparadas usando pH 2 e pH 6 foram 6005,8 e 5377,0 Oe, respectivamente. O M s valores para pH 2 e pH 6 foram observados como 7,8 emu / g (226,2 emu / cm 3 ) e 7,0 emu / g (35,8 emu / cm 3 ), respectivamente, enquanto o M r os valores para pH 2 e pH 6 foram dados como 4,9 emu / ge 4,4 emu / g, respectivamente. Embora o tamanho de grão maior estivesse presente nas amostras, os valores registrados ainda eram baixos, uma vez que a presença de grãos alongados foi detectada (ver os círculos pontilhados em vermelho na Fig. 6c, g) nas amostras preparadas usando pH 2 e 6. Uma vez que é sabido que a barreira de energia de anisotropia total depende do volume e das densidades de energia de anisotropia de superfície, portanto, para um determinado volume de uma partícula, a área de superfície é mais para partículas de forma alongada. Conseqüentemente, a principal contribuição da superfície para a anisotropia efetiva e um aumento em H c também é esperado em partículas alongadas [36], reduzindo assim o M s .
O terceiro grupo foi detectado em uma única amostra preparada usando pH 0. Uma lacuna significativa foi observada entre o segundo e o terceiro grupos, indicando as propriedades de mudança nas amostras dentro deste grupo, particularmente no M s valores. O ciclo de histerese para pH 0 tem o maior M s , M r , e H c com os valores significativos de 44,19 emu / g (226,2 emu / cm 3 ), 27,59 emu / g e 6403,6 Oe, respectivamente. Geralmente, o M s valores para SrFe 12 O 19 pode variar de 74 a 92 emu / g, que geralmente são medidos na forma de um único cristal [8]. O valor de M s para a amostra preparada usando pH 0 foi relativamente menor do que os valores dados e também com estudos relatados anteriormente que foram 56 emu / g [37] e 53 emu / g [38], ambas as sínteses através do método sol-gel. Espera-se que o valor de M s neste estudo seria aumentado com o aumento adicional das temperaturas de sinterização. No entanto, o H c valor mostrou um valor relativamente maior do que estudos anteriores que foram 5000 Oe [37] e 5200 Oe [38], e de acordo com Pullar [8], nenhum valor preciso é dado para H c pois varia muito com os métodos de processamento e tamanho do grão. Enquanto isso, nenhuma diferença significativa de M r foi visto como foi relatado anteriormente que era de 30 emu / g [38]. Podem ser observados loops de histerese obviamente eretos, maiores e bem definidos. É devido ao forte comportamento ferromagnético, resultante da formação de fração de alto volume do SrFe cristalino completo 12 O 19 fase, como visto na Fig. 2. Assim, uma forte interação de momentos magnéticos dentro dos domínios ocorreu devido às forças de troca. Este fenômeno observado pode ser considerado um magnetismo ordenado na amostra. Na verdade, a fim de obter um magnetismo ordenado e um M bem formado - H loop de histerese, deve existir uma formação de domínio significativa, um campo de anisotropia suficientemente forte, H a , and optional addition contributions which come from defects such as grain boundaries and pores [39]. It is interesting to note that the broad loops in this group means substantial magnetic storage; thus, the samples possess characteristics which may be useful for practical applications [40].
The H c variation in Figs. 9a and 10 should deserve some mention:The H c is observed to generally reduce as pH increased. The decrease in H c with increasing pH can be attributed to decrement of magnetocrystalline anisotropy with anisotropic Fe 2+ ions locating on a 2a site and the enlargement of the grain size and is evident in FESEM micrographs (Fig. 6). Furthermore, at pH 8, the coercivity H c which is 5117.7 Oe was recorded due to the presence of 28.2% α-Fe2 O 3 impurity (Fig. 2). The decrease in H c was due to the presence of impurity α-Fe2 O 3 which affected the crystalline and grain boundary since it has been reported that the H c could be affected by important parameters such as particle size, ion substitution, morphology, interface structure, crystal defects, magnetocrystalline anisotropy, and strain [41]. The squareness ratio, M r /M s , is calculated from the magnetic data and tabulated in Table 1. Generally, a large M r /M s value is preferred in many applications such as magnetic recording media of high density and permanent magnet [42]. The calculated M r /M s in this study was found to be in the range of 0.63 to 0.65, indicating that all the samples are predominantly in single magnetic domain structure [43]. M r /M s equal to or above 0.5 indicates that the particles are in the single magnetic domain and below 0.5 may be attributed to the formation of multidomain structure [43, 44].
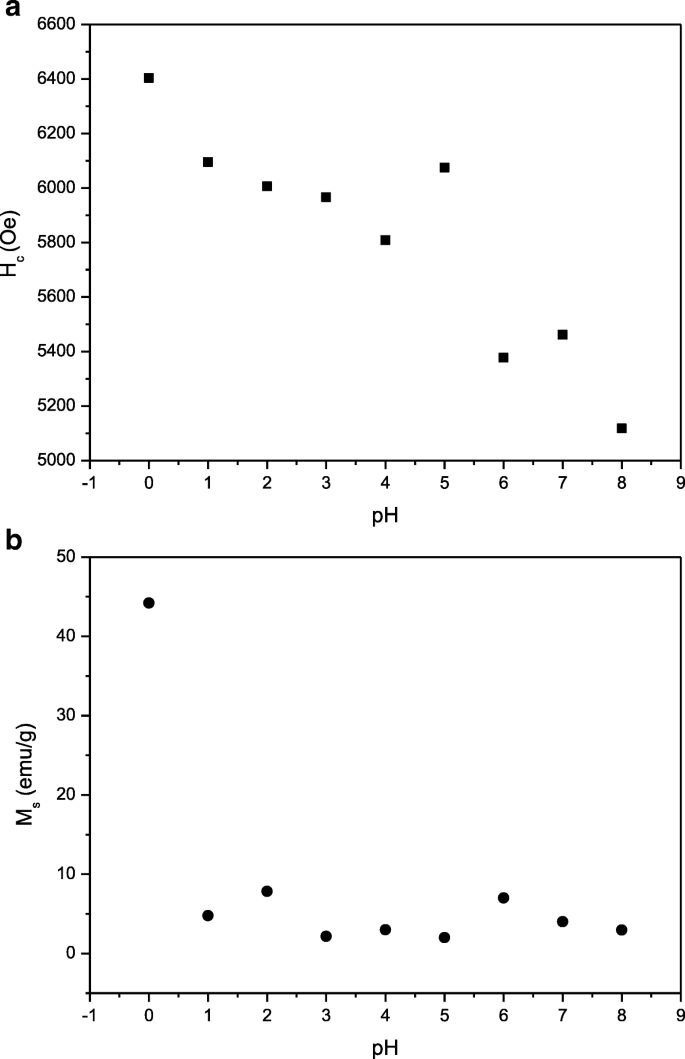
a H c and b M s of SrFe12 O19 at varied pH sintered at 900 °C
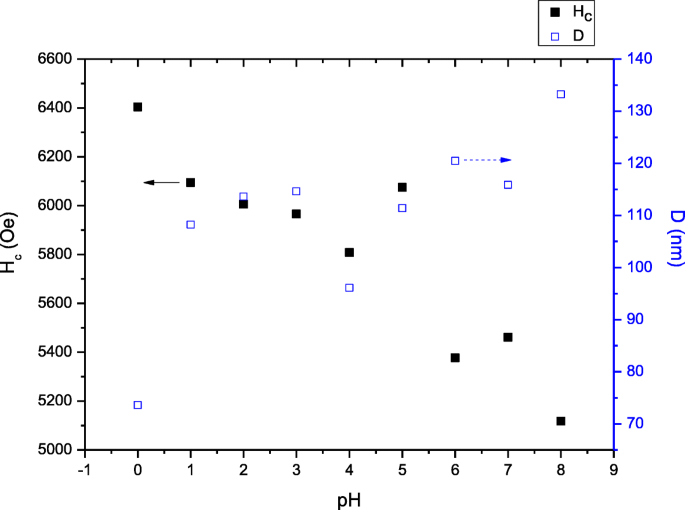
Relation of H c and grain size of SrFe12 O19 at varied pH sintered at 900 °C
Conclusions
Single-phase nanoparticles of SrFe2 O19 prepared using different pH were successfully synthesized by sol–gel method. The effects of structural, microstructural, and magnetic behavior of SrFe2 O19 were studied by modifying the pH values at the fix sintering temperature of 900 °C. From this study, it can be concluded that pH values play an important role in the formation of single-phase SrFe12 O19 which required pH not more than 7 and, by increasing pH from 0 to 3, the formation of SrFe12 O19 is favored. SEM micrographs exhibited a circular crystal type of SrFe2 O19 with average grain size in the range of 73 to 133 nm. The single-phase SrFe2 O19 with optimum magnetic properties are observed in sample prepared at pH 0 which displayed best in-plane saturation magnetization of 44.188 emu/g and remnant magnetization of 27.593 emu/g and with high coercivity of 6403.6 Oe.
Abreviações
- ρ exp :
-
Measured sample’s density
- ρ theory :
-
Theoretical density
- ρ w :
-
Density of water
- ρ xrd :
-
Density of XRD
- a :
-
Lattice parameter
- C:
-
Carbono
- c :
-
Lattice parameter
- C/N:
-
Citrate to nitrate
- C3 H4 (OH)(COOH)3 :
-
Ácido Cítrico
- EDX:
-
Energy-dispersive X-ray
- Fe:
-
Ferro
- Fe(NO3 )3 :
-
Iron(III) nitrate
- Fe2 O 3 :
-
Hematita
- FESEM:
-
Field emission scanning microscope
- FTIR:
-
Fourier transform infrared
- H:
-
Hidrogênio
- H a :
-
Anisotropy field
- Hc :
-
Coercividade
- IR:
-
Infravermelho
- K 1 :
-
Anisotropy constant
- M :
-
Molecular weight
- M r :
-
Remanence
- M r /M s :
-
Squareness ratio
- Ms :
-
Saturation magnetization
- N:
-
Azoto
- N A :
-
Avogadro’s number
- NH3 :
-
Amônia
- NH4 OH:
-
Amônia
- O:
-
Oxigênio
- P :
-
Porosidade
- Sr:
-
Strontium
- Sr(NO3 ) 2 :
-
Strontium nitrate anhydrous granular
- SrFe12 O19 :
-
Strontium ferrite
- V cell :
-
Volume cell
- VSM:
-
Vibrating sample magnetometer
- W ar :
-
Sample’s weight in air
- W water :
-
Sample’s weight in water
- XRD:
-
Difração de raios X
Nanomateriais
- Preparação e propriedades magnéticas de nanopartículas de espinélio FeMn2O4 dopadas com cobalto
- O rearranjo atômico de poços quânticos múltiplos baseados em GaN em gás misto H2 / NH3 para melhorar propriedades estruturais e ópticas
- O efeito do plasma sem equilíbrio de contato nas propriedades estruturais e magnéticas de Mn Х Fe3 - X О4 Spinels
- Propriedades de infravermelho e modulação de onda Terahertz de grafeno / ferrita MnZn / heterojunções p-Si
- Influência da Água na Estrutura e Propriedades Dielétricas da Microcristalina e Nano-Celulose
- Novel Biocompatible Au Nanostars @ PEG Nanopartículas para imagens In Vivo CT e propriedades de depuração renal
- Efeito sinérgico do grafeno e MWCNTs na microestrutura e propriedades mecânicas de nanocompósitos Cu / Ti3SiC2 / C
- Propriedades ópticas estruturais e de infravermelho próximo visível de TiO2 dopado com Cr para pigmentos frios coloridos
- Sondando as propriedades estruturais, eletrônicas e magnéticas dos aglomerados Ag n V (n =1–12)
- Influência de Mg Doping em Nanopartículas de ZnO para Avaliação Fotocatalítica Aprimorada e Análise Antibacteriana



